-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Farmakoterapie srdečního selhání
se sníženou ejekční frakcí:
novější léčebné postupy
Autoři: MUDr. Vachek Jan
Působiště autorů: Interní oddělení Klatovské nemocnice a. s. ; Klinika nefrologie 1. LF UK a VFN v Praze
Vyšlo v časopise: Svět praktické medicíny, 2, 2021, č. 2, s. 70-76
Kategorie: Medicína v ČR: přehledový článek
Souhrn
Srdeční selhání se sníženou ejekční frakcí (HFrEF) je definováno jako přítomnost typických příznaků chronického srdečního selhání (CHSS) a současně snížení ejekční frakce levé komory ≤ 40 %. Nemocní s HFrEF tvoří přibližně 50 % všech pacientů s klinickým HF. I přes průlomové objevy a pokroky ve farmakoterapii představuje HFrEF významnou ekonomickou zátěž v důsledku progresivního charakteru onemocnění charakterizovaného opakujícími se hospitalizacemi a potřebou komplexní léčby. I přes existenci efektivních terapeutických postupů vycházejících z guidelines není významná část pacientů se srdečním selháním léčena vhodnými kombinacemi nebo optimálními tolerovanými dávkami léků. Optimální komplexní léčba (včetně farmakoterapie) je přitom předpokladem snížení morbidity, mortality a také příznivého ovlivnění kvality života, prognózy nemocných a rovněž omezení výdajů na zdravotní péči.
V posledních letech vedly pokroky v poznání patofyziologie srdečního selhání k vývoji a schválení nových léčiv – nejzajímavějšími přírůstky v této oblasti jsou sakubitril/valsartan a inhibitory SGLT2. Tato léčiva jsou v současné době schválena pro použití při srdečním selhání se sníženou ejekční frakcí (HFrEF) a představují novou možnost k dalšímu zlepšování prognózy a výsledků u pacientů se srdečním selháním.
Inhibitory neprilysinu a receptoru angiotenzinu
Standardní léčba srdečního selhání se sníženou ejekční frakcí (inhibitory ACE/ blokátory receptorů pro angiotenzin, betablokátory a antagonisté mineralokortikoidních receptorů) je k dispozici již mnoho let, ale terapeutické úspěchy, kterých s ní lze dosáhnout, nejsou uspokojivé. S vývojem a schválením sakubitril/ valsartanu bylo ve srovnání s dosavadním standardem léčby dosaženo pokroku v léčbě HFrEF.
Sakubitril/valsartan, duální antagonista receptorů AT1 pro angiotenzin II (ARB) a neprilysinu, byl klinicky ověřován pro léčbu hypertenze a srdečního selhání. Mechanismus jeho účinku je dán blokádou receptorů AT1 valsartanem v kombinaci s blokádou degradace vazodilatačních natriuretických peptidů a tím intenzifikované vazodilatace. První klinická studie PARAMOUNT se sakubitril/ valsartanem v léčbě srdečního selhání se zachovalou ejekční frakcí prokázala významné snížení koncentrace NT proBNP. Klinická studie PARADIGM-HF u nemocných se srdečním selháním se sníženou ejekční frakcí a vysokými hodnotami natriuretických peptidů byla předčasně ukončena pro příznivý vliv studijní medikace ve srovnání s enalaprilem (tedy s aktivní léčbou, nikoli s placebem) jak na mortalitu, tak na hospitalizace. Kardiovaskulární mortalita byla snížena o 20 %, první hospitalizace pro srdeční selhání o 21 %. Vzhledem k míře poklesu mortality není dosažení primárního endpointu tedy způsobeno „pouze“ snížením počtu hospitalizací.
Následné analýzy studie PARA DIGM -HF prokázaly snížení rehospitalizací po dimisi z nemocnice a také stabilizaci stavu u přežívajících pacientů. Klinicky významný rozdíl mezi terapií sakubitril/valsartanem a enalaprilem byl zaznamenán již během prvního měsíce léčby, což je významné vzhledem k tomu, že velká část chronických pacientů je opětovně přijata k hospitalizaci pro dekompenzované srdeční selhání již po měsíci od propuštění.
Jsou k dispozici zajímavá farmakoekonomická data k nákladové efektivitě zahájení léčby sakubitril/valsartanem za hospitalizace. Pokud byla léčba sakubitril/ valsartanem iniciována za pobytu v nemocnici, byla spojena se snížením hospitalizací pro srdeční selhání ve srovnání se situací, kdy byla léčba zahájena ambulantně, nebo se situací, kdy bylo pokračováno v léčbě enalaprilem.
U pacientů s HFrEF bylo zahájení léčby sakubitril/valsartanem během hospitalizace také spojeno s úsporou nákladů ve srovnání se zahájením léčby dva měsíce po hospitalizaci. Zahájení léčby během hospitalizace pro HFrEF bylo ve srovnání s pokračováním léčby enalaprilem rovněž spojeno s úsporou nákladů a bylo také vysoce nákladově efektivní.
Tato zjištění tedy naznačují, že u pacientů s HFrEF může být zahájení léčby sakubitril/valsartanem během hospitalizace spojeno se snížením počtu hospitalizací, zvýšenou délkou života upravenou podle kvality a úsporami nákladů.
Dalším zajímavým nálezem je zpomalení poklesu glomerulární filtrace a nižší výskyt závažné hyperkalemie při léčbě sakubitril/valsartanem v porovnání s enalaprilem.
Podle doporučení Evropské kardiologické společnosti z roku 2016 by měli být sakubitril/valsartanem léčeni pacienti se srdečním selháním a sníženou ejekční frakcí, kteří zůstávají symptomatičtí, a pacienti s ejekční frakcí nižší než 35 % při léčbě inhibitorem ACE nebo blokátorem receptoru AT1 pro angiotenzin II, betablokátorem a inhibitorem mineralokortikoidních receptorů. U těchto pacientů má být inhibitor angiotenzin konvertujícího enzymu nebo blokátor receptoru AT1 pro angiotenzin II nahrazen sakubitril/valsartanem.
Postavení sakubitril/valsartanu v léčbě pacientů s ejekční frakcí ve středním rozmezí a u pacientů se srdečním selháním se zachovanou ejekční frakcí zatím zůstává nejasné.
Inhibitory SGLT2
Diabetes mellitus 2. typu je běžný u pacientů s chronickým srdečním selháním a je spojen s vysokou morbiditou a mortalitou. V poslední době došlo k významnému pokroku v léčbě diabetes mellitus 2. typu a kardiovaskulárních onemocnění. Některá nová antidiabetika prokázala neutrální nebo pozitivní kardiovaskulární účinek, zejména na hospitalizace pro srdeční selhání, ale také na úmrtnost – například inhibitory transportéru sodíku a glukózy typu 2 (SGLT2). Jejich dalším efektem je snížení závažných nežádoucích renálních příhod.
Ukázalo se, že zlepšení glykemické kontroly u pacientů s diabetem snižuje mikrovaskulární, ale nikoli makrovaskulární komplikace. Empagliflozin, inhibitor sodíko-glukózového kotransportéru 2 (SGLT2), jako první prokázal snížení kardiovaskulární mortality u nemocných s DM. Rovněž bylo zaznamenáno snížení hospitalizací pro srdeční selhání.
Studie EMPA-REG OUTCOME byla prezentována na podzim roku 2015. Tohoto dlouhodobého, multicentrického, randomizovaného, dvojitě zaslepeného, placebem kontrolovaného hodnocení se zúčastnilo více než 7000 pacientů ze 42 zemí světa s diabetes mellitus 2. typu s vysokým kardiovaskulárním rizikem (medián doby sledování byl 3,1 roku). Nemocní užívali v kombinaci se standardní terapií (antidiabetika, antihypertenziva, hypolipidemika) 1krát denně perorálně buď 10 mg, nebo 25 mg empagliflozinu, nebo placebo. Primárním sledovaným cílem byl výskyt úmrtí v důsledku kardiovaskulárních onemocnění a dále výskyt nefatálního infarktu myokardu nebo nefatální cévní mozkové příhody.
Empagliflozin ve studii EMPA-REG OUTCOME snížil výskyt úmrtí v důsledku kardiovaskulárních onemocnění a výskyt nefatálního infarktu myokardu nebo nefatální cévní mozkové příhody o 14 %. Během sledování došlo ke snížení kardiovaskulární úmrtnosti o 38 %, jakož i celkové úmrtnosti o 32 % a ke snížení hospitalizací pro srdeční selhání o 35 %. Výsledky studie EMPEROR Reduced byly prezentovány na evropském kongresu v září 2020. V této placebem kontrolované studii fáze III bylo zahrnuto 3730 pacientů se srdečním selháním třídy NYHA II, III nebo IV s ejekční frakcí levé komory 40 %, kteří byli randomizováni na placebo, nebo empagliflozin 10 mg denně. Kromě studijní medikace měli optimální léčbu srdečního selhání podle doporučení (diuretika, inhibitory ACE, sartany nebo sakubitril/ valsartan, betablokátory, blokátory mineralokortikoidních receptorů a v případě dané indikace i přístrojovou podporu). Během mediánu 16 měsíců se primární endpoint (kardiovaskulární úmrtí a hospitalizace pro srdeční selhání) objevil u 361 z 1863 pacientů (19,4 %) ve skupině s empagliflozinem a u 462 z 1867 pacientů (24,7 %) ve skupině s placebem (HR: 0,75; 95% CI: 0,65–0,86; p < 0,001). Léčba empagliflozinem tedy snížila primární cíl o 25 %, což bylo způsobeno především snížením hospitalizací pro srdeční selhání (o 31 %), snížení mortality bylo 8 %.
Účinek empagliflozinu na primární výsledek byl konzistentní u pacientů s diabetem nebo bez diabetu a u pacientů se sakubitril/valsartanem nebo bez něj. Pokles eGFR byl pomalejší ve skupině s empagliflozinem než ve skupině s placebem (−0,2 ml/min/1,73 m2 za rok vs. −2,3 ml/min/1,73 m2 za rok; p < 0,001). Tato studie došla k podobným zjištěním jako klinické hodnocení DAPA-HF s dapagliflozinem, kde bylo pozorováno vyšší snížení celkové mortality (18 %, ve studii EMPEROR Reduced 8 %) – studie však nejsou zcela porovnatelné vzhledem k rozdílům ve studijní populaci.
Efekt studijní medikace nebyl vykoupen zvýšenými nežádoucími účinky (až na častější výskyt urogenitálních infekcí v empagliflozinové větvi). Nelišil se výskyt hypoglykemií, amputací dolních končetin ani zlomenin končetin, nedocházelo ke snížení krevního tlaku. Bylo pozorováno mírné snížení biomarkerů srdečního selhání a snížení tělesné hmotnosti. Celkový bezpečnostní profil léku byl v souladu s předchozími studiemi.
Ferroterapie
Anemie z nedostatku železa je u pacientů se srdečním selháním velmi častá – odhadovaná prevalence anemie je více než 50 % u ambulantních pacientů. Jde o nezávislý prediktor horší funkční kapacity a přežití. Mezi rizikové faktory nedostatku železa patří ženské pohlaví, pokročilé srdeční selhání a zvýšené koncentrace NT-pro BNP a C-reaktivního proteinu. Definice deficitu železa při srdečním selhání je odlišná od ostatních stavů chronického zánětu a je definována jako snížení sérové koncentrace ferritinu < 100 μg/l nebo sérová koncentrace ferritinu 100–299 μg/l se saturací transferinu < 20 %. V současné době je preferovanou cestou léčby pacientů se srdečním selháním i. v. ferroterapie. Ve většině studií byl užit komplex oxidu železitého se sacharózou (v maximální jednotlivé dávce 200 mg) nebo ferrikarboxymaltóza (maximální týdenní dávka 1000 mg). Bylo provedeno několik placebem kontrolovaných, randomizovaných klinických studií s i. v. železem u pacientů se srdečním selháním třídy NYHA II–III s ejekční frakcí ≤ 45 %, kteří splňovali kritéria pro nedostatek železa, bez ohledu na to, zda byla přítomna anemie. Intravenózní podání železa bylo spojeno se zlepšením subjektivních symptomů a funkční kapacity. Tyto studie však nezkoumaly vliv i. v. železa na úmrtnost a hospitalizace.
Ve dvou samostatných metaanalýzách bylo užívání i. v. železa u pacientů se srdečním selháním s nedostatkem železa spojeno se sníženým rizikem pro složený cílový parametr mortality ze všech příčin a kardiovaskulární hospitalizace. V současné době probíhá rozsáhlá klinická studie zaměřená na zkoumání účinnosti i. v. železa na snížení kardiovaskulární mortality a opakovaných hospitalizací u pacientů se srdečním selháním. Žádná studie však dosud neprokázala účinnost perorálního železa u pacientů se srdečním selháním se sníženou ejekční frakcí. Kromě toho jsou perorální přípravky obsahující železo spojeny s vysokým výskytem nežádoucích účinků (až u 40 % pacientů), jsou špatně absorbovány v důsledku edému střevní stěny a může trvat až 6 měsíců, než se zásoby železa doplní.
V guidelines Evropské kardiologické společnosti pro srdeční selhání je zahrnuto doporučení, aby všichni pacienti se srdečním selháním byli vyšetřeni na anemii a nedostatek železa (ferritin, saturace transferrinu v séru). Evropská guidelines doporučují léčbu i. v. ferrikarboxymaltózou u pacientů se symptomatickým srdečním selháním s nedostatkem železa k ovlivnění příznaků srdečního selhání a kvality života (třída IIa, doporučení úrovně důkazu A). Americká guidelines jsou obecnější – doporučují i. v. železo u pacientů se srdečním selháním a nedostatkem železa jako doporučení třídy B, úroveň důkazu B. Úloha železa u pacientů se srdečním selháním a zachovanou ejekční frakcí (HFpEF) nebyla dosud dostatečně prozkoumána. V současné době probíhá klinické hodnocení zaměřené na vliv ferroterapie u nemocných s HFpEF.
Závěr
• Srdeční selhání je často asociováno s poruchou metabolismu glukózy (diabetes mellitus 2. typu nebo prediabetes) a naopak prevalence srdečního selhání u osob s diabetes mellitus je vysoká.
• Pravidelné stanovení BNP/NT-proBNP se proto doporučuje také pro screening srdečního selhání; vyšetření biomarkerů srdečního selhání by mělo být provedeno rovněž v případě nových symptomů nebo nových změn na EKG.
• V případě patologické hodnoty biomarkerů srdečního selhání je třeba provést echokardiografické vyšetření se stanovením ejekční frakce levé komory (EF).
• Léčba srdečního selhání se sníženou ejekční frakcí (HFrEF) by se měla řídit schématem v doporučeních Evropské kardiologické společnosti (ESC). Je třeba respektovat renální funkci (Obr. 1).
Obr. 1. Algoritmus léčby pacienta se symptomatickým srdečním selháním se sníženou ejekční frakcí
ACEI – inhibitory ACE, ARB – angiotenzin II receptorové blokátory, ARNI – angiotensin receptor neprilysin inhibitor (sakubitril/valsartan), CRT – resynchronizační terapie, EF – ejekční frakce, H-ISD – isosorbid dinitrát, LVAD – levokomorové srdeční podpory, MRA – blokátory mineralokortikoidních receptorů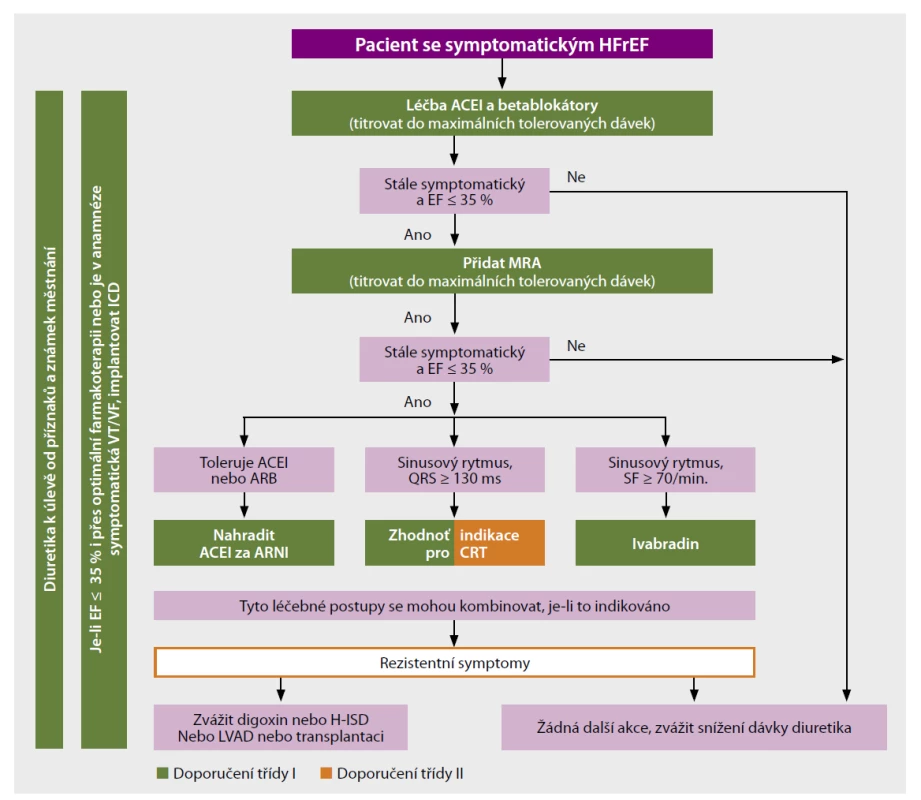
• Dle doporučení Evropské kardiologické společnosti z roku 2016 by měli být sakubitril/ valsartanem léčeni pacienti se srdečním selháním a sníženou ejekční frakcí, kteří zůstávají symptomatičtí, a pacienti s ejekční frakcí nižší než 35 % při léčbě inhibitorem ACE nebo blokátorem receptoru AT1 pro angiotenzin II, betablokátorem a inhibitorem mineralokortikoidních receptorů.
• U diabetiků je třeba preferovat vysoce selektivní betablokátory, které nevedou k zastření symptomů hypoglykemie.
• V případě manifestního DM by měla být zahájena léčba inhibitory SGLT2 s prokázaným kardiovaskulárním benefitem. Robustní data jsou k dispozici pro empagliflozin a dapagliflozin. Empagliflozin v recentní studii statisticky významně snížil kombinovaný primární cíl hospitalizace pro srdeční selhání a kardiovaskulární mortalitu. Dále zabránil zhoršení ledvinných funkcí u pacientů se srdečním selháním se sníženou ejekční frakcí. Tyto výsledky podporují užití inhibitorů SGLT2 u nemocných se srdečním selháním.
Zdroje
1. Anwaruddin S, Lloyd Jones DM, Baggish A, et al. Renal function, congestive heart failure, and amino terminal pro brain natriuretic peptide measurement: results from the ProBNP Investigation of Dyspnea in the Emergency Department (PRIDE) Study. J Am Coll Cardiol 2006;47 : 91–97.
2. Beck-da-Silva L, Rohde LE, Pereira-Barretto AC, de Albuquerque D, Bocchi E, Vilas - -Boas F, Moura LZ, Montera MW, Rassi S, Clausell N. Rationale and design of the IRON-HF study: a randomized trial to assess the effects of iron supplementation in heart failure patients with anemia. J Card Fail 2007;13 : 14–17.
3. Charloux A, Piquard F, Doutreleau S, et al. Mechanisms of renal responsiveness to ANP in heart failure. Eur J Clin Invest 2003;33 : 769–778.
4. Cook JD. Diagnosis and management of iron-deficiency anaemia. Best Pract Res Clin Haematol 2005;18 : 319–332.
5. Desai AS, McMurray JJ, Packer M, et al. Effect of the angiotensin receptor neprilysin inhibitor LCZ696 compared with enalapril on mode of death in heart failure patients. Eur Heart J 2015;36 : 1990–1997.
6. Geisser P. Safety and efficacy of iron(III)-hydroxide polymaltose complex / a review of over 25 years experience. Arzneimittelforschung 2007;57 : 439–452.
7. Kato ET, Silverman MG, Mosenzon O, et al. Effect of dapagliflozin on heart failure and mortality in type 2 diabetes mellitus. Circulation 2019;139 : 2528–2536.
8. Lo KB, Gul F, Ram P, et al. The effects of SGLT2 inhibitors on cardiovascular and renal outcomes in diabetic patients: a systematic review and meta-analysis. Cardiorenal Med 2020;10 : 1–10.
9. McMurray JJ, Packer M, Desai AS, et al. Angiotensin neprilysin inhibition versus enalapril in heart failure. N Engl J Med 2014;371 : 993–1004.
10. McMurray JJ, Packer M, Desai AS, et al. Dual angiotensin receptor and neprilysin inhibition as an alternative to angiotensin converting enzyme inhibition in patients with chronic systolic heart failure: rationale for and design of the Prospective comparison of ARNI with ACEI to Determine Impact on Global Mortality and morbidity in Heart Failure trial (PARADIGM HF). Eur J Heart Fail 2013;15 : 1062–1073.
11. McMurray JJ. Neprilysin inhibition to treat heart failure: a tale of science, serendipity, and second chances. Eur J Heart Fail 2015;17 : 242–247.
12. McMurray JJV, Solomon SD, Inzucchi SE, et al; DAPA-HF Trial Committees and Investigators. Dapagliflozin in patients with heart failure and reduced ejection fraction. N Engl J Med 2019;381 : 1995–2008.
13. Monson ER. Iron and absorption: dietary factors which impact iron bioavailability. J Am Dietet Assoc 1988;88 : 786–790.
14. Nanas JN, Matsouka C, Karageorgopoulos D, Leonti A, Tsolakis E, Drakos SG, Tsagalou EP, Maroulidis GD, Alexopoulos GP, Kanakakis JE, Anastasiou-Nana MI. Etiology of anemia in patients with advanced heart failure. J Am Coll Cardiol 2006;48 : 2485–9.
15. Neuen BL, Young T, Heerspink HJL, et al. SGLT2 inhibitors for the prevention of kidney failure in patients with type 2 diabetes: a systematic review and meta-analysis. Lancet Diabetes Endocrinol 2019;7 : 845–854.
16. Packer M, McMurray JJ, Desai AS, et al. Angiotensin receptor neprilysin inhibition compared with enalapril on the risk of clinical progression in surviving patients with heart failure. Circulation 2015;131 : 54–61.
17. Packer M. SGLT2 inhibitors produce cardiorenal benefits by promoting adaptive cellular reprogramming to induce a state of fasting mimicry: a paradigm shift in understanding their mechanism of action. Diabetes Care 2020;43(3):508–511.
18. Singh JSS, Burrell LM, Cherif M, et al. Sacubitril/valsartan: beyond natriuretic peptides. Heart 2017;103 : 1569–1577.
19. Solomon SD, McMurray JJ, Anand IS, et al. Angiotensin neprilysin inhibition in heart failure with preserved ejection fraction. N Engl J Med 2019 Sep 1. doi: 10.1056/ NEJMoa1908655.
20. Solomon SD, Rizkala AR, Gong J, et al. Angiotensin receptor neprilysin inhibition in heart failure with preserved ejection fraction: rationale and design of the PARAGON HF trial. JACC Heart Fail 2017;5 : 471–482.
21. Solomon SD, Rizkala AR, Lefkowitz MP, et al. Baseline characteristics of patients with heart failure and preserved ejection fraction in the PARAGON HF trial. Circ Heart Fail 2018;11:e004962.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek Úvodní slovoČlánek COVID-19: aktuální přehled
Článek vyšel v časopiseSvět praktické medicíny
Nejčtenější tento týden
- Na inkontinenční pomůcky nově dosáhne více pacientů
- MUDr. Jiří Kornoušek: Program našich konferencí stavíme tak, aby reflektoval skutečně aktuální a praktická témata
- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
- Úloha praktického lékaře v péči o inkontinentní pacienty
- Zápach při inkontinenci je častou obavou pacientů
-
Všechny články tohoto čísla
- Úvodní slovo
-
COVID-19:
aktuální přehled - Časté bolesti hlavy: hodnocení a léčba
-
Komentář k článku
Časté bolesti hlavy:
hodnocení a léčba -
Farmakoterapie neuropatické bolesti
pohledem diabetologa -
Prediabetes:
včasnou léčbou lze výrazně ovlivnit prognózu pacienta -
Cíle kompenzace
a farmakologické možnosti léčby diabetu
u starších pacientů -
Profesor Štěpán Svačina:
Technika umí hodně, ale setkání s pacientem nenahradí -
Psoriatická artritida –
současné možnosti diagnostiky a léčby -
Onemocnění příštítných tělísek –
nenápadný, ale často závažný stav
Co je třeba znát v praxi? Pohled nefrologa -
Léčba osteoporózy v roce 2021 –
zaměřeno na denosumab -
Jaký diagnostický ultrazvuk
do ordinace praktického lékaře? -
Horké aktuality
v registracích EMA -
Farmakoterapie srdečního selhání
se sníženou ejekční frakcí:
novější léčebné postupy -
Komplexní terapie
chronických bércových ulcerací venózní etiologie -
Infekce močového traktu:
jak správně diagnostikovat a léčit? -
Sebevražedné jednání:
motivy, rizika, prevence, pandemie -
Specifika komunikace a nové výzvy
při sdělování závažných zpráv během pandemie COVID-19
- Svět praktické medicíny
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle-
Onemocnění příštítných tělísek –
nenápadný, ale často závažný stav
Co je třeba znát v praxi? Pohled nefrologa -
Psoriatická artritida –
současné možnosti diagnostiky a léčby -
Infekce močového traktu:
jak správně diagnostikovat a léčit? -
Farmakoterapie srdečního selhání
se sníženou ejekční frakcí:
novější léčebné postupy
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: MUDr. Petr Výborný, CSc., FEBO
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




