-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Cíle kompenzace
a farmakologické možnosti léčby diabetu
u starších pacientů
Autoři: MUDr. Lášticová Martina
Působiště autorů: Lékařská fakulta a Fakultní nemocnice ; Hradec Králové ; III. interní gerontometabolická klinika
Vyšlo v časopise: Svět praktické medicíny, 2, 2021, č. 2, s. 39-44
Kategorie: Medicína v ČR: přehledový článek
Souhrn
Incidence a prevalence diabetu s věkem stoupá a v důsledku prodlužující se délky života a zlepšující se péče o diabetiky představují pacienti s diabetes mellitus významnou část starší populace. Senioři s diabetem jsou heterogenní skupina pacientů s odlišnými charakteristikami po stránce zdravotního, psychologického stavu, kognitivních funkcí, soběstačnosti a sociálního zázemí. Mají větší riziko makrovaskulárních komplikací a jsou vulnerabilnější vůči hypoglykemii ve srovnání s mladšími diabetiky. Vyžadují proto individuální přístup při stanovování léčebných cílů a volbě terapeutického postupu.
Incidence a prevalence pacientů s diabetes mellitus má stoupající trend, podle údajů ÚZIS (Ústav zdravotnických informací a statistiky) v roce 2016 bylo v České republice hlášeno 929 945 pacientů. Každoročně zemře mezi 20 až 30 tisíci pacienty s diabetes mellitus (přičemž diabetes nemusí být přímou příčinou úmrtí). S narůstajícím počtem diabetiků a stárnutím populace narůstá i počet starších diabetiků a ve věku nad 65 let má diabetes téměř třetina populace.31 S ohledem na zaznamenané trendy se očekává další rapidní nárůst pacientů s diabetes mellitus ve starší populaci.
Starší diabetici představují heterogenní skupinu pacientů s odlišnými potřebami ve srovnání s mladšími věkovými skupinami diabetiků. Někteří jsou relativně zdraví, plně soběstační, s minimálním výskytem komplikací a komorbidit, u dalších je zdravotní stav komplexní, s přítomností mnoha přidružených nemocí a omezení. Specifický přístup zahrnuje pravidelné zhodnocení zdravotního, ale též psychického a funkčního stavu, a sociálního zázemí pacienta. Mezi specifika staršího diabetika patří častější ztráta soběstačnosti, riziko akcelerované ztráty svalové hmoty a častá přítomnost dalších chronických nemocí, např. arteriální hypertenze, ischemické choroby srdeční, mozkové aterosklerózy, ve srovnání s nediabetiky stejné věkové skupiny. Současně je u starších diabetiků častý výskyt geriatrických syndromů, jako jsou polypragmazie, kognitivní dysfunkce, deprese, inkontinence, pády a perzistující bolest.14 Přítomnost těchto syndromů může ovlivnit schopnost starších pacientů dodržovat léčebná opatření a má dopad na kvalitu jejich života, pokud jim nevěnujeme pozornost.30 Uvedené skutečnosti a posouzení schopnosti samostatného zvládání léčebného režimu pacientem, zapojení rodiny/opatrovníka či plné převzetí péče jinou osobou, případně zařízením sociální péče je nezbytné zohledňovat při volbě léčebného přístupu a stanovení cílů léčby seniora s diabetes mellitus.
Léčba staršího diabetika by měla být cílená na prevenci (případně zabránění progrese) geriatrických syndromů, hypoglykemie a kognitivních dysfunkcí, zlepšení anebo alespoň zachování stávající kvality života.
Definice staršího pacienta s diabetes mellitus není jednotná, IDF (International Diabetes Federation) používá toto označení pro pacienty starší 70 let,8 ADA (American Diabetes Association) používá věkovou hranici 65 let.1 WHO (World Health Organization) rozšiřuje věkovou hranici pro osoby starší 60 let.38
Metabolismus glukózy a věk
Glukózový metabolismus se s věkem mění, a to i u nediabetiků. Udržování glukózové homeostázy je závislé na adekvátní pankreatické sekreci inzulinu a citlivosti inzulinových receptorů vůči glukóze. Inzulinová sekrece i inzulinová senzitivita se s věkem zhoršují. Na rozvoji inzulinové rezistence se podílí centrální obezita, sarkopenie, snížená fyzická aktivita. K dalším faktorům, které mohou přispívat k zhoršení glukózového metabolismu, patří léčba potenciálně diabetogenními léky (diuretika, betablokátory, kortikoidy, psychotropní léky, statiny). Na patogenezi diabetu ve stáří mohou mít vliv i deficit vitaminu D a hypomagnezemie. 5
Symptomatologie
Renální práh pro glukózu se s věkem zvyšuje, snižuje se glomerulární filtrace a nálož glukózy v renálních tubulech dostupná k reabsorpci. Starší diabetici proto tolerují relativně vyšší hodnoty glykemie, než dojde k rozvoji osmotické diurézy. S věkem též dochází k oslabení pocitu žízně. Důsledkem je, že v časných stadiích diabetu u starších pacientů nemusí být přítomny typické symptomy – polyurie a polydipsie. Častěji se můžeme setkávat s únavou, recidivujícími infekcemi, hubnutím, případně chronickými cévními komplikacemi. Závažnější hyperglykemie vede k dehydrataci, zhoršení zraku a kognitivních funkcí.23 Následkem pak může být zhoršování funkčního stavu pacienta a zvýšení rizika pádů.
Přítomnost geriatrických syndromů ovlivňuje soběstačnost a kvalitu života seniora. Patří k nim dekubitální vředy, inkontinence, pády, deliria, demence, zhoršení zraku a sluchu, sarkopenie, malnutrice, křehkost, imobilita a poruchy chůze. Diabetes mellitus může přispívat k rozvoji těchto syndromů – buď prostřednictvím symptomů hyperglykemie a diabetických komplikací, anebo tím, že zpomaluje rekonvalescenci po prodělání akutního onemocnění.12
Geriatrické vyšetření
Podrobné geriatrické vyšetření a zhodnocení pacienta je zásadní v léčbě seniora s diabetes mellitus. Umožňuje určit, jak je daný nemocný schopný zvládat samostatnou péči o sebe a celý léčebný proces. Zahrnuje rozbor základních a pokročilých aktivit běžného života. Na základě něj pak můžeme starší pacienty klasifikovat podle funkčního stavu, přítomnosti komorbidit a očekávané délky života a též plánovat podpůrnou a léčebnou strategii. Zvláštní pozornost je pak důležité věnovat komplikacím, které se mohou rozvinout v průběhu krátkého času a signifikantně ovlivní funkční stav nemocného (např. zrakové komplikace, komplikace postihující dolní končetiny).3 U každé osoby je nezbytné zhodnotit kognitivní funkce, riziko hypoglykemie, kardiovaskulární riziko a psychosociální aspekty, což jsou důležité faktory ovlivňující volbu léčebné strategie.
Kognitivní funkce
Diabetici staršího věku mají vyšší riziko kognitivních dysfunkcí. Tyto poruchy zahrnují široké spektrum od mírné exekutivní dysfunkce až po ztrátu paměti a demenci. Pacienti s diabetes mellitus mají vyšší incidenci demence z jakékoli příčiny, Alzheimerovy demence a vaskulární demence než pacienti s normální glukózovou tolerancí.39 Neuspokojivá kompenzace diabetu je spojena s rozvojem kognitivní dysfunkce40 a delší trvání diabetu je rizikem pro zhoršování kognitivních funkcí. Na druhé straně studie, které zkoumaly možnosti ovlivnění mozkových funkcí intenzivní kompenzací diabetu a krevního tlaku, neprokázaly benefit intenzivní léčby.16, 25
Přítomnost poruchy kognitivních funkcí výrazně ovlivňuje schopnosti pacienta dosáhnout léčebných cílů ve smyslu kompenzace diabetu a cílových hodnot krevního tlaku i lipidogramu. Pro pacienta je obtížné provádět složitější úkoly, jako je selfmonitoring glykemie a úprava dávkování inzulinu, a omezena je i jeho schopnost adekvátního načasování konzumace stravy a dodržování dietního doporučení.32 Při léčbě pacienta s kognitivní poruchou je proto nezbytné zjednodušit léčebný režim (snížit frekvenci dávkování antidiabetické medikace, umožnit flexibilní načasování a jednoduchý způsob aplikace léků) a zajistit asistenci ve všech aspektech léčby.
U starších pacientů s diabetem je důležité pravidelně provádět screening ke zhodnocení kognitivních funkcí k časnému odhalení poruchy. K dispozici jsou jednoduché testy, např. MMSE (Mini-Mental State Examination), Mini-Cog, Montreal Cognitive Assessment (MoCA). U pacientů ve věku nad 65 let je screeningové vyšetření doporučeno 1x ročně a dále v případě, že je zaznamenáno zhoršení schopnosti dodržovat léčebný režim (např. chyby v aplikaci inzulinu, aplikace neadekvátních dávek inzulinu, problémy s počítáním sacharidů, vynechávání jídel, vynechávání dávek inzulinu, problémy s prevencí, rozpoznáváním a léčbou hypoglykemie).22
Hypoglykemie
Hypoglykemie se při léčbě diabetika vyskytuje často a senioři s diabetes mellitus mají riziko hypoglykemie vyšší.17 Ve stáří se zhoršuje schopnost rozpoznávání hypoglykemie a hormonální ochranný mechanismus v podobě sekrece glukagonu a adrenalinu je oslaben, převažují proto neuroglykopenické příznaky hypoglykemie (závratě, slabost, zmatenost) a chybí adrenergní projevy (třes, pocení). 21 Neuroglykopenické příznaky mohou být považovány za projevy neurologického onemocnění (např. tranzitorní ischemická ataka) a tím může dojít k opožděnému odhalení hypoglykemie. Kognitivní dysfunkce je dalším faktorem, který zhoršuje rozpoznávání hypoglykemie. Navíc těžká hypoglykemie vyžadující hospitalizaci zvyšuje riziko demence, zejména v případě opakovaných epizod, i když přímá souvislost nebyla prokázána. 37 Hypoglykemické epizody u seniorů mohou zvyšovat riziko kardiovaskulárních příhod.13 I výskyt mírných hypoglykemických epizod může mít pro starší křehké pacienty závažné důsledky. Závratě a slabost doprovázející lehkou hypoglykemii zvyšují riziko pádů a zlomenin.
Nastavení cílových hodnot glykemie a volba antidiabetické léčby by měly minimalizovat riziko výskytu hypoglykemie. Pravidelné přehodnocování soběstačnosti pacienta a jeho kognitivních funkcí je zásadní k dosažení rovnováhy mezi adekvátní kompenzací diabetu a minimalizací rizika hypoglykemie.
Kardiovaskulární riziko
Starší pacienti s diabetes mellitus mají obdobné riziko rozvoje mikrovaskulárních komplikací jako mladší diabetici, ale jejich absolutní riziko je v případě vzniku diabetu později v životě nižší. V případě makrovaskulárních komplikací je riziko vyšší než u mladších pacientů. Ischemická choroba srdeční je nejčastější příčinou smrti starších diabetiků. Snížení kardiovaskulárního rizika (zejména léčba hypertenze a dyslipidemie) vede u těchto pacientů k výraznějšímu snížení morbidity a mortality než těsná kompenzace diabetu. Výsledky studie ACCORD naznačují, že těsná kompenzace diabetu u osob s vysokým kardiovaskulárním rizikem zvyšuje riziko celkové i kardiovaskulární mortality.10 Snížení kardiovaskulárního rizika dosáhneme ovlivněním známých rizikových faktorů: zanecháním kouření, léčbou hypertenze, léčbou dyslipidemie, protidestičkovou terapií a pravidelnou fyzickou aktivitou.9
Psychosociální aspekty
U staršího pacienta s diabetem je kromě zdravotního stavu důležité posuzovat i psychosociální stránku. Častější je u nich výskyt deprese a v některých případech problematické sociální zázemí. Výborné sociální zázemí, pečující blízcí ochotní provádět častý monitoring glykemií, schopní zajistit adekvátní dietní režim a podávání medikace, to vše představuje podmínky, kdy i při horším funkčním stavu pacienta a současném zajištění prevence hypoglykemie můžeme nastavit intenzivnější léčbu a ambicióznější cíle než v případě, kdy pacient takové podmínky nemá.
Léčebné cíle
Pro populaci starších diabetiků nemáme k dispozici dostatek důkazů ze studií, které by hodnotily vztah mezi intenzitou kompenzace diabetu a rozvojem komplikací. V zásadě ale kromě léčby hyperglykemie a rizikových faktorů je zvlášť nutné myslet na prevenci hypoglykemie, hypotenze a lékových interakcí.18 Péče o starší pacienty s diabetes mellitus je komplikovaná jejich heterogenitou po stránce přítomných komorbidit, kognitivních funkcí a funkčního stavu ovlivňujícího soběstačnost nemocného. V ordinacích se setkáváme jednak s relativně „zdravými“ pacienty s minimem komorbidit, kteří jsou fyzicky i mentálně zdatní, jednak s pacienty s omezenou soběstačností, přítomnými komorbiditami vyžadujícími dopomoc při běžných aktivitách a také s velmi křehkými jedinci, těžce polymorbidními, kteří jsou plně odkázáni na péči jiné osoby. Tyto aspekty je nutné zohledňovat při nastavování léčebných cílů a cílové hodnoty glykovaného hemoglobinu (HbA1c) a glykemií je nutné individualizovat na základě přítomných komorbidit, očekávané délky života, rizika hypoglykemie a schopnosti pacienta dodržovat léčebná opatření (Obr. 1).
Zde je nutné si uvědomit, že použití glykovaného hemoglobinu jako ukazatele kompenzace diabetu má ve starší věkové skupině pacientů některé limitace; neadekvátní hodnoty HbA1c získáme u anemie a stavů, které ovlivňují přežívání červených krvinek, jako je pravidelná hemodialýza, recentní podání krevních transfuzí, léčba erytropoetinem, dále chronické onemocnění ledvin, recentní hospitalizace nebo akutní onemocnění, chronické onemocnění jater.
Doporučené cíle
1. U relativně „zdravých“ starších diabetiků s minimem komorbidit, s intaktními kognitivními funkcemi, s očekávanou délkou života nad 10 let je doporučena intenzivnější kompenzace diabetu s cílovými hodnotami HbA1c do 58 mmol/ mol s preprandiálními hodnotami glykemie v rozmezí 7,8–8,3 mmol/l.36
2. U křehkých pacientů s četnými komorbiditami a funkčním omezením, očekávanou délkou přežití nižší než 10 let je vhodné nastavit vyšší cílové hodnoty kompenzace s hodnotami HbA1c do 64 mmol/mol.
3. U některých velmi křehkých pacientů, plně odkázaných na péči jiné osoby, je možné nastavit cílové hodnoty HbA1c na ještě vyšší hodnoty (kolem 69 mmol/mol, případně i vyšší, s průměrnými hodnotami glykemie kolem 11 mmol/l) za podmínek udržení kvality života, prevence hypoglykemie a souvisejících komplikací a závažné hyperglykemie (Tab. 1).
Tab. 1. Cílové hodnoty kompenzace diabetu, krevního tlaku a dyslipidemie u starších pacientů s diabetes mellitus 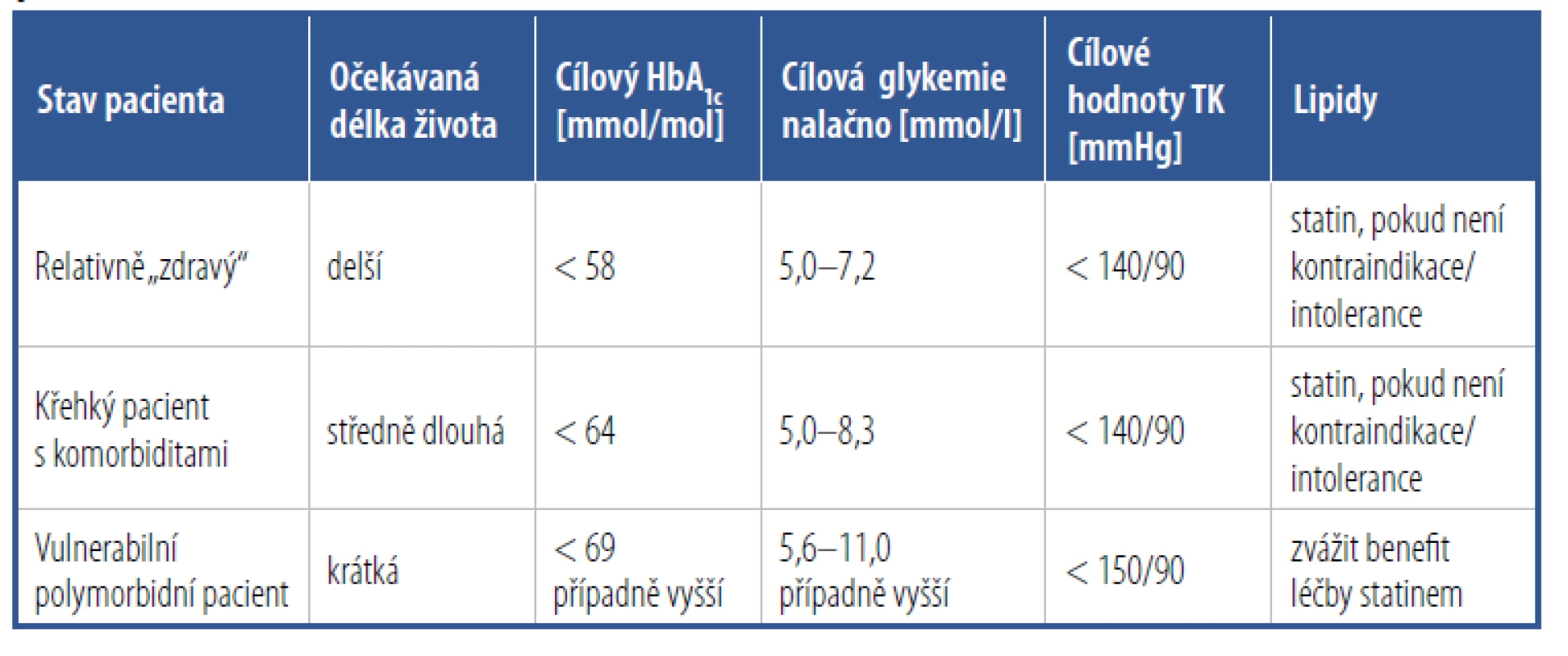
Podobně jako u ostatních pacientů s diabetes mellitus i u starších diabetiků je důležitý screening komplikací diabetu; ten je nutný individualizovat a věnovat zvláštní pozornost těm komplikacím, které mohou vést k omezení soběstačnosti pacienta.
Relativně „zdraví“ senioři v dobrém funkčním stavu
Pacienti s delší očekávanou dobou přežití, bez kognitivních poruch, soběstační, mohou profitovat z intenzivnější dlouhodobé kompenzace diabetu. Takový pacient by měl být ochoten a schopen provádět intenzivní selfmonitoring glykemie a mít předpoklady k samostatným úpravám léčby. Tyto schopnosti je nutné pravidelně prověřovat a při zaznamenání problémů je kdykoli možné přehodnotit postup, upravit cíle a zajistit adekvátní podporu při léčbě.40
Pacienti s komplikujícími komorbiditami a omezenou soběstačností
Senioři s pokročilými komplikacemi diabetu, přítomností závažných komorbidit, poruchou kognitivních funkcí a omezenou soběstačností jsou více ohroženi důsledky hypoglykemie a jejich profit z intenzivní kompenzace diabetu je sporný. Proto je namístě nastavit méně intenzivní cíle kompenzace. Na druhé straně je nutné nastavit cílové hodnoty tak, abychom se vyhnuli dekompenzaci diabetu, která může vést k dehydrataci, zhoršenému hojení ran a rozvoji hyperglykemického hyperosmolárního stavu. Individuální nastavení cíle kompenzace zohledňuje doporučení ADA/EASD (Obr. 1).
Obr. 1. Volba cíle kompenzace. [Upraveno podle doporučení EASD a ADA 2017] ![Volba cíle kompenzace. [Upraveno podle doporučení EASD a ADA 2017]](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/69b8eab4b4947b17a25d9eb708062881.png)
Vulnerabilní pacienti v preterminálním a terminálním stavu
Při léčbě pacientů v paliativní péči patří k základním principům zajištění komfortu a kvality života, symptomatická léčba a léčba bolesti. Po stránce léčby diabetu je vhodné redukovat antidiabetickou léčbu, která může být spojena s diskomfortem. Léčba by měla být nastavena tak, aby umožňovala méně frekventní monitorování glykemie, ale současně byla bezpečná ve smyslu prevence hypoglykemie a zamezovala rozvoji závažné hyperglykemie. Do rozhodovacího procesu má být zapojen pacient a také rodina a pečující osoby.20 V první linii je vhodné volit perorální antidiabetika, eventuálně jednoduchý inzulinový režim. Současně je vhodné zvážit podávání další medikace, jako jsou antihypertenziva či hypolipidemika. Zejména pak u pacientů s problematickým perorálním příjmem je racionální tuto léčbu ukončit.
Léčba diabetu ve stáří
Nefarmakologická opatření
Podobně jako u jiných věkových skupin diabetiků je i ve stáří důležitá úprava životního stylu ve smyslu dietních opatření a pravidelné fyzické aktivity. Starší pacienti s diabetes mellitus jsou ohroženi ztrátou svalové hmoty, snížením svalové síly a sarkopenií.26 Diabetes je také nezávislým rizikovým faktorem pro křehkost, což je věkem podmíněný pokles potenciálu zdraví, zdatnosti, odolnosti a adaptability lidského organismu. Nedostatečný příjem živin, zejména bílkovin, zvyšuje riziko sarkopenie a křehkosti ve stáří. Nefarmakologická opatření jsou cílena na snížení tohoto rizika a zahrnují optimální výživu bohatou na bílkoviny v kombinaci s pravidelnou fyzickou aktivitou.
Dieta
V dietních opatřeních postupujeme individuálně, v zásadě se snažíme vyhýbat složitým dietním doporučením. Přihlížíme na specifické problémy daného pacienta, které souvisí s věkem – změny chuti, dietní restrikce související s přidruženými nemocemi, stav chrupu, změny funkce trávicího traktu. U obézních pacientů může být prospěšná kalorická restrikce.15 Častěji jsou ale tito pacienti ohroženi podvýživou a ztráta hmotnosti u nich představuje další zvýšení rizika morbidity a mortality. Dietní doporučení u těchto nemocných musí daná rizika zohledňovat.35
Fyzická aktivita
Pravidelné cvičení napomáhá udržovat funkční stav jedince, snižuje kardiovaskulární riziko a zlepšuje inzulinovou senzitivitu. Ve stáří vede pravidelná fyzická aktivita ke zlepšení tělesného složení, snižuje riziko pádů a deprese, zlepšuje svalovou sílu a kvalitu života, prodlužuje délku života.6 I zde platí individuální přístup. Fyzicky zdatným jedincům je možné doporučit 30 minut aerobní fyzické aktivity střední intenzity, např. rychlou chůzi alespoň 5x týdně v kombinaci se silovým cvičením. U křehkých pacientů jsou vhodné posilovací cviky ke zlepšení nebo zachování svalové síly a cvičení k udržování rovnováhy za dodržení podmínek bezpečnosti.34
Farmakoterapie
Při rozhodování o antidiabetické léčbě ve stáří se řídíme několika zásadami:
• preferujeme lékové skupiny s nízkým rizikem hypoglykemie,
• vyhýbáme se polypragmazii,
• volíme jednoduchý léčebný režim, který respektuje individuální možnosti a schopnosti pacienta, případně jeho pečovatelů. 33
Cíle kompenzace je nezbytné pravidelně revidovat na základě aktuálního zdravotního stavu, mentálních funkcí a schopností samostatně zvládat léčebný režim. U pacientů, kteří dosahují nebo téměř dosahují cílové hodnoty kompenzace, mají mnohočetné komorbidity, případně se z různých důvodů chceme vyhnout polypragmazii, je možná léčba bez farmakoterapie, při dodržování nefarmakologických opatření, za pravidelných kontrol kompenzace.
Metformin
Metformin je lékem první volby u starších pacientů s diabetes mellitus 2. typu, pokud není kontraindikován (chronické onemocnění ledvin s odhadovanou glomerulární filtrací pod 0,5 ml/s, pokročilé srdeční selhání a jiné potenciálně hypoxemizující stavy, jaterní insuficience). Výhodou je nízké riziko hypoglykemie a vysoká účinnost. U některých pacientů mohou být problémem gastrointestinální nežádoucí účinky a hubnutí. Zde je možné vyzkoušet preparáty s prodlouženým uvolňováním a podávání nižších dávek. Při poklesu glomerulární filtrace pod 1,0 ml/s snižujeme dávku na polovinu. Léčbu přerušujeme před vyšetřením s podáním rtg kontrastní látky, v perioperačním období a při akutním onemocnění. Při léčbě metforminem u starších diabetiků je nutná opatrnost a častější kontroly renálních funkcí,11 ideálně v 3 - až 6měsíčních intervalech.
Inzulinová sekretagoga
Deriváty sulfonylurey a další inzulinová sekretagoga jsou spojena s rizikem hypoglykemie a jejich použití u starší populace vyžaduje opatrnost. Vhodnější jsou preparáty s kratším poločasem, např. glimepirid, glipizid, gliklazid. Dlouho působící glibenklamid je ve stáří kontraindikován pro významné riziko hypoglykemie. 2 Frekvence výskytu hypoglykemie ve starší populaci se podle různých zdrojů liší; data z USA ukazují, že hospitalizace z důvodu hypoglykemie je častější u pacientů nad 75 let než ve věkové skupině 65–74 let.19 Podle další studie z USA představovala perorální antidiabetika 10 % hospitalizací z důvodu nežádoucích účinků léků.4 Poléková hypoglykemie u starších diabetiků se nejčastěji vyskytuje:
1. po cvičení nebo vynechání jídla,
2. při nízkém perorálním příjmu,
3. při abúzu alkoholu,
4. při zhoršení renálních funkcí, kardiálním selhání nebo onemocnění gastrointestinálního traktu,
5. při léčbě salicyláty, deriváty sulfonamidů, fibráty, warfarinem,
6. po hospitalizaci.29
Na riziko polékové hypoglykemie je nutné myslet vždy při změně zdravotního stavu u seniora s diabetes mellitus, u pacientů léčených deriváty sulfonylurey je důležité ptát se při každé návštěvě v ordinaci na výskyt a frekvenci hypoglykemie. Může nás na ni upozornit nízká hodnota glykovaného hemoglobinu, která může být nesprávně interpretována jako dobře kompenzovaný diabetes.
Repaglinid a nateglinid jsou krátce působící inzulinová sekretagoga, která mají podobný mechanismus účinku jako deriváty sulfonylurey. Mají o něco nižší účinnost a nevýhodou je nutnost častějšího podávání s hlavními jídly.
Thiazolidindiony
Jediný u nás dostupný zástupce této lékové skupiny, pioglitazon, by měl být používán ve stáří s velkou opatrností a je vhodné vyhýbat se jeho použití u pacientů s chronickým srdečním selháním, osteoporózou, rizikem pádů, anamnézou fraktur a u pacientů s edémem makuly.27
Inkretinová léčba
Inhibitory dipeptidylpeptidázy 4 (DPP - 4). Inhibitory DPP-4 jsou perorální antidiabetika podávaná v jedné denní dávce, s neutrálním účinkem na hmotnost a bezpečná pro starší populaci pro minimální riziko hypoglykemie a dalších nežádoucích účinků. Nezvyšují riziko kardiovaskulárních komplikací,7 jenom ve studii se saxagliptinem byl pozorován signifikantně vyšší výskyt hospitalizace pro srdeční selhání.28 Mají relativně nižší účinnost a v monoterapii se používají obvykle jenom při mírné hyperglykemii. Užitečné mohou být pro křehké starší pacienty s pozdním vznikem diabetu, zejména u pacientů s vysokým rizikem hypoglykemie a syndromem nerozpoznané hypoglykemie. Linagliptin je možné použít i u pacientů s renální insuficiencí, u ostatních gliptinů se dávka upravuje podle renálních funkcí a v pokročilejších stadiích renální insuficience jsou kontraindikovány.
GLP-1 RA (glucagon-like peptide 1 receptoroví agonisté). V poslední době byly prokázány mnohé přínosy léčby GLP-1 RA, zejména na kardiovaskulární systém u nemocných s přítomným kardiovaskulárním onemocněním.7 Jejich dlouhodobá bezpečnost ve skupině starších pacientů ale zatím nebyla ověřena. Nevýhodou je injekční podávání, vyžadující zrakové, motorické a kognitivní schopnosti k zajištění aplikace, a také relativně časté gastrointestinální nežádoucí účinky (nauzea, zvracení, průjem). Nejsou proto vhodné pro křehké seniory trpící nechutenstvím a hubnutím.
Inhibitory SGLT2 (sodíkovo-glukózový kontransportér 2)
Inhibitory SGLT2 jsou perorální antidiabetika s prokázanými benefity u pacientů s přítomným aterosklerotickým kardiovaskulárním onemocněním.7 Léčba těmito preparáty může být přínosná u pacientů se srdečním selháním a při zpomalení progrese chronického onemocnění ledvin. Dalšími výhodami jsou perorální cesta podávání a nízké riziko hypoglykemie. Podobně jako u GLP 1-RA ani zde nebyla zatím ověřena dlouhodobá bezpečnost v kategorii starších diabetiků. K nežádoucím účinkům patří častější genitourinární infekce a riziko dehydratace, pádů a fraktur.
Inzulin
Aplikace inzulinu vyžaduje dobré zrakové, motorické a kognitivní schopnosti pacienta anebo jeho opatrovníka. Zahájení inzulinoterapie je často odkládáno ze strachu z hypoglykemie, případně náročnosti léčby. V současné době, při dostupnosti dlouho působících inzulinových analog, může být inzulin podáván v jedné denní dávce v monoterapii, případně v kombinaci s perorálními antidiabetiky. Taková léčba má nízké riziko nežádoucích účinků a je dostatečně účinná u pacientů s nedostatečnou kompenzací diabetu při léčbě neinzulinovými antidiabetiky. Léčba vyžaduje pravidelnou titraci dávky k dosažení individuálně nastavených cílových hodnot glykemie a minimalizaci rizika hypoglykemie. Vyhýbáme se složitějším schématům léčby s aplikací několika denních dávek. U pacientů se zhoršujícími se renálními funkcemi je nutné myslet na nižší potřebu inzulinu.
Monitorace glykemie
K hodnocení kompenzace diabetu je potřebná monitorace glykemie a vyšetření HbA1c. Glykovaný hemoglobin kontrolujeme 2x ročně u pacientů, kteří dosahují léčebných cílů a mají stabilní hodnoty glykemie. U pacientů, kteří nedosahují cílových hodnot, případně jim byla měněna léčba, kontrolujeme HbA1c v tříměsíčních intervalech.
Monitorace glykemie v domácím prostředí je prováděna pacientem nebo jeho opatrovníkem. Důležitá je zejména tehdy, pokud je pacient léčen medikací s rizikem hypoglykemie (deriváty sulfonylurey, inzulin). Dále pak v případě intenzivněji nastavených léčebných cílů a také v situacích, kdy pacient mění jídelníček a pohybovou aktivitu. Na druhé straně, provádění selfmonitoringu glykemie není nezbytné u pacientů léčených dietou a antidiabetiky bez rizika hypoglykemie.
Ve vybraných situacích můžeme použít modernější technologie – okamžité monitorování glykemie (FGM) a kontinuální monitorování glykemie (CGM), např. u velmi dobře spolupracujících pacientů s diabetes mellitus 1. typu, na intenzivní léčbě s těsnějšími cílovými hodnotami kompenzace. CGM je dále vhodným doplňujícím vyšetřením např. v situacích, kdy máme podezření na výskyt asymptomatické či nedetekované hypoglykemie nebo hyperglykemie, a perspektivně by mohlo být komplementárním vyšetřením při léčbě preparáty s rizikem hypoglykemie.24
Starší pacienti s diabetes mellitus 1. typu
Speciální skupinou pacientů jsou senioři s diabetes mellitus 1. typu. Díky úspěchům moderní medicíny se pacienti s diabetem 1. typu dožívají vyššího věku a ve věkové kategorii nad 65 let jejich počet narůstá. Zde je nutný osobitý přístup. Inzulin je pro tyto pacienty nezbytný a aplikaci bazálního inzulinu nesmíme vynechat ani v případě, kdy pacient nepřijímá stravu, abychom zabránili rozvoji diabetické ketoacidózy. Aplikace inzulinu může být zajištěna pomocí několika denních dávek, případně inzulinovou pumpou. Ve stáří, kdy se objevují další komplikující onemocnění, poruchy kognitivních funkcí a zhoršování soběstačnosti, se často objevují problémy s aplikací inzulinu a péči musí převzít druhá osoba. Pak je vhodné zvážit zjednodušení inzulinového režimu s aplikací menšího počtu dávek inzulinu, ukončení léčby inzulinovou pumpou (ta může být u některých pacientů riziková, můžeme se setkat např. s vytažením kanyly a přerušením kontinuálního podávání inzulinu u pacienta s demencí). Někteří pacienti se dostávají do zařízení sociální péče, kde si ošetřovatelský personál nemusí uvědomovat rozdíly mezi diabetem 1. a 2. typu, případně nemusí mít zkušenosti s moderními technologiemi, jako je inzulinová pumpa nebo CGM. Zde je pak důležitá spolupráce ošetřujícího personálu s rodinou pacienta a se zdravotnickým týmem a edukace personálu.
Závěr
Starší pacienti s diabetes mellitus představují heterogenní populaci. Přístup k jejich léčbě musí zohledňovat jejich biologický věk, fyzickou a mentální kondici, přítomnost dalších komorbidit, motivaci pacienta a sociální zázemí. Cílové hodnoty ukazatelů kompenzace diabetu nastavujeme individuálně na základě komplexního posouzení všech těchto aspektů a též s ohledem na riziko hypoglykemie a schopnosti pacienta přijmout navrhované léčebné cíle a terapeutický plán. Při doporučení nefarmakologických opatření postupujeme individuálně s ohledem na další chronická onemocnění a dosavadní životní styl. Důležitá je pravidelná fyzická aktivita k zachování soběstačnosti, snížení kardiovaskulárního rizika, zlepšení tělesného složení a inzulinové senzitivity. Prevence hypoglykemie patří k nejdůležitějším zásadám léčby seniora s diabetem. Ke snížení morbidity a mortality diabetika ve stáří je důležité zaměřit se také na ovlivnění kardiovaskulárního rizika, a to zejména léčbou hypertenze a dyslipidemie. Cílem léčby diabetu ve stáří je zlepšení, případně alespoň udržení stávající kvality života pacienta.
Podporováno projektem AZV ČR NV17-31754A.
Zdroje
1. American Diabetes Association. Older adults: standards of medical care in diabetes – 2020;43(Suppl. 1):S152–S162.
2. American Geriatrics Society. 2015 updated beers criteria for potentially inappropriate medication use in older adults. J Am Geriatr Soc 2015;63 : 2227–2246.
3. Blaum C, Cigolle CT, Boyd C, et al. Clinical complexity in middle-aged and older adults with diabetes: The Health and Retirement Study. Med Care 2010;48 : 327–334.
4. Budnitz DS, Lovegrove MC, Shehab N, et al. Emergency hospitalizations for adverse drug events in older Americans. N Engl J Med 2011;365 : 2002.
5. Chentli F, Azzoug S, Mahgoun S. Diabetes mellitus in elderly. Indian J Endocrinol Metab 2015;19(6):744.
6. Christmas C, Andersen RA. Exercise and older patients: guideline for the clinician. J Am Geriatr Soc 2000;48 : 318.
7. Davies MJ, D’Alessio DA, Fradkin J, et al. Management of hyperglycemia in type 2 diabetes, 2018. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care 2018;41 : 2669–2701.
8. Dunning T, Sinclair A, Colagiuri S. New IDF guideline for managing type 2 diabetes in older people. Diabetes Res Clin Pract 2014;103(3):358–540.
9. Emdin CA, Rahimi K, Neal B, et al. Blood pressure lowering in type 2 diabetes: a systematic review and meta-analysis. JAMA 2015;313 : 603.
10. Gerstein HC, Miller ME, et al.; Action to Control Cardivascular Risk in Diabetes Study Group. Effects of intensive glucose lowering in type 2 diabetes. N Engl J Med 2008;358 : 2545.
11. Inzucchi SE, Lipska KJ, Mayo H, et al. Metformin in patients with type 2 diabetes: a systematic review. JAMA 2014;312 : 2668–2675.
12. Kalra S. Geriatric diabetes. J Pak Med Assoc. 20136;63(3):403–405.
13. Khunti K, Davies M, Majeed A, et al. Hypoglycemia and risk of cardiovascular disease and all-cause mortality in insulin-treated people with type 1 and type 2 diabetes: a cohort study. Diabetes Care 2015;38 : 316.
14. Kimbro LB, Mangione CM, Steers WN, et al. Depression and all-cause mortality in persons with diabetes mellitus: are older adults at higher risk? Results from the Translating Research Into Action for Diabetes Study. J Am Geriatr Soc 2014;62 : 1017–1022.
15. Kirkman MS, Briscoe VJ, Clark N, et al. Diabetes in older adults: a consensus report. J Am Geriatr Soc 2012;60 : 2342.
16. Launer LJ, Miller ME, Williamson JD, et al. ACCORD MIND investigators. Effects of intensive glucose lowering on brain structure and function in people with type 2 diabetes (ACCORD MIND): a randomised open-label substudy. Lancet Neurol 2011;10 : 969–977.
17. Lee AK, Lee CJ, Huang ES, et al. Risk factors for severe hypoglycemia in black and white adults with diabetes: the Atherosclerosis Risk in Communities (ARIC) Study. Diabetes Care 2017;40 : 1661–1667.
18. Ligthelm RJ, Kaiser M, Vora J, et al. Insulin use in elderly adults: risk of hypoglycemia and strategies for care. J Am Geriatr Soc 2012;60 : 1564.
19. Lipska KJ, Ross JS, Wang Y, et al. National trends in US hospital admissions for hyperglycemia and hypoglycemia among Medicare beneficiaries, 1999 to 2011. JAMA Intern Med 2014;174 : 1116.
20. Mallery LH, Randsom T, Steeves B, et al. Evidence-informed guidelines for treating frail older adults with type 2 diabetes: from the Diabetes Care Program of Nova Scotia (DCPNS) and the Palliative and Therapeutic Harmonization (PATH) program. J Am Med Dir Assoc 2013;14 : 801–808.
21. Matyka K, Evans M, Lomas J, et al. Altered hierarchy of protective responses against severe hypoglycemia in normal aging in healthy men. Diabetes Care 1997;20 : 135.
22. Moreno G, Mangione CM, Kimbro L, et al. American Geriatrics Society Expert Panel on Care of Older Adults with Diabetes Mellitus. Guidelines abstracted from the American Geriatrics Society Guidelines for Improving the Care of Older Adults with Diabetes Mellitus:2013 update. J Am Geriatr Soc 2013;61 : 2020–2026.
23. Mooradian AD, Perryman K, Fitten J, et al. Cortical function in elderly non-insulin dependent diabetic patients. Behavioral and electrophysiologic studies. Arch Intern Med 1988;148 : 2369.
24. Munshi MN, Segal AR, Weinger K. Frequent hypoglycemia among elderly with poor glycemic control. Arch Intern Med. 2011;171(4):362–364.
25. Murray AM, Hsu F-C, Williamson JD, et al. Action to Control Cardiovascular Risk in Diabetes Follow-On Memory in Diabetes (ACCORDION MIND) Investigators. ACCORDION MIND: results of the observational extension of the ACCORD MIND randomised trial. Diabetologia 2017;60 : 69–80.
26. Park SW, Goodpaster BH, Strotmeyer ES, et al. Decreased muscle strenght and quality in older adults with type 2 diabetes: the health, aging and body composition study. Diabetes 2006;55 : 1813–1818.
27. Schwartz AV, Chen H, Ambrosius WT, et al. Effects of TZD use and discontinuation on fracture rates in ACCORD bone study. J Clin Endocrinol Metab 2015;100 : 4059–4066.
28. Scirica BM, Bhatt DL, Braunwald E, et al. Saxagliptin and cardiovascular outcomes in patients with type 2 diabetes mellitus. N Engl J Med 2013;369 : 1317.
29. Shorr RI, Ray WA, Daugherty JR, et al. Incidence and risk factors for serious hypoglycemia in older persons using insulin or sulfonylureas. Arch Intern Med 1997;157 : 1681.
30. Sudore RL, Karter AJ, Huang ES, et al. Symptom burden of adults with type 2 diabetes across the disease course: Diabetes Aging Study. J Gen Intern Med 2012;27 : 1674–1681
31. Svačina S, Jurašková B, Karen I, et al. Doporučené postupy v léčbě starších pacientů s diabetes mellitus v ČR. DMEV 2013;16 : 82–89.
32. Tomlin A, Sinclair A. The influence of cognition on self-management of type 2 diabetes in older people. Psychol Res Behav Manag 2016;9 : 7–20.
33. Valencia WM, Florez H. Pharmacological treatment of diabetes in older people. Diabetes Obes Metab 2014;16 : 1192–1203.
34. Villareal DT, Aguirre L, Gurney AB, et al. Aerobic or resistance exercise, or both, in dieting obese older adults. N Engl J Med 2017;376 : 1943–1955.
35. Wedick NM, Barret-Connor E, Knoke JD, et al. The relationship between weight loss and all-cause mortality in older men and women with and without diabetes mellitus: the Rancho Bernardo study. J Am Geriatr Soc 2002;50 : 1810.
36. Wei N, Zheng H, Nathan DM. Empirically establishing blood glucose targets to achieve HbA1c goals. Diabetes Care 2014;37 : 1048.
37. Whitmer RA, Karter AJ, Yaffe K, et al. Hypoglycemic episodes and risk of dementia in older patients with type 2 diabetes mellitus. JAMA 2009;301 : 1565.
38. World Health Organization. World report on ageing and health. Geneva: World Health Organization; 2015.
39. Xu WL, von Strauss E, Qiu CX, et al. Uncontrolled diabetes increases the risk of Alzhei mer‘s disease: a population-based cohort study. Diabetologia 2009;52 : 1031–1039.
40. Yaffe K, Falvey C, Hamilton N, et al. Diabetes, glucose control, and 9-year cognitive decline among older adults without dementia. Arch Neurol 2012;69 : 1170–1175.
41. Young-Hyman D, de Groot M, Hill-Briggs F, Gonzales JS, et al. Psychosocial care for people with diabetes: a position statement of the American Diabetes Association. Diabetes Care 2016 : 39 : 2126–2140.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek Úvodní slovoČlánek COVID-19: aktuální přehled
Článek vyšel v časopiseSvět praktické medicíny
Nejčtenější tento týden
- Na inkontinenční pomůcky nově dosáhne více pacientů
- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Strava bohatá na arginin a prolin slibuje urychlení hojení ran u diabetických pacientů
- Úloha růstového faktoru TGF-β v procesu hojení ran
-
Všechny články tohoto čísla
- Úvodní slovo
-
COVID-19:
aktuální přehled - Časté bolesti hlavy: hodnocení a léčba
-
Komentář k článku
Časté bolesti hlavy:
hodnocení a léčba -
Farmakoterapie neuropatické bolesti
pohledem diabetologa -
Prediabetes:
včasnou léčbou lze výrazně ovlivnit prognózu pacienta -
Cíle kompenzace
a farmakologické možnosti léčby diabetu
u starších pacientů -
Profesor Štěpán Svačina:
Technika umí hodně, ale setkání s pacientem nenahradí -
Psoriatická artritida –
současné možnosti diagnostiky a léčby -
Onemocnění příštítných tělísek –
nenápadný, ale často závažný stav
Co je třeba znát v praxi? Pohled nefrologa -
Léčba osteoporózy v roce 2021 –
zaměřeno na denosumab -
Jaký diagnostický ultrazvuk
do ordinace praktického lékaře? -
Horké aktuality
v registracích EMA -
Farmakoterapie srdečního selhání
se sníženou ejekční frakcí:
novější léčebné postupy -
Komplexní terapie
chronických bércových ulcerací venózní etiologie -
Infekce močového traktu:
jak správně diagnostikovat a léčit? -
Sebevražedné jednání:
motivy, rizika, prevence, pandemie -
Specifika komunikace a nové výzvy
při sdělování závažných zpráv během pandemie COVID-19
- Svět praktické medicíny
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle-
Onemocnění příštítných tělísek –
nenápadný, ale často závažný stav
Co je třeba znát v praxi? Pohled nefrologa -
Psoriatická artritida –
současné možnosti diagnostiky a léčby -
Infekce močového traktu:
jak správně diagnostikovat a léčit? -
Farmakoterapie srdečního selhání
se sníženou ejekční frakcí:
novější léčebné postupy
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



