-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Chronická dušnost:
diagnostika a hodnocení
Autoři: Budhwar Nitin; Md; Syed Zubair
Působiště autorů: Dallas, Texas ; University of Texas Southwestern Medical Center
Vyšlo v časopise: Svět praktické medicíny, 2, 2021, č. 1, s. 16-21
Kategorie: Medicína ve světě: překladový článek s komentáři
Souhrn
Dušnost je symptom vyplývající ze složité souhry chorob a fyziologických stavů a běžně se s ní setkáváme v primární péči. Považuje se za chronickou, pokud je přítomna déle než jeden měsíc. Jako symptom je dušnost prediktorem úmrtnosti ze všech příčin. Nejpravděpodobnějšími příčinami dušnosti jsou chorobné stavy (zahrnující srdeční nebo respirační systém), jako jsou astma, chronická obstrukční plicní nemoc, srdeční selhání, pneumonie a ischemická choroba srdeční. Diagnostika by měla začít podrobnou anamnézou a fyzickým vyšetřením, z výsledků by se měly odvíjet další testy. K testování se doporučuje přistupovat ve fázích, počínaje testy první linie, včetně kompletního krevního obrazu, základní biochemie, elektrokardiografie, rtg hrudníku, spirometrie a pulzní oxymetrie. Pokud není zjištěna žádná příčina, doporučuje se neinvazivní testování druhé linie, jako je echokardiografie, zátěžové testy srdce, testy plicních funkcí a skenování plic pomocí počítačové tomografie. Další možnosti zahrnují invazivnější testy, které by měly být provedeny ve spolupráci s odbornými pracovišti. Existují tři hlavní cíle léčby: správně identifikovat proces základního onemocnění a vhodně léčit, optimalizovat zotavení a zlepšit příznaky dušnosti. Šestiminutový test chůze může být užitečný při měření účinku probíhající léčby. Péče o pacienty s chronickou dušností obvykle vyžaduje multidisciplinární přístup, lékař primární péče je proto ideální pro vedení léčby.
Dušnost je komplexní příznak, který je důsledkem environmentálních, fyziologických a psychologických faktorů. Americká hrudní společnost (The American Thoracic Society) definuje dušnost jako subjektivní zkušenost s dechovým nepohodlím, které zahrnuje kvalitativně odlišné vjemy, jež se liší intenzitou.1 Pokud příznaky přetrvávají déle než jeden měsíc, je stav považován za chronický.2
Prevalenci dušnosti v prostředí primární péče je obtížné kvantifikovat. Různé studie odhadují, že až 2,5 % všech návštěv rodinného lékaře a až 8,4 % ná vštěv lékařských pohotovostí souvisí s léčbou dušnosti.3 Přibližně 30 % pacientů starších než 65 let hlásí určitý stupeň náročnosti dýchání při chůzi.4 Ve studii s komunitní populací starší 70 let byla prevalence dušnosti 32 %.5
Dyspnoe jako symptom má prognostickou hodnotu. Longitudinální studie návštěv lékařských pohotovostí kvůli dušnosti jako aktuálnímu problému (kromě sípání) prokázaly 1,37krát vyšší 10letou úmrtnost oproti běžné populaci. 6 Studie pacientů s chronickou obstrukční plicní nemocí (CHOPN) zjistila, že dušnost je pro predikci mortality ze všech příčin stejně dobrá nebo lepší než usilovně vydechnutý objem vzduchu za první sekundu (FEV1).7 Systematický přehled 10 longitudinálních studií dospěl k závěru, že dušnost jako symptom předpovídá úmrtnost a je užitečným ukazatelem pro stanovení přítomnosti základního onemocnění, které obvykle postihuje srdce nebo plíce.8
Příčiny dušnosti jsou zpravidla nemoci zahrnující plicní nebo kardiovaskulární systém. Astma, CHOPN, srdeční selhání, pneumonie a ischemická choroba srdeční tvoří téměř 85 % základní etiologie.9 Mezi další běžné příčiny patří obezita,10,11 námahou vyvolaná dušnost v důsledku dekondice, 12 těhotenství,13,14 a psychologické stavy, jako je například úzkost.
Klíčová doporučení pro praxi 
A = konzistentní, kvalitní důkazy zaměřené na pacienta; B = nekonzistentní důkazy orientované na pacienta s omezenou kvalitou; C = shoda, důkazy zaměřené na onemocnění, obvyklá praxe, znalecký posudek nebo série případů. Informace o systému hodnocení důkazů najdete na : https://www.aafp.org/afpsort. Anamnéza
Pro zahájení účinné léčby dušnosti u pacienta je zásadní komplexní anamnéza. Praktický lékař by měl při stanovení chroničnosti zvážit dobu trvání příznaků včetně jejich kolísání, výsledná funkční omezení, zhoršující se faktory, úlevové faktory, lékařskou a chirurgickou anamnézu, sociální a pracovní anamnézu, věk, historii užívání tabáku a užívání léků.
Nemoci plicního parenchymu, jako jsou intersticiální fibróza a sarkoidóza, mají obvykle pomalý a progresivní průběh se zhoršující se dušností a zhoršením v průběhu času. Příznaky spojené s nemocemi ovlivňujícími dýchací cesty, včetně astmatu, chronické bronchitidy nebo bronchiektazie, mohou přibývat a ubývat, během vzplanutí se zvyšuje kašel a produkce sputa.
U pacientů se srdečním onemocněním by měla být zjištěna anamnéza příznaků souvisejících se srdečním selháním (např. námahová dušnost, ortopnoe, sípání, pocit plnosti v pravém horním břišním kvadrantu, dolní končetiny nebo generalizovaný edém, paroxysmální noční dyspnoe).
U pacientů s chronickými kardiopulmonálními chorobami dochází k vysokému výskytu úzkosti a deprese, které mohou vést k nepřiměřenému projevu symptomů dušnosti pacienta.15 Dušnost, která se časem zlepšuje úmyslnou aktivitou (například během rehabilitačních programů), může znamenat dekondici. Pokud při tělesné námaze nedochází ke zhoršení dušnosti, měly by být zohledněny funkční příčiny, jako jsou úzkostné poruchy.16
Posturální nebo noční pocity dušnosti indikující zánět horních cest dýchacích mohou být důsledkem chronické sinusitidy nebo žaludeční refluxní choroby.17
Je třeba zvážit iatrogenní příčiny dušnosti, zejména při nedávné změně léčebného režimu pacienta. Například použití betablokátorů může zhoršit astma. Bylo prokázáno, že užívání nesteroidních protizánětlivých léků způsobuje bronchokonstrikci a zadržování tekutin a užívání methotrexátu v jakékoli dávce je spojeno s intersticiální pneumonitidou.18 Imunosupresivní látky, chemoterapie a radiační terapie mohou způsobit dušnost několika způsoby, od přímého poškození parenchymu až po dušnost a sekundární anemii.
Je známo, že expozice azbestu a v poslední době také arzenu mají za následek intersticiální plicní onemocnění a malignity. 19
Historie kouření, včetně pasivní expozice (expozice tabákovému kouři v prostředí nejméně 10 cigaret denně),20,21 výrazně zvyšuje riziko vzniku dušnosti. Rodinná anamnéza může poskytnout vodítko ke genetické složce přispívající k chronické dušnosti; například v případech atypické cystické fibrózy, nedostatku alfa1-antitrypsinu, plicní hypertenze a plicní fibrózy.
Je důležité se ptát na použití doplňkových léčiv, aby se předešlo možným nežádoucím účinkům drog. Například výrobky obsahující ephedru (chvojník) mohou zvyšovat krevní tlak. Jiné, jako je třezalka tečkovaná, ženšen, hloh, danshen, a dokonce i zelený čaj, mohou interferovat s běžně užívanými léky na srdeční selhání, což zhoršuje základní stavy.22
Fyzikální vyšetření
Fyzikální vyšetření by mělo začít kontrolou životních funkcí (srdeční frekvence, krevního tlaku, dechové frekvence a hmotnosti), po které následuje vyšetření příslušných tělesných systémů na základě podezření na diagnózu (včetně horních cest dýchacích, orofaryngu, krku, hrudníku, plic, srdce, břicha, končetin a kůže).
Pulsus paradoxus (pokles systolického krevního tlaku o více než 10 mmHg během inspirační fáze) je spojen s těžkou CHOPN, astmatem, velkými bilaterálními pleurálními výpotky, plicní embolií a subakutní srdeční tamponádou.23
Vyšetření krku může odhalit posun průdušnice, adenopatie, distální jugulární žíly nebo zvětšení štítné žlázy, které vedou k pocitu dušnosti.
Cyanóza, dušnost, dýchací šelesty a potlačené srdeční ozvy jsou v souladu s diagnózou CHOPN, stejně jako používání přídatných svalů pro dýchání, soudkovitý hrudník a dýchání přes našpulené rty.
Šelesty, pozitivní hepatojugulární reflux, zvětšení jater, S3 cval, ascitus a jugulární venózní distenze naznačují srdeční selhání jako základní příčinu. Poslech nepravidelného srdečního rytmu může indikovat arytmie provázející chronickou dušnost.
Muskuloskeletální vyšetření, které hledá příznaky onemocnění hrudní stěny, jako jsou těžká kyfoskolióza, vpáčený hrudník nebo Bechtěrevova nemoc, může identifikovat omezující prvky způsobující dušnost.
Snížené exkurze hrudní stěny, otupělost perkusí, snížený hmatový fremitus, egofonie a pleurální třecí šelest jsou příznaky pleurálního výpotku; při chronické anemii lze pozorovat bledost kůže a nehtů.
Paličkovité prsty jsou příznakem, který by měl být signálem pro okamžité vyšetření k vyloučení karcinomu plic, abscesů plic, bronchiektazie nebo idiopatické plicní fibrózy.24
Počáteční testování
Navzdory své všudypřítomnosti v klinické medicíně neexistuje žádný standardizovaný postup pro vyhodnocování chronické dušnosti. Byly navrženy algoritmy klinické praxe pro stupňovitý přístup a bylo zjištěno, že jsou účinné při identifikaci příčin chronické dušnosti25 – 27 (Obr. 1 a Tab. 125).
Obr. 1. Postup k identifikaci příčin chronické dušnosti. 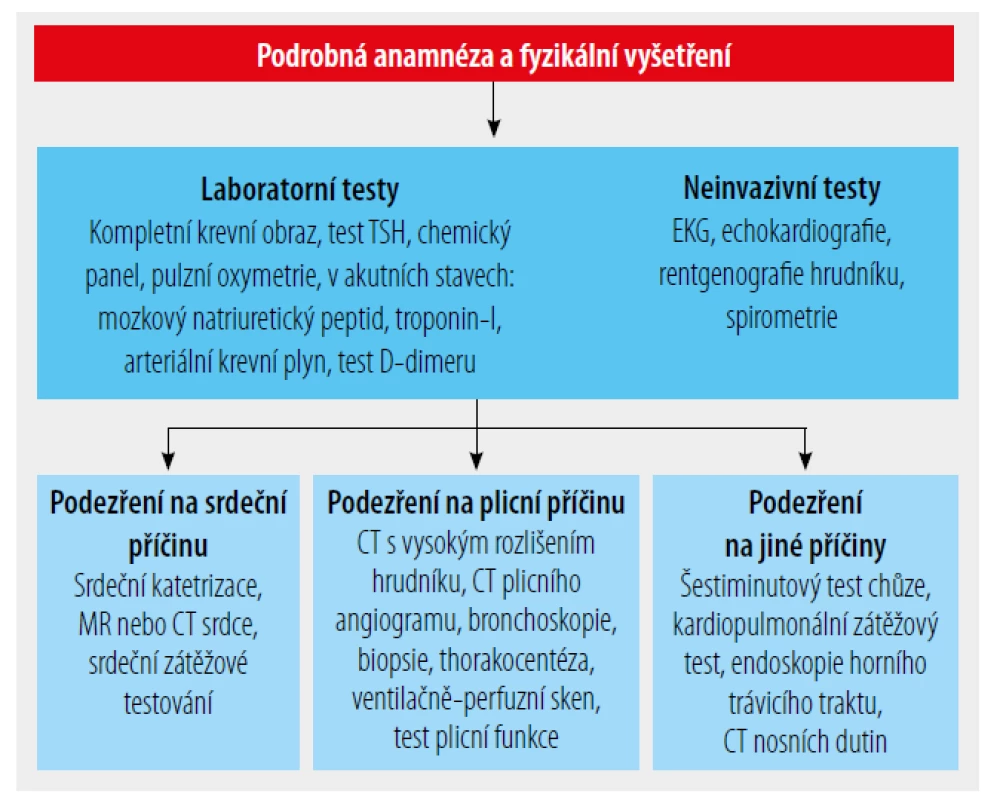
Tab. 1. Diferenciální diagnostika a doporučené testy pro určení příčiny dušnosti 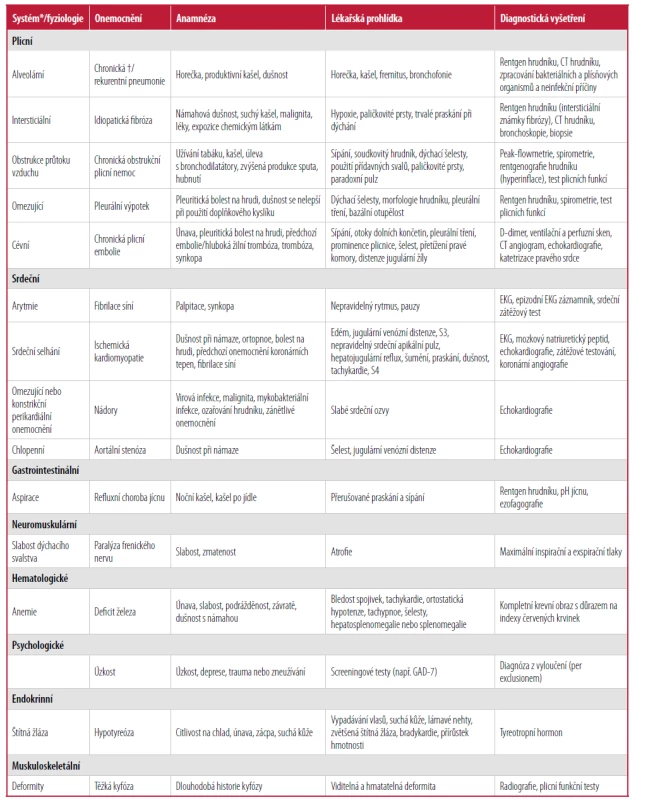
CT = počítačová tomografie; EKG = elektrokardiograf; GAD = generalizovaná úzkostná porucha.
*Frekvence od nejvyššího po nejnižší.
†Trvající několik týdnů až měsíců.
Upraveno se souhlasem Wahls SA. Příčiny a hodnocení chronické dušnosti. AFP 2012;86(2):175.Počáteční testování pro hodnocení dušnosti by mělo zahrnovat pulzní oxymetrii. 25 Počáteční laboratorní testování může zahrnovat kompletní krevní obraz, testování funkce štítné žlázy a základní chemická vyšetření. Ta mohou pomoci identifikovat ane mii, sekundární erytrocytózu způsobenou CHOPN, hypera hypotyreózu a abnormální metabolické a renální stavy (Obr. 1).
Je-li podezření na srdeční selhání, měla by být provedena elektrokardiografie (EKG), testování mozkových natriuretických peptidů a srdeční ultrasonografie; až 29 % pacientů s potvrzeným srdečním selháním se zachovanou ejekční frakcí však má normální hodnoty natriuretického peptidu v mozku (často pozorované u pacientů mladších 50 let, kteří jsou obézní).16,18,22,26,28,29 U pacientů starších 75 let mohou být hladiny vyšší kvůli chronickému onemocnění ledvin, anemii a plicním onemocněním, jako je CHOPN a infekce.29
EKG dokáže identifikovat blokády převodního systému a arytmie, přičemž v takových případech je nejčastější příčinou dušnosti fibrilace síní. EKG může také podporovat diagnostiku stavů, jako je hypertrofie levé komory, perikardiální výpotek nebo ischemická choroba srdeční. Normální EKG znamená, že existuje nízká pravděpodobnost srdečního selhání (89% citlivost).30
Rentgen hrudníku zůstává cenným počátečním testem pro hodnocení dušnosti při podezření na příčiny, jako je srdeční selhání, pleurální výpotek, intersticiální plicní onemocnění a CHOPN.16,24,26,27
Usilovně vydechnutý objem vzduchu za první sekundu (FEV1) nebo poměr FEV1 a usilovné vitální kapacity (FEV1/ FVC) naznačuje obstrukční onemocnění dýchacích cest, jako jsou CHOPN, chronická bronchitida nebo astma. Omezující plicní onemocnění je naznačeno snížením FVC a normálním nebo zvýšeným poměrem FEV1/FVC, ale musí být potvrzeno měřením objemů plic. Restrikční plicní onemocnění je naznačeno snížením FVC a normálním nebo zvýšeným poměrem FEV1/FVC, ale musí být potvrzeno měřením objemů plic.31 Další informace o spirometrii najdete v článku AFP.32 Smyčka (křivka) průtok–objem může pomoci rozlišit příčiny dušnosti způsobené nitrohrudními (např. zúžení dýchacích cest, struma) nebo extrathorakálními překážkami (např. tracheomalacie, tracheální nádory).33
Stanovení D-dimeru je markerem degradace fibrinu. Negativní výsledek testu může pomoci vyloučit plicní embolii jako příčinu dušnosti u pacientů s nízkou pravděpodobností předběžného testu.34
Další testování
V rámci vyšetření může být indikováno další testování, zejména pokud testování v první linii a informace z anamnézy a fyzikální vyšetření neposkytují uspokojivé vysvětlení příčiny dušnosti. Tyto testy by měly být zaměřeny podle podezření lékaře na základní příčinu a mohou zahrnovat testování srdečního stresu, zobrazování srdeční magnetickou rezonancí, testování plicních funkcí, nekontrastní počítačový tomografický sken hrudníku s vysokým rozlišením a skenování ventilace a perfuze24,26,27,34 (Obr. 1). Pokud tyto neinvazivní testy nepřinesou jasnější výsledky, je vhodné obrátit se na specialisty s invazivnějšími testy, jako je bronchoskopie, biopsie plic nebo srdeční či plicní katetrizace.35 Při hodnocení dušnosti mohou pomoci kardiopulmonální zátěžové testy, pokud je dušnost nepřiměřeně horší než závažnost základního srdečního nebo plicního onemocnění pacienta.36
Léčba
Poté, co byla identifikována základní příčina dušnosti, je cílem zahájit vhodnou léčbu, optimalizovat zotavení a zlepšit subjektivní a měřitelné příznaky dušnosti. Chronická dušnost je spíše souborem symptomů než konkrétním onemocněním, proto by měla být vhodná léčba zaměřena na základní příčinu. Měla by se také zvážit adresná léčba přímo zaměřená na příznaky. U pacientů s CHOPN s těžkou klidovou hypoxií se již dlouho používá doplňkový kyslík (méně než 89 % O2).37,38 Nedávná metaanalýza naznačuje, že doplňkový kyslík může u lehce hypoxických nebo nehypoxických pacientů zmírnit dušnost, je však zapotřebí dalších důkazů. 39 Nedávná studie užívání doplňkového kyslíku u pacientů se stabilní CHOPN a střední desaturací (89 % až 93 % O2), s námahou nebo bez ní, neprokázala prodloužení doby do smrti nebo hospitalizace. Nebyly ani zjištěny žádné měřitelné přínosy v kvalitě života, funkce plic nebo zlepšení v ušlé vzdálenosti.40
V zařízeních paliativní péče jsou jednou z možností pro tlumení dušnosti perorální nebo nebulizované opioidy, měly by být titrovány na nejnižší účinnou dávku.
V případech závažných onemocnění plic nebo srdce lze reakci na lékařskou intervenci u dušnosti sledovat pomocí šestiminutového testu chůze,41 při kterém je pacient požádán, aby ušel co nejdelší vzdálenost za dobu šesti minut v prostoru pro chůzi (např. chodba, hala). Před testem i po testu pacient použije k hodnocení dušnosti a celkové únavy revidovanou Borgovu stupnici42 0 až 10, kde 0 neindikuje žádné příznaky a 10 indikuje závažné příznaky. Výsledky může ovlivnit řada faktorů, včetně věku, pohlaví, výšky, motivace, vyšší tělesné hmotnosti a komorbidit, jako jsou muskuloskeletální problémy, závažná srdeční nebo plicní onemocnění pacienta a potřeba doplňkového kyslíku. Podrobnosti o provádění šestiminutového testu chůze jsou k dispozici na stránkách Americké hrudní společnosti (https://www.thoracic.org/statements/resources/pfet/sixminute. pdf).41 Jako jednorázové měřítko funkčního stavu je navíc test prediktorem morbidity a mortality u pacientů se srdečním selháním, CHOPN a plicní hypertenzí.41
Je třeba zvážit i jiné způsoby léčby, jako je plicní rehabilitace,43 včetně domácí terapie u pacientů s CHOPN 44; kognitivně - behaviorální terapie pro zvládání úzkosti, a dietetické/výživové poradenství pro optimalizaci hmotnosti.
Studie ukázaly, že pro zmírnění pocitů dušnosti u CHOPN má určité slibné výsledky akupunktura.45 Nedávná recenze Cochrane přináší důkazy o účincích aktivní terapie mysli a těla, jako je jóga, ta j-či čchi-kung, jako doplněk k plicní rehabilitaci u pacientů s CHOPN.46 Měl by probíhat otevřený dialog s pacienty, kteří uvažují o přidání doplňkové medicíny ke svému konvenčnímu léčebnému plánu, aby byla zajištěna bezpečnost pacientů, zejména pokud jde o lékové inte rakce, které mohou narušit probíhající léčebný plán nebo mít nepříznivý vliv na proces základního onemocnění.47
Tento článek aktualizuje předchozí články na toto téma od Wahls25; Karnani, et al.48; a Morgan a Hodge.49
Zdroje dat: Hledání PubMed bylo provedeno pomocí MeSH (Tezaurus Medical Subject Headings) pro termíny dyspnoe, chronická dušnost, diferenciální diagnostika, léčba, zpracování a léčba. Rovněž byly prohledány databáze Cochrane Systematic Review, National Guideline Clearinghouse, American Thoracic Society guidelines a American Heart Association guidelines. Zkontrolovány byly pouze odkazy publikované v angličtině. Rovněž byly přezkoumány bibliografie příslušných dokumentů. Data vyhledávání: leden 2000 až prosinec 2018; leden 2020.
Autoři děkují Soraya Gollop, PhD, za pomoc při přípravě tohoto recenzního článku.
Článek v původním znění
Am Fam Physician 2020;101(9):542–548.
Překlad: J. Moravcová
Publikováno se souhlasem AAFP.
Chráněno autorským právem.
Tento článek splňuje kritéria AAFP pro další vzdělávání lékařů (CME).
Zveřejnění autorů: Žádné relevantní finanční vztahy.
Informace pro pacienty k tomuto tématu jsou dostupné na: https://family doctor.org/condition/shortness-of-breath.
Zdroje
1. Parshall MB, Schwartzstein RM, Adams L, et al.; American Thoracic Society Committee on Dyspnea. An official American Thoracic Society statement: update on the mechanisms, assessment, and management of dyspnea. Am J Respir Crit Care Med 2012;185(4):435–452.
2. Karnani NG, Reisfield GM, Wilson GR. Evaluation of chronic dyspnea. Am Fam Physician 2005;71(8):1529–1537. Accessed November 25, 2019. https://www.aafp.org/ afp/2005/0415/p1529.html
3. Viniol A, Beidatsch D, Frese T, et al. Studies of the symptom dyspnoea: a systematic review. BMC Fam Pract 2015;16 : 152.
4. Mahler DA. Evaluation of dyspnea in the elderly. Clin Geriatr Med 2017;33(4):503–521.
5. Ho SF, O‘Mahony MS, Steward JA, et al. Dyspnoea and quality of life in older people at home. Age Ageing 2001;30(2):155–159.
6. Safwenberg U, Terént A, Lind L. Differences in long-term mortality for different emergency department presenting complaints. Acad Emerg Med 2008;15(1):9–16.
7. Nishimura K, Izumi T, Tsukino M, et al. Dyspnea is a better predictor of 5-year survival than airway obstruction in patients with COPD. Chest 2002;121(5):1434–1440.
8. Pesola GR, Ahsan H. Dyspnea as an independent predictor of mortality. Clin Respir J 2016;10(2):142–152.
9. Pratter MR, Curley FJ, Dubois J, et al. Cause and evaluation of chronic dyspnea in a pulmonary disease clinic. Arch Intern Med 1989;149(10):2277–2282.
10. Sahebjami H. Dyspnea in obese healthy men. Chest 1998;114(5):1373–1377.
11. Sin DD, Jones RL, Man SF. Obesity is a risk factor for dyspnea but not for airflow obstruction. Arch Intern Med 2002;162(13):1477–1481.
12. Depiazzi J, Everard ML. Dysfunctional breathing and reaching one‘s physiological limit as causes of exercise-induced dyspnoea. Breathe (Sheff) 2016;12(2):120–129.
13. Milne JA, Howie AD, Pack AI. Dyspnoea during normal pregnancy. Br J Obstet Gynaecol 1978;85(4):260–263.
14. Choi HS, Han SS, Choi HA, et al. Dyspnea and palpitation during pregnancy. Korean J Intern Med 2001;16(4):247–249.
15. Kunik ME, Roundy K, Veazey C, et al. Surprisingly high prevalence of anxiety and depression in chronic breathing disorders. Chest 2005;127(4):1205–1211.
16. Sarkar S, Amelung PJ. Evaluation of the dyspneic patient in the office. Prim Care 2006;33(3):643–657.
17. Gaude GS. Pulmonary manifestations of gastroesophageal reflux disease. Ann Thorac Med 2009;4(3):115–123.
18. Berliner D, Schneider N, Welte T, et al. The differential diagnosis of dyspnea. Dtsch Arztebl Int 2016;113(49):834–845.
19. Parvez F, Chen Y, Yunus M, et al. Arsenic impairs lung function: findings from the Health Effects of Arsenic Longitudinal Study. Am J Respir Crit Care Med 2013;188(7): 813–819.
20. Jaakkola MS, Jaakkola JJ, Becklake MR, et al. Effect of passive smoking on the development of respiratory symptoms in young adults: an 8-year longitudinal study. J Clin Epidemiol 1996;49(5):581–586.
21. Leuenberger P, Schwartz J, Ackermann-Liebrich U, et al. Passive smoking exposure in adults and chronic respiratory symptoms (SAPALDIA Study). Swiss study on air pollution and lung diseases in adults, SAPALDIA Team. Am J Respir Crit Care Med 1994;150(5 pt 1):1222–1228.
22. Page RL II, O‘Bryant CL, Cheng D, et al.; American Heart Association Clinical Pharmacology and Heart Failure and Transplantation Committees of the Council on Clinical Cardiology; Council on Cardiovascular Surgery and Anesthesia; Council on Cardiovascular and Stroke Nursing; Council on Quality of Care and Outcomes Research. Drugs that may cause or exacerbate heart failure: a scientific statement from the American Heart Association [published correction appears in Circulation. 2016;134(12):e261]. Circulation 2016;134(6):e32–e69.
23. Van Dam MN, Fitzgerald BM. Pulsus Paradoxus. Updated October 27, 2018. StatPearls Publishing, 2018.
24. Currie GP, Legge JS. ABC of chronic obstructive pulmonary disease. Diagnosis. BMJ 2006;332(7552):1261–1263.
25. Wahls SA. Causes and evaluation of chronic dyspnea. Am Fam Physician 2012;86(2):173–182. Accessed November 25, 2019. https://www.aafp.org/ afp/2012/0715/p173.html
26. Pratter MR, Abouzgheib W, Akers S, et al. An algorithmic approach to chronic dyspnea. Respir Med 2011;105(7):1014–1021.
27. Bostwick D, Hatton ND, Mayeux JD, et al. The approach to the patient with chronic dyspnea of unclear etiology. Adv Pulmonary Hypertension 2018;16(3):103–111.
28. Anjan VY, Loftus TM, Burke MA, et al. Prevalence, clinical phenotype, and outcomes associated with normal B-type natriuretic peptide levels in heart failure with preserved ejection fraction. Am J Cardiol 2012;110(6):870–876.
29. Fabbian F, De Giorgi A, Pala M, et al. Elevated NT-proBNP levels should be interpreted in elderly patients presenting with dyspnea. Eur J Intern Med 2011;22(1):108–111.
30. Ponikowski P, Voors AA, Anker SD, et al.; ESC Scientific Document Group. 2016 ESC guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure of the European Society of Cardiology (ESC) developed with the special contribution of the Heart Failure Association (HFA) of the ESC [published correction appears in Eur Heart J. 2018;39(10):860]. Eur Heart J 2016;37(27):2129–2200.
31. J ohnson JD, Theurer WM. A stepwise approach to the interpretation of pulmonary function tests. Am Fam Physician 2014;89(5):359–366. https://www.aafp.org/afp/2014/0301/ p359.html
32. Langan RC, Goodbred AJ. Office spriometry: indications and interpretation. Am Fam Physician. 2020;101(6):362–368. Accessed March 15, 2020. https://www.aafp.org/ afp/2020/0315/p362.html
33. Stoller JK. Spirometry: a key diagnostic test in pulmonary medicine. Cleve Clin J Med 1992;59(1):75–78.
34. Adam SS, Key NS, Greenberg CS. D-dimer antigen: current concepts and future prospects. Blood 2009;113(13):2878–2887.
35. Huang W, Resch S, Oliveira RK, et al. Invasive cardiopulmonary exercise testing in the evaluation of unexplained dyspnea: insights from a multi-disciplinary dyspnea center. Eur J Prev Cardiol 2017;24(11):1190–1199.
36. American Thoracic Society; American College of Chest Physicians. ATS/ACCP statement on cardiopulmonary exercise testing [published correction appears in Am J Respir Crit Care Med. 2003;167(10):1451–1452]. Am J Respir Crit Care Med 2003;167(2):211–277.
37. Nocturnal Oxygen Therapy Trial Group. Continuous or nocturnal oxygen therapy in hypoxemic chronic obstructive lung disease: a clinical trial. Ann Intern Med. 1980;93(3):391–398.
38. Medical Research Council Working Party. Long term domiciliary oxygen therapy in chronic hypoxic cor pulmonale complicating chronic bronchitis and emphysema. Report of the Medical Research Council working party. Lancet 1981;317(8222):681–686.
39. Uronis HE, Ekström MP, Currow DC, et al. Oxygen for relief of dyspnoea in people with chronic obstructive pulmonary disease who would not qualify for home oxygen: a systematic review and meta-analysis. Thorax 2015;70(5):492–494.
40. Long-Term Oxygen Treatment Trial Research Group, Albert RK, Au DH, Blackford AL, et al. A randomized trial of long-term oxygen for COPD with moderate desaturation. N Engl J Med 2016;375(17):1617–1627.
41. ATS Committee on Proficiency Standards for Clinical Pulmonary Function Laboratories. ATS statement: guidelines for the six-minute walk test [published correction appears in Am J Respir Crit Care Med. 2016 : 193(10):1185]. Am J Respir Crit Care Med 2002;166(1):111–117.
42. Borg G. Psychophysical scaling with applications in physical work and the perception of exertion. Scand J Work Environ Health 1990;16(suppl 1):55–58.
43. Carlin BW. Pulmonary rehabilitation and chronic lung disease: opportunities for the respiratory therapist. Respir Care 2009;54(8):1091–1099.
44. Holland AE, Mahal A, Hill CJ, et al. Home-based rehabilitation for COPD using minimal resources: a randomised, controlled equivalence trial. Thorax 2017;72(1):57–65.
45. Coyle ME, Shergis JL, Huang ET, et al. Acupuncture therapies for chronic obstructive pulmonary disease: a systematic review of randomized, controlled trials. Altern Ther Health Med 2014;20(6):10–23.
46. Gendron LM, Nyberg A, Saey D, et al. Active mind-body movement therapies as an adjunct to or in comparison with pulmonary rehabilitation for people with chronic obstructive pulmonary disease. Cochrane Database Syst Rev 2018;(10): CD012290.
47. Anthonisen NR, Connett JE, Murray RP. Smoking and lung function of Lung Health Study participants after 11 years. Am J Respir Crit Care Med 2002;166(5):675–679.
48. Karnani NG, Reisfield GM, Wilson GR. Evaluation of chronic dyspnea. Am Fam Physician. 2005;71(8):1529–1537. Accessed November 21, 2019. https://www.aafp.org/ afp/2005/0415/p1529.html
49. Morgan WC, Hodge HL. Diagnostic evaluation of dyspnea. Am Fam Physician 1998;57(4):711–716. Accessed November 21, 2019. https://www.aafp.org/ afp/1998/0215/p711.html
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek Úvodní slovo
Článek vyšel v časopiseSvět praktické medicíny
Nejčtenější tento týden
2021 Číslo 1- Na inkontinenční pomůcky nově dosáhne více pacientů
- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Strava bohatá na arginin a prolin slibuje urychlení hojení ran u diabetických pacientů
- Úloha růstového faktoru TGF-β v procesu hojení ran
-
Všechny články tohoto čísla
- Úvodní slovo
-
Vakcíny proti COVID-19,
jejich vývoj a přehled -
Chronická dušnost:
diagnostika a hodnocení -
Komentář k článku
Chronická dušnost:
diagnostika a hodnocení -
Komentář k článku
Chronická dušnost:
diagnostika a hodnocení -
Jak je důležité mít při diabetes mellitus všech pět pohromadě a v normě,
tedy pět hlavních kardiovaskulárních rizikových faktorů -
Nová naděje pro pacienty se vzácnými chorobami
Novela, která usnadní dostupnost léčiv, zamíří do druhého čtení -
Vaskulární věk:
vhodná pomůcka pro edukaci o konceptu kardiovaskulárního rizika -
Hypertriglyceridemie –
současnost a budoucnost -
Význam betablokátorů v současnosti
aneb jak šel čas s betablokátory -
Profesor Vladimír Staněk:
Kardiologie se změnila téměř k nepoznání -
Připomenutí supraventrikulárních tachykardií ve světle nových doporučení
Evropské kardiologické společnosti - Klostridiové průjmy u diabetiků
-
Karcinom pankreatu
u diabetiků -
Antikoagulační léčba u malignit:
mění nové studie přístup? -
Fixní kombinace
paracetamolu s ibuprofenem -
Sdělování závažných zpráv:
jedna z nejnáročnějších situací v medicínské praxi -
Horké aktuality
v registracích EMA
- Svět praktické medicíny
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle-
Chronická dušnost:
diagnostika a hodnocení -
Význam betablokátorů v současnosti
aneb jak šel čas s betablokátory -
Fixní kombinace
paracetamolu s ibuprofenem -
Vakcíny proti COVID-19,
jejich vývoj a přehled
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



