-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Hypertriglyceridemie –
současnost a budoucnost
Autoři: MUDr. Šatný Martin; prof. MUDr. Vrablík Michal, Ph.D.
Působiště autorů: Centrum preventivní kardiologie, 3. interní klinika –, klinika endokrinologie a metabolismu 1. LF UK, a VFN v Praze
Vyšlo v časopise: Svět praktické medicíny, 2, 2021, č. 1, s. 33-37
Kategorie: Medicína v ČR: přehledový článek
Souhrn
Hypertriglyceridemie (HTG) představuje marker zvýšených hladin vysoce aterogenních na triglyceridy (TG) bohatých, tj. remnantních, částic. Tyto se zásadním způsobem podílejí nejen na rozvoji aterosklerotických cévních lézí, ale také závažných gastrointestinálních komplikací – akutních pankreatitid. Ovlivnění hladiny triglyceridů, respektive remnantních částic, je považováno za jednu z modalit redukce reziduálního kardiovaskulárního (KV) rizika. Základem léčebné intervence jsou režimová opatření (dieta a pravidelná fyzická aktivita), jež jsou v indikovaných případech doplněna farmakoterapií. Lékem volby zůstávají i při léčbě hypertriglyceridemie statiny, případně kombinované s fibráty či omega-3 mastnými kyselinami (MK).
V současnosti máme k dispozici (částečně v rámci studií) i nové terapeutické možnosti ovlivnění HTG, využívající například anti-sense oligonukleotidy či cílené protilátky.
Hypertriglyceridemie, respektive akumulace na TG bohatých remnantních částic, bývá označována nejen za nezávislý rizikový faktor aterosklerotických KV onemocnění (ASKVO), ale i marker rizika rozvoje akutních pankreatitid.
Patogeneze vzniku akutní pankreatitidy při HTG není zcela objasněna, je však známo, že jako vysoce rizikové jsou považovány koncentrace TG nad 10 mmol/l.1
Podíváme-li se na význam HTG v kontextu ASKVO, nebylo dlouho jasné, zda zvýšené koncentrace TG (zejména měřené nalačno) vedou k akceleraci aterosklerotického procesu.
Exkurze do historie…
Asociace částic bohatých na triglyceridy s vyšším výskytem infarktů myokardu (IM) byla poprvé popsána již v roce 1953.2 O dvě desetiletí později Donald Zilversmit dokládá přímou souvislost akumulace remnantních částic s akcelerací aterosklerózy, kdy za možný patogenetický mechanismus považuje ukládání hydrolýzou triglyceridů zmenšených remnantních částic přímo do cévní stěny.3
V průběhu dalších let se objevila ještě řada prací analyzujících vztah HTG s AS KVO (zejména IM), avšak jejich výsledky byly často rozporuplné. V roce 1991 Austin et al. publikovali data dokazující, že vyšší koncentrace remnantních částic sice signifikantně zvyšují riziko výskytu ASKVO, avšak po jejich adjustaci na další rizikové faktory AS KVO (zejména HDL-cholesterolu) se toto riziko významně snižuje.4
Na tuto práci pak navázala rozsáhlá metaanalýza sedmnácti studií s více než 56 000 participanty, přičemž základním sledovaným cílem byla ve většině případů KV úmrtnost. Z výsledků univariantní analýzy studie bylo patrné, že vyšší koncentrace TG nalačno významně zvyšují KV riziko. Multivariantní analýzou [po adjustaci na HDL-cholesterol (HDL-Ch), celkový cholesterol (TC), LDL-cholesterol (LDL-Ch), body mass index (BMI), krevní tlak (TK)] získaná data pak dokumentovala následující: zvýšení TG o 1 mmol/l vede k nárůstu KV rizika o 14 % u mužů a dokonce o 37 % u žen. Výsledky této práce lze považovat za možnou odpověď na vztah HTG a ASKVO.5
Od triglyceridů k remnantům…
Řada studií si kladla za cíl ozřejmit, zda snížení TG povede k redukci výskytu ASKVO, jejich výsledky však nebyly jednoznačné. Proto postupem času došlo k přehodnocení role TG, kdy na ně začalo být pohlíženo spíše jako na marker aterogenních na TG bohatých (remnantních) částic, typicky se kumulujících v terénu inzulinové rezistence, diabetu či obecněji metabolického syndromu. Cholesterol nesený remnantními částicemi je vychytáván scavengerovými receptory a spolupodílí se tak na genezi pěnových buněk, jakožto základních kamenů aterosklerotických cévních lézí. Práce autorů Copenhagen study poukázala na zajímavý fakt, kdy relativní koncentrace cholesterolu v remnantech narůstá úměrně rostoucí hladině TG, proto přináší snížení hladin TG další přidanou hodnotu v redukci reziduálního KV rizika, a to zejména v kontextu metabolického syndromu, respektive inzulinové rezistence.6
Jak tedy bojovat s hypertriglyceridemií?
Režimová opatření
Základem léčby jsou neodmyslitelně nefarmakologická, tj. režimová opatření – pravidelná pohybová aktivita, a zejména vhodná dieta. Obecná doporučení vedoucí ke snížení hladin TG shrnul ve své práci Re iner et al., tato jsou pro přehlednost uvedena v tabulce 1.7
Tab. 1. Nefarmakologické možnosti ovlivnění TG [Upraveno podle 7] ![Nefarmakologické možnosti
ovlivnění TG [Upraveno podle 7]](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/9310c92bc5dfb7661cc8c4cb0c2be240.png)
Stran KV prevence se podle současných doporučení pro management léčby dyslipidemií (DLP) jeví jako nejvhodnější tzv. středomořská dieta, což doložila například studie PREDIMED, do které bylo zařazeno takřka 5000 pacientů ve vysokém KV riziku (avšak dosud v primární prevenci). Studijní populace se následně rozdělila do tří dietních skupin, a sice: středomořská dieta + extrapanenský olivový olej, středomořská dieta + ořechy a kontrolní skupina, které bylo doporučeno redukovat nasycené tuky ve stravě. Primární sledovaný endpoint zahrnoval tvrdá kritéria, tj. výskyt IM, cévních mozkových příhod (CMP) či KV úmrtí. Během doby sledování došlo v intervenovaných skupinách k poklesu primárního cíle o 30 %, resp. 28 % ve srovnání s kontrolní skupinou.8
Gardner et al. pu blikovali v roce 2007 práci zabývající se studiem různých typů „alternativních diet“ na hladiny TG, jako nejvhodnější se jevila tzv. Atkinsonova dieta, charakterizovaná naprostou restrikcí sacharidů v konzumované stravě.9
Stran pohybové aktivity bylo dokumentováno, že nejvyššího poklesu TG lze dosáhnout rezistentním, ale nikoliv aerobním tréninkem, a to zejména v populaci pacientů s diabetes mellitus.10
Možnosti farmakoterapie hypertriglyceridemie
Statiny
V souladu s posledními doporučenými postupy pro management léčby DLP jsou pilířem farmakoterapie hypertriglyceridemie statiny, jež jsou schopny snížit hladiny TG přibližně o 7–20 % podle zvolené molekuly (k nejúčinnějším řadíme atorvastatin či rosuvastatin, viz Obr. 1).11 Mechanismus, jakým statiny ovlivňují hladiny TG, není dosud zcela objasněn. Předpokládá se však, že dochází ke zvýšené clearance a snížené syntéze VLDL-částic v hepatocytech.12
Obr. 1. Vliv statinů na hladiny triglyceridů podle jednotlivých studií. 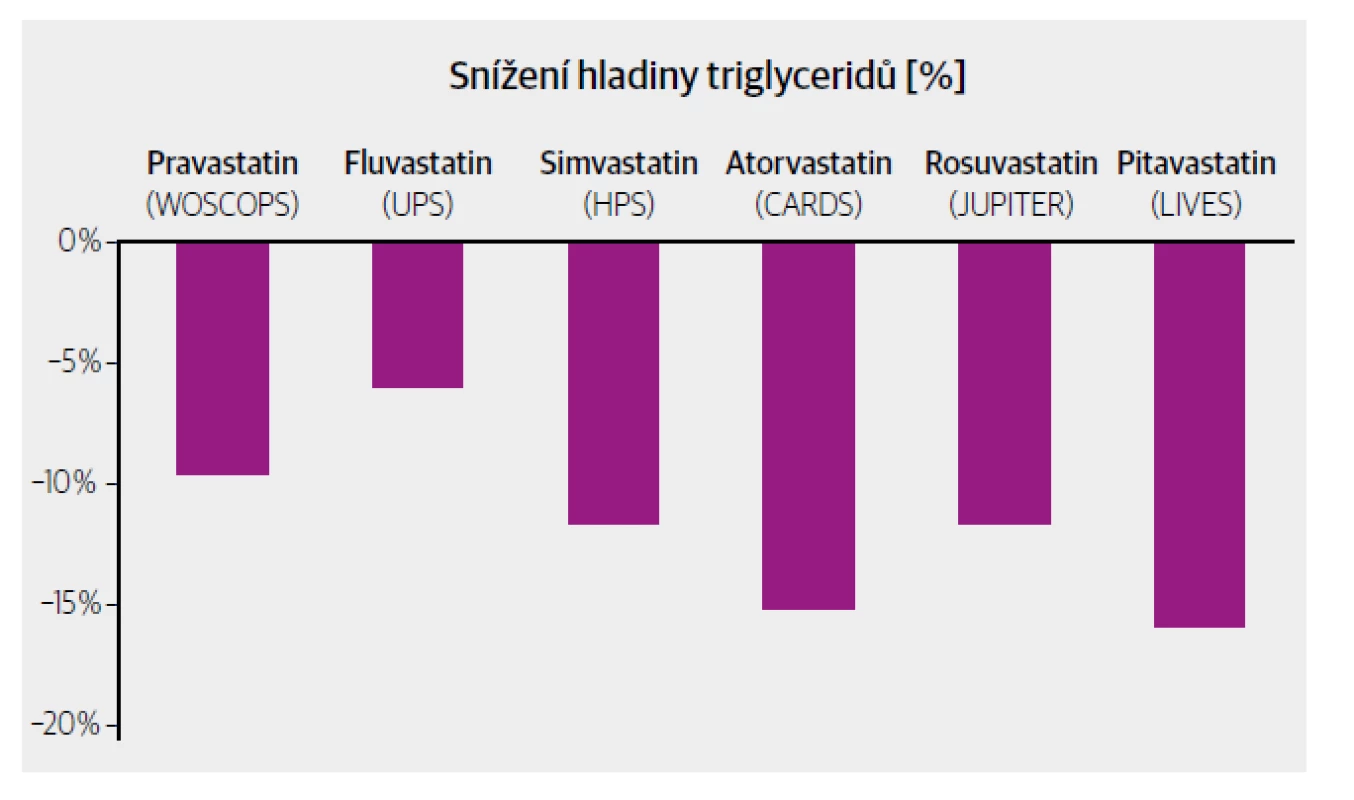
Fibráty
Fibráty (respektive v ČR dominantně užívaný fenofibrát) – agonisté nukleárních PPAR alfa receptorů – jsou dalším stěžejním lékem v boji s izolovanou HTG či smíšenou (resp. aterogenní) DLP. Díky aktivaci PPAR receptorů dochází k řadě změn intermediárního metabolismu, jako například k zvýšení be ta - -oxidace mastných kyselin vedoucí k snížení sekrece VLDL-částic (ovlivněno také sníženou expresí apolipoproteinu B), dále k aktivaci lipoproteinové lipázy (LPL) či supresi transkripce apolipoproteinu C III (apoCIII, inhibitor LPL), což v konečném důsledku vede ke zvýšené clearance a katabolismu na TG bohatých částic, tj. k redukci plazmatických hladin TG.13, 14
Léčba fenofibrátem je indikována v případě trvající HTG nad 2,3 mmol/l (i přes léčbu statiny), přičemž jeho užitím můžeme docílit poklesu hladiny TG až o 30 % (v menších studiích dokonce o 60 %).15, 16 Monoterapie fenofibrátem pak nachází uplatnění především u pacientů s izolovanou HTG (typicky > 10 mmol/l), u nichž hrozí vysoké riziko rozvoje akutní pankreatitidy (primomanifestace či recidivy). Fe nofibrát má dokonce kýžený efekt na postprandiální lipemii, což dobře zdokumentovala například subanalýza studie AC CORD.17
Omega-3 mastné kyseliny
Dalším milníkem v léčbě HTG v kontextu ASKVO se stala studie REDUCE -IT, zkoumající vliv podávání icosapent - -ethylu (2 g 2× denně) na výskyt KV příhod. Do studie bylo zařazeno necelých 9 tisíc pacientů s DM či známou ischemickou chorobou srdeční (TG 1,52 až 5,63 mmol/l, LDL-Ch 1,06 – 2,59 mmol/l); primárním sledovaným cílem byl kompozit – KV úmrtí, nefatální IM, CMP, koronární revaskularizace a výskyt nestabilní anginy pectoris. Během 5leté doby sledování došlo k poklesu primárního cíle o 25 %.18 Nutno však podotknout, že testovaná molekula není bohužel na českém trhu dostupná.
Ezetimib
Ezetimib – inhibitor Niemann-Pick - 1-C1-like proteinu v kartáčovém lemu enterocytů – snižuje vstřebávání cholesterolu ze střeva a nachází tak své uplatnění zejména v kombinacích se statiny, kdy se podílí na poklesu LDL-Ch tzv. duální inhibicí. Díky nedostatečné absorpci alimentárního cholesterolu se zvyšuje exprese LDL-receptorů na povrchu hepatocytů a tím následně clearance LDL-částic z oběhu. Zamyslíme-li se nad mechanismem působení ezetimibu, není překvapující, že vede ke snížení fluktuace postprandiální lipemie.
Ezetimib má také pozitivní vliv na metabolismus remnantních částic, a to především u pacientů s inzulinovou rezistencí, respektive diabetem 2. typu (doloženo například studií IMPROVE-IT). Efekt ezetimibu na hladiny TG je však relativně malý – literárně se uvádí redukce hladin TG maximálně o 10 %.19
Lomitapid
Lomitapid je selektivní inhibitor mikrozomálního TG transportujícího proteinu (MTTP). Původně byl vyvinut pro léčbu homozygotní familiární hypercholesterolemie, avšak jeho působení významně ovlivňuje i hladiny plazmatických TG, a to až o 60 %. MTTP zprostředkovává lipidaci apoB (v enterocytech i hepatocytech), což je kruciální krok tvorby řady lipoproteinových částic – chylomikronů, VLDL - či LDL-částic. Jiný slovy mechanismus jeho účinku je zcela nezávislý na LDL-receptorech, proto ho lze výhodně využít právě u pacientů s minimální nebo žádnou receptorovou aktivitou. Díky jeho účinku ho lze také podávat pacientům s familiární chylomikronemií. Jsou popsána kazuistická sdělení, ve kterých jeho použití u pacientů s recidivujícími pankreatitidami (refrakter ními na jinou léčbu) vedlo nejen k vymizení těchto komplikací, ale také poklesu TG až o 80 %.20, 21
Mipomersen
Mipomersen – antisense mRNA oligonukleotid 2. generace – představuje další modalitu ke kontrole HTG. Jeho podávání interferuje s mRNA pro apolipoprotein B100 (apoB100), což má v konečném důsledku vliv na jeho translaci, a tedy i tvorbu všech lipoproteinových částic obsahujících apoB100 (VLDL-, IDL-, LDL-částice). Mipomersen byl původně testován v léčbě homozygotní familiární hypercholesterolemie, kdy podmiňoval až 65% pokles všech apoB 100-částic.22 Jeho působení má očekávaně dopad také na hladiny TG, a to i v populacích s primárně normální hladinou TG (dokumentovaný pokles TG o 15–25 %).23 Metaanalýza několika studií s mipomersenem doložila dokonce průměrný pokles hladiny TG o 36 %, současně byl také zřejmý pokles apoCIII – významného inhibitoru přirozené clearance VLDL - a LDL-částic.24
PCSK9 inhibitory
PCSK9 inhibitory patří dnes již mezi rutinně užívaná hypolipidemika, která jsou zpravidla indikována u pacientů nedosahujících cílových hodnot LDL-Ch při maximální (tolerované) hypolipidemické léčbě. Díky blokádě proteinu PCSK9 dochází k omezení degradace povrchových LDL-receptorů hepatocytů, což vede ke zvýšené clearance LDL-Ch z cirkulace a současně také k omezení tvorby endogenního cholesterolu. Z klinických studií vyplynulo, že PCSK9 inhibitory jsou schopné snížit hladiny LDL-Ch až o 70 %, přičemž hladina TG bývá ovlivněna méně, a to maximálně o necelých 30 % v závislosti na studované molekule a její dávce. Jejich užití při léčbě HTG je tedy spíše okrajové.25
Volanesorsen
Velmi nadějným lékem pro pacienty s těžkou HTG (např. familiární chylomikronemií) se jeví volanesorsen, který působí jako antisense oligonukleotid blokující formaci mRNA pro apoCIII – inhibitor LPL. V květnu 2019 byl tento lék schválen Evropskou unií pro léčbu familiární chylomikronemie, a to na základě velmi dobrých výsledků dvou studií – COMPASS a APPROACH. Během doby sledování došlo při současné léčbě fibráty a aplikaci 1× týdně k poklesu výchozích hladin TG až o 77 %, resp. 19,3 mmol/l. Volanesorsen je sice velmi účinným lékem, avšak vzhledem k enormní nákladnosti této léčby zůstává otázkou, nakolik je využitelný v běžné klinické praxi.26
Evinacumab
Poslední významnou molekulou je evinacumab – inhibitor angiopoietin-like proteinu 3 (ANGPTL3, inhibitor LPL), který je důležitým prvkem metabolismu na TG bohatých částic. Z dosud provedených studií (I. fáze) s evinacumabem byl doložen pokles TG o 77–83 %, a to v závislosti na podávané dávce. Změny lipidového spektra jsou podobné jako u ztrátových mutací ANGPLT3 spojovaných s redukcí KV rizika. Lze tedy předpokládat, že dopady inhibice AN GPLT3 budou mít obdobný efekt.27
Management HTG v klinické praxi aneb co na to doporučení
Základem léčby jsou vždy odpovídající režimová opatření (viz výše), která jsou v indikovaných případech doplněna farmakoterapií.
Podle aktuálních guidelines zůstávají lékem volby u nejrizikovějších nemocných s TG > 2,3 mmol/l statiny, jež mají být při trvající HTG kombinovány s fenofibrátem či omega-3 mastnými kyselinami (icosapent-ethyl testovaný v rámci sledování REDUCE-IT není v ČR dostupný). Pro úplnost je shrnut management farmakoterapie HTG v tabulce 2.16
Tab. 2. Management farmakoterapie HTG [Upraveno podle 16] ![Management farmakoterapie HTG [Upraveno podle 16]](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/e83cf255b583b5e1785c64d6ae6d6521.png)
Pár slov závěrem…
Hypertriglyceridemie je úzce spojena s akumulací vysoce aterogenních remnantních částic, a představuje tak důležitý ukazatel reziduálního kardiovaskulárního rizika. Základem léčby HTG jsou vždy režimová opatření, která jsou v kontextu vyššího KV rizika doplněna o adekvátní hypolipidemickou terapii. Její pilíře pak představují statiny, fibráty či vysoce dávkované omega-3 mastné kyseliny (tyto však nejsou bohužel na českém trhu k dispozici). Pro nejrizikovější nemocné, zejména s recidivujícími pankreatitidami, máme k dispozici moderní preparáty (lomitapid, mipomersen, volanesorsen…), které mohou být pacientům podávány v rámci specifických léčebných programů či jako léčba studiová.
Částečně podpořeno grantem Univerzity Karlovy, projekt GA UK č. 70220.
Zdroje
1. Hegele RA, Ginsberg HN, Chapman MJ, et al. The polygenic nature of hypertriglyceridaemia: Implications for definition, diagnosis and management. Lancet Diabetes Endocrinol 2013;2 : 655–666.
2. Gofman J, Strisower B, deLalla O, et al. Index of coronary artery atherogenesis. Mod Med 1953;21 : 19–140.
3. Zilversmit DB. A proposal linking atherogenesis to the interaction of endothelial lipoprotein lipase with triglyceride-rich lipoproteins. Circ Res 1973;33 : 633–638.
4. Austin MA Plasma triglyceride and coronary heart disease. Arterioscler Thromb 1991;11 : 12–14.
5. Langsted A, Freiberg JJ, Tybjærg-Hansen A, et al. Nonfasting cholesterol and triglycerides and association with risk of myocardial infarction and total mortality: the Copenhagen City Heart Study with 31 years of follow-up. J Intern Med 2011;270 : 65–75.
6. Hokanson JE, Austin MA. Plasma triglyceride level is a risk factor for cardiovascular disease independent of high-density lipoprotein cholesterol level: a meta-analysis of population-based prospective studies. J Cardiovasc Risk 1996;3 : 213–219.
7. Reiner Z. Managing the residual cardiovascular disease risk associated with HDL-cholesterol and triglycerides in statin-treated patients: a clinical update. Nutr Metab Cardiovasc Dis 2013;23 : 799–807.
8. Estruch R, Eos E, Salas-Salvadó J, et al. Primary prevention of cardiovascular disease with a mediterranean diet supplemented with extra-virgin olive oil or nuts. N Eng J Med [online]. 2018, 378(25) [cit. 2020-09-10]. DOI: 10.1056/NEJMoa1800389. ISSN 0028-4793. Dostupné z: http://www.nejm.org/doi/10.1056/NEJMoa1800389
9. Gardner CD, Kiazand A, Alhassan S, et al. Comparison of the Atkins, Zone, Ornish, and LEARN diets for change in weight and related risk factors among overweight premenopausal women. JAMA [online] 2007;297(9) [cit. 2020-09-10]. doi: 10.1001/ jama.297.9.969. ISSN 0098-7484. Dostupné z: http://jama.jamanetwork.com/article. aspx?doi=10.1001/jama.297.9.969.
10. Gavin C, Sigal RJ, Cousins M, et al. Resistance exercise but not aerobic exercise lowers remnant-like lipoprotein particle cholesterol in type 2 diabetes: A randomized controlled trial. Atherosclerosis [online] 2010;213(2):552–557 [cit. 2020-09-10]. doi: 10.1016/j.atherosclerosis.2010.08.071. ISSN 00219150. Dostupné z: https://linkinghub. elsevier.com/retrieve/pii/S0021915010007197.
11. Reiner Z. Combined therapy in the treatment of dyslipidemia. Fundam Clin Pharmacol 2010;24 : 19–28.
12. Sharma A, Joshi PH, Rinehart S, et al. Baseline very low-density lipoprotein cholesterol is associated with the magnitude of triglyceride lowering on statins, fenofibric acid, or their combination in patients with mixed dyslipidemia. J Cardiovasc Transl Res 2014;7 : 465–474.
13. Saha SA, Kizhakepunnur LG, Bahekar A, Arora RR. The role of fibrates in the prevention of cardiovascular disease – a pooled meta-analysis of long-term randomized placebo-controlled clinical trials. Am Heart J 2007;154 : 943–953.
14. Shah A, Rader DJ, Millar JS. The effect of PPAR-alpha agonism on apolipoprotein metabolism in humans. Atherosclerosis 2010;210 : 35–40.
15. McKeage K, Keating GM. Fenofibrate: a review of its use in dyslipidaemia. Drugs 2011;71 : 1917–1946.
16. Mach F, Baigent C, Catapano AL, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J [online] 2020;41(1),111–188. [cit. 2020-09-10]. DOI: 10.1093/eurheartj/ehz455. ISSN 0195 - 668X. Dostupné z: https://academic.oup.com/eurheartj/article/41/1/111/5556353.
17. Reyes-Soffer G, Ngai CI, Lovato L, et al. Effect of combination therapy with fenofibrate and simvastatin on postprandial lipemia in the ACCORD Lipid Trial. Diabetes Care [online]. 2013;36(2):422–428. [cit. 2020-09-10]. DOI: 10.2337/dc11-2556. ISSN 0149 - 5992. Dostupné z: http://care.diabetesjournals.org/cgi/doi/10.2337/dc11-2556.
18. Bhatt DL, Steg PG, Miller M, et al. Cardiovascular risk reduction with icosapent ethyl for hypertriglyceridemia. N Eng J Med [online] 2019;380(1):11–22. [cit. 2020-09-10]. DOI: 10.1056/NEJMoa1812792. ISSN 0028-4793. Dostupné z: http://www.nejm.org/ doi/10.1056/NEJMoa1812792.
19. Cannon CP, Blazing MA, Giugliano RP, et al. Ezetimibe added to statin therapy after acute coronary syndromes. N Eng J Med [online] 2015;372(25):2387–2397. [cit. 2020 - 09-10]. DOI: 10.1056/NEJMoa1410489. ISSN 0028-4793. Dostupné z: http://www. nejm.org/doi/10.1056/NEJMoa1410489.
20. Raper A, Kolansky DM, Sachais BS, et al. Long-term clinical results of microsomal triglyceride transfer protein inhibitor use in a patient with homozygous familial hypercholesterolemia. J Clin Lipidol 2015;9 : 107–112.
21. Sacks FM, Stanesa M, Hegele RA. Severe hypertriglyceridemia with pancreatitis: thirteen years‘ treatment with lomitapide. JAMA Intern Med 2014;174 : 443–447.
22. Gouni-Berthold I, Berthold HK. Mipomersen and lomitapide: two new drugs for the treatment of homozygous familial hypercholesterolemia. Atheroscler Suppl 2015;18 : 28–34.
23. Najam O, Ray KK. Familial hypercholesterolemia: a review of the natural history, diagnosis, and management. Cardiol Ther 2015;4 : 25–38.
24. Li N, Li Q, Tian XQ, et al. Mipomersen is a promising therapy in the management of hypercholesterolemia: a meta-analysis of randomized controlled trials. Am J Cardiovasc Drugs 2014;14 : 367–376.
25. Giugliano RP, Sabatine MS. Are PCSK9 inhibitors the next breakthrough in the cardiovascular field? J Am Coll Cardiol 2015;65 : 2638–2651.
26. Gelrud A, Digenio A, Alexander V, et al. Treatment with volanesorsen (VLN) reduced triglycerides and pancreatitis in patients with FCS and sHTG vs placebo: Results of the APPROACH and COMPASS †. J Clin Lipidology [online] 2018;12(2) [cit. 2020-09 - 10]. doi: 10.1016/j.jacl.2018.03.032. ISSN 19332874. Dostupné z: https://linkinghub. elsevier.com/retrieve/pii/S1933287418301016.
27. Ahmad Z, Banerjee P, Hamon S, et al. Inhibition of angiopoietin-like protein 3 with a monoclonal antibody reduces triglycerides in hypertriglyceridemia. Circulation [online]. 2019;140(6):470–486. [cit. 2020-09-10]. DOI: 10.1161/CIRCULATIONAHA. 118.039107. ISSN 0009-7322. Dostupné z: https://www.ahajournals.org/ doi/10.1161/CIRCULATIONAHA.118.039107
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek Úvodní slovo
Článek vyšel v časopiseSvět praktické medicíny
Nejčtenější tento týden
2021 Číslo 1- Na inkontinenční pomůcky nově dosáhne více pacientů
- MUDr. Jiří Kornoušek: Program našich konferencí stavíme tak, aby reflektoval skutečně aktuální a praktická témata
- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
- Úloha praktického lékaře v péči o inkontinentní pacienty
- Zápach při inkontinenci je častou obavou pacientů
-
Všechny články tohoto čísla
- Úvodní slovo
-
Vakcíny proti COVID-19,
jejich vývoj a přehled -
Chronická dušnost:
diagnostika a hodnocení -
Komentář k článku
Chronická dušnost:
diagnostika a hodnocení -
Komentář k článku
Chronická dušnost:
diagnostika a hodnocení -
Jak je důležité mít při diabetes mellitus všech pět pohromadě a v normě,
tedy pět hlavních kardiovaskulárních rizikových faktorů -
Nová naděje pro pacienty se vzácnými chorobami
Novela, která usnadní dostupnost léčiv, zamíří do druhého čtení -
Vaskulární věk:
vhodná pomůcka pro edukaci o konceptu kardiovaskulárního rizika -
Hypertriglyceridemie –
současnost a budoucnost -
Význam betablokátorů v současnosti
aneb jak šel čas s betablokátory -
Profesor Vladimír Staněk:
Kardiologie se změnila téměř k nepoznání -
Připomenutí supraventrikulárních tachykardií ve světle nových doporučení
Evropské kardiologické společnosti - Klostridiové průjmy u diabetiků
-
Karcinom pankreatu
u diabetiků -
Antikoagulační léčba u malignit:
mění nové studie přístup? -
Fixní kombinace
paracetamolu s ibuprofenem -
Sdělování závažných zpráv:
jedna z nejnáročnějších situací v medicínské praxi -
Horké aktuality
v registracích EMA
- Svět praktické medicíny
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle-
Chronická dušnost:
diagnostika a hodnocení -
Význam betablokátorů v současnosti
aneb jak šel čas s betablokátory -
Fixní kombinace
paracetamolu s ibuprofenem -
Vakcíny proti COVID-19,
jejich vývoj a přehled
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: MUDr. Petr Výborný, CSc., FEBO
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



