-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaStenty v liečbe zhubných nádorov kolorekta – prehľad a vlastné skúsenosti
Stents in treatment of colorectal cancer – summary and personal experience
Colorectal cancer is one of the diseases with the highest incidence in developed countries. This disease is still only widely diagnosed in an advanced stage, despite the introduction of screening. In some of these patients, endoscopic treatment using stents may be applicable. There are two basic indications: using stents as a bridge to radical surgical treatment; and palliative indications. Using stents as a bridge to surgery is now questionable, after initial enthusiasm surrounding the procedure. Stents have been used for a long time in palliation of malignant stenoses in the colon, and their application as a response to a correct indication has been validated by several studies. Our experience shows that stents represent suitable and effective treatment with acceptable risk of complications within the palliative management of patients with advanced disease. Particularly, these include patients with obstruction symptoms who are not good candidates for palliative surgery due to their general condition and poor survival prognosis.
Key words:
colorectal neoplasms – stents – palliative care
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.Submitted:
9. 10. 2012Accepted:
5. 1. 2013
Autoři: Ľ. Žitňan 1; J. Májek 1; B. Pekárek 1; P. Makovník 2
Působiště autorů: Národný onkologický ústav, Bratislava 1; Onkologický ústav Sv. Alžbety, Bratislava 2
Vyšlo v časopise: Gastroent Hepatol 2013; 67(1): 49-53
Kategorie: Digestivní endoskopie: přehledová práce
Souhrn
Rakovina hrubého čreva a konečníka je vo vyspelých krajinách na poprednom mieste v incidencii zhubných ochorení. Napriek zavedenému screeningu sa toto ochorenie stále často diagnostikuje v pokročilom štádiu. U časti týchto pacientov prichádza do úvahy endoskopická liečba stentami. Existujú dve základné indikácie: použitie stentu ako most k radikálnej chirurgickej liečbe a paliatívne indikácie. Použitie stentov v indikácii „most k chirurgii“ je po počiatočnom nadšení spochybnené. Stenty v paliácii malígnych stenóz v oblasti hrubého čreva sa už dlhšie používajú a ich miesto pri správnej indikácii potvrdili viaceré štúdie. Z našich skúseností môžeme povedať, že stenty sú vhodnou a účinnou liečbou pri akceptovateľnom riziku komplikácií v paliatívnom manažmente pacientov s pokročilým ochorením. Ide najmä o pacientov s prejavmi obštrukcie, ktorí vzhľadom na celkový stav a zlú prognózu dožitia nie sú vhodnými kandidátmi na paliatívny chirurgický výkon.
Klúčové slová:
kolorektálny karcinóm – stenty – paliatívny manažment
Éra zavádzania stentov do hrubého čreva začala v roku 1991, keď Dohmoto prvý raz zaviedol samorozťažný metalický stent (SEMS) do rekta. Prvú generáciu stentov predstavovali stenty používané na prekonanie malígnej stenózy v pažeráku. Tieto stenty boli rigidné a nedali sa dobre zaviesť cez prudké ohyby lúmenu, aké sú v kolone bežné počínajúc rektosigmou. Použitie stentov v dolnom GIT bolo spočiatku zriedkavé a publikované skúsenosti sa týkali malého počtu pacientov. Neskôr boli vyvinuté špeciálne stenty s vysokou ohybnosťou. Zmenila sa i dľžka zavádzacieho systému, ktorá umožnila naložiť stent aj v proximálnejších častiach kolonu. Spočiatku sa stenty implantovali pacientom, ktorí odmietali operáciu, alebo pacientom s pokročilou metastatickou chorobou bez šance na zlepšenie v porovnaní s vysokým operačným rizikom. Až neskôr sa pridala indikácia nazývaná ako „most k chirurgii“.
Aj napriek celosvetovo prebiehajúcim screeningovým programom na prevenciu kolorektálneho karcinómu stále značná časť pacientov (10–15 %) [1] má v čase stanovenia diagnózy prejavy akútnej obštrukcie hrubého čreva. Až 30 % pacientov je v čase stanovenia diagnózy zachytených v pokročilom štádiu, kde sa stáva chirurgický zákrok už len fakultatívnou súčasťou komplexnej paliatívnej liečby [2]. Nie je prekvapivé, že ide o pacientov v zlom stave. Emergentný operačný výkon u týchto pacientov býva zaťažený vyšším stupňom morbidity a mortality, často spojený s nutnosťou vyšitia stómie, prípadne dvojdobej operácie. Riešenie tejto situácie sa hľadalo v indikácii „most k chirurgii“. Primárne sa neodkladne riešila stenóza zavedením stentu. Vznikol tak „priestor“ k stabilizácii pacienta a adekvátnej predoperačnej laváži hrubého čreva. Výsledky viacerých štúdií však nepotvrdili jednoznačný prínos takéhoto postupu. V závere multicentrickej randomizovanej štúdie z Francúzska sa uvádza, že zavedenie stentu nie je bezpečnejšou ani účinnejšou liečbou v stavoch akútnej črevnej obštrukcie ako chirurgický výkon [3]. V prípade, že sa stent zavedie a dôjde ku komplikácii, napr. perforácii, sú výsledky následnej operácie horšie, ako keby boli urgentne operovaní [6]. Rovnako negatívne výsledky k zavádzaniu stentov v indikácii nazývanej most k chirurgii vyplynuli aj v randomizovanej štúdii van Hoofta et al publikovanej v roku 2011 [4].
Opačné výsledky sú v prípadoch, ak sa stent zavádza u pacientov v IV. štádiu ochorenia v tých situáciách, kedy operačné riešenie nie je možné. Môže ísť o neresekabilné pokročilé ochorenie alebo operačný výkon nie je možný kvôli pridruženým ochoreniam. Tu má zavedenie stentu oproti chirurgii viacero výhod. Nie je potrebná kolostómia, ktorá negatívne zasahuje do kvality života pacienta s inkurabilným ochorením a krátkym predpokladaným dožitím. Ďalej ide o pomerne rýchlu úľavu od ťažkostí, nutnosť len krátkodobej hospitalizácie. Výkon môže prebiehať v analgosedácii a bez potreby laparotómie. V dnešnej dobe nemalým prínosom je aj finančná stránka. Zavedenie SEMS sa tak za ostatné roky stalo akceptovateľnou metódou liečby malígnej stenózy u pacientov s pokročilým metastatickým ochorením.
Súbor pacientov a metódy
Naše oddelenie poskytuje onkologickým, ale aj neonkologickým pacientom komplexnú endoskopicko-gastroenterologickú starostlivosť. Prvý samorozťažný metalický stent do hrubého čreva sme zaviedli v roku 2010. Následne až do 4. 6. 2012 sme zaviedli spolu päť SEMS. Použité boli nepovlečené stenty „SX-ELLA Stent Kolorektálny – ENTERELLA“. Ide o samorozťažné nitinolové stenty, ktoré sú uložené v „pull“ zavádzači. Všetky boli implantované pacientom s pokročilým metastatickým ochorením, ktorí mali prejavy obštrukcie hrubého čreva a boli u nich vyčerpané iné možnosti liečby.
Stenty sme zaviedli trom mužom a dvom ženám. Priemerný vek bol 72,2 rokov, pričom najmladší mal 46 a najstarší 93 rokov. Dvom pacientom bol stent zavedený do oblasti sigmy, po jednom do stenóz uložených v konečníku, zostupnej časti hrubého čreva a lienálnej flexury. V štyroch prípadoch išlo už o liečených pacientov v predchádzajúcom období. Z toho dvaja sa pôvodne podrobili primárnym paliatívnym resekčným výkonom, pričom stent sme zaviedli do stenóz v dôsledku recidívy v mieste anastomózy. Tretiemu pacientovi bol stent zavedený do metachrónneho nálezu v čase, keď už bola z pohľadu internistu možná ďalšia operácia len z vitálnej indikácie. Jednej predliečenej pacientke bol stent zavedený do stenotizujúceho nádoru po ukončenej paliatívnej externej rádioterapii. Všetky výkony sme uskutočnili elektívne po predchádzajúcej príprave hrubého čreva makrogolovým preparátom.
Obr. 1. Kolorektálny stent – Enterella (Ella-CS). Fig. 1. Colorectal stent – Enterella (Ella-CS). 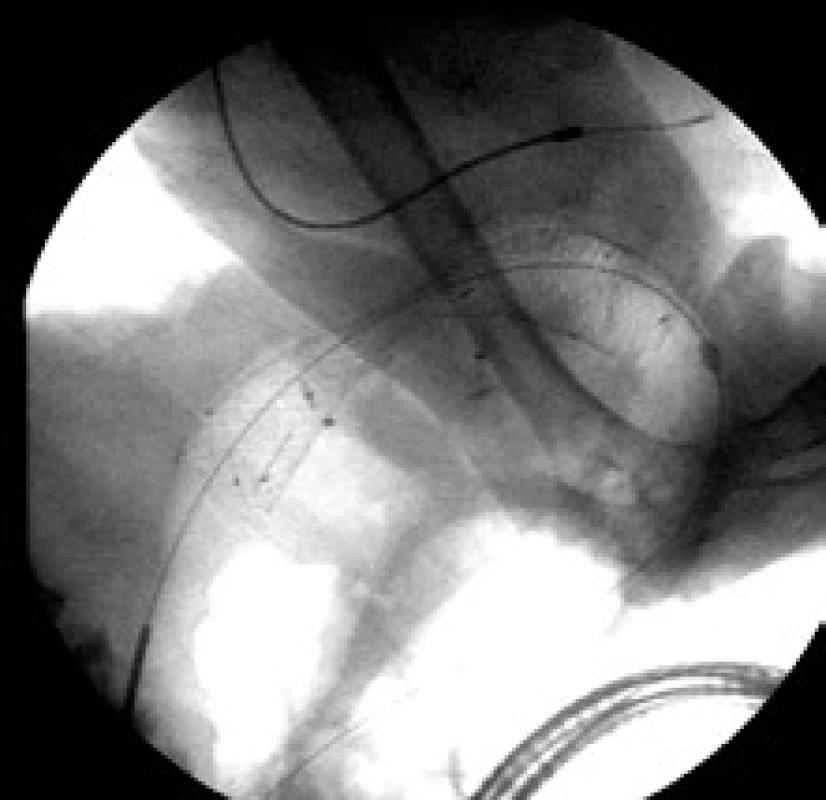
Obr. 2. Endoskopický obraz rozvinutého stentu. Fig. 2. Endoscopic image of developed stent. 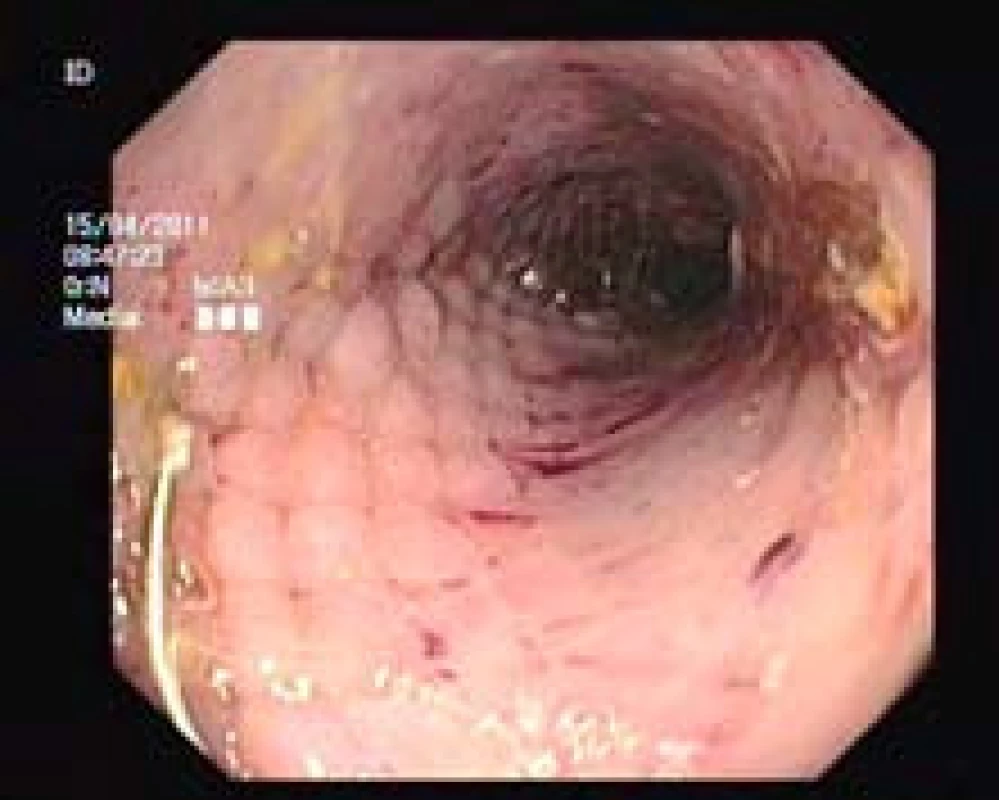
Stenty sme zavádzali na röntgenologickom pracovisku kombinovaným spôsobom za použitia kolonoskopu a flouroskopickej kontroly. Každého výkonu sa zúčastnili dvaja lekári a dve asistujúce sestry. Po endoskopickej vizualizácii stenózy sa nám v štyroch prípadoch podarilo stenózou prejsť kolonoskopom a v jednom prípade bola stenóza tak tesná, že to nebolo možné. Za pomoci röntgen-kontrastných hemoklipov sme si pred zavedením stentu označili oba konce stenózy. V jednom prípade sme dľžku stenózy určili po irigografickom vyšetrení, pri ktorom bola použitá jódová kontrastná látka. Stenty boli následne zavádzané po vodiči, ktorý sme zaviedli cez pracovný kanál kolonoskopu. Pod fluoroskopickou kontrolou sme sledovali postup zavádzacieho mechanizmu k stenóze, umiestnenie a uvoľnenie stentu v správnej polohe. V jednom prípade sa nám týmto spôsobom nedarilo zaviesť stent pre ostré angulácie pred stenózou, ktorá bola v oblasti lienálnej flexury. Pravdepodobne boli spôsobené prerastaním nádoru do okolia a fixáciou tumorózne zmenenej kľučky hrubého čreva. Preto sme opätovne zaviedli kolonoskop a kliešťami sme uchopili zavádzač. Týmto spôsobom sa nám podarilo nakoniec stent umiestniť a následne uvoľniť v mieste stenózy. Vo všetkých prípadoch sme stenty naložili v správnej pozícii na prvý pokus, bez potreby repozície. Priechodnosť stentu sme po výkone kontrolovali irigograficky ihneď po výkonoch, pričom sme znovu použili vodnú jódovú kontrastnú látku. Stenty sme zavádzali pacientom v sedácii. Použili sme midazolam v dávke cca 1 mg na 10 kg hmotnosti. Pacienti boli počas výkonu monitorovaní za použitia pulzného oxymetra. U žiadneho nebolo nutné podávanie analgetík po aplikácii stentu.
Výsledky
Stenty sme zaviedli úspešne všetkým pacientom (technická úspešnosť 100 %). Deň po výkone sme kontrolovali polohu stentu natívnou snímkou brucha. U všetkých pacientov došlo k regresii hladiniek. Bezprostredne po výkonoch nedošlo k žiadnym komplikáciám. Nezaznamenali sme žiadnu perforáciu, krvácanie ani žiadnu inú komplikáciu, ktorá by vyžadovala následnú endoskopickú či chirurgickú intervenciu. U jedného pacienta došlo na tretí deň po inzercii stentu k infarktu myokardu. Išlo o 90-ročného pacienta s karcinómom lienálnej flexúry. Mal ischemickú chorobu srdca a implantovaný kardiostimulátor pre AV blokádu II. stupňa. K implantácii stentu sme sa rozhodli pre vysokú rizikovosť pacienta k operácii. Na ôsmy deň exitoval v dôsledku komplikácií po infarkte myokardu.
Pacienti, ktorým sme zaviedli stenty, boli hospitalizovaní na chirurgickom, onkologickom a jedna pacientka na rádioterapeutickom oddelení. Bezprostredne po ukončení výkonov sa vrátili späť na oddelenia, kde boli ďalej sledovaní. Dľžka hospitalizácie u našich pacientov bola 2, 5, 8 (+), 9 a 11 dní. Všetci pacienti okrem jedného, ktorý exitoval, boli prepustení do ambulantnej starostlivosti onkológa. Pacienti exitovali 8, 16, 87, 102 a 208 dní po zavedení stentu. Traja pacienti exitovali na komplikácie základného ochorenia. U jedného pacienta, ktorý nebol sledovaný na našom ústave, sa nám nepodarilo okrem dňa úmrtia získať ďalšie informácie, posledný zomrel na infarkt myokardu.
Diskusia
V súčasnosti sú k dispozícii stenty od rôznych výrobcov (tab. 1). Prevažne sú vyrobené z nitinolu a bývajú nepovlečené. Je to dané vysokým stupňom migrácie povlečených stentov. Priemer zavádzacieho systému niektorých stentov umožňuje ich zavedenie cez pracovný kanál endoskopu. Konečný priemer stentu po inzercii býva 20–30 mm, hoci ideálny priemer je neznámy.
Tab. 1. Prehľad dostupných stentov [9]. Tab. 1. Overview of available stents [9]. ![Prehľad dostupných stentov [9].
Tab. 1. Overview of available stents [9].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/535ff5ede03c7503c91b3348b6067d0e.png)
SEMS možno zaviesť pod fluoroskopickou kontrolou alebo kombinovaným spôsobom za endoskopickej asistencie. V porovnaní s pažerákom býva zavedenie SEMS v hrubom čreve omnoho náročnejšie. Je to podmienené samotnou anatómiou hrubého čreva a skutočnosťou, že mnoho nádorov býva uložených v ohyboch. Pri zavádzaní SEMS v rekte je vhodné dodržať minimálne 2cm odstup medzi distálnym okrajom stentu a análnym kanálom. Predíde sa tým nepríjemným tenezmom a prípadnej inkontinencii.
V súčasnosti je k dispozícii niekoľko prác z viacerých endoskopických centier popisujúcich úspešné riešenie malígnej stenózy u pacientov s nonresekabilným ochorením. V analýze retrospektívnych štúdií publikovaných pred rokom 2003 sa dosahuje kumulatívna technická a klinická úspešnosť na úrovni 93 % a 89 % pacientov [5]. Svoje skúsenosti publikoval aj Baron et al z Mayo Clinic v roku 2010. Zaviedli 168 stentov, pričom úspešnú paliáciu dosiahli u 96 % pacientov po aplikácii jedného stentu. Medián udržania priechodnosti stentu udávajú 145 dní [6]. Zaujímavé sú porovnania chirurgického a endoskopického riešenia malígnej stenózy v paliatívnej intencii. Randomizovaná štúdia z Nizozemska musela byť predčasne ukončená pre vysoký počet perforácií po zavedení SEMS. Významnou limitáciou tejto štúdie bola skutočnosť, že do nej boli zaradení len pacienti s hroziacou ľavostrannou obštrukciou [7]. V ďalšej, retrospektívnej porovnávacej štúdii Faragher et al popisujú rovnakú dľžku prežívania v oboch skupinách. Významným benefitom v skupine pacientov po zavedení SEMS je kratšia dľžka hospitalizácie (4 vs 13,5 dní). Ďalším prínosom v porovnaní s chirurgickým výkonom je významne nižšie riziko potreby stómie. U operovaných bývajú aj častejšie pooperačné komplikácie: pneumónia a infekcia v rane [8].
Komplikácie súvisiace so zavedením SEMS sa rozdeľujú na včasné (< 30 dní) a neskoré (> 30 dní). Ďalej ich je vhodné deliť na nezávažné a závažné (tab. 2). Nezávažné komplikácie nevyžadujú následnú intervenciu. Závažné vyžadujú rádiologickú, endoskopickú, chirurgickú intervenciu, prípadne hospitalizáciu. Najvážnejšou komplikáciou je smrť pacienta, ktorá je našťastie zriedkavá [9]. Faktory, ktoré zvyšujú riziko komplikácií, sú viaceré. Patria k nim aj skúsenosti endoskopistu. Excesívna manipulácia pri zavádzaní stentu môže viesť k perforácii. Ide najmä o nešetrné a opakované pokusy zaviesť vodič alebo stent, cez stenózu. Taktiež nepresné umiestnenie stentu vedie k skorej migrácii, prípadne neskôr k tumoróznemu prerastaniu na koncoch stentu a jeho znefunkčneniu. Dôležitým faktorom je aj výber vhodného stentu. Niektoré bývajú príliš rigídne, aby sa mohli prispôsobiť prirodzeným ohybom hrubého čreva. V štúdii Smalla a Barona uvádzajú, že použitie Wallstent od Boston Scientific bolo spojené s technickými problémami ako nedostatočná postprocedurálna expanzia a nesprávna poloha stentu v stenóze. Taktiež pri použití Ultraflex stentu popisujú vyššiu incidenciu výskytu veľkých komplikácií, ako je perforácia, oklúzia stentu a jeho migrácia. Niektoré komplikácie môžu byť vysvetlené malým kalibrom tela stentu (22 mm) [10]. Potiahnuté stenty, ktoré sa začali používať s úmyslom znížiť riziko vrastania tumoru cez sieť stentu, majú vyššiu incidenciu migrácie [11]. Rozhodujúcim faktorom, ktorý zvyšuje neúspech endoskopickej liečby, je aj charakter stenózy. Tie, ktoré vznikajú na podklade extraluminálneho útlaku hrubého čreva, sú spojené s nižším úspechom, vyšším počtom komplikácií a nutnosťou definitívneho chirurgického riešenia [5]. Dlhé stenózy (> 10 cm) majú taktiež horšie výsledky ako kratšie [12]. Pravdepodobne to bude podmienené skutočnosťou, že takto dlhé stenózy často zasahujú do prirodzených ohybov hrubého čreva. Predpokladať sa dá aj to, že čím je stenóza závažnejšia, resp. užšia, tým sú výsledky liečby horšie (rovnako ako v iných lokalitách zažívacieho traktu). Najčastejšou závažnou komplikáciou býva migrácia stentu. Pri nepovlečených stentoch sa udáva 3–12 %. U povlečených sa udával vysoký stupeň migrácie až na úrovni 30–50 % [5]. K migrácii mnohokrát dochádza včasne po inzercii stentu pri jeho nesprávnom uložení. Odporúča sa aplikovať stent minimálne 2 cm nad okraj aj pod oba okraje stenózy do zdravého čreva a centrovať ho do najužšieho miesta. Migrácia sa častejšie pozoruje po chemoterapii a po aplikácii laseru pred naložením stentu [5]. Klinicky sa prejavuje príznakmi rekurentnej obštrukcie hrubého čreva, ale po chemoterapii a regresii tumoru môže byť priebeh aj asymptomatický. Najzávažnejšou komplikáciou je perforácia, ktorá nezriedka končí fatálne. K perforácii obvykle dochádza v priebehu prvých troch dní po inzercii. Incidencia sa pohybuje v rozmedzí 5–16 %. Najrizikovejšia je rektosigmoidálna oblasť. Ostatnou závažnou komplikáciou je reobštrukcia. Môže k nej dôjsť na podklade malígneho prerastania tumoru cez sieť stentu. V dostupnej literatúre sú popísané aj prípady fragmentácie stentu [9]. Ak dôjde k reobštrukcii malígnym tkanivom, postup je rovnaký ako pri riešení podobnej komplikácie napríklad v pažeráku. K obnoveniu priechodnosti stentu sa teda dá použiť laser, APC alebo sa zavedie stent do stentu. Endoskopicky nezvládnuteľné stavy vyžadujú chirurgickú intervenciu.
Tab. 2. Komplikácie po zavedení stentu v súbore Lopera et al [9]. Tab. 2. Complications after stent application in the group of patients studied by Lopera et al [9]. ![Komplikácie po zavedení stentu v súbore Lopera et al [9].
Tab. 2. Complications after stent application in the group of patients studied by Lopera et al [9].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/e3a08d0c82c0a3b6c24a7de0d554ce62.png)
Najčastejšou nezávažnou komplikáciou býva krvácanie. Môže k nemu dôjsť tlakom stentu na krehké nádorové tkanivo včasne po inzercii stentu. Zväčša ide o stav, ktorý sa zvládne konzervatívne. Chirurgická intervencia je skôr výnimkou. K výraznejšiemu krvácaniu dochádza pri traumatizácii steny hrubého čreva koncami stentu. V týchto situáciách býva nezriedka nevyhnutné chirurgické riešenie. Bolesť po aplikácii stentu je prevažne prechodná, ktorá reaguje na podanie analgetík. Pretrvávajúca bolesť, resp. nereagujúca na medikáciu, môže svedčať na prítomnosť závažnej komplikácie, akou je perforácia. Aplikácia stentu blízko anorektálneho prechodu môže mať za následok tenezmy, prípadne rôzne senzácie z cudzieho predmetu v konečníku. Pri nesprávnom diétnom režime môže dôjsť k obštrukcii stentu bolusom stolice. Niektoré prípady vyžadujú urgentnú endoskopickú intervenciu. Pri čiastočnej obštrukcii sa vystačí s lavážou hrubého čreva so salinickým preháňadlom. Vhodné je takýmto stavom predchádzať odporučením bezzvyškovej stravy a užívaním laxatív na báze laktulózy. K ďalším nezávažným komplikáciám sa radí bakteriémia spojená s horúčkami. Z tohto dôvodu niektorí autori odporúčajú podanie širokospektrálnych antibiotík v periprocedurálnom období [13].
V súbore našich pacientov sme zaznamenali jednu včasnú závažnú komplikáciu, ktorá viedla k úmrtiu (infarkt myokardu). Inak neboli zaznamenané žiadne komplikácie. Stent bol však zavedený len malému počtu pacientov, čo ovplyvňuje uvedené výsledky.
Vychádzajúc z dát retrospektívnych štúdií možno povedať, že riešenie malígnej obštrukcie hrubého čreva zavedením SEMS s paliatívnym úmyslom je bezpečnou a efektívnou liečebnou metódou. Zavedenie stentu do oblasti pravého kolon má porovnateľnú úspešnosť ako zavedenie do ľavého. Pri výbere spôsobu liečby, stent vs chirurgia, treba brať do úvahy skúsenosti endoskopického pracoviska, krvácanie z tumoru (nedá sa riešiť zavedením stentu), prípadne zvažovanú onkologickú liečbu (chemoterapia zvyšuje riziko perforácie a migrácie) [14].
Záver
V ostatnom čase sa implantácia stentu do malígnej stenózy v hrubom čreve u pacientov s pokročilým ochorením stáva štandardným spôsobom liečby. Pri akceptovateľnom množstve komplikácií má oproti chirurgickému riešeniu niektoré výhody. V popredí je najmä rýchla úprava, resp. úľava ťažkostí pacienta. Ďalej ide o možnosť krátkodobej hospitalizácie. Tieto dva faktory sú pre pacientov vo veľakrát zlom celkovom stave s krátkodobou expektáciou života rozhodujúce. Z pohľadu ekonomiky je zavedenie stentu v paliatívnej indikácii lacnejšie oproti chirurgickému výkonu. Binkert udáva 20–30 % redukciu nákladov, ak sa použije stent [15]. Aj keď ekonomický aspekt je v dnešnej dobe významným faktorom pri výbere spôsobu liečby, nemal by byť tým rozhodujúcim. Tým by mala byť správna indikácia a skúsenosti endoskopického pracoviska, pričom by sa mala rešpektovať predpokladaná dľžka dožitia a v neposlednom rade postoj pacienta.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 9. 10. 2012
Přijato: 5. 1. 2013
MUDr. Ľuboš Žitňan
Endoskopické poliklinické oddelenie
Gastroenterologická ambulancia
Národný onkologický ústav
Klenová 1833 10 Bratislava
lubos.zitnan@nou.sk
Zdroje
1. Cheynel N, Cortet M, Lepage C et al. Trends in frequency and management of obstructing colorectal cancers in a well-defined population. Dis Colon Rectum 2007; 50(10): 1568–1575.
2. Šálek T, Hlavatá Z. Systémová terapia karcinómu konečníka a hrubého čreva. In Bolješíková E, Májek J, Makovník P et al. Gastrointestinálna onkológia. Infoma 2008: 136–142.
3. Pirlet IA, Slim K, Kwiatkowski F et al. Emergency preoperative stenting versus surgery for acute left-sided malignant colonic obstruction: a multicenter randomized controlled trial. Surg Endosc 2011; 25(6): 1814–1821.
4. van Hooft JE, Bemelman WA, Oldenburg B et al. Colonic stenting versus emergency surgery for acute left sided malignantcolonic obstruction: a multicentre randomized trial. Lancet Oncol 2011; 12(4): 344–352.
5. Sebastain S, Johnston S, Georghegan T et al. Pooled analysis of the efficacy and safety of self-expanding metal stenting in malignant colorectal obstruction. Am J Gastroenterol 2004; 99(10): 2051–2057.
6. Baron TH. Colonic Stenting: a palliative measure only or a bridge to surgery? Endoscopy 2010; 42(2): 163–168.
7. van Hooft JE, Fockens P, Marinelli AW et al. Early closure of multicenter randomized clinical trial of endoscopic stenting versus surgery for stage IV left-sided colorectal cancer. Endoscopy 2008; 40(3): 184–191.
8. Faragher IG, Chaitowitz IM, Stupart DA. Long term results of palliative stenting or surgery for incurable obstructing colon cancer. Colorectal Dis 2008; 10(7): 668–672.
9. Lopera JE, De Gregario MA. Flouroscopic management of complication after Colorectal Stent placement. Gut Liver 2010; 4 (Suppl 1): S9–18.
10. Small AJ, Baron TH. Comparison of Wallstent and Ultraflex Stents for palliation of malignant left-sided colon obstruction: a retrospective, case-matched analysis. Gastrointest Endosc 2008; 67(3): 478–488.
11. Lee KM, Shin SJ, Hwang JC et al. Comparison Of uncovered stent with covered stent for treatment of malignant colorectal obstruction. Gastrointest Endosc 2007; 66(5): 931–936.
12. Jung MK, Park SY, Jeon SW et. al. Factors associated with the long term outcome of a self-expandable colon stent used for palliation of malignant large bowel obstruction. Surg Endosc 2010; 24(3): 525–530.
13. Small AJ, Coelho-Prabhu N, Baron TH. Endoscopic placement of selfexpandable metal stents for malignant colonic obstruction:long-term outcomes and complication factors. Gastrointest Endosc 2010; 71(3): 560–572.
14. Cennamo V, Fuccio L, Mutri V et al. Does stent placement for advanced colon cancer increse the risk of perforation during bevacizumab based therapy? Clin Gastroenterol Hepatol 2009; 7(11): 1174–1176.
15. Binkert CA, Ledermann H, Jost R et al. Acute colonic obstruction: clinical aspects and cost-effektivenessof preoperative and palliative treatment with self-expanding metallic stents – a prelimenary report. Radiology 1998; 206(1): 199–204.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2013 Číslo 1- Hydrofilní gel má pozitivní vliv na uzavírání rány a vzhled jizvy
- Jak souvisí postcovidový syndrom s poškozením mozku?
- Vliv pantoprazolu na duální antiagregační léčbu u pacientů se stabilní anginou pectoris po perkutánní koronární intervenci
- Inhibitory protonové pumpy zkracují délku Barrettova jícnu
- Kožní problematika u pacientů s idiopatickými střevními záněty
-
Všechny články tohoto čísla
- Sérové protilátky proti zymogenovému glykoproteinu 2 (anti-GP2) u nemocných s idiopatickými střevními záněty
- Recidivující subileózní stavy na tenkém střevě mohou skýtat překvapení
- Hodnocení slizničního hojení v průběhu biologické léčby Crohnovy choroby tenkého střeva pomocí kapslové endoskopie: prospektivní observační studie
- Mesalazin u Crohnovy nemoci: obsolentní nebo neprávem opomíjená léčba?
- Současný pohled na léčbu perianálních píštělí u nemocných s Crohnovou chorobou
- Akutní krvácení do GIT a změny v lipidovém spektru – pilotní projekt
- Perforující gangrenózní cholecystitida
- Dysfunkce horní části trávicího traktu u kriticky nemocných: současný pohled a perspektiva
- 18FDG-PET/CT diagnostika adenokarcinomu pankreatu
- Stenty v liečbe zhubných nádorov kolorekta – prehľad a vlastné skúsenosti
- Metastáza maligního melanomu v bulbu duodena jako vzácná příčina obstrukce výtokového traktu žaludku
- Segmentálna portálna hypertenzia
- Plány a představy redakční rady na rok 2013
-
Imunosupresivní a biologická léčba u CN „šitá na míru“.
Komentář ke studii STORI - Aminosalicyláty v liečbe aktívnej Crohnovej choroby – kedy a prečo nie
- Komentář: Perforující gangrenózní cholecystitida
- UEGW Amsterdam 2012 – pohled z jiné strany
- Gastrofórum – Pankreatofórum v januári 2013
- Správná odpověď na kvíz
- Leading change in IBD
- Pangrol 20000
- Za vším hledej peníze (... a nebo ženu)
- Autodidaktický test: idiopatické střevní záněty
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Segmentálna portálna hypertenzia
- Současný pohled na léčbu perianálních píštělí u nemocných s Crohnovou chorobou
- Perforující gangrenózní cholecystitida
- Recidivující subileózní stavy na tenkém střevě mohou skýtat překvapení
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



