-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Progresivní multifokální leukoencefalopatie – editorial
Autoři: Pavel Polák
Působiště autorů: Oddělení klinické hematologie FN Brno
Vyšlo v časopise: Vnitř Lék 2017; 63(1): 22-23
Kategorie: Editorialy
Komentář k | Editorial on
Sokol J et al. Rituximab-associated progressive multifocal leukoencephalopathy. Vnitř Lék 2017; 63(1): 60–64.
Progresivní multifokální leukoencefalopatie (PML) patří stále k velmi vzácným onemocněním. Virus byl poprvé prokázán v roce 1971 u pacienta s chronickou lymfatickou leukemií [1]. V 90. letech 20. století byl zaznamenán epidemický výskyt PML u pacientů infikovaných lidským virem imunitní nedostatečnosti (human immunodeficiency virus – HIV), a proto PML patří mezi tzv. onemocnění indikativní pro AIDS [2]. V rámci diferenciální diagnostiky PML je tedy vždy nezbytné nákazu HIV vyloučit. S vývojem transplantační medicíny a imunosupresivní a imunomodulační terapie se spektrum pacientů ohrožených PML výrazně rozšiřuje – incidenci PML v těchto jednotlivých skupinách uvádí tab. Z tohoto důvodu představuje případ prezentovaný slovenskými kolegy s největší pravděpodobností spíše pověstnou špičku ledovce.
Tab. 1. Incidence PML u různých skupin nemocných. 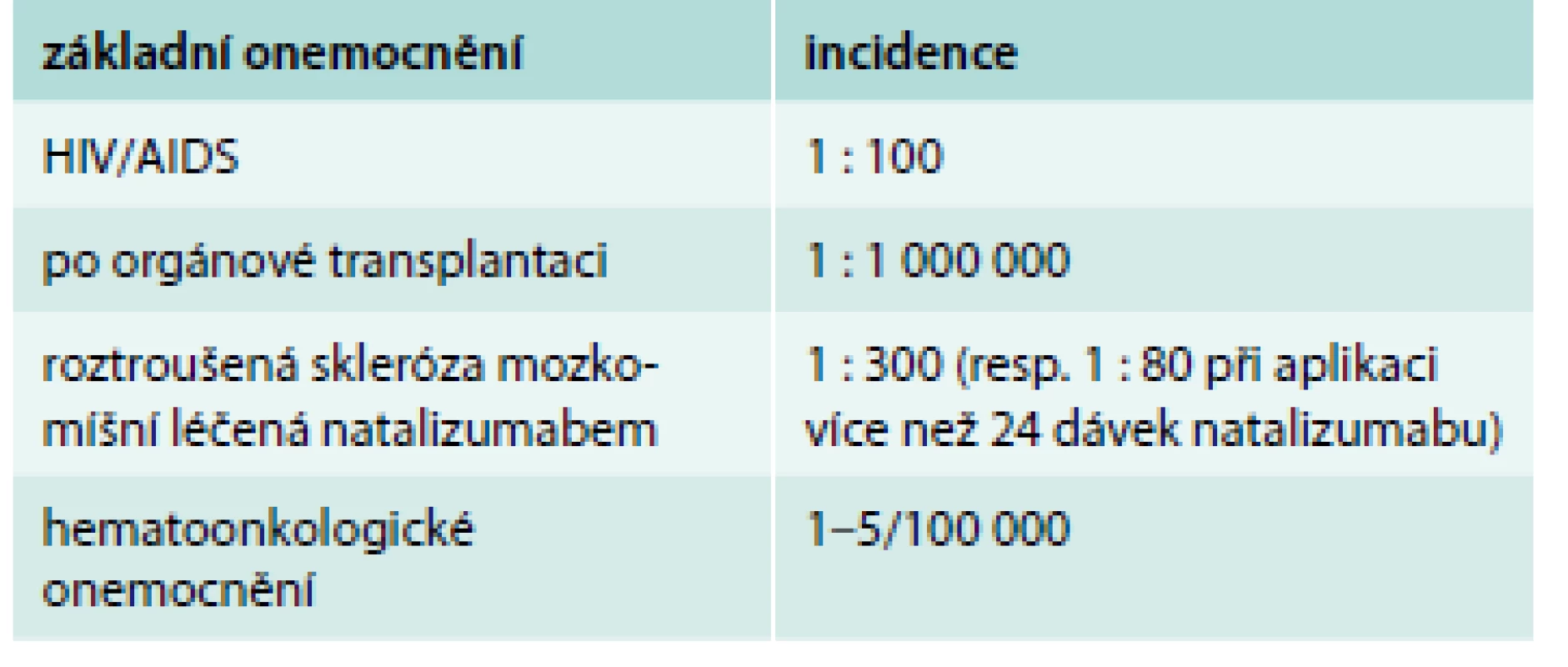
Upraveno dle [3] Samotný původce PML, označovaný jako JC virus (iniciály pacienta Johna Cunninghama, od nějž byl virus poprvé izolován), patří do čeledi polyomavirů (v literatuře lze rovněž nalézt zkratku JCpyV odpovídající JC-polyomaviru). Jedná se o neobalený virus, jehož genetická informace je nesena dvouvláknovou deoxyribonukleovou kyselinou (deoxyribonucleic acid – DNA). Z epidemiologických studií vyplývá vysoká promořenost populace celosvětově (dosahující až 60–70 %), patogenita viru je však nízká – jedná se tedy o velmi úspěšný patogen [2]. Primoinfekce nastává po vstupu viru do makroorganizmu v oblasti orofaryngu a není doprovázena specifickými příznaky. Část nakažených jedinců vylučuje virus močí i několik týdnů a stává se tak asymptomatickým zdrojem nákazy, která nemusí být nutně doprovázena sérokonverzí. Následuje fáze tzv. virové latence, během níž virus přetrvává v buňkách kostní dřeně či sekundárních lymfatických orgánů a jeho replikační aktivita je nulová či velmi nízká. Při poruše imunitních regulací (pokles počtu CD4+/CD8+ T-lymfocytů, biologická terapie apod) dochází k dynamické replikaci viru a k jeho diseminaci. Způsob přestupu viru do tkání centrální nervové soustavy (CNS) není jednoznačně objasněn, spekuluje se o přímém průniku viru nebo o jeho transportu přes hematoencefalickou bariéru infikovanými lymfocyty, monocyty nebo endoteliemi. V CNS jeví virus zvláštní afinitu k astrocytům a oligodendrocytům, v nichž nastává tzv. lytická replikační fáze doprovázená balonovou degenerací a následně i lýzou postižených buněk. Replikace viru je pomalá a trvá řádově týdny. Tyto základní patofyziologické mechanizmy rozvoje PML vysvětlují, proč je vývoj klinického stavu zpravidla postupný (subklinický). V této době lze i u těžce imunokompromitovaných prokázat výrazný vzestup titru protilátek anti-JCV v séru i v likvoru (je pozitivní index intratekální syntézy); naopak virus nemusí být nutně průkazný v moči (pomocí polymerázové řetězové reakce/polymerase chain reaction – PCR, detekční limity současných metod jsou 10 kopií viru/ml). Bylo prokázáno, že absolutní počet kopií viru v moči nekoreluje s výší titru protilátek v séru a dále že nepřítomnost viru v moči zcela nevylučuje možnost rozvoje PML. Diagnostiku dále znesnadňuje možnost přítomnosti JCV-DNA v likvoru i u jedinců bez klinických či radiologických známek PML. Samotný virus vykazuje vysokou mutační aktivitu a perzistuje intracelulárně, proto nedochází k jeho absolutní neutralizaci a eradikaci již vytvořenými protilátkami [3–6,9,10].
Mezi rizikové faktory pro rozvoj PML patří pozitivita protilátek proti JCV v séru, předchozí imunosupresivní terapie a délka léčby natalizumabem [4]. Pro samotný rozvoj onemocnění musí být splněno několik podmínek:
- porucha imunitního systému hostitele (nejvýznamnější faktor)
- mutační aktivita viru se zvýšenou replikací v B-lymfocytech a postižených gliových buňkách
- přítomnost viru v CNS
- zvýšená koncentrace tzv. DNA vázajících faktorů [2]
Podezření na PML by mělo být vždy vyjádřeno u imunokompromitovaného pacienta s atypickým klinickým neurologickým nálezem a s multifokálními lézemi CNS zjištěnými pomocí magnetické rezonance. A naopak – u všech pacientů s multifokálními lézemi CNS a s atypickým klinickým neurologickým nálezem musí být vyloučen těžký imunodeficit včetně onemocnění HIV/AIDS.
Kauzální léčba této infekce není známa. U pacientů léčených natalizumabem (a pravděpodobně i u pacientů léčených efalizumabem) lze provést výměnné plazmaferézy (5 cyklů). Naopak u pacientů léčených rituximabem nemá pro krátký biologický poločas léčiva plazmaferéza prakticky žádný význam. Během plazmaferézy dochází však i ke clearance protilátek anti-JCV a další sérologické testy mohou být falešně negativní [4,7]. Oproti tomu je po nitrožilní aplikaci imunoglobulinů (IVIG) možná falešná pozitivita protilátek anti-JCV. Postupem času od aplikace IVIG dochází k poklesu titru těchto protilátek a je možná i séroreverze do jejich neprůkaznosti. Vyšetření protilátek anti-JCV by tedy nemělo být provedeno dříve než 30 dnů po aplikaci IVIG. Vliv ostatních krevních derivátů a přípravků na hladiny protilátek anti-JCV není plně vyloučen, a proto by mělo být sérologické vyšetření prováděno opakovaně se zohledněním uvedené léčby a klinického stavu [8].
Pravidelnou a velmi závažnou komplikací léčby PML (zvláště po plazmaferéze) je rozvoj imunorestitučního zánětlivého syndromu (immune restoration inflammatory syndrome – IRIS). Tento stav nastává při obnovení imunitních funkcí s následnou excesivní zánětlivou aktivitou destruktivně působící na tkáně, ve kterých IRIS probíhá. V případě PML dochází po jisté době stabilizace klinického stavu k další prudké deterioraci s možným fatálním vyústěním [4].
Prognóza onemocnění je velmi vážná, přibližně 20 % nemocných umírá na PML a na přidružené (zpravidla infekční) komplikace.
Přestože několik případů PML bylo popsáno i v českém písemnictví, je toto onemocnění natolik vzácné, že jeho diagnostika klade extrémní nároky na ošetřující lékaře různých odborností (i s ohledem na dlouhou fázi preklinického rozvoje PML) [11–14]. Je tedy obdivuhodné, že se navzdory veškerým nesnázím podařilo slovenským kolegům případ diagnosticky uzavřít a že nám jej nabízejí k poučení.
MUDr. Pavel Polák, Ph.D.
pavel.polak@fnbrno.cz
Oddělení klinické hematologie FN Brno
www.fnbrno.cz
Doručeno do redakce 21. 3. 2016
Zdroje
1. Padgett BL, Walker DL, ZuRhein GM et al. Cultivation of papova-like virus from human brain with progressive multifocal leucoencephalopathy. Lancet 1971; 1(7712): 1257–1260.
2. Ferenczy MW, Marshall LJ, Nelson ChDS et al. Molecular biology, epidemiology, and pathogenesis of progressive multifocal leukoencephalopathy, the JC virus-induced demyelinating disease of the human brain. Clin Microbiol Rev 2012; 25(3): 471–506. Dostupné z DOI: <http://dx.doi.org/10.1128/CMR.05031–11>.
3. Monaco MC, Major EO. Immune system involvement in the pathogenesis of JC virus induced PML: what is learned from studies of patients with underlying diseases and therapies as risk factors. Front Immunol 2015; 6 : 159. Dostupné z DOI: <http://dx.doi.org/10.3389/fimmu.2015.00159>.
4. Kornek B. An update on the use of natalizumab in the treatment of multiple sclerosis: appropriate patient selection and special considerations. Patient Prefer Adherence 2015; 9 : 675–684. Dostupné z DOI: <http://dx.doi.org/10.2147/PPA.S20791>.
5. Berger JR, Sidney MD, Houff MD et al. JC virus antibody status underestimates infection rates. Ann Neurol 2013; 74(1): 84–90. Dostupné z DOI: <http://dx.doi.org/10.1002/ana.23893>.
6. Nakamichi K, Mizusawa H, Yamada M et al. Characteristics of progressive multifocal leukoencephalopathy clarified through internet-assisted laboratory surveillance in Japan. BMC Neurol 2012; 12 : 121. Dostupné z DOI: <http://dx.doi.org/10.1186/1471–2377–12–121>.
7. Fox R Advances in the management of PML: focus on natalizumab. Cleve Clin J Med 2011; 78(Suppl 2): S33-S37. Dostupné z DOI: <http://dx.doi.org/10.3949/ccjm.78.s2.08>.
8. Kister I, Kuesters G, Chamot E et al. IV immunoglobulin confounds JC virus antibody serostatus determination. Neurol Neuroimmunol Neuroinflammation 2014; 1(3): e29. Dostupné z DOI: <http://dx.doi.org/10.1212/NXI.0000000000000029>.
9. Bozic C, Subramanyam M, Richman S et al. Anti-JC virus (JCV) antibody prevalence in the JCV epidemiology in MS (JEMS) trial. Eur J Neurol 2014; 21(2): 299–304. Dostupné z DOI: <http://dx.doi.org/10.1111/ene.12304>.
10. Rossi F, Newsome SD, Viscidi R Molecular diagnostic tests to predict the risk of progressive multifocal leukoencephalopathy in natalizumab-treated multiple sclerosis patients. Mol Cell Probes 2015; 29(1): 54–62. Dostupné z DOI: <http://dx.doi.org/10.1016/j.mcp.2014.11.007>.
11. Štětkářová I, Medová E, Bučilová V et al. Progresivní multifokální leukoencefalopatie u nemocné s roztroušenou sklerózou léčenou natalizumabem. Čes Radiol 2013; 67(1): 35–38.
12. Vališ M, Belada D, Taláb R et al. Progresivní multifokální leukoencefalopatie jako komplikace léčby lymfomu – kazuistika. Česk Slov Neurol N 2009; 72/105(2): 159–161.
13. Táborský P, Hrabánek J, Jirásek A et al. Progresivní multifokální leukoencefalopatie u nemocné po transplantaci ledviny. Vnitř Lék 1998; 44(2): 108–110.
14. Horáková D, Havrdová E. Protilátky proti JC viru a stratifikace rizika progresivní multifokální leukoencefalopatie u pacientů s roztroušenou sklerózou. Doporučení k použití nového testu STRATIFY JCVTM. Neurol praxi 2011; 12(5): 364–365.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2017 Číslo 1- Přínos perorálního semaglutidu pro pacienty s DM 2. typu v ordinaci praktického lékaře
- Prognostický význam hladiny natriuretických peptidů při léčbě empagliflozinem
- Levothyroxin a zaměnitelnost přípravků s jeho obsahem
- Romosozumab zlepšuje kostní mikroarchitekturu u postmenopauzálních žen s osteoporózou
- S MUDr. Janem Rosou o problematice osteoporózy u revmatologických pacientů: Kdy začít s osteoanaboliky a jak minimalizovat selhání léčby?
-
Všechny články tohoto čísla
- Familiární hypercholesterolermie: z Čech a Moravy do celého světa – editorial
- Význam hodnocení ventilační efektivity VE/VCO2 slope u pacientů se srdečním selháním – editorial
- Progresivní multifokální leukoencefalopatie – editorial
- ScreenPro FH – projekt v oblasti screeningu zaměřený na familiární hypercholesterolemii ve střední, jižní a východní Evropě: základní epidemiologie
- Uzávěr ouška levé síně systémem AtriClip
- Léčba pacientů infikovaných virem hepatitidy C genotypu 2
- ScreenPro FH – projekt v oblasti screeningu zaměřený na familiární hypercholesterolemii ve střední, jižní a východní Evropě: odůvodnění a záměr
- Appendix diagnostica – Familial hypercholesterolemia diagnostic criteria
- Predátorské časopisy: praktiky jejich vydavatelů a jak se jim bránit
- Příspěvek k diferenciální diagnostice sklerozujících cholangitid
- Význam hodnocení ventilační efektivity VE/VCO2 slope u pacientů se srdečním selháním
- Progresívna multifokálna leukoencefalopatia spojená s rituximabom
- 2nd Prague European Days of Internal Medicine
- Spomienka na profesora MUDr. Karla Horkého, DrSc., FACP (Hon), FEFIM
- Z odborné literatury
- Z odborné literatury
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Uzávěr ouška levé síně systémem AtriClip
- Význam hodnocení ventilační efektivity VE/VCO2 slope u pacientů se srdečním selháním
- Progresívna multifokálna leukoencefalopatia spojená s rituximabom
- Příspěvek k diferenciální diagnostice sklerozujících cholangitid
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



