-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Ireverzibilní elektroporace: lokální, non-termální, ablační léčba maligních nádorů
Autoři: Václav Janík 1; Dana Škrabalová 1; Robert Gürlich 2; Jiří Málek 3
Působiště autorů: Radiodiagnostická klinika 3. LF UK a FNKV, Praha 1; Chirurgická klinika 3. LF UK a FNKV, Praha 2; Klinika anesteziologie a resuscitace 3. LF UK a FNKV, Praha 3
Vyšlo v časopise: Čas. Lék. čes. 2013; 152: 67-75
Kategorie: Původní práce
Souhrn
Východisko:
Ireverzibilní elektroporace (IRE) je nová, lokální léčebná metoda maligních nádorů, založena na bioelektrickém účinku elektrického proudu. Krátké elektrické pulzy o vysokém napětí vytváří v buněčných membránách nádorových buněk drobné póry o nano-rozměrech, jejichž výsledkem je apoptóza exponovaných buněk. Cílem naší studie bylo ověřit techniku IRE prováděnou perkutánně, pod CT navigací a zhodnotit výsledky této léčebné metody u primárních a sekundárních nádorů jater, pankreatu, ledvin a plic. Metody a výsledky: Od listopadu 2011 do října 2012 jsme IRE provedli pomocí NanoKnife (firma Angio-Dynamics) u souboru 15 pa-cientů – šest mužů a devět žen. IRE jsme prováděli v celkové anestezii pomocí dvou až pěti jehlových elektrod, které jsme pod CT navigací zavedli do nádorového ložiska. Výsledky léčby jsme hodnotili podle modifikovaných RECIST kritérii v 1-, 3 - a 6měsíčních intervalech. Kontrolní CTnebo MR vyšetření za 6 měsíců po IRE absolvovalo deset pa-cientů. Jeden pacient zemřel po měsíci na plicní embolii, dva se odmítli ke kontrolnímu vyšetření dostavit a u dvou bude 6měsíční kontrola teprve provedena. U těchto deseti vyšetřených pacientů byla IRE úspěšná u sedmi pacientů (70,0 %) a neúspěšná u tří pacientů (30,0 %). Závěr: IRE je nová, minimální invazivní léčebná metoda použitelná při lokální léčbě maligních nádorů v případech, kdy je chirurgický zákrok technicky neproveditelný nebo neúměrně rizikový. Na základě našich prvních zkušeností u nevelkého souboru pacientů můžeme konstatovat, že IRE prováděná pod CT navigací je efektivní a bezpečná ablační metoda s velkým terapeutickým potenciálem. Její výsledky bude však nutné posoudit v delším časovém úseku u většího souboru pacientů. Klíčová slova: maligní nádory – ireverzibilní elektroporace – NanoKnife – termoablační léčebné metodyÚVOD
Ablační léčebné metody nádorových lézí jsou alternativou pro pacienty, kteří nejsou kandidáty chirurgického odstranění nádorové tkáně, ať již vzhledem k nevhodné lokalizaci nádoru v blízkosti kritických tubulárních struktur (cévy a dukty), z důvodu technické neproveditelnosti, nebo neúměrného rizika. Mezi ablační léčebné metody patří intersticiální laserová koagulace, kryoablace, katetrizační chemoterapie s embolizací, radiofrekvenční ablace (RFA), mikrovlnná ablace (MA) a nově též ireverzibilní elektroporace (IRE). IRE, která je založena na bioelektrickém účinku elektrického proudu, přináší nové možnosti ablační léčby nádorů (1).Její princip spočívá v aplikaci milisekundových pulzů elektrického proudu o nízké intenzitě a vysokém napětí do oblasti nádorové tkáně pomocí technologie NanoKnife (2). Tyto vysokonapěťové elektrické pulzy jsou aplikovány jehlovými elektrodami, které jsou perkutánně zaváděny do oblasti nádorového ložiska pomocí CT nebo UZ navigace nebo také během otevřené operace (2, 3). Elektrické pulzy vytváří v buněčných membránách drobné otvory – póry o nano-rozměrech. Pokud je elektrické pole aplikováno odpovídajícím počtem pulzů a dostatečně dlouhou dobu, dochází k trvalému – ireverzibilnímu otevření těchto pórů v buněčných membránách. Výsledkem poškozené membránové permeability je porucha homeostázy exponovaných buněk a buněčná apoptóza (4). Mechanismus buněčné smrti není dosud jednoznačně objasněn, nicméně studie na zvířatech prokázaly, že buňky tkání exponovaných IRE vykazovaly ztrátu viability, zatímco pojivové a elastické struktury obsahující kolagen (např. cévy a žlučovody) zůstaly nepoškozené (5, 6). Protože fenomén elektroporace není založen na tepelném účinku, hovoří se o non-termální „studené“ ablační léčbě maligních nádorů.
SOUBOR NEMOCNÝCH A POUŽITÉ METODY
K IRE jsme použili NanoKnife (firmy AngioDynamics), který je určen k ablaci měkkotkáňových struktur. Přístroj NanoKnife disponuje mobilním generátorem stejnosměrného proudu, zobrazovacím monitorem, synchronizovanou EKG jednotku a nožním spínačem. Při jednotlivých elektroporacích jsme použili stejnosměrný proud (25–45 A) o napětí 1500–3000 V, který byl aplikován 90 pulzy (tj. devíti sekvencemi po deseti pulzech) při délce jednoho pulzu v rozmezí 30–100 µs. Tyto vysokonapěťové pulzy jsme aplikovali unipolárními18 G jehlovými elektrodami (AngioDynamics) délky 25 cm, které jsme pomocí CT navigace zavedli do nádorového ložiska. Přesné hodnoty dosaženého vysokého napětí potřebného k elektroporaci nádorového ložiska určuje test, který vychází z počítačového modelu vzdálenosti jehlových elektrod ve vztahu k velikosti nádorového ložiska. Vzdálenost mezi párem kladné a záporné elektrody nebyla u všech provedených elektroporací menší než 2 a větší než 2,4 cm. Podle velikosti nádoru jsme k elektroporaci nádorového ložiska použili nejméně dvě a nejvíce pět elektrod. Počet elektroporací se u jednotlivých nádorů lišil podle jejich velikosti a podle hodnot elektrického pole dosažených u každé série pulzů. Během IRE jsme použili napětí stejnosměrného proudu v hodnotách od 1200 V do 3000 V podle rezistence tkáně a stupně dosažené buněčné membránové permeability. K IRE byli všichni pacienti našeho souboru indikováni na základě CT nebo MR nálezu maligní nádorové léze (játra, pankreas, plíce a ledviny), která nebyla řešitelná jinými léčebnými metodami (chirurgicky nebo onkologickou léčbou). Před IRE byla u všech pacientů provedena laboratorní vyšetření krve (včetně koagulace), moči, elektrolytů a funkční vyšetření jater a ledvin. Vzhledem k tomu, že nezbytnou podmínkou IRE je celková anestezie a hluboká svalová relaxace, byli všichni pacienti před zákrokem vyšetřeni také anesteziologem. Léčba IRE byla ve Fakultní nemocnici Královské Vinohrady zahájena na základě povolení etické komise. Pacienti byli před zákrokem seznámeni se všemi aspekty této léčebné metody včetně možných komplikací a svůj souhlas s léčbou potvrdili podpisem na formuláři informovaného souhlasu. Vlastní ireverzibilní elektroporaci jsme u všech pacientů souboru prováděli v celkové anestezii, dokonalé svalové relaxaci v synchronizaci s generátorem NanoKnife a s EKG přístrojem. Nejprve jsme provedli nativní a postkontrastní CT vyšetření, abychom mohli optimálně naplánovat směr punkce a určit počet jehlových elektrod ve vztahu k velikosti nádoru. Za sterilních podmínek jsme pod CT navigací paralelně, vždy v apnoi, zavedli do nádoru unipolární jehlové elektrody tak, aby vzdálenost mezi párem kladné a záporné elektrody nebyla menší než 2 cm a větší než 2,5 cm. Pokud následně provedený test vodivosti na monitoru NanoKnife ukázal, že hodnoty intenzity a napětí elektrického proudu nejsou k provedení IRE dostatečné, změnili jsme polohu jedné z elektrod a test zopakovali. Počet a rozmístění jehlových elektrod jsme plánovali podle software NanoKnife tak, aby ablační zóna pokrývala ve všech třech rozměrech celý nádor. U nádorů do velikosti 2 cm jsme obvykle použili dvě elektrody, u nádorů velikosti do 3 cm jsme použili tři jehlové elektrody, u objemnějších nádorů až pět elektrod. Při použití dvou elektrod jsme kladnou zavedli do horní periferní zóny nádoru, zápornou elektrodu k jeho dolnímu okraji. Délka aktivních úseků na koncích obou jehlových elektrod byla 1,5 cm. Následně jsme provedli první elektroporaci. Po jejím ukončení jsme elektrody povytáhli, podle velkosti nádoru, o 1–2 cm a následovala druhá elektroporace za stejných energetických parametrů. Vytvořená ablační zóna měla rektagonální, resp. válcovitý tvar, což potvrdilo následně provedené postkontrastní CT vyšetření (obr. 1).
Obr. 1. A – na axiálním CT skenu je patrná metastáza karcinomu prostaty v pravém jaterním laloku před IRE (šipka); B – počáteční uložení dvojice elektrod; C – konečná pozice dvojice elektrod; D – rozsah nekrózy po IRE 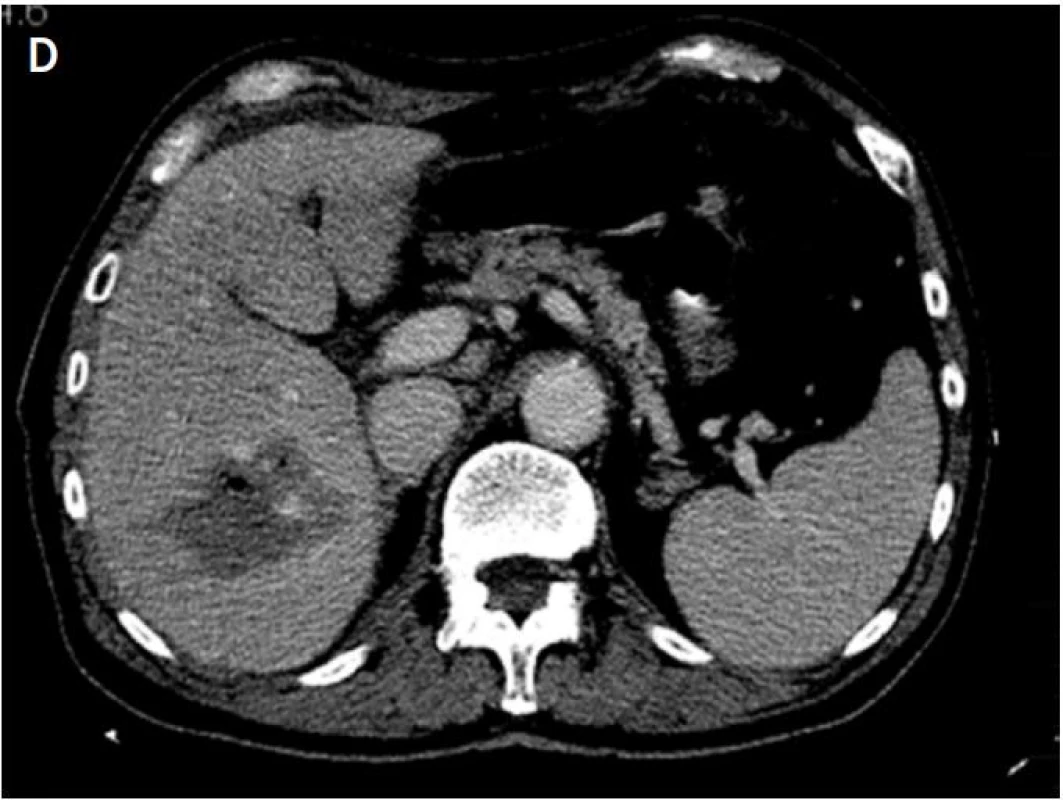
Hodnoty vysokého napětí a intenzity aplikovaného elektrického proudu a vzdálenost mezi elektrodami byly po každé IRE počítačově zpracovány a zaznamenány na monitoru. Délka jedné IRE se pohybovala mezi 2–3 min, délka zákroku v celkové anestezii byla 135 ± 10 min (medián 125 min). Po IRE byli pacienti převezeni na jednotku JIP a po 24 hodinách na standardní lůžko. Délka hospitalizace s pohybovala 2–7 dní podle toho, zda se po IRE objevila nějaká komplikace (např. PNO). Před propuštěním byli pacienti opět klinicky a laboratorně vyšetřeni (krev, moč a elektrolyty) a rovněž jim byla provedena funkční vyšetření jater, ledvin a CT vyšetření. Úspěšnost léčby jsme při kontrolním CT nebo MR vyšetření za 1, 3 a 6 měsíce hodnotili podle modifikovaných RECIST kritérií (7). Skupina A reprezentovala pacienty, u kterých byla IRE úspěšná. Na kontrolním CT nebo MR vyšetření byl patrný nález nekrózy nádoru bez známek postkontrastního enhacementu. Do skupiny B byli zařazeni pacienti, u kterých byla léčba částečně úspěšná, tzn., že v periferii nádorové nekrózy byly přítomny známky reziduálního enhacementu. Skupinu C tvořili pacienti, u kterých byla IRE neúspěšná, neboť nekróza centrální části nádoru byla neúplná a v místě původního nádoru byly výrazné známky postkontrastního enhacementu.
VÝSLEDKY
V období od listopadu 2011 do října 2012 jsme IRE provedli IRE u 15 pacientů – šest mužů a devět žen ve věku od 51 do 82 let (věkový průměr 66 let) s primárními nebo sekundárními maligními nádory jater, plic, ledvin a pankreatu. Ve všech případech byla IRE provedena perkutánně pod CT navigací. Jednu maligní lézi jsme léčili u jedenácti pacientů, dvě a více lézí u čtyř pacientů. U jedenácti pacientů jsme léčili metastázy v játrech, kdy se v devíti případech jednalo o metastázy karcinomu rekta, v jednom případě se jednalo o metastázu karcinomu prsu a o metastázu karcinomu prostaty. U dvou pacientů jsme léčili nádorové léze v plicích, kde se v jednom případě jednalo o metastázu karcinomu lienální flexury, ve druhém o karcinom plic. V ledvinách byla IRE provedena u pacienta s adenokarcinomem v solitární ledvině (obr. 2). a v jednom případě jsme pomocí IRE léčili karcinom pankreatu.
Obr. 2. A – na koronárním skenu je patrná metastáza adenokarcinomu v horním pólu solitární ledviny před IRE (šipka); B – uložení dvojice elektrod v oblasti nádoru; C – nekrotické ložisko v místě nádoru po IRE; D – při kontrolním MR vyšetření za 6 měsíců jen jizevnaté změny v oblasti původního nádoru (šipka) 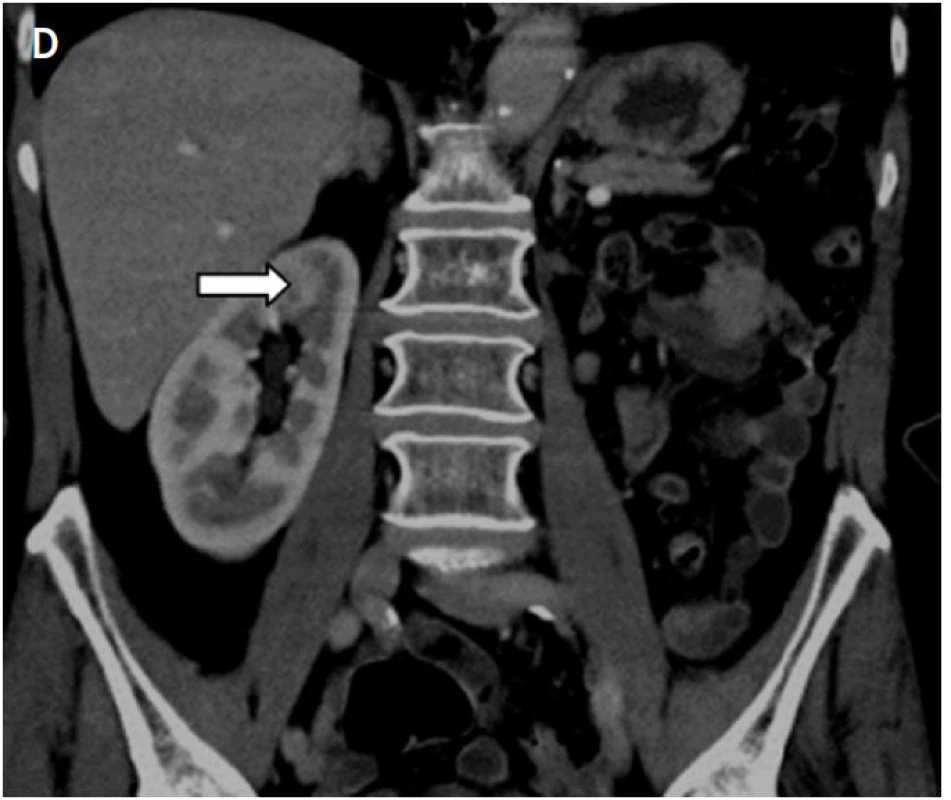
K IRE jsme použili dvě až pět jehel podle velikosti nádoru. Průměrná velikost léčených nádorů byla 4, 5 cm3 (od 2,5–88,5 cm3). Úspěšnost léčby IRE jsme hodnotili kontrolním CT nebo MR za 1, 3 a 6 měsíce podle modifikovaných RECIST kritérií (7). U souboru 15 pacientů bylo za 1 měsíc po IRE hodnoceno 14 pacientů, jeden se k vyšetření nedostavil. Podle modifikovaných RECIST kritérií byla IRE úspěšná u 13 pacientů (92,8 %) a neúspěšná u jednoho pacienta (7,2 %) s rychle progredující jaterními metastázami karcinomu štítné žlázy. Při kontrolních vyšetřeních CT a MR vyšetřeních za 3 měsíce po IRE bylo vyšetřeno 13 pacientů. Jedna pacientka nebyla vyšetřena z důvodu úmrtí na plicní embolii, další pacientka se ke kontrolnímu vyšetření nedostavila. IRE byla úspěšná u jedenácti pacientů (84,6 %), jedna pacientka (7,7 %) s progresí metastatického postižení jater u metastázy karcinomu mammy byla hodnocena jako částečně úspěšná, další pacientka (7,7 %) s metastázou karcinomu štítné žlázy byla hodnocena jako neúspěšná. Kontrolní CT nebo MR vyšetření za 6 měsíců bylo zatím provedeno u deseti pacientů. Jedna pacientka nebyla vyšetřena z důvodu úmrtí na plicní embolii, jeden pacient kontrolní vyšetření odmítl, další se přes opakované vyzvání k vyšetření nedostavil a u dvou pacientů teprve bude 6měsíční kontrola provedena. IRE byla úspěšná u sedmi pacientů (70,0 %) (obr. 3). U tří pacientů byla IRE neúspěšná (30,0 %). Jednalo se o pacienty s jaterními metastázami kolorektálního karcinomu, karcinomu štítné žlázy a karcinomu mammy. Kromě toho se u šesti pacientů při kontrolních CT nebo MR vyšetřeních objevily nové metastázy. U tří pacientů s původním karcinomem rekta se objevily nové metastázy v játrech, u jednoho karcinomem plic nová metastáza v kontralaterálním plicním křídle a u dalších dvou (s karcinomem štítné žlázy a s karcinomem mammy) se objevily nové metastázy v játrech (tab. 1). Nejčasnější nové metastázy se objevily již při kontrole za 1 měsíc u pacienta s primárním karcinomem štítné žlázy. Kromě postkontrastního enhacementu v oblasti původního nádoru se objevila řada dalších meta ložisek. Proto již nebyla další IRE indikována a pacient byl převeden na biologickou léčbu (obr. 4).
Obr. 3. A – na axiálních MR skenech je patrná metastáza kolorektálního karcinomu v pravém jaterním laloku před IRE (šipky); B – uložení dvojice elektrod; C – ložisko nekrózy v místě původní metastázy 1 měsíc po IRE; D – regrese nekrotického ložiska při kontrole za 6 měsíců (šipka) 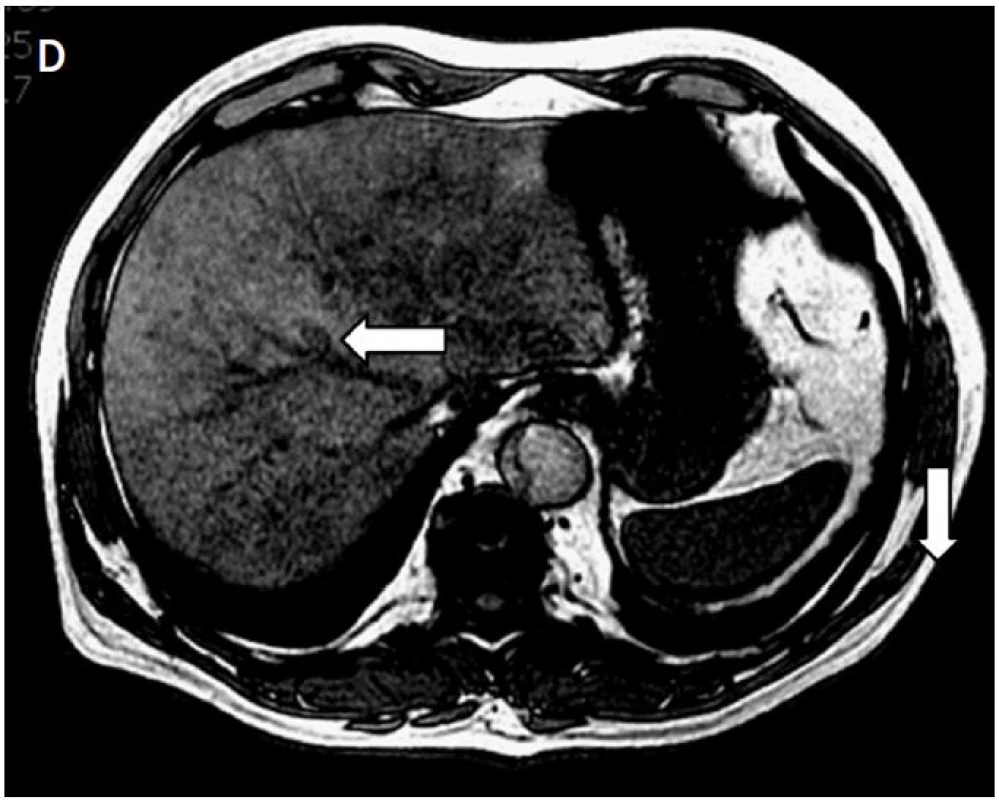
Tab. 1. Výsledky CT/MR vyšetření podle modifikovaných RECIST kritérií 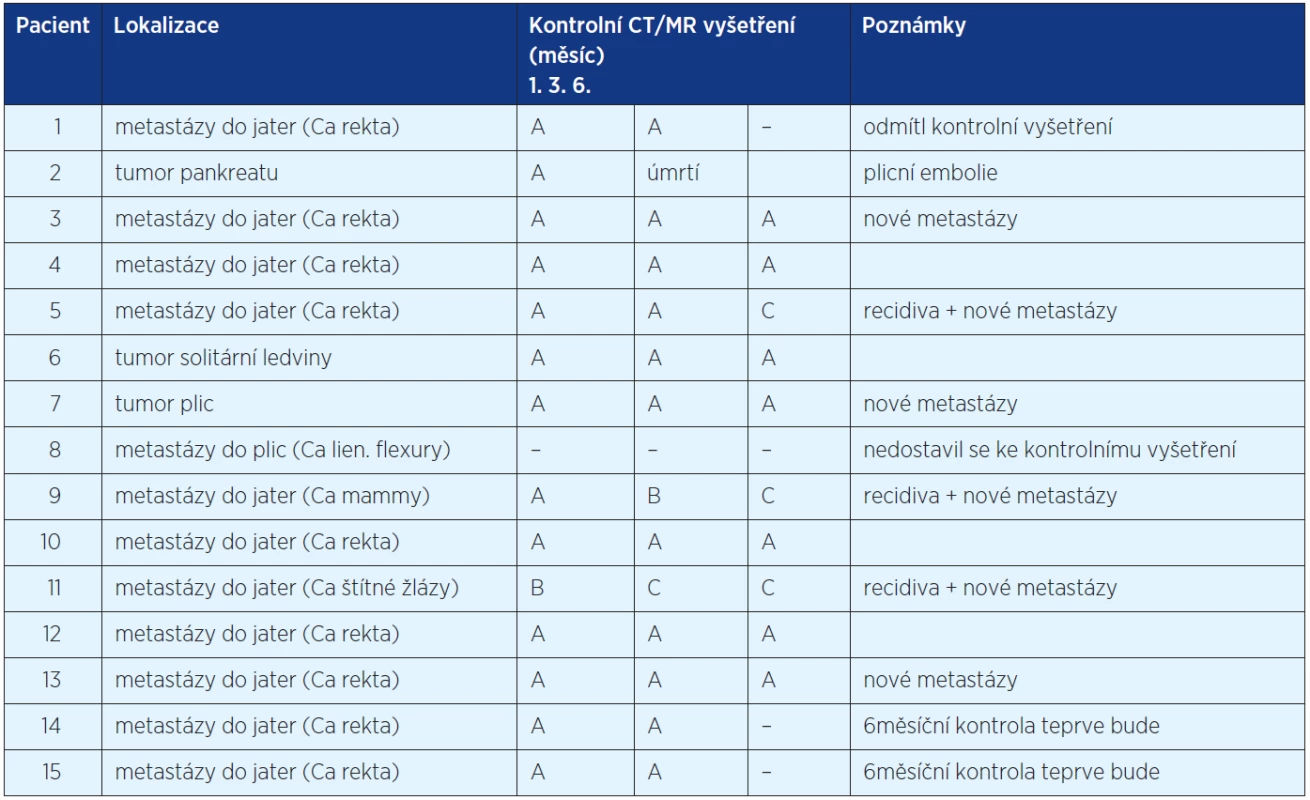
Obr. 4. A – na axiálních CT skenech je patrná metastáza karcinomu štítné žlázy v levém jaterním laloku před IRE (šipka); B – uložení dvojice elektrod; C – rozsah nekrózy po IRE; D – výrazný enhacement v oblasti původního nádorového ložiska svědčí pro časnou postablační recidivu, další nová meta ložiska v obou jaterních lalocích (šipky) 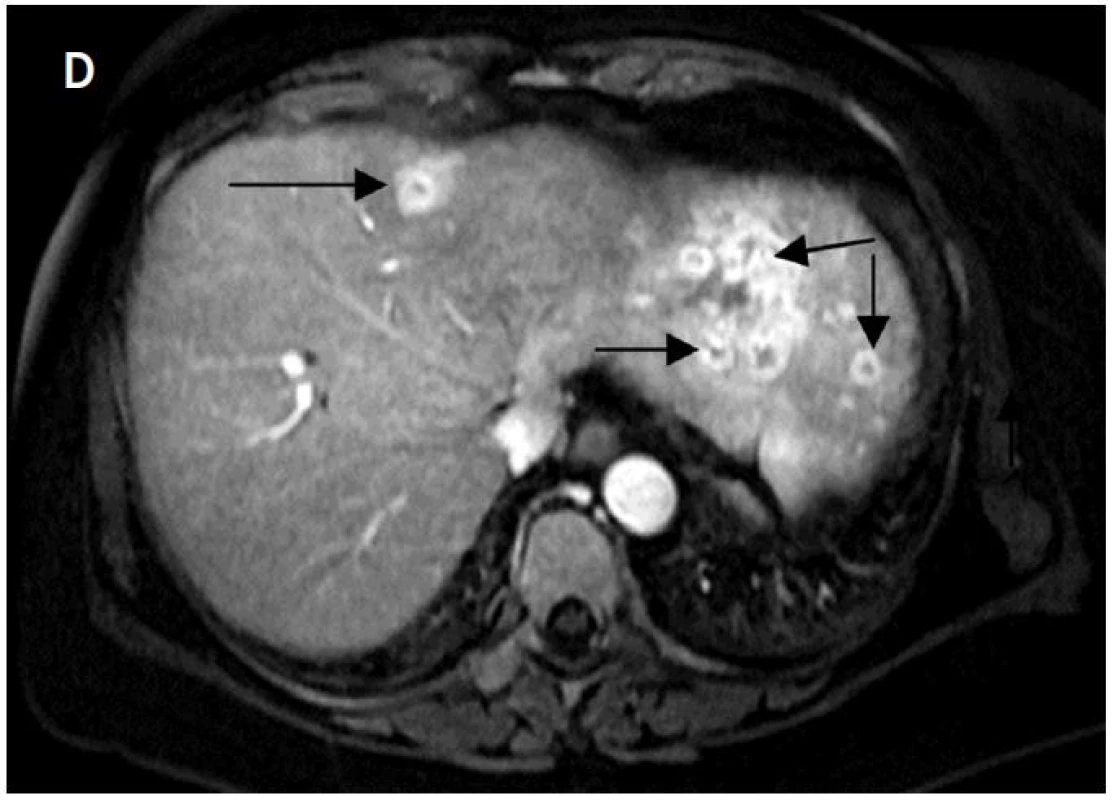
Postprocedurální komplikace jsme pozorovali u deseti pacientů. U tří se jednalo o plášťové PNO šíře od 1 do 3 cm, které vznikly při zavádění jehlových elektrod. V jednom případě vznikl PNO pacienta léčeného IRE pro meta plic, u dalších dvou případů se jednalo o léčbu jaterních metastáz. Ve všech třech případech se PNO spontánně upravil bez nutnosti specifické léčby během 3–5 dnů. U sedmi pacientů se na kontrolních CT skenech po IRE objevil minimální oboustranný fluidothorax, který se rovněž beze zbytku upravil. Postproceduální bolesti, známky síňové fibrilace, neuropraxie brachiálního plexu ani žádné jiné závažné komplikace jsme nezaznamenali.
Biochemické sledování u našich pacientů ukázalo, že kontrolní mineralogram v první pooperační den byl bez pozoruhodností, jen s minimální tendencí k hypokalémii. K elevaci jaterních testů (ALT i AST do 10 µkat/l) a bilirubinu na hodnoty kolem 40 µmol/l, (v jednom případě na 350 µmol/l) došlo u pacientů s výkony na játrech. Patologické laboratorní hodnoty se při další kontrole – 3. pooperační den, většinou buď normalizovaly, nebo jsme pozorovali postupný pokles k normálu (extrémní hodnota bilirubinu byla po týdnu poloviční). Renální funkce zůstaly beze změny nebo došlo ke klinicky nevýznamnému poklesu hodnot urey a kreatininu. Při ošetření dvou pacientů s plicními metastázami nebyly v laboratorních výsledcích pooperačně pozorovány žádné podstatné změny.
DISKUZE
IRE je nová ablační léčebná metoda vycházející z výzkumů působení elektrického pole na celulární a subcelulární struktury živých organizmů (5, 6). Výzkumné práce Davalose ukázaly, že při aplikaci nízkoenergetického proudu a při použití mikrosekundových pulzů o vysokém napětí dochází v buněčných membránách k otevření drobných pórů o nano-rozměrech , což vede ke zvýšení jejich permeability (4). Tyto elektrické pulzy lze aplikovat pomocí jehlových elektrod zaváděných do nádoru buď pod kontrolou zraku během otevřené operace, nebo pomocí CT, eventuálně UZ navigace (2, 6). Za předpokladu dostatečné intenzity a délky trvání pulzů se stává fenomén elektroporace ireverzibilní, což má za následek apoptózu exponovaných buněk. Vzniklá nádorová nekróza je resorbována lymfatickým systémem a hojí se jizvou (1). Elektroporační efekt se používá k léčbě maligních měkkotkáňových nádorů jater, pankreatu, ledvin, prostaty, plic, nádorů kožních, mamárních a některých nádorů pojivových (2).
Na rozdíl od radiofrekvenční ablace, kdy vzniká termální nekróza při teplotách kolem 100 oC, nedochází při ireverzibilní elektroporaci k tepelnému poškození tkání vzhledem k tomu, že maximální dosažená teplota nepřesahuje 50 oC. Tato skutečnost je významná zejména ve vztahu ke kolagenním strukturám, které jsou základem tubulárních struktur – žlučovodů, ledvinných kalichů, močovodů, bronchiálních struktur a cév, protože zůstávají nepoškozené (obr. 5).
Obr. 5. A – na axiálních CT skenech je patrná metastáza v pravém jaterním laloku před IRE (šipka); B – uložení čtyř elektrod v oblasti; C – rozsah nekrózy po IRE v oblasti odstupu jaterních žil; D – při kontrole za 1 měsíc jsou patrné intaktní, kontrastně zobrazené jaterní žíly v místě nekrotického ložiska po IRE 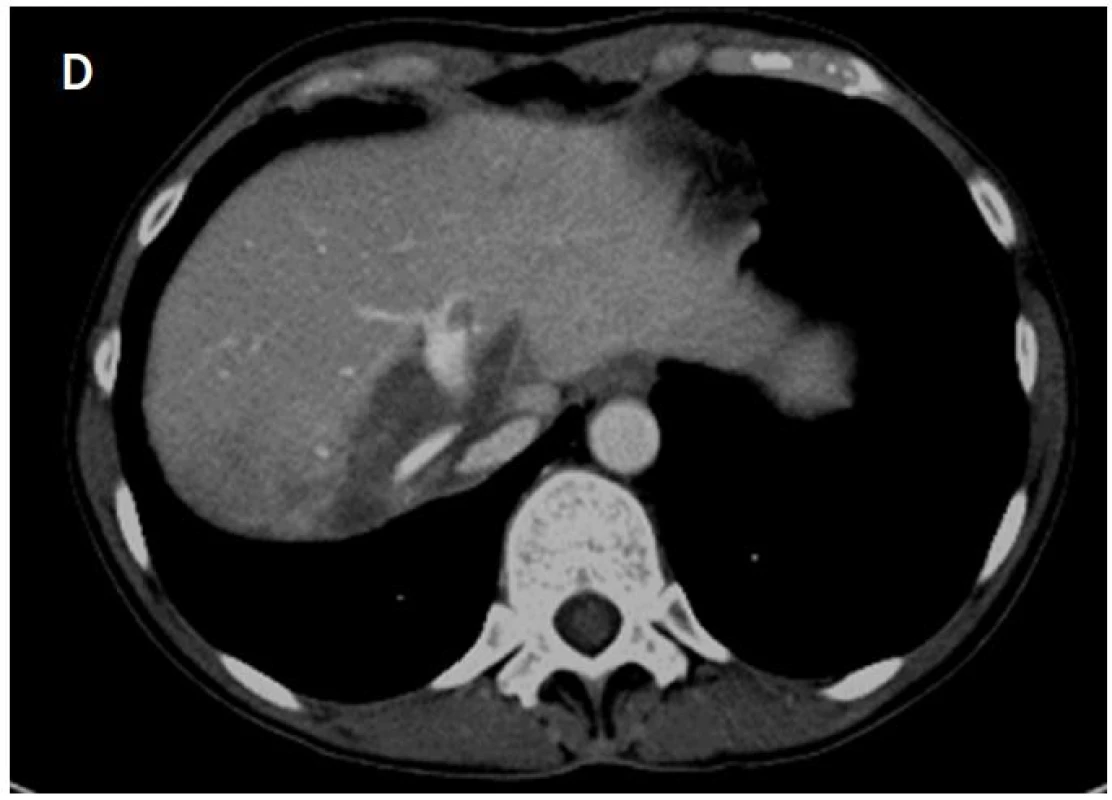
Při IRE nebyl rovněž pozorován tzv. heat-sink efekt – snížení teploty v blízkosti velkých cév v důsledku proudící krve. Tímto způsobem vzniká deficit teploty potřebné k dosažení termální destrukce nádorové tkáně, což má za následek persistenci viabilních nádorových struktur a recidivu nádoru. Heat-sink efekt snižuje léčebný účinek radiofrekvenční ablace zvláště v případech, kdy je nádor lokalizován v blízkostí aorty, vena portae nebo dolní duté žíly (1, 2). Vlastní ireverzibilní elektroporace je prováděna v celkové anestezii a dokonalé svalové relaxaci tak, aby při elektropolarizačních pulzech nedošlo ke vzniku generalizovaných svalových záškubům připomínajícím grand mal (3). Jehlové elektrody jsou do nádoru zaváděny v apnoické pauze, aby bylo jejich umístění co nejpřesnější. Vzhledem k opakovanému zavážení pacienta dovnitř a ven z vyšetřovacího tunelu je nezbytný dostatečně dlouhý dýchací okruh. Během IRE je standardně monitorováno EKG, neinvazivně krevní tlak, pulzní oxymetrie, kapnometrie a hloubka svalové relaxace. Prevencí neurapraxie brachiálního plexu je pečlivé vypodložení a fixace horních končetin (3, 8).
Z dostupné literatury vyplývá, že IRE lze jako miniinvazivní alternativu s úspěchem použít při léčbě řady primárních a sekundárních nádorů zejména v situacích, kdy je konvenční operační řešení po pacienta značně rizikové nebo technicky neschůdné a kdy je použití ostatních termoablačních metod limitované (9–11). Jedná se zejména o léčbu maligních lézí, které jsou lokalizovány v blízkosti vývodných žlučových a pankrea-tických cest nebo cév probíhajících v oblasti hilu (9)(obr. 6). Také při léčbě nádorů plic a mediastina nedochází při IRE k poškození důležitých hilových struktur – bronchů a velkých cév nebo inervace bránice. Rovněž při IRE léčbě nádorů ledvin a prostaty nedochází k postižení důležitých tubulárních struktur, jako jsou močovody, močová trubice nebo přilehlé nervově-cévní svazky (10, 11).
Obr. 6. A – na axiálních CT skenech je patrný karcinom hlavy pankreatu před IRE (šipky); B – uložení čtyř elektrod v oblasti nádoru; C – rozsah nekrózy bezprostředně po IRE; D – při kontrole za 1 měsíc je patrné ložisko nekrózy v místě původního nádoru a drén zavedený via PTD do žlučových cest (šipky) 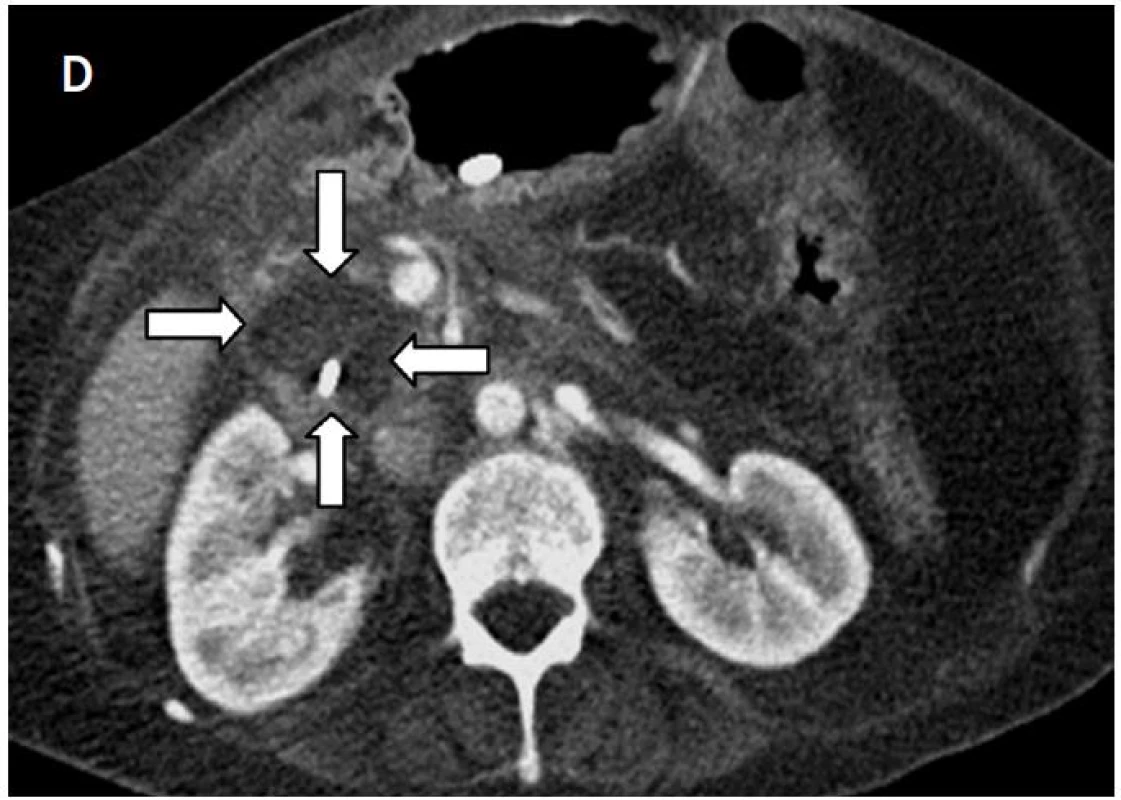
Proceduální a postproceduální komplikace léčby maligních nádorů pomocí IRE jsou ve srovnání s konvenčními operacemi a termoblačními technikami kvalitativně i kvantitativně menší (1). Zatímco preparace tkání při konvenční chirurgickém zákroku přináší značné riziko krvácení a při termoablaci může dojít k poškození cévní stěny s následným krvácením do ablační nekrózy, nedochází při IRE k poškození cév vzhledem k tomu, že jsou používané 22 G jehlové elektrody šíře 1 mm. Riziko infekce, které při operačních zákrocích vyplývá z rozsahu poškození kůže a dalších struktur, je při IRE minimální, neboť integrita kůže a dalších struktur je narušena pouze několika vpichy tenkými jehlovými elektrodami a vzniklá tkáňová nekróza je netermální. Minimální invazivita IRE je ve srovnání s operačními zákroky a termoablačními metodami spojena s kratší dobou hospitalizace a následné rekonvalescence. Mezi potenciálními riziky IRE je vznik subkapsulárního hematomu při mnohočetných punkcích a možná implantace nádorových buněk do punkčního kanálu (2).
ZÁVĚR
IRE je nová alternativní miniinvazivní léčebná metoda použitelná k lokální léčbě maligních nádorů v případech, kdy chirurgický zákrok je technicky neproveditelný nebo neúměrně rizikový. Na základě našich prvních zkušeností můžeme konstatovat, že IRE prováděná pod CT navigací je efektivní a bezpečná ablační metoda s velkým terapeutickým potenciálem. K posouzení efektivity účinků IRE budou nezbytná kontrolní vyšetření u většího počtu pacientů v delším časovém úseku.
Zkratky
CT – výpočetní tografie
IRE – ireverzibilní elektroporace
MA – mikrovlnná ablace
PNO – pneumothorax
RFA – radiofrekvenční ablace
UZ – ultrazvuk
Práce je podpořena z výzkumného projektu P 27/2012 Univerzity Karlovy, 3. lékařské fakulty v Praze.
Adresa pro korespondenci:
doc. MUDr. Václav Janík, CSc.
Radiodiagnostická klinika 3. LF UK a FNKV
Šrobárova 50, 100 34 Praha 10
e-mail: janik@fnkv.cz
Zdroje
1. Rubinsky B, Onik G, Mikus P. Irreversible electroporation. A new ablation modality – clinical implication. Technology in Cancer Research and Treatment 2007; 6(1): 37–48. PubMed PMID:17241099
2. Thomson KR, Cheung W, Ellis SJ, Park D, Kavnoudias H, Loader-Oliver D, Roberts S, Evans P, Ball Ch, Haydon A. Investigation of the Safety of Irreversible Electroporation in Humans. J Vasc Interv Radiol 2011; 22 : 611–621.
3. Ball C, Thomson KR, Kavnoudias H. Irreversible Electroporation: A New Challenge in „Out of Operating Theater“ Anesthesia Anesth Analg 2010; 110 : 1305–1309.
4. Davalos R, Mir LM, Rubinsky B. Tissue ablation with Irreversible Electorporation. Ann Biomed Eng 2005; 33 : 223–231.
5. Edd JF, Horowitz L, Davalos RV. In vivo results of new focal tissu ablation technique: irreversible electroporation. IEEE Trans Biomed Eng 2006; 53(7): 1409–1415.
6. Lee EW, Loh CT, Kee ST. Imaging guided percutaneous irreversible electroporation: ultrasound and immunohistological correlation. Technol Cancer Res Treat 2007; 6 : 287–293.
7. Husband JE, Schwartz LH, Spencer J, Olivier L, King DM, Johnson R, Reznek R. Evaluation of the response to treatment of solid tumours: a consensus statement of the International Cancer Imaging Society. Br J Cancer 2004; 90(12): 2256–2260.
8. Málek J, Šturma J, Janík V, Kurzová A. Anesteziologická problematika CTnavigované ireverzibilní elektroporace (přístroj NanoKnife™). Anest Intenziv Med 2013; 24(1): v tisku.
9. Bagla S, Papadouris D. Percutaneous Irreversible Electroporation of Surgically Unresectable Panceratic Cancer: A case report. J Vasc Interv Radiol 2012; 23 : 142–145.
10. Pech M, Janitzky A, Wendler JJ, Strang C, Blaschke S, Dudek O, Ricke J, Liehr UB. Irreversible electroporation of renal cell carcinoma: a first-in-man phase clinical study. Cardiovasc Intervent Radiol 2011; 34 : 132–138.
11. Onik G, Rubinsky B, Mikus P. Irreversible Electroporation: implication for prostate ablation. Technol Cancer Res.Treat 2007; 6(4): 295–300.
Štítky
Adiktologie Alergologie a imunologie Anesteziologie a resuscitace Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská dermatologie Dětská gastroenterologie Dětská gynekologie Dětská chirurgie Dětská kardiologie Dětská nefrologie Dětská neurologie Dětská onkologie Dětská otorinolaryngologie Dětská pneumologie Dětská psychiatrie Dětská radiologie Dětská revmatologie Dětská urologie Diabetologie Endokrinologie Farmacie Farmakologie Fyzioterapie Gastroenterologie a hepatologie Genetika Geriatrie a gerontologie Gynekologie a porodnictví Hematologie a transfuzní lékařství Hygiena a epidemiologie Hyperbarická medicína Chirurgie cévní Chirurgie hrudní Chirurgie plastická Chirurgie všeobecná Infekční lékařství Intenzivní medicína Kardiochirurgie Kardiologie Logopedie Mikrobiologie Nefrologie Neonatologie Neurochirurgie Neurologie Nukleární medicína Nutriční terapeut Obezitologie Oftalmologie Onkologie Ortodoncie Ortopedie Otorinolaryngologie Patologie Pediatrie Pneumologie a ftizeologie Popáleninová medicína Posudkové lékařství Praktické lékařství pro děti a dorost Protetika Psychologie Radiodiagnostika Radioterapie Rehabilitační a fyzikální medicína Reprodukční medicína Revmatologie Sestra Sexuologie Soudní lékařství Stomatologie Tělovýchovné lékařství Toxikologie Traumatologie Urgentní medicína Urologie Laboratoř Domácí péče Foniatrie Algeziologie Zdravotnictví Dentální hygienistka Student medicíny
Článek BCC A JEHO ANAMNÉZA
Článek vyšel v časopiseČasopis lékařů českých
Nejčtenější tento týden
- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Doc. Jitka Fricová: V USA nasazovali fentanyl poměrně nekriticky, v Česku je situace jiná
-
Všechny články tohoto čísla
- 13. konference Tabák a zdraví v Lékařském domě (Praha, 15. listopadu)
- Vědecká schůze České psychoterapeutické společnosti ČLS JEP (Praha, 18. ledna 2013)
- Pražské Fyziologické dny 2013 (Praha, 5. až 7. února 2013)
- Olomoucké onkologické dny (Olomouc, 7. a 8. února 2013)
- SNOWDERM 2013 aneb zimní setkání sekce mladých dermatovenerologů ČDS ČLS JEP (Počátky, 9. až 10. února 2013)
- Biochemická a molekulárně biologická vyšetření v onkologii – zpráva o pracovní konferenci (Olomouc, 13. února 2013)
- Spolek lékařů českých v Praze pořádá v dubnu, květnu a červnu 2013 pravidelné přednáškové večery s diskuzí
-
Prof. MUDr. Pavel Barták, CSc.
*9. září 1927 †4. února 2013 - Zemřel farmakolog a člen redakční rady Časopisu lékařů českých MUDr. Norbert Gaier, CSc.
- Dr. Alexander Schirger — Rochester
-
Prof. MUDr. Vlastimil Víšek, DrSc.
*19. srpen 1928 †28. leden 2013 - Paramagnetická rezonance v diagnostice malanomu
-
Richard Rokyta, Miloslav Kršiak, Jiří Kozák (eds.)
BOLEST
Přepracované, doplněné vydání - Howard Martin Temin (1934–1994)
- Mikroskopické záněty tlustého střeva
- Ireverzibilní elektroporace: lokální, non-termální, ablační léčba maligních nádorů
- Plánované akce odborných složek ČLS JEP
- Vleklý problém se závislostí na návykových látkách a jeho řešení
- Joint Programming, Společné programování – nový nástroj intenzivní spolupráce v oblasti biomedicínského výzkumu v Evropě
- Marcus Tullius Cicero a lékařství
- BCC A JEHO ANAMNÉZA
- UNICEF a Světová zdravotnická organizace odsuzují útoky na zdravotnické pracovníky v Nigérii
- Ateroskleróza 2012 (12. až 14. září, Praha)
- 16. celostátní konferenceDNA diagnostiky (28. až 30. listopadu, Brno)
- Časopis lékařů českých
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Mikroskopické záněty tlustého střeva
- Ireverzibilní elektroporace: lokální, non-termální, ablační léčba maligních nádorů
- Vleklý problém se závislostí na návykových látkách a jeho řešení
-
Richard Rokyta, Miloslav Kršiak, Jiří Kozák (eds.)
BOLEST
Přepracované, doplněné vydání
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání





















