-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaHemadsorpční metody u kriticky nemocných – dvojitá sázka naslepo?
Hemadsorption therapy in critically ill patients – double blind bet?
Recently, the therapeutic approach using the extracorporeal hemadsorption technologies attracted much attention. Effort to affect the patophysiological processess associated with critical illness represents an attractive concept, that penetrates into clinical practice. Here we present the critical opinion on current status of hemadsorption therapy in critical ill patients in the context of published evidence.
Keywords:
hemadsorption – sepsis – critical illness – CytoSorb – oXiris
Autoři: J. Horák 1,2; J. Chvojka 1,2; V. Tégl 2,3
; L. Nalos 2,4; M. Peltanová 2,3; J. Beneš 2,3
; M. Matějovič 1,2
Působiště autorů: I. interní klinika, Lékařská fakulta v Plzni, Univerzita Karlova a Fakultní nemocnice Plzeň 1; Biomedicínské centrum, Lékařská fakulta v Plzni, Univerzita Karlova 2; Klinika anesteziologie, resuscitace a intenzivní medicíny, Lékařská fakulta v Plzni, Univerzita Karlova, a Fakultní nemocnice Plzeň 3; Ústav fyziologie, Lékařská fakulta v Plzni, Univerzita Karlova 4
Vyšlo v časopise: Anest. intenziv. Med., 31, 2020, č. 4, s. 172-175
Kategorie: Přehledové články
Souhrn
V posledních letech přitahuje terapeutický přístup s využitím mimotělních hemadsorpčních metod u kriticky nemocných stále větší zájem. Snaha o časný zásah do patofyziologických procesů, které doprovázejí řadu inzultů u pacientů v intenzivní péči, představuje nepochybně atraktivní koncept, v současnosti pronikající do klinické praxe navzdory absenci evidence. Níže uvedený text představuje kritický pohled autorů na současný stav problematiky hemadsorpčních metod a jejich využití u kriticky nemocných, zejména septických pacientů.
Klíčová slova:
hemadsorpce – sepse – kritické onemocnění – CytoSorb – oXiris
Úvod
Série nepříliš robustních vědeckých prací (kazuistik, retrospektivních sledování atp.) publikovaných v nedávné době vynesla na výsluní zájmu klinického výzkumu intenzivní medicíny extrakorporální hemadsorpční metody. Časný zásah do excesivní inflamatorní odpovědi, která doprovází řadu inzultů u kriticky nemocných, zůstává dlouhodobě neopuštěným a pochopitelně (i komerčně) líbivým konceptem léčby těchto pacientů. Jeho cílem je regulace rozvíjející se nepřiměřené systémové zánětlivé odpovědi a tím zabránění vzniku a progresi multiorgánové dysfunkce a šokového stavu. Právě mimotělní eliminace cirkulujících mediátorů inflamatorní odpovědi představuje jednu z cest tohoto konceptu. Prezentovaný text představuje pohled autorů na současný stav problematiky hemadsorpčních metod, které pronikají do dnešní klinické praxe.
Neselektivní hemadsorpční systémy
Adsorpční systém CytoSorb® (CytoSorbents, New Jersey, USA) představuje vysoce kapacitní adsorpční médium schopné adsorpce molekul o hmotnosti 5–60 kDa tvořené porézními polymerovanými kuličkami s povrchem 45 000 m2, které přineslo řadu slibných výsledků v dílčích kazuistických sděleních [1–3]. Retrospektivní analýza série 26 případů časného užití adsorpčního systému zaznamenala u sledovaných pacientů rychlou hemodynamickou stabilizaci a snížení 28denní mortality; z analýzy však byli vyloučeni pacienti s předpokládanou dobou přežití kratší než 28 dní – celkový počet vyřazených pacientů studie neuvádí [4]. Celkem 20 pacientů bylo po kardiochirurgickém výkonu napojeno na adsorpční médium; jeho vliv na průběh pooperační systémové zánětové odpovědi byl následně retrospektivně analyzován. Pacienti, u nichž byl v pooperačním období využit systém CytoSorb, měli signifikantně nižší sérové hladiny interleukinu-6 (25 kDa) a prokalcitoninu (17 kDa), než byly zjištěny u nemocných po výkonu, kteří nebyli na tento systém napojeni; u obou skupin nebyl v rámci studie zahrnut klinický obraz a další vývoj těchto nemocných [5]. V klinicky relevantním modelu popáleninového traumatu u prasete Linden et al. [6] prokázali schopnost CytoSorbu snížit koncentrace některých cytokinů a myoglobinu v extrakorporálním okruhu „za filtrem“, ovšem bez vlivu na systémové hladiny, což autoři připisují omezené vazebné kapacitě při kontinuální produkci postiženým organismem. Doposud největší publikovanou retrospektivní studii představili Brouwer et al. [7], kteří sledovali celkem 116 nemocných v septickém šoku, kteří si vyžádali náhradu funkce ledvin; 67 nemocných pak bylo intervenováno CytoSorbem v kombinaci s kontinuální náhradou funkce ledvin (CRRT). Intervenovaná skupina měla vyšší SOFA score. Nekorigovaná 28denní mortalita nebyla mezi skupinami rozdílná, nicméně při korekci na tíži stavu byla úmrtnost významně nižší než předpokládaná. Další výsledky, zahrnující pokles hladin prozánětlivých cytokinů a hemodynamickou stabilizaci, nabízejí i další retrospektivní analýzy a kazuistiky, které zahrnují pouze malé počty nemocných; jejich autoři se však shodují na naplnění potřeby prospektivních randomizovaných studií.
Doposud byl publikován relativně malý počet takových studií. První větší randomizovaná studie Schadlera et al. [8] zahrnula 97 pacientů v septickém šoku, kteří byli současně napojeni na umělou plicní ventilaci z důvodu ALI/ARDS. Intervence v podobě 6hodinové hemoperfuze s využitím systému CytoSorb v sedmi po sobě jdoucích dnech nevedla k poklesu plazmatických hladin IL-6; intervenovaná skupina pak vykazovala vyšší 60denní mortalitu, vyšší míru potřeby náhrady funkce ledvin, přičemž nebyl rozdíl v predikované mortalitě dle APACHE II v době zařazení do studie. Současně byla pozorována signifikantně nižší koncentrace leukocytů, trombocytů, dále nižší hladina plazmatických proteinů včetně albuminu a nemocní v kontrolní skupině měli signifikantní nižší tělesnou teplotu. Další menší prospektivní studie zaznamenala pokles dávky vazopresoru a zvýšenou clearance laktátu u 20 pacientů v refrakterním septickém šoku, kde byla hemadsorpce CytoSorbem užita jako rescue léčba [9]. Tato intervence však neměla vliv na vývoj tíže MODS (hodnocena prostřednictvím SOFA score); 28denní mortalita byla 45 %. Významnými nedostatky této studie jsou absence kontrolní skupiny, absence standardizace intervence a limitace na jediné centrum. Pokles hladin IL-6, IL-8 a pozitivní vliv 24hodinové hemoperfuze CytoSorbem na mikrocirkulaci a celkové SOFA score byla pozorována v rámci malé prospektivní studie (9 pacientů). Autoři však současně popisují významný pokles srdečního indexu a významně vyšší potřebu dobutaminu u těchto pacientů [10]. V další malé randomizované studii ACESS u 20 pacientů v septickém šoku vedla intervence CytoSorbem k signifikantnímu, leč klinicky nevýznamnému, snížení potřeby noradrenalinu a hladin prokalcitoninu; vliv na klinický výstup nebyl i s ohledem na extrémně malý počet zařazených osob pozorován [27]. V posledních letech se objevila řada dalších adsorpčních médií, která pracují na podobném principu jako CytoSorb: NKU-9 (Čína), HA-330, HA-380 (Jafron, Čína), BL-300 (Japonsko). Tato média nabízejí podobné vlastnosti jako CytoSorb s různou, zatím pouze spíše proklamovanou, efektivitou. První a zatím jediná prospektivní studie [11] zahrnující 23 nemocných v septickém šoku popisuje pokles srdeční frekvence a zánětlivých parametrů (C‑reaktivní protein a prokalcitonin) u intervenované (HA-330) skupiny nemocných. Prognóza a vývoj nemocných však nebyl touto intervencí ovlivněn. Místo těchto neselektivních hemadsorpčních systémů v klinické praxi však bude nezbytné evaluovat prostřednictvím dalších studií.
Aktuálně se lze kazuisticky setkávat s případy, kdy jsou hemadsorpční metody typu CytoSorb implementovány od úvodu do mimotělních okruhů extrakorporální membránové oxygenace (ECMO) [12, 13]. Indikační kritéria pro VA či VV‑ECMO jsou v současné době relativně široká a autoři uvedených kazuistik argumentují potenciální snahou příznivě ovlivnit molekulární a hemodynamický profil kritického onemocnění tak, aby byl maximálně eliminován potenciální detrimentální dopad mimotělního okruhu na aktivaci koagulace, systémové zánětové odpovědi, hemolýzu a vice versa modifikací imunitní odpovědi na vstupní inzult zvýšit šanci na udržení a funkčnost mimotělního okruhu, příznivě ovlivnit kapilární leak, snížit potřebu vazopresorické podpory. Využití ECMO jako „rescue“ terapie např. u septického šoku je ale stále relativně kontroverzní modalitou. Zatímco v pediatrické a novorozenecké populaci se jedná o metodu relativně etablovanou, u dospělých pacientů lze úspěch veno‑arteriálního ECMO (VA‑ECMO) očekávat především u hypodynamického fenotypu septického šoku. Jak jsme potvrdili i v našem experimentálním pokusu, přemostit kritické období na vazopresory rezistentní vazoplegie u hyperdynamického šoku pomocí VA‑ECMO je problematické [14]. Při absenci kvalitních experimentálních a klinických dat nelze v současné době kazuisticky popisovanými dílčími úspěchy kombinace hemadsorpčních metod a ECMO podepřít rutinní doporučení těchto terapeutických modalit v léčbě kriticky nemocných.
Na rozdíl od dubiozní indikace k ovlivnění inflamatorní odpovědi se extrakorporální eliminace hemadsorpcí s využitím CytoSorbu ukázala jako efektivní u některých endogenních a exogenních intoxikací (tab. 1). Existuje však i skupina léčiv, jejichž eliminace, zejména v kontextu probíhající sepse či septického šoku, není žádoucí, a to jsou antibiotika. Recentní in vitro a in vivo studie ukazují schopnost CytoSorbu redukovat množství cirkulujícího antiinfekčního agens [19, 20]. Nicméně vliv hemadsorpce na hladiny a efektivitu podávaných antimikrobiálních látek, případně vliv na rozvoj bakteriální rezistence při nedosažení efektivních koncentrací během procedury a také na případnou nutnost navýšení dávek, zůstávají dosud neuspokojivě zodpovězeny, hlavně v kontextu absence rutinního stanovování jejich sérových hladin.
Tab. 1. Příklady efektivního využití hemadsorpčních metod v případně život ohrožující intoxikace 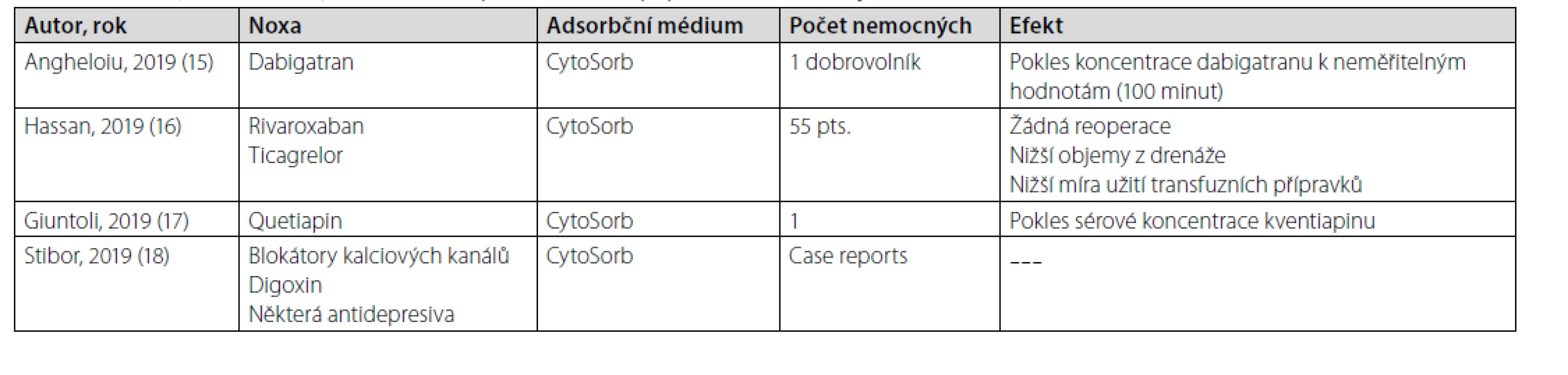
Endotoxin‑adsorpční systémy
Endotoxin stěny gramnegativních bakterií je potentním spouštěčem zánětové odpovědi v sepsi, proto se jeho eliminace v časných fázích sepse zdá logickou možností léčebného zásahu. Polymyxin B je antibiotikem pokrývajícím široké spektrum gramnegativní flóry. Jeho užití je však asociováno s řadou nežádoucích účinků, proto není v současné době rutinně využíváno k systémové léčbě infekcí. Současně se však vyznačuje schopností vázat cirkulující endotoxin, čehož využívají některá hemadsorpční média (Toraymyxin, Toray Industries Inc., Japan). Pozitivní výsledky přinesla studie EUPHAS; u septických nemocných s intraabdominálním zdrojem infekce vedlo využití polymyxinového adsorpčního systému k hemodynamické stabilizaci spolu s poklesem dávky vazopresoru, dále k poklesu SOFA score a celkové 28denní mortality oproti neintervenované skupině, která byla léčena standardně [21]. Multicentrická studie ABDOMIX [22] však tyto povzbuzující výsledky nepotvrdila. Obdobně jako další studie EUPHRATES neprokázala pozitivní vliv na 28denní mortalitu septických pacientů [23]. Nicméně post‑hoc analýza podskupiny nemocných s extrémními koncentracemi endotoxinu ukázala nižší mortalitu, počet ventilovaných dnů a vliv na hemodynamické parametry [24]. Nabízí se proto otázka možnosti optimalizace výběru cílové skupiny pacientů, jež by z této metody mohli profitovat.
Systém oXiris (Baxter Int., USA) je trojkombinací dialyzační membrány a systémů schopných adsorpce cytokinů a vazby endotoxinu, která byla představena relativně nedávno. Intervence v podobě 24hodinového využití systému oXiris u 20 pacientů v septickém šoku a s poškozením ledvin vyžadujícím náhradu jejich funkce vedla k redukci dávky použitého vazopresoru, dále k signifikantnímu poklesu cirkulujícího endotoxinu a vybraných cytokinů [25]. Obdobný pokles potřeby katecholaminů a pokles mortality ve srovnání s předpokládanou mortalitou dle SAPS II (Simplified acute physiological score II) skóre prezentovaly i výsledky francouzské retrospektivní kohortní studie [26]. K ovlivnění tíže MODS však nedošlo; vliv na prognózu nemocných studie nezmiňuje.
Diskuze
Více než 30letá neslavná historie výzkumných pokusů zameřených na zkrocení „zlé“ zánětové odpovědi u široké skupiny kriticky nemocných by měla být dostatečně silným varovným signálem před ukvapenými závěry jakkoliv koncepčně atraktivních hemoeliminačních inovací a jejich implementací do klinické praxe. Individualizovaná biologická léčba v onkologii je pro intenzivní medicínu modelem budoucnosti. Sepse je pouhý koncept, umělý konstrukt pro popis život ohrožujícího stavu vyvolaného deregulovanou, ale velice proměnlivou a nesourodou odpovědí hostitele na závažnou infekci. Ve skutečnosti pod jeden pojem (sepse) v klinické praxi zahrnujeme biologicky extrémně heterogenní interakci mezi mnoha různými predátory (patogenem), kořistí (pacientem) a zásahy lékaře. Predátoři, tj. původci infekcí, se značně liší svou schopností a mechanismy, jak aktivovat imunitní systém. Kořistí, tj. pacientem, může být dosud zcela zdravý, mladý člověk nebo naopak senior s mnoha různě závažnými komorbiditami. Naše léčebné intervence (operační trauma, léky, imunosuprese, onkologická léčba apod.) samy o sobě významně ovlivňují reakci hostitele na infekci. Míra i charakter hostitelské odpovědi jsou tak ovlivněny mnoha faktory. Na tomto pozadí se jeví pokus o neselektivní eliminaci (zlých i žádoucích) působků, aplikovaný na neselektovanou populaci kriticky nemocných, jako krok opačným směrem, tedy zpět. Alespoň do doby skutečně důvěryhodných vědeckých důkazů. Bohužel opora pro využití adsorpčních systémů, které v současnosti intenzivně pronikají do klinické praxe, vychází převážně z kazuistických sdělení a retrospektivních analýz nemocných. Nevelké, byť narůstající, množství prospektivních studií zatím nabízí pouze relativně malé počty zařazených pacientů nebo jejich významnou selekci. Např. ACESS studie zařadila 20 ze 716 zvažovaných pacientů [27], přičemž z analýzy vyloučila pacienty s akutním či chronickým selháním ledvin s potřebou náhrady jejich funkce, imunosuprimované pacienty, nemocné s trombocytopenií, hemato‑onkologické pacienty či pacienty na chronické kortikoterapii – tedy skupiny nemocných, které tvoří nemalou část pacientů v intenzivní péči. Míra, do jaké se v současné literatuře, týkající se hemadsorpčních metod, promítá pozitivní publikační bias, zůstává nejasná. Nicméně s ohledem na rozšířování metod a minimální množství publikovaných negativních výsledků lze předpokládat, že se v ní zrcadlí tendence k nadhodnocování pozitivních výsledků [28]. Některé výše uvedené práce srovnávají analyzovanou mortalitu s mortalitou předpokládanou, vycházející ze skórovacího systému SAPS II. Systematická analýza srovnávající prognostické modely [29] však jako vhodnější model u medical pacientů upřednostňuje SOFA skóre; některé studie pak hodnotí SAPS II jako model, který nadhodnocuje mortalitu ICU pacientů [30].
V současné době je registrováno (clinicaltrials.gov) 13 studií s využitím hemadsorpčního systému CytoSorb u kriticky nemocných pacientů, z nichž pouze 3 jsou designovány jako prospektivní, kontrolované a multicentrické. Bohužel, čím více bude přibývat nekvalitních studií, tím větší chaos v jejich interpretaci nastane. V tomto ohledu je překvapivé, do jaké míry se těmto metodám podařilo vyhnout se základnímu preklinickému testování na klinicky relevantních zvířecích modelech za účelem analýzy dané metody. Experiment zaměřený na komplexní analýzu týkající se bezpečnosti a efektivity systému CytoSorb s využitím etablovaného klinicky relevantního modelu progresivní peritoneální sepse a septického šoku v současnosti probíhá na pracovišti autorů (projekt MSMT-18726/2019-3). Výsledky experimentu budou dostupné v druhé polovině letošního roku.
Závěr
Extrakorporální hemadsorpční metody představují stále zajímavý koncept v terapeutickém přístupu ke kriticky nemocným pacientům. Zatím ale stále jen koncept, nic víc. Naštěstí vstupujeme do doby, kdy pomalu opouštíme „geocentrický“ model sepse 80.–90. let, který přinesl téměř 30 let nereprodukovatelných randomizovaných kontrolovaných studií. Kombinace umělé inteligence (big data analýzy) a pokročilých omických metod nám poodhaluje cestu vpřed a ukazuje na existenci řady odlišných endotypů, které charakterizují reakci organismu na infekci či trauma. Je tak pravděpodobné, že se dočkáme posunu od nespecifické syndromologie (např. sepse, ARDS, AKI) k mnohem přesnějším subtypům endogenní (imunitní, metabolické, hormonální) odpovědi na infekci/trauma, které nám umožní cílenou terapeutickou intervenci.
PROHLÁŠENÍ AUTORŮ: Prohlášení o původnosti: Práce je původní a nebyla publikována ani není zaslána k recenznímu řízení do jiného média. Střet zájmů: Autoři prohlašují, že nemají střet zájmů v souvislosti s tématem práce. Podíl autorů: Všichni autoři rukopis četli, souhlasí s jeho zněním a zasláním do redakce časopisu Anesteziologie a intenzivní medicína. JH, JCh, VT, LN, MP, JB i MM se podíleli na zpracování manuskriptu. Financování: 1. Program rozvoje vědních oborů Univerzity Karlovy (Progres – projekt Q39). 2. Projekt CZ.02. 1. 01/0.0/0.0/16_019/0000787, Centrum výzkumu infekčních onemocnění, uděleného MŠMT ČR, financovaného z EFRR. 3. Národní program udržitelnosti I (NPU I) č. LO1503 poskytovaný Ministerstvem školství, mládeže a tělovýchovy.
KORESPONDENČNÍ ADRESA AUTORA:
Článek přijat redakcí: 14. 5. 2020; Článek přijat k tisku: 18. 8. 2020
MUDr. Bc. Jan Horák, Ph.D.
Cit. zkr: Anest intenziv Med. 2020; 31(4): 172–175
Zdroje
1. Basu R, Pathak S, Goyal J, Chaudhry R, Goel RB, Barwal A. Use of a novel hemoadsorption device for cytokine removal as adjuvant therapy in a patient with septic shock with multi‑organ dysfunction: A case study. Ind J Crit Care Med. 2014; 18 : 822–824. doi. org/10.4103/0972-5229.146321
2. Hinz B, Jauch O, Noky T, Friesecke S, Abel P, Kaiser R. CytoSorb, a novel therapeuticapproach for patients with septic shock: a case report. Int J Artif Org. 2015; 38(8): 461–464. doi.org/10.5301/ijao.5000429
3. Steltzer H, Grieb A, Mostafa K, Berger R. Use of CytoSorb in Traumatic Amputation of the Forearm and Severe Septic Shock. Case Rep Crit Care. 2017 : 8747616. doi. org/10.1155/2017/8747616
4. Kogelmann K, Jarczak D, Scheller M, Druner M. Hemoadsorption by CytoSorb in septic patients: a case series. Crit Care. 2017; 21(1): 74. doi.org/10.1186/s13054-017-1662-9
5. Born F, Pichlmaier M, Peterß S, Khaladj N, Hagl C. Systemic Inflammatory ResponseSyndrome in der Herzchirurgie: Neue Therapiemöglichkeiten durch den Einsatz eines Cytokin‑Adsorpers während EKZ. Kardiotechnik. 2014; 23(2): 41–46.
6. Linden K, Scaravilli V, Kreyer SFX, Belenkiy SM, Stewart IJ, Chung KK, et al. Evaluation of the Cytosorb Hemoadsorptive Column in a Pig Model of Severe Smoke and Burn Injury. Shock. 2015; 44(5): 487–495. doi.org/10.1097/SHK.0000000000000439
7. Brouwer WP, Duran S, Kuijper M, Ince C. Hemoadsorption with CytoSorb shows a decreased observed versus expected 28-day all ‑ cause mortality in ICU patients with septic shock: a propensity‑score‑weighted retrospective study. Crit Care. 2019; 23(1): 317. doi. org/10.1186/s13054-019-2588-1
8. Schadler D, Pausch C, Heise D, Meier‑Hellmann A, Brederlau J, Weiler N, et al. The effect of a novel extracorporeal cytokine hemoadsorption device on IL-6 elimination in septic patients: A randomized controlled trial. PloS One. 2017; 12(10): e0187015. doi.org/10.1371/ journal.pone.0187015
9. Friesecke S, Stecher SS, Gross S, Felix SB, Nierhaus A. Extracorporeal cytokine elimination as rescue therapy in refractory septic shock: a prospective single ‑ center study. J Artif Org. 2017; 20(3): 252–259. doi.org/10.1007/s10047-017-0967-4
10. Zuccari S, Damiani E, Domizi R, Scorcella C, D’Arezzo M, Carsetti A, et al. Changes in Cytokines, Haemodynamics and Microcirculation in Patients with Sepsis/Septic Shock Undergoing Continuous Renal Replacement Therapy and Blood Purification with Cyto - Sorb. Blood Purif. 2019 : 1–7. doi.org/10.1159/000502540
11. Kacar CK, Uzundere O, Kandemir D, Yektas A. Efficacy of HA330 Hemoperfusion Adsorpent in Patients Followed in the Intensive Care Unit for Septic Shock and Acute Kidney Injury and Treated with Continuous Venovenous Hemodiafiltration as Renal Replacement Therapy. Blood Purif. 2020; 1–9. doi.org/10.1159/000505565
12. Datzmann T, Träger K. Extracorporeal membrane oxygenation and cytokine adsorption. J Thorac, DiS. 2018; 10(S5 Suppl 5): 653–660.
13. Bruenger F, Kizner L, Weile J, Morshuis M, Gummert JF. First successful combination of ECMO with cytokine removal therapy in cardiogenic septic shock: a case report. Int J Artif Organs. 2015; 38(2): 113–116.
14. Chvojka J, Martinkova V, Benes J, Valesova L, Danihel V, Nalos L, et al. Mechanical circulatory support in refractory vasodilatory septic shock: A randomized controlled porcine study. Shock. 2020; 53(1): 124–131.
15. Angheloiu AA, Angheloiu GO. Removal of dabigatran using sorbent hemadsorption. Int J Cardiol. 2019; 293 : 73–75. doi.org/10.1016/j.ijcard.2019. 06. 078
16. Hassan K, Kannmacher J, Wohlmuth P, Budde U, Schmoeckel M, Geidel S. Cytosorb Adsorption During Emergency Cardiac Operations in Patients at High Risk of Bleeding. Ann Thor Surg. 2019; 108(1): 45–51. doi.org/10.1016/j.athoracsur.2018. 12. 032
17. Giuntoli L, Dalmastri V, Cilloni N, Orsi C, Stalteri L, Demelas V, et al. Severe quetiapine voluntary overdose successfully treated with a new hemoperfusion sorbent. Int J Artif Org. 2019; 42(9): 516–520. doi.org/10.1177/0391398819837686
18. Stibor B. Použití cytokinových filtrů na ICU – kdy, komu a jak? Colours of Sepsis [přednáška]. 2020 [cit. 2020-4-22]. Dostupné z: http://www.sepseostrava.cz/sepse/sbornik/2020/2. Pou.it.cytokinov.ch.filtr…kdy.komu.a.jak.pdf
19. Poli EC, Simoni C, Andre P, Buclin T, Longchamp D, Perez MH, Schneider AG. Clindamycin clearance during Cytosorb hemoadsorption: A case report and pharmacokinetic study. Int J Artif Org. 2019; 42(5): 258–262. doi.org/10.1177/0391398819831303
20. Konig C, Rohr AC, Frey OR, Brinkmann A, Roberts JA, Wichmann D, et al. In vitro removal of anti ‑ infective agents by a novel cytokine adsorpent system. Int J Artif Org. 2019; 42(2): 57–64. doi.org/10.1177/0391398818812601
21. Cruz DN, Antonelli M, Fumagalli R, Foltran F, Brienza N, Donati A, et al. Early use of polymyxin B hemoperfusion in abdominal septic shock: the EUPHAS randomized controlled trial. JAMA. 2009; 301(23): 2445–2452. doi.org/10.1001/jama.2009.856
22. Payen DM, Guilhot J, Launey Y, Lukaszewicz AC, Kaaki M, Veber B, et al. Early use of polymyxin B hemoperfusion in patients with septic shock due to peritonitis: a multicenter randomized control trial. Intensive Care Med. 2015; 41(6): 975–984. doi.org/10.1007/ s00134-015-3751-z
23. Dellinger RP, Bagshaw SM, Antonelli M, Foster DM, Klein DJ, Marshall JC, et al. Effect of Targeted Polymyxin B Hemoperfusion on 28-Day Mortality in Patients With Septic Shock and Elevated Endotoxin Level: The EUPHRATES Randomized Clinical Trial. JAMA, 2018; 320(14): 1455–1463. doi.org/10.1001/jama.2018.14618
24. Klein DJ, Foster D, Walker PM, Bagshaw SM, Mekonnen H, Antonelli M. Polymyxin B hemoperfusion in endotoxemic septic shock patients without extreme endotoxemia: a post hoc analysis of the EUPHRATES trial. Intensive Care Med. 2018; 44(12): 2205–2212. doi.org/10.1007/s00134-018-5463-7
25. Broman ME, Hansson F, Vincent JL, Bodelsson M. Endotoxin and cytokine reducing properties of the oXiris membrane in patients with septic shock: A randomized crossover double‑blind study. PloS One. 2019; 14(8): e0220444. doi.org/10.1371/journal.pone.0220444
26. Schwindenhammer V, Girardot T, Chaulier K, Gregoire A, Monard C, Huriaux L, et al. oXiris( R) Use in Septic Shock: Experience of Two French Centres. Blood Purif. 2019; 47(Suppl 3): 1–7. doi.org/10.1159/000499510
27. Hawchar F, Laszlo I, Oveges N, Trasy D, Ondrik Z, Molnar Z. Extracorporeal cytokine adsorption in septic shock: A proof of concept randomized, controlled pilot study. J Crit Care. 2019; 49 : 172–178. doi.org/10.1016/j.jcrc.2018. 11. 003
28. Mlinaric A, Horvat M, Supak Smolcic V. Dealing with the positive publication bias: Why you should really publish your negative results. Biochem Medica. 2017; 27(3): 30201. doi. org/10.11613/BM.2017.030201
29. Minne L, Abu‑Hanna A, de Jonge E. Evaluation of SOFA‑based models for predicting mortality in the ICU: A systematic review. Crit Care. 2008; 12(6): 161. doi.org/10.1186/cc7160
30. Poncet A, Perneger TV, Merlani P, Capuzzo M, Combescure C. Determinants of the calibration of SAPS II and SAPS 3 mortality scores in intensive care: a European multicenter study. Crit Care. 2017; 21(1): 85. doi.org/10.1186/s13054-017-1673-6
Štítky
Anesteziologie a resuscitace Intenzivní medicína
Článek vyšel v časopiseAnesteziologie a intenzivní medicína
Nejčtenější tento týden
2020 Číslo 4- Jak souvisí postcovidový syndrom s poškozením mozku?
- Neodolpasse účinně snižuje pooperační bolest
- Neodolpasse jako ideální volba tam, kde je bolest provázena spasmem kosterního svalstva
- Optimalizace léčby pooperační bolesti snižuje nároky na zdravotní péči
- Použití Neodolpasse v indikaci pooperační bolesti
-
Všechny články tohoto čísla
- Doporučené postupy anestezie u pacientů trpících vzácným onemocněním v češtině – „OrphanAnesthesia.cz“
- Efekt midazolamu a dexmedetomidinu na funkci srdečních komor s využitím MRI – pilotní randomizovaná studie
- Perioperační péče o transgender pacienty/pacientky
- Audit antibiotické profylaxe v chirurgii
- Sto šedesát let od izolace kokainu a 115 let od syntézy prokainu – historie lokálních anestetik a jejich objevitelů
- Renesance ketaminu v léčbě dospělých pacientů v akutním a v kritickém stavu
- Náš článek po 10 letech: The practice of therapeutic mild hypothermia in cardiac arrest survivors in the Czech Republic
- Hemadsorpční metody u kriticky nemocných – dvojitá sázka naslepo?
- Inzulinová rezistence, hyperglykemie a proteinový katabolismus u kriticky nemocných: hledání klíčů k uzamčeným dveřím
- Suspektní imunitní trombocytopenie při Morbus Crohn
- Diagnostika COVID-19 pneumonie pomocí výpočetní tomografie, naše zkušenosti
- Perioperační použití gabapentinoidů v léčbě akutní pooperační bolesti – systematický přehled a metaanalýza
- Infekce krevního řečiště u kriticky nemocných: expertní stanovisko
- Tranexamová kyselina
- Hypoxie a hyperkapnie – jak fungují chemoreceptory?
- Disrupce rytmicity melatoninu v kritickém stavu
- Zajímavosti, tipy a triky, informace z jiných oborů
- CO2 oproti vzduchu významně sníží riziko vzduchové embolie při intervenčních ERCP a GIT endoskopiích
-
MEZIOBOROVÉ STANOVISKO
(evidenční číslo ČSARIM: 11/2020)
ZÁSADY ÚČELNÉ INDIKACE REMDESIVIRU U PACIENTŮ S COVID-19
- Anesteziologie a intenzivní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Tranexamová kyselina
- Hypoxie a hyperkapnie – jak fungují chemoreceptory?
- Audit antibiotické profylaxe v chirurgii
- Sto šedesát let od izolace kokainu a 115 let od syntézy prokainu – historie lokálních anestetik a jejich objevitelů
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



