-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Izolovaná infiltrace ledviny suspektními leukemickými buňkami – kazuistika s komplexní diferenciální diagnostikou neobvyklého stavu
Isolated kidney infiltration by suspected leukemic cells – complex differential diagnostics and an unusual case report
This article describes a case of highly suspected isolated diffuse kidney infiltration by myeloid leukemic cells, without primary bone marrow involvement or any pathological imaging findings in a patient presenting with fever of unknown origin, acute kidney injury, microcytic anaemia, weight loss, anorexia, dry cough and mild splenomegaly. This complex diagnostic process thus required repeated biopsy of both bone marrow and kidney, which subsequently ruled out leukemic infiltration. The presenting symptoms and pathological laboratory findings responded promptly to corticosteroid treatment, and our patient was finally diagnosed with tubulointerstitial nephritis.
Keywords:
acute myeloid leukaemia – fever of unknown origin – tubulointerstitial nephritis – acute kidney injury – kidney leukemic infiltration – myelosarcoma
Autoři: P. Vičar 1; B. Weinbergerová 2; M. Krejčí 2; D. Žáčková 2; N. Podstavková 2; P. Divácká 3; S. Hotárková 4; I. Svobodová 4; Z. Bednařík 4; K. Kamarádová 5,6; M. Borský 2; I. Ježíšková 2; M. Doubek 2; M. Hermanová 4; Z. Král 2; J. Mayer 2
Působiště autorů: LF MU Brno 1; Interní hematologická a onkologická klinika LF MU a FN Brno 2; Interní gastroenterologická klinika LF MU a FN Brno 3; I. ústav patologie LF MU a FN u sv. Anny v Brně 4; AeskuLab Patologie, Unilabs Company, Praha 5
Vyšlo v časopise: Transfuze Hematol. dnes,28, 2022, No. 1, p. 38-45.
Kategorie: Kazuistiky
doi: https://doi.org/10.48095/cctahd2022prolekare.cz5Souhrn
Práce předkládá popis případu s vyslovenou závažnou suspekcí na izolovanou difuzní infiltraci ledviny leukemickými myeloidními buňkami, avšak bez primárního postižení kostní dřeně a bez patologického nálezu na zobrazovacím vyšetření. To vše u pacientky došetřované pro současné febrilie nejasné etiologie, akutní neoligurickou renální insuficienci, mikrocytární anémii, váhový úbytek, nechutenství, suchý kašel a mírnou splenomegalii. Pro hematologa neobvyklý a nevysvětlitelný případ tak vyžadoval komplexní diagnostický postup zahrnující opakovaná bioptická vyšetření kostní dřeně a ledviny, která následně leukemickou infiltraci nepotvrdila. Symptomatologie a patologické laboratorní nálezy promptně zareagovaly na zavedenou léčbu kortikoidy a stav byl uzavřen jako akutní tubulointersticiální nefritida.
Klíčová slova:
akutní myeloidní leukemie – tubulointersticiální nefritida – renální insuficience – leukemická infiltrace ledviny – myelosarkom – teploty nejasné etiologie
ÚVOD
Akutní myeloidní leukemie (AML) je vzácné onemocnění s incidencí 3,5 případů na 100 000 obyvatel za rok charakteristické nádorovou transformací hematopoetické kmenové buňky a s ní spojenou ztrátou schopnosti buněčné diferenciace a následnou nekontrolovanou proliferací leukemických blastů s útlakem fyziologické krvetvorby [1]. Leukemické blasty mohou infiltrovat de facto jakýkoli orgán s nejčastějším výskytem extramedulárního postižení u AML s vyzráváním, myelomonoblastické a monoblastické AML [2–4]. Myelosarkom (myeloidní sarkom, granulocytární sarkom, chlorom) představuje extramedulární nádorovou masu proliferujících myeloidních blastů diagnostikovanou obvykle souběžně s diagnózou AML nebo v jejím průběhu, s incidencí 2–9 % a velmi špatnou prognózou [3,5,6]. Ve výjimečných případech se může myelosarkom (MS) objevit i před nástupem leukemie, a to až v řádu několika měsíců, s incidencí 0,6–2 % [4–9]. Běžnými místy postižení MS jsou kůže, kosti, měkké tkáně a další orgány, jako jsou reprodukční orgány, lymfatický aparát, orgány zažívacího traktu a centrální nervový systém [4–6,8]. Na rozdíl od pitevních nálezů, které velmi často myelosarkom popisují v ledvinách, je jeho výskyt ante mortem popisován zřídka – pravděpodobně vzhledem k současné chabé symptomatologii [9–11]. Akutní renální insuficience v souvislosti s extramedulární infiltrací ledvin při AML je v literatuře popsána většinou pouze formou kazuistik [12–14].
V naší práci popisujeme případ pacientky s vysloveným závažným a pro hematologa nevysvětlitelným podezřením na izolovanou leukemickou infiltraci ledviny, avšak bez primárního postižení kostní dřeně a bez korelátu na zobrazovacím vyšetření, zjištěnou v rámci diferenciální diagnostiky febrilií nejasné etiologie, akutní neoligurické renální insuficience, anémie a váhového úbytku. Kazuistika popisuje širokou komplexní diferenciální diagnostiku indukovanou závažným histologickým nálezem u mladé ženy.
POPIS PŘÍPADU
Začátkem května roku 2020 byla na naši kliniku po předchozím 2měsíčním došetřování na spádovém interním a hematologickém pracovišti přijata do té doby zdravá 18letá žena pod obrazem febrilií nejasné etiologie (subfebrilie až febrilie lehce nad 38 °C, dominantně v odpoledních a večerních hodinách, bez třesavky medikamentózně řešené paracetamolem bez antibiotik), suchého kašle, nechutenství s váhovým úbytkem 8 kg za měsíc, mikrocytární anémie nevyžadující substituční léčbu, hraniční splenomegalie na ultrazvuku a hraniční fluoro-deoxy-glukózové (FDG) aktivitě v tělech obratlů a zvětšené sleziny dle PET/CT (positron emission tomography/computed tomography). Trepanobiopsie provedená 27. dubna 2020 neprokázala žádný signifikantní patologický nález v kostní dřeni vč. imunofenotypizačního vyšetření, pouze reaktivní populaci plazmocytů bez průkazu klonality. Podobně ani ostatní vyšetření provedená lékaři referujícího pracoviště během posledních 2 měsíců před příjmem na naši kliniku – transthorakální echokardiografie, prostý zadopřední snímek hrudníku, sonografie třísel a axil – neodhalila možnou etiologii obtíží pacientky. V předchorobí nebyl zaznamenán kontakt s infekcí, toxickými látkami, pacientka nebrala žádné léky vč. hormonální antikoncepce. V době zahájení vyšetřování na spádovém pracovišti byly dostupné parametry renálních funkcí: S-kreatinin: 114 µmol/l, CKD-EPI: 1,01 ml/s/1,73m2.
Objektivní vyšetření při přijetí identifikovalo pouze bledší kolorit kůže a sliznic. Laboratornímu nálezu dominovaly nefropatie se sníženou kreatininovou clearance grade 3 a mikrocytární anémie chronických chorob grade 2 dle CTCAE verze 5.0 (Common Terminology Criteria for Adverse Events) [15]. V močovém sedimentu byla pouze mírná erytrocyturie a leukocyturie. Vedlejšími nálezy byly mírná elevace D-dimerů, fibrinogenu a C-reaktivního proteinu a zvýšená sedimentace erytrocytů. Dvacetičtyřhodinový sběr moči prokázal zvýšené odpady celkové bílkoviny. V diferenciálním rozpočtu leukocytů nebyly zaznamenány žádné početní odchylky. Pro vysoké suspicium na možnou infekční bakteriální etiologii uvedené symptomatologie jsme 14. května 2020 zahájili empirickou antibiotickou léčbu amoxicilinem-kyselinou klavulanovou. Vstupní výsledky analyzovaných laboratorních parametrů a zobrazovacích vyšetření jsou uvedeny v tab. 1.
Tab. 1. Vstupní charakteristika popisovaného případu – výsledky laboratorních a zobrazovacích vyšetření provedených v rámci diferenciální diagnostiky. 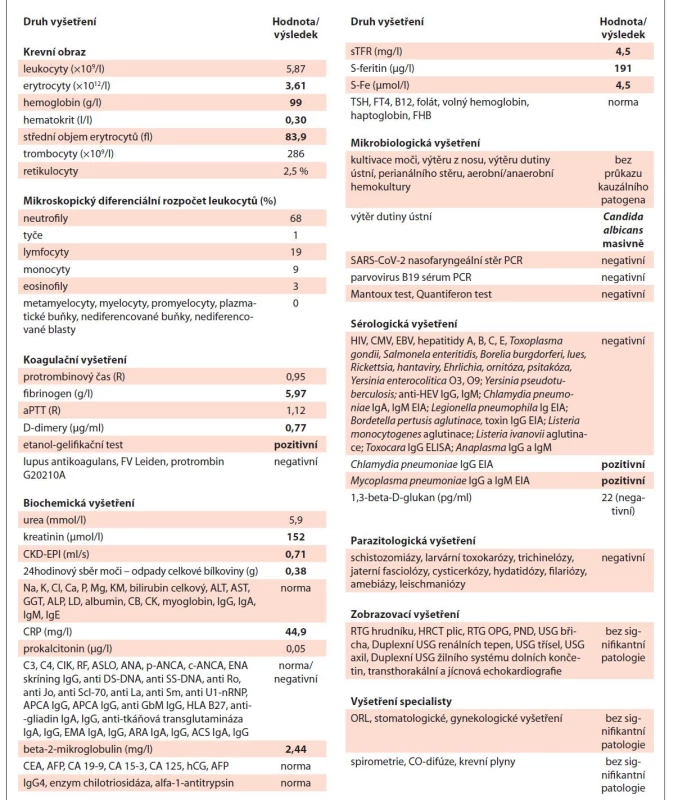
EIA – enzymová imunoassay, ELISA – Enzyme-Linked ImmunoSorbent Assay, HRCT – high resolution computed topography, ORL – otorinolaryngologické vyšetření, PET – pozitronová emisní tomografie, RTG – rentgenové vyšetření, UZ – vyšetření ultrazvukem V rámci široké diferenciální diagnostiky jsme zvažovali infekční, autoimunitní a nádorovou etiologii. Indikovali jsme sérii laboratorních testů k průkazu autoimunitních nemocí (RF, ASLO, C3, C4, CIK, ANA, ANCA, ENA a další), ke screeningu infekční a nádorové etiologie vč. opakovaného provedení SARS-CoV-2 PCR nazofaryngeálního stěru, série mikrobiologických vyšetření hemokultur, moči a stěrů dutiny ústní a rekta, sérologických vyšetření virových a bakteriálních původců infekce (hepatitidy A, B, C, E, a další), testy na průkaz parazitárních nemocí, tuberkulózy, HRCT (high resolution computed tomography) plic, sonografie ledvin a vývodného močového systému vč. dopplerovské monitorace renálních tepen, gynekologického, ORL a stomatologického vyšetření, transesofageální echokardiografie (tab. 1). Antibiotickou léčbu jsme dne 19. května 2020 změnili na cílený klaritromycin pro sérologický průkaz protilátek třídy IgG a IgM proti Mycoplasma pneumoniae. V opakovaně provedeném aspirátu kostní dřeně vč. trepanobiopsie byl nález normální trilineární hematopoézy s reaktivním zmnožením plazmocytů, monoklonalita séra nebyla prokázána. Všechna ostatní uvedená vyšetření nevykázala žádný patologický nález či odchylku, které by přiblížily etiologii klinického stavu naší pacientky.
Vzhledem k trvající symptomatologii s mírnými laboratorními známkami postižení ledvin, jejíž patogenezi jsme neznali, jsme se nakonec rozhodli indikovat biopsii ledviny. V lokální anestezii byla dne 20. května 2020 provedena biopsie levé ledviny pod ultrazvukovou kontrolou. Výkon proběhl bez komplikujících událostí. V rámci komplexního došetření zobrazovacími technikami byla dne 3. června 2020 navíc provedena PET/MR (PET/magnetická rezonance) hrudníku až pánve s nálezem přetrvávající stacionární mírné splenomegalie 12,5 × 10,0 × 5,0 cm s difuzně lehce vyšší FDG aktivitou v kostní dřeni a thymu uzavřené jako reaktivní etiologie při probíhajícím zánětlivém procesu. Vzhledem k výskytu plicní embolie v rodinné anamnéze (2× u otce) a vstupních známek aktivace procesů krevního srážení u pacientky byla provedena rozsáhlá diagnostika vrozených a získaných trombofilních stavů vč. vyšetření dopplerovské ultrasonografie žilního systému dolních končetin bez průkazu jakékoli laboratorní patologie a bez známek klinicky němé trombózy.
Biopsie ledviny zastihla renální kůru délky 10 mm s celkem 33 zachycenými glomeruly normálního vzhledu (0 globálně zaniklých), bez proliferace, bez depozit (IF detekce IgG, IgA, IgM, C3, C1q, lehkých řetězců kappa a lambda: vše negativní). Dominující morfologií byla infiltrace intersticia hodnocená jako součást tubulointersticiální nefritidy. Vzhledem k ne zcela typické morfologii zánětlivých intersticiálních elementů v I. čtení patologem byl zaslán bioptický vzorek ledviny ke II. čtení. Na základě výsledku I. čtení histologie bioptického vzorku ledviny se závěrem tubulointersticiální nefritidy při současně trvající symptomatologii subfebrilií, nechutenství, elevace CRP, neoligurické renální insuficience s proteinurií a anémie jsme v kooperaci s nefrology zahájili dne 9. června 2020 pulz kortikosteroidů (Solumedrol 125 mg/den i.v. celkem 3 dny) s promptním efektem ústupu subfebrilií, nechutenství, poklesu CRP. Pacientku jsme propustili z hospitalizace dne 12. června 2020 na pokračující perorální kortikoterapii – Medrol 32 mg/den.
Výsledek II. čtení přinesl dne 22. června 2020 překvapivou diferenciálně diagnostickou rozvahu nálezu intersticiální infiltrace populací elementů se suspektní monocytárně/monoblastickou diferenciací, případně plazmocytoidními dendritickými buňkami (obr. 1A–1E). Jednalo se tedy o závažné podezření na infiltraci leukemického charakteru. Přesná imunohistochemická charakteristika infiltrátu je popsána v tab. 2.
Obr. 1. Mikroskopický nález biopsie ledvinného parenchymu v základním barvení hematoxylin-eosinem v celkovém zvětšení 400x (A), v celkovém zvětšení 200x v barvení Periodic Acid Schiff (B) a imunohistochemický průkaz CD4 (C), CD43 (D) a CD34 (E). 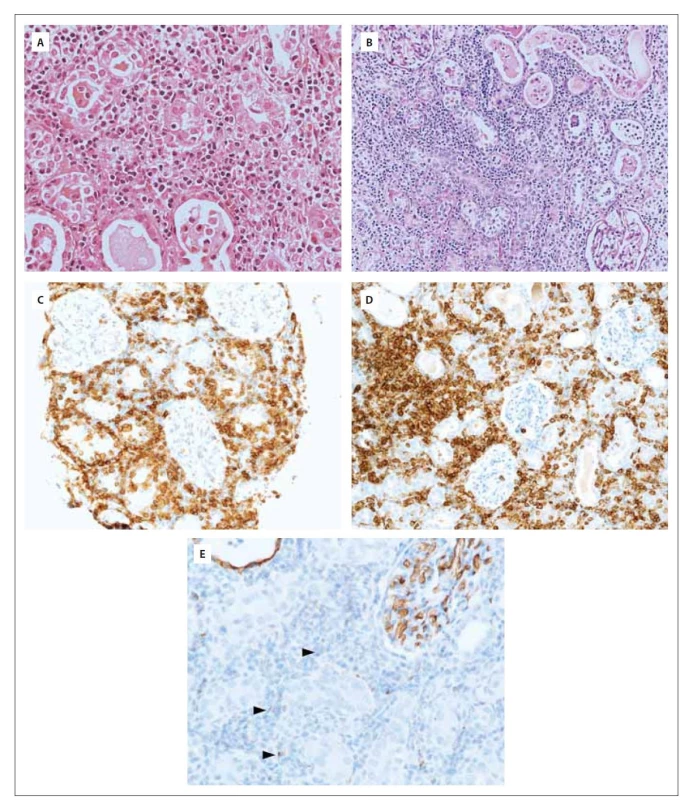
Ve všech snímcích zachyceno rozšířené tubulointersticium ledviny s denzní smíšenou zánětlivou celulizací. Tubuly multifokálně se zánětlivým infiltrátem intraepiteliálně (tubulitidou), intraluminálně četné neutrofilní granulocyty, uromukoid a proteinový exsudát. Zastižené elementy jsou střední velikosti a exprimují markery CD4 a CD43. Zhruba 5 % buněk je granulárně pozitivní v průkazu CD34 (šipky). Tab. 2. Imunohistochemická charakteristika intersticiálního infiltrátu ledviny se suspektní monocytárně/ monoblastickou diferenciací. 
CD – cluster of differentiation, LCA – leukocyte common antigen, TdT – terminální deoxynucleotidyl transferáza Z pohledu hematologa se diagnóza izolované leukemické infiltrace parenchymového orgánu bez patologického korelátu na zobrazovacím vyšetření a bez leukemické infiltrace kostní dřeně zdála jako vysoce nepravděpodobná. Navzdory tomu jsme v té době u již zcela asymptomatické pacientky s normálními parametry krevního obrazu vč. diferenciálního rozpočtu leukocytů, ledvinných funkcí a CRP vzhledem k suspekci na závažné hematoonkologické onemocnění indikovali komplexní přešetření. Dne 30. června 2020 jsme provedli re-trepanobiopsii bez průkazu jakékoli patologie krvetvorby vč. imunofenotypizačního, cytogenetického a histologického vyšetření kostní dřeně. Dne 21. července 2020 byla vzhledem k neobvyklé morfologii infiltrace ledvinného parenchymu při současné nemožnosti dalšího detailního imunohistochemického dourčení pro nedostatek materiálu (a tak i nevhodnosti provedení III. čtení bioptického vzorku) provedena nekomplikovaná re-biopsie levé ledviny s odběrem vzorků ke komplexnímu vyšetření histologickému, imunotypizačnímu a technikou sekvenování nové generace (next generation sequencing – NGS) pomocí genového panelu VariantPlex® Core Myeloid Kit for Illumina (Archer). Histologické vyšetření verifikovalo intersticiální infiltrát s převahou T buněčné populace v souvislosti s tubulointersticiální nefritidou. Původní zvažovaný infiltrát leukemického vzhledu již ve vzorku přítomen nebyl (obr. 2A, B). Imunotypizačním vyšetřením byly zachyceny převážně T lymfocyty, přičemž populace blastů či myeloidních buněk nebyla prokázána. NGS analýza vzorku ledvinné tkáně neidentifikovala žádnou mutaci v rámci panelu 37 testovaných genů u myeloidních malignit.
Obr. 2. Mikroskopický nález biopsie ledvinného parenchymu v celkovém zvětšení 100x v kombinovaném barvení PAS + Alcianová modř (A), v celkovém zvětšení 200x v kombinovaném barvení PAS + Alcianová modř (B). 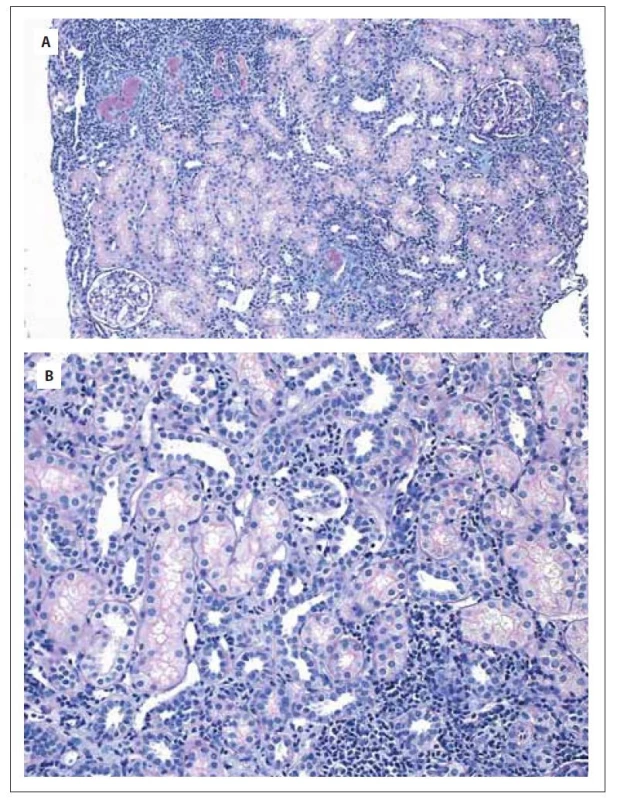
V obou snímcích patrný výrazný úbytek zánětlivého infiltrátu v intersticiu, tvořený dominantně mononukleáry a minoritně polymorfonukleáry, v tubulech jen fokálně tubulitida, místy uromukoid intraluminálně. V rámci pravidelné dispenzarizace v hematologické a nefrologické ambulanci byla u pacientky postupně snižována dávka kortikoidů a k 2. listopadu 2020 byla tato zcela ukončena. V současné době trvá kompletní remise tubulointersticiální nefritidy, pacientka je zcela bez symptomů s normálními parametry laboratorních testů (tab. 3).
Tab. 3. Výstupní charakteristika popisovaného případu – výsledky laboratorních vyšetření. 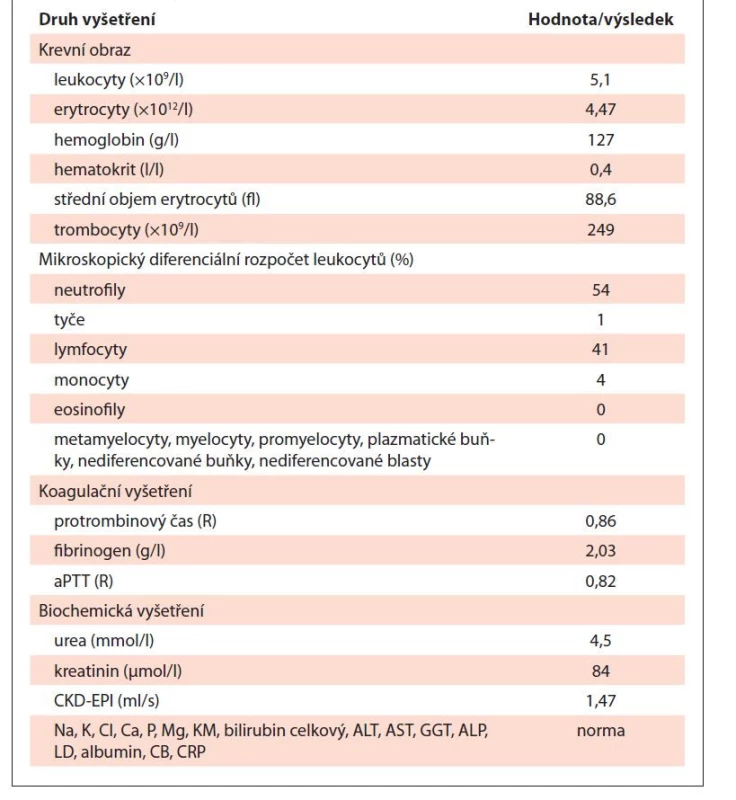
DISKUZE
Popsaný případ pacientky dokumentuje závažné a nezvyklé podezření na izolovanou infiltraci ledviny leukemickými myeloidními buňkami vyslovený na základě komplexní diferenciální diagnostiky horeček neznámého původu a současné neoligurické renální insuficience.
Diferenciální diagnostika febrilií nejasné etiologie (fever of unknown origin – FUO) se úzce prolíná všemi obory medicíny a představuje často svízelný, postupný a rozsáhlý diagnostický proces využívající řadu speciálních laboratorních a zobrazovacích metod a vyšetření [16]. Akutní tubulointersticiální nefritida (TIN) představuje skupinu chorob s velmi rozdílnou etiologií. Často se na jejím rozvoji uplatňuje současně několik faktorů (např. infekce a obstrukce). Vyloučíme-li pyelonefritidu, pak u většiny případů jde o imunitně zprostředkovanou reakci na nejrůznější léky, autoantigeny a infekce, vč. extrarenálních (např. spála). Akutní TIN je relativně vzácná diagnóza (představuje méně než 2 % renálních biopsií). V posledních letech se uvádí, že nejčastějším důvodem rozvoje TIN jsou reakce na léky (cca 70 % případů). U naší pacientky bylo postižení ledvin dominujícím příznakem a manifestovalo se dříve, než započala léčba antibiotiky. Biopsie ledviny byla provedena 6 dní od započetí antibiotické léčby. Infiltrace parenchymu ledviny u TIN je obvykle smíšená s variabilní příměsí plazmocytů a eozinofilů. Monotónní typ infiltrace „blastického“ vzhledu, jako je v našem případě, je krajně neobvyklý. I když jednoznačná etiologie TIN určena nebyla a můžeme o ní pouze spekulovat, mezioborová spolupráce, cílené hematologické vyšetření a reakce na zvolenou léčbu naštěstí pro pacientku vedly ke kompletní normalizaci ledvinných funkcí a kompletnímu ústupu klinických obtíží.
Kazuistika naší pacientky dokumentuje komplexnost vyšetřovacího postupu u FUO se současnou neoligurickou renální insuficiencí, proteinurií, mikrocytární anémií a váhovým úbytkem, který ve svém důsledku vyžadoval provedení renální biopsie. Následně bylo vysloveno závažné, avšak pro hematology nezvyklé a nepravděpodobné podezření na leukemickou infiltraci ledvinného parenchymu bez průkazu primárního postižení kostní dřeně při AML a bez korelátu na zobrazovacím vyšetření při myelosarkomu.
Extramedulární infiltrace tkání a orgánů leukemickými blasty (extramedulární leukemie, EML) je v literatuře popisována až u 40 % pacientů s AML [2,17]. Častěji se EML vyskytuje u dětí s AML typu M4 a M5 dle FAB klasifikace [2,17]. Nejčastěji postiženými orgány EML jsou kůže, měkké tkáně, kosti, gingivy a centrální nervový systém [4–6,8]. Myelosarkom je nejčastější forma EML představující lokalizovanou nádorovou masu s velmi raritním průkazem v ledvinách ante mortem [12–14]. Diagnóza je založena na průkazu ložiskového procesu pomocí zobrazovacího vyšetření a na histologické a imunohistochemické analýze bioptického vzorku. Daleko častěji je MS ledvin diagnostikovaný post mortem [10]. Extramedulární ložisková infiltrace ledviny myelosarkomem, projevující se jako první příznak AML (nebo předcházející její diagnózu AML), byla publikována formou kazuistik, přičemž v jednom případě byla diagnostikována AML a v druhém případě blastický zvrat CML [9,11].
Doposud byly podobně v literatuře popsány – opět pouze formou kazuistik – případy difuzní extramedulární infiltrace ledviny bez průkazu ložiskového procesu (myelosarkomu) při AML s akutní renální insuficiencí [12–14]. Čtyři publikované případy uváděly anamnézu variabilní symptomatologie vč. únavy, břišní bolesti, zvracení a průjmů, váhového úbytku. Pacienti vykazovali akutní renální insuficenci a zobrazovacími vyšetřeními byla ve třech případech zjištěna oboustranná nefromegalie. Současně měly uvedené případy diagnostikovanou AML typu M2 nebo M4 s doprovodnou leukocytózou a onkologická léčba u všech vedla k úpravě renálních parametrů.
Podobné symptomy byly prezentovány i v případě naší pacientky s vysloveným podezřením na difuzní leukemickou infiltraci ledviny, u které jsme však na rozdíl od publikovaných případů ani opakovaným trepanobioptickým vyšetřením kostní dřeně infiltraci hematologickou malignitou neprokázali. Izolovaná difuzní leukemická infiltrace ledviny bez primárního postižení kostní dřeně nebyla doposud v literatuře popsána. Pokud se jednalo o lokalizované postižení ledvin, jak bylo popsáno výše, pak pouze formou myeloidního sarkomu s korelátem na zobrazovacím vyšetření. V našem případě jsme zobrazovacími vyšetřeními vč. PET/MR žádný patologický nález na ledvinách opakovaně nedetekovali. Navzdory zmíněným skutečnostem jsme z důvodu vyslovení podezření na tak závažný nález infiltrace tkáně hematologickým maligním onemocněním u mladé pacientky a kvůli nedostatečnému materiálu první biopsie přistoupili k rebiopsii ledviny. Ať už se její provedení retrospektivně jeví jako jakkoli diskutabilní, při provedení zkušeným nefrologem je bezpečná. Také jsme přistoupili k důslednému opakovanému došetření kostní dřeně a zároveň histologickému došetření bioptického vzorku postižené tkáně vč. využití metod imunofenotypizačních a molekulárně-biologických s vědomím zpracování materiálu nestandardního pro uvedené techniky. Uvedená komplexní diagnostika již v našem případě následně leukemickou infiltraci nepotvrdila. Pacienti s takto závažnou suspekcí na onkologické onemocnění by každopádně měli být dlouhodobě a pravidelně dispenzarizováni v kooperaci erudovaného hematologa a nefrologa.
ZÁVĚR
Kazuistika představila v literatuře doposud nepublikovaný a z pohledu hematologa nezvyklý případ popisující závažné podezření na izolovanou extramedulární difuzní leukemickou infiltraci ledviny bez korelátu na zobrazovacím vyšetření u mladé pacientky komplexně došetřované pro současnou neoligurickou akutní renální insuficienci a horečky nejasné příčiny. Práce dokumentovala význam hodnocení nálezu z jednoho bioptického vzorku více patology a někdy nevyhnutelnou nutnost rebiopsie k verifikaci závažného nálezu. Zároveň je však potřeba posuzovat nálezy s rozvahou a vyhnout se případnému excesivnímu vyšetřování a unáhleným diagnostickým závěrům.
PODÍL AUTORŮ NA PŘÍPRAVĚ RUKOPISU
PV, BW – napsání rukopisu
BW, MK, DŽ, NP, PD, SH, IS, ZB, KK, MB, IJ, MD, MH, ZK, JM – diagnostika a léčba pacienta, revize rukopisu.
PODĚKOVÁNÍ
Práce byla podpořena grantem MZ ČR – RVO (FNBr 65269705).
PROHLÁŠENÍ AUTORŮ O KONFLIKTU ZÁJMŮ
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Do redakce doručeno dne: 26. 10. 2021.
Přijato po recenzi dne: 22. 11. 2021.
MUDr. Barbora Weinbergerová, Ph.D.
Interní hematologická a onkologická klinika LF MU a FN Brno
Jihlavská 20
625 00 Brno
e-mail: weinbergerova.barbora@fnbrno.cz
Zdroje
1. Arber DA, Orazi A, Hasserjian R, et al. The 2016 revision to the World Health Organization classification of myeloid neoplasms and acute leukemia. Blood. 2016; 127 (20): 2391–2405.
2. Byrd JC, Edenfield WJ, Shields DJ, Dawson NA. Extramedullary myeloid cell tumors in acute nonlymphocytic leukemia: a clinical review. J Clin Oncol. 1995; 13 (7): 1800–1816.
3. Wang HQ, Li J. Clinicopathological features of myeloid sarcoma: Report of 39 cases and literature review. Pathol Res Pract. 2016; 212 (9): 817–824.
4. Pileri SA, Ascani S, Cox M-C, et al. Myeloid sarcoma: Clinico-pathologic, phenotypic and cytogenetic analysis of 92 adult patients. Leukemia. 2007; 21 : 340–350.
5. Almond LM, Charalampakis M, Ford SJ, et al. Myeloid sarcoma: presentation, diagnosis, and treatment. Clin Lymphoma Myeloma Leuk. 2017; 17 (5): 263–267.
6. Paydas S, Zorludemir S, Ergin M. Granulocytic sarcoma: 32 cases and review of the literature. Leuk Lymphoma. 2006; 47 : 2527–2541.
7. Meis JM, Butler JJ, Osborne BM, Manning JT. Granulocytic sarcoma in nonleukemic patients. Cancer. 1986; 58 : 2697–2709.
8. Yamauchi K, Yasuda M. Comparison in treatments of nonleukemic granulocytic sarcoma: Report of two cases and a review of 72 cases in the literature. Cancer. 2002; 94 : 1739–1746.
9. Agrawal V, Gupta A, Gupta R, Sharma MC, Das P. Nonleukemic granulocytic sarcoma of kidney with mixed phenotype blasts: a diag - nostic dilemma. Indian J Pathol Microbiol. 2011; 54 (3): 606–608.
10. Liu PI, Ishimaru T, McGregor DH, Okada H, Steer A. Autopsy study of granulocytic sarcoma (chloroma) in patients with myelogenous leukemia, Hiroshima-Nagasaki 1949–1969. Cancer. 1973; 31 : 948–955.
11. Bagg MD, Wettlaufer JN, Willadsen DS, et al. Granulocytic sarcoma presenting as a diffuse renal mass before hematological manifestations of acute myelogenous leukemia. J Urol. 1994; 152 (20): 2092–2093.
12. Duda J, Zoger S. Presentation of M4 acute myeloid leukemia in anuric renal failure with hyperuricemia and enlarged kidneys. J Pediatr Hematol Oncol. 2002; 24 : 55–58.
13. Tapper EB, Luptakova K, Joyce RM, Tzachanis D. A 78-year-old man with acute myeloid leukemia (AML) and acute renal failure. Am J Case Rep. 2014; 15 : 364–367.
14. Aratani S, Aburakawa S, Ryotokuji T, et al. Primary tumor infiltration and severe acute kidney injury in patients with acute myeloblastic leukemia. J Nippon Med Sch. 2020; 87 (1): 43–48.
15. https: //ctep.cancer.gov/protocoldevelopment/electronic_applications/docs/ctcae_v5_quick_reference_5x7.pdf. Accessed 23 January 2021.
16. Křivanová A, Adam Z, Mayer J, et al. Teplota nejasné etiologie: příčiny a diagnostický postup. Vnitř Lék. 2007; 53 (2): 169–178.
17. Bisschop MM, Révész T, Bierings M, et al. Extramedullary infiltrates at diagnosis have no prognostic significance in children with acute myeloid leukaemia. Leukemia. 2001; 15 (1): 46–49.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek EditorialČlánek Dr. Horská slaví 70 let
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2022 Číslo 1- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Steroidní a nesteroidní inhibitory aromatázy v léčbě rakoviny prsu u postmenopauzálních žen
- Ibrance® – nová šance pro pacientky s HR+/HER2– karcinomem prsu
-
Všechny články tohoto čísla
- Novinky v léčbě mycosis fungoides a Sézaryho syndromu
- Současný výskyt akutní megakaryoblastické leukemie a germinálního tumoru mediastina – kazuistika a přehled literatury
- Editorial
- Izolovaná infiltrace ledviny suspektními leukemickými buňkami – kazuistika s komplexní diferenciální diagnostikou neobvyklého stavu
- Doporučení České společnosti paliativní medicíny ČLS JEP a Společnosti pro transfuzní lékařství ČLS JEP
- Doporučení laboratorní sekce České hematologické společnosti ČLS JEP
- MUDr. Marcela Lukášová – ušlechtilá dáma české hematologie
- Muž s dýmkou, prof. MUDr. Pavel Klener, DrSc., se v dubnu 2022 dožívá 85 let
- Doc. RNDr. Miroslav Pecka, CSc., slaví 75 let
- Primář MUDr. Vladimír Komrska, CSc., sedmdesátiletý
- MUDr. Jan Haber, CSc., sedmdesátiletý
- Dr. Horská slaví 70 let
- Letermovir u pacientů po alogenní transplantaci krvetvorných buněk – přehled literatury
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Doporučení laboratorní sekce České hematologické společnosti ČLS JEP
- MUDr. Jan Haber, CSc., sedmdesátiletý
- Letermovir u pacientů po alogenní transplantaci krvetvorných buněk – přehled literatury
- Doporučení České společnosti paliativní medicíny ČLS JEP a Společnosti pro transfuzní lékařství ČLS JEP
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



