-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Vzdělávací workshop – uplatnění nových technologií v precizní medicíně CML a ALL
Autoři: N. Čuřík; J. Koblihová
Působiště autorů: Ústav hematologie a krevní transfuze, Oddělení molekulární genetiky, Praha
Vyšlo v časopise: Transfuze Hematol. dnes,26, 2020, No. 1, p. 66-69.
Kategorie: Vzdělávací workshop
Oddělení molekulární genetiky Ústavu hematologie a krevní transfuze (ÚHKT) pod vedením doc. Kateřiny Machové Polákové organizuje pod záštitou České hematologické společnosti (ČHS) a České leukemické skupiny – pro život (CELL) na svém pracovišti každé dva roky vzdělávací workshop zaměřený především na prohlubování znalostí a výměnu zkušeností domácí a slovenské odborné veřejnosti zabývající se diagnostikou, monitorováním a léčbou chronické myeloidní leukemie (CML). 15. listopadu 2019 se konal již 5. ročník této odborné akce. Letošní workshop se v duchu svého názvu zaměřil na využití nových molekulárně genetických technologií, především sekvenování nové generace, nejen pro precizní medicínu CML, ale také pro stratifikaci a sledování měřitelné reziduální nemoci u akutní lymfocytární leukemie (ALL).
Odborný program zahájila svojí přednáškou dr. Simona Soverini z italské University of Bologna, která představila studii NEXT-IN-CML zaměřenou na využití sekvenování nové generace (NGS) pro detekci mutací v kinázové doméně (KD) onkogenu BCR-ABL1. Vývoj těchto mutací je spojen nejen s rezistencí pacientů s CML na léčbu inhibitory tyrozinových kináz (TKI), ale také s přeprogramováním genové exprese leukemických buněk na pokročilou fázi choroby [1]. Pacienti s mutacemi v KD BCR-ABL1 mají zvýšenou pravděpodobnost získání dalších mutací, přičemž dvě a více mutací v KD BCR-ABL1 v jednom leukemickém klonu (tzv. kompozitní mutace) představují, zejména v případě přítomnosti mutace T315I, stále významný klinický problém léčby CML. Existuje proto potřeba spolehlivé detekce mutací v KD BCR-ABL1 již na nízké hladině (low-level mutace), aby mohlo dojít ke včasnému a s ohledem na typ mutace vhodně navrženému terapeutickému zásahu. Standardní a v současnosti rutinně využívaná metoda Sangerova sekvenování s citlivostí detekce na úrovni 15–20 % mutovaného transkriptu BCR-ABL1 tomuto požadavku nevyhovuje. S využitím NGS byly u pacientů s CML s rezistencí na TKI retrospektivně vysledovány mutace výrazně dříve, než se je podařilo detekovat Sangerovým sekvenováním. Metoda NGS rovněž na rozdíl od Sangerova sekvenování umožňuje ve většině případů odlišit kompozitní od polyklonálních mutací. Dosud nicméně stále chybí prokázání klinické relevance detekce low-level mutací na rozsáhlé kohortě prospektivně sledovaných pacientů, přičemž rutinní implementace vyšetřování mutací v KD BCR-ABL1 pomocí NGS je ve většině laboratoří stále pouze v přípravě. Za tímto účelem vznikla v roce 2015 NEXT-IN-CML studie, která se v první fázi zaměřila na správnost, přesnost a reprodukovatelnost stanovení mutací pomocí NGS ve čtyřech italských laboratořích. Falešná negativita i falešná pozitivita stanovení mutací nepřekročila 3 %. V druhé fázi proběhlo paralelní srovnání Sangerova sekevenování a NGS na pacientech (n = 236) s neoptimálním výsledkem léčby CML (n = 142 failure; n = 112 warning podle kritérií stávajících doporučení Evropské leukemické sítě [2]). Sangerovo sekvenování stanovilo přítomnost mutací v KD BCR-ABL1 u 25 % těchto pacientů, zatímco pomocí NGS byla detekována přítomnost mutací v nízké hladině u dalších 22 % pacientů (celkem tedy u 47 % pacientů celého souboru). Využitím citlivější metody NGS se navíc zjistilo, že u poloviny pacientů, u kterých přítomnost dominantní mutace odhalilo Sangerovo sekvenování, je přítomna další mutace v nízké hladině, kterou již Sangerovo sekvenování neodhalilo. Dr. Soverini na několika příkladech demonstrovala, jak nezachycení konkrétních mutací v nízkých hladinách chybně ovlivnilo volbu (či nevyužití) terapeutického zásahu a umožnilo následnou evoluci a expanzi mutovaného klonu. Studie rovněž ukázala, že u pacientů, kterým byla pomocí NGS detekována přítomnost dvou a více mutací, častěji dochází k selhání léčby než u pacientů s jednou mutací, přičemž kompozitní mutace se vyskytovaly poměrně vzácně (n = 5).
Předběžné výsledky NEXT-IN-CML studie ukazují, že přítomnost opakovaně detekovaných mutací v KD BCR-ABL1 v nízké hladině může mít prognostický význam. Využití metody NGS, která je schopná tyto mutace odhalit, poskytuje přesnější obraz stavu pacienta a může vést k proaktivní změně léčby, z níž má pacient prospěch. Při centralizaci vzorků pacientů do několika referenčních laboratoří přitom vyjdou NGS analýzy cenově srovnatelně nebo i výhodněji než využití Sangerova sekvenování. Na základě výše uvedených skutečností dr. Soverini doporučuje zavedení rutinního vyšetřování mutací v KD BCR-ABL1 u všech pacientů s neoptimální léčbou na 1. nebo 2. linii terapie TKI, stejně jako u pacientů v pokročilých fázích CML a u pacientů s časným relapsem nemoci po vysazení TKI. V současné době dr. Soverini et al. data a doporučení publikovali jako souborné stanovisko v časopise Journal of Hematology & Oncology (2019 Dec 5;12(1):131) [3].
Po tomto sdělení následovala moderovaná diskuse na téma zavedení NGS a digitální PCR pro detekci BCR-ABL1 mutací u CML a Ph+ALL do lékařské praxe, které se chopila doc. Kateřina Machová Poláková. Není sporu o tom, že NGS dříve či později nahradí v molekulárně genetických laboratořích při rutinním vyšetřování pacientů s CML vývojem překonané Sangerovo sekvenování. Diskuse se vedou o tom, kdy mutační analýzy u CML pomocí NGS provádět. Obecně panuje shoda, že k takové analýze by se mělo přistoupit u všech pacientů v pokročilých fázích onemocnění, při selhání léčby (failure) a před její změnou. Ukazuje se, že detekce mutací do 3. měsíce po nasazení léčby TKI naznačuje (evolučně biologicky) rozvinutou CML a predikuje progresi onemocnění do pokročilých klinických fází. Konsenzus využití NGS analýzy není jasný u pacientů s odpovědí ´warning´ a pacientů na 2. linii léčby s TKI. Tato problematika by měla být řešena v rámci nových doporučení Evropské leukemické sítě, jejichž příprava se ale zpožďuje. Limitaci využití NGS také představuje neexistence softwaru pro spolehlivou filtraci nukleotidových záměn (odlišení skutečných mutací od technických chyb čtení nukleotidové sekvence) a chybějící doporučení, jak vyhodnocovat získané výsledky.
Doc. Machová ve svém příspěvku rovněž ukázala, že alelově specifická – kapková – digitální PCR (ASO-ddPCR), detekující na rozdíl od NGS mutace přímo na genomické úrovni, disponuje v některých případech ještě vyšší senzitivitou než NGS. Je ovšem zřejmé, že ddPCR představuje oproti NGS limitaci v podobě analýzy jen konkrétních typů mutací. Nicméně v příhodných případech může využití ddPCR potvrdit přítomnost mutace a zajistit vysoce senzitivní monitorování měřitelné reziduální nemoci, resp. monitorování klonální evoluce mutovaných klonů, jak ukazuje navrhované schéma (obr. 1) Také díky své rychlosti provedení analýzy a vysoké citlivosti je ddPCR užitečná pro rychlé zjištění přítomnosti klinicky vysoce rezistentních mutací vůči TKI, jako T315I, zejména u Ph+ALL, kde rychlost znalosti mutačního stavu je zásadním parametrem v lékařské praxi.
Obr. 1. Navrhované využití NGS a alelově specifické ddPCR v klinické praxi u CML v chronické fázi (autor obrázku K. Machová Poláková) 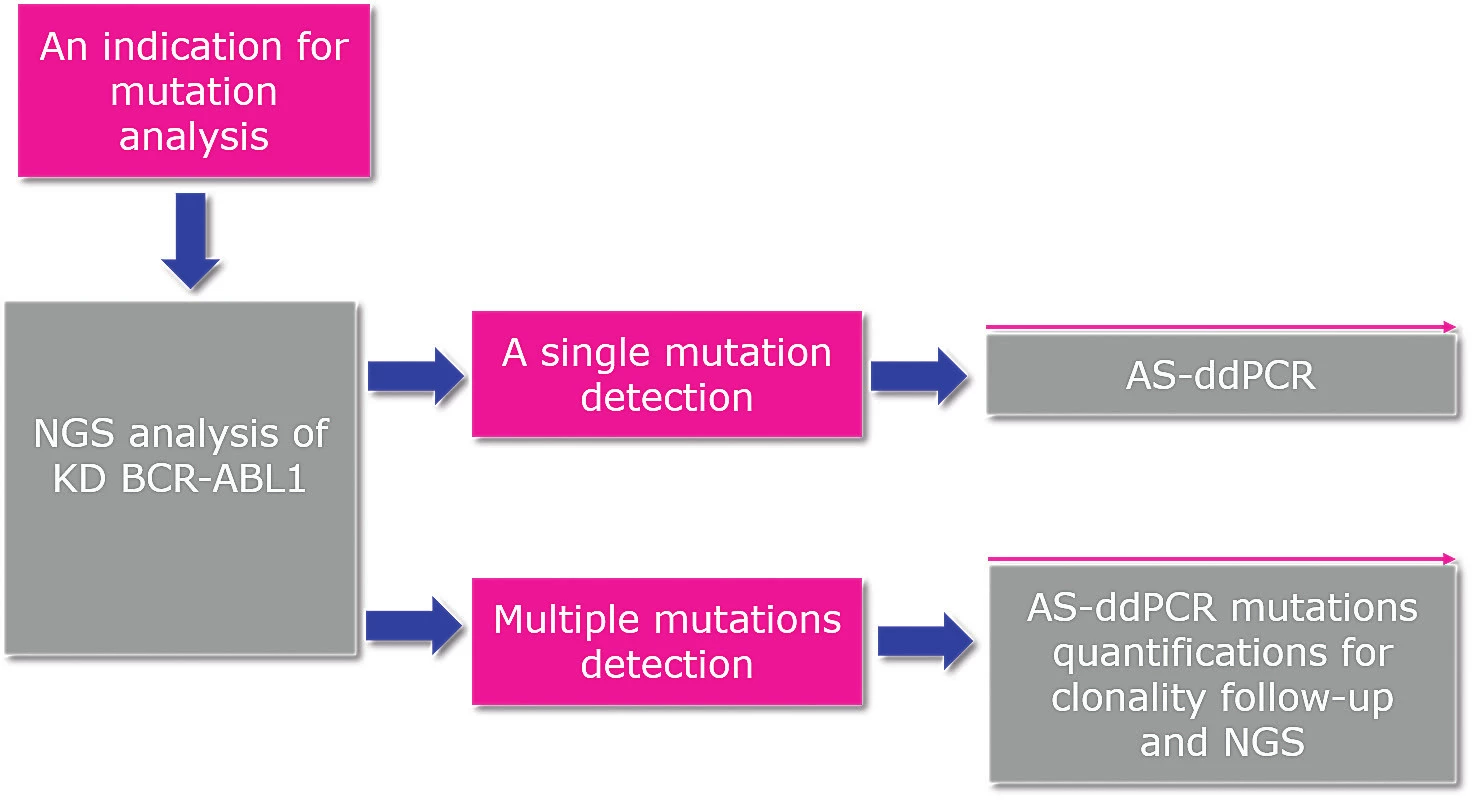
Dopolední přednáškový blok zakončil prof. Jan Zuna z CLIP (Childhood Leukemia Investigation Prague), Kliniky dětské hematologie a onkologie 2. LF UK a FN Motol. Jeho přednáška se týkala využití NGS v diagnostice a monitorování ALL. ALL představuje biologicky a klinicky vysoce heterogenní onemocnění. Od roku 1970, kdy byly u pacientů s ALL zavedeny první stratifikační protokoly podle rizika selhání léčby, došlo do dnešních dní postupně k úplnému nahrazení „klasických“ prognostických kritérií (leukocytóza, postižení mediastina, věk apod.) kritérii molekulárně genetickými s výrazným prognostickým významem samotné odpovědi na léčbu.
V molekulárně genetické diagnostice subtypů ALL se uplatňuje PCR, celogenomové vyšetření jednobodových polymorfismů (SNP-array) a v neposlední řadě na NGS založené sekvenování celkového transkriptomu (RNA-seq) a celkového exomu (WES) pacienta. Zatímco SNP-array umožňuje stanovit monoalelické a bialelické delece, amplifikace částí genomu a odlišit stavy hyperdiploidie, duplikované hypodiploidie a uniparentální disomie, pomocí RNA-seq a WES lze stanovit fúzní geny, mutace a expresní profily, které upřesňují zařazení pacientů do genetických podskupin i do léčebných protokolů. Díky využití NGS schopného odhalit primární aberace u jednotlivých pacientů z původně heterogenních a nejasně vymezených skupin („B-other“) se podařilo dosáhnout rozdělení téměř všech případů ALL do příslušných subtypů, jak ukazuje obrázek 2 [3].
Obr. 2. Rozdělení 410 dětských BCR-ABL1-negativních ALL z B-prekurzorů na základě „klasických“ metod a s pomocí NGS (Zaliova et al., Haematologica 2019) [4] poskytl prof. Jan Zuna ![Rozdělení 410 dětských BCR-ABL1-negativních ALL z B-prekurzorů na základě „klasických“ metod a s pomocí NGS (Zaliova et al., Haematologica 2019) [4] poskytl prof. Jan Zuna](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/3b1581195660723aec6e1f8518114707.jpeg)
NGS se vedle jiných metod dále používá pro monitorování měřitelné reziduální nemoci ALL na základě detekce přestaveb genů pro imunoglobuliny a T-buněčné receptory (IG/TCR) specifických pro leukemický klon. Do nedávna se tyto přestavby rutinně stanovovaly Sangerovým sekvenováním a následně se monitorovaly pomocí pacient specifické qPCR (se specifickými primery), což je časově náročné a pracné. NGS přístup umožňuje, vedle časové a pracovní úspory při srovnatelných nákladech (závislých především na počtu vyšetření a obratu vzorků), stanovit repertoár fyziologických IG/TCR přestaveb, jehož rozsah je sám o sobě prognostický faktor; čím je po skončení indukční léčby širší, tím příznivější je prognóza. Přístup aplikovaný v laboratořích CLIP pro dětské pacienty s ALL představuje v současnosti již kombinaci využití NGS pro stanovení fúze a qPCR pro její další monitorování, což lze označit za „polo-NGS postup“. Standardizace monitorování pomocí NGS zatím probíhá v rámci EuroMRD skupiny.
Prof. Zuna v neposlední řadě připomněl nové postupy v léčbě ALL, zahrnující inhibitory kináz, proteazomu (bortezomib) nebo antiapoptotických proteinů (anti-BCL2 venetoclax), využití monoklonálních (anti-CD22 inotuzumab, anti-CD38 daratumumab) a případně bispecifických (anti-CD19 + anti-CD3 blinatumomab) protilátek a rovněž CAR-T buněk, které lze využít mimo jiné i při relapsu onemocnění v CNS. Celkově lze shrnout, že NGS umožňuje u pacientů s ALL spolehlivě detekovat získané genetické aberace, odhalit heterogenní biologickou podstatu a charakter jednotlivých subtypů onemocnění a díky novým postupům a řízení intenzity a typu léčby dosáhnout dalšího zlepšení terapeutických výsledků.
V odpolední přednášce dr. Hany Žižkové z Oddělení molekulární genetiky ÚHKT bylo v návaznosti na předchozí sdělení doc. Machové představeno využití ddPCR pro detekci měřitelné zbytkové nemoci u CML. V současné klinické praxi CML – a zejména s ohledem na snahu bezpečně vysazovat pacientům léčbu TKI s dosažením dlouhodobé remise bez léčby (TFR) – se klade stále větší důraz na spolehlivé monitorování hlubokých molekulárních odpovědí s detekcí ≤ 0,01 % BCR-ABL1 v IS (při detekci dostatečného počtu transkriptu kontrolního genu).
Digitální PCR skýtá výhody absolutní kvantifikace BCR-ABL1 molekul bez potřeby referenčních vzorků a dosažení vysoké citlivosti a spolehlivosti měření. Paralelní testování qPCR a ddPCR v laboratoři ÚHKT ukázalo, že ddPCR poskytuje výrazně citlivější detekci měřitelné reziduální nemoci v porovnání s qPCR při hladinách transkriptu pod 0,01 % BCR-ABL1 IS. Pro obě metody byly stanoveny limity detekce (LoD) a limity kvantifikace (LoQ). Na jejich základě při splnění dalších technických kritérií byly výsledky interpretovány a stratifikovány jako (1) negativní – v žádném z replikátů nebyly detekovány BCR-ABL1 kopie nebo průměrný počet kopií detekovaný v replikátech < LoD; (2) pozitivní nekvantifikovatelné – průměrný počet detekovaných kopií BCR-ABL1 leží v rozmezí LoD-LoQ; (3) pozitivní kvantifikovatelné – průměrný počet detekovaných kopií BCR-ABL1 je ≥ LoQ. ddPCR byla při detekci BCR-ABL1 citlivější než qPCR u 243 vzorků a qPCR byla při detekci BCR-ABL1 citlivější než ddPCR u 22 vzorků. U 527 vzorků byly výsledky měření konkordantní. Do této skupiny spadaly prakticky všechny vzorky (n = 294) s detekcí ≥ 0,01 % BCR-ABL1 IS. Porovnání qPCR a ddPCR při detekci BCR-ABL1 prokázalo, že ddPCR se jeví jako optimální metoda detekce onkogenu u pacientů s CML v TFR, po transplantaci kostní dřeně, při monitorování přítomnosti raritních typů přestaveb BCR-ABL1, kde pro qPCR chybí standardizace detekce, případně u pacientů s BCR-ABL1+ ALL.
Závěr vzdělávacího workshopu patřil kulatému stolu věnovanému mezilaboratorní standardizaci vyšetřování BCR-ABL1. V rámci konsorcia evropských odborníků The European Treatment and Outcome Study for CML (EUTOS 2018) se chýlí ke zdárnému konci mezinárodní koncept pro standardizaci vyhodnocování BCR-ABL1 s přestavbou major. Na základě metodologie původně vyvinuté laboratoří v australském Adelaide, využívající při standardizaci měření mezi jednotlivými laboratořemi konverzní faktory, došlo v posledních letech k rozšíření mezinárodních porovnání zkoušek kvality a především k výraznému nárůstu laboratorně vydávaných výsledků kvantifikace BCR-ABL1 transkriptu v IS. Mezi současné cíle v rámci EUTOS patří příprava sekundárních referenčních panelů kalibrovaných na primární standardy kvantifikace BCR-ABL1 podle WHO a také validace měření BCR-ABL1 na hladině MR4,5. Koordinátorem projektu je Wessex Regional Genetics Laboratory v britském Salisbury pod vedením prof. Crosse. LyoPanel, který využívá set pěti vzorků lyofilizovaných směsí buněčných linií K562 (BCR-ABL1 pozitivní) a HL-60 (BCR-ABL1 negativní) kalibrovaných pro měření BCR-ABL1 major v hladinách od 10 do 0,0032 (MR4,5) % IS, byl po počáteční evaluaci ve 44 laboratořích od září 2018 testován padesáti laboratořemi. Byly ověřeny a hodnoceny rozdíly konverzních faktorů LyoPanelu a předchozích konverzních faktorů, přičemž kritérium maximálně 1,6násobného rozdílu obou faktorů vyhověla velká většina laboratoří. Problémem některých laboratoří byla nelinearita nebo nestabilita esejí. Od září 2019 byl na trh uveden AcrometrixTM RUO panel, fungující na podobném principu, který aktuálně čeká na schválení americkou FDA. Rovněž validace měření BCR-ABL1 na hladině MR4,5 proběhla v zúčastněných laboratořích úspěšně, a to bez ohledu na použitý kontrolní gen. Úzus nicméně nepanuje ohledně používaných standardů interní kontroly kvality, které si laboratoře vybírají různě. Jako optimální se jeví využití standardů pro vysokou a nízkou hladinu BCR-ABL1. I zde se čeká na nová doporučení Evropské leukemické sítě.
Vzdělávací workshop
RNDr. Nikola Čuřík, Ph.D.
UHKT, Odděleni molekulárni genetiky
U Nemocnice 1
128 20 Praha2
e-mail: nikola.curik@uhkt.cz
Zdroje
- Radich JP, Dai H, Mao M, et al. Gene expression changes associated with progression and response in chronic myeloid leukemia. Proc Natl Acad Sci USA. 2006;103(8):2794–2799.
- Baccarani M, Deininger MW, Rosti G, et al. European LeukemiaNet recommendations for the management of chronic myeloid leukemia: 2013. Blood. 2013;122(6):872–884.
- Soverini S, Abruzzese E, Bocchia M, et al. Next-generation sequencing for BCR-ABL1 kinase domain mutation testing in patients with chronic myeloid leukemia: a position paper. J Hematol Oncol. 2019;12(1):131.
- Zaliova M, Stuchly J, Winkowska L, et al. Genomic landscape of pediatric B-other acute lymphoblastic leukemia in a consecutive European cohort. Haematologica. 2019;104(7):1396–1406.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2020 Číslo 1- U pacientů s traumatem je častěji dosaženo adekvátních hladin anti-Xa při dávkování enoxaparinu podle hmotnosti
- Steroidní a nesteroidní inhibitory aromatázy v léčbě rakoviny prsu u postmenopauzálních žen
- Nedostatečné dávkování enoxaparinu je u pacientů po ortopedickém výkonu časté a zvyšuje riziko tromboembolické nemoci
-
Všechny články tohoto čísla
- Chromozomové změny u chronické lymfocytární leukemie, jejich prognostický a prediktivní význam
- Chromozomové aberace a jejich role v transformaci chronické lymfocytární leukemie v éře léčby inhibitory BCR signalizace
- Molekulárně genetické změny u Richterovy transformace chronické lymfocytární leukemie
- Mutace asociované s rezistencí u pacientů s chronickou lymfocytární leukemií léčených ibrutinibem, idelalisibem a venetoklaxem
- Rozvoj Richterovy transformace u nemocného s refrakterní chronickou lymfocytární leukemií na léčbě ibrutinibem
- Transformace chronické lymfocytární leukemie do Hodgkinovy varianty Richterova syndromu
- Vzdělávací workshop – uplatnění nových technologií v precizní medicíně CML a ALL
- Novinky z redakce
- Prof. MUDr. Ladislav Jebavý, CSc., slaví 70 let
- Životní jubileum MUDr. Věry Vozobulové
- Editorial
- Richterova transformace chronické lymfocytární leukemie v éře léčby inhibitory buněčných drah
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Chromozomové změny u chronické lymfocytární leukemie, jejich prognostický a prediktivní význam
- Molekulárně genetické změny u Richterovy transformace chronické lymfocytární leukemie
- Richterova transformace chronické lymfocytární leukemie v éře léčby inhibitory buněčných drah
- Transformace chronické lymfocytární leukemie do Hodgkinovy varianty Richterova syndromu
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: MUDr. Petr Výborný, CSc., FEBO
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



