-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Transrektální sonografie prostaty u mužů s vrozeným hypogonadismem léčeným dlouhodobou substituční terapií testosteronem
Autoři: Jiří Heráček 1,2; Karim El Balouly 1; Vladimír Sobotka 1,2; Marta Šnajderová 3; Božena Kalvachová 4; Michael Urban 1,2
Působiště autorů: Univerzita Karlova v raze, 3. lékařská fakulta, Urologická klinika 1; Fakultní nemocnice Královské Vinohrady, Urologická klinika 2; Univerzita Karlova v raze, 2. lékařská fakulta, Pediatrická klinika 3; Endokrinologický ústav, Praha 4
Vyšlo v časopise: Čas. Lék. čes. 2012; 151: 392-396
Kategorie: Původní práce
Souhrn
Východisko.
Cílem práce bylo vyhodnotit sonografické nálezy na prostatě u mužů léčených pro vrozený hypogonadismus dlouhodobou kontinuální substituční terapií testosteronem.Metody.
Od roku 2001 do roku 2011 jsme do souboru postupně zařadili 31 mužů s vrozeným hypogonadismem. Průměrná doba sledování byla 7,3 roku (2 měsíce až 10,8 roku). Pro kontinuální substituční léčbu testosteronem jsme používali Sustanon® 250 i.m. á 3 týdny nebo Nebido® i.m. á 3 měsíce. Každých 6 měsíců jsme pacientům provedli transrektální sonografii prostaty a semenných váčků biplanární rektální sondou.Výsledky.
U 22 (71,0 %) pacientů jsme v průběhu léčby zaznamenali při transrektální sonografii změny v prostatické tkáni. U 12 pacientů jsme diagnostikovali cysty prostaty, u devíti pacientů prostatolitiázu a u pěti pacientů změny v echogenitě prostatické tkáně. U dvou pacientů jsme nalezli současný výskyt cysty prostaty a prostatolitiázy, u dalších dvou pacientů pak současný výskyt hyperechogenních oblastí ve tkáni prostaty a prostatolitiázy. Výše popsané nálezy jsme diagnostikovali u pěti pacientů při léčbě trvající od 3 do 5 let, u ostatních 17 mužů s hormonální substituční léčbou delší než 5 let.Závěry.
Studie prezentuje dlouhodobé výsledky komplexní péče o pacienty s poruchou pohlavního vývoje, nástupu a průběhu puberty. Dlouhodobé sledování těchto pacientů v mezioborové spolupráci endokrinologa a androloga může významně přispět k objasnění vlivu substituční léčby testosteronem na vývoj prostaty.Klíčová slova:
hypogonadismus, hormonální substituční terapie, testosteron, transrektální sonografie, prostatická cysta, prostatolitiáza, karcinom prostaty, sledování.ÚVOD
S mužským hypogonadismem se v klinické praxi setkáváme poměrně často. Dopady na plodnost, sexuální funkce a pocit celkového zdraví jsou dobře známé (1–2).
Mužský hypogonadismus má pestrou etiologii. Testikulární poruchy různého původu jsou příčinou primárního (hypergonadotropního) hypogonadismu. Poruchy funkce hypotalamu a hypofýzy způsobují sekundární (hypogonadotropní) hypogonadismus. Mužský hypogonadismus může vzniknout i vlivem poruchy na úrovni androgenního receptoru, chybným metabolismem androgenů, závažným systémovým onemocněním, některými léky a drogami nebo fyziologickým stárnutím.
Klinické projevy hypogonadismu závisí na stadiu dosaženého pohlavního vývoje při vzniku poruchy. V dětském věku a v adolescenci se hyper - i hypogonadotropní hypogonadismus projevuje chybějícím, neúplným či spontánně nepostupujícím pohlavním vývojem.
U chlapců s primárním hypogonadismem se doporučuje zahájit postupnou indukci puberty nízkou dávkou androgenu po dosažení 13–14 let (12 let kostního věku), tedy ve věku obvyklém pro začátek puberty (3–4). Substituční léčba navozuje normální koncentraci testosteronu a jeho aktivních metabolitů a umožňuje napodobení spontánního pohlavního vývoje (5–8). Pacientům s hypogonadotropním hypogonadismem lze zpočátku přechodně podávat lidský choriový gonadotropin, který pomůže zvětšit objem varlat (5). Obvyklejší je však adolescentům s hypo - i s hypergonadotropním hypogonadismem podávat léčiva s testosteronem (perorální nebo častěji injekční formou) již od počátku indukce puberty. Záměrem je navodit a udržet vývoj sekundárních pohlavních znaků, optimalizovat pubertální růstový spurt, vývoj tělesných proporcí a dosáhnout normálního vývoje svalové a kostní hmoty. Léčba podporuje kromě vývoje penisu také vývoj prostaty a mužského vnitřního genitálu. Dalším cílem substituční hormonální léčby je snížit kardiovaskulární riziko (metabolické faktory), navodit specifické mužské psychosociální a psychosexuální dozrávání a umožnit normální socio/sexuální život v adolescenci a v dospělosti (8).
Vývoj lidské prostaty při substituční léčbě androgeny, která začíná v adolescenci, nebyl dosud podrobněji studován. Cílem naší práce bylo sledovat u mladých mužů s vrozeným hyper - i hypogonadotropním hypogonadismem vývoj prostaty v průběhu dlouhodobé substituční léčby testosteronem.
SOUBOR NEMOCNÝCH A POUŽITÉ METODY
Soubor nemocných
Do studie jsme od roku 2001 do roku 2011 postupně zařadili 31 adolescentů s vrozeným hypogonadismem. Tabulka 1 shrnuje základní charakteristiku souboru před zahájením léčby. Pacienti podstoupili komplexní andrologické a endokrinologické vyšetření, diagnózu hypogonadotropního hypogonadismu jsme potvrdili GnRH testem. Po ukončení indukce puberty postupně stoupající dávkou androgenu (Undestor p. o. nebo Sustanon inj. podle schématu doporučeného pro indukci puberty, podle 5) jsme pro dlouhodobou substituční léčbu používali estery testosteronu (250 mg intramuskulárně jednou za 3 týdny, Sustanon, Organon; od roku 2005 jsme u všech pacientů používali depotní testosteron v dávce 1000 mg intramuskulárně jednou za 3 měsíce, Nebido, Bayer Shering Pharma).
Tab. 1. Demografické a klinické charakteristiky souboru před začátkem substituční léčby testosteronem (průměr ± SD) 
SD – směrodatná odchylka, HST – hormonální substituční léčba, T – celkový testosteron, FSH – folikulostimulační hormonů LH – luteinizační hormon, PSA – prostatický specifický antigen Pacienti podepsali informovaný souhlas schválený Etickou komisí 3. lékařské fakulty Univerzity Karlovy v Praze.
Transrektální sonografie prostaty
U pacientů jsme každých 6 měsíců provedli transrektální sonografii prostaty a semenných váčků biplanární rektální sondou 7,5 MHz (BK Medical, Herlev, Dánsko) se dvěma krystaly v příčné a podélné rovině. Vyšetření jsme prováděli v poloze vleže na levém boku. Při sonografii jsme hodnotili objem prostaty, echogenitu tkáně, přítomnost patologických odchylek a vývoj jednotlivých zón prostaty.
Sérologická vyšetření
Vzorky periferní žilní krve jsme odebírali nalačno v den sonografického vyšetření prostaty mezi 7. a 8. hodinou ranní a bezprostředně po odběru centrifugovali 20 minut při 2000 otáčkách za minutu. Séra jsme do definitivního zpracování uchovávali při teplotě –70° C. Sérovou koncentraci celkového testosteronu jsme určili pomocí radioimunoanalytické soupravy, sérové koncentrace folikulostimulačního hormonu a luteinizačního hormonu jsme vyhodnotili s využitím radioimunometrických souprav, ve všech případech od dodavatele Immunotech (česká divize Beckman Coulter, Marseille, Francie). Sérovou koncentraci celkového prostatického specifického antigenu (PSA) jsme stanovili pomocí radioimunoanalytického kitu (Abbott, Chicago, USA).
Statistický rozbor
Demografická a klinická data pacientů jsme zpracovali metodami popisné statistiky. Pro statistickou analýzu jsme použili neparametrický Mannův-Whitneyův test, který jsme vyhodnotili na 5% hladině významnosti s využitím softwaru Statistica 8.0 (Statsoft, Tulse, USA). Při zpracování článku jsme se řídili současnými mezinárodními doporučeními pro publikaci výsledků observačních studií (9).
VÝSLEDKY
Průměrná doba sledování pacientů souboru byla 7,3 roku (2 měsíce až 10,8 roku).
Průměrný věk v celém sledovaném období byl ve skupině pacientů s primárním, resp. sekundárním hypogonadismem 20,1 ± 6,2, resp. 21,5 ± 7,0 roku.
Průměrná sérová koncentrace celkového testosteronu v celém sledovaném období byla u pacientů s primárním, resp. sekundárním hypogonadismem 14,0 ± 5,1, resp. 15,9 ± 6,6 nmol/l, sérová koncentrace PSA 0,5 ± 0,2, resp. 0,5 ± 0,2 ng/ml a objem prostaty 14,0 ± 2,7, resp. 11,9 ± 5,3 ml. Průměrné hodnoty celkového testosteronu, PSA a objemu prostaty v průběhu léčby uvádějí grafy 1–3. Nezaznamenali jsme statisticky významné rozdíly mezi těmito parametry v obou skupinách v průběhu celého sledovaného období.
Graf 1. Průměrná sérová koncentrace celkového testosteronu v průběhu substituční léčby 
Graf 2. Průměrná sérová koncentrace PSA v průběhu substituční léčby 
Graf 3. Průměrný objem prostaty v průběhu substituční léčby 
Před začátkem substituční léčby testosteronem měli všichni pacienti při transrektální sonografii prostaty a semenných váčků normální nález (obr. 1) a negativní nález při digitálním rektálním vyšetření prostaty.
Obr. 1a,b. Transrektální sonografie prostaty s normálním nálezem u 18letého muže s vrozeným hypogonadismem před zahájením substituční léčby testosteronem, příčná (a) a podélná (b) rovina 
Sonografické nálezy shrnuje tabulka 2. U devíti (29,0 %) pacientů jsme během léčby při sonografických vyšetřeních nezaznamenali změny v prostatické tkáni. U 22 (71,0 %) pacientů jsme v průběhu léčby zaznamenali při transrektální sonografii změny v prostatické tkáni. U 12 pacientů jsme diagnostikovali cysty prostaty (obr. 2), u devíti pacientů prostatolitiázu (obr. 3) a u pěti pacientů změny v echogenitě (hyperechogenní oblasti) prostatické tkáně (obr. 4). U dvou pacientů jsme nalezli současný výskyt cysty prostaty a prostatolitiázy, u dalších dvou pacientů pak současný výskyt hyperechogenních oblastí ve tkáni prostaty a prostatolitiázy. Všichni pacienti měli v průběhu léčby negativní nález při digitálním rektálním vyšetření.
Tab. 2. Sonografické nálezy při transrektálním vyšetření prostaty v průběhu substituční léčby testosteronem 
Obr. 1. Cysta o velikosti 10 × 8 mm v levém laloku prostaty blízko střední čáry u 25letého muže (7. rok substituční léčby), příčná rovina 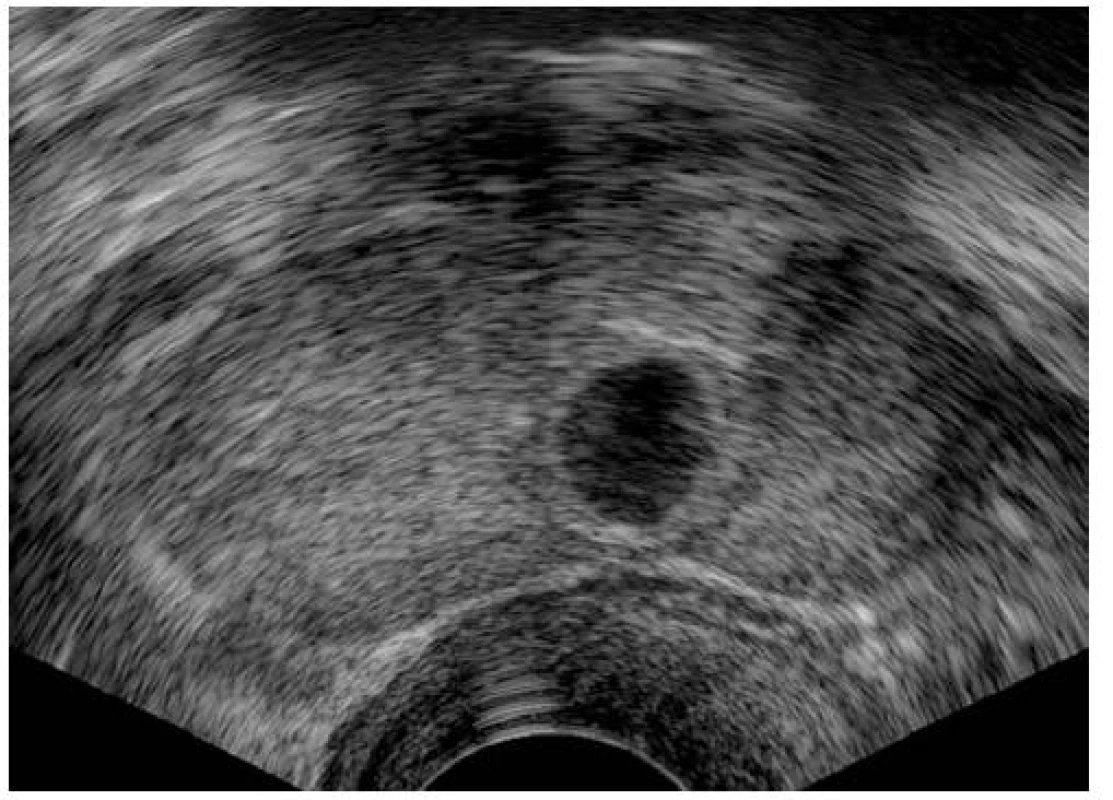
Obr. 2. Prostatolitiáza o velikosti 5 × 3 mm v levém laloku prostaty u 31letého muže (5. rok substituční léčby), příčná rovina 
Obr. 4a. Hyperechogenní oblast o velikosti 6 × 5 mm v pravém laloku prostaty u 22letého muže (5. rok substituční léčby), příčná rovina 
Obr. 4b. Hyperechogenní oblast o velikosti 9 × 7 mm v pravém laloku prostaty u 22letého muže (9. rok substituční léčby), podélná rovina 
V prvních 3 letech léčby jsme při transrektální sonografii nezaznamenali u pacientů patologické odchylky. Výše popsané nálezy jsme diagnostikovali u pěti pacientů při léčbě trvající od 3 do 5 let, u ostatních 17 mužů s hormonální substituční léčbou delší než 5 let.
DISKUZE
V odborném tisku jsme nenalezli publikaci, která by se zabývala tématem shodným se zaměřením naší práce.
Prostatické cysty, které se vyskytují u mladých mužů velmi vzácně, dělíme na vrozené a získané (10–11). Vrozené cysty se tvoří v prostatickém kanálku rozšířením verumontana a vznikají z Müllerova vývodu, který se nachází ve střední ose mezi prostatou a konečníkem anebo z Wolffova vývodu, který je uložen laterálně mezi prostatou a konečníkem (12). Cysty ve střední části prostaty jsou původem z Müllerova vývodu nebo utrikulární cysty. Cysty z Müllerova vývodu jsou mezodermálního původu, nejsou spojeny s prostatickou částí močové trubice nebo se semennými váčky a nikdy neobsahují spermie. Utrikulární cysty mají endodermální původ. V jejich boční stěně můžeme nacházet ejakulatorní vývody, které je spojují s prostatickou částí močové trubice, a proto mohou obsahovat spermie (13); jedná se o nejběžnější typ vrozených cyst prostaty, které často souvisí s pseudohermafroditismem, hypospadií (14–17), kryptorchismem nebo unilaterální renální agenezí (17). Klinické příznaky prostatických cyst se projevují nejčastěji opakovanými infekcemi dolních močových cest, syndromem chronických pánevních bolestí, neplodností, bolestmi při ejakulaci a hematospermií (10). V naší studii byli pacienti bez klinických příznaků, cysty jsme diagnostikovali při pravidelných sonografických vyšetřeních prostaty. Všichni pacienti měli cysty ve střední části prostaty, což ukazuje na původ z Müllerova vývodu či na utrikulární cysty. Skutečný původ cyst nelze na základě sonografických snímků určit, pouze v případě, že bychom provedli punkci (pokud by byly obsahem cysty i spermie, jednalo by se o utrikulární cystu).
Prostatolitiáza se u mladých mužů vyskytuje velmi řídce. Jedná se o kalcifikovaná corpora amylacea (18), jejichž výskyt je spojen s chronickými záněty, lézemi epiteliální tkáně a obstrukcí glandulární tkáně (19). Prostatolitiáza je u většiny pacientů asymptomatická, avšak objemné prostatolity se mohou spolupodílet na zánětech prostaty, syndromu chronických pánevních bolestí nebo zástavě močení (20–21). Chronickým drážděním prostatické tkáně spolu s lokální infekcí mohou pravděpodobně spoluiniciovat vznik zhoubného nádorového bujení. V naší studii byli pacienti bez klinických příznaků, prostatolitiázu jsme diagnostikovali při pravidelných sonografických vyšetřeních prostaty. Pacienti anamnesticky neprodělali infekci močových cest.
Změny v echogenitě tkáně prostaty vždy budí podezření na karcinom. Normální vývoj prostaty, stejně jako uchování její struktury a funkce, závisí na přítomnosti androgenů (22). Endokrinní závislost prostaty prokázal na experimentálně kastrovaných zvířatech Hunter již v roce 1786 (23). Ve čtyřicátých letech 20. století ji potvrdili Huggins et al. (24). Androgeny prostřednictvím androgenního receptoru regulují expresi mnoha genů, které v prostatické tkáni ovlivňují zejména diferenciaci a proliferaci buněk, regulaci buněčného cyklu a buněčnou smrt – apoptózu (25). Údaje o účincích dlouhodobé hormonální substituční léčby u mladých mužů nejsou k dispozici. Muže, kterého léčíme testosteronovou terapií, musíme sledovat pomocí standardního monitorovacího plánu. Je důležité, zda je léčba účinná a vede ke zlepšení příznaků testosteronové nedostatečnosti, ale neméně důležité je včas zjistit vedlejší účinky léčby (26). Nejsložitějším problémem při sledování hypogonadálních mužů s hormonální substituční léčbou jsou kritéria pro provádění biopsie prostaty. Změny v echogenitě tkáně prostat u našich mladých pacientů jsou alarmující. U těchto pacientů jsme snížili od poloviny roku 2011 substituční dávky testosteronu na polovinu a podrobujeme je pečlivé monitoraci. V případě progrese nálezů provedeme biopsii ložiska pod transrektální sonografickou kontrolou. Je třeba se vážně zabývat myšlenkou, zda dávky testosteronu běžně užívané pro substituční léčbu nejsou suprafyziologické pro pacienty s vrozeným hypogonadismem.
ZÁVĚR
Studie prezentuje dlouhodobé výsledky komplexní péče o mladé muže s poruchou nástupu a průběhu puberty a spontánního pohlavního vývoje v adolescenci. V průběhu dlouhodobé substituční léčby injekčními preparáty testosteronu jsme pomocí transrektálního sonografického vyšetření u 71 % pacientů nalezli změny v prostatické tkáni. Diagnostikovali jsme nově vzniklé cysty, kalcifikace a změny v echogenitě tkáně, které u některých pacientů měli progredující tendenci. Pro své nositele mají tyto nálezy značný klinický význam. Mezioborová spolupráce endokrinologa a androloga může v rámci dlouhodobého sledování významně přispět k objasnění vlivu substituční léčby testosteronem na vývoj prostaty, rozšířit poznatky o vývoji lidské prostaty a bezpečnosti dlouhodobé substituce androgeny u mužů s hypogonadismem, u nichž byla léčba zahájena již v adolescenci. Výsledky lze považovat za prioritní. Další sledování a rozšíření počtu pacientů považujeme za nezbytné.
Zkratky
- FSH – folikulostimulační hormon
- HST – hormonální substituční terapie
- LH – luteinizační hormon
- PSA – prostatický specifický antigen
- SD – směrodatná odchylka
- T – testosteron
Práce vznikla za podpory grantu č. NS9983 IGA MZ ČR. Projekt byl schválen Etickou komisí 3. lékařské fakulty Univerzity Karlovy v Praze.
ADRESA PRO KORESPONDENCI:
doc. MUDr. Jiří Heráček, Ph.D., MBA
Urologická klinika 3. LF UK a FNKV
Ruská 87, 100 00 Praha 10
fax: + 420 267 162 999, e-mail: jiri.heracek@lf3.cuni.cz
Zdroje
1. Griffin JE, Wilson JD. Disorders of the testes and male reproductive tract. In: Wilson JD, Foster DW, eds. Williamęs Textbook of Endocrinology, 8th ed. Philadelphia: Saunders 1992; 799–852.
2. Vermeulen A, Kaufman J. Aging of the hypothalamopituitary testicular axis in men. Horm Res 1995; 43 : 25–28.
3. Ambler G. Androgen therapy for delayed male puberty. Curr Opin Endocrinol Diabetes Obes 2009; 16 : 232–239.
4. Walvoord E. Sex steroid replacement for induction of puberty in multiple pituitary hormone deficiency. Pediatr Endocrinol Rev 2009; 6 : 298–305.
5. Pozo J, Argente J. Ascertainment and treatment of delayed puberty. Horm Res 2003; 60 : 35–48.
6. Lee PA. Puberty and its disorders. In: Lifshitz F, Pediatric endocrinology, 4th ed. New York: Marcel Dekker 2003; 231.
7. Rogol A. New facets of androgen replacement therapy during childhood and adolescence. Expert Opin Pharmacother 2005; 6 : 1319–1336.
8. Bertelloni S, Baroncelli G, Garofalo P, Cianfarani S. Androgen therapy in hypogonadal adolescent males. Horm Res Paediatr 2010; 74 : 292–296.
9. von Elm E, Altman D, Egger M, Pocock S, Gotzsche P, Vandenbroucke J, et al. The strengthening the reporting of observational studies in epidemiology (STROBE) statement: guidelines for reporting observational studies. Gaceta Sanitaria 2008; 22 : 144–150.
10. Dik P, Lock T, Schrier B, Zeijlemaker B, Boon T. Transurethral marsupialization of a medial prostatic cyst in patients with prostatitis-like symptoms. J Urol 1996; 155 : 1301–1304.
11. Ishikawa M, Okabe H, Oya T, Hirano M, Tanaka M, Ono M, et al. Midline prostatic cysts in healthy men: incidence and transabdominal sonographic findings. Am J Roentgenol 2003; 181 : 1669–1672.
12. Sivaraman L, Sivasubramani S. Prostatic cysts. Ann R Coll Surg Eng 1978; 60 : 476–478.
13. Van Poppel H, Vereecken R, De Geeter P, Verduyn H. Hemospermia owing to utricular cyst: embryological summary and surgical review. J Urol 1983; 129 : 608–609.
14. Shima H, Ikoma F, Terakawa T. Developmental anomalies associated with hypospadias. J Urol 1979; 122 : 619–621.
15. Devine C, Horton C, Scaff J. Epispadias. Urol Clin North Am 1980; 7 : 465–476.
16. Ritchye M, Benson R, Kramer S. Managment of Mullerian duct remnants in the male patient. J Urology 1988; 140 : 795–799.
17. Gevenois P, Vansinoy M, Sintznoff S. Cysts of the prostate and seminal vesicles – 11 cases. Am J Roentgenol 1990; 155 : 1021–1024.
18. Hwang EC, Choi HS, Im CM, Jung SI, Kim SO, Kang TW, et al. Prostate calculi in cancer and BPH in a cohort of Korean men: Presence of calculi did not correlate with cancer risk. Asian J Androl 2010; 12 : 215–220.
19. De Marzo AM, Nakai Y, Nelson WG. Inflammation, atrophy, and prostate carcinogenesis. Urol Oncol 2007; 25 : 398–400.
20. Bedir S, Kilciler M, Akay O, Erdemir F, Avci A, Ozgok Y. Endoscopic treatment of multiple prostatic calculi causing urinary retention. Int J Urol 2005; 12 : 693–695.
21. Geramoutsos I, Gyftopoulos K, Perimenis P, Thanou V, Liagka D, Siamblis D, et al. Clinical correlation of prostatic lithiasis with chronic pelvic pain syndromes in young adults. Eur Urol 2004; 45 : 333–337.
22. Wilding G. Endocrine control of prostate cancer. Cancer Surv 1995; 23 : 43–62.
23. Hunter J. Observations on the structure situated between the rectum and bladder, called vesiculae seminales. Coll. Works of J. Hunter, Vol. 4. London: J.F. Palmer 1786; 31.
24. Huggins C. Effect of orchiectomy and irradiation on cancer of the prostate. Ann Surg 1942 : 6: 1192–1200.
25. Stárka L, Heráček J, Kuncová J, Sachová J, Urban M, Bendlová B. Receptor pro androgeny a karcinom prostaty. DMEV 2005; 7 : 125–131.
26. Bhasin S, Cunningham GR, Hayes FJ, Matsumoto AM, Snyder PJ, Swerdloff RS, et al. Testosterone therapy in adult men with androgen deficiency syndromes: an endocrine society clinical practice guideline. J Clin Endocrinol Metab 2010; 95 : 2536–2559.
Štítky
Adiktologie Alergologie a imunologie Anesteziologie a resuscitace Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská dermatologie Dětská gastroenterologie Dětská gynekologie Dětská chirurgie Dětská kardiologie Dětská nefrologie Dětská neurologie Dětská onkologie Dětská otorinolaryngologie Dětská pneumologie Dětská psychiatrie Dětská radiologie Dětská revmatologie Dětská urologie Diabetologie Endokrinologie Farmacie Farmakologie Fyzioterapie Gastroenterologie a hepatologie Genetika Geriatrie a gerontologie Gynekologie a porodnictví Hematologie a transfuzní lékařství Hygiena a epidemiologie Hyperbarická medicína Chirurgie cévní Chirurgie hrudní Chirurgie plastická Chirurgie všeobecná Infekční lékařství Intenzivní medicína Kardiochirurgie Kardiologie Logopedie Mikrobiologie Nefrologie Neonatologie Neurochirurgie Neurologie Nukleární medicína Nutriční terapeut Obezitologie Oftalmologie Onkologie Ortodoncie Ortopedie Otorinolaryngologie Patologie Pediatrie Pneumologie a ftizeologie Popáleninová medicína Posudkové lékařství Praktické lékařství pro děti a dorost Protetika Psychologie Radiodiagnostika Radioterapie Rehabilitační a fyzikální medicína Reprodukční medicína Revmatologie Sestra Sexuologie Soudní lékařství Stomatologie Tělovýchovné lékařství Toxikologie Traumatologie Urgentní medicína Urologie Laboratoř Domácí péče Foniatrie Algeziologie Zdravotnictví Dentální hygienistka Student medicíny
Článek Ateroskleróza 2012Článek Nikolaas Tinbergen
Článek vyšel v časopiseČasopis lékařů českých
Nejčtenější tento týden
- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
-
Všechny články tohoto čísla
- Statistika v klinické a experimentální medicíně
- Marek Vácha, Radana Königová, Miloš Mauer: Základy moderní lékařské etiky
- Zmeny váhy u pacientov v metadónovej udržiavacej liečbe počas štyroch rokov
- Psoriáza a analoga D vitaminu
- Transrektální sonografie prostaty u mužů s vrozeným hypogonadismem léčeným dlouhodobou substituční terapií testosteronem
- Hodnocení malnutrice hospitalizovaných dětí pomocí škály The Screening Tool for the Assessment of Malnutrition in Paediatrics
-
BIOLAB 2012 – celostátní sjezd biochemických laborantů
Písek, 13. až 15. května 2012 -
IX. seminář mladých revmatologů
Špindlerův Mlýn, 17. až 19. května 2012 -
10. mezinárodní kongres České společnosti refrakční a kataraktové chirurgie
Hradec Králové, 25. a 26. května 2012 -
XXX. mezikrajské dny klinické biochemie Královéhradeckého, Pardubického a jihočeského kraje
Prachatice, 28. až 30. května 2012 -
XIX. pražské chirurgické dny
Praha, 1. června 2012 -
12. setkání mladých oftalmologů
Tábor, 8.–10. června 2012 -
IV. sjezd v rámci Human Variome Project (HVP) pod záštitou UNESCO
Paříž, 11.–15. června 2012 - Ateroskleróza 2012
- Prof. MUDr. Pavel Barták, CSc., slaví pětaosmdesátiny
- ČGGS a Česká lékařská společnost JEP
- Nikolaas Tinbergen
- Časopis lékařů českých
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Hodnocení malnutrice hospitalizovaných dětí pomocí škály The Screening Tool for the Assessment of Malnutrition in Paediatrics
- Statistika v klinické a experimentální medicíně
- Transrektální sonografie prostaty u mužů s vrozeným hypogonadismem léčeným dlouhodobou substituční terapií testosteronem
- Marek Vácha, Radana Königová, Miloš Mauer: Základy moderní lékařské etiky
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



