-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Hemodynamické změny v pronační poloze – neinvazivní fyziologická studie
Hemodynamic changes in prone position – a non‑invasive physiological study
Background and Goal of the study: The aim of this physiological study was to observe changes in cardiac output and other hemodynamic parameters after proning and to compare hemodynamic profile of prone position with and without chest and pelvic support.
Type of study: Prospective, observational study.
Setting: Clinical laboratory of a university hospital.
Material and Methods: Twelve healthy volunteers older than 18 years were included in the study. Non-invasive hemody namic measurement was initiated using ClearSight/EV 1000 system in supine position (S position). Cardiac index (CI), stroke volume index (SVI), stroke volume variation (SVV), systemic vascular resistance index (SVRI) and mean arterial pressure (MAP) were recorded. Following parameters were measured using ultrasound at predefined sites: expiratory area of v. cephalica (sVCe), v. saphena (sVSe), v. jugularis interna (sVJe), expiratory and inspiratory area (sVCIe a sVCIi), and maximum and minimum diameter (dVCImax a dVCImin) of v. cava inferior and index of colapsibility (VCI CI) were calculated. Corrected carotid flow time (ccFT) was measured using a Doppler ultrasound. All measurements were repeated in unsupported (P1 position) and supported (P2 position) prone positions with supported chest and pelvic regions.
Results and Discussion: There were no differences in CI, SVI, SVV and ccFT values between positions. Significantly different values of MAP and VCI CI were observed between positions. Higher SVRI in P1 position in comparison with S position, higher sVJe in prone positions and lower dVCImin in P2 position in comparison with P1 position were recorded.
Conclusion: No differences in cardiac output and preload were detected after proning in unsedated healthy volunteers. Prone position was associated with changes of systemic vascular resistance, blood stagnation in jugular catchment area and, in unsupported prone position, increased collapsibility of inferior vena cava.
Keywords:
prone position – Cardiac output – preload
Autoři: L. Kukrálová; V. Dostálová; P. Dostál
Působiště autorů: Fakultní nemocnice Hradec Králové ; Klinika anesteziologie, resuscitace a intenzivní medicíny, Univerzita Karlova, Lékařská fakulta v Hradci Králové
Vyšlo v časopise: Anest. intenziv. Med., 32, 2021, č. 2, s. 82-86
Kategorie: Původní práce
Souhrn
Cíl studie: Cílem této fyziologické studie bylo sledovat změny srdečního výdeje a další hemodynamické parametry v pro nační poloze a srovnat vliv podložení hrudníku a pánve na hemodynamické parametry.
Typ studie: Prospektivní, observační studie.
Typ pracoviště: Experimentální laboratoř fakultní nemocnice.
Materiál a metoda: Do studie bylo zařazeno 12 zdravých dobrovolníků starších 18 let. V supinní poloze (poloha S) bylo zahájeno neinvazivní hemodynamické monitorování systémem ClearSight/EV 1000. Po stabilizaci byly zaznamenány: srdeční index (CI), index tepového objemu (SVI), variabilita tepového objemu (SVV), index systémové vaskulární rezis tance (SVRI). Dále byly v definovaných místech sonograficky sledovány: exspirační plocha v. cephalica (sVCe), v. saphena (sVSe), v. jugularis interna (sVJe), exspirační a inspirační plocha (sVCIe a sVCIi) a maximální a minimální předozadní průměr (dVCImax a dVCImin) v. cava inferior a kalkulován index kolapsibility (VCI CI). Sonograficky byl stanoven corrected carotid flow time (ccFT). Měření byla opakována v nepodložené (poloha P1) a podložené pronační poloze s podporou proximální části hrudníku a pánve (poloha P2).
Výsledky: Mezi jednotlivými polohami nebyly zjištěny rozdíly v hodnotách CI, SVI, SVV a ccFT. Mezi polohami byly zjištěny signifikantní rozdíly v hodnotách MAP a VCI CI. Ve srovnání s polohou S byla v poloze P1 pozorována vyšší hodnota SVRI a vyšší hodnota sVJe. Nižší hodnota dVCImin byla zaznamenána v poloze P2 ve srovnání s polohou P1.
Závěr: U zdravých nesedovaných dobrovolníků nebyl v pronační poloze pozorován pokles srdečního výdeje ani preloadu, ale byly zjištěny změny systémové vaskulární rezistance a stagnace krve v jugulárním řečišti. V nepodložené pronační poloze byla zjištěna zvýšená kolapsibilita dolní duté žíly.
Klíčová slova:
pronační poloha – srdeční výdej – preload
Úvod
Pronační poloha, která je obvykle používána v průběhu mnoha spondylochirurgických operačních výkonů, je spojena s rizikem vzniku peroperační oběhové nestability [1, 2]. Provedené studie prokázaly, že u pacientů v celkové anestezii, monitorovaných pomocí transezofageální echokardiografie (TEE) nebo pomocí plicnicového katétru [1, 3] dochází k poklesu srdečního výdeje o 10–20 %. U zdravých pacientů je snížení srdečního výdeje provázeno poklesem indikátorů preloadu a zvýšením ejekční frakce levé srdeční komory, u nemocných s preexistujícím srdečním onemocněním naopak dochází k jejímu snížení [1, 2, 4]. Neschopnost kompenzovat pokles preloadu a případné změny afterloadu zvýšením srdeční kontraktility je považována za důvod závažnější oběhové nestability u nemocných s preexistující systolickou dysfunkcí levé srdeční komory [2, 5]. U pacientů s kardiálními komorbiditami byla také častěji popisována dyssynchronie srdečního stahu po uložení do pronační polohy [5].
Význam změn preloadu a přesný mechanismus jeho ovlivnění v pronační poloze je předmětem přetrvávající kontroverze [1, 2, 6]. V závislosti na použitém způsobu provedení pronační polohy může docházet ke zvýšení nitrobřišního a nitrohrudního tlaku, což potenciálně ovlivňuje velikost žilního návratu a interakce srdce‑plíce v průběhu umělé plicní ventilace [1, 6, 7]. Může také docházet k redukci žilního návratu přímou kompresí dolní duté žíly [1]. Další z možných příčin snížení preloadu je venózní stagnace, tzv. pooling krve v končetinách svěšených pod úroveň srdce [1, 2]. Přetlaková ventilace a farmaka použitá při úvodu a vedení celkové anestezie mohou také způsobit hypotenzi snížením žilního návratu nebo ovlivněním srdeční kontraktility [8].
Hemodynamické změny je možné neinvazivně monitorovat pomocí techniky tzv. analýzy kontury pulzové křivky systémem ClearSight/EV 1000 Clinical Platform (Edwards Lifesciencies, Irvine, Kalifornie, USA). Systém využívá speciální prstovou manžetu a mimo kontinuálního neinvazivního měření středního arteriálního tlaku umožňuje průběžně stanovit srdeční výdej a další odvozené makrohemodynamické parametry [9]. Systém byl extenzivně validován v perioperačním období a přestože jeho výsledky nejsou zcela zaměnitelné s invazivně získanými metodami [10, 11], je jeho schopnost trendové analýzy srovnatelná s invazivními hemodynamickými monitorovacími systémy založenými na principu analýzy kontury pulzové křivky [12].
Hodnocení venózního poolingu a posouzení změn srdečního preloadu je možné nepřímo použitím ultrazvukových metod [13]. Většina provedených studií použila k posouzení změn preloadu tlakové hemodynamické parametry nebo sledování změn end ‑ distolického objemu levé komory [1, 2, 14]. Relativně nedávno byl do klinické praxe zaveden nový ukazatel objemového stavu, tzv. corrected carotid flow time (ccFT) [15]. Jak absolutní hodnoty ccFT [15, 16, 17], tak velikost změny ccFT po pasivní elevaci dolních končetin [17, 18] odrážejí změny objemového stavu a jsou považovány za další prediktor tzv. fluid responsiveness [15, 17, 19].
Vzhledem k potenciálnímu vlivu farmak, přetlakové ventilace a případných preexistujících patologických stavů je pro klinickou praxi důležitá znalost základních fyziologických vzorců hemodynamické odpovědi na pronační polohu. Primárním cílem této neinvazivní fyziologické studie bylo proto ozřejmit, zda u zdravých nesedovaných dobrovolníků dochází ke změnám srdečního výdeje a odvozených hemodynamických parametrů. Sekundárním cílem bylo identifikovat mechanismy případných změn preloadu a zhodnotit vliv typu pronační polohy na hemodynamické změny.
Soubor a metoda
Etika
Protokol této prospektivní observační studie provedené na Klinice anesteziologie, resuscitace a intenzivní medicíny Univerzity Karlovy, Lékařské fakulty v Hradci Králové a Fakultní nemocnice Hradec Králové, byl schválen Etickou komisí Fakultní nemocnice Hradec Králové (předseda MUDr. Jiří Vortel) pod jednacím číslem 202006 S15 dne 4. 6. 2020. Studie byla registrována na ClinicalTrials.gov pod identifikátorem NCT04491331.
Protokol studie
Do studie byli po získání informovaného souhlasu zařazováni dobrovolníci starší 18 let bez známých komorbidit, sběr dat byl proveden dle jednotného protokolu.
V první fázi studie byly subjekty uloženy do supinní polohy (poloha S) a bylo zahájeno neinvazivní hemodynamické monitorování systémem ClearSight/EV 1000 Clinical Platform (Edwards Lifesciencies, Irvine, Kalifornie, USA) naloženým na levou horní končetinu. Systém umožňuje kontinuální stanovení středního arteriálního tlaku (MAP) a dalších makrohemodynamických parametrů – tepové frekvence (TF), srdečního indexu (CI), indexu tepového objemu (SVI), variabilitu tepového objemu (SVV) a indexu systémové vaskulární rezistance (SVRI). Při všech měřeních byly po pětiminutové stabilizaci odečteny makrohemodynamické parametry třikrát v odstupu pěti minut a byl stanoven jejich průměr.
Pomocí přístroje Philips CX 50 (Philips, Eidhoven, Holandsko) se sondami L12-1 a C5-1 bylo provedeno standardizované ultrazvukové vyšetření, všechny sledované rozměry byly odečítány za záznamu pořízeného v B‑modu. Exspirační plocha cévních řezů byla určena vizuálně jako největší plocha na kolmém řezu cévou v průběhu dechového cyklu, při vyšetření periferních žil byl vyvíjen minimální tlak na kožní kryt tak, aby nedošlo k deformaci tvarů cévy, místo vyšetření bylo označeno pro další opakovaná vyšetření.
Byly sledovány následující parametry: exspirační plocha v. cephalica na pravé horní končetině (sVCe); exspirační plocha v. saphena na pravé dolní končetině (sVSe); exspirační plocha v. jugularis interna vpravo (sVJe) – místo vyšetření bylo lokalizováno cca 2 cm proximálně od horního okraje klíční kosti; exspirační a inspirační plocha (sVCIe a sVCIi) a maximální a minimální předozadní průměr (dVCImax a dVCImin) v. cava inferior. Z hodnot předozadního průměru byl následně kalkulován index kolapsibility (VCI CI) dle vzorce VCI CI = (dVCImax – dVCImin)/ (dVCImax) vyjádřený v procentech. Průměr a plocha řezu v. cava inferior byly měřeny transhepatálně z horizontálního řezu sondou umístěnou zhruba ve střední axilární čáře, měření bylo prováděno bezprostředně kaudálně od vstupu hepatálních žil do v. cava inferior.
Pomocí lineární sondy s kurzorem směřujícím kraniálně, umístěné iniciálně zhruba v úrovni prstenčité chrupavky podél mediálního okraje m. sternocledomastoideus, byl na pravostranné a. carotis communis identifikován karotický bulbus a kurzor vzorkovacího objemu byl následně umístěn do středu karotického lumen cca 1 cm distálně od karotického bulbu. Po úhlové korekci (přípustný úhel do 60 stupňů) byl proveden záznam pulzního dopplerovského signálu. Ze záznamu trvajícího minimálně dva dechové cykly byl následně vybrán cyklus s maximální systolickou průtokovou rychlostí a v rámci tohoto cyklu byly odečteny systolický průtokový čas (systolic flow time), jako rozdíl času od zahájení toku do času maximální amplitudy dikrotického zářezu, a délka srdečního cyklu (tzv. cycle time) [15, 17]. Tzv. corrected carotid flow time byl následně kalkulován dle Bazetovy formule jako poměr systolic flow time a cycle flow time a dle Woodeyho formule jako změřený systolic flow time – 1,29 × (TF – 60) a vyjádřen v milisekundách [19, 20].
Po provedení ultrazvukového vyšetření byl subjekt polohován (aktivní pohyb subjektu) do pronační polohy na horizontální pevné podložce (poloha P1) simulující polohu na operačním stole bez dodatečného podložení, byly zaznamenány makrohemodynamické parametry a provedena výše popsaná ultrazvuková měření.
Ve třetí fázi studie byl každý subjekt polohován na měkkou oporu proximální části hrudního koše a pánve, eliminující tlak podložky na dutinu břišní (poloha P2). V této poloze, ve které byla provedena všechna měření, byly horní i dolní končetiny umístěny pod úrovní srdce. Všechna měření byla provedena pouze jedním vyšetřujícím, makrohemodynamická měření provedla LK, ultrazvuková měření PD.
Statistika
Tzv. power analýza s chybou α 0,05 a chybou β 0,20 byla provedena pro Repeated Measures ANOVA test pomocí software G*Power verze 3.1.9.2 (Kiel University, Kiel, Německo) s předpokladem tří měření v rámci jedné skupiny, velikostí efektu v rámci subjektů 0,45, korelací mezi opakovanými měřením 0,5 a hodnotou epsilon = 0,9. Tato kalkulace ukázala minimální počet 11 subjektů, počet zařazených byl následně zvýšen na 12 subjektů vzhledem k možné nepřesnosti predikce.
Výsledky jsou vyjádřeny jako průměr ± směrodatná odchylka nebo jako medián (mezikvartilové rozpětí) na základě výsledků testu normality distribuce pomocí jednovýběrového Kolmogorov‑Smirnovova testu. Rozdíly mezi jednotlivými polohami byly testovány pomocí jednofaktorového Repeated Measures ANOVA s Huynh‑Feldtovou korekcí nebo Greenhouse‑Geisserovou korekcí dle dosažené hodnoty epsilon v testu sféricity. Pro párové srovnání mezi polohami byla použita Bonferoniho metoda, hodnota P byla korigována na mnohočetná pozorování. Pro srovnání metod výpočtu ccFT v jednotlivých polohách byl použit nepárový t‑test, P < 0,05 bylo považováno za statisticky významné. Statistické analýzy byly provedeny na software MedCalc 7.6.0 (Ostende, Belgie).
Výsledky
Do studie bylo zařazeno 12 dobrovolníků, 6 mužů a 6 žen. Průměrný věk byl 29 ± 3 roky, hodnota body mass indexu sledovaného souboru byla 23,6 ± 3,4 kg/m2 a povrchu těla 1,87 ± 0,25 m2.
Vývoj makrohemodynamických ukazatelů je shrnut v tabulce 1.
Tab. 1. Vývoj makrohemodynamických parametrů v jednotlivých polohách 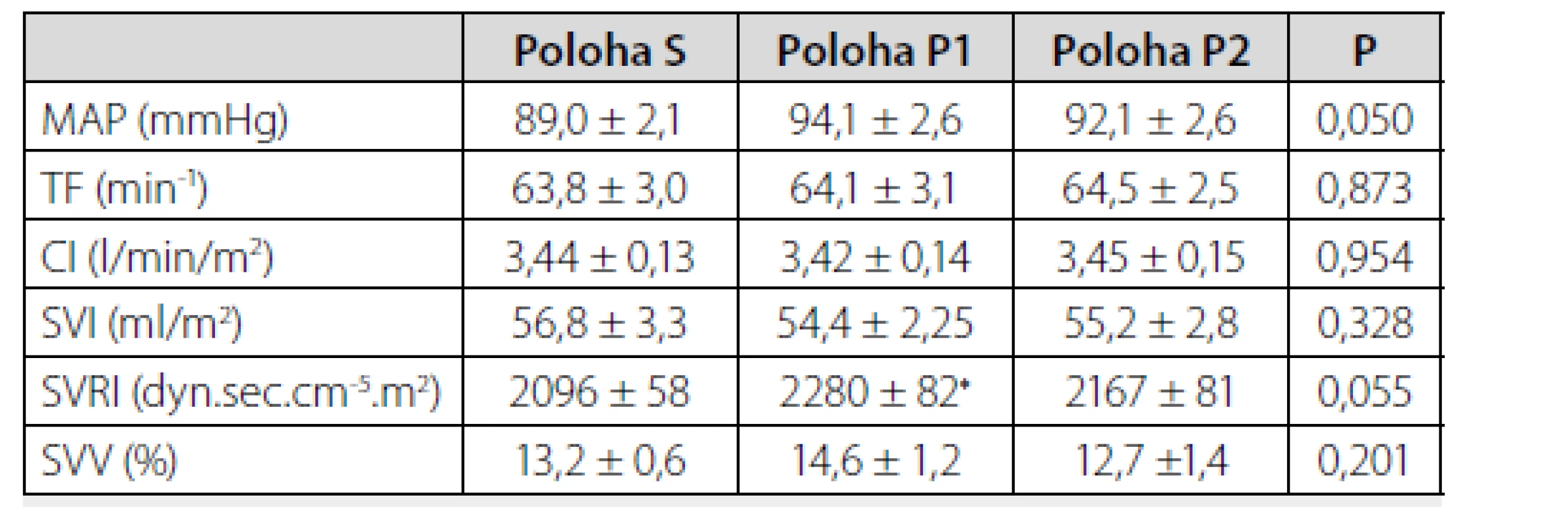
* P < 0,05 vs Poloha S
S – supinní poloha S, P1 – pronační poloha P1, P2 – pronační poloha P2, MAP – střední arteriální tlak, TF – tepová frekvence, CI – srdeční index, SVI – index tepového objemu, SVRI – index systémové vaskulární rezistence, SVV – variabilita teplového objemu.Byly zjištěny signifikantní rozdíly v hodnotě MAP mezi jednotlivými polohami, F(1,367/13,668) = 4,21, P = 0,050, η2 = 0,299. Korigované P při vzájemném srovnání rozdílů v hodnotách MAP mezi jednotlivými polohami nedosáhlo statistické významnosti.
V hodnotě SVRI byl obdobně pozorován trend k rozdílným hodnotám mezi jednotlivými polohami, tento rozdíl ale nebyl statisticky signifikantní, F (2/20) = 3,35, P = 0,055, η2 = 0,251. Přímé vzájemné srovnání mezi jednotlivými polohami ukázalo signifikantní rozdíl mezi polohou S a polohou P1 (P = 0,0392). Mezi jednotlivými polohami nebyly zjištěny rozdíly v hodnotách CI, SVI nebo SVV.
V tabulce 2 je uveden vývoj hodnot ccFT. Rozdíly mezi jednotlivými polohami, ani mezi použitými metodami výpočtu nedosáhly statistické významnosti.
Tab. 2. Korigovaný karotický průtokový čas (ccFT) v jednotlivých polohách 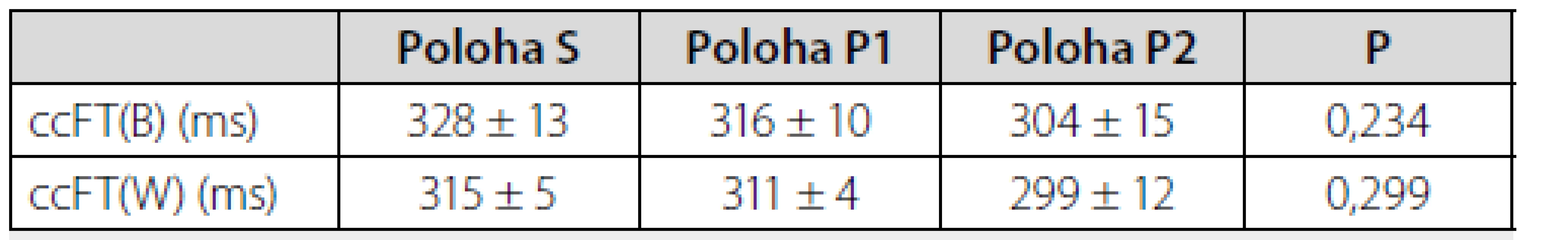
S – supinní poloha S, P1 – pronační poloha P1, P2 – pronační poloha P2, ccFT(B) – korigovaný karotický průtokový čas dle Bazetta, ccFT (W) – korigovaný karotický průtokový čas dle Wodey. V tabulce 3 jsou uvedeny plochy řezů sledovaných žil a minimální a maximální průměr a kolapsibilita v. cava inferior. Mezi polohami nebyly zjištěny rozdíly v ploše v. cephalica, v. saphena, ani exspirační a inspirační ploše řezu a exspiračním předozadním průměru v. cava inferior.
Tab. 3. Plochy a průměry sledovaných žil 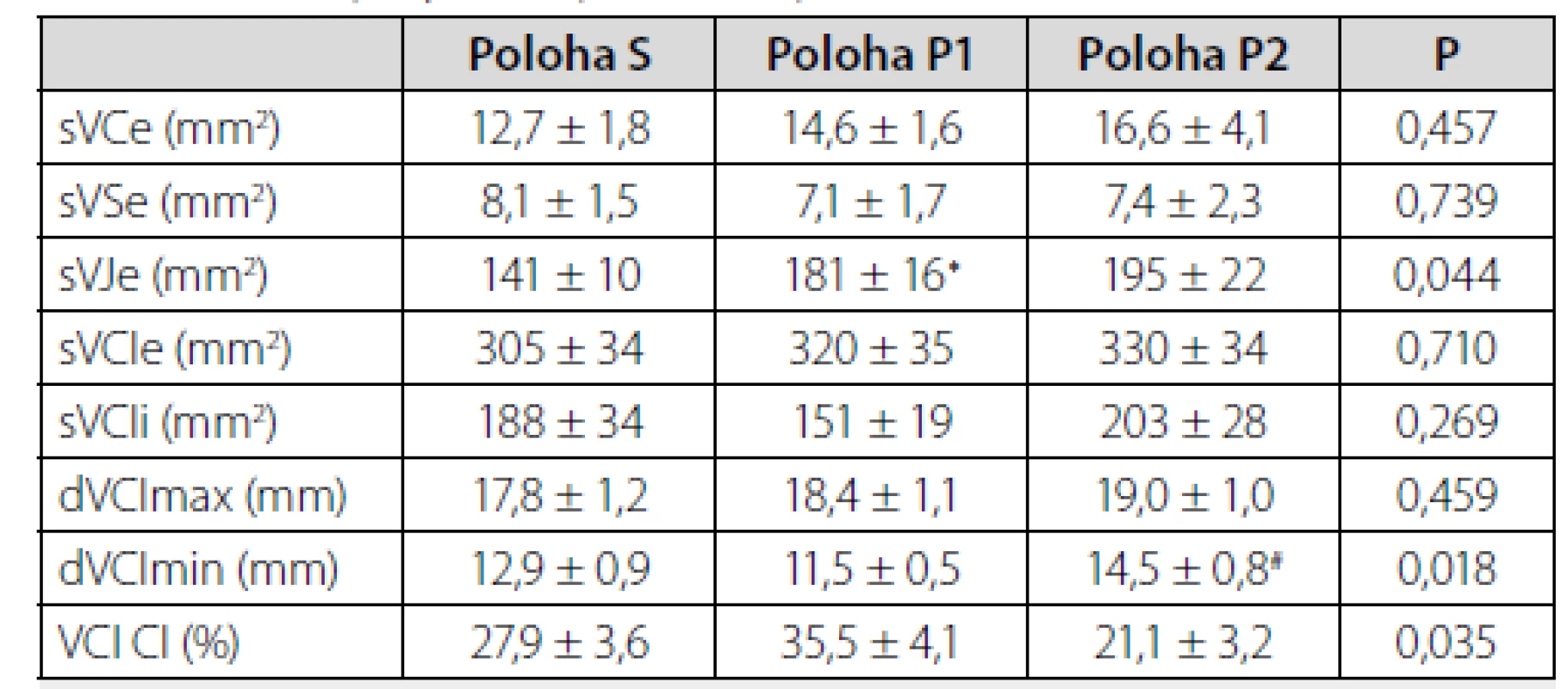
* P < 0,05 vs. Poloha S, # P < 0,05 vs. Poloha P1
S – supinní poloha S, P1 – pronační poloha P1, P2 – pronační poloha P2, sVCe – exspirační plocha v. cephalica na pravé horní končetině; sVSe – exspirační plocha v. saphena na pravé dolní končetině; sVJe – exspirační plocha v. jugularis interna vpravo, sVCIe – exspirační plocha v. cava inferior, sVCi – inspirační plocha v. cava inferior, dVCI max – maximální předozadní průměr v. cava inferior, dVCImin – minimální předozadní průměr v. cava inferior, VCI CI – index kolapsibility v. cava inferior.Byly zjištěny rozdíly v hodnotách sVJe, F (2/20) = 3,68, P = 0,044, η2 = 0,273. Srovnání mezi jednotlivými polohami ukázalo signifikantní rozdíl mezi polohou S a polohou P1 (P = 0,0260), rozdíl mezi hodnotami S a P2 nedosáhl statistické významnosti (P = 0,0878), mezi polohami P1 a P2 nebyl zjištěn rozdíl (P = 1,000).
Signifikantní rozdíly byly také zjištěny mezi hodnotami dVCImin, F (2/20) = 4,85, P = 0,018, η2 = 0,306, srovnání mezi jednotlivými polohami ukázalo signifikantní rozdíl mezi polohou P1 a P2 (P = 0,0315), a hodnotami VCI CI, F (1,812/18,123) = 4,20, P = 0,035, η2 = 0,296, kde korigované P při vzájemném srovnání rozdílů mezi polohami P1 a P2 nedosáhlo statistické významnosti (P = 0,0856).
Diskuze
Hlavním zjištěním této studie je nález nezměněného srdečního výdeje v pronační poloze u zdravých a spontánně ventilujících dobrovolníků. V pronační poloze dochází ke stagnaci krve v povodí jugulární žíly. Pronační poloha je spojena s hemodynamickými projevy zvýšeného dechového úsilí – snížením minimálního, tj. inspiračního průměru dolní duté žíly a se změnou dechové variability průměru dolní duté žíly – a s nepřímými projevy zvýšení tonu sympatiku – zvýšením středního arteriálního tlaku a trendu k vyšším hodnotám systémové vaskulární rezistence. Mimo rozdílný minimální průměr dolní duté žíly nebyly pozorovány hemodynamické rozdíly mezi oběma variantami pronační polohy.
Dosud publikované studie hodnotící změny hemodynamiky v pronační poloze se zaměřují především na pacienty v celkové anestezii [1, 2, 3, 4]. Při porovnání našich výsledků s již publikovanými studiemi se ukazuje, že k poklesu srdečního výdeje dochází pouze u pacientů v celkové anestezii [1, 2, 5, 6]. Za bdělého stavu a spontánní ventilace nebyly při vyšetření srdečních objemů a ejekční frakce levé srdeční komory scintigrafickou metodou zjištěny změny srdečního výdeje ani u neobézních pacientů [21], ani u pacientů s preexistujícím kardiálním onemocněním, u kterých bylo pozorováno pouze mírné zvýšení tepové frekvence [22]. Tuto skutečnost si vysvětlujeme zachováním autoregulačních mechanismů v bdělém stavu, kdy změny tonu sympatického nervového systému umožňují modulaci žilního návratu [23] a kontraktility myokardu [24] a kdy zvýšení dechového úsilí příznivě ovlivňuje žilní návrat [25]. Tyto mechanismy jsou v celkové anestezii potlačeny a dochází ke snížení žilního návratu a srdečního výdeje i u zdravých jedinců [1, 2].
Tradičně se ve spondylochirurgii peroperačně používá podložení těla speciálními polohovacími pomůckami s cílem vyrovnat bederní lordózu a zlepšit přístup do operačního pole [2, 7]. Argumentem pro užití některého ze způsobů podložení je také snaha o uvolnění tlaku na dutinu břišní s cílem snížit hydrostatický tlak v paravertebrálních žilních pleteních a tím snížit velikost krevní ztráty a zlepšit přehlednost operačního pole. Velikost zvýšení intraabdominálního tlaku koreluje s výší krevní ztráty [2, 7]. Hemodynamický efekt pronační polohy v celkové anestezii na různých typech polohovacích stolů hodnotí práce z roku 2005 [1], použité polohovací stoly ale nejsou plně srovnatelné s metodami polohování použitými v naší studii, a proto jsou tyto výsledky s našimi obtížně porovnatelné. V této studii jsme při srovnání obou variant pronační polohy nepozorovali rozdíl ve vlivu na stagnaci krve v povodí dolní duté žíly – exspirační průměr a plocha dolní duté žíly nevykazují statisticky významné rozdíly mezi polohami. Vysvětlením může být skutečnost, že v obou polohách byl tlak podložky na břišní stěnu minimální.
V této studii nebyl potvrzen nález předpokládaného poolingu krve v končetinách na rozdíl od jugulárního řečiště. Výsledek ale může být ovlivněn odlišnou distenzibilitou centrálních a periferních žil, venózní tlak nebyl v této neinvazivní studii sledován. Stagnace krve v končetinách, diskutovaná v literatuře jako možná příčina hemodynamické nestability [1, 2], nebyla dosud prokázána v žádné publikované práci.
Vyšší dechová variabilita průměru dolní duté žíly a její menší inspirační průměr pozorované v naší studii v nepodložené pronační poloze jsou pravděpodobně způsobeny vyšším dechovým úsilím při snížené poddajnosti hrudní stěny a respiračního systému v nepodložené pronační poloze [26]. Vyšší dechové úsilí je v této situaci nutné k udržení dostatečného dechového objemu. Toto usilovné inspirium může mít vliv na udržení žilního návratu a zachování srdečního výdeje [25]. Zmiňovaný mechanismus je v celkové anestezii zcela limitován svalovou relaxací a přetlakovou umělou plicní ventilací.
V průběhu pronační polohy panují obavy z možné hyperemie v oblasti hlavy způsobené stagnací krve, která je v některých pracích spojována i s rizikem poškození zraku [27, 28]. Naše práce potvrzuje riziko stagnace krve v povodí jugulární žíly v pronační poloze.
Naše studie má také řadu limitací. Všechna data byla získávána neinvazivními technikami a ultrazvuková měření průměrů žil mohou být zkreslena jak změnou místa měření mezi polohami, tak také úhlem přiložení ultrazvukové sondy. Ultrazvukové hodnocení velikosti vena cava inferior bylo prováděno transhepatálně a nikoliv standardní technikou a nelze vyloučit případný vliv tlaku na jaterní parenchym a okolní struktury v některé z pronačních poloh. Přítomnost hyperemie v oblasti hlavy nebyla objektivizována jinou nezávislou technikou, např. pomocí NIRS (near‑infrared spectroscopy). Nebyla měřena hodnota nitrobřišního tlaku ani žilního tlaku v periferních žilách, jejichž znalost by přispěla k interpretaci pozorování. Pro hodnocení změn preloadu byl použit neinvazivní ukazatel ccFT, který nemusí mít dostatečnou diskriminační schopnost rozlišit menší změny preloadu. Studie byla provedena na zcela zdravých, mladých a neobézních dobrovolnících, což omezuje možnost extrapolace získaných výsledků. Vzhledem k velikosti souboru a použité metodě statistického hodnocení s Bonferonniho korekcí existuje riziko falešně negativních výsledků ve srovnáních dat mezi skupinami.
Závěry
V rámci limitací této studie bylo zjištěno, že u zdravých nesedovaných dobrovolníků nedochází v pronační poloze ke snížení srdečního výdeje ani preloadu, ale dochází ke změnám systémové vaskulární rezistence, ke stagnaci krve v jugulárním řečišti a v nepodložené pronační poloze ke zvýšení kolapsibility dolní duté žíly.
PROHLÁŠENÍ AUTORŮ: Prohlášení o původnosti: Předkládaná práce je původní a není zaslána k recenznímu řízení do jiného media. Střet zájmů: Autoři prohlašují, že nemají střet zájmů v souvislosti s tématem studie. Podíl autorů: LK spoluiniciovala vznik studie, podílela se na přípravě protokolu, sběru dat a připravila rukopis studie. VD spoluinicializovala vznik studie, podílela se na přípravě protokolu studie a přípravě rukopisu studie. PD se podílel na přípravě protokolu studie, sběru dat, provedl statistickou analýzu dat a finalizoval rukopis studie. Poděkování: Děkujeme kolegyním a kolegům z Kliniky anesteziologie, resuscitace a intenzivní medicíny Fakultní nemocnice Hradec Králové za účast v této studii, bez které by tato práce nebyla možná. Registrace: Studie byla registrována na ClinicalTrials.gov pod identifikátorem NCT04491331. Financování: Podpořeno MZ ČR – RVO (FNHK, 00179906). Projednání etickou komisí: Protokol studie byl schválen Etickou komisí Fakultní nemocnice Hradec Králové (předseda MUDr. Jiří Vortel) pod jednacím číslem 202006 S15 dne 4. 6. 2020.
KORESPONDENČNÍ ADRESA AUTORA:
doc. MUDr. Pavel Dostál, Ph.D., MBA
Článek přijat redakcí: 29. 11. 2020;
Článek přijat k tisku: 2. 3. 2021;
Zdroje
1. Dharmavaram S, Jellish WS, Nockels RP, Shea J, Mehmood R, Ghanayem A, et al. Effect of prone positioning systems on hemodynamic and cardiac function during lumbar spine surgery: an echocardiographic study. Spine (Phila Pa 1976). 2006; 31(12): 1388–1393; discussion 1394. doi: 10.1097/01.brs.0000218485.96713. 44.
2. Chui J, Craen RA. An update on the prone position: Continuing Professional Development. Can J Anaesth. 2016; 63(6): 737–767. English. doi: 10.1007/s12630-016-0634-x.
3. Yokoyama M, Ueda W, Hirakawa M, Yamamoto H. Hemodynamic effect of the prone position during anesthesia. Acta Anaesthesiol Scand. 1991; 35(8): 741–744. doi: 10.1111/ j.1399-6576.1991.tb03382.x.
4. Toyota S, Amaki Y. Hemodynamic evaluation of the prone position by transesophageal echocardiography. J Clin Anesth. 1998; 10(1): 32–35. doi: 10.1016/s0952-8180(97)00216-x.
5. Shimizu M, Fujii H, Yamawake N, Nishizaki M. Cardiac function changes with switching from the supine to prone position: analysis by quantitative semiconductor gated single‑photon emission computed tomography. J Nucl Cardiol. 2015; 22(2): 301–307. doi: 10.1007/ s12350-014-0058-3.
6. Edgcombe H, Carter K, Yarrow S. Anaesthesia in the prone position. Br J Anaesth. 2008; 100(2): 165–183. doi: 10.1093/bja/aem380.
7. Park CK. The effect of patient positioning on intraabdominal pressure and blood loss in spinal surgery. Anesth Analg. 2000; 91(3): 552–557. doi: 10.1097/00000539-200009000 - 00009.
8. Barash PG, Cullen FB, Stoelting KR, Cahalan MK, Stock Ch. (eds). Klinická anesteziologie. Překlad 6. vydání. Praha: Grada; 2015.
9. ClearSight system – Noninvasive hemodynamic monitoring [on ‑ line]. [cit. 2020-07-24]. Dostupné z: https://www.edwards.com/devices/Hemodynamic‑Monitoring/ clearsight.
10. Ameloot K, Palmers PJ, Malbrain ML. The accuracy of noninvasive cardiac output and pressure measurements with finger cuff: a concise review. Curr Opin Crit Care 2015; 21(3): 232–239. doi:10.1097/MCC.0000000000000198.
11. Fischer MO, Joosten A, Desebbe O, Boutros M, Debroczi S, Broch O, et al. Interchangeability of cardiac output measurements between non ‑ invasive photoplethysmography and bolus thermodilution: A systematic review and individual patient data meta‑analysis. Anaesth Crit Care Pain Med. 2020; 39(1): 75–85. doi: 10.1016/j.accpm.2019. 05. 007.
12. Boisson M, Poignard ME, Pontier B, Mimoz O, Debaene B, Frasca D. Cardiac output monitoring with thermodilution pulse‑contour analysis vs. non ‑ invasive pulse‑contour analysis. Anaesthesia. 2019; 74(6): 735–740. doi: 10.1111/anae.14638.
13. Rauch S, Schenk K, Gatterer H, Erckert M, Oberhuber L, Bliemsrieder B, et al. Venous Pooling in Suspension Syndrome Assessed with Ultrasound. Wilderness Environ Med. 2020; 31(2): 204–208. doi: 10.1016/j.wem.2019. 08. 012.
14. Yokoyama M, Ueda W, Hirakawa M, Yamamoto H. Hemodynamic effect of the prone position during anesthesia. Acta Anaesthesiol Scand. 1991; 35(8): 741–744. doi: 10.1111/ j.1399-6576.1991.tb03382.x.
15. Blehar DJ, Glazier S, Gaspari RJ. Correlation of corrected flow time in the carotid artery with changes in intravascular volume status. J Crit Care. 2014; 29(4): 486–488. doi: 10.1016/j.jcrc.2014. 03. 025.
16. Mackenzie DC, Khan NA, Blehar D, Glazier S, Chang Y, Stowell ChP, et al. Carotid Flow Time Changes With Volume Status in Acute Blood Loss. Annals of Emergency Medicine. 2015; 66(3): 277–282. doi: org/10.1016/j.annemergmed.2015. 04. 014.
17. Kim D‑H, Shin S, Kim N, Choi T, Choi SH, Choi YS. Carotid ultrasound measurements for assessing fluid responsiveness in spontaneously breathing patients: corrected flow time and respirophasic variation in blood flow peak velocity. British Journal of Anaesthesia 2018; 121(3): 541–549. doi: 10.1016/j.bja.2017. 12. 047.
18. Chebl RB, Wuhantu J, Kiblawi S, Dagher GA, Zgheib H, Bachir R, et al. Corrected carotid flow time and passive leg raise as a measure of volume status. Am J Emerg Med. 2019 Aug; 37(8): 1460–1465. doi: 10.1016/j.ajem.2018. 10. 047.
19. Barjaktarevic I, Toppen WE, Hu S, Aquije Montoya E, Ong S, Buhr R, et al. Ultrasound Assessment of the Change in Carotid Corrected Flow Time in Fluid Responsiveness in Undifferentiated Shock. Crit Care Med. 2018; 46(11): e1040–e1046. doi: 10.1097/ CCM.0000000000003356.
20. Payam M, Hooman H‑N. Calculation of corrected flow time: Wodey’s formula vs. Bazett’s formula, J Critical Care 2018; 44 : 154–155. doi: 0.1016/j.jcrc.2017. 10. 046.
21. Лизогуб М. Postural hemodynamic changes after turning to prone position. Science - Rise 2015; 3(4(8)): 71–74. doi: http://dx.doi.org/10.15587/2313-8416.2015.39269.
22. Yap K, Campbell P, Cherk M, McGrath C, Kalff V. Effect of prone versus supine positioning on left ventricular ejection fraction (LVEF) and heart rate using ECG gated Tl-201 myocardial perfusion scans and gated cardiac blood pool scans. J Med Imaging Radiat Oncol. 2012; 56(5): 525–531. doi: 10.1111/j.1754-9485.2012.02438.x.
23. Pang CC. Autonomic control of the venous system in health and disease: effects of drugs. Pharmacol Ther. 2001; 90(2–3): 179–230. doi: 10.1016/s0163-7258(01)00138-3.
24. Cohn JN. Sympathetic nervous system activity and the heart. Am J Hypertens. 1989; 2(12 Pt 2): 353S–356S.
25. Pinsky MR. Cardiovascular issues in respiratory care. Chest. 2005; 128(5 Suppl 2): 592S–597S. doi: 10.1378/chest.128.5_suppl_2.592S.
26. Palmon SC, Kirsch JR, Depper JA, Toung TJ. The effect of the prone position on pulmonary mechanics is frame‑dependent. Anesth Analg. 1998; 87(5): 1175–1180. doi: 10.1097/00000539-199811000-00037.
27. Gill B, Heavner JE. Postoperative visual loss associated with spine surgery. Eur Spine J. 2006; 15(4): 479–484. doi: 10.1007/s00586-005-0914-6.
28. Shriver MF, Xie JJ, Tye EY, Rosenbaum BP, Kshettry VR, Benzel EC, et al. Lumbar microdiscectomy complication rates: a systematic review and meta‑analysis. Neurosurg Focus. 2015; 39(4): E6. doi: 10.3171/2015. 7. FOCUS15281.
Štítky
Anesteziologie a resuscitace Intenzivní medicína
Článek vyšel v časopiseAnesteziologie a intenzivní medicína
Nejčtenější tento týden
2021 Číslo 2- Bezpečnostní profil metamizolu – systematický přehled
- Aktuální pohled na využití myorelaxancií a jejich antidot v moderní anesteziologii a intenzivní medicíně
- Perorální antivirotika jako vysoce efektivní nástroj prevence hospitalizací kvůli COVID-19 − otázky a odpovědi pro praxi
- Neodolpasse účinně snižuje pooperační bolest
- Neodolpasse jako ideální volba tam, kde je bolest provázena spasmem kosterního svalstva
-
Všechny články tohoto čísla
- Point of care ultrazvuk u kritických stavů
-
Bartonellová endokarditida jako příčina akutního srdečního selhání
Význam rutinního echokardiografického vyšetření u akutního respiračního selhání na jednotkách intenzivní péče - Co vše skrývá krevní obraz
- Perioperační diabetes insipidus
- Konsenzuální stanovisko: Univerzální definice a klasifikace srdečního selhání
- Léčba pacientů s onemocněním COVID-19
- Načasování operace po infekci SARS COVID-19, mezinárodní kohortová studie
- K článku: Odmítnutí převzetí pacienta z přednemocniční péče cílovým poskytovatelem akutní lůžkové péče
- Odpověď
-
Vyjádření k některým mediálním ohlasům na Stanovisko ČSARIM 13/2020
Rozhodování u pacientů v intenzivní péči v situaci nedostatku vzácných zdrojů - Odpověď
- Zajímavosti, tipy a triky, informace z jiných oborů
- Neinvazivní a invazivní monitorace hemodynamiky na jednotce intenzivní péče
- Premiéra akreditovaného kurzu Simulace kritických stavů proběhla v Brně
- Zhodnocení implementace simulační výuky do specializačního vzdělávání lékařů před absolvováním základního kmene
-
Diabetická neuropatie:
rizikový faktor těžkého průběhu COVID-19? - Hemodynamické změny v pronační poloze – neinvazivní fyziologická studie
-
Sto devadesát let od objevu chloroformu –
historie inhalačních anestetik. Část 2 - Náš článek po 10 letech: Intrathecal midazolam as supplementary analgesia for chronic lumbar pain – 15 years’experience
- Umělá plicní ventilace zvyšuje riziko zhoršení kognitivních funkcí a poškození mozku
- Blokády kožních nervů a uspořádání fascií v oblasti stehna
- Anesteziologie a intenzivní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Načasování operace po infekci SARS COVID-19, mezinárodní kohortová studie
- Blokády kožních nervů a uspořádání fascií v oblasti stehna
- Neinvazivní a invazivní monitorace hemodynamiky na jednotce intenzivní péče
- Hemodynamické změny v pronační poloze – neinvazivní fyziologická studie
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



