-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaVliv věku a pohlaví na farmakodynamické vlastnosti rokuronia během totální intravenózní anestezie – prospektivní studie
Influence of age and gender on the pharmacodynamic parameters of rocuronium during total intravenous anaesthesia – a prospective study
Influence of age and gender on the pharmacodynamic parameters of rocuronium during total intravenous anaesthesia – a prospective study
Objective:
To compare the pharmacodynamics of 0.6 mg . kg-1 rocuronium in young and older patients of both genders during total intravenous anaesthesia.Design:
Clinical, observational, non-blinded study.Setting:
Department of Anaesthesiology, University Hospital.Materials and methods:
Following local ethics committee approval and informed consent, patients scheduled for surgery under total intravenous anesthesia (propofol/sufentanil) were divided into 4 study groups: 37 males aged 20–40, 40 males aged 60–75 yrs, 43 females aged 20–40 and 38 females aged 60–75 yrs. Neuromuscular block following rocuronium (0.6 mg kg-1) was monitored as follows: train-of-four [TOF] stimulation of the ulnar nerve at 15-s intervals, EMG of the adductor pollicis muscle. The onset time (from application of rocuronium to maximum depression of T1), clinical duration (from application to 25% recovery of T1), and time to full spontaneous recovery (from application to TOF-ratio ≥ 0.9) were determined for each patient. The Kruskal-Wallis test was used to compare differences between the groups; P < 0.05 was considered statistically significant.Results:
The onset time (median [interquartile range]) in the respective groups was 90 [80–110]BCD, 135 [116–165]AC, 75 [60–90]ABD, and 120 [90–146]AC seconds. The clinical duration was 30 [25–42]BCD, 58 [53–67]AD, 50 [40–65]AD, and 85 [70–90]ABC min. The interval to full spontaneous recovery was 59 [51–67]BCD, 102 [75–106]A, 76 [66–91]AD, and 128 [94–137]AC min. (AP<0.05 vs. young males, BP<0.05 vs. elderly males, CP<0.05 vs. young females, DP<0.05 vs. elderly females).Conclusion:
Females and the elderly were more sensitive to rocuronium.Keywords:
rocuronium – neuromuscular blockade – age – gender
Autoři: Adamus Milan 1; Hrabálek Lumír 2; Wanek Tomáš 2; Gabrhelík Tomáš 1; Zapletalová Jana 3,4
Působiště autorů: Klinika anesteziologie, resuscitace a intenzivní medicíny, Fakultní nemocnice a Lékařská fakulta Univerzity Palackého v Olomouci 1; Neurochirurgická klinika, Fakultní nemocnice a Lékařská fakulta Univerzity Palackého v Olomouci 2; Ústav lékařské biofyziky, Lékařská fakulta Univerzity Palackého v Olomouci 3; Institut molekulární a translační medicíny, Lékařská fakulta Univerzity Palackého v Olomouci 4
Vyšlo v časopise: Anest. intenziv. Med., 23, 2012, č. 1, s. 21-27
Kategorie: Anesteziologie - Původní práce
Souhrn
Cíl studie:
Srovnání farmakodynamiky rokuronia (0,6 mg . kg-1) u mladších a starších nemocných obou pohlaví během totální intravenózní anestezie.Typ studie:
Klinická, observační, bez zaslepení.Typ pracoviště:
Klinika anesteziologie, resuscitace a intenzivní medicíny fakultní nemocnice.Materiál a metoda:
Po schválení etickou komisí a informovaném souhlasu nemocných jsme vyšetřovali nemocné, operované v totální intravenózní anestezii (propofol/sufentanil). U 37 mužů ve věku 20–40 let (skupina A), 40 mužů (60–75 let, skupina B), 43 žen (20–40 let, skupina C), 38 žen (60–75 let, skupina D) jsme monitorovali svalovou relaxaci po podání rokuronia (0,6 mg . kg-1): stimulace n. ulnaris v režimu TOF v 15sekundových intervalech, sledování EMG odpovědi m. adductor pollicis. U každého nemocného jsme stanovili rychlost nástupu účinku (od aplikace rokuronia do maximální deprese T1), délku klinického účinku (od aplikace rokuronia do 25% zotavení T1) a interval do plného zotavení (od aplikace do TOF-ratio ≥ 0,90). Skupiny jsme porovnali Kruskal-Wallisovým testem na 5% hladině významnosti.Výsledky:
Rychlost nástupu účinku (medián [IQR]) byla ve skupinách A, B, C, D 90 [80–110]BCD, 135 [116–165]AC, 75 [60–90]ABD a 120 [90–146]AC sekund. Délka klinického účinku byla 30 [25–42]BCD, 58 [53–67]AD, 50 [40–65]AD a 85 [70–90]ABC min. Interval do spontánního zotavení byl 59 [51–67]BCD, 102 [75–106]A, 76 [66–91]AD a 128 [94–137]AC min.
(AP < 0,05 vs. mladší muži, BP < 0,05 vs. starší muži, CP < 0,05 vs. mladší ženy, DP < 0,05 vs. starší ženy).Závěr:
Ženy a starší nemocní jsou citlivější k účinku rokuronia podaného v jedné dávce (0,6 mg . kg-1).Klíčová slova:
rokuronium – nervosvalová blokáda – věk – pohlavíÚvod
Rokuronium (ROC) bylo uvedeno do klinické praxe v roce 1994 [1]. V současnosti patří k nejčastěji používaným NMBAs (neuromuscular blocking agents), jeho obliba v moderní anesteziologii roste a u elektivních výkonů bez předpokládaného obtížného zajištění dýchacích cest postupně nahrazuje suxamethonium [2, 3].
Dávku léku zpravidla volíme podle hmotnosti nemocného. Účinek mnoha látek používaných během anestezie (včetně aminosteroidních NMBAs) však ovlivňuje velké množství jiných faktorů včetně pohlaví [4, 5] a věku [6–8]. Efekt všech NMBAs je spojen se značnou interindividuální variabilitou. Svalová relaxancia jsou vysoce účinné látky a pokud jsou použita nesprávně, zvyšují morbiditu operovaných nemocných [9]. Přesná znalost farmakologie NMBAs má tedy zásadní význam.
Cílem této studie bylo porovnat farmakodynamické parametry (rychlost nástupu, délku klinického účinku a interval do plného zotavení) jednotlivé dávky (0,6 mg . kg-1) rokuronia u mladých a starších pacientů obojího pohlaví během totální intravenózní anestezie.
Metoda
Klinická studie byla prospektivní, neintervenční, bez zaslepení. Po schválení etickou komisí a získání informovaného souhlasu jsme vyšetřovali nemocné, kteří byli indikováni k plánovanému operačnímu výkonu v celkové anestezii, s nutností svalové relaxace a tracheální intubace. Předpokládaná délka výkonu byla 60–120 min. Všem nemocným byla podána stejná celková anestezie, ale do studie byli zařazeni pouze muži a ženy dvou věkových skupin (20–40 a 60–75 let). Vylučovacími kritérii byly ASA (American Society of Anesthesiologists) klasifikace fyzického stavu více než 3, obezita (BMI [body mass index] nad 30 kg . m-2), predikovaná obtížná intubace [10], věk mimo zvolené rozmezí, užívání léků, které mohou ovlivnit nervosvalový přenos a přítomnost závažných renálních, jaterních, metabolických nebo nervosvalových onemocnění.
Z anesteziologického dotazníku jsme zjistili demografická data nemocných – věk, hmotnost, výšku, klasifikaci podle ASA a vypočítali BMI.
Anestezie
Nemocní byli premedikováni diazepamem 5–10 mg per os jednu hodinu před plánovaným začátkem operace. Před úvodem do anestezie jsme u nemocných zajistili nitrožilní vstup zavedením periferní kanyly velikosti 18 nebo 20 G na předloktí kontralaterálním k měření relaxace. Po tříminutové preoxygenaci jsme intravenózně podali midazolam (1–3 mg) a sufentanil (0,1 μg . kg-1). U všech nemocných jsme použili totální intravenózní anestezii (TIVA, total intravenous anaesthesia) v režimu TCI (target controlled infusion) pomocí infuzního přístroje Base Primea® (Fresenius Vial). Tímto způsobem jsme zabezpečili hypnotickou (propofol) a analgetickou (sufentanil) složku anestezie. Dávkovací zařízení Base Primea® bylo v úvodu naprogramováno pro dosažení cílové plazmatické hladiny propofolu 2,0 μg . ml-1 (model podle Schnidera [11]) a sufentanilu 1,8 ng . ml-1 (model podle Geptse [11]); tyto hodnoty byly následně korigovány podle klinického stavu (TK, P) nemocných během anestezie.
Svalovou relaxaci jsme zajistili jednorázově podanou bolusovou dávkou rokuronia (0,6 mg . kg-1). Vypočtené množství ROC jsme podali během 5 s do rychle běžící infuze fyziologického roztoku. Po dosažení maximální deprese T1 (stanovení rychlosti nástupu účinku) jsme provedli tracheální intubaci a parametry umělé plicní ventilace (směsí 40 % kyslíku a vzduchu) jsme nastavili v režimu „low-flow“ k dosažení hodnoty EtCO2 mezi 4,7–5,0 kPa. U každého nemocného jsme během anestezie umožnili z úvodní dávky relaxancia spontánní zotavení na 25 % T1 (stanovení délky klinického účinku) a k hodnotě TOF-ratio ≥ 0,9 (stanovení celkové délky účinku do plného zotavení). Pokud to vyžadoval průběh operace, další svalovou relaxaci jsme udržovali doplňujícími dávkami (top-ups) ROC (5 mg). Sufentanil jsme vysadili 10 minut před koncem operace. Reverzi (neostigmin 0,04 mg . kg-1) jsme podali po předchozí aplikaci parasympatolytika (atropin 0,015 mg . kg-1), jestliže to bylo nutné podle hodnot měření NMT (neuromuscular transmission) na konci anestezie.
Monitorování svalové relaxace
Metodika respektovala zásady GCRP (Good Clinical Research Practice, Stockholmská revize [12]) a byla popsána dříve [5]. Použili jsme modul NMT monitoru Datex-Ohmeda AS/3™, monitorovací systém byl připojen k nemocnému před úvodem do anestezie. Po pečlivé přípravě kůže distálního předloktí jsme nalepili 5 elektromyografických elektrod a předloktí imobilizovali v supinaci. Kožní teplotu jsme měřili teplotním čidlem umístěným na dorzu ruky končetiny, která byla použita k monitorování relaxace. Pro udržení teploty nad 34 °C jsme předloktí obalili vatovým obvazem.
Po úvodu do anestezie, ale před podáním ROC, jsme přístroj pro měření NMT zkalibrovali pomocí vnitřního algoritmu. Pro vlastní měření hloubky relaxace jsme používali režim TOF (train-of-four) s těmito parametry: supramaximální stimulace n. ulnaris s opakováním sérií TOF v 15sekundových intervalech, elektromyografické vyhodnocení odpovědi m. adductor pollicis.
U každého nemocného jsme stanovili tyto parametry:
- nástup účinku (onset time) [s] = interval od i. v. podání ROC do maximální deprese T1;
- délka klinického účinku (clinical duration) [min]) = interval od i. v. podání ROC do spontánního zotavení T1 na 25 % výchozí hodnoty;
- celková délka účinku do plného zotavení (dosažení TOF-ratio ≥ 0,9) [min] = interval od i. v. podání ROC do spontánního zotavení TOF-ratio na hodnotu nejméně 0,9;
Ze studie byli vyřazení nemocní, u nichž se nepodařilo zabezpečit spolehlivé monitorování nervosvalového přenosu. Délku klinického účinku jsme nehodnotili u nemocných, u nichž po podání úvodní dávky NMBA neklesla hodnota T1 pod 25 % nebo průběh operace vyžadoval doplnění relaxace jednorázovými dávkami rokuronia (top-ups). Celkovou délku účinku do plného zotavení jsme určili pouze u těch pacientů, u kterých průběh operačního výkonu umožnil odeznění blokády do úplného zotavení.
Statistická analýza
Ke statistické analýze jsme použili softwarový balík InStat v. 3.10 (GraphPad Software, USA, informace na www.graphpad.com). Skupiny jsme porovnali pomocí analýzy rozptylu (ANOVA s post-testem [Tukey-Kramer]), neparametrické analýzy rozptylu (Kruskal-Wallis) s post-testem podle Dunna. Pro srovnání četností jsme použili chí-kvadrát test. Výsledky jsou ve formátu průměr ± směrodatná odchylka (95% intervaly spolehlivosti), medián [mezikvartilové rozpětí] nebo četnosti. Za statisticky významnou hodnotu jsme považovali p < 0,05. Příslušné testy jsou uvedeny v tabulkách 1 a 2.
Výsledky
Demografii nemocných shrnuje tabulka 1. Muži byli vyšší (p < 0,0001) a měli vyšší hmotnost (p < 0,0001), BMI byl podobný u obou pohlaví. Starší nemocní (muži i ženy) měli vyšší ASA klasifikaci.
Tab. 1. Demografické údaje nemocných 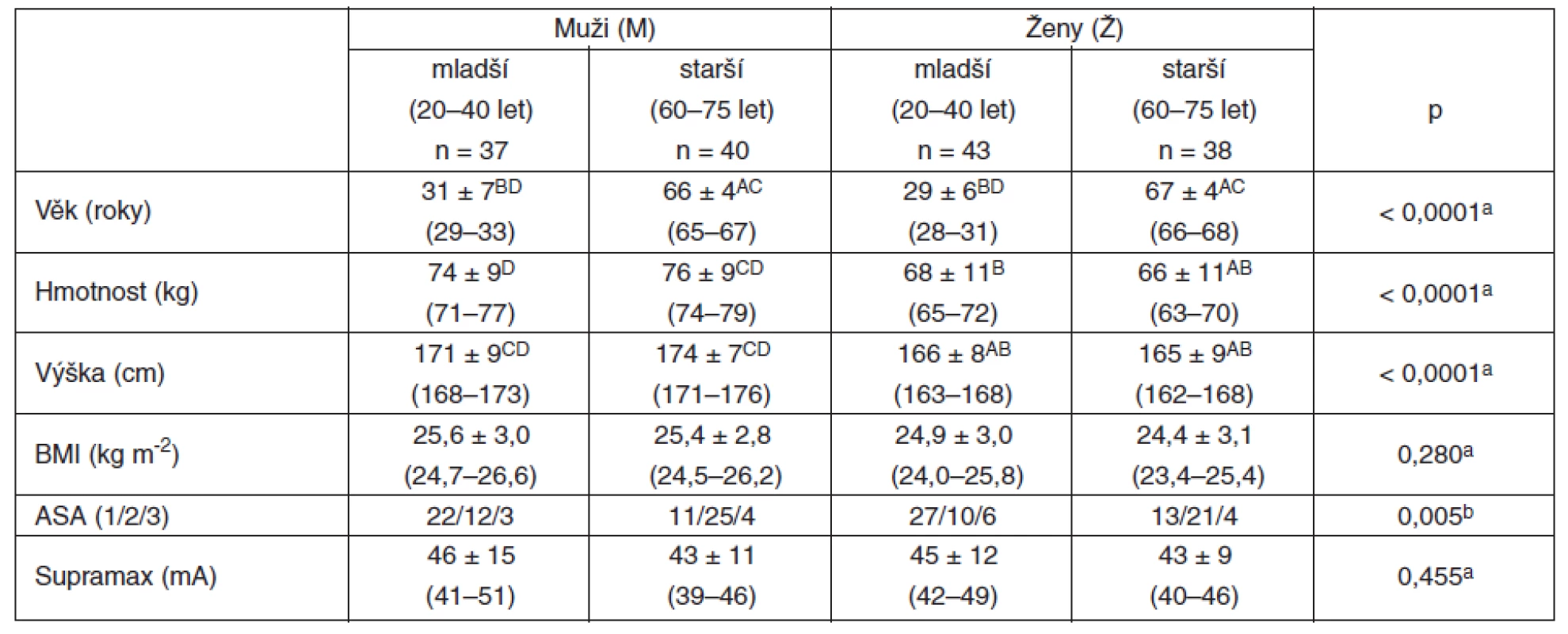
n = počet nemocných, BMI = body mass index, ASA = klasifikace fyzického stavu podle ASA (American Society of Anesthesiologists), supramax = velikost supramaximálního impulsu Data jsou ve formátu průměr ± SD (95% intervaly spolehlivosti) nebo četnosti. aANOVA s mnohonásobným porovnáním post-testem (Tukey-Kramer), bchí-kvadrát Ap < 0,05 vs. mladší M, Bp < 0,05 vs. starší M, Cp < 0,05 vs. mladší Ž, Dp < 0,05 vs. starší Ž Do studie bylo iniciálně zahrnuto 164 pacientů (79 mužů, 85 žen). Obrázek 1 ukazuje postupový diagram nemocných zařazených do studie a důvody pro vyřazování v jednotlivých fázích. U šesti nemocných se nepodařilo zajistit spolehlivé monitorování NMT. U čtyř nemocných neklesla po úvodní dávce ROC hodnota T1 pod 25 %, a proto u nich nebyla stanovena délka klinického účinku. Iniciální dávka ROC byla v průběhu operace doplněna u 22 nemocných, u 11 nemocných byla na konci operace podána reverze. Výsledný počet nemocných, u nichž jsme stanovili interval do plného zotavení, byl 121.
Obr. 1. Postupový diagram nemocných zařazených do studie 
Vysvětlivky: mladší = 20–40 let, starší = 60–75 let n = počet nemocných, nástup účinku = interval od intravenózního podání ROC do maximální deprese T1, délka klinického účinku = interval od intravenózního podání ROC do 25% zotavení T1, interval do plného zotavení = interval od intravenózního podání ROC do spontánního zotavení TOF-ratio na hodnotu nejméně 0,9 Důvody pro vyřazení ze studie jsou uvedeny v hranatých závorkách. U všech pacientů umožnilo jednorázové podání ROC tracheální intubaci. Farmakodynamické parametry udává tabulka 2. Nástup účinku byl nejrychlejší u mladých žen (medián 75, mezikvartilové rozpětí [IQR] 60–90 s), délka klinického účinku byla nejkratší u mladých mužů (medián 30, IQR 25–42 min), stejně jako interval do plného zotavení (medián 59, IQR 51–67 min). Obrázky 2–4 ukazují percentuální prodloužení těchto hodnot ve zbývajících skupinách nemocných.
Obr. 2. Rychlost nástupu účinku 0,6 mg kg<sup>-1</sup> rokuronia (= interval od intravenózního podání ROC do maximální deprese T<sub>1</sub> v sérii TOF) 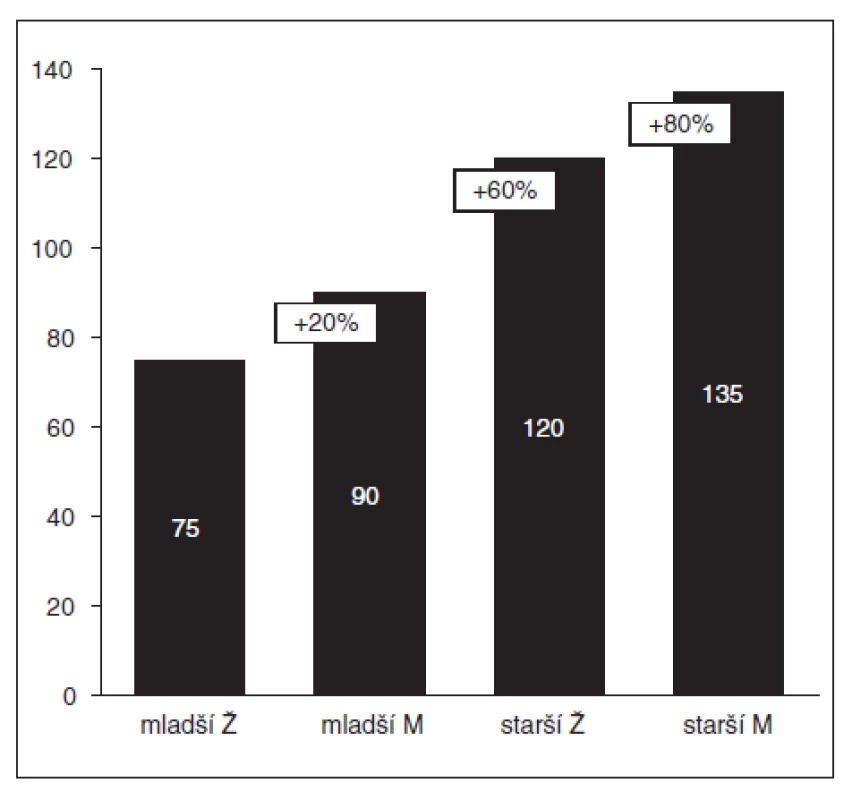
Obr. 3. Délka klinického účinku 0,6 mg . kg-1 rokuronia (= interval od intravenózního podání ROC do spontánního zotavení T1 na 25 % z výchozí hodnoty v sérii TOF). 
Medián, hodnoty v % udávají prodloužení délky klinického účinku v dané skupině ve srovnání se skupinou mladších mužů. M = muži, Ž = ženy, mladší = 20–40 let, starší 60–75 let věku Obr. 4. Interval do plného zotavení po podání 0,6 mg . kg-1 rokuronia (= interval od intravenózního podání ROC do spontánního zotavení TOF-ratio na hodnotu nejméně 0,9) 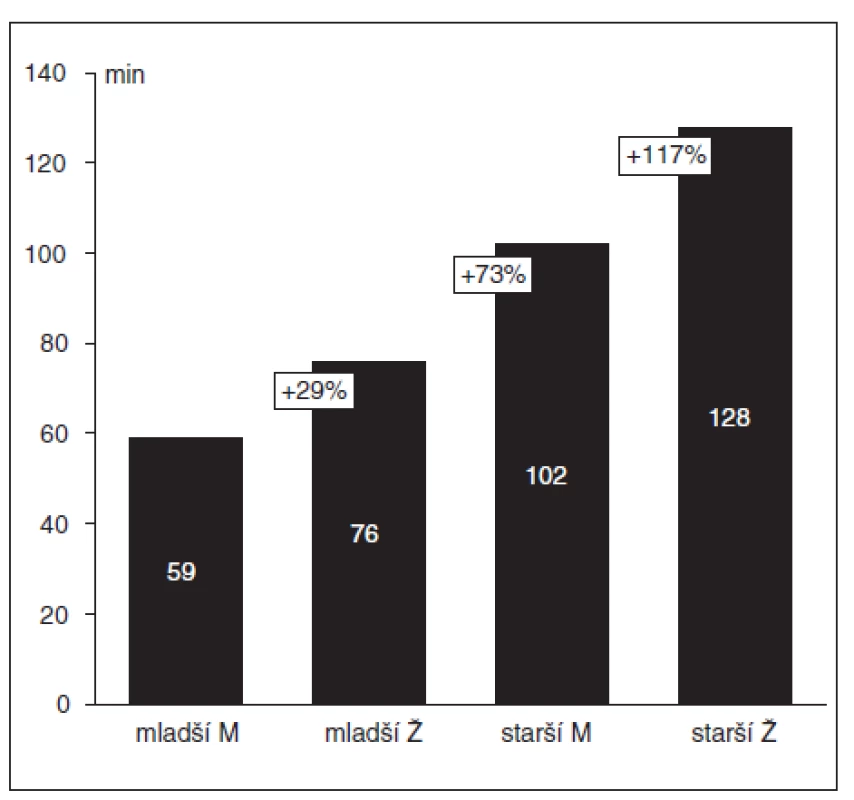
Medián, hodnoty v % udávají prodloužení doby do plného zotavení v dané skupině ve srovnání se skupinou mladších mužů. M = muži, Ž = ženy, mladší = 20–40 let, starší 60–75 let věku Diskuse
Studie potvrdila výraznou variabilitu farmakodynamických parametrů ROC po podání jednotlivé dávky (0,6 mg . kg-1) v závislosti na věku a pohlaví.
Nástup účinku byl rychlejší u žen a s věkem se prodlužoval u obou pohlaví. K navození nervosvalového bloku musí být rokuronium dopraveno k místu svého účinku (nervosvalové ploténce). Na pomalejším nástupu účinku u seniorů se tak mohou podílet: snížený srdeční výdej, delší oběhová doba, snížené prokrvení kosterních svalů a pomalejší vyrovnání biofází [13]. Délka klinického účinku byla výrazně delší u žen, s dalším prodloužením u starších nemocných obou pohlaví. Interval do plného zotavení (TOF-ratio ≥ 0,9) byl delší u žen a byl dále prodloužen u starších pacientů (skupiny 60–75 let) obou pohlaví. Sledované skupiny se lišily nejvíce v parametrech, které popisovaly délku účinku ROC (tj. doba klinického účinku a interval do plného zotavení). Například u starších žen byla délka klinického účinku téměř trojnásobná ve srovnání se skupinou mladých mužů.
Ve studii jsme prokázali rozdíly mezi muži a ženami různého věku, ale zároveň i výraznou variabilitu farmakodynamických parametrů uvnitř jednotlivých skupin (viz tab. 2). Například ve skupině starších žen byl medián délky klinického účinku 85 min s horním a dolním kvartilem 70 a 90 minut. Znamená to, že pouze u 50 % starších žen byla délka klinického účinku mezi 70 a 90 minutami.
Tab. 2. Farmakodynamika rokuronia (0,6 mg . kg-1) u mladších a starších nemocných obou pohlaví 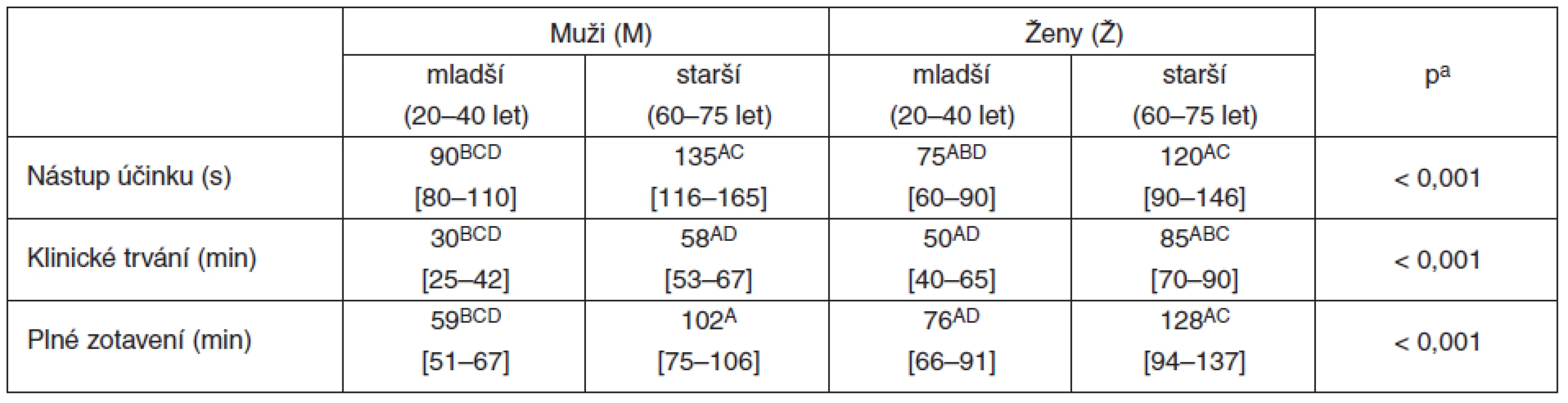
aneparametrická ANOVA (Kruskal-Wallisův test) s mnohonásobným porovnáním pomocí post-testu (Dunn) Ap < 0,05 vs. mladší M, Bp < 0,05 vs. starší M, Cp < 0,05 vs. mladší Ž, Dp < 0,05 vs. starší Ž Reziduální blok je jednou ze závažných komplikací nesprávného podávání NMBAs a jeho výskyt je stále vysoký [14]. Tato skutečnost má důležité klinické důsledky a má několik příčin.
V důsledku vysoké variability efektu nelze délku účinku NMBAs přesně předpovědět [15].
Dlouhý interval od podání relaxancia s intermediární délkou účinku nezaručuje adekvátní zotavení z účinku NMBA [16].
Neexistuje klinický test, kterým by bylo možné pooperační reziduální kurarizaci (PORC) spolehlivě detekovat a bez monitorování hloubky bloku nelze na konci anestezie vyloučit přetrvávání účinku NMBA [17–19].
I mělký reziduální blok zhoršuje koordinaci svalstva hltanu a snižuje citlivost karotických chemoreceptorů na nedostatek kyslíku. Nemocný je pak v pooperačním období ohrožen neschopností reagovat na hypoxii prohloubením ventilace [20], což společně s mikroaspiracemi může zvyšovat četnost pooperačních plicních komplikací [9, 21, 22].
Pohlaví
Současná medicína založená na důkazech (Evidence-based medicine) stále častěji poskytuje údaje o rozdílech mezi pohlavími ve farmakokinetice a farmakodynamice anestetik a NMBAs [23, 24]. Ženy jsou citlivější k účinku aminosteroidních NMBA, pravděpodobně v důsledku odlišné farmakokinetiky [4, 5]. Ženské tělo obsahuje vyšší procento tukové tkáně a nižší procento svalové hmoty a vody; důsledkem je menší distribuční objem pro ROC. Rovněž biodegradace a eliminace ROC jsou ovlivněny pohlavím, podobně jako aktivita jaterních mikrozomálních enzymů. U žen je snížená glomerulární filtrace a renální clearance (snížené vylučování ROC). Benzylizochinoliny na rozdíl od aminosteroidů podléhají Hofmannově eliminaci, což je chemický proces závislý na teplotě a pH. Tyto parametry jsou v organismu precizně kontrolovány, takže variabilita tohoto biodegradačního procesu není vysoká. Účinek benzylisochinolinů tak není pohlavím ovlivněn [5].
V souhrnu: vyšší citlivost žen k ROC je podmíněna odlišnou farmakokinetikou v důsledku rozdílné stavby těla.
Věk
Stárnutí doprovází velké množství fyziologických a patofyziologických změn, které ovlivňují farmakokinetiku i farmakodynamiku léků [6–8]. Nemocní pokročilejšího věku jsou častěji a závažněji nemocní a trpí četnými přidruženými chorobami (komorbidita). Jejich fyzický stav podle ASA je zpravidla horší než u mladých pacientů. Senioři často užívají léky, které sice dobře kompenzují přidružená onemocnění (např. hypertenzní nemoc, ischemickou chorobu srdeční či diabetes mellitus), ale mohou být zdrojem závažných interakcí. Při preskripci léků seniorům není vzácná polypragmazie, která riziko lékových interakcí dále zvyšuje a může být dokonce spojena s iatrogenním poškozením nemocného.
Stavba a složení tělesných tkání se s věkem mění společně s orgánovými funkcemi, především jaterními a ledvinnými. Rozsah a nástup těchto změn je variabilní a pravděpodobně závisí více na biologickém než kalendářním věku. Ve stáří se s poklesem celkové tělesné vody snižuje objem centrálního kompartmentu, takže vrcholová plazmatická hladina po podání jednotlivé dávky ROC je vyšší. Libová tělesná hmotnost (LBW, lean body weight) je snížena. Vyšší obsah tukové tkáně u seniorů může v této věkové skupině potenciálně prodloužit délku klinického účinku ROC i interval do plného zotavení.
Ve stáří se sice mění i vlastnosti nervosvalové synapse (např. pokles motorických jednotek, proliferace extrajunkčních receptorů, snížení množství uvolňovaného acetylcholinu) [25], ale tyto změny pravděpodobně nemají vliv na rozdíl ve farmakodynamice mladších a seniorů. ED95 rokuronia je podobná u starších (0,4 mg . kg-1) i mladších nemocných (0,5 mg . kg-1) [26] a pokud je u starších nemocných dosaženo stejné plazmatické hladiny ROC jako u mladých, hloubka bloku je podobná [25].
V souhrnu: k základním faktorům, které mění citlivost k ROC ve stáří, patří snížená vazba na bílkoviny, změny ve složení těla (svaly/tuk/voda), metabolismus a eliminace ROC (jaterní, renální funkce) [27].
Studie má omezení. Z logistických důvodů byla navržena jako observační a nezaslepená. Anestezii vedl vždy stejný anesteziolog (M. A.). Snahou bylo použít totožný postup u všech nemocných. Protokol byl stanoven velmi rigorózně, proto bylo z důvodu jeho porušení v průběhu studie vyřazeno velké množství nemocných (viz obr. 1).
K měření hloubky bloku jsme použili standardizovanou techniku měření [5]. Upřednostnili jsme elektromyografické vyhodnocení svalové odpovědi před akcelerometrií, protože první z těchto metod je odolnější k pohybovým artefaktům. U všech nemocných jsme použili totální intravenózní anestezii v režimu počítačem řízené TCI s identickými cílovými plazmatickými hladinami anestetika (propofol) a opioidu (sufentanil). Nepodávali jsme volatilní anestetika, abychom vyloučili jejich vliv na hloubku relaxace. Sledovali jsme relativně zdravé nemocné (převážně ASA klasifikace 1 nebo 2). Získané výsledky proto nelze automaticky přenášet na pacienty anestezované odlišným způsobem (např. inhalační anestezie) nebo na nemocné jiných ASA kategorií.
V současnosti patří ROC k nejčastěji používaným intermediárním NMBAs. Obliba ROC pravděpodobně ještě vzroste s širší dostupností sugammadexu. Sugammadex jako SRBA (selective relaxant-binding agent) antagonizuje účinek rokuronia a vekuronia enkapsulací [28]. Tento mechanismus nezávisí na enzymech a z farmakologického pohledu je výhodnější než reverze pomocí inhibitoru cholinesterázy (neostigmin) [2, 29, 30]. Na rozdíl od neostigminu je však sugammadex mnohonásobně dražší [31]. Tato fakta vytvářejí racionální podklad pro hlubokou znalost farmakodynamiky ROC.
Závěr
- Účinek ROC je výrazně ovlivněn pohlavím a věkem.
- U žen je nástup účinku rychlejší, délka klinického trvání a interval do plného zotavení z bloku jsou delší než u mužů. Tyto rozdíly jsou dále potencovány stářím.
- Výrazná interindividuální variabilita v účinku ROC a současně nemožnost přesně určit hloubku bloku klinickým vyšetřením jsou důvodem pro doporučení peroperačně monitorovat nervosvalový přenos [32].
Poznámka: Výsledky práce byly publikovány v Biomedical Papers [33] (Adamus M et al. Influence of age and gender on the pharmacodynamic parameters of rocuronium during total intravenous anesthesia. Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub 2011; 155 : 233–240).
Poděkování. Práce vznikla za podpory grantových projektů IGA MZ ČR (ND7665-3/2003 a NS9618-4/2008).
Konflikt zájmů: Hlavní autor (dr. Adamus) je členem expertní skupiny pro svalová relaxancia (MSD). Tato studie neslouží komerčním cílům.
Do redakce došlo dne 6. 1. 2012.
Přijato do tisku dne 15. 1. 2012.
Adresa pro korespondenci:
Doc. MUDr. Milan Adamus, Ph.D.
KARIM Fakultní nemocnice
I. P. Pavlova 6
775 20 Olomouc
e-mail: milan.adamus@seznam.cz
Zdroje
1. Herold, I. Svalová relaxancia v anesteziologii a intenzivní péči. 1. vydání. Praha: Maxdorf, 2004, 268 s.
2. Lee, C. L., Katz, R. L. Clinical implications of new neuromuscular concepts and agents: So long, neostigmine! So long, sux! J. Crit. Care, 2009, 24, p. 43–49.
3. Lee, C. L. Goodbye Suxamethonium! Anaesthesia, 2009, 64 (S1), p. 73–81.
4. Mencke, T., Soltesz, S., Grundmann, U., Bauer, M., Schlaich, N., Larsen, R., Fuchs-Buder, T. Time course of neuromuscular blockade after rocuronium. A comparison between women and men. Anaesthesist, 2000, 49, p. 609–612.
5. Adamus, M, Gabrhelik, T, Marek, O. Influence of gender on the course of neuromuscular block following a single bolus dose of cisatracurium or rocuronium. Eur. J. Anaesthesiol., 2008, 25, p. 589–595.
6. Arain, S., Kern, S., Ficke, D., Ebert, T. Variability of duration of action of neuromuscular blocking drugs in elderly patients. Acta Anaesthesiol. Scand., 2005, 49, p. 312–315.
7. Adamus, M. Vliv věku na farmakodynamické vlastnosti cisatrakuria, rokuronia a vekuronia u mužů během totální intravenózní anestezie – prospektivní studie. Anest. intenziv. Med., 2010, 21, p. 78–84.
8. Booij, L. H. D. J., Drobnik, L. Variability in the effect of muscle relaxants. Factors involved in the pharmacodynamic profile of neuromuscular blocking agents. Part II. Anestezjologia i Ratownictwo, 2009, 3, p. 154–184.
9. Murphy, G. S., Szokol, J. W., Marymont, J. H., Greenberg, S. B., Avram, M. J., Vender, J. S. Residual neuromuscular blockade and critical respiratory events in the postanesthesia care unit. Anesth. Analg., 2008, 107, p. 130–137.
10. Fritscherova, S., Adamus, M., Dostalova, K., Koutna, J., Hrabalek, L., Zapletalova, J., Uvizl, R., Janout, V. Can difficult intubation be easily and rapidly predicted? Biomed. Pap. Med. Fac. Univ. Palacky Olomouc Czech Repub., 2011, 155, p. 165–172.
11. Cazalaa, J. B., Levron, J. C., Servin, F. Anesthetic agents used in TCI. Bibliographical study of anesthetic agents used in the Orchestra® Base Primea and Injectomat® TIVA Agilia. 2nd ed. Le Grand Chemin, Brezins (France): Fresenius Vial, 2009.
12. Fuchs-Buder, T., Claudius, C., Skovgaard, L. T., Eriksson, L. I., Mirakhur, R. K., Viby-Mogensen, J. Good clinical research practice in pharmacodynamic studies of neuromuscular blocking agents II: the Stockholm revision. Acta Anaesthesiol. Scand., 2007, 51, 789–808.
13. Donati, F. Onset of action of relaxants. Can. J. Anaesth., 1988, 35, p. S52 – 58.
14. Naguib, M., Kopman, A. F., Ensor, J. E. Neuromuscular monitoring and postoperative residual curarisation: a meta-analysis. Br. J. Anaesth., 2007, 98, p. 302–316.
15. Adamus, M., Bělohlávek, R., Vujčíková, M., Janásková, E. Vliv odlišných dávek rocuronia na jeho farmakodynamický profil: prospektivní studie. Anest. intenziv. Med., 2004, 15, p. 269–275.
16. Debaene, B., Plaud, B., Dilly, M. P., Donati, F. Residual paralysis in the PACU after a single intubating dose of nondepolarizing muscle relaxant with an intermediate duration of action. Anesthesiology, 2003, 98, p. 1042–1048.
17. Murphy, G. S., Brull, S. J. Residual neuromuscular block: lessons unlearned. Part I: definitions, incidence, and adverse physiologic effects of residual neuromuscular block. Anesth. Analg., 2010, 111, p. 120–128.
18. Viby-Mogensen, J., Claudius, C. Evidence-based management of neuromuscular block. Anesth. Analg., 2010, 111, p. 1–2.
19. Donati, F. Neuromuscular monitoring: what evidence do we need to be convinced? Anesth. Analg., 2010, 111, p. 6–8.
20. Eriksson, L. I., Sundman, E., Olsson, R., Nilsson, L., Witt, H., Ekbery, O., Kuylenstierna, R. Functional assessment of the pharynx at rest and during swallowing in partially paralyzed humans. Anesthesiology, 1997, 87, p. 1035–1043.
21. Berg, H., Roed, J., Viby-Mogensen, J., Mortensen, C. R., Engbaek, J., Skovgaard, L. T., Kristel, J. J. Residual neuromuscular block is a risk factor for postoperative pulmonary complications. A prospective, randomised, and blinded study of postoperative pulmonary complications after atracurium, vecuronium and pancuronium. Acta Anaesthesiol. Scand., 1997, 41, p. 1095–1103.
22. Sauer, M., Stahn, A., Soltesz, S., Noeldge-Schomburg, G., Mencke, T. The influence of residual neuromuscular block on the incidence of critical respiratory events. A randomised, prospective, placebo-controlled trial. Eur. J. Anaesthesiol., 2011, 28, p. 842–848.
23. Pleym, H., Spigset, O., Kharasch, E. D., Dale, O. Gender differences in drug effects: implications for anesthesiologists. Acta Anaesthesiol. Scand., 2003, 47, p. 241–259.
24. Soldin, O. P., Mattison, D. R. Sex differences in pharmacokinetics and pharmacodynamics. Clin. Pharmacokinet., 2009, 48, p. 143–157.
25. Naguib, M., Lien, A. C. Pharmacology of Muscle Relaxants and their Antagonists. In Miller, R.D. (editor). Miller’s Anesthesia. 7th ed. Philadelphia: Churchill-Livingstone, Elsevier. 2010, p. 897.
26. Bevan, D. R., Fiset, P., Balendran, P., Law-Min, J. C., Ratcliffe, A., Donati, F. Pharmacodynamic behaviour of rocuronium in the elderly. Can. J. Anaesth., 1993, 40, p. 127–132.
27. Sieber, F. E., Pauldine, R. Geriatric Anesthesia. In Miller, R. D. (editor). Miller’s Anesthesia. 7th ed. Philadelphia: Churchill-Livingstone, Elsevier. 2010, p. 2271.
28. Naguib, M., Brull, S. J. Sugammadex: a novel selective relaxant binding agent. Expert Rev. Clin. Pharmacol., 2009, 2, p. 37–53.
29. Kopman, A. F., Eikermann, M. Antagonism of non-depolarising neuromuscular block: current practice. Anaesthesia, 2009, 64 (S1), p. 22–30.
30. Caldwell, J. E. Clinical limitations of acetylcholinesterase antagonists. J. Crit. Care, 2009, 24, p. 21–28.
31. Kopman, A. F. Neostigmine versus sugammadex: which, when, and how much? Anesthesiology, 2010, 113, p. 1010–1011.
32. Miller, R. D., Ward, T. A. Monitoring and pharmacologic reversal of a nondepolarizing neuromuscular blockade should be routine. Anesth. Analg., 2010, 111, p. 3–5.
33. Adamus, M., Hrabalek, L., Wanek, T., Gabrhelik, T., Zapletalova, J. Influence of age and gender on the pharmacodynamic parameters of rocuronium during total intravenous anesthesia. Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub., 2011, 155, p. 233–240.
Štítky
Anesteziologie a resuscitace Intenzivní medicína
Článek Errata
Článek vyšel v časopiseAnesteziologie a intenzivní medicína
Nejčtenější tento týden
2012 Číslo 1- Jak souvisí postcovidový syndrom s poškozením mozku?
- Neodolpasse účinně snižuje pooperační bolest
- Neodolpasse jako ideální volba tam, kde je bolest provázena spasmem kosterního svalstva
- Optimalizace léčby pooperační bolesti snižuje nároky na zdravotní péči
- Použití Neodolpasse v indikaci pooperační bolesti
-
Všechny články tohoto čísla
- Kardiorelax 2011 – pětidenní dotazníková studie svalové relaxace během kardiochirurgických výkonů v České republice
- Errata
- Vliv věku a pohlaví na farmakodynamické vlastnosti rokuronia během totální intravenózní anestezie – prospektivní studie
- Propofol vs. sevofluran jako hlavní anestetikum u pacientů podstupujících coiling mozkového aneurysmatu – randomizovaná prospektivní studie
- Quo vadis, porodnická analgezie a anestezie v České republice?
- Kvalita a včasné komplikace pooperační epidurální analgezie po rozsáhlých výkonech
- Tromboprofylaxe a neuroaxiální anestezie v porodnictví
- Zásady bezpečné anesteziologické péče
- Doporučení pro léčbu toxické reakce po podání lokálních anestetik
- Peripartální život ohrožující krvácení
- Nejbližší oborové konference a setkání
- Současné členství v ČSIM a Evropské společnosti intenzivní medicíny
- Zápis z jednání výboru č. 5/2011
- Použití svalových relaxancií při celkové anestezii v operačních oborech – tříměsíční unicentrická studie v české regionální nemocnici
- Anesteziologie a intenzivní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Kvalita a včasné komplikace pooperační epidurální analgezie po rozsáhlých výkonech
- Tromboprofylaxe a neuroaxiální anestezie v porodnictví
- Doporučení pro léčbu toxické reakce po podání lokálních anestetik
- Použití svalových relaxancií při celkové anestezii v operačních oborech – tříměsíční unicentrická studie v české regionální nemocnici
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



