-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
Reklama„Low volume“ laparoskopická nefrektomie pro příbuzenskou transplantaci
Dostalík J., Guňková P., Martínek L., Guňka I., Mazur M., Samlík J., Foltys A.: „Low volume“ Laparoscopic Nephrectomy for Relative-to-Relative Transplantation
Aim:
Worldwide, the number of suitable cadaverous donors is limited. Therefore, as a solution for patients with chronic renal failure appears to extend the group of living donors of healthy individuals who voluntarily donate kidney to relatives or emotionally related recipients. Given the altruistic circumstances of these operations, the main monitored parameters are security for donors and excellent graft function for recipients. Currently published works show that minimally invasive technique can guarantee comparable results with open access in both monitored parameters. The aim of this study is to asses our results with laparoscopic assisted living donor nephrectomy for transplantation.Patients and Methods:
In retrospective study we analyzed data of patients in whom laparoscopic donor nephrectomy was performed on the Surgical Clinic, University Hospital Ostrava in the period from May 13, 2002 to June 30, 2010. Group of 34 donors were analyzed according to demographic characteristics (sex, age, ASA classification and BMI). From the perioperative data were monitored length of operation and warm ischemia, blood loss, frequency of intraoperative complications and conversion rate. In the postoperative period were evaluated in donors length of postoperative hospitalization, frequency of early and late reoperations, causes of morbidity and mortality, dynamics of the levels of creatinine and in the recipients was monitored 1-year survival of the graft.Results:
There were 14 men (41%) and 20 women (59%), median age was 48 years (25–77 years), BMI 26.9 (18.7–37.0), 53% of patients were ASA II, 44% ASA I, 1 patient (3%) ASA III. Median length of operation was 180 min (90–300 min), warm ischemia 120 s (58–240 s), blood loss 50 ml (30–1000ml). There was no conversion. Intraoperative complications occured in 3 donors (8.8%). The length of hospital stay was 7 days (3–26 days), morbidity rate was 14.7%, without mortality. Early reoperations were in 2 patients (5.9%), late reoperations were performed in 4 patients (11.8%). In donors an average increase of creatinine value was 35.5 μmol/l the first postoperative day. One-year graft survival in our cohort was 94.1%.Conclusion:
For patients with terminal renal insufficiency the living donor kidney transplantation offers possibility to shorten time in waiting list and to ensure a better graft function with its longer survival. Minimally invasive laparoscopic technique (we prefer transperitoneal approach), represents a safe alternative to open operation.Key words:
living donor – laparoscopic donor nephrectomy – kidney transplantation
Autoři: J. Dostalík; P. Guňková; L. Martínek
; I. Guňka; M. Mazur; J. Samlík; A. Foltýs
Působiště autorů: Chirurgická klinika FN Ostrava, přednosta: doc. MUDr. Jan Dostalík, CSc.
Vyšlo v časopise: Rozhl. Chir., 2011, roč. 90, č. 5, s. 293-297.
Kategorie: Monotematický speciál - Původní práce
Souhrn
Cíl:
Celosvětově je počet vhodných kadaverózních dárců omezený, proto se jako řešení pro pacienty s chronickým ledvinným selháním jeví rozšíření skupiny dárců o živé a zdravé jedince, kteří poskytují dobrovolně příbuzným či emocionálně spřízněným příjemcům jednu ledvinu. Vzhledem k altruistickým okolnostem těchto operací jsou hlavními sledovanými parametry bezpečnost operace pro dárce a excelentní funkce graftu u příjemce. V současnosti publikované práce ukazují, že miniinvazivní technika může zaručit srovnatelné výsledky s otevřeným přístupem v obou sledovaných parametrech. Cílem naší práce je zhodnotit výsledky laparoskopické nefrektomie pro příbuzenskou transplantaci.Pacienti a metody:
Retrospektivní studií jsme analyzovali data pacientů, u kterých byla na Chirurgické klinice FN Ostrava od 13. 5. 2002 do 30. 6. 2010 provedena laparoskopická dárcovská nefrektomie. Soubor 34 dárců byl analyzován stran základních charakteristik, tedy pohlaví, věku, zařazení do ASA klasifikace a BMI. Z peroperačních údajů byla sledována délka operace a teplé ischemie, krevní ztráta, četnost peroperačních komplikací a konverzí. V pooperačním období byla u dárců hodnocena délka pooperační hospitalizace, četnost časných a pozdních reoperací, jejich příčiny, morbidita a mortalita, dynamika hodnoty kreatininu a u příjemců bylo sledováno roční přežívání graftu.Výsledky:
V souboru bylo 14 mužů (41 %) a 20 žen (59 %), medián věku byl 48 let (25–77 let), BMI 26,9 (18,7–37,0), 53 % pacientů bylo zařazeno do ASA II, 44 % do ASA I, 1 pacient (3 %) do ASA III. Medián délky operace byl 180 min (90–300 min.), medián teplé ischemie byl 120 sekund (58–240 sekund), medián krevní ztráty byl 50 ml (30–1000 ml). Ani v jednom případě nebyla operace konvertována. Peroperační komplikace se vyskytly u 3 dárců (8,8 %). Medián délky hospitalizace byl 7 dnů (3–26), morbidita byla 14,7 %, mortalita 0 %. Časně byli reoperováni 2 pacienti (5,9 %), pozdní reoperace byla provedena u 4 pacientů (11,8 %). U dárců došlo v pooperačním období o průměrné navýšení hodnoty kreatininu o 35,5 μmol/l. Roční přežívání graftu bylo v našem souboru 94,1 %.Závěr:
Odběr ledvin k transplantačním účelům od žijících dárců je možností jak zkrátit u pacienta s terminální renální insuficiencí dobu na „čekací listině“ a zajistit tak lepší funkci graftu s jeho delším přežíváním. Jako bezpečná alternativa otevřeného výkonu se jeví operace provedená miniinvazivní laparoskopickou technikou v našem případě transperitoneálním přístupem.Klíčová slova:
žijící dárce – laparoskopická dárcovská nefrektomie – transplantace ledvinÚVOD
Celosvětově je počet vhodných kadaverózních dárců omezený, proto na „čekací listině“ narůstá počet nemocných s chronickým selháním ledvin. Jako východisko se jeví rozšíření skupiny případných dárců o živé a zdravé jedince, kteří poskytují dobrovolně příbuzným v horizontálním nebo vertikálním vztahu či emocionálně spřízněným příjemcům jednu ledvinu. Vzhledem k altruistickým okolnostem těchto operačních výkonů jsou bezpečnost operace pro dárce a excelentní funkce graftu u příjemce nejdůležitějšími sledovanými parametry. Nespornou výhodou je zkrácení doby na „čekací listině“ a možnost provedení transplantace ještě před úplným renálním selháním. Cenný je také průkaz lepších dlouhodobých výsledků v délce přežívání štěpu, odebraného od žijícího dárce, ve srovnání se štěpem od dárce kadaverózního [1]. V případě kadaverózních odběrů se uvádí pětileté přežívání graftu 78,93 % proti 90,21 % u štěpů od žijících dárců. Desetileté přežívání štěpu od kadaverózních dárců je 55,07 % proti 74,84 % od dárců žijících [2].
V České republice je podíl dárcovských nefrektomií od žijících jedinců 7,2 %. Vysoký je tento podíl například v Japonsku, kde dosahuje více než 80 % [3] s peroperační mortalitou donorů 0,02–0,03 % [3] a nutností hemodialýzy po dárcovství 0,70 % [3]. V Německu v roce 2005 byli zastoupeni živí dárci ve 32, 4 % ze všech provedených odběrů [4].
Celosvětově je dosud přibližně polovina všech dárcovských nefrektomií prováděna otevřenou technikou [5]. Ve snaze minimalizovat morbiditu spojenou převážně s lumbotomií a zlepšit tím pooperační výsledky u živých dárců se začaly stejně jako v ostatních oblastech chirurgie uplatňovat miniinvazivní techniky. Jsou představovány transperitoneálním či retroperitoneálním přístupem, výkon může být rukou asistovaný, laparoskopicky asistovaný i robotický. Ve většině publikovaných prací je preferovanou technikou transperitoneální laparoskopický přístup [6] se zastoupením konverzí 0–13,3 % [5, 6, 7, 8].
Poprvé byla laparoskopická nefrektomie pro transplantační účely u žijícího dárce provedena v roce 1995 Ratnerem v Johns Hopkins University Hospital v Baltimore [9].
V roce 1998 pak byl proveden první odběr ledviny u žijícího dárce technikou MALCH (Manuálně asistovaná laparoskopická chirurgie) [10]. Zastánci této techniky uvádějí kratší dobu learning curve [11, 12], lepší taktilní vjem, kratší operační čas [5] i délku teplé ischemie [5, 13] a zejména vyšší peroperační bezpečnost díky lepší kontrole renálních cév při nenadálém krvácení. V práci, kterou v roce 2007 publikoval Chin [5], technika manuálně asistované laparoskopické chirurgie zkrátila operační čas z 3,6 na 2,8 hodin a teplou ischemii z 230 s na 100 s. Další předností manuálně asistované techniky je zajištění dostatečně dlouhé cévní stopky [13, 14]. Krátká cévní stopka může totiž znamenat technický problém při samotné transplantaci a může být příčinou trombózy graftu [14].
MATERIÁL A METODA
Do retrospektivní studie bylo zařazeno celkem 34 pacientů, u kterých byl proveden laparoskopický odběr ledviny pro transplantační účely. Pacienti byli operováni na Chirurgické klinice FN Ostrava v období od 13. 5. 2002 do 30. 6. 2010. Dárci byli předoperačně vyšetřeni podle standardů České transplantační společnosti a podepsali informovaný souhlas.
Operační výkon u pacienta v lumbotomické poloze byl prováděn v celkové anestezii, během které byla zajištěna vysokoobjemová diuréza. Vzhledem k tomu, že ve shodě s většinou publikovaných prací byla k odběru upřednostňována levá ledvina, u většiny pacientů se tedy jednalo o polohu na pravém boku. U všech pacientů byl operační výkon proveden technikou MALCH (Manuálně asistovaná laparoskopická chirurgie) transperitoneálně při výši kapnoperitonea 10–12 mmHg. Preparace ledvinných cév a ozřejmění případných větví bylo provedeno s ohledem na předoperační angiografii. Ledvinná tepna byla izolována do místa odstupu z aorty, ledvinná žíla do místa ústí do dolní duté žíly. Ureter byl preparován do úrovně křížení s ilickými cévami a v tomto místě klipován a přerušen. Do této fáze byla operace prováděna čistě laparoskopicky. Aby nedocházelo k případné peroperační torzi již uvolněné ledviny, která je v této fázi fixována pouze cévami, byla přidána minilaparotomie ve střední čáře pod pupkem a zaveden LapDisc. Před uzavřením a protětím cév pomocí endoskopických staplerů byl podán celkově heparin. Po přerušení cév byla asistující rukou vyjmuta ledvina z dutiny břišní a předána transplantujícímu chirurgovi k zahájení proplachu pomocí 4° roztoku Eurocollins (Fresenius, Germany). Transplantace u příjemce byla prováděna standardní technikou.
Metodika statistického zpracování dat, získaných ze zdravotnické dokumentace Chirurgické, Anesteziologicko-resuscitační a Interní kliniky FN Ostrava, souvisela s jejich charakterem. Demografické a klinické charakteristiky souboru pacientů byly zpracovány pomocí metod popisné statistiky (medián, rozmezí, relativní četnost). Stejnou metodikou byly zpracovány peroperační a pooperační charakteristiky souboru. Dynamika hodnoty kreatininu byla porovnávána párovým Student t-testem. P menší než 0,05 bylo hodnoceno jako statisticky významný výsledek.
VÝSLEDKY
Do souboru bylo zařazeno celkem 34 pacientů, u kterých byla provedena laparoskopická nefrektomie k transplantačním účelům. Dárci byli operováni na Chirurgické klinice FN Ostrava v období od 13. 5. 2002 do 30. 6. 2010. Základní charakteristiky jejich souboru jsou uvedeny v tabulce 1. Věk pacientů a BMI jsou uvedeny jako medián a rozmezí.
Tab. 1. Demografické a klinické charakteristiky souboru dárců Tab. 1. Demographic and clinical characteristics of the donor group 
U žádného z dárců nemusel být manuálně asistovaný laparoskopický výkon konvertován. Data související s operačním výkonem ukazuje tabulka 2. Operační čas, délka teplé ischemie a krevní ztráta jsou uvedeny jako medián a rozmezí. Délka operace je uváděna v minutách (čas od kožního řezu po poslední kožní steh), délka teplé ischemie (čas od přerušení renální arterie do zahájení perfuze graftu) v sekundách, peroperační krevní ztráta v mililitrech a rovněž je uvedena četnost peroperačních komplikací v procentech. V průběhu operačního výkonu se vyskytly komplikace u 3 dárců, ve všech případech byly zvládnuty laparoskopicky, resp. technikou MALCH. Jednalo se o poranění sleziny, renální žíly a ureteru.
Tab. 2. Peroperační charakteristiky souboru dárců Tab. 2. Intraoperative characteristics of the donor group 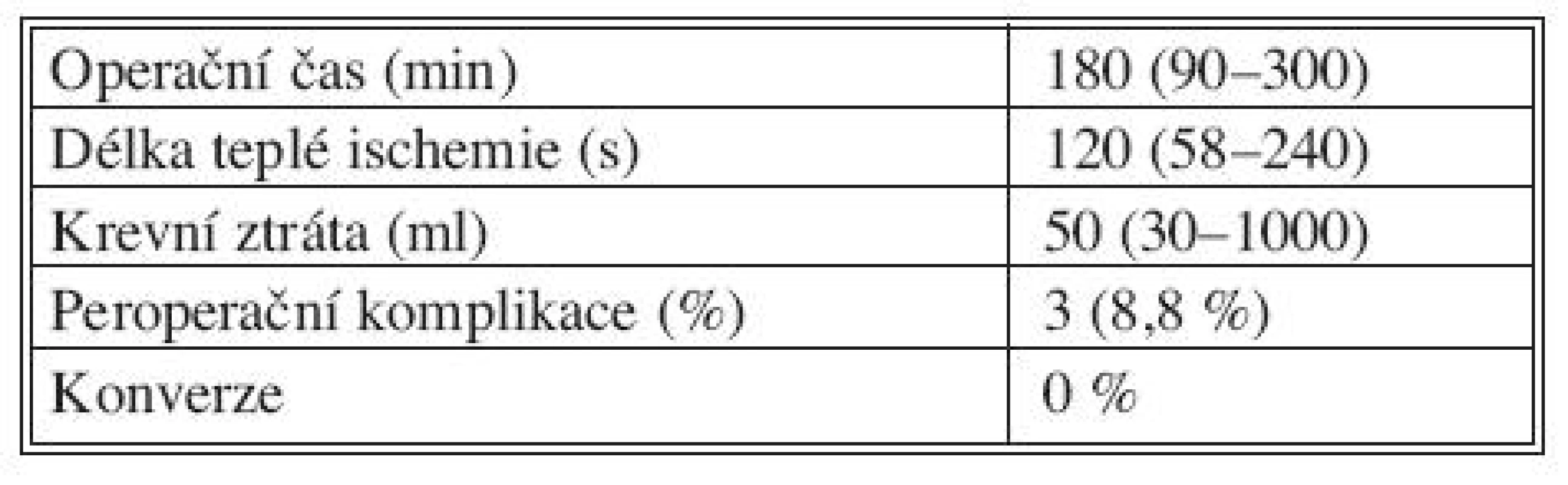
Z pooperačních charakteristik byla sledována délka pooperační hospitalizace ve dnech, četnost časných (do 30 dnů po operaci) a pozdních reoperací (Tab. 3, 4). Pozdní reoperace jsou navýšeny proti počtu pacientů (4 dárci) vzhledem k tomu, že 1 dárce byl reoperován dvakrát.
Tab. 3. Délka hospitalizace, reoperace časné a pozdní Tab. 3. Duration of hospitalization, early and late reoperations 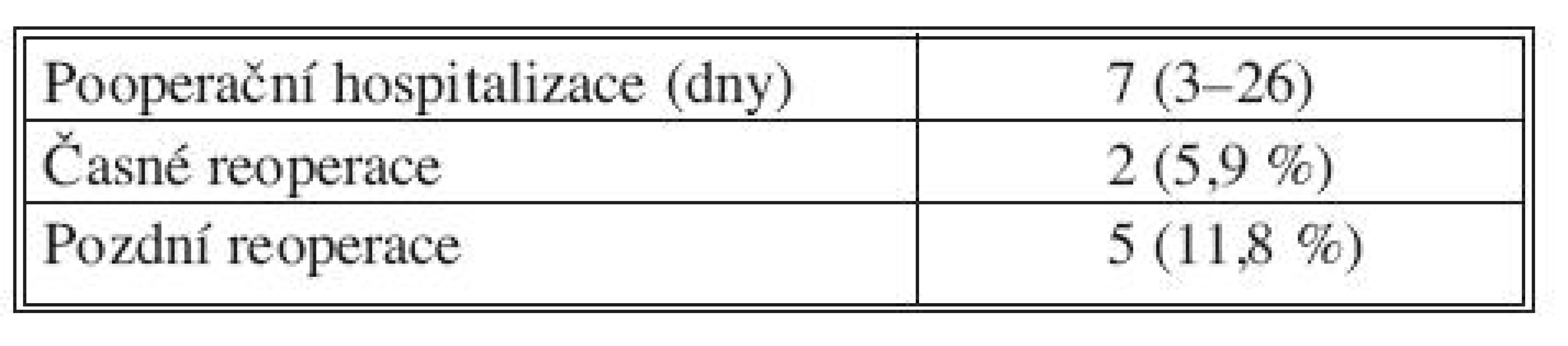
Tab. 4. Příčiny reoperací Tab. 4. Causes of reoperations 
Morbiditu a mortalitu ukazuje tabulka 5 a 6. Hodnocena byla časná (30denní) morbidita na základě všech zaznamenaných komplikací bez rozlišení, zda - li se u jednoho pacienta vyskytla jedna či více definovaných komplikací. Mortalita v námi sledovaném souboru pacientů byla 0%.
Tab. 5. Morbidita a mortalita Tab. 5. Morbidity and mortality 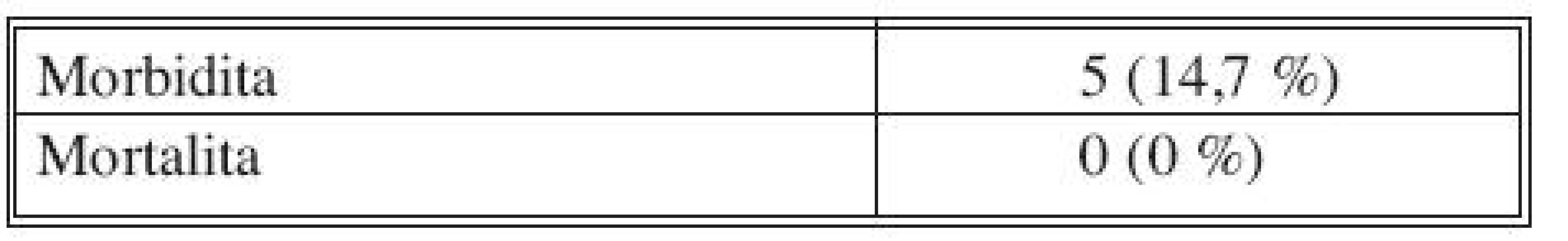
Tab. 6. Typy komplikací Tab. 6. Types of complications 
Dále byla sledována dynamika kreatininu v séru dárců (μmol/l). Srovnávána byla předoperační hodnota s hodnotou zjištěnou první pooperační den (Tab. 7). Hodnota kreatininu je uváděna jako medián a rozmezí. I když došlo ke statisticky významnému navýšení pooperační hodnoty kreatininu, tento nárůst není klinicky významný a u žádného z dárců nebylo nutno použít eliminačních metod.
Tab. 7. Dynamika hodnoty kreatininu Tab. 7. Dynamics of creatinine values 
U příjemců bylo sledováno roční přežívání graftu, které v našem souboru dosáhlo 94,1 %. U dvou pacientů byla popsána trombóza graftu (5,9 %), která si vyžádala časnou graftektomii. V jednom případě byla trombóza graftu způsobena paradoxní embolií při defektu síňového septa se současným trombofilním stavem, ve druhém případě došlo k trombóze na odchlípeném aterosklerotickém plátu renální arterie.
DISKUSE
V roce 1995 Ratner v Johns Hopkins University Hospital v Baltimore [9] poprvé provedl laparoskopickou nefrektomii pro transplantační účely u žijícího dárce. V roce 1998 [10] pak byl proveden první odběr ledviny u žijícího dárce technikou MALCH (Manuálně asistovaná laparoskopická chirurgie). V České republice byl tento typ výkonu proveden poprvé ve Fakultní nemocnici v Ostravě 13. 5. 2002 [15].
Zpočátku byla laparoskopická technika u nefrektomií pro transplantační účely vázána na ideální podmínky (nízké BMI, normální anatomie renálních cév, anatomicky výhodnější levá ledvina s delší renální žílou). Tyto limity jsou v dnešní době překonány, odběr lze provádět u obesních dárců, pravé ledviny i při předoperačním zobrazení vícečetných renálních tepen [16]. Práce, které byly publikovány v posledních letech [8], laparoskopický odběr považují za bezpečný „zlatý standard“ a nenalézají rozdíly v operačních časech a délce teplé ischemie u laparoskopických odběrů pravých a levých ledvin. Dokonce jsou pracoviště [17, 18], které k laparoskopickým odběrům preferují pravou ledvinu, kdy uvádějí kratší operační čas v důsledku snadnější mobilizace hepatální flexury a duodena bez rizika poranění sleziny, nižší riziko peroperačního krvácení vzhledem k tomu, že na pravé straně nadledvinná žíla a spermatická či ovariální žíla ústí nikoliv do renální žíly, ale přímo do dolní duté žíly. Dalším argumentem je obecně mírně nižší funkce pravé ledviny (o 5–10 %) oproti levé, takže dárci je ponechána ledvina výkonnější.
Nicméně, vzhledem k tomu, že celosvětově je stále přibližně polovina všech dárcovských nefrektomií prováděna otevřenou technikou [5] je důležité porovnat „klasický“ otevřený přístup z lumbotomie s relativně novými technikami miniinvazivními, kdy operační přístup může být transperitoneální či retroperitoneální, rukou asistovaný, laparoskopicky asistovaný i robotický. Většina v současnosti publikovaných studií prokázala, že miniinvazivní dárcovská nefrektomie je stejně bezpečná jako u otevřeného přístupu [6] při zachování všech obecně známých výhod v důsledku minimalizace chirurgického traumatu. Slibnou alternativou transperitoneálního laparoskopického přístupu je přístup retroperitoneoskopický s menším rizikem poranění střeva a vzniku hernie v jizvě. Nevýhodou je zmenšení operačního pole.
V případě dárcovských nefrektomií z lumbotomie jsou nejčastější komplikace právě ve vztahu k operační ráně, jako jsou ranná infekce, vytvoření hernie, chronické bolesti v ráně a rozvoj ileózního stavu v časném i pozdním pooperačním období. Rovněž plicní komplikace jako atelektáza, pneumotorax či edém plic a flebotrombóza se častěji vyskytují ve skupině otevřených dárcovských nefrektomií [6]. Obecně je literárně uváděna četnost komplikací spojených s odběrem ledviny z lumbotomie 3–38 % [6, 7].
Laparoskopický odběr ledviny pro transplantační účely je spojen s komplikacemi v rozmezí 5–26 % [5, 6, 7, 13]. Mezi komplikace, které jsou v literatuře udávány, se řadí poranění sleziny, střeva a střevního závěsu, lacerace omenta, devaskularizace ureteru, hematomy v břišní stěně, vznik pankreatické píštěle, chylózní leak a komplikace v souvislosti s použitím staplerů a dále při manipulaci s ledvinou, kdy může dojít k poškození graftu kompresí či lacerací parenchymu. Samozřejmě větší část těchto výše zmíněných komplikací se může vyskytnout i v případě otevřeného přístupu. Pooperačně může dojít ke vzniku hernie v minilaparotomii či v incizi po trokaru, které mohou být společně s adhezemi nebo vzniklým defektem v mezokolon příčinou ileózního stavu.
Nejčastější peroperační komplikací u obou technik odběru je krvácení, nejčastěji z lumbálních žil, renální žíly nebo artérie. Krvácení tvoří 93,1 % všech peroperačních komplikací [5]. Při hodnocení peroperační krevní ztráty část publikovaných prací nenalezla statisticky významný rozdíl při porovnání obou technik [6].
Důležitým hodnoceným parametrem je i výsledná funkce a životnost štěpu u příjemce. Jsou práce, ve kterých nebyl prokázán statisticky významný rozdíl v četnosti akutních rejekcí u laparoskopicky odebraných štěpů (2–30 %) ve srovnání s otevřeně odebranými (3–44 %) [6]. Roční přežívání graftu po laparoskopickém odběru je 93–100 %, v případě otevřeného odběru pak 91–100 % [6]. V souladu s výše uvedeným, roční přežívání graftu v našem souboru dosáhlo 94,1 %. Recentní práce udávají dokonce lepší výsledky v délce přežívání štěpu, odebraného od žijícího dárce, ve srovnání se štěpem od dárce kadaverózního [1]. V případě kadaverózních odběrů se uvádí pětileté přežívání graftu 78,93 % proti 90,21 % u štěpů od žijících dárců. Desetileté přežívání štěpu od kadaverózních dárců je 55,07 % proti 74,84 % od dárců žijících [2].
V roce 2008 byla Nanidisem publikována metaanalýza [19], zahrnující 6594 pacientů ze 73 studií, z nichž bylo 3751 (57 %) operováno laparoskopicky a 2843 (43 %) otevřenou technikou. I když laparoskopický přístup znamenal průměrně o 52 minut delší operační čas a delší dobu teplé ischemie, neodrazilo se to negativně na funkci graftu. Dárci z laparoskopické skupiny byli kratší dobu hospitalizováni (o 1,58 dne) s nižší četností pooperačních komplikací (13,7 %) ve srovnání s dárci, u kterých byl odběr proveden z lumbotomie (16,4 %). Četnost reoperací se nelišila v obou skupinách, peroperační krevní ztráta byla nižší ve skupině miniinvazivně operovaných. Srovnatelné byly i výsledky u příjemců, kdy u laparoskopicky odebraných štěpů byla nefunkčnost po roce 4,2 % a u otevřeně odebraných štěpů 4,8 %.
Důležité je také zjištění, že i „low volume“ laparoskopická nefrektomie pro příbuzenskou transplantaci, pokud je realizována erudovaným laparoskopickým chirurgem, představuje bezpečně a kvalitně provedený odběr ledviny od žijících dárců [7]. Příkladem může být soubor 17 pacientů za 2 roky, které publikoval Duchene [20] či soubor 12 pacientů za 3 roky, který presentoval Dalla Valle [21]. Analýza těchto malých souborů přinesla podobné výsledky jako zpracování dat našeho souboru pacientů.
ZÁVĚR
Odběr ledvin k transplantačním účelům od žijících příbuzných či emocionálně spřízněných dárců je možností jak u pacientů s terminální renální insuficiencí zkrátit dobu na „čekací listině“ a zajistit tak lepší funkci graftu s jeho delším přežíváním. Jako minimálně stejně bezpečná alternativa otevřeného výkonu se jeví operace provedená miniinvazivní laparoskopickou technikou v našem případě transperitoneálním přístupem.
Seznam zkratek:
- ASA – předoperační klasifikace pacientů Americké společnosti anesteziologů (American Society of Anesthesiologists)
- BMI – Body Mass Index
- MALCH – Manuálně asistovaná laparoskopická chirurgie
MUDr. Lubomír Martínek
Odboje 1164/4
739 32 Vratimov
e-mail: lubomir.martinek@fnspo.cz
Zdroje
1. Drognitz, O., Donauer, J., Kamgang, J., et al. Living - donor kidney transplantation: the Freiburg experience. Langenbecks Arch. Surg., 2007; 392 : 23–33.
2. Pacovský, J., Navrátil, P., Baker, K., et al. Trasplantace ledvin od žijících dárců. Urologie pro praxi, 2004; 3 : 101–104.
3. Masahiko, O., Akioka, K., Nobori, S., et al. Short - and long - term donor outcomes after kidney donation: analysis of 601 cases over a 35 - year period at Japanese single center. Transplantation, 2009, 87 : 419–423.
4. Paul, A., Treckmann, J., Gallinat, A., et al. Current concepts in transplant surgery: laparoscopic living donor of the kidney. Langenbecks Arch. Surg., 2007, 392 : 501–509.
5. Chin, E. H., Hazzan, D., Herron, D. M., et al. Laparoscopic donor nephrectomy – intraoperative safety, immediate morbidity and delayed complications with 500 cases. Surg. Endosc., 2007; 21 : 521–526.
6. Tooher, R. L., Rao, M. M., Scott, D. F., et al. A systematic review of laparoscopic live - donor nephrectomy. Transplantation, 2007; 78(3): 404–414.
7. Saad, S., Paul, A., Treckmann, J., et al. Laparoscopic live donor nephrectomy: Are ten cases per year enough to reach the quality standarts? A report from a single small-volume transplant center. Surg. Endosc., 2010; 24 : 594–600.
8. Saad, S., Paul, A., Treckmann, J., et al. Laparoscopic live donor nephrectomy for right kidneys: Experience in a German community hospital. Surg. Endosc., 2008; 22 : 674–678.
9. Ratner, L. E., Ciseck, L. J., Moore, R. G., et al. Laparoscopic live donor nephrectomy. Transplantation, 1995; 60 : 1047–1049.
10. Wolf, J. S., Tchetgen, M. B., Merion, R. M. Hand-assisted laparoscopic live donor nephrectomy. Urology, 1998; 52(5): 885–887.
11. Bemelman, W. A., van Doorn, R. C., de Wit, L. T., et al. Hand-assisted laparoscopic donor nephrectomy. Ascending the learning curve. Surg. Endosc., 2001; 15 : 442–444.
12. Buell, J. F., Hanaway, M. J., Potter, S. R., et al. Hand-assisted laparoscopic living - donor nephrectomy as an alternative to traditional laparoscopic living - donor nephrectomy. Am. J. Transplant., 2002; 2 : 983–988.
13. Dolce, Ch. J., Keller, J. E., Walters, K. Ch., et al. Laparoscopic versus open live donor nephrectomy: outcomes analysis of 266 consecutive patients. Surg. Endosc., 2009; 23 : 1564–1568.
14. Oyen, O., Andersen, M., Mathisen, L., et al. Laparoscopic versus open living - donor nephrectomy: experiences from a prospective, randomized, single - center study focusing on donor safety. Transplantation, 2005; 79 : 1236–1240.
15. Dostalík, J., Samlík, J., Martínek, L., et al. Manuálně asistovaná laparoskopická nefrektomie od živého dárce. Rozhl. Chir., 2003; 82(3): 188–191.
16. Su, L. M., Ratner, L. E., Montgomery, R. A., et al. Laparoscopic live donor nephrectomy: trends in donor and recipient morbidity following 381 consecutive cases. Ann. Surg., 2004; 240 : 358–363.
17. Berends, F. J., Den Hoed, P. T., Bonjer, H. J., et al. Technical considerations and pitfalls in laparoscopic live donor nephrectomy. Surg. Endosc., 2002; 16 : 893–898.
18. Sawatzky, M., Altaf, A., Ellsmere, J., et al. Is right laparoscopic donor nephrectomy right? Surg. Endosc., 2009; 23 : 1321–1325.
19. Nanidis, T. G., Antcliffe, D., Kokkinos, C. Laparoscpic versus open live donor nephrectomy in renal transplantation: a meta - analysis. Ann. Surg., 2008; 247 : 58–70.
20. Duchene, D. A., Johnson, D. B., Li, S., et al. Laparoscopic donor nephrectomy at a low volume living donor transplant center: successful outcomes can be expected. J. Urol., 2003; 170 : 731–733.
21. Dalla Valle, R., Mazzoni, M. P., Capocasale, E., et al. Laparoscopic donor nephrectomy: short learning curve. Transplant. Proc., 2006; 38 : 1731–1733.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2011 Číslo 5- Strava bohatá na arginin a prolin slibuje urychlení hojení ran u diabetických pacientů
- Úloha růstového faktoru TGF-β v procesu hojení ran
- Topicky aplikovaný propolis může urychlovat hojení diabetických bércových vředů
- HemaGel jako moderní prostředek vlhkého hojení ran
- Perorální antivirotika jako vysoce efektivní nástroj prevence hospitalizací kvůli COVID-19 − otázky a odpovědi pro praxi
-
Všechny články tohoto čísla
- Epidemiológia defektov neurálnej rúry
- Chirurgická léčba symptomatických obratlových hemangiomů
- Mnohočetný myelom páteře a jeho chirurgická léčba
- Mediastinální cysty, chirurgické řešení
- Caroliho nemoc – dilatace intrahepatálních žlučových cest
- Mohou nádorové markery předpovídat výsledek embolizace větve portální žíly u nemocných s primárně inoperabilním nádorem jater?
- Perforace žaludku patnáctileté dívky, způsobená objemným trichobezoárem–Rapunzelin syndrom
- „Low volume“ laparoskopická nefrektomie pro příbuzenskou transplantaci
- Uskřinutí akcesorního orgánu břišní dutiny jako neobvyklá peroperační diagnóza – kazuistika
- Pilonidální sinus – chirurgická léčba na našem pracovišti
- Intratorakální struma – nediagnostikovatelná – přece odoperovaná
- Augmentace dekompresivní kraniektomie obvazovou textilií COM 30 v terapii refrakterní nitrolební hypertenze – kazuistika
- Památce prof. MUDr. Jaroslava Mayzlíka, CSc.
- Zápis z Redakční rady časopisu Rozhledy v chirurgii
- Několik slov k imprimatur a ke článku „Přednosti klasického operačního přístupu v chirurgické léčbě plicních metastáz“ (Rozhl. Chir., 2011, roč. 90, č. 3, s. 162–165).
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Pilonidální sinus – chirurgická léčba na našem pracovišti
- Caroliho nemoc – dilatace intrahepatálních žlučových cest
- Chirurgická léčba symptomatických obratlových hemangiomů
- Mediastinální cysty, chirurgické řešení
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



