-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Výsledky léčby mozkových tumorů stereotaktickou radioterapií a radiochirurgií
Therapeutic Results of the Treatment Brain Tumors Using Radiosurgery and Stereotactic Radiotherapy
Background:
We reviewed the results of treatment of patiens treated with stereotactic radiation methods in our department.Material and methods:
Patients with primary brain tumor or brain metastases underwent CT and MR examination. Then they were treated on X knife in the Clinic of Radiation Oncology in Masaryk Memorial Cancer Institute Brno.Results:
A total of 101 patients with primary brain tumors underwent stereotactic treatment. These were mainly meningeomas, high-grade gliomas and low-grade gliomas. In 37% of cases patients underwent reiradiation. Stereotactic radiosurgery was applied with a median dose of 18 Gy. Hypofrakcionated stereotactic radiotherapy was applied at a doses of mostly 5 × 5 Gy. Total toxicity of treatment was low: 8% acute G1, late toxicity in 1% of cases. In the whole group achieved partial remission 10 patients (9,9%). One patient had complete remission (0,99%). It was a diagnosis of pituitary adenoma. In 69 patients stable disease was observed (68,3%) and 12 patients had progression (11,88%). Median follow up the entire group was 22,4 months. A statistically significant difference in survival was found in the comparison of different diagnosis, patiens who recieved prior radiotherapy and patiens without previous irradiation. Another significant difference in survival was observed compared to patients treated with stereotactic treatment or stereotactic radiosurgery and the size of the tumor volume larger / smaller 10 cm3. In the group with brain metastases there were 56 patients. In 10% of cases preceded radiotherapy neurosurgical performance. Twenty four patients underwent cranial irradiation entire dose of 30 Gy. Median stereotactic radiosurgery dose was 20 Gy, the application of stereotactic treatment were mostly of 5 × 5 Gy. G1 acute toxicity occurred in 2 patients (3.8%), grade G2 in one patient (1.9%). Late toxicity was observed in 2 patients (one G1 and one G3). Complete remission was achieved in 4 patients (7.1%), partial remission in 27 patients (48.2%), stable disease in 9 (16.1%) and progression was observed in 5 patients (8.9%). Median follow-up the entire group was 13.3 months. There was no statistically significant difference in survival with respect to gender, age, KI, irradiation of the whole brain or type of treatment used. Patients who have undergone neurosurgery prior to irradiation had no difference in survival compared to patients without surgery, but the time to progression was significantly longer (p = 0.016).Conclusion:
Stereotactic radiation methods are part of modern radiotherapy. Their indication is necessary to consider with regard to the benefit of the patient. Quality equipment radiotherapy department and trained personnel are the condition for their correct using.Key words:
radiosurgery – brain neoplasms – locoregional neoplasm recurrence – stereotactic radiotherapy
Autoři: H. Doleželová 1; L. Hynková 1; P. Pospíšil 1
; T. Kazda 1; P. Šlampa 1
; I. Čoupková 1; I. Šiková 2; P. Fardus 3; T. Svoboda 4; J. Garčic 5; M. Vrzal 5; I. Selingerová 6; I. Horová 6
Působiště autorů: Klinika radiační onkologie LF MU a MOÚ Brno 1; Neurologická ambulance MOÚ Brno 2; Neurochirurgická klinika LF MU a FN Brno 3; Klinika komplexní onkologické péče LF MU a MOÚ Brno 4; Oddělení radiologické fyziky MOÚ Brno 5; Ústav matematiky a statistiky PřF MU Brno 6
Vyšlo v časopise: Klin Onkol 2012; 25(6): 445-451
Kategorie: Původní práce
Práce byla podpořena Evropským fondem pro regionální rozvoj a státním rozpočtem České republiky (OP VaVpI – RECAMO, CZ.1.05/2.1.00/03.0101).
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do bi omedicínských časopisů.
Souhrn
Východiska:
V práci jsou zhodnoceny výsledky terapie pacientů léčených stereotaktickými ozařovacími metodami na našem pracovišti.Materiál a metody:
Pacienti s primárními mozkovými nádory a s mozkovými metastázami podstoupili CT a MRI vyšetření a následně stereotaktickou léčbu na X noži.Výsledky:
Celkem 101 pacientů s primárním mozkovým nádorem podstoupilo stereotaktickou léčbu. Jednalo se především o meningeomy, high-grade gliomy a low-grade gliomy. V 37 % případů se jednalo o reiradiaci. Stereotaktická radiochirurgie byla aplikována s mediánem dávky 18 Gy. Frakcionovaná stereotaktická radioterapie byla aplikována nejčastěji v dávce 5 × 5 Gy. Celková toxicita léčby byla nízká: akutní stupeň G1 v 8 %, pozdní toxicita v 1 % případů. V celém souboru dosáhlo parciální remise 10 pacientů (9,9 %). Jeden pacient měl kompletní remisi (0,99 %). Jednalo se o diagnózu adenomu hypofýzy. U 69 pacientů byla zaznamenána stabilizace onemocnění (68,3 %), u 12 pacientů byla progrese onemocnění (11,88 %). Celkově došlo k progresi u 38 pacientů s mediánem doby do progrese 6,48 měsíce. Medián sledování celého souboru byl 22,4 měsíce. Statisticky významný rozdíl v přežití byl zjištěn v porovnání různých diagnóz; u pacientů, kteří podstoupili předchozí radioterapii a pacientů bez předchozího ozáření. Další významný rozdíl v přežití byl zjištěn v porovnání pacientů léčených stereotaktickou radioterapií nebo stereotaktickou radiochirurgií a při velikosti nádorového objemu větší/menší 10 cm3. Ve skupině s mozkovými metastázami se jednalo o 56 pacientů. V 10 % případů předcházel radioterapii neurochirurgický výkon. Celkem 24 pacientů podstoupilo ozáření celé mozkovny v dávce 30 Gy. Medián dávky stereotaktické radiochirurgie byl 20 Gy; při aplikaci stereotaktické radioterapie se jednalo nejčastěji o dávku 5 × 5 Gy. Akutní toxicita stupně G1 se objevila u 2 pacientů (3,8 %), stupeň G2 u jednoho pacienta (1,9 %). Pozdní toxicita byla zjištěna u 2 pacientů, u jednoho G1 a u druhého G3. Kompletní remise bylo dosaženo u 4 pacientů (7,1 %), parciální remise byla u 27 pacientů (48,2 %), stabilizace onemocnění u 9 (16,1 %) a progrese byla zaznamenána u 5 pacientů (8,9 %). Medián sledování celého souboru byl 13,3 měsíce. Nebyl zjištěn statisticky významný rozdíl v přežití s ohledem na pohlaví, věk, KI, ozáření celé mozkovny či typ použité léčby. Pacienti, kteří podstoupili před ozařováním neurochirurgický zákrok, nevykazovali rozdíl v přežití oproti pacientům bez operace, ale jejich doba do progrese byla statisticky významně delší (p = 0,016).Závěr:
Stereotaktické ozařovací metody jsou součástí moderní radioterapie. Jejich indikaci je nutné dobře zvažovat s ohledem na prospěch pacienta. K jejich použití je nutné kvalitní vybavení radioterapeutického pracoviště a vyškolený personál.Klíčová slova:
radiochirurgie – mozkové nádory – lokoregionální rekurence – stereotaktická radioterapieÚvod
Stereotaktické ozařovací metody nabízejí možnost aplikace vysoké dávky záření do malého objemu s velkým spádem dávky do okolí. Nejvíce se uplatňují při ozařování mozkových lézí. Na prvním místě léčby jde především o mozkové metastázy. Dále lze stereotakticky ozářit primární mozkové tumory, jako jsou gliomy, meningeomy, neurinomy akustiku či tumory hypofýzy, ale také arteriovenózní malformace. Radiochirurgie (SRS) připomíná chirurgický výkon jednorázovou aplikací. Při frakcionované stereotaktické radioterapii (SRT) je celková dávka rozdělena do několika frakcí zpravidla akcelerovaně, s vyšší jednotlivou dávkou. Oproti konformní radioterapii mají tyto metody výhodu nižšího rizika nežádoucích účinků [1–4].
Metodika a zpracování
Pacienti, kteří podstoupili stereotaktické ozáření, byli pro tuto léčbu doporučeni multioborovou komisí pro mozkové nádory. Pacienti byli seznámeni s nežádoucími účinky léčby a podepsali informovaný souhlas. Podstoupili plánovací CT a MRI vyšetření. Plánování a zakreslení cílového objemu a kritických struktur bylo provedeno v plánovací části Brain--Lab systému pro stereotaktické ozařování ve spolupráci diagnostika, neurochirurga a radioterapeuta. Pacienti byli ozářeni na lineárním urychlovači s mikrokolimátorem (X nůž) fotonovým svazkem energií 6 MV. Po léčbě byli sledováni na ambulanci Kliniky radiační onkologie, neurologické ambulanci MOÚ a v pravidelných intervalech byli vyšetřováni magnetickou rezonancí.
Statistické zpracování bylo provedeno ve spolupráci s Ústavem matematiky a statistiky Přírodovědecké fakulty Masarykovy univerzity v Brně. Byl použit program Matlab, Kaplan-Meierova funkce přežití a Coxův model [5].
Výsledky
Na Klinice radiační onkologie Masarykova onkologického ústavu v Brně bylo od července 2004 do ledna 2012 ozářeno 101 pacientů s diagnózou primárního mozkového nádoru a 56 pacientů s mozkovými metastázami. Obě skupiny byly zpracovány samostatně.
Primární mozkové nádory
Medián věku pacientů s primárním mozkovým nádorem byl 56 let. Poměr zastoupení mužů a žen byl přibližně stejný, 53 žen a 48 mužů. Histologicky byl nejčastěji zastoupen meningeom (48,5 %), dále pak high-grade gliomy (26 %). Zastoupení jednotlivých diagnóz je uvedeno v tabulce (tab. 1). Většina nádorů (74 případů) byla uložena supratentoriálně (73,26 %). Infratentoriálně bylo uloženo 22 tumorů. Pět nádorů prorůstalo supra i infratentoriálně.
Tab. 1. Zastoupení diagnóz primárních nádorů mozku. 
Medián sledování pacientů s primárním mozkovým nádorem byl 22,4 měsíce. Většina pacientů měla celkový stav KI větší 80 % (72,6 %). Stav KI nižší 80 % mělo 21 % pacientů.
Předchozí radioterapie na mozkovnu byla aplikována u 37 pacientů (37 %), takže se při použití stereotaktické radioterapie jednalo o reiradiaci. Průměrná dávka předchozí radioterapie byla 56 Gy. Nejčastěji byli předchozím ozařováním léčeni pacienti s high-grade gliomy – 23 pacientů (64 %), dále pak 8 pacientů s low-grade gliomy (22 %) a dva pacienti s meningeomy. Všichni uvedení pacienti podstoupili nejdříve zevní 3D konformní radioterapii na lineárním urychlovači.
Medián nádorového objemu GTV při aplikaci stereotaktického ozařování byl 4,82 cm3. Nejmenší objem dosahoval 0,01 cm3 a největší objem GTV byl 86,43 cm3.
Dvacet čtyři pacientů, kteří podstoupili SRS, mělo medián dávky 18 Gy (12,5–40 Gy). Tito pacienti měli nejčastěji diagnózu meningeomu (66 %), u dvou pacientů se jednalo o high-grade gliom a low-grade gliom.
Sedmdesát šest pacientů bylo ozářeno technikou SRT s mediánem dávky 25 Gy (12–58 Gy). Jednalo se především o pacienty s meningeomem (43 %) a high-grade gliomem (31 %). Průměrný počet 5 frakcí byl s mediánem dávky 5 Gy. Plánovací referenční izodóza měla rozpětí od 70 do 100 % s mediánem 100 %. Nejčastěji byla použita kombinace 10 polí (6–23 polí) s jedním společným izocentrem.
Zjištěná toxicita léčby byla mírná, resp. minimální. Akutní toxicita G1 byla zaznamenána u 8 pacientů (8 %), pozdní jen u jednoho pacienta (1 %). Radionekróza při MRI vyšetření byla diagnostikována u 4 pacientů (3,9 %).
V celém souboru dosáhlo PR (parciální remise) 10 pacientů (9,9 %). Jeden pacient měl kompletní remisi (0,99 %). Jednalo se o diagnózu adenomu hypofýzy. U 69 pacientů byla zaznamenána stabilizace onemocnění (stable disease – SD: 68,3 %), u dvanácti došlo k progresi onemocnění (11,88 %; PD). U 9 pacientů nebylo možné posoudit výsledek při první kontrole, většinou pro špatný stav pacienta.
Celkově došlo k progresi u 38 pacientů s mediánem doby do progrese 6,48 měsíce (1,4–71,63 měsíce). Progrese onemocnění byla nejčastěji dále léčena chemoterapií v monoterapii nebo jen symptomatickou léčbou. U tří pacientů byla provedena reiradiace a u 4 nemocných došlo k chirurgickému řešení recidivy.
Při poslední kontrole přežívalo 59 pacientů (58,4 %). Čtyřicet dva pacientů zemřelo s mediánem přežití 11,5 měsíce.
Byla provedena také analýza přežití pro celý soubor i pro jednotlivé diagnózy (graf 1), nejlepší výsledky byly zaznamenány u pacientů s meningeomem, nejhorší přežití vykazovali pacienti s diagnózou high-grade gliomu.
Graf 1. Kumulativní podíl přežívajících (Kaplan-Meier). 
Dále byly testovány různé nulové hypotézy. Dle testovací analýzy není rozdíl v přežití mezi ženami a muži ani mezi pacienty staršími nebo mladšími 50 let. Stejně tak není rozdíl v přežití podle lokalizace tumoru či podle celkového stavu (KI).
Statisticky významný rozdíl byl zjištěn v případě porovnání pacientů s plánovacím nádorovým objemem (GTV) menším/větším 10 cm3 (p = 0,001). Další statisticky významný rozdíl byl v případě srovnání léčby radiochirurgií a stereotaktickou radioterapií (p = 0,009); lepších výsledků bylo dosaženo u pacientů léčených stereotaktickou radioterapií (frakcionované ozařování). Pacienti, kteří podstoupili předchozí radioterapii, měli horší přežití než pacienti bez předchozího ozařování mozkovny (p = 0,00047). Funkce přežití také ukázala statisticky významný rozdíl při porovnávání jednotlivých diagnóz (p = 0,00002) – nejlepší pro meningeomy, nejhorší přežití pro pacienty s high-grade gliomy (graf 1).
Mozkové metastázy
U pacientů s mozkovými metastázemi byl medián věku 60 let. Častěji byly zastoupeny ženy (55 % případů), muži byli v 45 % případů. Zastoupení jednotlivých primárních diagnóz je v tabulce (tab. 2). Většina pacientů měla diagnostikovánu jednu metastázu. V 75 % případů byly metastázy uloženy supratentoriálně. V deseti případech byly diagnostikovány infratentoriálně a u čtyř pacientů byly metastázy nalezeny supra i infratentoriálně. Většina pacientů měla klinický stav KI větší 80 %.
Tab. 2. Zastoupení primárních diagnóz ve skupině mozkových metastáz. 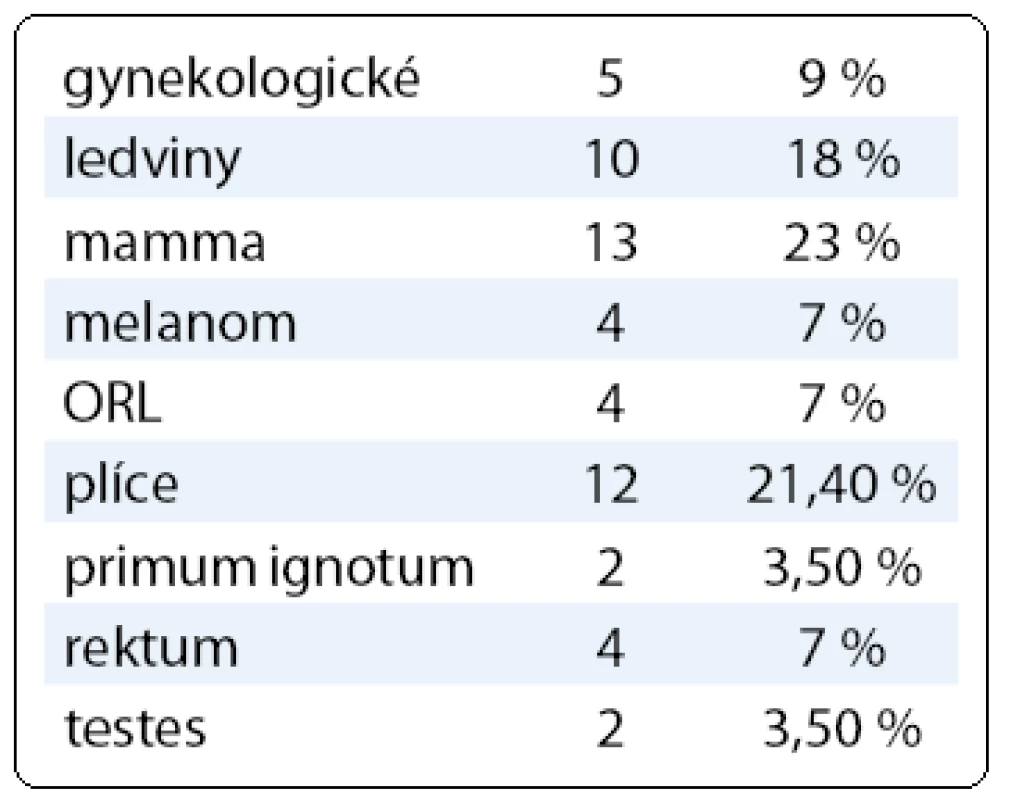
Medián objemu metastáz při plánování radioterapie byl 3,36 cm3 (0,01–22,93 cm3). V době diagnózy mozkových metastáz byly u 68 % pacientů zjištěny i jinde lokalizované metastázy. Osmnáct pacientů mělo pouze mozkové metastázy. U pacientů s metastázami ve více lokalizacích bylo v 21 případech toto onemocnění stabilizované, u 16 z nich byla zaznamenána progrese onemocnění.
U šesti pacientů (10 %) předcházela radioterapeutickou léčbu mozkových metastáz operace – neurochirurgická exstirpace metastázy. Dvacet čtyři pacientů před stereotaktickou léčbou bylo ozářeno na celý mozek s mediánem dávky 30 Gy.
Stereotaktická léčba byla zahájena s mediánem doby čekání 28 dní od stanovení diagnózy. Typy použité stereotaktické léčby jsou v tabulce (tab. 3). V případě jednoho pacienta byl výkon invazivní fixace pomocí stereotaktického rámu zatížen rizikem akutních komplikací při neurochirurgickém výkonu fixace. Tento pacient byl jednorázově stereotakticky ozářen s fixací ve stereotaktické masce. Tento výkon jsme označili jako modifikovaná radiochirurgie. Dávky radiochirurgie se pohybovaly od 10 do 28 Gy s mediánem dávky 20 Gy. Při aplikaci SRT byl medián dávky 24,5 Gy s rozmezím od 15 do 51 Gy. Nejčastěji byla dávka plánována na 80% izodózu s mediánem počtu polí 10 (6–18 polí) a s jedním nebo dvěma izocentry.
Tab. 3. Typy použité radioterapie v léčbě mozkových metastáz. 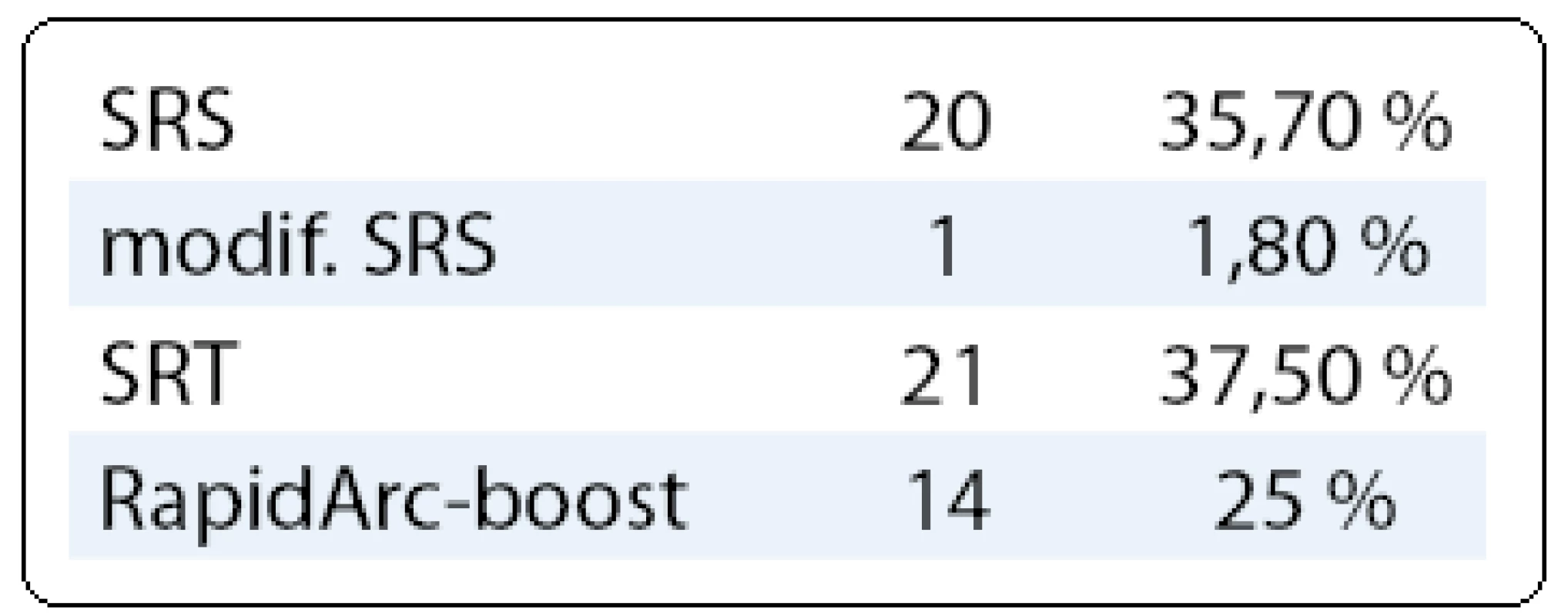
Současně byla u 11,7 % pacientů aplikována systémová léčba. Toxicita léčby byla mírná. Akutní toxicita G1 se objevila u 2 pacientů (3,8 %), stupeň G2 u jednoho pacienta (1,9 %). Devadesát čtyři procent pacientů neudávalo žádnou akutní toxicitu. Pozdní toxicita byla zjištěna u 2 pacientů, a sice u jednoho G1 a u druhého G3.
Medián doby sledování pacientů s mozkovými metastázami byl 8,5 měsíce (1,2–99 měsíců). Kompletní remise (CR) bylo dosaženo u 4 pacientů (7,1 %), parciální remise (PR) byla u 27 pacientů (48,2 %), stabilizace onemocnění u 9 (16,1 %) a progrese byla zaznamenána u 5 pacientů (8,9 %). Výsledky léčby nebylo možné zjistit u 11 pacientů pro zhoršení stavu. Medián doby do další progrese byl 6 měsíců. V současné době žije 13 pacientů (23,6 %) se stabilizovaným onemocněním, 8 pacientů přežívá s progredujícím onemocněním (14,5 %) a 34 pacientů zemřelo (62 %). Žijící pacienti mají medián sledování 10 měsíců. Jednalo se o 9 mužů a 12 žen. U nemocných se jednalo o nález 1–4 metastáz. Klinický stav KI byl vyšší 70 %.
Medián přežití celého souboru byl 13,3 měsíce. Funkce přežití pro tento soubor pacientů je znázorněna na grafu (graf 2).
Také u tohoto soubory byly testovány různé hypotézy. Nebyl zjištěn rozdíl v přežití či PFS (doby přežití bez známek progrese) mezi pacienty mladšími či staršími 50 let, mezi muži a ženami, mezi pacienty se solitárními nebo mnohočetnými metastázami. Také nebyl nalezen statisticky významný rozdíl v přežití mezi pacienty s pouze mozkovými metastázami a pacienty s aktivním celkovým onemocněním ani pacienty, kteří podstoupili ozáření celé mozkovny se stereotaktickým cíleným ozářením (boost), a pacienty léčenými samostatnou stereotaktickou léčbou. Pacienti, kteří podstoupili před ozařováním neurochirurgický zákrok, neměli rozdíl v přežití oproti pacientům bez operace, ale jejich PFS byla statisticky významně delší (p = 0,016).
Diskuze
Stereotaktické ozařovací metody mají své místo v léčbě mozkových lézí. V případě primárních mozkových nádorů se uplatňují především při léčbě recidivujících onemocnění, neúplné exstirpaci tumoru či v lokalizaci nádorů v eloquentních oblastech. Nejčastější diagnózou pro jejich použití bývají meningeomy. Meningeomy tvoří 15–25 % intrakraniálních nádorů. Klinické příznaky závisí na jejich velikosti a lokalizaci. Existuje řada studií zabývajících se léčbou meningeomů metodami SRT nebo SRS pomocí X nože. Majboub et al sledovali 78 pacientů s meningeomy. Při aplikaci SRS byla povrchová dávka 12 Gy, maximální dávka 16 Gy a terapeutická izodóza 75 %. Ve studii dosáhli parciální remise u 26,9 %, stabilizace onemocnění nastala u 70,5 % a jen u dvou pacientů došlo k progresi. Pětileté a devítileté přežití bez známek progrese PFS (progression free survival) uvádí v 98 % a 96 % [6]. Polloch et al sledovali 251 pacientů, u kterých byla průměrná aplikovaná dávka 15,8 ± 2 Gy. Ke zmenšení tumoru došlo u 72,1 % pacientů, stabilizace onemocnění byla prokázána u 26,7 % a progrese onemocnění u 1,2 % pacientů. Ozářením indukované potíže byly u 3,2 % dočasného a u 9,2 % trvalého charakteru. Tříletá a desetiletá lokální kontrola byla 99,4 % [7].
Attia et al zkoumali u atypických meningeomů příčiny relapsu po ozáření. Sledovali 24 pacientů s atypickým meningeomem léčených na gamma noži s mediánem dávky 14 Gy. Roční, dvouletá a pětiletá lokální kontrola byla 75 %, 51 % a 44 %. Dávky vyšší než 14 Gy byly z hlediska lokální kontroly statisticky signifikantní [8].
Minniti et al vypracovali analýzu z více publikovaných studií. V souhrnu doporučují optimální použití stereotaktických léčebných metod v léčbě meningeomů. Radiochirurgie je doporučována pro tumory menší než 3 cm s minimální vzdáleností od optických drah 3 mm. Poté může radiochirurgie dosáhnout pětileté lokální kontroly u 85–97 % pacientů. Frakcionovaná stereotaktická radioterapie je pak určena pro větší nebo nepravidelné tumory či meningeomy v blízkosti kritických struktur. Pětiletá lokální kontrola pak dosahuje 85–100 % [9]. Metellus et al hledali rozdíl mezi SRT a SRS v léčbě meningeomů. Celkem 38 pacientů mělo SRT a 36 podstoupilo SRS. Přežití bez známek progrese (PFS) uvádějí 94,7 % a 94,4 %. Trvalé poškození kognitivních funkcí bylo zaznamenáno u 2,6 % pro SRT a 0 % pacientů pro SRS [10]. Torres et al sledovali 77 pacientů léčených metodou SRS a 51 pacientů léčených SRT s podobnými výsledky [11]. Další obdobnou studii vedli Lo et al se souborem 35 pacientů léčených SRS a s 18 pacienty léčenými SRT. V obou skupinách byla stejná tříletá lokální kontrola 94 % s morbiditou 2,6 % pro SRS a 0 % pro SRT. Dávky se pohybovaly od 12 do 18 Gy [12].
Také v našem souboru jsme stereotakticky ozářili 24 pacientů s meningeomy. Stabilizace onemocnění bylo dosaženo u 81 % pacientů, k parciální remisi (PR) došlo u 4 pacientů (8%) a u dvou pacientů byla zaznamenána progrese (4 %). Dvouleté přežití bylo 86,8 %, dvouleté přežití bez známek progrese (PFS) bylo 82 %. Toxicita léčby byla mírná, jak je uvedeno výše.
High-grade gliomy patří mezi nejvíce agresivní tumory. Jejich prognóza je i přes veškeré pokroky medicíny tristní. Radioterapie se uplatňuje v léčebné strategii především jako adjuvantní metoda; primární metodou léčby je chirurgický výkon. Při recidivě může být radioterapie jednou z možných alternativ salvage léčby. Vzhledem k již vysoké aplikované pooperační dávce jsou možnosti konformní radioterapie omezené. Zde může být prostor pro stereotaktické ozařovací metody. Výsledky však nejsou dobré [13]. Bismas et al v retrospektivní analýze sledovali použití radiochirurgie v léčbě glio-blastomů. Nezjistili rozdíl v přežití u pacientů, kteří podstoupili SRS jako boost při primární léčbě, a pacientů, u kterých byla radiochirurgie použita jako salvage léčba při recidivě onemocnění. Léčba byla dobře tolerována [14]. Kong et al sledovali 114 pacientů, kteří podstoupili SRS pro relaps glioblastomu. Medián doby přežití bez známek progrese (PFS) po této léčbě byl 8,6 měsíce pro gliomy GIII a 4,6 měsíce pro glioblastomy. Radioterapií indukovaná nekróza mozkové tkáně byla zjištěna u 24,4 % pacientů. Oproti historické kontrole zvyšovala salvage SRS přežití u recidivujících glioblastomů, ale ne u gliomů grade III. Jako významný prognostický faktor přežití byl prokázán nízký histologický grade a nádorový objem menší než 10 mL [15].
Další možnou alternativou léčby je frakcionovaná stereotaktická radioterapie (SRT). Stereotaktická radioterapie může být aplikována jak na malé objemy (podobně jako SRS), tak i na větší objemy bez velkého nárůstu nežádoucích účinků. Publikované studie se liší počtem frakcí i celkovou dávkou aplikovanou pomocí SRT. Celková dávka se většinou pohybuje od 25 do 35 Gy s mediánem dávky na frakci 2–5 Gy. Fokas et al léčili 53 pacientů s recidivujícím glioblastomem. Medián celkové dávky byl 30 Gy s mediánem dávky na frakci 3 Gy. Po reiradiaci stereotaktickou radioterapií byl medián sledování 9 měsíců a jednoleté přežití bez známek progrese 22 %. Uváděné metody léčby byly dobře tolerovány [16]. Ernst-Stecken et al aplikovali 5 × 7 Gy s akceptovatelnou toxicitou a jednoletým přežitím bez progrese 53 % [17]. Podobně také Henke et al s mediánem celkové dávky 20 Gy dosáhli u 29 pacientů mediánu přežití 10,2 měsíce a celkového přežití 30,9 měsíce. Závažná toxicita také nebyla zaznamenána [18].
Také v našem souboru byla léčba dobře tolerována a míra vedlejších účinků odpovídá publikovaným výsledkům jiných pracovišť. Bohužel dosažené léčebné výsledky nedosahují úrovně citovaných zahraničních výsledků. Nicméně se ukazuje, že tato metoda salvage radioterapie může být použita u recidivujících high-grade gliomů u mladších pacientů v dobrém celkovém stavu.
V terapii mozkových metastáz má radioterapie své nezastupitelné místo. Mozkové metastázy se objevují u 20–40 % onkologických pacientů v celém průběhu jejich onemocnění. Léčba pouze kortikosteroidy má medián přežití 1 měsíc. Přidáním ozařování do léčebné strategie se medián přežití prodlužuje na 3 až 6 měsíců. Léčebným standardem je ozáření celé mozkovny dávkou 30 Gy. Ozáření celého mozku je však spojeno s vyšším rizikem nežádoucích účinků, především poruchou kognitivních funkcí. Stereotaktické metody mohou zajistit aplikaci vysoké dávky do oblasti metastázy a šetření zdravých tkání. Chirurgickou resekci metastáz lze zvažovat u solitární metastázy či malého počtu ložisek u pacientů v dobrém klinickém stavu s kontrolovaným primárním onemocněním. Chirurgická resekce má být doplněna u radiosenzitivních tumorů ozářením celé mozkovny. Radiochirurgie je indikována u solitární metastázy jako alternativa chirurgického zákroku. Lze ji také zvažovat u 2–4 ložisek do velikosti maximálně 3 cm. U větších metastáz lze indikovat frakcionovanou stereotaktickou radioterapii. Kombinace ozáření celého mozku (WBRT) a neurochirurgické resekce výrazně zlepšuje přežití, snižuje riziko vzniku intrakraniálních rekurencí a vykazuje menší mortalitu na neurologickou symptomatiku [2]. Dle doporučení americké radioterapeutické společnosti (ASTRO) je pro pacienty s nově diagnostikovanými mozkovými metastázami doporučováno ozáření celého mozku (WBRT) nebo WBRT s radiochirurgickým cíleným ozářením (boost). Pro pacienty s více než třemi metastázami do 4 cm radiochirurgický boost po WBRT výrazně zlepšuje lokální kontrolu onemocnění [19]. Existuje také několik studií, kde byla SRS použita samostatně. Výsledky neovlivnily přežití oproti použití WBRT, ale bylo zaznamenáno zhoršení lokální kontroly onemocnění [20]. Přidání SRS boostu se neprojeví na zhoršení míry toxicity. Velký soubor zkoumal Sanghavi et al. Porovnávali celkem 502 pacientů s mozkovými metastázami. Pacienti se SRS boostem měli prokazatelně vyšší přežití oproti pacientům se samostatnou WBRT [21].
V naší studii nebyl prokázán rozdíl v přežití u pacientů s WBRT a SRS boostem a pacienty léčenými samostatnou radiochirurgií.
Vzhledem k možným nežádoucím pozdním účinkům při ozáření celého mozku se objevují studie srovnávající WBRT se SRT boostem se samostatnou radiochirurgií. Randomizovaná studie Aoyama et al rozdělila pacienty do dvou skupin: 67 pacientů se samostatnou SRS a 65 s kombinovanou léčbou. Šestnáct procent pacientů v rameni se samostatnou SRS muselo podstoupit salvage WBRT. V druhé skupině 15 % podstoupilo salvage SRS. Nebyl zjištěn statisticky významný rozdíl v mediánu přežití v lokální kontrole či incidenci smrti v obou skupinách. Ve skupině se samostatnou SRS bylo v prvním roce vyšší riziko lokálního a vzdáleného relapsu [22].
Podobně také Chang et al léčili 58 pacientů s mozkovými metastázami. Celkové přežití bylo vyšší ve skupině se samostatnou SRS (15,2 vs 5,7 měsíce), ale jednoletá lokální a vzdálená kontrola byla v této skupině horší. Zhoršení kognitivních funkcí bylo více zastoupeno ve skupině s kombinovanou léčbou [23].
Šimonová et al sledovali 400 pacientů se solitární mozkovou metastázou léčenou na gamma noži. Kompletní nebo částečná remise byla zjištěna u 74 % pacientů, progrese u 7 % pacientů. Medián PFS pro solitární metastázu byl 10 měsíců, pro vícečetné metastázy 7 měsíců. Akutní toxicita stupně 3 a 4 byla u 20 %, u 5 % pacientů byla zaznamenána pozdní toxicita [24].
V současnosti je SRS indikována jako boost po WBRT u pacientů s méně než pěti metastázami. Dále pak v monoterapii u pacientů s předpokládaným dlouhodobým přežitím, kdy je snaha vyhnout se vysokému riziku nežádoucích účinků po ozáření celého mozku, a dále jako salvage terapie po selhání ozáření celého mozku. Také může být samostatně indikována v léčbě radiorezistentních mozkových metastáz a jako adjuvantní léčba po resekci radiorezistentních metastáz [25,26].
V našem souboru byla také zaznamenána nízká toxicita léčby a podobné výsledky léčby jako v jiných studií.
Závěr
Stereotaktické ozařovací metody jsou součástí moderní radioterapie. Jejich indikaci je nutné dobře zvažovat s ohledem na prospěch pacienta. K jejich použití je nutné kvalitní vybavení radioterapeutického pracoviště a vyškolený personál. Uvedená data z našeho pracoviště prokazují srovnatelné výsledky v porovnání s jinými specializovanými ozařovacími systémy pro radiochirurgii. Další prospektivní randomizované studie jsou potřebné k další přesnější indikaci těchto léčebných modalit.
MUDr. Hana Doleželová, Ph.D.
Klinika radiační onkologie LF MU a MOÚ Brno
Žlutý kopec 7
656 53 Brno
e-mail: dolezelova@mou.cz
Obdrženo: 17. 10. 2012
Přijato: 30. 10. 2012
Zdroje
1. National Comprehensive Cancer Network [online]. www.NCCN.org
2. Šlampa P a kol. Radiační onkologie v praxi. 3. vyd. Brno: Masarykův onkologický ústav 2011 : 201–225.
3. Šimonová G, Novotný J jr. Stereotaktická radiochirurgie a radioterapie. S. 413–425 V: Šlampa P, Petera J: Radiační onkologie. Praha: Galén 2007 : 413–426.
4. Liščák R a kol. Radiochirurgie gamanožem. Principy a neurochirurgické aplikace. Praha: Grada 2009 : 77–92.
5. Collet D. Modelling survival datat in medici research. Chapman and Hall/CRC 1999.
6. El Majdoub F, Elawady M, Bührle C et al. µMLC-LINAC radiosurgery for intracranial meningeomas: of komplex shape. Acta Neurochir (Wien) 2012; 154(4): 599–604.
7. Pollock BE, Stafford SL, Link MJ et al. Single-fraction Radiosurgery for Presumed Intracranial Meningiomas: Efficacy and Complications from a 22-Year Experience. Int J Radiat Oncol Biol Phys 2012; 83(5): 1414–1418.
8. Attia A, Chan MD, Mott RT et al. Patterns of failure after treatment of atypical meningioma with gamma knife radiosurgery. J Neurooncol 2012; 108(1): 179–185.
9. Minniti G, Amicheti M, Enrici RM et al. Radiotherapy and radiosurgery for benign skull base meningiomas. Radiat Oncol 2009; 4 : 42.
10. Metellus P, Regis J, Muracciole X et al. Evaluation of fractionated radiotherapy and gamma knife radiosurgery in cavernous sinus meningiomas: treatment strategy. Neurosurgery 2005; 57(5): 873–886.
11. Torres RC, Frighetto L, De Salles AA et al. Radiosurgery and stereotactic radiotherapy for intracranial meningiomas. Neurosurg Focus 2003; 14(5): e5.
12. Lo SS, Cho KH, Hall WA et al. Single dose versus fractionated stereotactic radiotherapy for meningiomas. Can J Neurol Sci 2002; 29(3): 240–248.
13. Lakomý R, Fadrus P, Šlampa P et al. Výsledky multimodální léčby glioblastoma multiforme: Konsekutivní série 86 pacientů diagnostikovaných v letech 2003–2009. Klin Onkol 2011; 24(2): 112–120.
14. Biswas T, Okunieff P, Schell MC et al. Stereotactic radiosurgery for glioblastoma. Retospective analysis. Radiat Oncol 2009, 4 : 11.
15. Kong DS, LeeJI, Park K. Efficacy of stereotactic radiosurgery as a salvage treatment for recurrent malignit gliomas. Cancer 2008; 112(9): 2046–2051.
16. Fokas E, Wacker U, Gross MW et al. Hypofractionated stereotactic reirradiation of recurrent glioblastomas: a beneficial treatment option after high-dose radiotherapy? Strahlenther Onkol 2009; 185(4): 235–240.
17. Ernst-Stecken A, Ganslandt O, Lambrecht et al. Survival and quality of life after hypofactionated stereotacitc radiotherapy for recurrent malignit glioma. J Neurooncol 2007 : 81(3): 287–294.
18. Henke G, Paulsen F, Steinbach JP et al. Hypofractionated reiradiation for recurrent malignit glioma. Strahlenther Onkol 2009; 185(2): 113–119.
19. Mentha MP, Tsao MN, Whelan TJ et al. The American Society for Therapeutic Radiology and Oncology (ASTRO) evidence-based review of the role of radiosurgery for brain metastases. Int J Radiat Oncol Biol Phys 2005; 63(1): 37–46.
20. Chang EL, Wefel JS, Hess KR et al. Neurocognition in patients with brain metastases treated with radiosurgery or radiosurgery plus whole-brain irradiation: a randomised controlled trial. The Lancet Oncology 2009; 10(11): 1037–1044.
21. Sanghavi SN, Miranpuri SS, Chappell R et al. Radiosurgery for patients with brain metastases: a multi-institutional analysis, stratified by the RTOG recursive partitioning analysis method. Int J Radiat Oncol Biol Phys 2001; 51(2): 426–434.
22. Aoyama H, Shirato H, Tago M et al. Stereotactic radiosurgery plus whole-brain radiation therapy vs stereotactic radiosurgery alone for treatment of brain metastases: a randomized controlled trial. JAMA 2006; 295(21): 2483–2491.
23. Chang EL, Wefel JS, Hess KR et al. Neurocognition in patients with brain metastases treated with radiosurgery or radiosurgery plus whole-brain irradiation: a randomised controlled trial. Lancet Oncology 2009; 10(11): 1037–1044.
24. Simonova G, Liscak R. Radiosurgery of brain metastases usisng Leskell gamma knife – results of 400 treated patiens. ECCO poster 2011. DOI:10.1016/S0959-8049(11)72291-2.
25. Chorváth M, Bolješíková E. Metastázy do centrálního nervového systému. In: Jurga Ľ et al (ed). Klinická a radiačná onkológia. 1. vyd. Martin: Osveta 2010 : 1309–1315.
26. Ellis TL, Neal MT, Chan MD et al. The role of Surgery, Radiotherapy and Whole Brain Radiation Therapy in the Management of Patients with Metastatic Brain Tumors. Int J Surg Oncol 2012; 2012 : 952345.
Štítky
Dětská onkologie Chirurgie všeobecná Onkologie
Článek Klinický registr CORECT
Článek vyšel v časopiseKlinická onkologie
Nejčtenější tento týden
2012 Číslo 6- Ibrance® – nová šance pro pacientky s HR+/HER2– karcinomem prsu
- Vliv alkoholu na riziko vzniku karcinomu prsu, nově podle histologického typu nádoru a jeho senzitivity k estrogenovým receptorům
- Exemestan zlepšuje interval bez relapsu při karcinomu prsu
- Význam a prognostická hodnota nádorových markerů
- Přítomnost genetické mutace BRCA vede k častějšímu výskytu rakoviny i ve druhém prsu
-
Všechny články tohoto čísla
- Klinická onkologie slaví 25. výročí
- Molekulární podstata Waldenströmovy makroglobulinemie
- Prečo sú mitochondrie vhodné ciele pre liečbu rakoviny
- Hodnocení jaterní funkce v onkologické praxi
- EML4-ALK fúzní gen u pacientů s plicním karcinomem: biologie, diagnostika a cílená terapie
- Porovnání nákladů u režimů XELOX a FOLFOX-4 v léčbě kolorektálního karcinomu
- Výsledky léčby mozkových tumorů stereotaktickou radioterapií a radiochirurgií
- Profil pacientů s nádory léčených na pohotovosti referenčního střediska nádorové péče v jižní Brazílii
- Proteiny rezistence a chemorezistence u pacientek s karcinomem ovaria
- Kazuistika: Podpůrná léčba u pacientky s rozsáhlým tumorem ovaria
- Bílé subkapsulární jaterní uzly objevené náhodně během laparoskopické operace: žlučové hamartomy a peribiliární žlázový hamartom
- Paraneoplastický neurologický syndrom u 64letého pacienta s malobuněčným karcinomem plic – kazuistika
- Vzpomínka na MUDr. Vladimíra Spurného, CSc.
- Prof. MUDr. Rostislav Vyzula, CSc., již a teprve šedesátiletý
- Klinický registr CORECT
- Možnosti překonání rezistence k hormonální léčbě u pacientek s hormonálně dependentním metastatickým karcinomem prsu
- Aprepitant a pruritus – komentář k článku
- Informace z České onkologické společnosti
- Klinická onkologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Hodnocení jaterní funkce v onkologické praxi
- Porovnání nákladů u režimů XELOX a FOLFOX-4 v léčbě kolorektálního karcinomu
- Bílé subkapsulární jaterní uzly objevené náhodně během laparoskopické operace: žlučové hamartomy a peribiliární žlázový hamartom
- Kazuistika: Podpůrná léčba u pacientky s rozsáhlým tumorem ovaria
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




