-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaKlinický registr CORECT
Autoři: R. Němeček 1
; J. Tomášek 1
; K. Hejduk 2
; Z. Bortlíček 2
Působiště autorů: Klinika komplexní onkologické péče, Masarykův onkologický ústav a Lékařská fakulta Masarykovy univerzity, Brno 1; Institut biostatistiky a analýz Masarykovy univerzity, Brno 2
Vyšlo v časopise: Klin Onkol 2012; 25(6): 480-485
Kategorie: Aktuality z registrů
Klinický registr CORECT vznikl v polovině roku 2011 sloučením do té doby úspěšných registrů Avastin a Erbitux a rozšířením o sledování preparátu Vectibix. Technickým převodem dříve získaných dat odpadla nutnost zadávat data o léčbě jednoho pacienta do různých registrů, čímž došlo k získání ucelených a přehledných informací o celkové léčbě daného pacienta a možnostech sledování sekvence léčby. Registr CORECT, obdobně jako jeho předchůdci byl založen za účelem monitorace efektivity a spotřeby cílené léčby metastatického kolorektálního karcinomu (mCRC). Intenzivní spoluprací všech komplexních onkologických center se podařilo vytvořit rozsáhlou a podrobnou retrospektivní populační analýzu výsledků léčby mCRC, která v současné době obsahuje data více než 5 000 pacientů léčených Avastinem, Erbituxem, Vectibixem, případně jejich sekvencí. Jedná se o data z běžné klinické praxe, ve které jsou na rozdíl od randomizovaných studií léčeni i pacienti polymorbidní, v horším celkovém stavu. Kromě dat o počtech léčených pacientů jsou nejcennějšími výstupy z registru především údaje o jejich celkovém přežití a době do progrese onemocnění. Validita těchto dat je ze strany brněnského Institutu biostatistiky a analýz (IBA), který registr ve spolupráci s klinickými onkology vytvořil a spravuje, pravidelně ověřována.
Bevacizumab (AVASTIN)
Klinický registr Avastin byl založen 1. 1. 2005. Po více než šesti letech samostatné existence (k datu 1. 7. 2011) byla získaná data převedena pod klinický registr CORECT.
Do 8. 10. 2012 bylo do registru zařazeno celkem 4 510 pacientů s mCRC z 22 onkologických center v České republice, z toho 4 487 pacientů s dostatečně vyplněným záznamem. Počty pacientů zařazených v jednotlivých letech od založení registru ukazuje obr. 1. Byli léčeni pacienti ve věku od 20 do 88 let s mediánem věku 62 let. Téměř dvě třetiny z nich (62,9 %) tvořili muži, ženy se na celkovém počtu pacientů podílely 37,1 %. Stran lokalizace primárního nádoru převažovaly nádory kolon (60,4 %) nad nádory rekta (39,6 %), při hodnocení metastáz dominovaly metastázy jaterní (66,1 %) nad metastázami plicními (26,8 %), metastázami v lymfatických uzlinách retroperitonea (22,3 %) a metastázami peritoneálními (19,4 %). Naprostá většina pacientů (88,9 %) byla léčena kombinací s bevacizumabem v rámci 1. linie paliativní chemoterapie, 8,6 % pak v rámci 2. linie systémové léčby a 2,5 % pacientů v rámci dalších linií. Mezi používanými chemoterapeutickými režimy převažovaly režimy FOLFOX (42,2 %) a XELOX (30,0 %), následovány režimy FOLFIRI (10,5 %), XELIRI (5,0 %), Xeloda (4,4 %) a FU/FA de Gramont (2,8 %). Pouze 1,4 % pacientů bylo léčeno primárně bevacizumabem v monoterapii. K datu aktualizace (8. 10. 2012) mělo 78 % (3 502) hodnotitelných pacientů léčbu bevacizumabem již ukončenou, medián délky léčby byl u těchto pacientů stanoven na 6,4 měsíce. V souboru hodnotitelných pacientů bylo dosaženo 12,5 % kompletních remisí (CR), 28,6 % parciálních remisí (PR) a 37,4 % stabilizací onemocnění (SD), což představuje četnost léčebných odpovědí (RR) 41,1 % a klinický benefit u 78,5 % léčených pacientů, tedy hodnoty srovnatelné s daty z randomizovaných klinických studií [1,2]. Je vhodné upozornit, že v registru CORECT jsou zaznamenávány výsledky komplexní léčby pacienta, tedy že kompletní remise mohlo být dosaženo také resekcí metastáz po předchozí cytostatické léčbě s bevacizumabem. Nejdůležitějšími výstupy z registru jsou však data týkající se celkového přežití pacientů (OS) a přežití bez známek progrese onemocnění (PFS): medián celkového přežití byl u 4 487 hodnocených pacientů stanoven na 27,6 měsíce (obr. 2), medián PFS pak na 11,1 měsíce (obr. 3). Tyto hodnoty výrazně převyšují publikovaná prospektivní data (Hurwitz et al – medián OS 20,3 měsíce [1], Saltz et al – medián OS 21,3 měsíce [2]), při porovnání s výsledky retrospektivních populačních analýz a observačních studií však podobné mediány nejsou výjimkou (Kopetz et al – medián OS 29,3 měsíce [3], Renouf et al – medián OS 26 měsíců u pacientů mladších 70 let [4], observační studie BRiTE – medián OS 28 měsíců u pacientů pod 65 let věku [5]). Dle očekávání bylo lepšího přežití i času do progrese dosaženo při podání bevacizumabu v rámci léčby 1. linie mCRC oproti použití v dalších terapeutických liniích. Uváděná toxicita léčby se nelišila od standardně publikovaných dat (akcelerace hypertenze, zvýšené riziko arteriálních tromboembolických příhod, proteinurie, krvácení, vliv na hojení ran a další).
Obr. 1. Počet pacientů léčených Avastinem dle roku zahájení léčby. 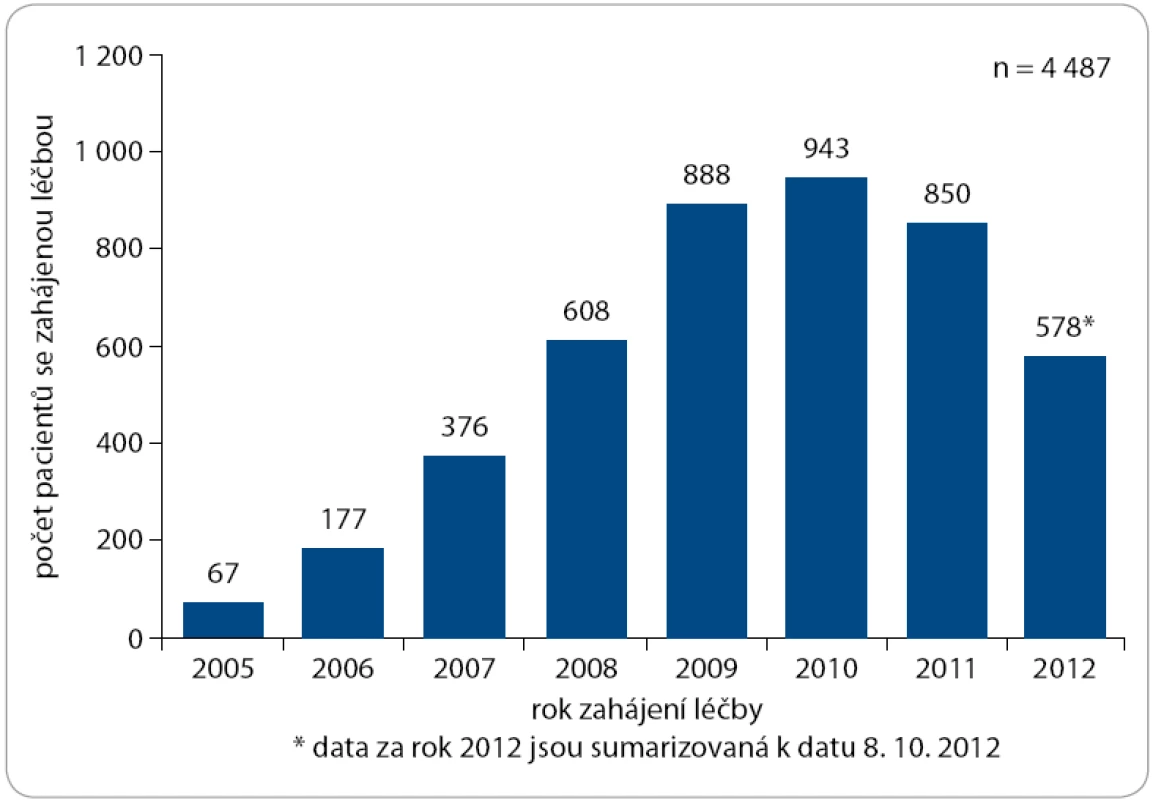
Obr. 2. Celkové přežití od data zahájení léčby Avastinem. 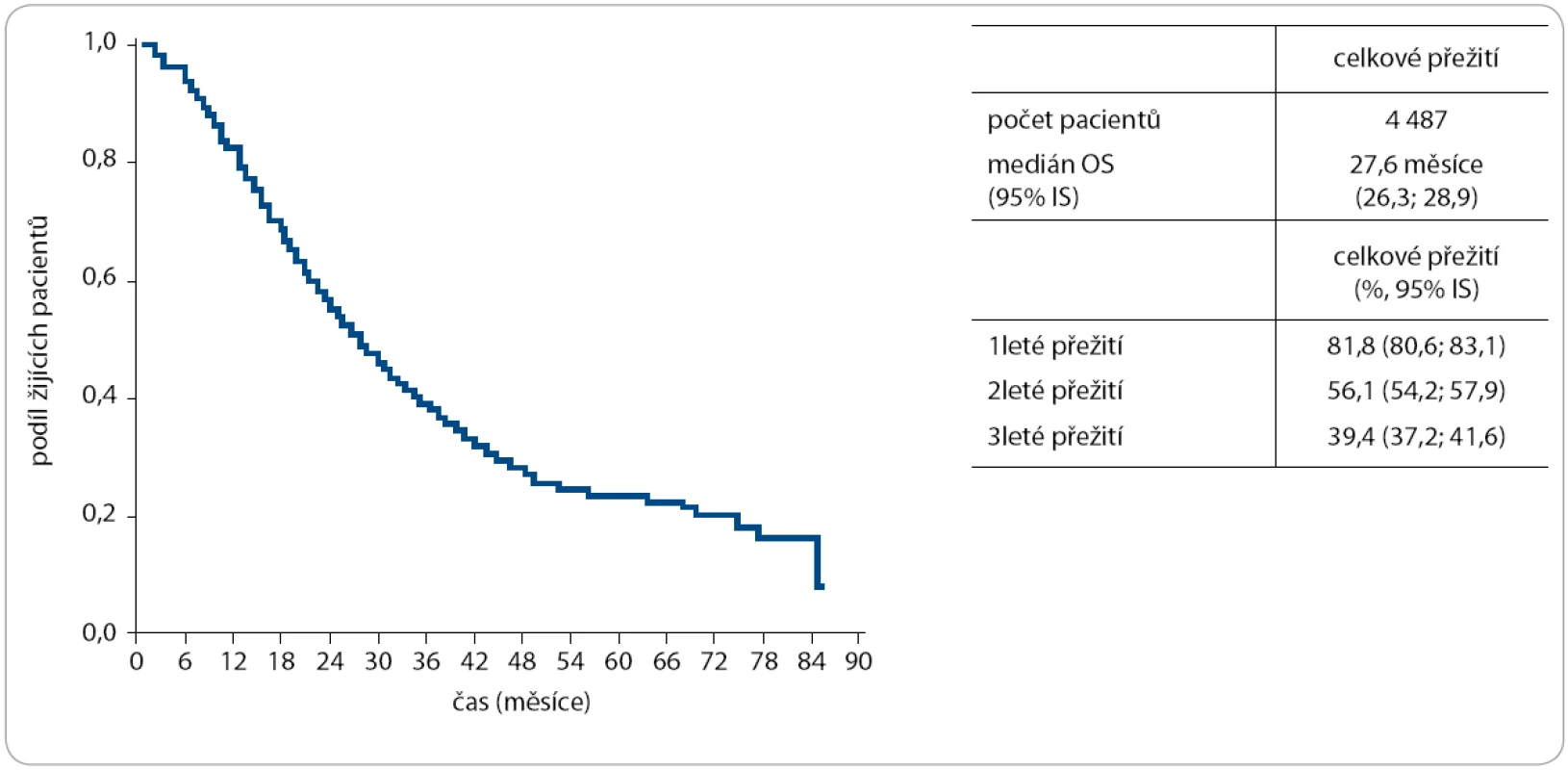
Obr. 3. Přežití bez známek progrese od data zahájení léčby Avastinem. 
Cetuximab (ERBITUX)
Klinický registr Erbitux byl založen 1. 1. 2009. K datu 8. 10. 2012 byla do registru vložena data od 1 160 pacientů, plně hodnotitelných bylo 1 142 z nich. Počty pacientů zařazených v jednotlivých letech jsou znázorněny na obr. 4. Byli léčeni pacienti ve věku od 20 do 84 let s mediánem věku 62 let, dvě třetiny z nich (65,9 %) tvořili muži, jednu třetinu (34,1 %) ženy.
Obr. 4. Počet pacientů léčených Erbituxem dle roku zahájení léčby. 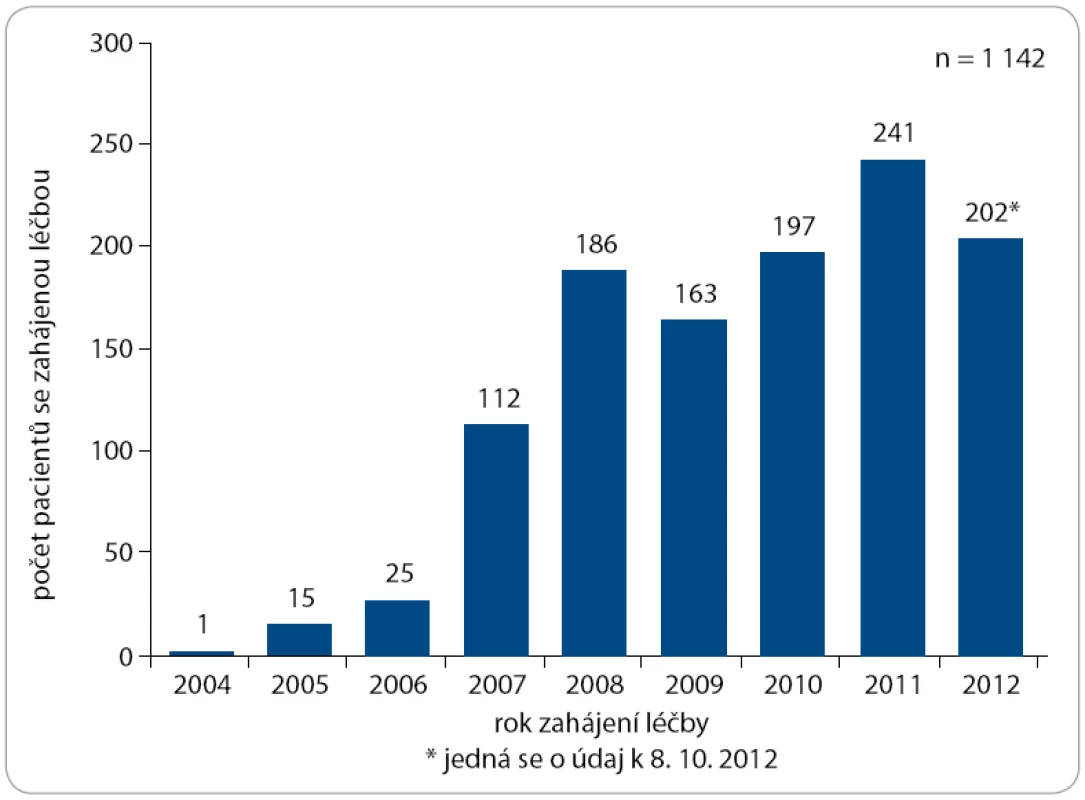
Podobně jako u pacientů léčených bevacizumabem dominovaly nádory kolon (62,4 %) nad nádory rekta (37,6 %) a metastázy jaterní (71,6 %) nad metastázami plicními (36,9 %), metastázami v lymfatických uzlinách retroperitonea (32,5 %) a metastázami peritoneálními (19,5 %). Protože cetuximab byl u nás v rámci 1. linie léčby mCRC pojišťovnou schválen až od poloviny roku 2011, byla většina pacientů zařazených do registru léčena cetuximabem v rámci druhé (41,2 %) a třetí (37,5 %) linie léčby mCRC. V první linii bylo léčeno pouze 13,0 % zařazených pacientů. 50,4 % hodnotitelných pacientů dostávalo v kombinaci s cetuximabem irinotekan, 26,0 % pacientů režim FOLFIRI, 6,8 % režim FOLFOX a 2,6 % režim XELIRI. Jen 7,9 % pacientů bylo léčeno již primárně cetuximabem v monoterapii. K datu poslední aktualizace záznamů mělo 935 pacientů sledovanou léčbu již ukončenou, medián délky léčby cetuximabem byl u těchto pacientů 4,3 měsíce. Kombinovanou léčbou bylo dosaženo efektu CR u 5,3 %, PR u 19,5 % pacientů a stabilizace onemocnění u 34,8 % pacientů, což představuje RR 24,8 % a klinický benefit u 59,6 % léčených pacientů, tedy opět hodnoty srovnatelné s daty z klinických studií u předléčených pacientů s mCRC (kteří v registru naprosto převažují) [7]. Nutno zdůraznit, že se jedná o data od pacientů nestratifikovaných – tedy s mutací v genu KRAS i bez této mutace (označovaných jako wt-KRAS), neboť mutace KRAS se v ČR vyšetřuje rutinně až od roku 2009. V rámci parametrů OS a PFS však již byl status onkogenu KRAS zohledněn – medián OS u neselektované populace byl 15,7 měsíce vs 17,1 měsíce u 782 pacientů s wt-KRAS, medián PFS byl 6,4 měsíce (versus 6,6 měsíce u pacientů s wt-KRAS). Po odečtení 148 pacientů léčených v rámci první linie a analýze pouze pacientů předléčených (n = 994) byl medián OS stanoven na 15,2 měsíce (resp. 16,2 měsíce u 654 pacientů s wt-KRAS, obr. 5) a medián PFS na 6,3 měsíce u obou skupin (obr. 6). Tyto výsledky opět výrazně převyšují publikovaná prospektivní data u chemorefrakterních pacientů s mCRC (Cunnigham et al – medián OS 8,6 měsíce, medián PFS 4,1 měsíce) [6]. Uváděná toxicita léčby se nelišila od standardně publikovaných dat (akneiformní exantém, průjem, hypersenzitivní infuzní reakce a další).
Obr. 5. Celkové přežití od data zahájení léčby Erbituxem – pacienti léčení v rámci druhé a vyšší linie léčby. 
Obr. 6. Přežití bez známek progrese od data zahájení léčby Erbituxem – pacienti léčení v rámci druhé a vyšší linie léčby. 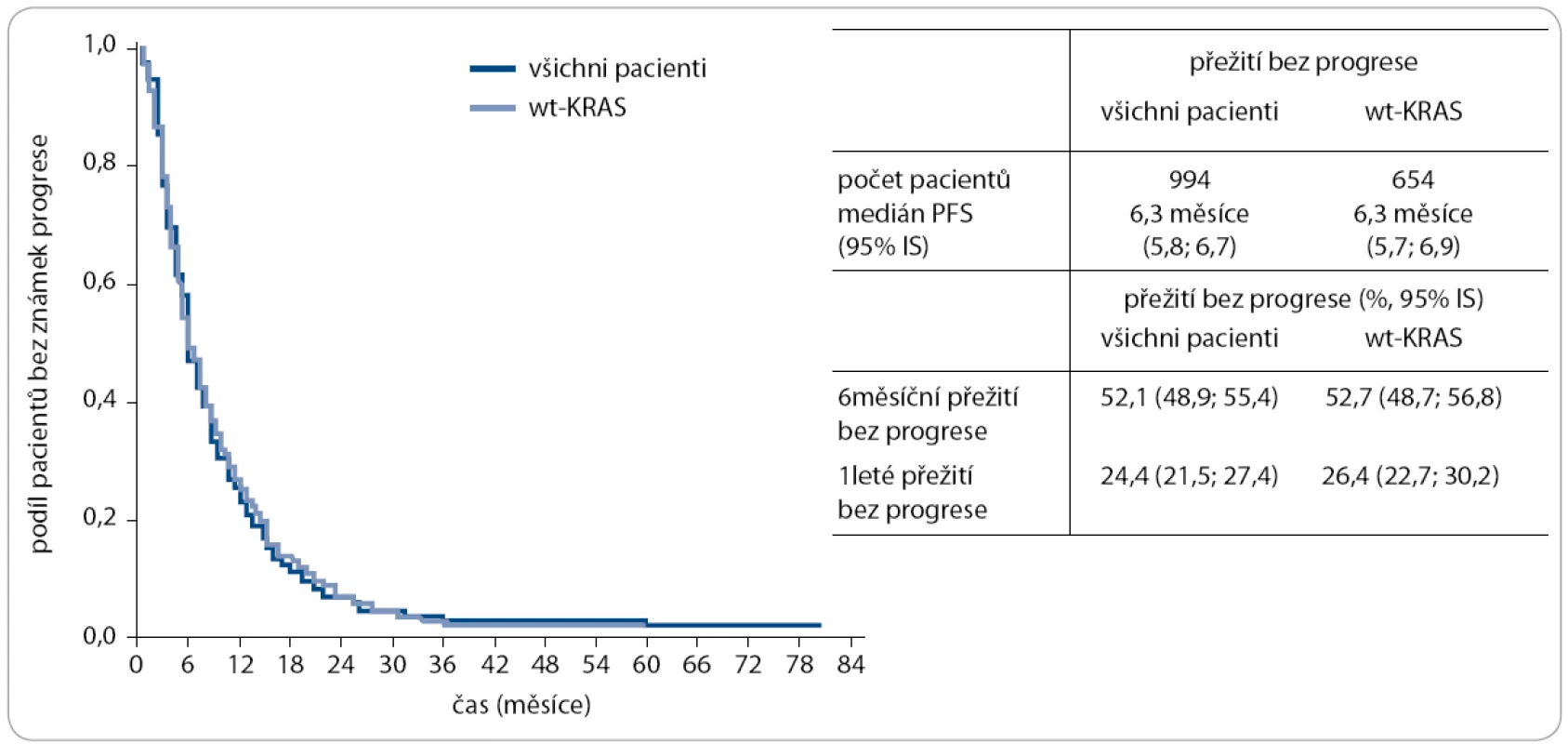
Panitumumab (VECTIBIX)
Přípravek panitumumab (Vectibix) původně neměl vlastní klinický registr vedený IBA a data pacientů léčených tímto preparátem jsou zaznamenávána až v rámci společného registru CORECT – tedy od 1. 7. 2011. Pokud byl však pacient léčen v první linii bevacizumabem a až následně v některé z dalších léčebných linií panitumumabem, byla jeho data k dispozici již v registru Avastin a do registru CORECT byla převedena při jeho vzniku v polovině roku 2011.
K datu 8. 10. 2012 bylo možno hodnotit účinnost panitumumabu celkem u 390 pacientů s mCRC, z toho mělo 382 pacientů dostatečně vyplněný záznam. Byli léčeni pacienti ve věku od 31 do 86 let s mediánem věku 63 let. 61,8 % z nich tvořili muži, 38,5 % ženy. Jako obvykle dominovaly nádory kolon (55,2 %) nad nádory rekta (44,8 %) a jaterní metastázy (69,1 % pacientů) nad metastázami plicními (39,3%), retroperitoneálními (34,3 %) a peritoneálními (16,8 %). Nemutovaný gen KRAS byl potvrzen u 94,3 % zařazených pacientů. Panitumumab byl podáván výhradně v monoterapii, a to u 28,8 % pacientů v rámci druhé linie, u 57,1 % pacientů v rámci třetí linie a u 9,4 % pacientů v rámci čtvrté linie léčby mCRC. K datu aktualizace mělo 78,8 % pacientů léčbu panitumumabem již ukončenou – v naprosté většině (81,1 %) pro progresi onemocnění. Medián délky léčby panitumumabem byl stanoven na 3,4 měsíce.
Stran hodnocení nejlepší léčebné odpovědi v souboru 301 hodnotitelných pacientů s ukončenou léčbou bylo dosaženo 1,0 % kompletních remisí, 13,3 % parciálních remisí a 35,5 % stabilizací onemocnění, což představuje RR 14,3 % a klinický benefit u 49,8 % léčených pacientů – opět hodnoty srovnatelné s daty z publikovaných klinických studií u předléčených pacientů [7]. Medián přežití bez známek progrese onemocnění byl stanoven na 4,9 měsíce (obr. 7), medián celkového přežití dokonce na 12,5 měsíce – tento výsledek však může být v důsledku zatím nedostatečného follow-up nadhodnocen (obr. 8). Toxicita léčby byla přijatelná – kromě očekávaného akneiformního exantému byla zaznamenána především toxicita gastrointestinální a hypomagnezémie. Vzhledem k potvrzení úhrady panitumumabu pro kombinaci s chemoterapií v časných liniích léčby mCRC lze očekávat širší použití tohoto preparátu v běžné onkologické praxi.
Obr. 7. Přežití bez známek progrese od data zahájení léčby Vectibixem. 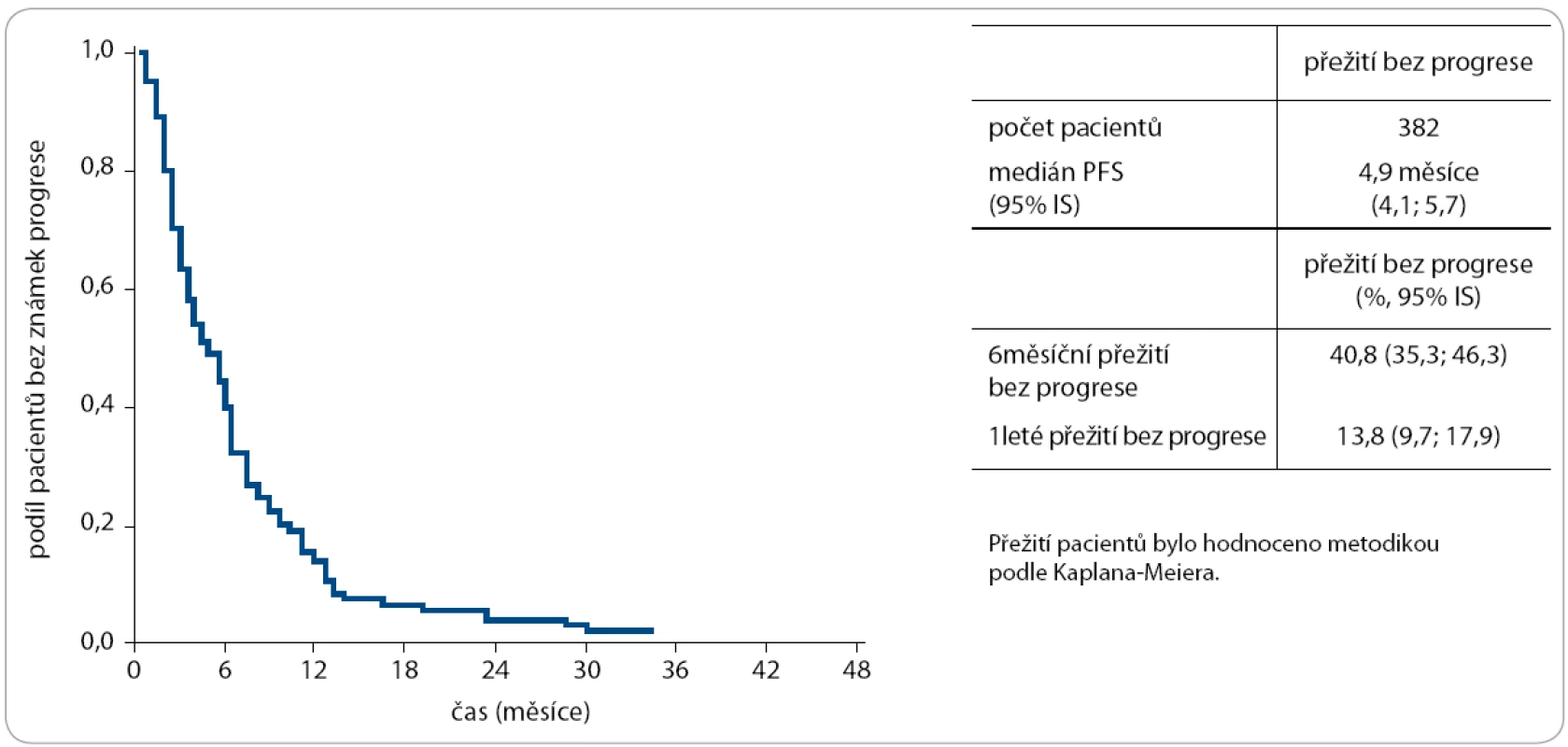
Obr. 8. Celkové přežití od data zahájení léčby Vectibixem. 
Závěr
Registr CORECT, který vznikl integrací dat z registrů Avastin a Erbitux (a nově monitoruje i data o pacientech léčených přípravkem Vectibix), se stal důležitým nástrojem České onkologické společnosti při plánování nákladů na protinádorovou terapii. Kromě údajů o efektivitě léčby (RR, PFS, OS) umožňuje zmapovat použití cílené biologické léčby v jednotlivých oblastech ČR a posoudit vliv rizikových faktorů na přežívání pacientů. Sjednocením registrů došlo k získání ucelených a přehledných informací o celkové léčbě daného pacienta, o možnostech sekvence cílených preparátů a odpovědi pacienta na podanou léčbu.
Děkujeme za spolupráci všem zapojeným onkologickým centrům:
Fakultní nemocnice Brno (Bednařík O.)
Fakultní nemocnice u svaté Anny v Brně (Katolická J.)
Masarykův onkologický ústav (Vyzula R.)
Nemocnice České Budějovice, a.s. (Janovský V.)
Fakultní nemocnice Hradec Králové (Petera J.)
Nemocnice Chomutov (Chodacká M.)
Nemocnice Jihlava (Slavíček L., Benešová V.)
Krajská nemocnice Liberec (Bartoš J.)
Nemocnice s poliklinikou v Novém Jičíně (Soumarová R., Gruna J.)
Fakultní nemocnice Olomouc (Melichar B.)
Fakultní nemocnice Ostrava (Feltl D.)
Pardubická krajská nemocnice (Vaňásek J., Kolářová I.)
Fakultní nemocnice Plzeň (Fínek J.)
Nemocnice Na Bulovce (Stáhalová V.)
Nemocnice Na Homolce (Šafanda M.)
Všeobecná fakultní nemocnice v Praze (Petruželka L.)
Fakultní nemocnice v Motole (Prausová J.)
Thomayerova nemocnice (Abrahámová J.)
Masarykova nemocnice v Ústí nad Labem (Lysý M.)
Krajská nemocnice T. Bati (Kohoutek M., Jakšičová A.)
MUDr. Radim Němeček
Klinika komplexní onkologické péče
Masarykův onkologický ústav
Žlutý kopec 7
656 53 Brno
e-mail: nemecek@mou.cz
Zdroje
1. Hurwitz H, Fehrenbacher L, Novotny W et al. Bevacizumab plus irinotecan, fluorouracil, and leucovorin for metastatic colorectal cancer. N Engl J Med 2004; 350(23): 2335–2342.
2. Saltz LB, Clarke S, Díaz-Rubio E et al. Bevacizumab in combination with oxaliplatin-based chemotherapy as first-line therapy in metastatic colorectal cancer: a randomized phase III study. J Clin Oncol 2008; 26(12): 2013–2019.
3. Kopetz S, Chang GJ, Overman MJ et al. Improved survival in metastatic colorectal cancer is associated with adoption of hepatic resection and improved chemotherapy. J Clin Oncol 2009; 27(22): 3677–3683.
4. Renouf DJ, Lim HJ, Speers C et al. Survival for metastatic colorectal cancer in the bevacizumab era: a population-based analysis. Clin Colorectal Cancer 2011; 10(2): 97–101.
5. Kozloff M, Yood MU, Berlin J et al. Investigators of the BRiTE study. Clinical outcomes associated with bevacizumab-containing treatment of metastatic colorectal cancer: the BRiTE observational cohort study. Oncologist 2009; 14(9): 862–870.
6. Cunningham D, Humblet Y, Siena S et al. Cetuximab monotherapy and cetuximab plus irinotecan in irinotecan-refractory metastatic colorectal cancer. N Engl J Med 2004; 351(4): 337–345.
7. Van Cutsem E, Peeters M, Siena S et al. Open-label phase III trial of panitumumab plus best supportive care compared with best supportive care alone in patients with chemotherapy-refractory metastatic colorectal cancer. J Clin Oncol 2007; 25(13): 1658–1664.
Štítky
Dětská onkologie Chirurgie všeobecná Onkologie
Článek vyšel v časopiseKlinická onkologie
Nejčtenější tento týden
2012 Číslo 6- Ibrance® – nová šance pro pacientky s HR+/HER2– karcinomem prsu
- Vliv alkoholu na riziko vzniku karcinomu prsu, nově podle histologického typu nádoru a jeho senzitivity k estrogenovým receptorům
- Ženy s falešně pozitivním nálezem na mamografii pociťují zvýšenou úzkost a sníženou kvalitu života
- Exemestan zlepšuje interval bez relapsu při karcinomu prsu
- Přítomnost genetické mutace BRCA vede k častějšímu výskytu rakoviny i ve druhém prsu
-
Všechny články tohoto čísla
- Klinická onkologie slaví 25. výročí
- Molekulární podstata Waldenströmovy makroglobulinemie
- Prečo sú mitochondrie vhodné ciele pre liečbu rakoviny
- Hodnocení jaterní funkce v onkologické praxi
- EML4-ALK fúzní gen u pacientů s plicním karcinomem: biologie, diagnostika a cílená terapie
- Porovnání nákladů u režimů XELOX a FOLFOX-4 v léčbě kolorektálního karcinomu
- Výsledky léčby mozkových tumorů stereotaktickou radioterapií a radiochirurgií
- Profil pacientů s nádory léčených na pohotovosti referenčního střediska nádorové péče v jižní Brazílii
- Proteiny rezistence a chemorezistence u pacientek s karcinomem ovaria
- Kazuistika: Podpůrná léčba u pacientky s rozsáhlým tumorem ovaria
- Bílé subkapsulární jaterní uzly objevené náhodně během laparoskopické operace: žlučové hamartomy a peribiliární žlázový hamartom
- Paraneoplastický neurologický syndrom u 64letého pacienta s malobuněčným karcinomem plic – kazuistika
- Vzpomínka na MUDr. Vladimíra Spurného, CSc.
- Prof. MUDr. Rostislav Vyzula, CSc., již a teprve šedesátiletý
- Klinický registr CORECT
- Možnosti překonání rezistence k hormonální léčbě u pacientek s hormonálně dependentním metastatickým karcinomem prsu
- Aprepitant a pruritus – komentář k článku
- Informace z České onkologické společnosti
- Klinická onkologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Hodnocení jaterní funkce v onkologické praxi
- Porovnání nákladů u režimů XELOX a FOLFOX-4 v léčbě kolorektálního karcinomu
- Bílé subkapsulární jaterní uzly objevené náhodně během laparoskopické operace: žlučové hamartomy a peribiliární žlázový hamartom
- Kazuistika: Podpůrná léčba u pacientky s rozsáhlým tumorem ovaria
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



