-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Historie a současnost tenkojehlové aspirační cytologie
Autoři: J. Dvořáčková; Magdalena Uvírová
Působiště autorů: Ústav patologie, Lékařská fakulta, Ostravská univerzita v Ostravě
Vyšlo v časopise: Čes.-slov. Patol., 48, 2012, No. 3, p. 167-168
Kategorie: Kapitoly z historie
Tenkojehlová aspirační cytologie (FNAB/FNAC) je všeobecně používanou metodou pro objasňování a management klinických diagnóz. Je to diagnostický postup, který používá tenkou jehlu 22G či užší k získání cytologického materiálu za účelem objasnění různých onemocnění od nádorových až po choroby infekčního původu. Její využití je nejen u hmatných lézí, ale taktéž se za pomocí moderních zobrazovacích metodik prosadila u vyšetření hluboko uložených a nehmatných afekcí. Jde o minimálně invazivní bezpečnou metodu, která je poměrně přesná, rychlá a nákladově efektivní. Pro pacienta je vysoce komfortní a takřka bez závažných komplikací. Její budoucnost je ve spojení s dalšími moderními laboratorními metodikami zvl. molekulárně genetickými.
První zprávy o tenkojehlové aspirační cytologii pocházejí z konce 19. století, když byl chirurgy Stanleym a Earleym z St. Bartolomewęs Hospital v Londýně získán první cytologický vzorek. Šlo o materiál z obrovské masy nádorové tkáně v játrech. „Aspiraci“ jako vyšetřovací metodu obhajoval ve svých přednáškách neméně slavný lékař Sir James Paget. Menetrier byl pravděpodobně první, který použil tuto vyšetřovací metodu k objasnění diagnózy plicního karcinomu. Pionýrským týmem v USA se stali lékaři z Memorial Hospital v New Yorku – Martin, Ellis a Stewart, když odborné veřejnosti presentovali studii cca 2500 cytologických aspiračních vyšetření. Právě Stewart obhajoval ve svých sděleních výhody tenkojehlové aspirační cytologie a současně zdůrazňoval úzkou spolupráci patologa s klinickým lékařem tak, aby došlo k zvýšení přesnosti diagnostického závěru. Navzdory iniciativě amerických lékařů se jejich pionýrská aktivita neshledala s úspěchem a upadla pro skepticismus kolegů k této metodice tenkojehlové aspirační cytologie téměř v zapomnění.
„Pravá“ tenkojehlová aspirační cytologie (18–27 gauge) byla představená v Evropě až v roce 1950 Lopez-Cardozem v Holandsku a Soderströmem ve Švédsku. Široká publikační aktivita dr. Zajicka z Karolinska Hospital ve Stockholmu, týkající se FNAB/FNAC na sebe strhla mezinárodní pozornost. Společně s Espositem a Lohagenem se stal Zajicek (původem Čech) průkopníkem evropské cytologie. Na jejich práce s úspěchem navázali kliničtí lékaři z řad hematologů zavedením Romanowského a May Grunwald Giemsa barvení cytologických nátěrů pro zrychlení interpretačních hematologických nálezů. Navzdory jejich úspěchu se FNAB dostalo širokého uplatnění až v roce 1980. Hlavním důvodem bylo jednak chybění důvěry v senzitivitu a specificitu tohoto vyšetření, dále strach z implantace nádorových buněk do odběrového kanálu, stejně jako obava ze soudních procesů při neúspěchu odběru, a konečně nechuť kolegů chirurgů vzdát se diagnostiky klasickým bioptickým vyšetřením.
Wiliam Frable revokoval cytologické vyšetření v řadách amerických lékařů touto větou: „Good surgical pathologist who have expressed a negative reaction to FNAB simply do not realise how closely allied recognation of patterns are between aspiration biopsy cells spred and its tissue section counterpart“.
Konec 20. století byl ve znamení FNAB patologických ložisek v prsu, ve štítné žláze a slinných žlázách a také v plicích. Nedůvěra patologů ve správnost vlastní diagnózy mnohdy limitovala výsledek na pouhé stanovení benignity či malignity nálezu. Diagnostická přesnost patologického nálezu souvisela se stále se rozšiřujícími IHC technikami a současně trvalým požadavkem kliniků vytěžit z takto miniinvazívního odběru maximum (obr. 1).
Obr. 1. GIST – imunocytochemický průkaz CD117. 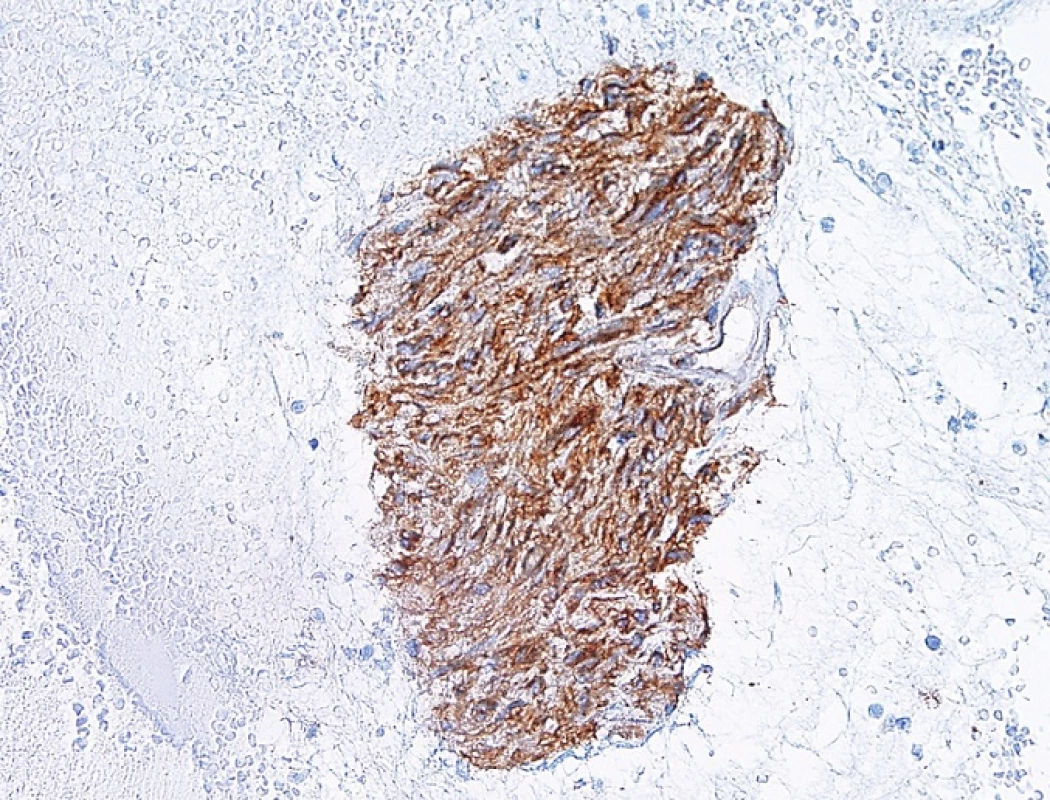
Spolehlivost a přesnost metodiky, jejíž úspěšnost zvl. u nepalpovatelných lézí rostla s ochotou kliniků spolupracovat s patology, se odrazila i na rozšíření spektra diagnostikovaných lézí. Proto je 21. století ve znamení FNAB s úspěchem používané i v diagnostice měkkotkáňových a kostních lézí (obr. 2) či lymfadenopatií včetně maligních lymfomů (obr. 3).
Obr. 2. Obrovskobuněčný kostní nádor. 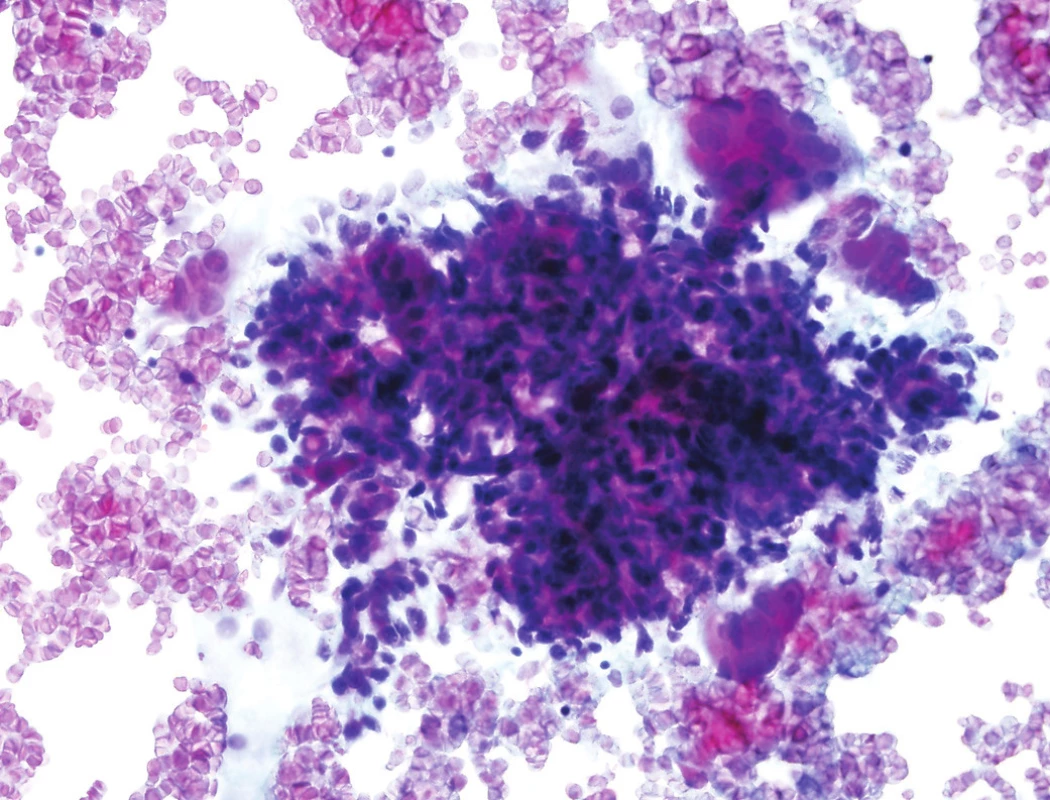
Modernizace se projevila i v zavádění nových vyšetřovacích způsobů. K nim patří i tzv. endoscopic ultrasound fine needle aspiration cytology (EUS FNAC). První ultrasonografický endoskop byl sice vyroben již v roce 1990, metodika však zažila boom až v 21. století. V souvislosti s touto diagnostikou se do povědomí odborné veřejnosti zapsal termín “on - site cytologie”. Význam tohoto vyšetření spočívá v okamžitém zhodnocení cytologického vzorku patologem na odběrovém sálku. Pacient je seznámen s diagnostikujícím patologem, je informován o úspěšnosti odběru, eventuálně i o diagnóze, je-li jednoznačná. Díky novým léčebným trendům se kladou na diagnostikujícího lékaře stále vyšší požadavky. Termín prognostické a prediktivní medicíny je rozšířen o termín medicíny personifikované.
Materiálu z tenkojehlové aspirační cytologie lze využít i pro moderní molekulárně genetickou analýzu maligních nádorů. Pro analýzu kvalitní DNA postačí 200 – 400 nádorových buněk. Mutační status DNA nádoru pacienta může poskytnout účinný nástroj pro stanovení nejefektivnější strategie léčby. Nejčastější využití cytologického materiálu je v současné době při stanovení mutačního statutu genu EGFR jako prediktivního markeru v léčebné odpovědi u nemalobuněčného karcinomu plic. Nadměrná exprese EGFR genu je však popisována u různých typů solidních nádorů jako jsou nádory prsu, hlavy a krku, trávicího traktu, močového měchýře, vaječníků, kolorektálních nádorů a glioblastomů. Tato nadměrná exprese je v těchto případech spojována s pokročilým stupněm rozvoje onemocnění a horší prognózou. Výskyt somatických mutací v genu pro EGFR koreluje s efektivitou účinku tyrozinkinázových inhibitorů (TKI), jako jsou gefitinib nebo erlotinib při léčbě NSCLC. Výskyt aktivačních mutací v EGFR genu koreluje s vnímavostí nádoru na léčbu, zatímco přítomnost jedné z mutací, T790M, koreluje s rezistencí vůči TKI. Mutační status DNA nádoru získaného převážně z cytologického nátěru pacienta může tudíž poskytnout účinný nástroj pro stanovení nejrychlejší a nejefektivnější strategie léčby NSCLC a prodloužit život pacienta (obr. 4).
Obr. 4. Papilární karcinom plic (A). Mutační status DNS (B). 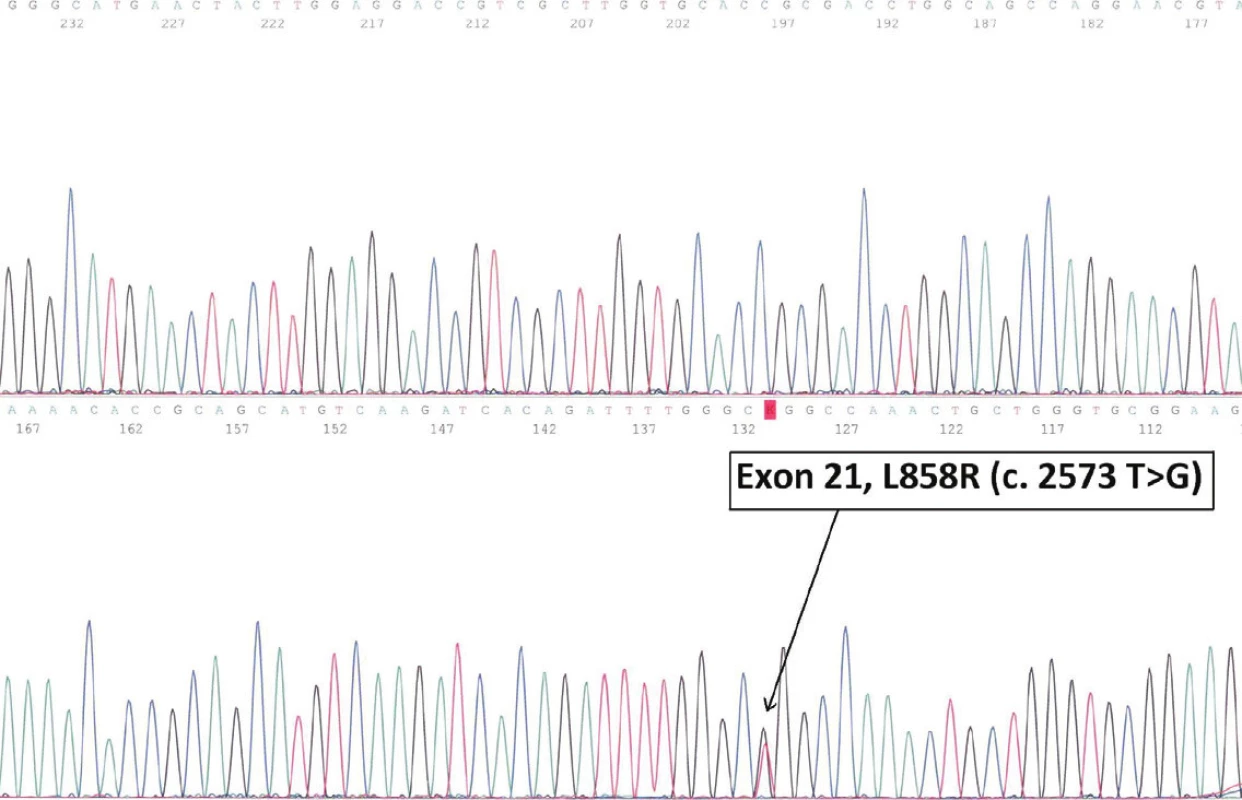
Více než stoletá historie tenkojehlové aspirační cytologie zažívá nové obrození zvláště v kontextu s využíváním tohoto materiálu pro molekulárně genetická vyšetření a tím i pro personifikovanou léčbu.
Adresa pro korespondenci:
MUDr. Jana Dvořáčková, Ph.D.
Ústav patologie, Lékařská fakulta, Ostravská univerzita v Ostravě
17. listopadu 1970, Ostrava – Poruba, 708 00
tel: +420 597 372 301
Štítky
Patologie Soudní lékařství Toxikologie
Článek vyšel v časopiseČesko-slovenská patologie

2012 Číslo 3-
Všechny články tohoto čísla
- Pseudotumors & MIMICKERS
- SLINNÉ ŽLÁZY VYPADAJÍ V MIKROSKOPU TAK KRÁSNĚ!
- HEMATOPATOLOGIE, UROPATOLOGIE, NEFROPATOLOGIE...
- Pseudotumors & Mimickers: Přehled vybraných pseudotumorů s uvedením nádorů, které mohou mikroskopicky imitovat
- Melanocytární pseudotumory
- Změny ve specializačním vzdělávání v patologii od roku 2012
- Diferenciální diagnostika chronické pankreatitidy a duktálního adenokarcinomu pankreatu
- Obrovskobuněčné léze kostí a jejich diferenciální diagnostika
- Pseudotumory varlete a adnexálních testikulárních struktur
- Patologie slinných žláz
- Primární dlaždicobuněčný karcinom vagíny vzniklý na podkladě skvamózní inkluzní cysty zadní stěny vagíny – popis případu
- Sarkomatoidní (metaplastický) vřetenobuněčný karcinom prsu vznikající ve fyloidním tumoru s rozsáhlou skvamózní metaplázií – kazuistika a přehled literatury
- Rozbor histopatologických pitevních nálezů u 8 pacientů s chřipkovou (H1N1) pneumonií
- Imunoexprese adiponektinového receptoru typu 1 v lidském střevě
- Historie a současnost tenkojehlové aspirační cytologie
- Česko-slovenská patologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Obrovskobuněčné léze kostí a jejich diferenciální diagnostika
- Diferenciální diagnostika chronické pankreatitidy a duktálního adenokarcinomu pankreatu
- Sarkomatoidní (metaplastický) vřetenobuněčný karcinom prsu vznikající ve fyloidním tumoru s rozsáhlou skvamózní metaplázií – kazuistika a přehled literatury
- Melanocytární pseudotumory
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání