-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Výsledky bezinterferonové léčby virové hepatitidy C v ČR v reálné praxi
Results of interferon-free hepatitis C therapy in the Czech Republic in real-life
The first real-life data regarding the efficacy of interferon-free therapy for chronic hepatitis C in the Czech Republic are presented. Patients were treated with the combined therapy of paritaprevir/ritonavir plus ombitasvir plus dasabuvir with or without ribavirin. There were 109 patients, who were predominantly men (62, 57%). Most patients were infected by subtype 1b (101, 93%); six patients (5%) had subtype 1a infections and two patients (2%) had genotype 4 infections. Both treatment-naive (43/109, 39%) and pegylated interferon - and ribavirin-experienced patients (66/109, 61%) were treated. A sustained virological response 12 weeks after therapy termination was achieved in 107 patients (98.2%). After excluding two patients from the analyses for reasons other than virological treatment failure, the treatment efficacy was 100%.
Key words:
chronic hepatitis C – paritaprevir/ritonavir – ombitasvir – dasabuvir – ribavirin
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.Submitted:
7. 11. 2016Accepted:
20. 11. 2016
Autoři: P. Husa 1; L. Husová 2
Působiště autorů: Klinika infekčních chorob LF MU a FN Brno 1; Centrum kardiovaskulární a transplantační chirurgie Brno 2
Vyšlo v časopise: Gastroent Hepatol 2016; 70(6): 500-507
Kategorie: Hepatologie
doi: https://doi.org/10.14735/amgh2016500Souhrn
Práce prezentuje první reálná data o úspěšnosti bezinterferonové léčby chronické hepatitidy C v ČR. Pacienti byli léčeni kombinovanou terapií paritaprevir/ ritonavir + ombitasvir + dasabuvir s ribavirinem nebo bez něj. Soubor tvořilo 109 pacientů, převážně mužů (62; 57 %). Převládajícím genotypem byl subtyp 1b (101 ze 109 pacientů; 93 %), infekce subtypem 1a byla přítomna u šesti (5 %) a genotypem 4 u dvou (2 %) nemocných. Byli léčeni jak pacienti dříve neléčení – naivní (43 ze 109; 39 %), tak již v minulosti neúspěšně léčení kombinací pegylovaného interferonu a ribavirinu (66 ze 109; 61 %). Setrvalé virologické odpovědi 12 týdnů po ukončení terapie (SVR12) bylo dosaženo u 107 pacientů (98,2 %). Pokud z analýzy vyloučíme dva pacienty, kteří nedosáhli SVR12 z jiného důvodu než virologického selhání léčby, byla úspěšnost léčby 100%.
Klíčová slova:
chronická hepatitida C – paritaprevir/ ritonavir – ombitasvir – dasabuvir – ribavirinÚvod
Infekce virem hepatitidy C (HCV) je celosvětově jednou z hlavních příčin chronického onemocnění jater. Dlouhodobý efekt infekce HCV je velmi variabilní, kolísá od minimálních histologických změn až po extenzivní fibrózu a cirhózu s hepatocelulárním karcinomem (HCC) nebo bez něj. Odhaduje se, že na světě žije okolo 180 mil. osob s chronickou infekcí HCV, ale většina z nich o této infekci neví. Péče o pacienty infikované HCV se za posledních 20 let významně zlepšila díky lepšímu porozumění patofyziologii onemocnění, zdokonalení diagnostiky, terapeutických a preventivních možností.
Primárním cílem léčby chronické hepatitidy C je vyléčení infekce, tedy dosažení setrvalé virologické odpovědi (SVR) definované jako nedetekovatelná nukleová kyselina viru (HCV RNA) v periferní krvi 12 nebo 24 týdnů po skončení antivirové léčby. Dosažení SVR je obecně spojeno s normalizací aktivity alaninaminotransferázy (ALT) a aspartátaminotransferázy, s ústupem nebo úplným vymizením jaterních nekroticko-zánětlivých změn a fibrózy. Pacienti s pokročilou jaterní fibrózou (F3 dle klasifikace METAVIR) nebo jaterní cirhózou (F4) zůstávají i po dosažení SVR v riziku vzniku závažných jaterních komplikací, i když fibróza většinou regreduje a nebezpečí vzniku jaterního selhání a portální hypertenze je sníženo. Podle výsledků recentních klinických studií je u úspěšně léčených osob riziko vzniku HCC signifikantně redukováno oproti neléčeným pacientům a těm, kteří nedosáhli SVR, ale není zcela eliminováno. Chronická infekce HCV je spojena s výskytem celé řady extrahepatálních manifestací (zejména se smíšenou kryoglobulinemií, řadou ledvinných chorob, non-Hodgkinovým B-buněčným lymfomem). Antivirová léčba s velkou pravděpodobností zlepší nejen jaterní onemocnění a sníží riziko progrese choroby do jaterní cirhózy nebo HCC, ale u významné části alespoň přechodně sníží intenzitu projevů základní choroby [1].
Léčba chronické hepatitidy C prodělává v posledních pěti letech zcela mimořádné změny. Do praxe se postupně zavádějí přímo působící antivirotika (DAA – direct acting antivirals), která se podávají především v bezinterferonových (interferon-free) režimech, nebo dokonce v bezribavirinových (ribavirin-free) režimech. Tyto režimy eliminují závažné nežádoucí účinky pegylovaného interferonu (PEG-IFN) α a ribavirinu (RBV), nemají prakticky kontraindikace a jejich účinnost se blíží 100 %.
Výrazné změny v možnostech léčby chronické hepatitidy C vedou k rychlým inovacím doporučených postupů. Evropská asociace pro studium jater (EASL – European Association for the Study of the Liver) vydala doporučení léčby hepatitidy C v dubnu 2014 [2] a během jednoho roku došlo k takovému vývoji léčebných možností, že v rámci 50. výročního zasedání EASL ve Vídni v dubnu 2015 byla představena doporučení nová [3]. Nejnovější verze doporučeného postupu EASL byla oficiálně představena 22. září 2016 na speciální konferenci EASL New perspectives in hepatitis C virus infection – the roadmap for cure konané v Paříži [1]. Americká asociace pro studium jater přestala svá doporučení vydávat v tištěné formě a zpřístupnila je pouze online na webových stránkách, kde jsou plynule doplňována o výsledky nových klinických hodnocení. Při každém stažení tohoto doporučeného postupu se k textu automaticky přiřadí datum, ve kterém daná verze platila a byla uživatelem získána [4]. Podle posledních evropských i amerických doporučení je nejlepší možností léčby hepatitidy C bezinterferonová terapie.
Současné možnosti bezinterferonové léčby v ČR představují kombinace sofosbuviru s jinými DAA s RBV nebo bez RBV a kombinace paritapreviru potencovaného ritonavirem + ombitasvir + dasabuvir s RBV nebo bez RBV [5]. Nové léky se stále vyvíjejí a postupně přicházejí i na český trh, v prvním čtvrtletí roku 2017 se očekává dostupnost nové fixní kombinace elbasviru s grazoprevirem a sofosbuviru s velpatasvirem, které mají rovněž mimořádně vysokou účinnost a bezpečnost.
Paritaprevir/ ritonavir, ombitasvir a dasabuvir
Léčebná kombinace paritaprevir/ ritonavir, ombitasvir a dasabuvir (Viekirax, Exviera) obsahuje v jedné tabletě paritaprevir (inhibitor NS3/ 4A proteázy) v dávce 75 mg, potencovaný 50 mg ritonaviru, a ombitasvir (inhibitor NS5A) v dávce 12,5 mg. Doporučenou dávkou jsou dvě tablety 1× denně s jídlem. Druhá tableta obsahuje dasabuvir (Exviera), nenukleosidový inhibitor NS5B polymerázy v dávce 250 mg. Užívá se 2× denně jedna tableta. Kombinace těchto léčiv, která se pro zjednodušení označuje jako 3D režim, blokuje všechny dosud známé úrovně replikace HCV. Ritonavir nepůsobí proti HCV, ovlivňuje farmakokinetiku a umožňuje podávání paritapreviru v nižší dávce pouze 1× denně. Tato kombinace je určena pro léčbu pacientů infikovaných genotypem 1, v případě infekce genotypem 4 se používá pouze paritaprevir/ ritonavir + ombitasvir, tedy bez dasabuviru. Oba léky byly v ČR registrovány 1. ledna 2015 a maximální cena a úhrada (vč. úhradových podmínek) byla stanovena od 15. ledna 2016 [6].
Z bezpečnostní analýzy dosud publikovaných klinických studií s 3D kombinací s/ bez RBV vyplynulo, že nejčastějšími nežádoucími účinky byly svědění kůže, únava, nauzea, astenie a nespavost. Příčinou největšího množství nežádoucích reakcí byl RBV, jehož dávku bylo nutno u 7 % pacientů během terapie snížit. Sama 3D kombinace vedla pouze ke svědění kůže. Podstatné je, že závažné nežádoucí účinky léčby se vyskytly u < 2,5 % léčených pacientů. Nežádoucí účinky vedly k předčasnému ukončení léčby v 1–2 % případů. Asymptomatické zvýšení aktivity ALT se obvykle objevilo během prvních čtyř týdnů léčby, vždy odeznělo bez terapeutické intervence a nikdy nebylo provázeno vzestupem sérové hladiny bilirubinu. Naopak přechodný vzestup nepřímého bilirubinu v séru byl pozorován u pacientů léčených 3D a RBV, příčinou byla inhibice bilirubinových transportérů QATP1B1 a QATP1B3 paritaprevirem a hemolýza vyvolaná RBV. Vyšší frekvence vzestupu hladin celkového bilirubinu byla zaznamenána u nemocných s jaterní cirhózou. Při současném užívání léků s estrogeny bylo riziko elevace aktivity ALT vyšší. Použité režimy (s/ bez RBV), podávané po dobu 12 nebo 24 týdnů, byly dobře tolerovány, výskyt nežádoucích reakcí byl velmi nízký [6].
Výsledky
V prezentovaném souboru bylo léčeno 109 pacientů 3D režimem s/ bez RBV. V ČR se na léčbě podílelo celkem devět center (Centrum kardiovaskulární a transplantační chirurgie Brno, FN Brno, FN Motol, FN Olomouc, FN Plzeň, IKEM Praha, Slezská nemocnice Opava, ÚVN Praha, VFN v Praze). U všech pacientů uplynulo v době hodnocení min. 12 týdnů od skončení léčby, a proto bylo možné posoudit dosažení SVR12. Soubor tvořilo 62 mužů (57 %) a 47 žen (43 %). Většina pacientů měla infekci subtypem 1b, a to 101 pacientů (93 %), zbytek byl infikován subtypem 1a (6 ze 109; 5 %) nebo genotypem 4 (2 ze 109; 2 %). Průměrný věk pacientů byl 56 let, u většiny pacientů byla pokročilá jaterní fibróza a vysoká viremie, podrobné charakteristiky souboru jsou uvedeny v tab. 1. Převažovali dříve léčení pacienti (66 ze 109; 61 %), a to jak pacienti relabující po ukončení léčby, tak pacienti, kteří na léčbu neodpověděli, respektive během léčby nedošlo k vymizení viremie (nuloví respondéři) nebo netolerující léčbu PEG-IFN a RBV (tab. 2). Po 8 i 12 týdnech léčby byla negativní viremie u 107 pacientů (98,2 %). Rovněž 12 týdnů po skončení léčby byla nedetekovatelná viremie u 107 pacientů (SVR12 – 98,2 %). U dvou pacientů došlo k předčasnému ukončení léčby v prvním měsíci bezinterferonové terapie z důvodu jiného než virologického selhání léčby, podle modifikované intent-to-treat analýzy (mITT) bylo dosaženo SVR12 ve 100 % případů (graf 1).
Tab. 1. Základní parametry celého souboru (n = 109). Tab. 1. Basic parameters of the entire group (n = 109). 
Tab. 2. Rozdělení pacientů podle předchozí léčby. Tab. 2. Categorisation of patients according to prior treatment. 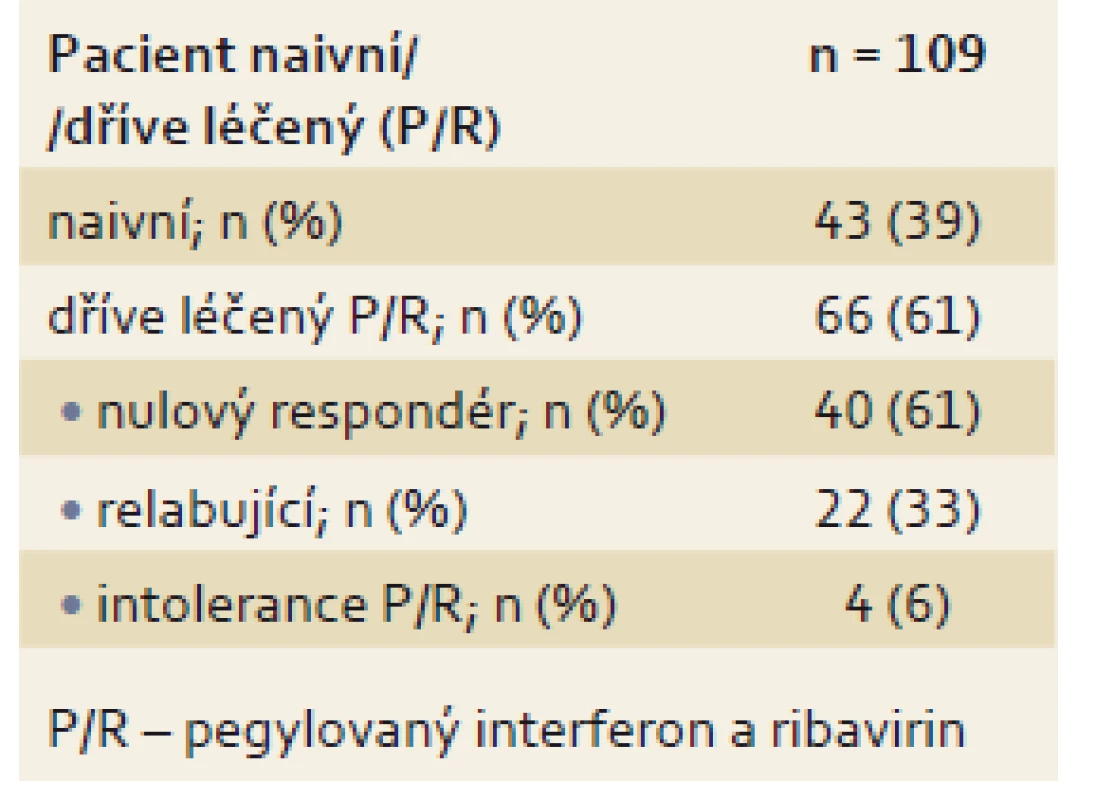
Graf 1. Účinnost 3D léčby. Graph 1. Efficacy of 3D treatment. 
U skupiny nulových respondérů na předchozí léčbou PEG-IFN a RBV vedlo podání 3D režimu k dosažení SVR12 u všech pacientů. Soubor tvořilo 40 nemocných, převažovali muži infikovaní subtypem 1b (tab. 3). U všech pacientů po osmi týdnech léčby byla negativní viremie. Celková účinnost léčby byla velmi vysoká, dosáhla 100 % (SVR12) (tab. 4, graf 2).
Tab. 3. Základní parametry nulových responderů (n = 40). Tab. 3. Basic parameters of zero responders (n =40). 
Tab. 4. Změny hladin HCV RNA během léčby u nulových respondérů. Tab. 4. Changes in HCV RNA levels during treatment in zero responders. 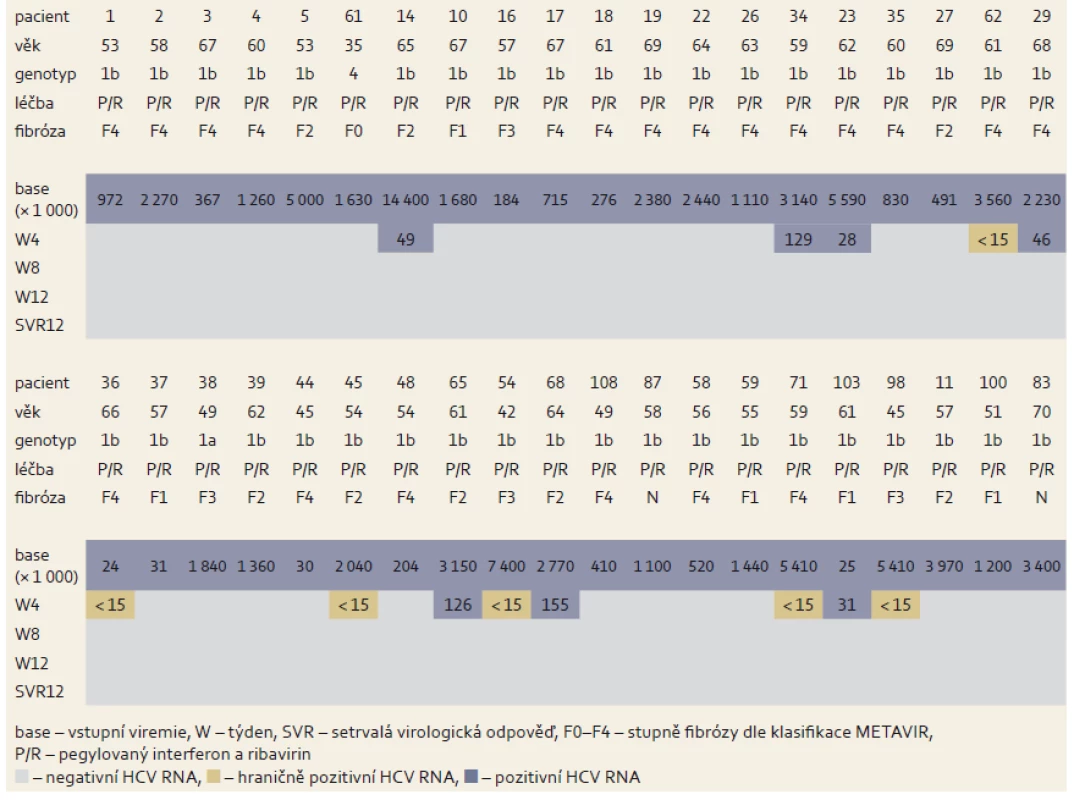
Graf 2. Účinnost 3D léčby u nulových respondérů. Graph 2. Efficacy of 3D treatment in zero responders. 
Další skupinu tvořili pacienti s jaterní cirhózou, u kterých je obecně účinnost a tolerance léčby založené na PEG-IFN velmi špatná. Bezinterferonovou léčbu velmi dobře tolerovali. Léčba jednoho pacienta byla předčasně ukončena po 10 dnech pro progredující ikterus a nově diagnostikovaný HCC. V souboru bylo léčeno 43 pacientů, převažovala infekce subtypem 1b. Podrobná charakteristika souboru je uvedena v tab. 5. Pravděpodobnost dosažení SVR12 byla velmi vysoká (97,7 %). Pokud se z analýzy vyřadí pacient, u kterého byla léčba přerušena z jiného než virologického selhání léčby, pak byla účinnost léčby 100% (mITT SVR12) (tab. 6, graf 3).
Tab. 5. Základní parametry pacientů s jaterní cirhózou (n = 43). Tab. 5. Basic parameters of patients with liver cirrhosis (n = 43). 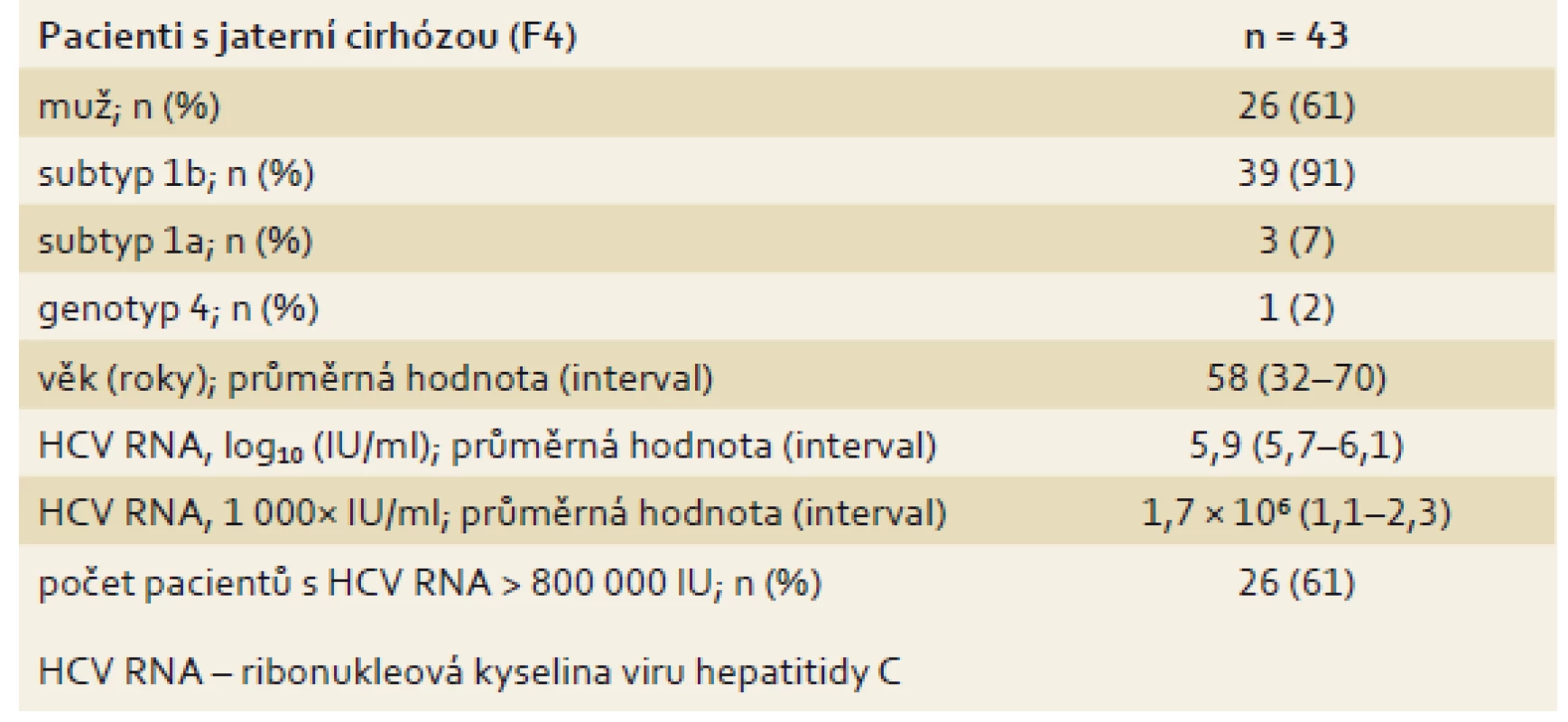
Tab. 6. Změny hladin HCV RNA během léčby u cirhotiků. Tab. 6. Changes in HCV RNA levels during treatment of cirrhotic patients. 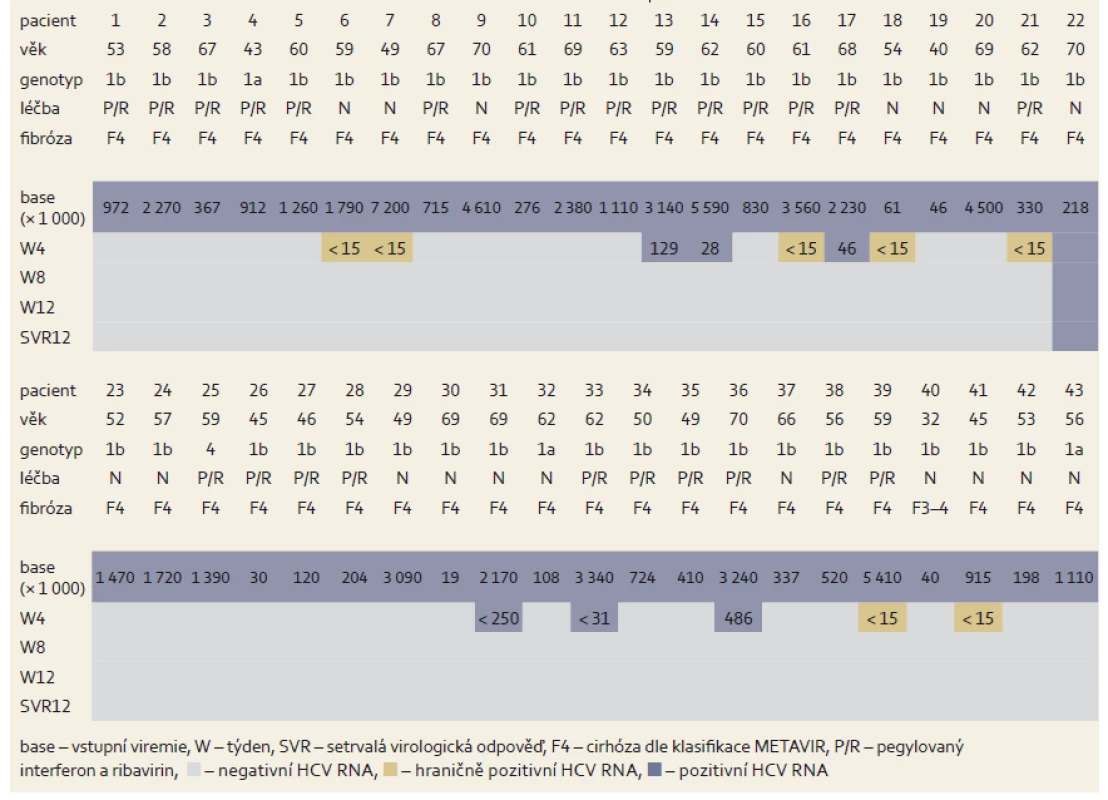
Graf 3. Účinnost 3D léčby u cirhotiků. Graph 3. Efficacy of 3D treatment in cirrhotic patients. 
Velmi zajímavou skupinu tvořili pacienti s rekurující virovou hepatitidoupo transplantaci jater. Virová hepatitida C je jednou z předních indikací k transplantaci jater ve většině transplantačních center. Problém spočívá v časné rekurenci infekce HCV po transplantaci, pokud se transplantuje viremický pacient s rychlým rozvojem jaterní cirhózy. V prezentované skupině bylo léčeno 23 pacientů s rekurující virovou hepatitidou C, převažovali muži (15 z 23; 65 %), všichni se subtypem 1b. Podrobná charakteristika souboru je uvedena v tab. 7. Léčba byla velmi dobře tolerována, bez závažných nežádoucích účinků. Jediným relativním problémem byla nutnost redukce imunosupresivní léčby při současné 3D terapii. U jednoho pacienta byla léčba přerušena po 23 dnech pro závažné biliární komplikace, které si vyžádaly reoperaci. Šlo o chirurgický problém, nikoli o nežádoucí účinek bezinterferonové léčby. Po osmi týdnech léčby byla u všech pacientů vyšetřených v tomto týdnu viremie negativní. SVR12 byla zaznamenána v 95,7 % případů, a pokud vyřadíme pacienta, u kterého nebyla dosažena SVR z jiného důvodu než virologického selhání léčby, tak byla účinnost léčby opět 100% (mITT SVR12) (tab. 8, graf 4).
Tab. 7. Základní parametry pacientů po transplantaci jater (n = 23). Tab.7. Basic parameters of liver transplant patients (n = 23). 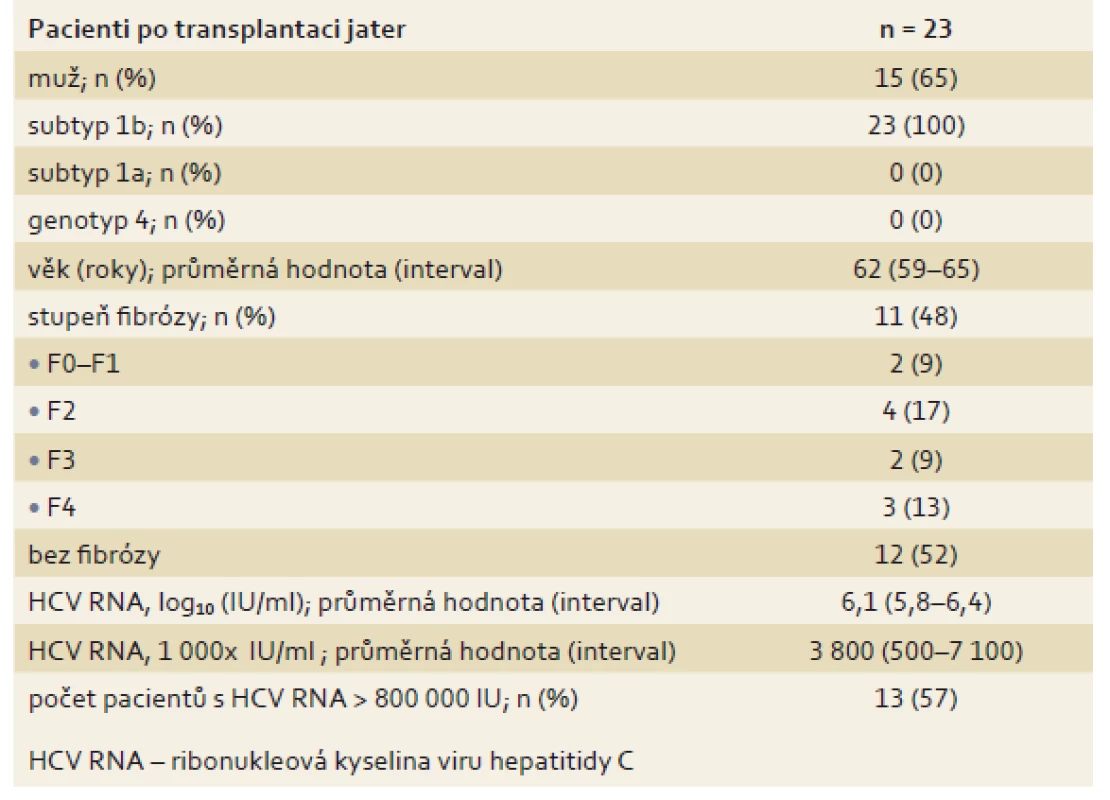
Tab. 8. Změny hladin HCV RNA během léčby u pacientů po transplantaci jater. Tab. 8. Changes in HCV RNA levels during treatment in patients after liver transplantation. 
Graf 4. Účinnost 3D léčby u pacientů po transplantaci jater. Graph 4. Efficacy of 3D treatment in patients after liver transplantation. 
Diskuze
Naše výsledky podporují výsledky klinických studií SAPHIRE I a II, PEARL II–IV, TURQUIOSE I–III o vysoké účinnosti 3D léčby v závislosti na pokročilosti jaterního procesu, daném genotypu a přidání RBV k 3D léčbě [7–13]. Ve studii SAPHIRE I bylo léčeno 12 týdnů 473 naivních (dosud antivirově neléčených) pacientů bez jaterní cirhózy 3D kombinací – SVR12 dosáhlo 95 % infikovaných subtypem 1a a 98 % se subtypem 1b [7]. Ve studii PEARL III bylo dosaženo SVR12 u 99 % pacientů léčených kombinací 3D ± RBV. Šlo opět o nemocné naivní, bez jaterní cirhózy a infikované subtypem 1b – přidání RBV neovlivnilo dosažený výsledek [8]. Výsledky studie TURQUISE I potvrdily účinnost a bezpečnost 3D léčby i u osob koinfikovaných HCV a virem lidského imunodeficitu (HIV). Jednalo se o pacienty naivní, bez jaterní cirhózy a po stránce infekce HIV stabilizované léčbou raltegravirem nebo atazanavirem. Dvanáct týdnů léčby 3D kombinací vedlo k dosažení SVR12 v 93 %, prodloužením délky léčby na 24 týdnů se úspěšnost léčby nezvýšila (91 %) [9]. Studie SAPHIRE II prokázala vynikající úspěšnost 3D léčby i u pacientů v minulosti neúspěšně léčených kombinací PEG-IFN a RBV – SVR 12 bylo dosaženo po 12 týdnech léčby u 96 % osob infikovaných subtypem 1a a 97 % se subtypem 1b [10]. Ve studii PEARL II byl zkoumán efekt přidání RBV k 3D kombinaci u pacientů infikovaných subtypem 1b. Význam přidání RBV se neprokázal – SVR12 ve 100 % případů bez RBV a v 97 % s RBV [11]. Výsledky studie TURQUISE II prokázaly srovnatelnou účinnost 3D kombinace s RBV u pacientů s jaterní cirhózou léčených 12 nebo 24 týdnů (92 vs. 96 %) [12]. Studie TURQUOISE III ukázala, že u kompenzovaných cirhotiků infikovaných subtopem 1b není nutné přidávat RBV – 12 týdnů 3D léčby vedlo k dosažení SVR12 ve 100 % [13].
Závěr
Bezinterferonová léčba je zcela revoluční změnou terapeutických možností chronické hepatitidy C. Po více než 20 letech mizí nutnost použití IFNa se všemi jeho nežádoucími účinky, kontraindikacemi i nutností injekční aplikace. Za absolutní minimum účinnosti se u bezinterferonové léčby bere dosažení SVR v 90 % případů. Většinou je však tohoto cíle dosaženo u ≥ 95 % léčených, v některých podskupinách pacientů je úspěšnost léčby 100%, a to po 12 týdnech léčby (v některých případech po osmi týdnech léčby) a s minimem nežádoucích účinků. Naše výsledky s bezinterferonovou 3D terapií zcela potvrzují dobrou snášenlivost i bezpečnost léčby a její vysokou až 100% účinnost.
Autoři děkují lékařům z FN Motol, FN Olomouc, FN Plzeň, IKEM Praha, Slezské nemocnice Opava, ÚVN Praha a VFN v Praze za poskytnutá data o pacientech a výsledcích jejich léčby.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 7. 11. 2016
Přijato: 20. 11. 2016
prof. MU Dr. Petr Husa, CSc.
Klinika infekčních chorob
LF MU a FN Brno
Jihlavská 20
625 00 Brno
husa.petr@fnbrno.cz
Zdroje
1. European Association for the Study of Liver. EASL recommendations on treatment of hepatitis C 2016. Summary. [online]. Available from: www.easl.eu/ medias/ cpg/ HCV2016/ Summary.pdf.
2. European Association for the Study of Liver. EASL recommendations on treatment of hepatitis C 2014. J Hepatol 2014; 61(2): 373–395. doi: 10.1016/ j.jhep. 2014.05.001
3. European Association for the Study of Liver. EASL recommendations on treatment of hepatitis C 2015. J Hepatol 2015; 63(1): 199–236. doi: 10.1016/ j.jhep.2015.03.025.
4. AASLD recommendation for testing, managing, and treating hepatitis C. [online]. Available from: www.hcvguidelines.org.
5. Urbánek P, Husa P, Šperl J et al. Standardní diagnostický a terapeutický postup chronické infekce virem hepatitidy C (HCV). Klin Mikrobiol Infekc Lek 2015; 21(3): 83–98.
6. Urbánek P. Exviera, Viekirax. Gastroent Hepatol 2015; 69(1): 75–80. doi: 10.14735/ amgh201575.
7. Feld JJ, Kowdley KV, Coakley E et al. Treatment of HCV with ABT-450/ r-ombitasvir and dasabuvir with ribavirin. N Engl J Med 2014; 370(17): 1594–1603. doi: 10.1056/ NEJMoa1315722.
8. Ferenci P, Bernstein D, Lalezari J et al. ABT-450/ r, ombitasvir and dasabuvir with or without ribavirin for HCV. N Engl J Med 2014; 370(21): 1983–1992. doi: 10.1056/ NEJMoa1402338.
9. Wyles DL, Sulkowski MS, Eron JJ et al.TURQUOISE-I: 94% SVR12 in HCV/ HIV-1coinfected patients treated with ABT-450/ r/ ombitasvir, dasabuvir and ribavirin. Hepatology 2014; 60 (Suppl 1): 136A.
10. Zeuzem S, Jacobson IM, Baykal T et al.Retreatment of HCV with ABT-450/ r-ombitasvir and dasabuvir with ribavirin. N Engl J Med 2014; 370(17): 1604–1614. doi: 10.1056/ NEJMoa1401561.
11. Andreone P, Colombo MG, Enejosa JV et al. ABT-450, ritonavir, ombitasvir, and dasabuvir achieves 97% and 100% sustained virologic response with or without ribavirin in treatment experienced patients with HCV genotype 1b infection. Gastroenterology 2014; 147(2): 359–365. doi: 10.1053/ j.gastro.2014.04.045.
12. Poordad F, Hezode C, Trinh R et al. ABT--450/ r-ombitasvir and dasabuvir with ribavirin for hepatitis C with cirrhosis. N Engl J Med 2014; 370(21): 1973–1982. doi: 10.1056/ NEJMoa1402869.
13. Feld JJ, Moreno C, Trinh R et al. Sustained virological response of 100% in HCV genotype 1b patients with cirrhosis receiving ombitasvir/ paritaprevir/ r and dasabuvir for 12 weeks. J Hepatol 2016; 64(2): 301–307. doi: 10.1016/ j.jhep.2015.10.005.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2016 Číslo 6- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Riziko rozvoje závažné infekce po císařském řezu lze snížit provedením antiseptického výplachu vaginy
- Spolehlivý systém skórování jizev k hodnocení fotografií popálenin
- Nedostatečné dávkování enoxaparinu je u pacientů po ortopedickém výkonu časté a zvyšuje riziko tromboembolické nemoci
- Spasmolytický účinek metamizolu
-
Všechny články tohoto čísla
- Dětská gastroenterologie a hepatologie
- Bariatrie
- Jaká je Vaše diagnóza?
- Niektoré genetické determinanty celiakie, význam HLA typizácie v klinickej praxi a zastúpenie HLA-DQ haplotypov v súbore 306 detských pacientov
- Význam fekálního kalprotektinu v diagnostice a sledování dospělých a dětských pacientů s idiopatickými střevními záněty
- Současná bariatricko-metabolická chirurgie
- Endoskopický duodenojejunální bypass (EndoBarrier®) jako nový terapeutický přístup u obézních diabetiků 2. typu – efektivita a faktory predikující optimální efekt
- Výsledky bezinterferonové léčby virové hepatitidy C v ČR v reálné praxi
- Budesonid MMX (Cortiment® 9 mg) v léčbě ulcerózní kolitidy v reálné klinické praxi
- Biosimilární infliximab v terapii anti-TNF naivních pacientů s IBD – jednoleté klinické sledování
- Doporučené postupy České gastroenterologické společnosti ČLS JEP pro diagnostickou a terapeutickou koloskopii
- Vídeňské ozvěny
- 1st National Congress of Gastrointestinal Oncologywith international participation
- Výběr z mezinárodních časopisů
-
Správná odpověď na kvíz
Diferenciální diagnóza – Crohnova choroba nebo hypersekreční stav podmíněný hypergastrinemií? - Kreditovaný autodidaktický test: dětská gastroenterologie a hepatologie + bariatrie
- Kombinace sofosbuviru a velpatasviru (Epclusa®)
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Význam fekálního kalprotektinu v diagnostice a sledování dospělých a dětských pacientů s idiopatickými střevními záněty
- Budesonid MMX (Cortiment® 9 mg) v léčbě ulcerózní kolitidy v reálné klinické praxi
- Doporučené postupy České gastroenterologické společnosti ČLS JEP pro diagnostickou a terapeutickou koloskopii
- Endoskopický duodenojejunální bypass (EndoBarrier®) jako nový terapeutický přístup u obézních diabetiků 2. typu – efektivita a faktory predikující optimální efekt
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



