-
Články
Reklama
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaOxidační stres u nemocných po léčbě antracyklíny pro solidní nádorová onemocnění
Autoři: Kocík Miroslav 1; Zimovjanová Martina 2; Petruželka Luboš 2; Kodydková Jana 1; Vávrová Lucie 1; Žák Aleš 1
Působiště autorů: Charles University in Prague, 1. Faculty of Medicine, 4. Department of Internal Medicine, Czech Republic 1; Charles University in Prague, 1. Faculty of Medicine, Department of Oncology, Czech Republic 2
Vyšlo v časopise: Čas. Lék. čes. 2012; 151: 463-467
Kategorie: Původní práce
Souhrn
Východisko.
Antracyklíny jsou považovány za induktory oxidačního stresu. Přestože indukce oxidačního stresu je považována za významný faktor v rozvoji antracyklíny indukované kardiotoxicity, dynamika oxidačního stresu po jejich podání známá není. Cílem práce bylo posoudit úroveň oxidačního stresu u nemocných po léčbě solidních nádorů antracyklíny.Metody a výsledky.
Soubor představuje 128 pacientů (114/14 ženy/muži, průměrný věk 56 ± 10 let) se solidními nádory indikovanými k léčbě antracyklíny. Kontrolní skupina byla tvořena 38 jedinci (34/4 ženy/muži, průměrný věk 59 ± 11 let), u kterých nebylo nádorové onemocnění léčeno antracyklíny.
U všech zařazených jedinců byly před zahájením léčby a po jejím ukončení (medián 45; IQR 27–69 dní od ukončení léčby antracyklíny) stanoveny aktivity hlavních antioxidačních enzymů (kataláza, glutathionperoxidáza-1, superoxiddismutáza, paraoxonáza) a koncentrace konjugovaných dienů jako markerů úrovně oxidačního stresu. Porovnáním změn aktivit antioxidačních enzymů a koncentrací konjugovaných dienů byla posuzována dynamika změn úrovně oxidačního stresu v čase v rámci jednotlivých souborů a rovněž rozdíly v těchto změnách mezi dvěma studovanými soubory.Závěry.
U nemocných se solidními nádory léčených podle protinádorových protokolů obsahujících antracyklíny je přítomna i v odstupu po léčbě zvýšená úroveň oxidačního stresu. Naše práce však ukazuje, že zvýšený oxidační stres v tomto období patrně není způsoben vlastní léčbou antracyklíny.Klíčová slova:
oxidační stres, antracyklíny, solidní nádory.Úvod
Antracyklíny (ANTRA) představují základní součást léčebných protokolů řady nádorových onemocnění. Jsou to velmi účinná chemoterapeutika, jejichž nejobávanější komplikací je rozvoj kardiotoxicity (1–3). Kromě nepříliš často se vyskytující akutní kardiotoxicity je to především oddálená (chronická) forma kardiotoxity, která představuje závažný klinický problém. Přestože přesný mechanismus rozvoje antracyklínové kardiotoxicity není znám, předpokládáme, že nejvýznamnějším faktorem pro vznik této komplikace je oxidační stres (OS), jehož jsou prokazatelně ANTRA induktory (4).
O schopnosti ANTRA indukovat OS existuje řada dokladů, a mechanismus, jakým dochází k tomuto jevu je dopodrobna popsán na subcelulární a molekulární úrovni (5). Řada prací jak experimentálních tak klinických ukazuje, že po podání ANTRA dochází k rozvoji OS. Všechny tyto práce však prokazují indukci OS ANTRA v průběhu či časně po ukončení léčby (6–8). Na druhou stranu však k rozvoji chronické ANTRA indukované kardiotoxicity dochází až v oddáleném období po ukončení léčby a v současné době nemáme po ukončení léčby ANTRA žádných echokardiografických ukazatelů, které by byly schopny s dostatečnou senzitivitou a specificitou predikovat rozvoj dysfunkce levé komory srdeční a srdečního selhání.
Jaká je přesná patogeneze vzniku chronické ANTRA kardiotoxicity není přesně známo. Jedná se pouze o negativní impulz v průběhu léčby ANTRA s nastartováním morfologických a/nebo funkčních myokardiálních změn, které přestože nejsou našimi současně dostupnými metodami detekovatelné časně po léčbě dále běží autochtonně a v delším období nezadržitelně vedou k poškození srdce? Nebo dochází léčbou ANTRA k indukci déletrvajícího OS, který v delším časovém horizontu poškozuje srdce? Základní otázkou se tak z pohledu této problematiky jeví jako důležitá znalost dynamiky změn úrovně OS po podání ANTRA. Vzhledem k tomu, že indukce OS v průběhu a časně po podání ANTRA je dobře dokumentována (6–8), bylo cílem naší studie posoudit, zda-li zvýšená úroveň OS indukovaná léčbou ANTRA přetrvává i v delším období po ukončení této léčby.
SOUBOR NEMOCNÝCH A POUŽITÉ METODY
Studijní soubor
Studijní soubor představuje 128 pacientů (114/14 ženy/muži, průměrný věk 56 ± 10 let) se solidními zhoubnými nádory, kteří byli léčeni protokoly obsahující ANTRA. Kontrolní soubor je tvořen 38 jedinci (34/4 ženy/muži, průměrný věk 59 ± 11 let), u kterých nebylo nádorové onemocnění léčeno ANTRA. Obě sledované skupiny se nikterak nelišily v základních demografických údajích (tab. 1). Všichni pacienti zařazeni do studie podepsali informovaný souhlas.
Tab. 1. Základní demografické údaje sledovaných souborů 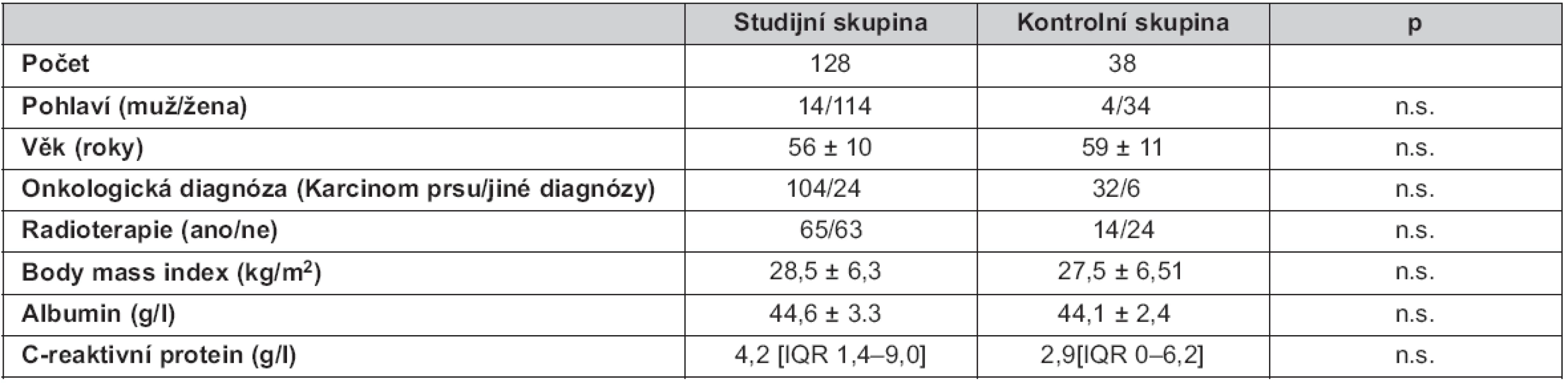
Počty jsou vyjadřovány v absolutních číslech. Kontinuální proměnné jako průměr ± SD (normální rozložení) nebo medián a IQR (nesplňující normální rozložení). Metody
Protokol studie
Ve studijní skupině byla před zahájením léčby ANTRA odebrána krev ke stanovení aktivit hlavních antioxidačních enzymů (kataláza, glutathionperoxidáza, superoxiddismutáza, paraoxonáza) a koncentrací konjugovaných dienů jako markeru modifikace makromolekul OS. Stejná vyšetření pak byla provedena po ukončení léčby ANTRA (127 ± 35 dní po zařazení do studie; což odpovídalo 45; IQR 27–69 dnům od ukončení léčby ANTRA). V kontrolní skupině byla kontrolní vyšetření provedena v době odpovídající době odběrů ve skupině studijní (doba kontrolních odběrů v kontrolní skupině: 143 ± 47 dní od zahájení léčby, nevýznamný rozdíl oproti studijní skupině (p = 0,07)).
Protokol studie byl schválen Etickou komisí Všeobecné fakultní nemocnice v Praze.
Laboratorní metody
Aktivita glutathionperoxidázy byla stanovována prostřednictvím modifikované metody Paglia and Valentine (9) za použití tert-butyl-hydroperoxidu jako substrátu. Do kyvety bylo k 580 μl tris-HCl pufru (172,4 mM, s 0,86 mM ethylendiamintetraoctové kyseliny, pH = 8,0) přidáno 100 μl 20 mM glutathionu, 100 μl 10 U/ml glutathionreduktázy, 100 μl 2 mM redukovaného nikotinamid adenin dinukleotid fosfátu a 100 ml zředěného vzorku. Po 10minutové inkubaci při 37 °C byla reakce nastartována přidáním 20 μl 9,99 mM tert-butyl-hydroperoxidu. Při 340 nm byla sledována degradace redukovaného nikotinamid adenin dinukleotid fosfátu, jehož extinkční koeficient byl využit k výpočtu aktivity glutathionperoxidázy (εNADPH 6220 M-1cm-1), která byla poté vyjádřená v jednotkách U/g hemoglobin.
Aktivita katalázy byla stanovována podle modifikované metody Aebiho (10). Jedná se o spektrofotometrické kinetické stanovení, při kterém je sledován úbytek peroxidu vodíku při 240 nm a 30 °C a aktivita je počítána pomocí molárního extinkčního koeficientu pro H2O2 (ε = 43,6 M-1cm-1). Reakční směs v kyvetě obsahuje 876 μl fosfátového pufru (50 mM, pH = 7,0) a 25 μl ředěného hemolyzátu erytrocytů a reakce je startována přidáním 99 μl H2O2 (zásobní roztok 10 mM). Aktivita je vyjádřena v jednotkách kU/g hemoglobinu.
Aktivita superoxiddismutázy byla měřena podle metody převzaté z práce Štípek et al. (11). Při této spektrofotometrické kinetické metodě je sledována tvorba nitrobluetetrazolin-formazanu při 540 nm. Reakční směs v kyvetě obsahuje 700 μl 50 mM fosfátového pufru (pH = 7,2), 50 μl xanthinoxidázy, 100 μl NBT a 50 μl zředěného vzorku. Reakce byla startována po 10 minutách inkubace při 25 °C přidáním 100 μl 1 mM xanthinu. Aktivita je počítána z kalibrační křivky a vyjádřena v jednotkách kU/g hemoglobinu.
Arylesterázová aktivita paraoxonázy-1 byla měřena podle metody Eckerson et al. (12) za použití fenylacetátu jako substrátu. Do 900 μl Tris-HCl pufru (20 mM, s 1 mM CaCl2, pH = 8,0) bylo přidáno 50 μl zředěného vzorku. Reakce byla zahájena přidáním 50 μl 100 mM fenylacetátu. Sledován byl nárůst absorbance při 270 nm, způsobený rozkladem fenylacetátu na fenol. Aktivita byla počítána s použitím molárního extinkčního koeficientu pro fenol (1310 M-1cm-1) a vyjádřena v jednotkách U/ml séra.
Koncentrace konjugovaných dienů v precipitovaných lipidech o nízké hustotě (LDL): Sérové LDL byly izolovány srážecí metodou dle Ahotupa et al (13). Koncentrace konjugovaných dienů v precipitovaných LDL byla měřena modifikovanou metodou dle Wieland et al (14). Srážecí pufr složený z 0,064 M citrátu sodného a 50 000 IU/l heparinu byl upraven na pH 5,05 pomocí 5 M kyseliny chlorovodíkové. Vzorek – 110 μl séra s přídavkem ethylendiamintetraoctové kyseliny (10 : 01 V/V) byl přidán do 1 ml citrátového pufru. Po promíchání se suspenze inkubuje 10 minut při pokojové teplotě. Vysrážené lipoproteiny byly pak odděleny centrifugací při 2800 otáčkách za minutu po dobu 10 min. Supernatant byl odstraněn a sraženina byla rozpuštěna ve 100 μl izotonického roztoku NaCl (9g/l). Lipidy byly extrahovány směsí chloroform – methanol (2 : 1), směs byla inkubována 10 minut s častým mícháním, poté bylo přidáno 250 μl redestilované vody k rozdělení fází. Směs se stáčí při 3000 otáčkách za minutu po dobu 5 minut. Po odstředění se 800 μl nižší vrstvy (infranatant) suší pod dusíkem, následně se rozpustí ve 300 μl cyklohexanu. Koncentrace konjugovaných dienů v precipitovaných LDL byla měřena spektrofotometricky při 234 nm. Koncentrace konjugovaných dienů v precipitovaných LDL byla počítána s pomocí molárního extinkčního koeficientu 2,95 × 104 M-1cm-1 a vyjádřena v mmol/l séra.
Statistické metody
Kontinuální proměnné (data) s normálním rozložením jsou vyjadřovány jako průměr ± směrodatná odchylka (SD). Kontinuální proměnné (data) nesplňující normální rozložení jsou vyjadřována jako medián a interkvartilní rozdíl (IQR; 25.–75. percentil).
χ2-test (s korekcí dle Yatese v případě potřeby) byl použit k porovnávání rozdílů souborů v případě kategorických proměnných. Studentův t-test byl použit k porovnávání rozdílů souborů v případě kontinuálních proměnných.
Všechny testy byly dvoustranné a chyba 1. druhu p < 0,05 % byla považována za statisticky významnou. K posouzení míry závislosti dvou kontinuálních proměnných byl vypočten Pearsonův korelační koeficient. K výpočtům byl použit statistický software Microsoft Excel.
Výsledky
Aktivity antioxidačních systémů před zahájením léčby antracyklíny
Nebyl nalezen žádný statisticky významný rozdíl v aktivitách katalázy, glutathionperoxidázy, superoxiddismutázy a paraoxonázy-1 mezi studijní a kontrolní skupinou (tab. 2).
Tab. 2. Vstupní aktivity katalázy, glutathionperoxidázy, superoxiddismutázy, paraoxonázy-1 a koncentrace konjugovaných dienů u studovaných souborů 
Vysvětlivky: Hodnoty představují průměr ± SD. Statistické hodnocení: dvoustranný Studentův t-test. Koncentrace konjugovaných dienů v LDL před zahájením léčby antracyklíny
Nebyl nalezen žádný statisticky významný rozdíl v koncentracích konjugovaných dienů mezi studijní a kontrolní skupinou (tab. 2).
Časový průběh změn aktivit antioxidačních enzymů
Ve studijní skupině byly nalezeny při kontrolním vyšetření statisticky významné změny v aktivitách katalázy, glutathionperoxidázy a paraoxonázy-1 oproti vstupnímu vyšetření (tab. 3). V kontrolní skupině pak byly nalezeny statisticky významné změny v aktivitách katalázy, glutathionperoxidázy a superoxiddismutázy (tab. 4). Nicméně porovnáním změn mezi studijní a kontrolní skupinou nebyl nalezen žádný signifikantní rozdíl ve změnách aktivit sledovaných antioxidačních enzymů po léčbě v porovnání se vstupními hodnotami. (ΔKatalázastudijní vs. kontrolní: p = 0,18; ΔGlutathionperoxidázastudijní vs. kontrolní: p = 0,68; ∆Superoxiddismutázastudijní vs. kontrolní: p = 0,07; ΔParaoxonáza-1studijní vs. kontrolní: p = 0,74).
Tab. 3. Změny aktivit antioxidačních enzymů a koncentrací konjugovaných dienů u nemocných léčených antracyklíny 
Vysvětlivky: Hodnoty představují průměr ± SD. Statistické hodnocení: dvoustranný Studentův t-test. Tab. 4. Změny aktivit antioxidačních enzymů a koncentrací konjugovaných dienů v LDL u nemocných kontrolní skupiny 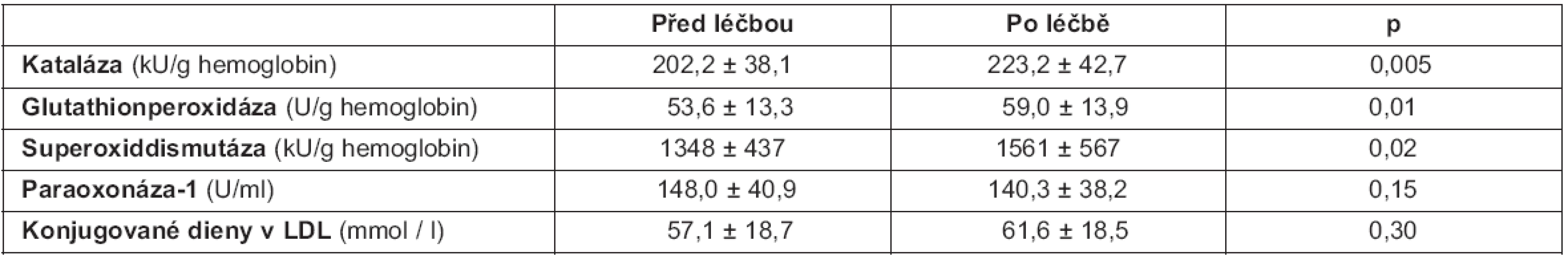
Vysvětlivky: Hodnoty představují průměr ± SD. Statistické hodnocení: dvoustranný Studentův t-test. Časový průběh změn koncentrací konjugovaných dienů
Ve studijní skupině byly nalezeny při kontrolním vyšetření statisticky významné změny v koncentracích konjugovaných dienů oproti vstupnímu vyšetření (tab. 3). V kontrolní skupině pak nebyly nalezeny statisticky významné změny (tab. 4). Nicméně porovnáním změn mezi studijní a kontrolní skupinou nebyl nalezen žádný signifikantní rozdíl ve změnách koncentrací konjugovaných dienů po léčbě v porovnání se vstupními hodnotami (ΔKonjugované dienystudijní vs. kontrolní: p = 0,91).
Diskuze
Výsledky naší práce ukazují, že u nemocných se solidními nádory podstupujících protinádorovou léčbu protokoly obsahující ANTRA dochází k déletrvajícímu (v případě naší studie 45; IQR 27–69 dní od ukončení léčby ANTRA) vzestupu aktivit hlavních antioxidačních enzymů (kataláza, glutathionperoxidáza) a produktů oxidačního stresu (konjugované dieny v precipitovaných LDL), který však velmi pravděpodobně není způsoben léčbou ANTRA. Naše práce tak ukazuje na přítomnost dlouhodobého OS u nemocných léčených ANTRA pro solidní nádory, tento však není vázán na léčbu ANTRA.
Antracykliny jsou považovány za mocné induktory OS (4). Indukce oxidačního stresu ANTRA je v experimentu velmi dobře dokumentována, a mechanismus jeho vzniku je podrobně popsán na subcelulární i molekulární úrovni (5). Méně informací máme o stupni a dynamice OS indukovaného léčbou ANTRA u lidí. Několik studií ukázalo, že k indukci OS v průběhu léčby ANTRA u lidí dochází (6–8). Tyto studie však nesledovaly změny zvolených parametrů OS u kontrolní skupiny jedinců se stejným typem onemocnění léčených jiným způsobem. Nelze tak spolehlivě říci, že pozorovaná indukce OS je způsobená pouze léčbou ANTRA a zda-li se na této nepodílí i další možné faktory. Z pohledu další dynamiky OS u nemocných léčených ANTRA mnoho informací nemáme. Dle našich znalostí pouze jedna studie zkoumala úroveň OS u nemocných po léčbě ANTRA. Tato studie přetrvávající elevaci OS v delším období (3–12 měsíců od ukončení léčby) po léčbě ANTRA neprokázala (15).
Naše studie dále výše citované znalosti doplňuje. V naší práci byla v období s mediánem 45 dní od ukončení léčby ANTRA prokázána zvýšená aktivita sledovaných antioxidačních enzymů a produktů OS oproti stavu před zahájením léčby. Vzhledem k tomu, že obdobné změny byly pozorované i v kontrolní skupině, nebyly tyto zjištěné změny způsobeny vlastní léčbou ANTRA. Příčinou přetrvávající zvýšené úrovně OS u nemocných po léčbě ANTRA tak patrně jsou jiné faktory jak léčba ANTRA. Odběry v případě naší studie probíhaly sice po ukončení léčby ANTRA, nicméně u řady pacientů za dále pokračující léčby – jiná chemoterapie a/nebo radioterapie (jiná chemoterapie ve studijní skupině u 59 % nemocných (z toho 59 % taxany), jiná chemoterapie v kontrolní skupině u 26 % nemocných (p = 0,0007); radioterapie ve studijní skupině u 51 % nemocných, radioterapie v kontrolní skupině u 37 % nemocných (p = 0,14)). Přestože by bylo možné spekulovat o možném vlivu této pokračující léčby na úroveň OS, v případě naší studie se nepodařilo prokázat při porovnání úrovně OS mezi pacienty s pokračující léčbou (chemoterapie a/nebo radioterapie) a pacienty bez takovéto léčby žádný statisticky významný rozdíl ve změně aktivit sledovaných antioxidačních enzymů či koncentracích konjugovaných dienů. U sledovaných pacientů došlo po léčbě dále k signifikantnímu poklesu hemoglobinu (p < 0,00001) a albuminu (p = 0,00004) oproti období před léčbou, další z možných faktorů, které mohou být spojeny s indukcí OS (anémie, malnutrice). Rovněž v tomto případě však žádná korelace mezi změnou koncentrace hemoglobinu či albuminu a změnou aktivit sledovaných antioxidačních systémů a/nebo koncentrací konjugovaných dienů nalezena nebyla, s výjimkou paraoxonázy-1, kde byla nalezena pozitivní korelace mezi změnami jak koncentrace albuminu, tak hemoglobinu na straně jedné a změnou aktivity PON-1 (Δalbumin/Δparaoxonáza-1: r = 0,25; p = 0,002, Δhemoglobin/Δparaoxonáza-1: r = 0,25; p < 0,0001) po léčbě v porovnání s hodnotami před léčbou.
Lze tak na základě známých literárních údajů a výsledků naší studie uzavřít, že u lidí ANTRA patrně vedou k indukci OS v průběhu léčby (6). V odstupu po ukončení léčby ANTRA přetrvává u nemocných léčených protokoly obsahujícími ANTRA zvýšená úroveň OS, která však není způsobena léčbou ANTRA, ale patrně jinými faktory: vliv vlastního nádoru, účinnost antioxidačních enzymů, následek další protinádorové léčby (mimo ANTRA) a komplikace základního onemocnění. V dlouhodobém horizontu (3–12 měsíců) po ukončení léčby ANTRA poté zvýšená úroveň OS prokazatelná není (13).
Z hlediska ANTRA indukované kardiomyopatie však tyto nálezy s sebou přináší několik otázek. Vzhledem k tomu, že ANTRA indukovaný OS je přítomen pouze v době léčby ANTRA, zůstává mechanismus rozvoje ANTRA indukované kardiomyopatie nejasný. Je pravděpodobné, že by změny způsobené OS v průběhu léčby ANTRA nebyly spolehlivě detekovatelné, a přesto samy o sobě postupně vedly k rozvoji ANTRA kardiomyopatie? Přestože po léčbě ANTRA jsou pozorovatelné morfologické i funkční změny myokardu, žádná z těchto změn doposud není schopna předpovědět rozvoj ANTRA kardiomyopatie a je tak otazné, zda-li tyto změny nejsou spíše odrazem akutní ANTRA kardiotoxicity. Považujeme-li OS za důležitý faktor v rozvoji ANTRA indukované kardiomyopatie, poté je navíc zcela neznámo, jak se na rozvoji ANTRA indukované kardiomyopatie podílí OS, který ANTRA indukován není (OS spojený se základním nádorovým onemocněním, OS spojený s jinou léčbou, OS spojený s komplikacemi onemocnění/léčby).
Limitace
Ve vztahu k ANTRA indukované kardiotoxicitě, která je primárním cílem našeho programu, je významnou limitací této studie skutečnost, že úroveň OS byla zjišťována na systémové úrovni a nikoliv na úrovni srdečního svalu, neboť nemáme žádných důkazů o tom, že systémová úroveň OS koreluje s úrovní OS na úrovni kardiomyocytu. Primárním cílem naší studie však bylo posoudit úroveň OS indukovaným léčbou ANTRA, proto námi zdůrazněná limitace nemá žádný vliv na výsledky studie, pouze představuje limitaci k aplikaci těchto výsledků na vlastní ANTRA indukovanou kardioxicitu.
Závěr
U nemocných se solidními nádory léčených protinádorovými protokoly obsahujícími ANTRA je přítomna i v odstupu po léčbě zvýšená úroveň OS. Naše práce však ukazuje, že zvýšený OS v tomto období již není způsoben vlastní léčbou ANTRA. Přestože důvod pro přetrvávající elevaci OS po léčbě ANTRA jasný není, lze předpokládat pokračující vliv nádorového onemocnění či komplikací ostatní léčby a/nebo základního onemocnění.
Považujeme-li pak zvýšený OS (indukovaný léčbou ANTRA) za významný faktor v rozvoji ANTRA indukované kardiotoxicity, zůstává otázkou, jak a jakou měrou se na rozvoji ANTRA indukované kardiotoxicity podílí OS indukovaný jinými faktory.
Zkratky
- ANTRA – antracyklíny
- IQR – interkvartilní rozdíl
- LDL – lipidy o nízké hustotě
- OS – oxidační stres
- SD – směrodatná odchylka
Práce byla podpořena grantem IGA MZ ČR NS 9774-4.
Adresa pro korespondenci:
MUDr. Miroslav Kocík, Ph.D.
IV. interní klinika 1. LF UK a VFN
U Nemocnice 2, 128 08 Praha 2
fax: +420 2 24 96 28 79
e-mail: miroslav.kocik@seznam.cz
Zdroje
1. Eschenhagen T, Force T, Ewer MS, et al. Cardiovascular side effects of cancer therapies: a position statement from the heart failure association of the European society of cardiology. Eur J Heart Fail 2011; 13 : 1–10.
2. Swain S, Whaley F, Ewer M. Congestive heart failure in patients treated with doxorubicin: a retrospective analysis of three trials. Cancer 2003; 97 : 2869–2879.
3. Bovelli D, Plataniotis G, Roila F. Cardiotoxicity of chemotherapeutic agents and radiotherapy-related heart disease: ESMO Clinical Practice Guidelines. Annals of Oncology 2010; 21(Suppl 5): v277–v282.
4. Sangeetha P, Das UN, Koratkar R, Suryaprabha P. Increase in free radical generation and lipid peroxidation following chemotherapy in patients with cancer. Free Rad Biol Med 1990; 8 : 15–19.
5. Minotti G, Menna P, Salvatorelli E, Cairo G, Gianni L. Anthracyclines: molecular advances and pharmacologic developments in antitumor activity and cardiotoxicity. Pharmacol Rev 2004; 56 : 185–229.
6. Atukeren P, Yavuz B, Soydine HO, Purisa S., Camlica H, Gumustas MK, Balcioglu I. Variations in systemic biomarkers of oxidative/nitrosative stress and DNA damage before and during the consequent two cycles of chemotherapy in breast cancer patients. Clin Chem Lab Med 2010; 48 : 1487–1495.
7. Erhola M, Kellokumpu-Lehtinen P, Metsa-Ketela T, Alanko K, Nieminen MM. Effects of anthracyclin-based chemotherapy on total plasma antioxidant capacity in small cell lung cancer patients. Free Radic Biol Med 1996; 21 : 383–390.
8. Il’yasova D, Mixon G, Wang F, Marcom PK, Marks J, Spasojevich I, Graft N, Arredondo F, DiGiulio R. Markers of oxidative status in a clinical model of oxidative assault: a pilot study in human blood following doxorubicin administration. Biomarkers 2009; 14 : 321–325.
9. Paglia DE., Valentine WN. Studies on the quantitative and qualitative characterization of erythrocyte glutathione peroxidase. J Lab Clin Med 1967; 70 : 158–169.
10. Aebi H, Bergmeyer HU. Catalase. In: Methods of enzymatic analysis. Weinheim: Verlag Chemie 1974; 673–684.
11. Štípek S, Crkovská J, Dvořák V. Spectrophotometric assay for superoxide dismutase controlled by PC programme developed in LabWindows system. Klin Biochem Metab 1995; 3 : 93–97.
12. Eckerson HW, Wyte CM. La Du BN. The human serum paraoxonase/arylesterase polymorfphism. Am J Genet 1983; 35 : 1126–1138.
13. Ahotupa M, Ruutu M, Mantyla E. Simple methods of quantifying oxidation products and antioxidant potential of low density lipoproteins. Clin Biochem 1996; 29 : 139–144.
14. Wieland H, Seidel D. A simple specific method for precipitation of low density lipoproteins. J Lipid Res 1983; 24 : 904–909.
15. Mantovani G, Madeddu C, Cadeddu C, Dessi M, Piras A, Mass E, Serpe R, Antoni C, Mercuro G. Perzistence, up to 18 months of follow up, of epirubicin induced myocardial dysfunction detected early by serial tissue Doppler echocardiography: correlation with inflammatory and oxidative stress markers. The Oncologist 2008; 13 : 1296–1305.
Štítky
Adiktologie Alergologie a imunologie Anesteziologie a resuscitace Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská dermatologie Dětská gastroenterologie Dětská gynekologie Dětská chirurgie Dětská kardiologie Dětská nefrologie Dětská neurologie Dětská onkologie Dětská otorinolaryngologie Dětská pneumologie Dětská psychiatrie Dětská radiologie Dětská revmatologie Dětská urologie Diabetologie Endokrinologie Farmacie Farmakologie Fyzioterapie Gastroenterologie a hepatologie Genetika Geriatrie a gerontologie Gynekologie a porodnictví Hematologie a transfuzní lékařství Hygiena a epidemiologie Hyperbarická medicína Chirurgie cévní Chirurgie hrudní Chirurgie plastická Chirurgie všeobecná Infekční lékařství Intenzivní medicína Kardiochirurgie Kardiologie Logopedie Mikrobiologie Nefrologie Neonatologie Neurochirurgie Neurologie Nukleární medicína Nutriční terapeut Obezitologie Oftalmologie Onkologie Ortodoncie Ortopedie Otorinolaryngologie Patologie Pediatrie Pneumologie a ftizeologie Popáleninová medicína Posudkové lékařství Praktické lékařství pro děti a dorost Protetika Psychologie Radiodiagnostika Radioterapie Rehabilitační a fyzikální medicína Reprodukční medicína Revmatologie Sestra Sexuologie Soudní lékařství Stomatologie Tělovýchovné lékařství Toxikologie Traumatologie Urgentní medicína Urologie Laboratoř Domácí péče Foniatrie Algeziologie Zdravotnictví Dentální hygienistka Student medicíny
Článek „Governance“ pro zdraví lidíČlánek Christian René de Duve
Článek vyšel v časopiseČasopis lékařů českých
Nejčtenější tento týden
- Při preskripci inkontinenčních pomůcek je nezbytné hlídat limity
- Příznivý vliv Armolipidu Plus na hladinu cholesterolu a zánětlivé parametry u pacientů s chronickým subklinickým zánětem
- Když se ve střevech děje něco nepatřičného...
-
Všechny články tohoto čísla
- „Governance“ pro zdraví lidí
- Sexuálně přenosné infekce a spermicidy
- Oxidační stres u nemocných po léčbě antracyklíny pro solidní nádorová onemocnění
- Jak chránit buňku před TNF smrtí
- Aktuální koncepce ošetření závažných poranění v Traumatologickém centru Fakultní nemocnice Královské Vinohrady
- Pseudoaneuryzma jaterní tepny fistulující do žlučových cest jako příčina opakovaných melén
- Spolek českých lékařů v Praze
- Jak číst kriticky odborné články
- Identifikace určujících regulátorů a role HLA allel
- „Kádrový posudek“ na chirurga Viléma Weisse z roku 1875
- XIV. kongres mladých otorinolaryngologů s mezinárodní účastí
- Plánované akce odborných složek ČLS JEP
-
Novinky v otorinolaryngologii
Humpolec, 30. až 31. března 2012 -
XVI. česko-slovenský kongres o infekčních nemocech
Ostrava, 6. až 8. června 2012 - Christian René de Duve
- Časopis lékařů českých
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Sexuálně přenosné infekce a spermicidy
- XIV. kongres mladých otorinolaryngologů s mezinárodní účastí
- Jak číst kriticky odborné články
- Aktuální koncepce ošetření závažných poranění v Traumatologickém centru Fakultní nemocnice Královské Vinohrady
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



