-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
XVI. kardioanesteziologické vědecké dny s mezinárodní účastí
Vybrané souhrny přednášek
Vyšlo v časopise: Anest. intenziv. Med., 26, 2015, č. 6, s. 364-371
Kategorie: Kongresy a konference
Pardubice 21.–22. května 2015
SLOVO NA ÚVOD I NA ZÁVĚR...
Vážení čtenáři, milé kolegyně, milí kolegové
je mi líto oznámit Vám jménem celého organizačního výboru, že soubor abstrakt z XVI. kardioanesteziologických vědeckých dní s mezinárodní účastí v Pardubicích, který máte možnost si v tomto čísle časopisu Anesteziologie a intenzivní medicína přečíst, je posledním! Letos jsme se sešli 21. a 22. května pod záštitou primátora krajského města Pardubice opět v moderním prostředí AFI Paláce na konci pěší zóny v centru města. Součástí programu byly 2 satelitní workshopy pro lékaře i sestry: „Komplexní hrudní péče“ a „Možnosti zajištění dýchacích cest“. V hlavním programu v pátek ve 3 blocích zaznělo 13 lékařských přednášek, 1 příspěvek od kolegů perfuzionistů a 1 pro-con debata, po kterých se většinou rozvinuly zajímavé debaty. Své příspěvky prezentovala téměř všechna kardiocentra v Česku a také kolegové z Polska, Rakouska a Slovenska. Pro nedostatek prostoru jsme některé nabízené přednášky museli odmítnout.
Příčin, proč podnik pořádaný úspěšně šestnáctkrát po sobě končí, je nepochybně celá řada. Těmi nejhlavnějšími jsou ekonomické důvody spolu s omezenou „populací“ kardioanesteziologů. Po několika předchozích ročnících, kdy přípravy vždy provázel urputný boj o finanční příspěvky od sponzorů a kdy účast lékařů, sester a firem postupně klesala, jsme se rozhodli další, takto úzce zaměřenou akci již nepořádat. KARIM VFN a 1. LF UK v Praze se tak může soustředit na další odborná sympozia, která tradičně organizuje – Hoderův den, četné kurzy, satelitní sympozia kongresů atd.
Pro zájemce o anestezii a intenzivní péči v kardiochirurgii je určitě dobrou zprávou, že o novinky a zajímavosti z našeho oboru ochuzeni nebudou. Blok přednášek bude velmi pravděpodobně od roku 2016 součástí národního kongresu ČSARIM.
Na závěr mi dovolte poděkovat všem sponzorům, tradičním či jen občasným účastníkům „Pardubic“ za přízeň, kterou nám věnovali a především organizátorům za nemalou práci, kterou při přípravách vždy vykonali.
Praha 23. 7. 2015
Za organizační výbor
doc. MUDr. Jan Kuns
PRO: iNO v kardiochirurgii
Říha H.1, 2, Matloch Z.1, Kotulák T.1, 2
1Klinika anesteziologie a resuscitace, Kardiocentrum IKEM, Praha
2Klinika anesteziologie, resuscitace a intenzivní medicíny, 1. LF UK, Praha
Inhalační oxid dusnatý (iNO) patří mezi selektivní vazodilatancia plicního řečiště; při jeho aplikaci dochází k dilataci plicních cév v oblasti ventilovaných alveolů, neventilované oblasti a systémové řečiště neovlivňuje [1]. Popis účinků iNO ve smyslu poklesu dotížení (afterload) pravé komory se zlepšením její funkce v klinické praxi spadá do poloviny 90. let minulého století [2]. Patofyziologickým podkladem relaxace hladké svaloviny v plicním řečišti je vzestup koncentrace cGMP po stimulaci guanylátcyklázy podávaným iNO. Poločas iNO je několik sekund; je deaktivován hemoglobinem za vzniku nitrosyl-hemoglobinu, který je okamžitě oxidován na methemoglogin a ten redukován zpět na hemoglobin [3]. Dříve popisované riziko vzniku methemoglobinémie bylo spojeno s vysokými dávkami iNO (80 ppm), které se dnes již nepoužívají.
Vzhledem k relativně vysoké ceně iNO je v posledních 10 letech hledána vhodná alternativa; jednu z molekul představuje prostacyklin (PGI2 v podobě epoprostenolu [poločas 5 min] nebo iloprostu [poločas 30 min]). Na buněčné úrovni zvyšuje prostacyklin koncentraci intracelulárního cAMP (podobně jako např. inhibitory fosfodiesterázy [PDE] III často používané u dysfunkce/selhání pravé komory). Jediná klinická studie, která přímo porovnávala iNO s inhalačním iloprostem v kardiochirurgii, měla řadu významných omezení; pacienti ve skupině iNO měli statisticky významně vyšší hodnoty EuroSCORE, aplikace obou farmak byla velmi krátká (pouze pro odpojení od mimotělního oběhu), v některých okamžicích ovlivňoval hemodynamiku příznivěji iloprost, někdy naopak iNO [4].
U pacientů s ARDS zlepšuje iNO výměnu krevních plynů, ale bohužel nesnižuje mortalitu [5]. Jedním z důvodů může být relativně dlouhá aplikace iNO ve studiích s ARDS (typicky > 7 dnů), protože takto dlouhá aplikace je spojena s vyšším výskytem poškození ledvin (AKI) [6].
Na našem pracovišti využíváme iNO v kardiochirurgii dospělých jako standardní součást komplexní strategie k podpoře funkce pravé komory (inhibitory PDE III, levosimendan, úprava rytmu a volémie, …) ve třech typických situacích: transplantace srdce [7], implantace dlouhodobých levostranných mechanických srdečních podpor (LVAD) [8] a komplexní kardiochirurgické výkony u pacientů s plicní hypertenzí [9]. Aplikaci dávek 5–20 ppm (výjimečně až 30–40 ppm) zahajujeme již v době odpojování od mimotělního oběhu a pokračujeme po dobu 12–72 h s postupným weaningem (á 5 ppm) a přechodem na intravenózně podávaný sildenafil (inhibitor PDE V).
Literatura
- Haddad, E., Lowson, S. M., Johns, R. A. et al. Use of inhaled nitric oxide perioperatively and in intensive care patients. Anesthesiology, 2000, 92, 6, s. 1821–1825.
- Rossaint, R., Slama, K., Steudel, W. et al. Effects of inhaled nitric oxide on right ventricular function in severe acute respiratory distress syndrome. Intensive Care Med., 1995, 21, 3, s. 197–203.
- Creagh-Brown, B. C., Griffiths, M. J., Evans, T. W. Bench-to--bedside review: Inhaled nitric oxide therapy in adults. Crit. Care, 2009, 13, 3, s. 221.
- Winterhalter, M., Simon, A., Fischer, S. et al. Comparison of inhaled iloprost and nitric oxide in patients with pulmonary hypertension during weaning from cardiopulmonary bypass in cardiac surgery: a prospective randomized trial. J. Cardiothorac. Vasc. Anesth., 2008, 22, 3, s. 406–413.
- Adhikari, N. K., Dellinger, R. P., Lundin, S. et al. Inhaled nitric oxide does not reduce mortality in patients with acute respiratory distress syndrome regardless of severity: systematic review and meta-analysis. Crit. Care Med., 2014, 42, 2, s. 404–412.
- Ruan, S. Y., Huang, T. M., Wu, H. Y. et al. Inhaled nitric oxide therapy and risk of renal dysfunction: a systematic review and meta-analysis of randomized trials. Crit. Care, 2015, 19, 1, s. 137.
- Costanzo, M. R., Dipchand, A., Starling, R. et al. The International Society of Heart and Lung Transplantation Guidelines for the care of heart transplant recipients. J. Heart Lung Transplant., 2010, 29, 8, s. 914–956.
- Říha, H., Netuka, I., Kotulák, T. et al. Dysfunkce pravé komory po implantaci levostranné mechanické srdeční podpory. Vnitř. Lék., 2010, 56, 1, s. 30–36.
- Germann, P., Braschi, A., Della Rocca, G. et al. Inhaled nitric oxide therapy in adults: European expert recommendations. Intensive Care Med., 2005, 31, 8, s. 1029–1041.
CON: iNO v kardiochirurgii
Kunstýř J.
KARIM VFN Praha a 1. LF UK v Praze
Perioperační kontrola a léčba plicní hypertenze je důležitým aspektem anesteziologické péče v průběhu kardiochirurgické operace, protože má významný vliv na rozvoj především pravostranného srdečního selhání. A to zejména u pacientů, kteří podstupují kombinované operace již s pravostrannou dysfunkcí, trpí předoperačně některou formou plicní hypertenze anebo u nemocných indikovaných k transplantaci srdce či implantaci levostranné srdeční podpory [1]. Inhalačně podávaný NO byl od počátku 90. let minulého století prvním účinným, lokálně aplikovaným prostředkem s minimálním či prakticky nulovým účinkem na systémovou cirkulaci. Stal se proto velmi populárním ve výše zmíněných i dalších indikacích [2]. Vzhledem k jeho potenciálně toxickým metabolitům (NO2, methemoglobin) vznikajícím pouze při vysokém dávkování, popsanému rebound fenomenu, možnosti aplikace jen během UPV a hlavně z farmako-ekonomických důvodů se hledaly adekvátně potentní, ale méně toxické a levnější náhrady. Jsou jimi nebulizací podávané látky ze skupiny prostaglandinů – nejdříve prostacyklin, později epoprostenol či nejnověji iloprost. Zvyšují intracelulární produkci cAMP, a proto mají s NO synergický účinek (ten funguje cestou cGMP). Díky spontánní hydrolýze mají poločas v řádu minut (NO je deaktivován v sekundách vazbou na hemoglobin červených krvinek) a ve standardním dávkování také jako NO postrádají klinicky významný systémový efekt na krevní tlak. Jejich cena i náklady na kvalitní nebulizátory ale tvoří zlomek nákladů, spojených s podáváním a analýzou koncentrací NO i jeho vedlejších produktů v dýchacích cestách [3] – tabulka 1.
Tab. 1. Farmakoekonomické srovnání NO a iloprostu 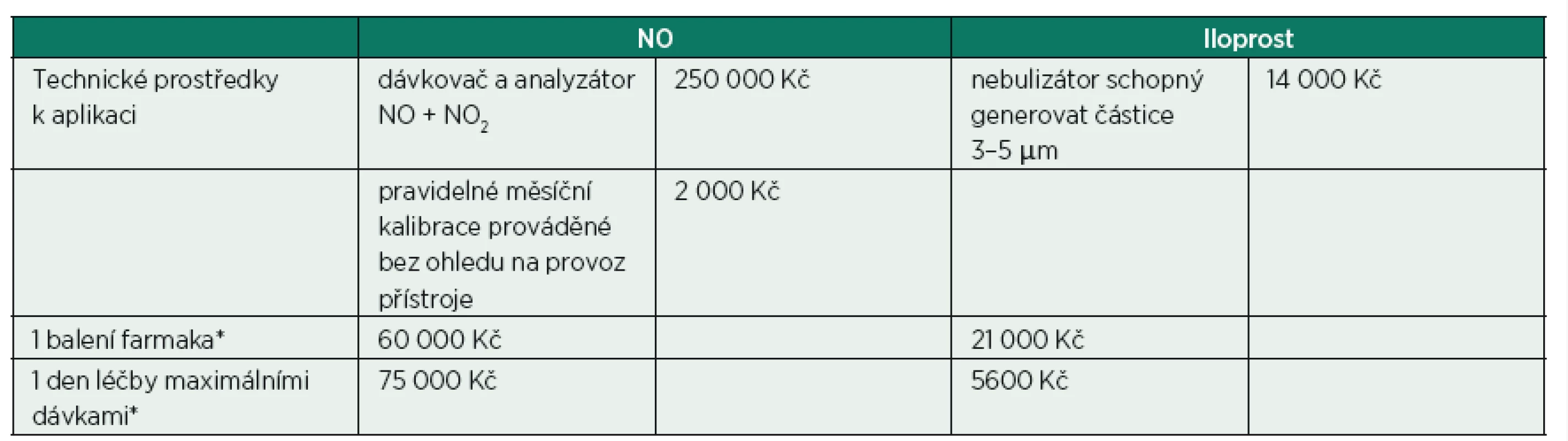
*Cenové kalkulace vycházejí z aktuálního kurzu USD a Kč a z aktuálních cen v nemocniční lékárně VFN. Z hlediska medicíny založené na důkazech neexistuje jasná evidence favorizující NO proti inhalačním prostaglandinům (a vice versa). Studie, které sledovaly účinky NO, prostaglandinů i dalších selektivně podávaných látek (milrinon, nitroglycerin a další) zahrnovaly malé počty pacientů a sledovaly ponejvíce hemodynamické, echokardiografické či jiné vedlejší cíle a nebyly zaměřené na porovnání výsledků. Taková je i jediná práce přímo srovnávající účinky NO a iloprostu [4]. Autoři zmíněných článků vesměs v závěrech svých prací uvádějí, že existují látky levnější a klinickým účinkem srovnatelné s inhalačním NO, ne-li superiorní. Nevidíme proto důvod k podávání NO dospělým pacientům v kardiochirurgii.
Literatura
- Maslow, A., Regan, M., Panzica, P. et al. Precardiopulmonary bypass right ventricular function is associated with poor outcome after coronary artery bypass grafting in patients with severe left ventricular systolic dysfunction. Anesth. Analg., 2002, 95, p. 1507–1518.
- Augoustides, J. G., Ochroch, E. A. Perioperative use of nitric oxide in cardiothoracic anesthesia and intensive care. Prog. Anesth., 2001, 15, p. 115–124.
- Augoustides, J. G., Ochroch, E. A. Pro: Inhaled Prostaglandin as a Pulmonary Vasodilator Instead of Nitric Oxide. J. Cardiothorac Vasc. Anesth., 2005, 19, 3, p. 400–402.
- Winterhalter, M., Simon, A., Fischer, S. et al. Comparison of inhaled iloprost and nitric oxide in patients with pulmonary hypertension during weaning from cardiopulmonary bypass in cardiac surgery: a prospective randomized trial. J. Cardiothorac Vasc. Anesth., 2008, 22, 3, p. 406–413.
New Guidelines of the Polish Society of Anaesthesiology and Intensive Therapy regarding termination of futile therapy in ICU patients incapable of giving informed statements of will
Nadziakiewicz P.
Zabrze, Poland
Objectives: Intensive care has created new possibilities for the effective treatment of severe diseases and traumas. The maintenance of organ functions can lead to patient’s recovery or can also prolong the process of dying and be of no benefit to patients.
Aim: Aim is to present Guidelines regarding the ineffective maintenance of organ functions (futile therapy) in ICU patients incapable of giving informed statements of will.
Body: Maintenance of organ functions which is of no benefit to patient and does not enable the achievement of the therapeutic goals is defined as futile therapy, and is considered medical malpractice.
The guidelines aim to define the best clinical practice for ICU patients whose therapy maintaining organ functions has become futile.
De-escalation of treatment can involve: withholding or withdrawing of treatment that is maintaining organ functions that are not beneficial to patients means that patients are provided with care; only the aim of treatment is different. Since the therapy is of no benefit to the patient, the further maintenance of organ functions is no longer its goal. The crucial therapeutic objective is to provide the patient with optimal comfort, which involves specialist nursing care, the elimination of adverse symptoms, such as pain, anxiety, dyspnea, seizures, fever, etc., nutrition and hydration as required.
- Proper communication with the patient and his/her relatives is essential for the appropriate therapeutic process during the period of dying, and for de-escalation of futile therapy.
- The decisions to de-escalate futile therapy are taken by two physicians of the attending team, specialists in anaesthesiology and intensive therapy or intensive Therapy, with the approval of the chief of the department. They can additionally contact some other specialists, if they find this is reasonable.
- Withholding or withdrawing the maintenance of organ functions particularly regards the following methods:
- cardiopulmonary resuscitation,
- mechanical ventilation,
- cardiac electrotherapy,
- mechanical circulatory support, and
- pharmacological liver support.
Improper use of the above methods of management only prolongs the process of dying.
- The provision of palliative treatment is to relieve suffering by making the most effective use of analgesics, sedatives or hypnotics. Palliative treatment must not hasten the natural process of dying.
- Each decision regarding de-escalation of futile therapy should have its clear written justification and cannot be conditioned by treatment costs or organisational aspects.
- Having decided to limit the maintenance of organ functions, the attending team adjusts to the management plan accepted, which can be modified in well-grounded cases.
- All actions purposefully aimed at causing or hastening death are medically, ethically and legally impermissible.
- The decision to withhold or withdraw the interventions maintaining organ functions is a formal procedure of management in the intensive care stations. It should be recorded in medical records (preferably in the form of a separate protocol), with a detailed description justifying the above-mentioned decision.
Anaesthesiology Intensive Therapy 2014, vol. 46, no 4, 215–220.
Kardiochirurgické výkony u osmdesátníků – pooperační výsledky a kvalita života
Pořízka M.1, Kunštýř J.1, Vaněk T.2, Novotný M.2,Jehlička P.3, Bucková J.3, Morkejš J.4, Mošna F.5
1KARIM VFN a 1. LF UK v Praze; 2Kardiocentrum FNKV v Praze; 3Kardiocentrum Nemocnice na Homolce v Praze; 4Kardiocentrum FN v Plzni; 5Kardiocentrum FN Motol v Praze
Úvod: V poslední době výrazně narůstá počet kardiochirurgických výkonů u vysoce rizikových pacientů ve věku nad 80 let, nicméně detailní analýzy pooperačních výsledků u těchto pacientů chybí.
Cíl: Cílem studie bylo srovnat pooperační výsledky a kvalitu života u nízce, středně a vysoce rizikových osmdesátníků podstupujících kardiochirurgický výkon.
Metody: Do studie bylo zahrnuto 285 pacientů ve věku 80 let a více, kteří podstoupili kardiochirurgický výkon od ledna 2011 do prosince 2012. Studie se účastnili pacienti z pěti z celkového počtu dvanácti kardiocenter v České republice, představující téměř polovinu osmdesátníků operovaných v té době. Na základě perioperačního rizika kalkulovaného podle Euroscore II byli pacienti rozděleni do tří skupin: nízkého, středního a vysokého rizika. Byl proveden retrospektivní sběr předoperačních, peroperačních a pooperačních dat s následnou analýzou a srovnáním mezi skupinami. V květnu 2014 byli pacienti telefonicky dotazováni s hodnocením objektivních a subjektivních parametrů kvality života po kardiochirurgickém výkonu.
Výsledky: U skupiny s vysokým rizikem ve srovnání se skupinou se středním a nízkým rizikem byla vyšší 30denní mortalita (20 % vs. 6,4 % vs. 5,2 %, p < 0,001), dlouhodobá mortalita (20 % vs. 8,5 % vs. 8,3 %, p < 0,05) a vyšší incidence syndromu nízkého srdečního výdeje (16,8 % vs. 1,1 % vs. 4,2 %, p < 0,05). Napříč skupinami byl zaznamenán trend k vyšší časné mortalitě ve srovnání s predikovanou hodnotou podle Euroscore II, nicméně tyto rozdíly nebyly statisticky významné. Kvalita života kvantifikovaná pomocí Karnofsky skóre byla významně nižší ve skupině s vysokým rizikem ve srovnání se zbylými skupinami (44,4 vs. 70,1 vs. 70,6, p < 0.001). Významné zlepšení ve třídě kategorie NYHA bylo pozorováno ve vysoce a středně rizikové skupině ve srovnání se skupinou s nízkým rizikem (51 % vs. 45 % vs. 24 %, p < 0,05).
Shrnutí: Naše studie ukazuje, že vysoce rizikoví osmdesátníci podstupující kardiochirurgickou operaci představují nadále významný medicínský problém. Při rozhodování o operabilitě a únosnosti výkonu je nutno brát v potaz vysokou incidenci pooperačních komplikací, vysokou časnou mortalitu a nízkou pooperační kvalitu života u těchto pacientů.
Hemodynamika v septickém šoku a možnosti ochrany myokardu
Rulíšek J.
KARIM VFN a 1. LF UK v Praze
Septická kardiomyopatie je jednou z mnoha orgánových dysfunkcí, které se demonstrují u pacientů v těžké sepsi a septickém šoku. Recentně se objevují data o výskytu této orgánové komplikace, která ukazují, že se může vyskytovat až u 60 % septických pacientů. Veillard-Baron poukazuje na to, že četnost výskytu závisí na čase od počátku sepse. Srdeční dysfunkce se prezentuje jako systolická a/nebo diastolická. Systolická dysfunkce má na rozdíl od diastolické paradoxně obrácený vztah k mortalitě pacientů, tedy pacienti s dilatovanou a dysfunkční komorou mají větší šanci na přežití. Zhoršení diastolické funkce levé komory srdeční oproti tomu je přímo úměrná mortalitě a v některých studiích se jeví jako unikátní parametr pro monitorování tíže stavu. Ochrana myokardu v sepsi není doposud dořešenou otázkou. Již od 90. let minulého století jsou v této indikaci užívány betablokátory. Pro aplikaci v této hemodynamicky nepredikovatelné situaci je výhodnější použít betablokátory s ultrakrátkým účinkem. Tyto jsou opakovaně užívány v animálních studiích, kde byl prokázán lepší výkon myokardu při betablokádě v sepsi. V humánních studiích tento efekt doposud přesvědčivě prokázán nebyl, nicméně řada autorů se snaží prokázat bezpečnost podávání betablokátorů i v případě nutnosti aplikace vazopresorů. Zdá se, že dominujícím pozitivním faktorem je prodloužení doby diastoly, zlepšení plnění levé komory a tím zvýšení tepového výdeje. To umožní, při poklesu frekvence, zachování dostatečného srdečního výdeje. Betablokátory pak nepřímo snižují poškození myokardu i na podkladě menšího uvolnění srdečních troponinů a zkrácení doby dosažení jejich vrcholové hladiny. Vysoce senzitivní troponin je dobrým monitorem poškození systolické i diastolické funkce levé komory srdeční.
Literatura
- Vieillard-Baron, A., Caille, V., Charron, C. et al. Actual incidence of global left ventricular hypokinesia in adult septic shock. Crit. Care Med., 2008, 36, 6, p. 1701–1706.
- Parker, M. M., Shelhamer, J. H., Bacharach, S. L. et al. Profound but reversible myocardial depression in patients with septic shock. Ann. Intern. Med., 1984, 100, 4, p. 483–490.
- Weng, L., Liu, Y. T., Du, B., Zhou, J. F., Guo, X. et al. The prognostic value of left ventricular systolic function measured by tissue Doppler imaging in septic shock. Crit. Care, 2012, 16, 3.
- Balik, M., Rulisek, J., Leden, P., Zakharchenko, M. Concomitant use of beta-1 adrenoreceptor blocker and norepinephrine in patients with septic shock. Reply to a letter to the authors. Wien Klin. Wochenschr, 2014, 126, 7–8, p. 246–247.
- Morelli, A., Ertmer, C., Westphal, M., Rehberg S. Effect of heart rate control with esmolol on hemodynamic and clinical outcomes in patients with septic shock: a randomized clinical trial.; JAMA, 2013 Oct 23;310(16):1683-91
Nová antikoagulancia (NOACs) v perioperačním období
Turek Z., Samek J.
Klinika anesteziologie, resuscitace a intenzivní medicíny FN Hradec Králové
Nová perorální antikoagulancia (NOACs) se postupně stávají rutinní součástí managementu fibrilace síní a v preventivních i léčebných postupech týkajících se tromboembolické nemoci. Inhibitory faktoru Xa (rivaroxaban, apixaban a edoxaban) a přímý inhibitor thrombinu (dabigatran) jsou již ve svých indikacích rutinně používaná nová perorální antikoagulancia. Vykazují předvídatelnou farmakokinetiku a biologickou dostupnost, nejeví významné metabolické interakce s léky a stravou, mají krátké biologické poločasy a nevyžadují rutinně laboratorní kontrolu účinku. Jednou z výhod jejich podání je nižší výskyt intracerebrálního krvácení v porovnání s warfarinem.
Zcela specifickou problematikou je přístup k terapii NOACs v perioperačním období, kdy krátké biologické poločasy zajišťují odeznění účinku těchto antikoagulancií za 36–48 hodin v případě normálních renálních funkcí, ale akutní zrušení jejich antikoagulačního účinku vyžaduje podávání koncentrátu faktorů prothrombinového komplexu, jehož efektivita byla prokázána v případě antagonizace inhibitorů faktoru Xa, nikoli v případě antagonizace dabigatranu, proto v případě elektivního výkonu je doporučeno vysazení NOACs 48 hodin před výkonem. V případě akutního výkonu s rizikem krvácení je doporučeno podávat vysoké dávky koncentrátu faktorů prothrombinového komplexu 25 až 50 IU/kg, v případě dabigatranu či předávkování tímto preparátem se také zvažuje jednak hemodialýza, jednak off-label podání fVIIa. Specifická antidota jednotlivých preparátů ze skupiny NOACs nejsou zatím v klinické medicíně k dispozici, ale jsou ve fázi vývoje, proto perioperační management krvácení vedle standardních postupů zahrnuje i rekuperaci krve, eventuálně podle rozsahu výkonu i damage control chirurgický přístup. Laboratorní monitorování účinku NOACs vyžaduje specifické testy, v případě dabigatranu je to specifický Thrombin Time (TT) tzv. Hemoclot, v případě inhibitorů faktoru Xa modifikovaná anti Xa assay, nebo aPTTi, diskutovanými metodami jsou i viskoelastometrické metody typu TEG a ROTEM v detekci účinku NOACs.
Nová antikoagulancia jsou léky potencí podobné warfarinu, jejich nevysazení je jednoznačnou indikací pro odklad plánované operace, vysoké riziko život ohrožujícího krvácení vzniká u nemocných s rozvojem renální insuficience, kde dochází ke zpomalení metabolismu NOACs a jejich akumulaci. Specifická antidota jsou předmětem klinických studií.
American Society For Extracorporeal Technology (AMSECT) Standards and Guidelines for Perfusion Practice 2013
Vlk R., Suchopárová Š., Vaněk T., Straka Z.
Kardiochirurgická klinika 3. LF UK a Fakultní nemocnice Královské Vinohrady, Praha
Příspěvek se zabývá problematikou bezpečnosti vedení mimotělního oběhu, a to jak pro pacienta, tak pro perfuzionistu. Praxe je taková, že nejen každé pracoviště, ale dokonce každý perfuzionista pracuje trochu odlišným způsobem, navíc s ohledem na variabilitu výkonů a pacientů. Vzhledem k tomu, že ani na základě EBM nejsou jednoznačně definována pravidla pro optimální vedení mimotělního oběhu, pokusila se American Society for Extracorporeal Technology (AMSECT) určit tematické okruhy této problematiky a v jejich rámci definovat optimální postupy. Tato přednáška tedy přináší doporučenou metodiku v několika hlavních oblastech vedení mimotělního oběhu tak, jak je v roce 2013 definovala AMSECT. Součástí přednášky je i srovnání těchto doporučených postupů s perfuziologickou praxí v ČR, která byla zjištěna na základě dotazníku, vyplněného na jednotlivých pracovištích v ČR.
Podávanie rekombinantného faktora viiau pacientov na ecmo/ECLS
Žarnovická V., Olejárová I.
OAIM NÚSCH, a. s., Bratislava, Slovenská republika
Úvod
Perioperačné krvácanie v kardiochirurgii je vážnym problémom a komplikáciou, ktorá má vplyv na morbiditu a mortalitu pacientov. Hľadanie optimálneho prístupu, ktorý by zredukoval významné pooperačné krvácanie stále pokračuje. Rekombinantný aktivovaný faktor VII (rFVIIa) je možné použiť u pacientov s hemofíliou A a B s inhibítormi faktora VIII alebo IX a u pacientov s deficitom faktora VII – ide o takzvanú on-label indikáciu. V súčasnosti sa stretávame s rastúcim použitím rFVIIa v kardiochirurgii pri život ohrozujúcich krvácaniach v tzv. off-label indikácii. S rozšíreným používaním tohto lieku narastá aj riziko tromboembolických komplikácií, zvlášť u pacientov na LVAD a najmä na ECMO/ECLS [1, 2, 3, 4].
Rekombinantný aktivovaný faktor VIIa ECMO/ECLS
rFVIIa (NovoSeven®, Novo Nordisk, Kodaň, Dánsko) zvyšuje tvorbu trombínu v mieste tkanivového poškodenia tým, že sa naviaže na tkanivový faktor (TF). Komplex TF – rFVIIa katalyzuje premenu faktora X na Xa, čím sa akceleruje aktivácia protrombínu a lokálna formácia trombínu. Výsledkom je trombínová zátka s tesnou fibrínovou štruktúrou, ktorá je rezistentná voči lýze [1, 2]. Zdá sa tiež, že rFVIIa má priaznivý vplyv na funkciu trombocytov, keďže zvyšuje množstvo trombínu na povrchu trombocytov nezávisle od tkanivového faktora [1, 2]. Tradičné dávkovanie rFVIIa u pacientov s hemofíliou pozostáva z opakovaných dávok 90–120 µg/kg. Ukazuje sa však, že koagulačné poruchy u pacientov po kardiochirurgickom výkone sú iné ako u hemofilikov – vládne preto kontroverzia ohľadom najlepšej dávky rFVIIa pri off-label podaní [1]. V skupine kardiochirurgických pacientov sa v posledných rokoch vyčlenila zvláštna podskupina pacientov s VAD a s ECMO. U týchto pacientov je vyššie riziko ako krvácania, tak aj tromboembolických komplikácií. Mimotelový obeh pri ECMO môže vyvolať tzv. získaný von Willebrandov syndróm [3]. Tromboembolické komplikácie viac ohrozujú pacientov na ECMO – je preto nutné sledovať, či sa na membráne oxygenátora netvoria fibrínové depozity alebo krvné zrazeniny, či sa nevyvíja hemolýza alebo trombocytopénia [3]. Vzhľadom na závery práce Brucknera et al. [1] sme začali u pacientov na ECMO/ECLS a na VAD dávať v prípade život ohrozujúceho krvácania polovičnú dávku rFVIIa – cca 45 µg/kg [5].
Súbor a metódy
V období od 1. 10. 2010 do 28. 2. 2015 sme na našom pracovisku implantovali ECMO 42 pacientom, u 41 išlo o venoarteriálne a u jedného pacienta o venovenózne ECMO. Zo 42 pacientov bolo 36 mužov a 6 žien, priemerný vek bol 54 ± 11,9 rokov. Mortalita bola 64% – zomrelo 27 pacientov (23 mužov a 4 ženy). rFVIIa sme podali 4 pacientom – trom mužom a jednej žene. Dodržali sme pri tom všetky zásady off-label podania rFVIIa – korekcia vnútorného prostredia a hemokoagulačných parametrov, chirurgické revízie. Retrospektívne sme analyzovali zdravotnú dokumentáciu a sledovali účinnosť podania rFVIIa (pokles počtu transfúzií a nutnosti chirurgických revízií), ako aj výskyt tromboembolických komplikácií. Vzhľadom na počet pacientov ide o súhrn kazuistík.
Pacient č. 1
Žena (57 rokov) žena s diagnózou hypertrofickej kardiomyopatie bola zaradená na waiting list transplantácie srdca. HTx mala komplikovaný priebeh, pre nemožnosť odpojenia od CPB (napriek vysokej farmakologickej podpore) bolo implantované venoarteriálne ECMO a ponechaný open chest. V operačný deň bola prvýkrát revidovaná s nájdením chirurgického zdroja krvácania, počas druhej operačnej revízie sa nenašiel žiaden chirurgicky ošetriteľný zdroj, a preto sme podali NovoSeven® v dávke 38,5 µg/kg (3 mg) i. v. Do podania rFVIIa dostala pacientka 40 transfúzií (20× Ery masa, 13 × ČZP, 7× trombocytárny koncentrát), po podaní 5 transfúzií Ery masy. Po 8 hodinách sme znovu podali rFVIIa (v tej istej dávke) pre opätovný výskyt vysokých krvných strát s dobrým efektom (krvácanie ustalo, nemuseli sme podať žiadne transfúzie). Nezaznamenali sme žiadnu tromboembolickú komplikáciu. Na 3. pooperačný deň pacientka zomiera na arytmologické zlyhanie myokardu.
Pacient č.2
Muž (62 rokov) bol zaradený na waiting list transplantácie srdca pre ischemickú dilatačnú kardiomyopatiu, ako bridge to transplant mu bol naimplantovaný LVAD HeartMate II. Po ohlásení vhodného darcu srdca pacient prichádza na operačný výkon – explantáciu HM II a HTx. Dochádza k akútnemu zlyhaniu štepu, pacienta nie je možné napriek vysokej farmakologickej podpore (dobutamín, adrenalín, noradrenalín, iNO) odpojiť od CPB, preto mu bolo implantované ECMO a ponechaný open chest (vstupné INR vzhľadom na LVAD bolo 4,0). Prvá chirurgická revízia bola do hodiny po príchode na OAIM s nájdením chirurgického zdroja, po revízii podávame rFVIIa v dávke 42,1 µg/kg (4 mg) i. v. Napriek podaniu rFVIIa pretrvávajú vysoké krvné straty vyžadujúce masívnu hemosubstitučnú a hemostyptickú liečbu (7× Ery masa, 7× ČZP, 2× trombocytárny koncentrát, Prothromplex® 600 I.U., fibrinogén, kyselina tranexámová, PAMBA, etamsylát), preto je indikovaná ďalšia operačná revízia. Pri nej sa však nenašiel žiaden chirurgický zdroj, preto 14 hodín po prvom podaní rFVIIa znovu podávame NovoSeven® v dávke 42,1 µg/kg priamo na operačnej sále. Toto druhé podanie už má priaznivý vplyv na krvácanie, ktoré postupne ustáva a znižuje sa aj potreba transfúznej liečby (3× Ery masa, 2× ČZP, 3× trombocytárny koncentrát). Stav pacienta sa postupne zlepšuje a 4. pooperačný deň je možné explantovať ECMO/ECLS. Výkon prebehol bez krvácavých komplikácií. Inotropnú podporu bolo možné úplne vysadiť na 19. pooperačný deň, extubovaný bol po 27 dňoch UPV (stav bol komplikovaný atypickou intersticiálnou pneumóniou). Nevyskytla sa žiadna tromboembolická komplikácia. Na 57. pooperačný deň bol pacient prepustený domov.
Pacient č. 3
Muž (66 rokov) po CABG v roku 1995 bol indikovaný na chirurgické riešenie mitrálnej a trikuspidálnej chlopne. Už predoperačne bola prítomná koagulopatia na podklade hepatopatie a trombocytopénia. Bola mu nahradená mitrálna chlopňa mechanickou protézou St. Jude Medical No 31 a trikuspidálna chlopňa bola splastikovaná ringom Physio No 34. Napriek farmakologickej podpore (dobutamín, adrenalín, noradrenalín, iNO) sa nám nedarí pacienta odpojiť od CPB – preto mu bolo implantované ECMO a ponechaný open chest. Pre masívne krvné straty do drénov a polytransfúznu liečbu (12× Ery masa, 2× ČZP, 2× trombocytárny koncentrát, fibrinogén, kyselina tranexámová, etamsylát, PAMBA, Prothromplex®) boli indikované postupne dve chirurgické revízie, obe bez nálezu chirurgického zdroja krvácania. Podali sme preto jednorazovo rFVIIa v dávke 91,8 µg/kg (9 mg) i. v. Pacientov stav sa veľmi rýchlo zhoršoval napriek masívnej farmakologickej a ECMO/ECLS podpore a 5 hodín po operácii dochádza k elektromechanickej disociácii a úmrtiu pacienta.
Pacient č. 4
Muž (57 rokov) po CABG v r. 2009 bol indikovaný na AVR + reCABG. Aortálna chlopňa mu bola nahradená mechanickou protézou On-X No 23 a bol našitý aortokoronárny bypass VSM/RIA. Pre nemožnosť odpojenia od CPB bolo implantované ECMO/ECLS a ponechaný open chest. Pacient trpel neutíšiteľným krvácaním, ktoré si vyžiadalo celkovo 21 chirurgických revízií a extrémne masívnu hemosubstitučnú a hemostyptickú liečbu. Po 7. chirurgickej revízii (s negatívnym výsledkom) a masívnej transfúznej liečbe (57× Ery masa, 39× ČZP, 13× trombocytárny koncentrát) sa rozhodujeme pre podanie rFVIIa v dávke 47,1 µg/kg (5 mg) i. v. Podanie však nie je úspešné, pretože naďalej trvá hemoragický šok z pokračujúcich krvných strát do drénov napriek opakovaným chirurgickým revíziám a masívnemu korigovaniu hemokoagulačných parametrov. (Po podaní rFVIIa sme dali 47× Ery masu, 30× ČZP a 3× trombocytárny koncentrát.) Tromboembolickú komplikáciu sme ani u tohto pacienta nemali. Kombinácia hemoragického a cirkulačného šoku vyústila do multiorgánového zlyhania a na 23. pooperačný deň pacient zomrel.
Diskusia
Pacienti s implantovaným ECMO/ECLS tvoria zvláštnu skupinu pacientov, ktorá je na jednej strane ohrozená krvácaním a na druhej strane tromboembolickými príhodami. Podávanie rFVIIa je u týchto pacientov zvlášť citlivé z pohľadu indikácie aj dávky. U našich pacientov sme pristúpili k podaniu rFVIIa po splnení kritérií pre off-label podanie a u 3 pacientov sme podali polovičnú dávku (cca 40 µg/kg) v porovnaní s konvenčným dávkovaním 90 µg/kg. Jeden pacient dostal plnú dávku vzhľadom na perakútny stav. Ako úspešné podanie z pohľadu zastavenia krvácania (menšie krvné straty do drénov, menej transfúzií) je podanie u prvých dvoch pacientov, u tretieho sa úspešnosť nedá posúdiť vzhľadom na progresiu cirkulačného zlyhania a u štvrtého pacienta bolo podanie neúspešné. U žiadneho pacienta sme nezaznamenali tromboembolickú komplikáciu (takýto prípad sme zatiaľ na našom pracovisku po podaní rFVIIa nemali). V súlade s novými poznatkami sa snažíme podať čo možno najnižšiu účinnú dávku (cca 45 µg/kg) s možnosťou jej opakovania [5]. Najmä u pacientov na LVAD a ECMO/ECLS je tento postup zvlášť odporúčaný [1, 3].
Záver
Rekombinantný aktivovaný faktor VII (rFVIIa, NovoSeven®) našiel svoje miesto u kardiochirurgických pacientov so život ohrozujúcim krvácaním. Stále je to off-label indikácia, pri ktorej treba dodržať všetky zásady podania (korekcia vnútorného prostredia a hemostázy – hemokoagulačných parametrov, chirurgickou revíziou vylúčený chirurgicky ošetriteľný zdroj krvácania). Vo všeobecnosti zaznamenávame ústup od dávkovacej schémy 90–120 µg/kg, ktorá je určená pre pacientov s hemofíliou. Koagulačné poruchy u pacientov po kardiochirurgickom výkone sú iného charakteru ako u hemofilikov a účinné sú nižšie dávky (35–50 µg/kg), ktoré je možné opakovať. Pri takto redukovanej dávkovacej schéme znižujeme riziko tromboembolických komplikácií. Tie sú zvlášť nebezpečné u pacientov na ECMO/ECLS [3, 4] a tiež u pacientov na LVAD [1]. Včasnej detekcii týchto stavov treba venovať veľkú pozornosť.
Literatúra
- Bruckner, B. A., DiBardino, D. J., Ning, Q. et al. High incidence of thromboembolic events in left ventricular assist device patients treated with recombinant activated factor VII. J. Heart Lung Transplant., 2009, 28, p. 785–790.
- Warren, O., Mandal, K. et al. Recombinant activated factor VII in cardiac surgery: a systematic review. Ann. Thorac. Surg., 2007, 83, p. 707–714.
- Repessé, X., Au, S. M. et al. Recombinant factor VIIa for uncontrollable bleeding in patients with extracorporeal membrane oxygenation: report on 15 cases and literature review. Critical Care, 2013, 17, R55, http://ccforum.com/content/17/2/R55.
- Syburra, T., Lachat, M. et al. Fatal outcome of recombinant factor VIIa in heart transplantation with extracorporeal membrane oxygenation. Ann. Thorac. Surg., 2010, 89, p. 1643–1645.
- Olejárová, I. Podávanie rFVIIa pri implantáciách mechanických podpôr srdca. In Zborník prednášok stretnutí Pracovnej skupiny kardiovaskulárnej anestézie a intenzívnej medicíny SSAIM, Bratislava/Košice 2014, s. 51–53.
Štítky
Anesteziologie a resuscitace Intenzivní medicína
Článek vyšel v časopiseAnesteziologie a intenzivní medicína
Nejčtenější tento týden
2015 Číslo 6- Bezpečnostní profil metamizolu – systematický přehled
- Aktuální pohled na využití myorelaxancií a jejich antidot v moderní anesteziologii a intenzivní medicíně
- Perorální antivirotika jako vysoce efektivní nástroj prevence hospitalizací kvůli COVID-19 − otázky a odpovědi pro praxi
- Neodolpasse účinně snižuje pooperační bolest
- Neodolpasse jako ideální volba tam, kde je bolest provázena spasmem kosterního svalstva
-
Všechny články tohoto čísla
- Nozokomiální pneumonie ventilovaných nemocných – je skutečně nevyhnutelnou komplikací umělé plicní ventilace?
- Vplyv profylaktického podávania melatonínu na výskyt včasného pooperačného delíria u kardiochirurgických pacientov
- Můžeme pouhou změnou premedikace dosáhnout snížení výskytu delirantního stavu u dětí po operaci?
- Rýchla diferenciálna diagnostika akútnej respiračnej insuficiencie pomocou ultrasonografie pľúc
- Vliv zavádění balíčků preventivních opatření na výskyt ventilátorových pneumonií
- Echokardiografické zhodnocení aortální chlopně u nestabilního pacienta – základní vyšetření
- Zajištění dýchacích cest
- Pacienti s rezavými vlasy mají vyšší výskyt komplikací – mýtus nebo důkazy?
- Stanovisko ke kalkulaci mozkového perfuzního tlaku u pacientů s traumatickým poraněním mozku
- Anesteziolog jako ochránce pacienta aneb čeká nás „povinnost donášet“ na naše kolegy?
-
XVI. kardioanesteziologické vědecké dny s mezinárodní účastí
Vybrané souhrny přednášek - Výborová schůze ČSARIM
- Zápis z jednání výboru č. 4/2015
- Rejstříky
- Anesteziologie a intenzivní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Echokardiografické zhodnocení aortální chlopně u nestabilního pacienta – základní vyšetření
- Rýchla diferenciálna diagnostika akútnej respiračnej insuficiencie pomocou ultrasonografie pľúc
- Můžeme pouhou změnou premedikace dosáhnout snížení výskytu delirantního stavu u dětí po operaci?
- Zajištění dýchacích cest
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



