-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Perkutánní implantace aortální chlopně z pohledu anesteziologa
Transcatheter Aortic Valve Implantation: The anaesthetist’s view
Transcatheter Aortic Valve Implantation is arising as a new modality in the treatment of severe symptomatic aortic stenosis. This method has recently been introduced to the Czech Republic. It is reserved for the high risk patient population and requires close interdisciplinary co-operation where an experienced cardiac anaesthetist has an important role. The authors present their initial experience with 7 cases.
Keywords:
aortic stenosis – percutaneous aortic valve implantation – aortic stenosis – anaesthesiological management
Autoři: Vaněk Tomáš 1; Bednář František 2; Kočka Viktor 2; Luha Olev 3; Toušek Petr 2; Jirmář Radovan 2; Widimský Petr 2
Působiště autorů: Kardiochirurgická klinika, Kardiocentrum 3. LF UK a FNKV, Praha 1; III. interní – kardiologická klinika, Kardiocentrum 3. LF UK a FNKV, Praha 2; Department of Internal Medicine, University of Graz, Austria 3
Vyšlo v časopise: Anest. intenziv. Med., 20, 2009, č. 6, s. 305-308
Kategorie: Anesteziologie - Původní práce
Souhrn
Novým způsobem léčby významné symptomatické aortální stenózy je perkutánní implantace aortální chlopně (Transcatheter Aortic Valve Implantation). Metoda, která je nově využívána i v České republice a je vyhrazena vysoce rizikovým nemocným, vyžaduje úzkou mezioborovou spolupráci – nedílným členem týmu je i anesteziolog zkušený v kardiovaskulární problematice. Autoři uvádějí iniciální zkušenosti s implantací chlopně u 7 nemocných.
Klíčová slova:
aortální stenóza – perkutánní implantace aortální chlopně – anesteziologický managementÚvod
V současnosti prudce roste počet perkutánních implantací aortální chlopně (Transcatheter Aortic Valve Implantation – TAVI), a to jak v zahraničí, tak v České republice [1–3]. TAVI je výkonem, který je prováděn na pracovišti intervenční kardiologie, avšak vyžaduje další mezioborovou spolupráci s kardiochirurgem či cévním chirurgem a v neposlední řadě též s anesteziologem zkušeným v kardiovaskulární problematice. Cílem tohoto sdělení je seznámit širší anesteziologickou obec s touto zcela novou metodou včetně jejích případných rizik a podělit se o naše iniciální zkušenosti.
Popis metody
Metoda TAVI je v přítomnosti vyhrazena pro ty nemocné se závažnou symptomatickou aortální stenózou, kteří jsou vzhledem ke svému věku a přidruženým onemocněním kontraindikováni či pouze hraničně indikováni ke konvenční kardiochirurgické operaci – náhradě aortální chlopně (hodnota logistického EuroSCORE, tj. skórovacího programu predikujícího rizikovost kardiochirurgického výkonu – 20 % a vyšší; www.euroscore.org). Kontraindikací k TAVI (kromě anatomických kritérií) je zejména významně snížená ejekční frakce levé srdeční komory, ta by měla být optimálně vyšší než 50 %, lze akceptovat 30–50 %. Indikace k TAVI by měla být schválena konziliem intervenčních kardiologů a kardiochirurgů. Během implantace musí být připraven kardiochirurgický tým a operační sál na eventuální možnost konverze na klasický operační výkon a též musí být k dispozici chirurg s erudicí v cévní chirurgii.
Komerčně jsou k dispozici (a v České republice se používají) dva systémy TAVI: chlopeň Edwards SAPIENTM (Edwards Lifesciences Inc., Irvin, CA, USA) a chlopeň Corevalve® Revalving System (CoreValve Inc., Irvin, CA, USA). Oba systémy se liší konstrukcí umělé chlopně, avšak obecné zásady perkutánní implantace jsou si víceméně podobné, s tím rozdílem, že systém Edwards SAPIENTM umožňuje též při těžkém aterosklerotickém postižení pánevního řečiště či přítomnosti tzv. „porcelánové aorty“ transapikální implantaci (punkcí srdečního hrotu z anterolaterální torakotomie). Použití tohoto přístupu se však blíží klasické kardiochirurgické operaci a přesahuje náplň a zaměření tohoto sdělení. V našem kardiocentru využíváme Corevalve® Revalving System a následující text se tedy bude týkat implantace této umělé srdeční chlopně.
Před započetím vlastní implantace musí být znám stav pánevního řečiště a velikost femorálních tepen, minimální průměr těchto tepen musí být 6–7 mm. Pacientovi je z jednoho třísla zaveden „pigtail“ katétr do bulbu aorty, který slouží k intermitentní aplikaci kontrastní látky – angiografii bulbu aorty. Do druhého třísla je zaveden sheath a následně perkutánní vaskulární uzavírací systém Prostar Suture-Mediated Closure (Abbott Vascular, Redwood City, CA, USA), který je přípravou na perkutánní suturu femorální tepny na konci výkonu. Poté je z tohoto třísla retrográdně proniknuto vodičem přes stenotickou aortální chlopeň do levé komory srdeční. Následně je nativní aortální chlopeň dilatována a v podstatě destruována valvuloplastickým balonkem válcovitého tvaru NuCLEUS (NuMED Inc., Cornwall, ON, Kanada), před jeho inflací je třeba přechodně snížit srdeční výdej rychlou stimulací srdečních komor (frekvence cca 180/min., trvání 10–15 vteřin) pomocí externího kardiostimulátoru (obr. 1). Poté by mělo dojít v poměrně rychlém sledu k vlastní implantaci aortální chlopně, která je předtím v lázni s ledovou tříští umístěna do zaváděcího pouzdra – obr. 2, 3 (velikost chlopně je stanovena před výkonem detailním vyšetřením pomocí jícnové echokardiografie, CT a angiografie a je znovu potvrzena během výkonu rozměrem aortálního anulu). Dále je provedena kontrolní angiografie aortálního bulbu, je změřen transvalvulární tlakový gradient (obr. 4), poté TAVI končí odstraněním katétrů a perkutánní suturou femorální tepny.
Obr. 1. Dilatace aortální chlopně valvuloplastickým balonkem při rychlé komorové stimulaci Pacient po předchozí operační revaskularizaci myokardu. 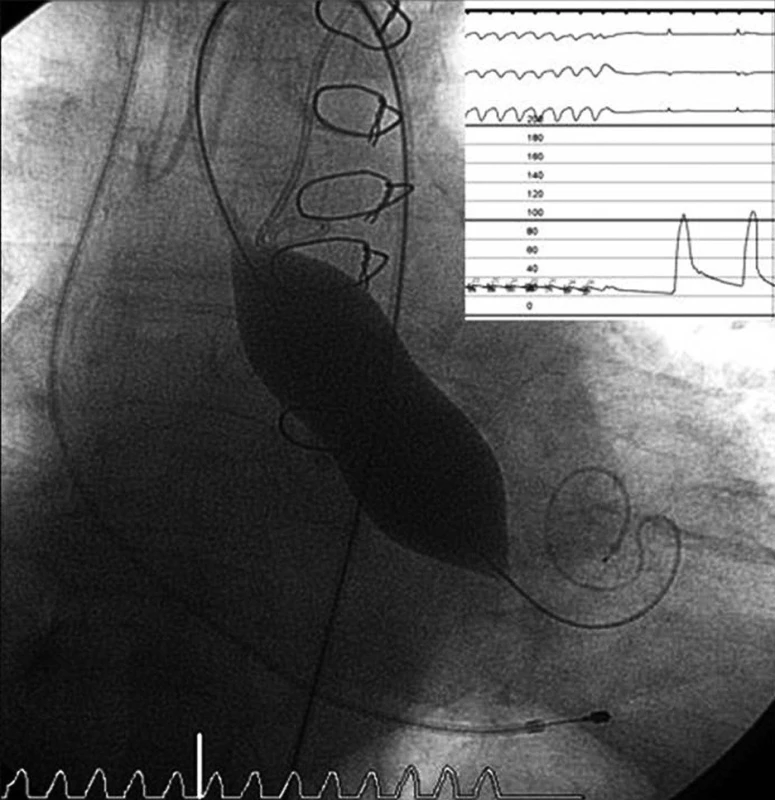
Obr. 2. Pouzdro systému Corevalve<sup>®</sup> připevněné na zaváděcí katétr 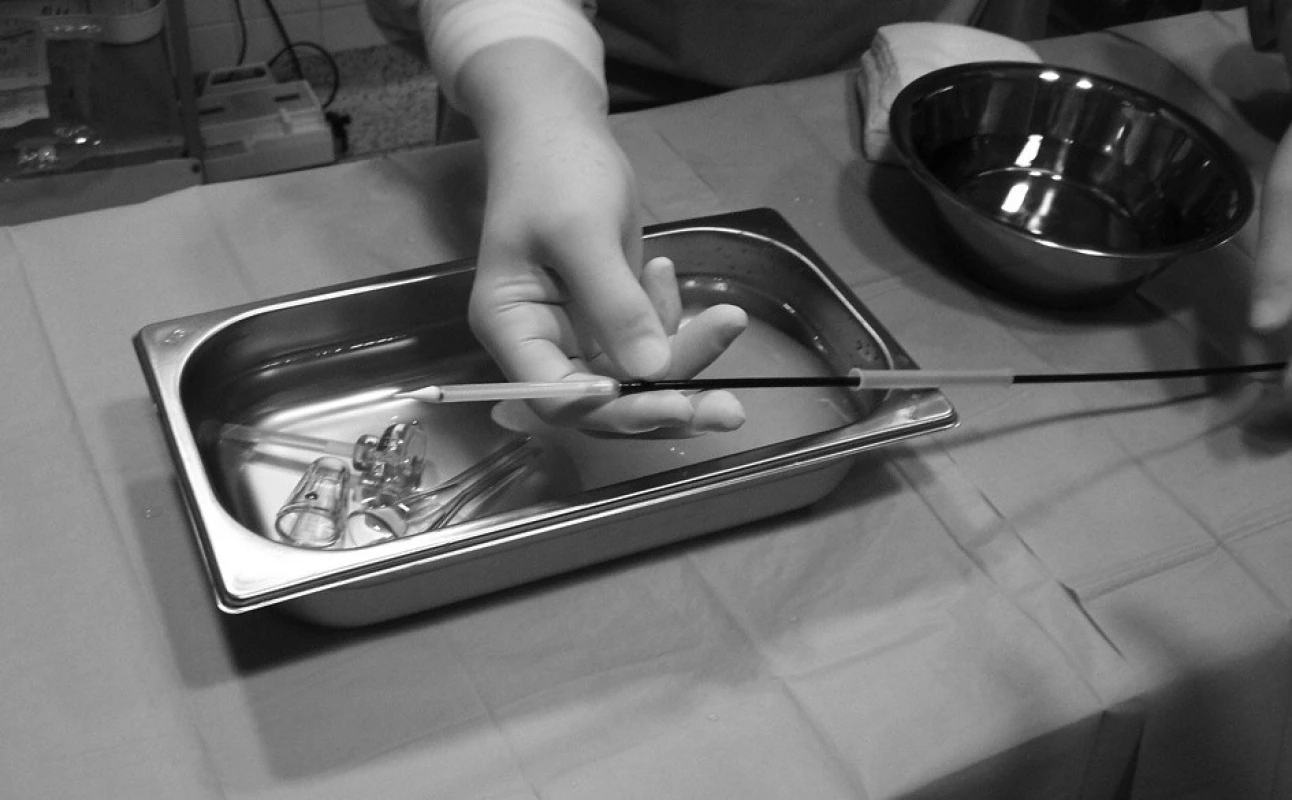
Obr. 3. Detail chlopně Corevalve<sup>®</sup> umístěné do zaváděcího pouzdra 
Obr. 4. Plně expandovaná chlopeň Corevalve<sup>®</sup> v optimální pozici, měření tlakových gradientů 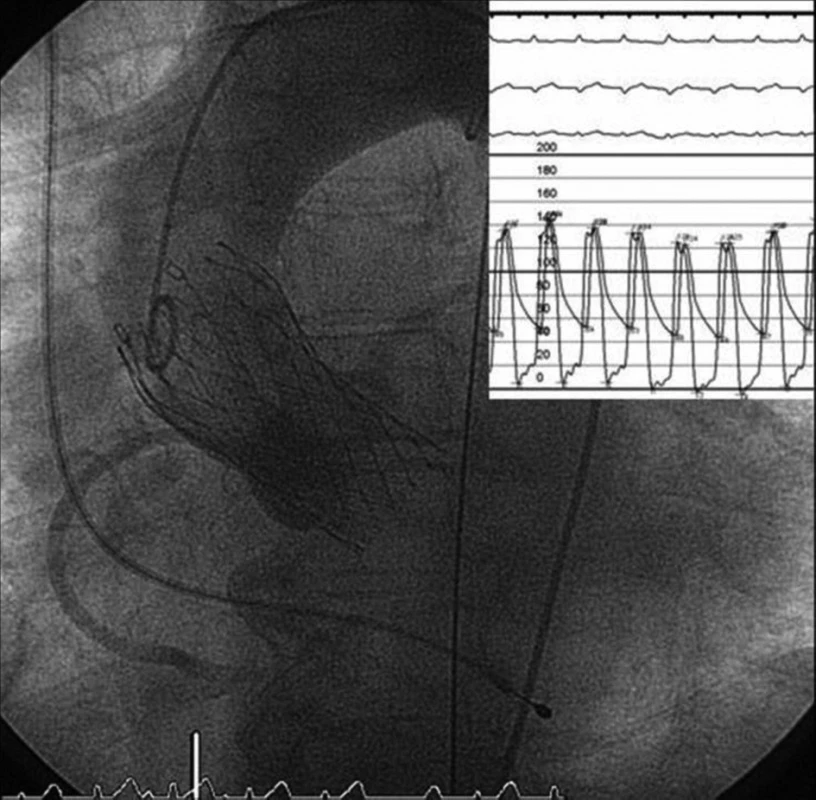
Chlopenní náhrada systému Corevalve® je trojcípou biologickou chlopní z prasečího perikardu, která je umístěna do košíku vyrobeného ze samorozpínacího materiálu nitinolu (obr. 5). V současné době je k dispozici ve dvou velikostech – 26 mm pro velikost aortálního anulu 20–23 mm a 29 mm pro velikost aortálního anulu 23–27 mm. Průměr zaváděcího systému je 18 Fr.
Obr. 5. Celkový pohled na chlopenní náhradu Corevalve<sup>®</sup> 
Vlastní zkušenost – pohled anesteziologa
V době od dubna do července 2009 bylo v Kardiocentru 3. lékařské fakulty Univerzity Karlovy a Fakultní nemocnice Královské Vinohrady uskutečněno 7 perkutánních implantací aortální chlopně – průměrný věk nemocných 81 let (77–86), poměr ženy/muži 3 : 4, průměrné logistické EuroSCORE 20 %. Ve všech případech byla implantace chlopně úspěšná, nedošlo k žádnému periprocedurálnímu úmrtí a též 30denní mortalita byla nulová. Vlastní implantace chlopně trvaly přibližně 2–3 hodiny, průměrná doba pobytu nemocných po výkonu na jednotce intenzivní péče byla 7 dní (3–13). V jednom případu došlo k laceraci femorální arterie, která byla ošetřena přímo na katetrizačním sále cévním chirurgem. Suturu tepny bylo možné provést v místním znecitlivění bez celkové anestezie bezprostředně po skončení implantace. V dalším případu došlo po nekomplikované implantaci během převozu na jednotku intenzivní péče k rozvoji cévní mozkové příhody – tranzitorní ischemické ataky, která si vyžádala intubaci a následnou umělou plicní ventilaci v trvání 4 hodin. Do 24 hodin došlo k úpravě neurologických funkcí ad integrum. U jiného pacienta vznikla po odstranění externí stimulační elektrody srdeční tamponáda s nutností punkce perikardu.
Přestože někteří autoři doporučují na počátku „learnig curve“ provádět TAVI v celkové anestezii [4], či celkovou anestezii s intubací pro tento výkon z mnoha důvodů rutinně používají (možnost snadnější periprocedurální jícnové echokardiografie, preventivní zajištění dýchacích cest, imobilita a komfort nemocného aj.) [5, 6], rozhodli jsme se od začátku pro kombinaci místní anestezie a analgosedace. K analgosedaci jsme užili bolusové dávky alfentanilu 0,25–1,00 mg nebo ketaminu 0,5–1,0 mg . kg-1, titrovaně podle stavu a kontinuálně propofol 0,3–4,0 mg . kg-1 . hod-1. Vzhledem k výše popsané povaze TAVI s očekáváním závažných hemodynamických komplikací považujeme za nesmírně důležité pečlivé kontinuální monitorování vitálních funkcí vlastním anesteziologickým bed-side monitorem, který je nezávislý na monitorovacím systému invazivního kardiologa. Nezbytné je zavedení kanyly do a. radialis k přímému měření krevního tlaku, dále zajištění centrálního žilního přístupu, samozřejmé jsou monitorování EKG a měření saturace kyslíkem pulzní oxymetrií. Jak již bylo popsáno výše, nedílnou součástí celé procedury implantace chlopně je krátkodobé výrazné omezení srdečního výdeje pomocí rychlé stimulace srdečních komor. K tomuto účelu je nutno zavést externí kardiostimulační elektrodu, na našem pracovišti nejčastěji cestou pravostranné v. jugularis interna. Dále jsou na pacienty umístěny externí nalepovací defibrilační elektrody pro případ, že dojde k vyvolání život ohrožujících tachyarytmií.
Během samotného výkonu se snažíme o udržení optimálního hemodynamického stavu. Používáme bolusové dávky nebo kontinuální infuzi vazopresorů (noradrenalinu) k udržení dostatečného perfuzního tlaku, a to především v období rychlé stimulace komor, kdy dochází k výraznému poklesu krevního tlaku, a proto je nezbytné zvýšení vaskulárního tonu k udržení dostatečné koronární perfuze. Po dilataci stenotické chlopně může dojít ke vzniku masivní aortální regurgitace, v této době se snažíme vyhnout hypertenzi a udržujeme spíše vyšší tepovou frekvenci (buď farmakologicky nebo pomocí zevní stimulace). Samozřejmé je také sledování acidobazické rovnováhy a krevních plynů, mineralogramu, hematokritu a případná korekce patologických hodnot.
TAVI je prováděna pod profylaktickou antibiotickou clonou (potencovaným amoxicilinem, při alergii na penicilinovou řadu teicoplaninem). Den před vlastní procedurou je aplikována perorální nasycovací dávka (300 mg) clopidogrelu, a pokud pacienti dosud neužívali acetylsalicylovou kyselinu, je započato s jejím podáváním. Během výkonu jsou pacienti antikoagulováni heparinem (5000 j. – cílová hodnota aktivovaného času srážení > 250 s.) a následně minimálně po dobu 6 měsíců užívají duální protidestičkovou terapii.
Pooperační sledování
Pacient je po skončení výkonu převezen na jednotku intenzivní péče – koronární jednotku. Zde je sledován minimálně po dobu prvních 48 hodin, kdy předpokládáme rozvoj eventuálních komplikací. Pacient je nadále invazivně monitorován, v případě potřeby je napojen na monitorovací systém VigileoTM(Edwards Lifesciences Inc., Irvin, CA, USA). Bezprostředně po výkonu je provedeno transtorakální echokardiografické vyšetření, které zhodnotí funkce implantované chlopně, určí tlakové gradienty na chlopni a stanoví případnou přítomnost aortální regurgitace. Pravidelné echokardiografické kontroly pak provádíme minimálně v prvních dvou poimplantačních dnech. Invazivní vstupy ponecháváme podle potřeby, externí kardiostimulaci však maximálně do 48 hodin od výkonu, pokud nejsou zaznamenány poruchy rytmu. Ty patří k nejčastějším komplikacím TAVI. Jedná se především o blokádu levého Tawarova raménka, která může být u více jak poloviny pacientů, nebo o kompletní AV blokádu, především u pacientů s již přítomným blokem pravého Tawarova raménka. Potřeba dočasné nebo trvalé kardiostimulace je udávána kolem 20 % [7]. Dále sledujeme dynamiku kardiospecifických enzymů, protože může dojít k embolizaci detritu do koronárních arterií a vzniku infarktu myokardu.
Velmi důležité je sledování stavu třísel po katetrizaci a také prokrvení obou dolních končetin. Kromě krvácení z míst vpichů může následně dojít k vývoji pseudoaneurysmatu arterie, či může vzniknout stenóza tepny v místě perkutánní sutury. Vzhledem k polymorbiditě pacientů a časté přítomnosti různého stupně renální insuficience je po TAVI nutné sledovat renální parametry, funkce ledvin může být zhoršena aplikací většího množství kontrastní látky během výkonu. Přítomnost plicních onemocnění vyžaduje intenzivní rehabilitaci respiračního systému, důležité je též časné zahájení celkové rehabilitace méně mobilních pacientů.
Diskuse
První katetrizační implantaci aortální chlopně provedl v roce 2002 profesor Alan Cribier [8]. Metoda byla zprvu kardiologickou komunitou přijímána velmi rezervovaně, avšak v současné době je program TAVI úspěšně nastartován v mnoha zahraničních a také v několika domácích centrech. Mnoho otázek dosud není jasně zodpovězeno (např. dlouhodobá spolehlivost této náhrady), a proto je metoda vyhrazena pouze vysoce rizikovým pacientům, jejich odhadovaná délka života by však měla přesahovat nejméně 1 rok. Po kladném vyhodnocení výsledků probíhajících studií lze v budoucnosti očekávat, že metoda bude stále více využívána i pro méně rizikové skupiny nemocných.
Vzhledem k věku a polymorbiditě nemocných je anesteziolog, který se TAVI účastní, postaven před nelehký úkol bezpečně provést vysoce rizikového pacienta celou procedurou. Měl by být v mezích možností připraven na komplikace, které mohou nastat během samotného výkonu či po něm. Jedná se především o různý stupeň krvácení při poškození femorální nebo ilické tepny, dále je možný vznik cévní mozkové příhody a infarktu myokardu embolizací detritu z rozvolněné kalcifikované chlopně anebo aortální disekce či ruptury stěny aorty.
Přes dosud omezené množství dat se metoda TAVI jeví ve zkušených zahraničních centrech jako úspěšná a perspektivní – dvouleté přežívání je u 70 až 80 % nemocných s výrazným zlepšením funkční klasifikace NYHA a tedy i kvality života [9]. Zajímavou indikací do budoucna se jeví i perkutánní implantace chlopně do degenerativně změněné aortální bioprotézy, zejména s ohledem na zvýšené riziko, které s sebou přináší klasická reoperace [10].
Podpořeno Kardiovaskulárním výzkumným záměrem Univerzity Karlovy v Praze č. MSM0021620817.
Došlo 20. 7. 2009.
Přijato 16. 9. 2009.
Adresa pro korespondenci:
Prof. MUDr. Tomáš Vaněk, CSc.
Kardiochirurgická klinika 3. LF UK a FNKV
Šrobárova 50
100 34 Praha 10
e-mail: vanek@fnkv.cz
Zdroje
1. Vojáček, J. První katetrizační implantace aortálních chlopní v České republice. Interv. Akut. Kardiol., 2009, roč. 8, s. 9–14.
2. Želízko, M., Janek, B., Netuka, I. et al. Perkutánní implantace aortální chlopně u nemocné s těsnou aortální stenózou. Interv. Akut. Kardiol., 2009, roč. 8, s. 43–46.
3. Šťásek, J., Vojáček, J., Bis, J. et al. První zkušenost s perkutánní transfemorální implantací chlopně Edwards SAPIENTM u nemocných s aortální stenózou. Interv. Akut. Kardiol., 2009, roč. 8, s. 47–51.
4. Basciani, R., Trachsel, S., Zobrist, C. et al. Anaesthesia options for transcatheter aortic valve implantation in high-risk patiens with severe aortic stenosis. J. Cardiothorac. Vasc. Anesth., 2009, roč. 23, s. S11.
5. Billings, F. T., Kodali, S. K., Shanewise, J. S. Transcatheter aortic valve implantation: anesthetic considerations. Anesth. Analg., 2009, roč. 108, s. 1453–1462.
6. Covello, R. D., Maj, G., Landoni, G. et al. Anesthetic management of percutaneous aortic valve implantation: focus on challenges encountered and proposed solutions. J. Cardiothorac. Vasc. Anesth., 2009, roč. 23, s. 280–285.
7. Pizza, N., Onuma, Y., Jesserun, E. et al. Early and persistent intraventricular conduction abnormalities and requirements for pacemaking after percutaneous replacement of aortic valve. JACC Cardiovasc. Interv., 2008, roč. 1, s. 310 až 316.
8. Cribier, A., Eltchanioff, H., Bash, A. et al. Percutaneous transcatheter implantation of an aortic valve prothesis for calcific aortic stenosis: first human case description. Circulation, 2002, roč. 106, s. 3006–3008.
9. Vahanian, A., Alfiery, O., Al-Attar, N. et al. Transcatheter valve implantation for patients with aortic stenosis: a position statement from the European Association of Cardio-Thoracic Surgery (EACTS) and the European Society of Cardiology (ESC), in collaboration with the European Association of Percutaneous Cardiovascular Interventions (EAPCI). Eur. Heart J., 2008, roč. 29, s. 1463–1470.
10. Attias, D., Himbert, D., Brochet, E., Laborde, J.C., Vahanian, A. “Valve-in-valve” implantation in a patient with degenerated aortic bioprosthesis and severe regurgitation. Eur. Heart J., 2009, [Epub ahead of print]
Štítky
Anesteziologie a resuscitace Intenzivní medicína
Článek Co přinesl rok 2009?Článek Primář MUDr. Jiří DostálČlánek Mitigace pandemie chřipkyČlánek JMENNÝ REJSTŘÍKČlánek VĚCNÝ REJSTŘÍK
Článek vyšel v časopiseAnesteziologie a intenzivní medicína
Nejčtenější tento týden
2009 Číslo 6- Bezpečnostní profil metamizolu – systematický přehled
- Aktuální pohled na využití myorelaxancií a jejich antidot v moderní anesteziologii a intenzivní medicíně
- Perorální antivirotika jako vysoce efektivní nástroj prevence hospitalizací kvůli COVID-19 − otázky a odpovědi pro praxi
- Neodolpasse účinně snižuje pooperační bolest
- Neodolpasse jako ideální volba tam, kde je bolest provázena spasmem kosterního svalstva
-
Všechny články tohoto čísla
- Co přinesl rok 2009?
- Kam směřuje Česká společnosti intenzivní medicíny v nejbližších letech?
- Perkutánní implantace aortální chlopně z pohledu anesteziologa
- Kontinuální versus intermitentní podání vankomycinu u grampozitivních infekcí rezistentních na beta-laktamová antibiotika u nemocných v intenzivní péči
- Prognostické faktory výsledku léčby komunitní purulentní meningitidy dospělých
- Krvácivé komplikace a předávkování antikoagulační léčby
- Etické problémy při poskytování neodkladné péče
- The development of intensive care medicine in Israel from its creation until today
- Primář MUDr. Jiří Dostál
- Blahopřání doc. MUDr. Adolfě Scheinarové, CSc., k životnímu jubileu
- Mitigace pandemie chřipky
- JMENNÝ REJSTŘÍK
- VĚCNÝ REJSTŘÍK
- Anesteziologie a intenzivní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Krvácivé komplikace a předávkování antikoagulační léčby
- Etické problémy při poskytování neodkladné péče
- Kontinuální versus intermitentní podání vankomycinu u grampozitivních infekcí rezistentních na beta-laktamová antibiotika u nemocných v intenzivní péči
- Primář MUDr. Jiří Dostál
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



