-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Konsenzuální doporučení Českého národního hemofilického programu (ČNHP) pro diagnostiku a léčbu pacientů s hemofilií, vydání 3., rok 2021
Consensual guidelines of the Czech National Haemophilia Programme (CNHP) for the diagnosis and treatment of patients with haemophilia, 3rd edition, year 2021
The aim of these guidelines is to set-up and standardize diagnostic as well as therapeutic approaches to patients with haemophilia according to updated scientific evidence. Update of the original consensual guidelines reflects new available data plus advent of new drugs and recommends the optimal dosage for treatment. The system for haemophilia care in Czech Republic is briefly described.
Keywords:
haemophilia – guidelines – diagnosis – treatment – Prophylaxis
Autoři: Pracovní Skupina Čnhp Pro Standardy:; P. Smejkal 1; J. Blatný 2; Z. Hajšmanová 3; A. Hluší 4; R. Hrdličková 5; E. Zápotocká 6; M. Penka 1; Rady Koordinační Jménem; Výkonné Rady Čnhp:; B. Blažek 7; Z. Čermáková 5; Z. Černá 8; P. Ďulíček 9; J. Hak 10; V. Komrska 6; P. Ovesná 11; D. Pospíšilová 12; D. Procházková 13; P. Timr 14; J. Ullrychová 15; I. Vonke 16; L. Walterová 17
Působiště autorů: Oddělení klinické hematologie, FN Brno 1; Oddělení dětské hematologie, FN Brno 2; Ústav klinické bio chemie a hematologie, FN Plzeň 3; Hemato-onkologická klinika, FN Olomouc 4; Klinika hematoonkologie a Krevní centrum, FN Ostrava 5; Klinika dětské hematologie a onkologie, FN Motol, Praha 6; Klinika dětského lékařství, FN Ostrava 7; Dětská klinika, FN Plzeň 8; IV. interní hematologická klinika, FN Hradec Králové 9; Dětská klinika, FN Hradec Králové 10; Institut bio statistiky a analýz LF MU, Brno 11; Dětská klinika, FN Olomouc 12; Dětská klinika, Krajská zdravotní a. s., Masarykova nemocnice v Ústí nad Labem 13; Dětské oddělení, Nemocnice České Budějovice 14; Oddělení klinické hematologie, Krajská zdravotní a. s., Masarykova nemocnice v Ústí nad Labem 15; Oddělení klinické hematologie, Nemocnice České Budějovice 16; Oddělení klinické hematologie, Krajská nemocnice Liberec 17
Vyšlo v časopise: Transfuze Hematol. dnes,27, 2021, No. 1, p. 73-90.
Kategorie: Doporučené postupy
doi: https://doi.org/10.48095/cctahd202173Souhrn
Cílem standardu je stanovit základní diagnostické a především terapeutické postupy v péči o pacienty s hemofilií na základě aktualizovaných vědeckých poznatků. Úprava původního konsenzuálního doporučení odráží nová data i příchod nových léků a doporučuje optimální dávkování pro léčbu. Stručně je popsán systém péče o hemofilii v České republice.
Klíčová slova:
hemofílie – doporučení – diagnostika – léčba – profylaxe
PREAMBULE
Ačkoli doporučení a informace obsažené v následujícím textu jsou formulovány v dobré víře a na základě znalostí aktuálně dostupných v době zveřejnění dokumentu, autoři, ČNHP (Český národní hemofilický program), žádná ze zainteresovaných odborných společností ani vydavatel tohoto doporučení nenesou žádnou právní zodpovědnost za obsah tohoto textu.
STRUČNÁ CHARAKTERISTIKA DOPORUČENÍ
Cílem doporučení je stanovit základní diagnostické a terapeutické postupy v péči o pacienty s hemofilií A a B. Na toto doporučení navazují doporučení pro zajištění chirurgických/ortopedických výkonů a doporučení pro léčbu hemofilie s inhibitorem.
HLAVNÍ EPIDEMIOLOGICKÉ CHARAKTERISTIKY
Doposud udávaná incidence choroby byla přibližně 1 případ na 5 000 narozených chlapců. Hemofilie A je častější než hemofilie B, hemofilie A tvoří 80–85 % hemofilické populace [1]. Výskyt hemofilie není závislý na rase. V roce 2018 bylo dle Světové federace hemofilie (World Federation of Hemophilia – WFH) registrováno 210 454 pacientů s hemofilií na 6,991 miliardy populace, ze které WFH čerpala data o prevalenci hemofilie [2]. Ve vyspělých státech je diagnostikováno 90–100 % případů. V ČR bylo v roce 2018 registrováno 867 pacientů s hemofilií A a 136 s hemofilií B, z toho cca 1/5 dětí [2]. V letošní aktualizaci Doporučení pro léčbu hemofilie WFH je však udaná o něco vyšší odhadovaná incidence hemofilie, pro hemofilii A 246 případů a pro hemofilii B 50 případů na milion mužské populace [3].
ETIOLOGIE
Hemofilie A a B jsou dědičné krvácivé choroby, které jsou způsobeny deficitem koagulačního faktoru (F) VIII, resp. FIX. Dle tíže defektu koagulační aktivity FVIII (FVIII: C) nebo FIX (FIX: C) se oba typy hemofilie dělí na hemofilii těžkou (< 1 %), středně těžkou (1–5 %) a lehkou (> 5–40 %) [1,3,4]. Za fyziologickou hladinu koagulační aktivity FVIII/FIX se považuje rozpětí 50–150 %.
Dědičnost je v obou případech recesivní, vázaná na pohlavní chromozom X. Ženy s postiženým chromozomem tuto nemoc přenášejí. Z uvedené dědičnosti vyplývá, že muž hemofilik (XHY) a zdravá žena (XX) budou mít všechny syny zdravé (XY) a všechny dcery přenašečky (XHX). Žena přenašečka (XHX) a zdravý muž (XY) budou mít 50 % synů zdravých (XY) a 50 % nemocných (XHY) a 50 % dcer zdravých (XX) a 50 % přenašeček (XHX). Nemocní hemofilií jsou muži, u žen se choroba vyskytuje velmi vzácně. Žena může mít hemofilii, pokud je dvojitý heterozygot XHXH nebo hemizygot chromozomu X, kdy se může projevit např. Turnerův syndrom (XO). U více než 1/3 postižených je rodinná anamnéza negativní. V tomto případě se jedná buď o nově vzniklou mutaci, nebo je postižení bez klinických projevů onemocnění po generace přenášeno pouze ženami. Hladina faktoru vč. poměru koagulační aktivity k antigenu FVIII/FIX jsou přímým výrazem genetického postižení a u členů jedné rodiny bývají stejné. U těžké hemofilie A se nejčastěji setkáváme s inverzí v intronu 22 (až ve 45 %) nebo v intronu 1 (kolem 3–5 %), s delecí části genu (5–8 %) či s bodovou mutací (asi 45 %) a méně často s inzercí nebo delecí několika nukleotidů. U středně těžkých a lehkých forem hemofilie A převládají bodové mutace [5,6]. U hemofilie B nebyla nalezena žádná predominantní mutace, převažují bodové mutace (80 %). Raritou je mutace v promotoru genu FIX, která se fenotypicky projevuje v dětství středně těžkou formou hemofilie B a v dospělosti vlivem androgenní stimulace dochází k vzestupu FIX na lehký deficit či až k jeho normalizaci (hemofilie B Leyden) [7]. V ostatních případech hemofilie A/B je hladina faktorů celoživotně stejná.
PODSTATA STRUKTURÁLNÍCH A FUNKČNÍCH ZMĚN
FVIII i FIX patří mezi plazmatické koagulační faktory. Oba se tvoří v játrech, FVIII v minimálním množství i v jiných tkáních. FIX je na vitamínu K závislá serinová proteáza, která se v krvi vyskytuje jako proenzym (zymogen). Na aktivní enzym je aktivován komplexem tkáňový faktor + FVIIa za přítomnosti fosfolipidů a vápníkových iontů nebo FXIa. Vitamin K je nutný pro gama-karboxylaci FIX, která je nezbytná pro jeho funkční aktivitu. FVIII není zymogen a je v plazmě chráněn před inaktivací vazbou na von Willebrandův faktor (VWF). I když jsou obě choroby způsobeny chyběním různého koagulačního faktoru, jejich klinické projevy jsou stejné, protože oba dva faktory působí v koagulační kaskádě společně; FVIIIa je kofaktorem FIXa při aktivaci FX (komplex je nazýván tenáza). Příčinou krvácení u hemofilie je selhání sekundární hemostázy. Dojde sice k vytvoření primární destičkové zátky a vzniku menšího množství trombinu, vlivem defektu FVIII či FIX však selhává cesta amplifikace koagulace a celkově vytvořené množství trombinu je nedostatečné pro vznik kvalitní fibrinové sítě. Nedochází tak k úplné zástavě krvácení, u těžkých forem hemofilie se sice dočasně zmírní, ale trvale se nezastaví [8].
Nejčastějším typem krvácení u těžké hemofilie je krvácení do kloubů, které většinou vzniká „spontánně“. Místem vzniku krvácení jsou pravděpodobně subsynoviální kapilární pleteně [9]. Opakované krvácení do kloubů vede k reaktivní synovitidě a k destrukci kloubní chrupavky. Klíčovou roli má železo uvolněné z erytrocytů. Depozita hemosiderinu v synoviální tkáni indukují proliferaci synovie a neovaskularizaci subsynoviální vrstvy. Důsledkem je snadnější zranitelnost synovie a následný vznik dalšího krvácení. Synovie po krvácení produkuje více zánětlivých cytokinů a byla prokázána zvýšená exprese různých genů podílejících se na buněčné proliferaci. Výsledkem je vystupňování fagocytární aktivity vedoucí k porušení integrity kloubní chrupavky až k její destrukci. To je navíc podpořeno současnou inhibicí syntézy proteoglykanů následkem kontaktu chrupavky s krví [10]. Po ztrátě chrupavky nastupuje destrukce kosti se vznikem subchondrálních cyst a osteofytů, postupně dochází k fibrotizaci kloubu až k jeho ankylóze. Současně se prohlubuje svalová atrofie, vznikají kontraktury a deviace kloubní osy.
KLINICKÝ OBRAZ
Tíže klinických projevů u obou typů nemoci zpravidla odpovídá koagulační aktivitě faktorů v plazmě. Většinou v průběhu druhého roku života se u těžké hemofilie objeví první kloubní krvácení, která patří vedle tzv. pozdního krvácení po poraněních a chirurgických zákrocích k hlavním příznakům této krvácivé nemoci. U těžké formy hemofilie dochází průměrně jednou měsíčně ke spontánnímu krvácení do kloubu a 1–2× do roka do svalu, avšak frekvence krvácivých epizod je značně individuální, od krvácení více než 1× týdně až po jen ojedinělé projevy 1–2× ročně. U těžkých hemofiliků se může objevit hematurie, krvácení do zažívacího traktu, retroperitonea (musculus iliopsoas). Velmi závažné je mozkové krvácení (větší riziko je perinatálně: 1–4 %) [11]. U lehčích forem hemofilie jsou krvácivé projevy méně nápadné a krvácení se může objevit pouze při úrazech a invazivních zákrocích. Krvácením mohou být ohroženy i ženy přenašečky, mají-li hladinu faktorů nižší než cca 40 %.
Následkem opakovaného krvácení do kloubů dochází u pacientů s těžkou hemofilií k jejich postupnému poškození až destrukci a rozvoji hemofilické artropatie.
DIAGNOSTIKA
Diagnózu onemocnění lze stanovit na základě stanovení snížené koagulační aktivity FVIII/FIX. Současně je nutné vyloučení inhibitoru a u hemofilie A von Willebrandovy choroby (VWCH) typ 2, Normandy. Významně k diagnóze přispívá pozitivní rodinná anamnéza s X-recesivním způsobem dědičnosti.
Základní vyšetření (na všech hematologických ambulancích ve spojení s hematologickou laboratoří regionálního hemofilického centra):
1. Screening krvácivého stavu:
a. anamnéza se zaměřením na krvácivé projevy – osobní i rodinná;
b. základní koagulační testy odebírané při screeningovém vyšetření krvácivého stavu – trombocyty, aktivovaný parciální tromboplastinový test (aPTT), protrombinový test (PT), fibrinogen. Pro hemofilii A/B je charakteristické prodloužení pouze aPTT a ostatní screeningová vyšetření jsou negativní s výjimkou vzácné varianty hemofilie Bm, kdy může být prodloužen i PT [12].
2. Stanovení FVIII: C a/nebo FIX: C jednofázovou koagulační metodou. Dle vybavení pracoviště, případně je nutné toto vyšetření provést na pracovišti vyššího stupně typu centra pro léčbu hemofilie (Hemophilia Treatment Centre – HTC) nebo centra komplexní hemofilické péče (Hemophilia Comprehensive Care Centre – HCCC). Diagnóza onemocnění musí být vždy potvrzena na pracovišti typu HTC/CCC. Především u lehčích forem hemofilie A může být hladina stanovená jednofázovou metodou u některých pacientů odlišná od hladiny stanovené metodou dvoufázovou, resp. fotometrickou pomocí chromogenního substrátu [3]. U lehké a středně těžké formy je doporučeno stanovit FVIII vždy oběma metodami (jednofázovou i chromogenní).
3. Orientační stanovení inhibitoru pomocí směsného testu na bázi aPTT vč. inkubace (tzv. stanovení cirkulujícího antikoagulans) nebo přímo vyšetření inhibitoru Bethesda metodou (na pracovišti typu HTC nebo HCCC).
Vyšetření uvedená v bodu 1 a 2 je nutno provést i u všech možných přenašeček hemofilie k vyloučení rizika krvácení.
Specializované vyšetření (na pracovištích typu HTC a HCCC):
1. Vyšetření inhibitoru a jeho přesné stanovení (titr) pomocí Bethesda metody, nejlépe Nijmegen modifikací [13], která odfiltruje falešně pozitivní hraniční inhibitory (0,5–1,5 BU/ml).
Poznámka: Inhibitor je nutno pravidelně sledovat v průběhu substituce koncentráty FVIII/FIX pro riziko vzniku alogenního inhibitoru FVIII/FIX. Během prvních 25 dnů expozice koncentrátů FVIII/FIX doporučujeme vyšetřit inhibitor FVIII/FIX po každých cca 3–5 dnech expozice (ED) alogennímu koncentrátu FVIII/FIX, později každých cca 10 ED do 50., ideálně až do 75. dne [14] expozice, a dál každých 20 ED do 100. dne expozice, resp. à 6 měsíců do 150. dne expozice. Dále stačí vyšetření inhibitoru provádět alespoň jednou ročně. Při změně koncentrátu FVIII/FIX je doporučeno během prvních 30 expozičních dnů inhibitor vyšetřovat po každých 5–10 ED, u dospělých pacientů již dříve léčených vícero koncentráty záleží na klinickém stavu. Inhibitor je třeba rovněž vyšetřit při podezření na snížení terapeutické odpovědi na podávaný faktor [3,15,16].
2. U všech hemofiliků je nezbytné molekulárně genetické vyšetření k identifikaci kauzální mutace a stanovení haplotypu hemofilické alely. Molekulárně genetické vyšetření je nutné pro:
a) charakterizaci onemocnění;
b) identifikaci přenašeček onemocnění;
c) zajištění možnosti prenatální diagnostiky (v případě přenašeček);
d) určení/odhad rizika vzniku inhibitoru (nejvyšší je v případě velkých delecí, nonsense mutací a inverze intronu 1 a 22).
Genetické vyšetření je doporučeno provést u všech pacientů, především však u těžké formy onemocnění. U lehčích forem zejména pokud je v rodině možná přenašečka ve fertilním věku. Přenašečství hemofilie by mělo být stanoveno před dosažením fertilního věku. Prenatální vyšetření se provádí z DNA izolované ideálně z choriové biopsie v 11.–13. týdnu gravidity. Po vyšetření pohlaví se u plodů mužského pohlaví stanovuje přítomnost hemofilické alely buď pomocí haplotypu polymorfních markerů nebo kauzální mutace. Alternativně lze v 15.–18. týdnu využít amniocentézu. Prenatální diagnostiku lze od 7.–9. týdne gravidity provést i z DNA plodu izolované z krve matky. Využít lze i diagnostiku preimplantační [1,3].
3. Pokud není pro hemofilii pozitivní rodinná anamnéza, je třeba provést vyšetření i ostatních koagulačních faktorů v rámci diferenciální diagnostiky prodloužení aPTT. U hemofilie A vyloučit zejména defekt faktoru V a von Willebrandovu chorobu (tuto vyloučit i u všech přenašeček hemofilie A). Pro vysokou frekvenci von Willebrandovy choroby je vhodné tuto vyloučit v rámci diferenciální diagnostiky u každého nového pacienta s hemofilií A i B.
4. Stanovení antigenu FVIII/FIX – pro klinický postup není nezbytné (pokud by bylo třeba, provedení by mělo zabezpečit pracoviště typu HCCC).
U každého nově diagnostikovaného pacienta s hemofilií doporučujeme vyšetřit:
- hladinu FVIII: C/FIX: C jednofázovou koagulační metodou minimálně ze dvou různých odběrů, VWF antigen (VWF: Ag) a ristocetin kofaktor (VWF: RCo);
- u lehké a středně těžké formy hemofilie A je vhodné provést vyšetření hladiny FVIII: C i metodou chromogenní vzhledem k možným diskrepantním nálezům FVIII: C stanoveným metodou jednofázovou a chromogenní;
- vyloučit inhibitor;
- provést genetické vyšetření a důkladnou anamnézu rodokmenu s cílem zaměřit se v rodině na možné přenašečky hemofilie ve fertilním věku (u přenašeček je také nutné vyšetření koagulační ke zhodnocení rizika krvácení). Je důležité shromažďovat i údaje o zemřelých hemofilicích;
- markery hepatitidy A, B, C a HIV (parvoviru B19);
- jaterní testy;
- krevní skupinu;
- protilátky proti krevním elementům;
- nově diagnostikovanému pacientovi vystavit průkazku o krvácivé chorobě.
Diferenciální diagnostika
Diferenciálně diagnosticky při nálezu snížené hladiny FVIII musíme vyloučit především získaný inhibitor (specifický proti FVIII nebo typu lupus antikoagulans), von Willebrandovu chorobu (především typ 2N – vyšetření vazebné kapacity VWF pro FVIII), kombinovaný defekt faktorů. Fyziologicky se s lehce nižší hladinou FVIII můžeme setkat u osob s krevní skupinou 0. Při snížení FIX vylučujeme opět inhibitor FIX a vzácné defekty jiných faktorů a/nebo jejich kombinace.
Dispenzarizace
Všichni pacienti s krvácivými projevy opakovaně léčení krevními deriváty musí být pravidelně dispenzarizováni na pracovišti typu HTC či HCCC vzhledem k riziku krví přenosných infekcí, rozvoji inhibitoru FVIII/FIX, progresi hemofilické artropatrie či jiného poškození organizmu v souvislosti s opakovaným krvácením a jeho léčbou. Děti doporučujeme dispenzarizovat častěji – těžké hemofiliky minimálně 2× ročně, středně těžké a lehké minimálně 1× ročně. Dospělé pacienty s lehkou a se středně těžkou formou hemofilie, kteří nemají krvácivé projevy a nevyžadující substituční léčbu koagulačními faktory, stačí dispenzarizovat 1× za 2–3 roky, dospělé těžké hemofiliky minimálně 1–2× ročně. Pacientům je vhodné doporučit očkování proti hepatitidě A a B.
V rámci dispenzarizace je nutno sledovat [3,17,18]:
- projevy, lokalizaci a frekvenci krvácení od poslední kontroly;
- způsob a účinnost hemostatické léčby;
- inhibitor FVIII/FIX;
- stav kloubního aparátu – u pacientů s těžkou hemofilií vhodné využívat hemofilické skóre kloubního zdraví (Haemophilia Joint Health Score – HJHS), v případě možností vhodné použití bedside ultrazvukového vyšetření k detekci subklinického krvácení, synovitidy ad.;
- bolest a užívaní analgetik;
- markery hepatitidy B, C a HIV;
- jaterní testy, u pacientů s chronickou hepatitidou i alfa-fetoprotein;
- krevní obraz;
- případně protilátky proti krevním elementům;
- jiné změny dle klinického stavu, resp. charakteru krvácivých projevů;
- dodržování stomatologických kontrol minimálně v rozsahu běžném pro zdravou populaci (1× za půl roku);
- krevní tlak 1× ročně u dospělých jedinců.
Pracoviště typu HTC/CCC mají také možnost nabídnout a/nebo zprostředkovat konzultaci psychologa a sexuologa. Zejména pro děti, ale nejen pro ně, je vhodný preventivní rehabilitační/fyzioterapeutický program. Fyzioterapie je rovněž nedílnou součástí léčby krvácení.
LÉČBA
Pilířem péče jsou centra typu HCCC/HTC akreditovaná ČNHP a/nebo Ministerstvem zdravotnictví (MZd) ČR [19,20,21]. Ošetření nekomplikované krvácivé epizody a vydávání koncentrátů lze realizovat i na regionálních/spádových hematologických pracovištích, jestliže na ně centrum tuto pravomoc deleguje. Léčba každého pacienta s hemofilií však musí být pod dohledem centra HCCC/HTC, které provádí pravidelnou dispenzarizaci, vede léčbu a odpovídá za ni.
Léčba u hemofiliků je v současné době možná formou substituční a nesubstituční. Substituční léčba spočívá v podávání chybějících/defektních faktorů k dosažení hemostaticky dostatečné hladiny. Cílem je zástava krvácení a/nebo prevence jeho vzniku.
Možnosti léčby jsou:
1. léčba „on demand“ – koncentrát FVIII/FIX je podáván až při objevení se krvácení;
2. léčba profylaktická.
U dětských pacientů je doporučeným standardem léčby profylaktická aplikace koncentrátů FVIII/FIX. Profylaxe je indikovaná u těžkých hemofiliků (případně s vyšší hladinou FVIII/FIX, pakliže je spojena s fenotypovými projevy těžké hemofilie). Cílem je trvale udržet hladiny faktorů minimálně nad 1 %, ideálně nad 2 % [3,22]. Zejména s nástupem koncentrátů faktorů s prodlouženým účinkem (extended half-life – EHL) je zvažováno cílit na vyšší bazální hladiny (trough level) profylakticky podávaných koncentrátů. Při dosažení trvalé hladiny nad 3 % dochází k eliminaci většiny spontánních krvácení, při trvalé hladině nad 12 % osoba s hemofilií nekrvácí téměř vůbec [23].
a) primární profylaxe – takto se označuje profylaktická aplikace koncentrátu FVIII/FIX započatá nejpozději po první klinicky významné krvácivé epizodě nebo do ukončení druhého roku života
b) sekundární profylaxe – toto označení nese profylaxe započatá později než primární
c) terciární profylaxe – profylaxe aplikovaná u jedinců s již existujícím kloubním postižením
d) krátkodobá profylaxe – dle klinického stavu se přechodně (v době nepřesahující 45 týdnů v roce) zavádí po operaci, úrazu, při rehabilitaci apod.
DDAVP
Vzestupu plazmatické hladiny FVIII lze dosáhnout u některých pacientů s lehkou a středně těžkou formou hemofilie A podáním DDAVP (1-deamino-8-D-arginin vasopressin). Tam, kde to není možné, vhodné nebo indikované, je nutno použít koncentráty FVIII [24,25,26]. Standardní dávkování DDAVP je 0,3 µg/kg v i.v. infuzi trvající 20–30 min. Lék lze podat 2–3× v odstupu 12–24 h. Po takové dávce dochází k vzestupu FVIII 2–4×, s maximální hladinou za 30–60 min od ukončení aplikace, s plazmatickým poločasem 8–12 h. Dosažení hemostaticky dostatečné hladiny FVIII nad 40–50 % lze tedy očekávat u hemofiliků s výchozí hladinou FVIII nad 10–15 %. Před terapeutickým použitím je vhodné provést terapeutický pokus, při kterém se ověří vzestup hladiny FVIII. Při léčbě krvácení pak lze očekávat obdobný vzestup FVIII. Při nutnosti opakované aplikace je nutné počítat s efektem tachyfylaxe, tedy že vzestup hladiny FVIII při opakované aplikaci bude nižší než po první. Při druhé aplikaci bude vzestup nižší cca o 30 % a k méně výraznému snížení může docházet i po dalších dávkách. Při použití DDAVP je třeba respektovat jeho kontraindikace (zejména věk pod 2 roky, srdeční insuficience) a současně omezit příjem tekutin p. o. na 1–1,5 litru denně (u dospělé osoby) či obecně o cca 1/3 denního příjmu. Po podání DDAVP je vhodné kontrolovat hladiny iontů, zejména natria. DDAVP lze ve stejné dávce jako i.v. použít i s.c. s dosažením téměř stejného vzestupu FVIII jako po i.v. aplikaci s odstupem cca 60–90 min. od podání. Podobný efekt jako podkožní aplikace má použití intranazální v dávce 150 µg do každé nosní dírky (celkem tedy 300 µg). Při váze pod 50 kg se dávka snižuje na polovinu.
DDAVP lze nyní v ČR použít v rámci Specifického léčebného programu v centrech typu HCCC a HTC (27).
Koncentráty koagulačního FVIII/FIX
V ČR jsou používány plazmatické (pd), vysoce čištěné a dvojitě protivirově ošetřené koncentráty FVIII/IX s vysokým stupněm bezpečnosti i koncentráty rekombinantní (r) [28]. U dosud neléčených a minimálně léčených hemofiliků jsou upřednostňovány rekombinantní koncentráty FVIII/FIX. Pediatrická společnost ČLS JEP na doporučení své Pracovní skupiny pro dětskou hematologii (PSDH) doporučuje tyto rekombinantní, humánních proteinů prosté preparáty používat zejména pro nově narozené, dosud neléčené či minimálně léčené pacienty s hemofilií, s ohledem na maximální „virovou“ bezpečnost takové léčby. Tento postup je v souladu s pediatrickými doporučeními většiny zemí Evropské unie (EU) [15,22,24,25,26].
Nejasná je otázka vyššího výskytu inhibitoru po rFVIII, která je intenzivně zkoumána s nejednoznačnými závěry. Nebylo jednoznačně a bez výhrad prokázáno, že by použití rekombinantních faktorů bylo spojeno se signifikantně vyšším rizikem vzniku inhibitoru [29–38]. Studie SIPPET [39] sice prokázala vyšší incidenci inhibitorů vč. „high responderů“ (osob, u nichž je vysoká anamestická odpověď na opakované podání FVIII) u rekombinantních koncentrátů, ale tato studie je zatížena metodickými chybami (převážně se jednalo o non-kavkazskou populaci, byli zahrnuti i pacienti s předchozí expozicí transfuzních přípravků do 5 ED a léčebný režim použitý ve studii se zásadně lišil od léčby běžné v ČR, resp. ostatních zemích EU). Data z ČR nepotvrdila rozdíl v incidenci inhibitorů u dříve neléčených pacientů (previously untreated patients – PUPs) s hemofilií A v závislosti na typu léčebně podávaného koncentrátu FVIII [40].
U jednotlivého pacienta je vhodné substituci chybějícího faktoru provádět pokud možno jedním koncentrátem, protože medicínsky neodůvodněné střídání různých koncentrátů koagulačního faktoru (liší se způsobem zpracování a protivirového ošetření, což může mít vliv na výslednou imunoreaktivitu antigenu FVIII) bylo podezřelé z vyšší frekvence výskytu inhibitoru (zejména pro koncentráty FVIII). V současnosti převažuje názor, že toto riziko není prokázané [34,41], ale i přesto doporučujeme změnit koncentrát léčebně podávaného faktoru jen tehdy, je-li to nutné a pro pacienta výhodné [42].
Dávka podaných koncentrátů závisí na tíži hemofilie a na závažnosti krvácení, event. na charakteru plánovaného výkonu. Obecně se předpokládá, že u FVIII zvýší 1 mezinárodní jednotka (IU) /kg hladinu v průměru o cca 2 %, zatímco u FIX 1 IU /kg asi o 1 %, resp. u rekombinantních koncentrátů o 0,8 % [3]. Plazmatický poločas FVIII je přibližně 12 h, FIX kolem 18–24 h [3]. Tyto údaje sice platí pro většinu pacientů, ale reakce na podaný FVIII či FIX je individuální s velkou interindividuální variabilitou [43]. Je proto vhodné mít u každého hemofilika provedené vyšetření farmakokinetiky koncentrátu, kterým je léčen, minimálně pak znát „in vivo recovery“ (IVR – poměr mezi očekávaným a reálným vzestupem léčebně podaného faktoru) posuzující, zda dochází k předpokládanému procentuálnímu vzestupu plazmatické hladiny FVIII/FIX po aplikaci daného množství koncentrátu v IU /kg, a individuální eliminační poločas podávaného preparátu. Tyto údaje je vhodné zohlednit zejména při plánování léčby v souvislosti s chirurgickým zákrokem a při nastavení profylaktické léčby. Je rovněž doporučeno zhodnotit/srovnat je před plánovanou změnou preparátu (minimálně k prokázání „non-inferiority“ léku, na který má pacient přejít v porovnání s léčbou stávající).
Není-li individuální farmakokinetika známa, je u dětí a zejména novorozenců vhodné navýšit substituci koncentráty FVIII/FIX oproti dospělým (cca o 10–25 %) vzhledem k předpokládanému kratšímu plazmatickému poločasu. Při akutním krvácení či perioperačně musíme rovněž počítat se zkrácením plazmatického poločasu. U rFIX je třeba zohlednit jeho až o 30 % nižší IVR ve srovnání s koncentráty plazmatickými [24]. Doporučené plazmatické hladiny FVIII/FIX a trvání substituce dle doporučení WFH uvádí tab. 1. Podle klinického stavu je po každém závažném krvácení ke zvážení krátkodobá profylaxe v řádu několika týdnů.
Tab. 1. Doporučované hladiny faktoru a délka substituce u jednotlivých krvácivých epizod a operací (1, 3, 22, 26). 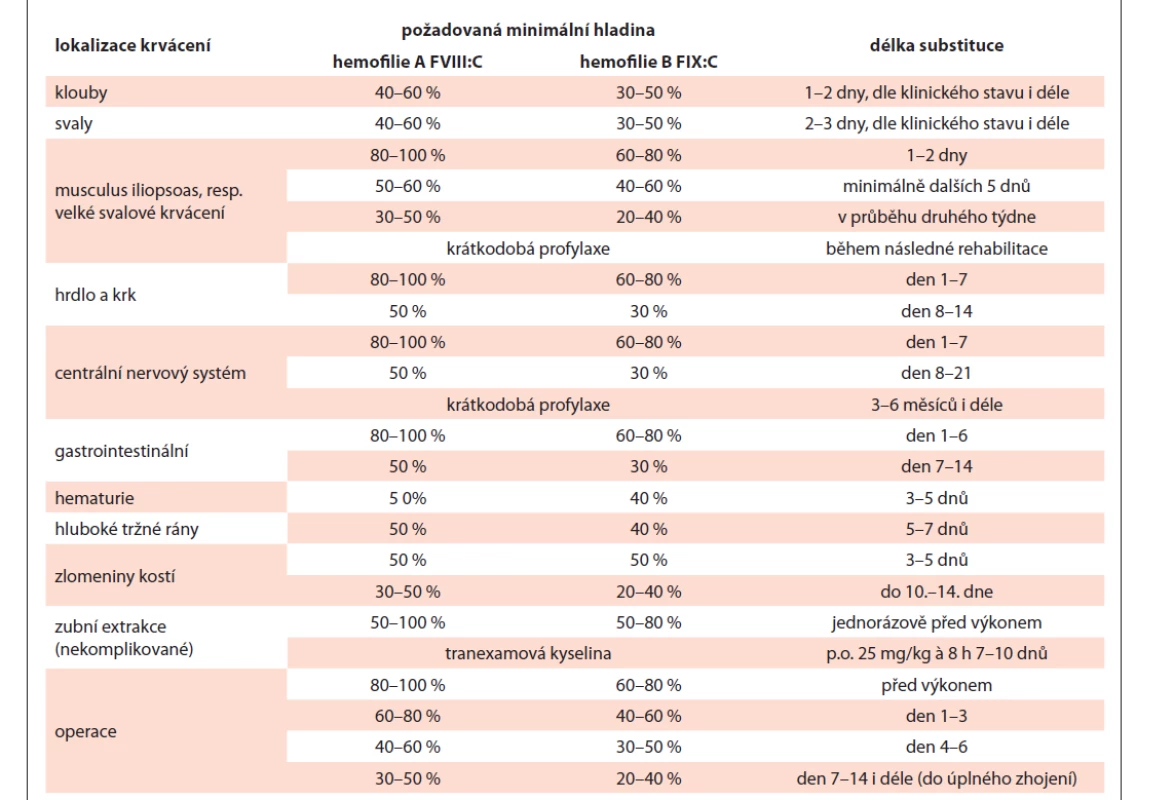
FVIII:C – koagulační aktivita faktoru VIII, FIX:C – koagulační aktivita FIX Kontinuální infuze FVIII/FIX
Kromě bolusové aplikace lze s úsporou množství až 30 % použitého koncentrátu podávat FVIII/FIX formou kontinuální infuze. Obava z vyššího výskytu inhibitorů při takové léčbě nebyla potvrzena [44,45].
Koncentráty rFVIII a rFIX s prodlouženým plazmatickým poločasem (extended half-life – EHL)
Do roku 2020 byly v ČR registrovány čtyři koncentráty rFVIII s prodlouženým plazmatickým poločasem (t1/2) (EHL-rFVIII) a jeden EHL-rFIX, které jsou i hrazeny ze zdravotního pojištění. Pegylované koncentráty EHL-rFVIII je doporučené používat až od věku 12 let, u koncentrátů vázaných s Fc fragmentem imunoglobulinu toto omezení není. Od zavedení EHL koncentrátů lze očekávat zvýšení efektivity léčby a kvality života osob s hemofilií bez zásadní změny nákladů. Dle britských doporučení UKHCDO z roku 2016 [46] jsou EHL vhodné pro dříve již léčené pacienty (previously treated patients – PTPs) a minimálně léčené pacienty (minimaly treated patients – MTPs) s více než 50 ED léčby. Toto doporučení je potvrzeno i stavajícím doporučením UKHCDO pro profylaxi [47]. Dle SPC EHL koncentrátů vázaných s Fc fragmentem imunoglobulinu není omezení pro použití u PUPs, na druhé straně britská doporučení UKHCDO doporučují u PUPs použití EHL koncentrátů pouze v rámci studií, resp. po 50 ED léčby standardním koncentrátem FVIII/FIX [46]. První klinická data o použití EHL u PUPs byla zveřejněna na kongresu ISTH v červenci 2020 [48], kde byla referována incidence inhibitoru u PUPs srovnatelná se stávajícími SHL rFVIII (31,1 % a high responderů 15,6 %). EHL rFVIII-Fc je nyní nově od 1. 11. 2020 hrazen v ČR i u PUPs a jeho použití v této věkové skupině může být s výhodou.
Pro stanovení vhodného dávkování, zejména v rámci profylaxe, britská guidelines doporučují zohlednit individuální farmakokinetiku těchto léčiv. Ne ve všech případech je užití EHL-rFVIII nutně spojeno s redukcí frekvence aplikace při profylaxi. EHL deriváty však mohou bez nutné změny intervalu podávání vést k možnosti dosahovat trvale vyšší hladiny (trough level) faktorů v plazmě pacienta, a tak zmírnit počet krvácení a zvýšit kvalitu života osob s hemofilií. T1/2 FVIII: C je u různých EHL-rFVIII koncentrátů v průměru prodloužen na 15–19 h. U EHL-rFIX koncentrátů je prodloužení t1/2 výraznější, pro různé koncentráty se pohybuje v průměru od 57 do 96 h [46].
Obsah jednotek FVIII: C a FIX: C v EHL koncentrátech je výrobci stanoven vůči standardu Světové zdravotnické organizace (World Health Organization – WHO). Evropská lékařská agentura (European Medicines Agency – EMA) doporučuje stanovovat obsah FVIII: C v EHL koncentrátech i měřit hladinu FVIII: C při léčebném užití chromogenní metodou. Pro EHL-rFIX koncentráty takové jednoznačné doporučení neexistuje. Výrobci je FIX: C stanovena většinou metodou jednofázovou. Jakou metodou je vhodné stanovovat FVIII: C/FIX: C v EHL koncentrátech, je na doporučení jeho výrobce [49–52]. Protože doposud je běžnou praxí stanovení FVIII: C i FIX: C jednofázovou metodou, jestliže v konkrétní laboratoři běžně používaná aPTT reagencie nestanoví po aplikaci EHL koncentrátu adekvátně hladinu FVIII: C
/FIX: C jednofázovou metodou, lze dosáhnout přesnějších výsledků použitím kalibrační plazmy specifické pro konkrétní EHL koncentrát faktoru [46]. Při stanovení hladiny FVIII/FIX je nutno zohlednit fakt, že u něktrých EHL přípravků mohou některé běžně používané reagencie dle typu obsaženého aktivátoru aktuální hladinu podměřovat či naopak nadměřovat. Je tedy vždy nutné úzce spolupracovat s hematologickou laboratoří. Nejpodrobnější zhodnocení na trhu dostupných reagencií aPTT pro jednofázovou metodu stanovení FVIII: C a FIX: C s ohledem na jejich vhodnost k monitorování EHL-rFVIII a EHL-rFIX udávají práce Younga a Grayové [53,54].
Nesubstituční terapie
Zahrnuje léčbu, při které je efektivní hemostázy dosaženo jiným způsobem než podáním deficitního faktoru (nefaktorová léčba). V současnosti je pro klinické použití dostupná tzv. mimikující léčba pro hemofilii A, ve vývoji jsou léky, jež působí proti přirozeným antikoagulantům, jako jsou TFPI (tissue factor pathway inhibitor); látka concizumab, antitrombin; látka fitusiran či aktivovaný protein C, a jež by se svým efektem mohly uplatnit u hemofilie A i hemofilie B [3].
Bispecifická monoklonální protilátka emicizumab mimikující funkci FVIII byla vyvinuta primárně k profylaktické léčbě pacientů s hemofilií A a inhibitorem FVIII, ale lze ji dle SPC, dle registrace EMA a FDA i dle britských doporučení UKHCDO použít k profylaxi i u pacientů s těžkou hemofilií A bez inhibitoru, s opatrností u pacientů ve věku < 2 roky [47]. Výrobcem doporučené dávkování emicizumabu bylo zvoleno tak, aby koagulační potenciál při plazmatické hladině emicizumabu 30–50 µg/ml odpovídal aktivitě FVIII přibližně 10–15 % [55]. Doposud ale nebyl nalezen způsob měření efektu emicizumabu, který by mohl být porovnatelný s fyziologickou hladinou FVIII: C; řečeno jinak, nelze přesně stanovit, jaké hladině FVIII: C odpovídá u konkrétního pacienta dosažená hladina emicizumabu. Přesnou odpověď nám nedají ani globální testy hemostázy jako generace trombinu či trombelastografické vyšetření vzhledem k odlišnému efektu emicizumabu od FVIII. Emicizumab se váže na jiná místa FIX, nerozlišuje mezi FIX a FIXa a FX a FXa, neváže se na von Willebrandův faktor ani na fosfolipidy. Jeho efekt není, na rozdíl od FVIIIa, regulován inhibitory krevního srážení [56].
Doporučené úvodní dávkování emicizumabu zahrnuje tzv. nasycovací fázi se 4 dávkami 3 mg/kg s.c. 1× týdně, jež je následovaná udržovací fází, kdy je podávána poloviční dávka 1× týdně. Alternativou je dávka 3 mg podávaná 1× za 2 týdny nebo 6 mg 1× za 4 týdny [57]. U prvních dvou dávkovacích režimů bylo dosaženo plazmatické hladiny emicizumabu před podáním další dávky v průměru kolem 50 µg/ml již 5. týden léčby [58,59]. U režimu s aplikací à 4 týdny se po třech měsících hladiny pohybovaly kolem 40 µg/ml [60]. Vzhledem k dosažení ustálené hladiny emicizumabu až s časovým odstupem je dle SPC doporučeno pokračovat v konkomitantní profylaktické aplikaci koncentrátem FVIII 1. týden zahájení terapie emicizumabem. Dle amerických doporučení u pacientů s krvácivým fenotypem může být opodstatněné pokračovat po zahájení léčby emicizumabem v profylaxi koncentráty FVIII i delší dobu než jeden týden [61]. Dle dosavadních zkušeností z ČR se zdá, že překlenutí je po dobu jednoho týdne postačující. Z praktického hlediska nutno zmínit, že již po první dávce emicizumabu dochází k normalizaci aPTT a obdobně jsou ovlivněny i všechny testy založené na aPTT (stanovení koagulačních faktorů VIII, IX, XI, XII jednofázovou metodou, vč. stanovení hladiny inhibitoru FVIII při použití standardních reagencií). Z tohoto důvodu při léčbě emicizumabem je nutné hladinu FVIII a inhibitor FVIII monitorovat chromogenní metodou s bovinními reagenciemi. Hladinu emicizumabu pak lze monitorovat jednofázovým testem FVIII nebo chromogenním testem FVIII s lidskými reagenciemi kalibrovaným na emicizumab [62]. Ovlivnění laboratorních testů emicizumabem přetrvává po dobu až 6 měsíců po jeho vysazení.
U pacientů léčených profylakticky emicizumabem některá drobná krvácení není třeba léčit, popřípadě je dostačující kombinace s antifibrinolytiky, pokud hladina FVIII, kterou mimikuje emicizumab (minimálně 10–15 % FVIII), postačuje k zástavě krvácení. Všechna závažnější krvácení a invazivní výkony je však nutné substituovat koncentrátem FVIII běžným způsobem, protože efekt podaného FVIII a emicizumabu se nepotencuje. Dokladováno je bezpečné podání opakovaných dávek koncentrátu FVIII v dávce 50 IU/kg podané ke kontrole krvácení. FVIII má vyšší afinitu k FIXa a FX než emicizumab [56]. Podstatný je klinický stav, protože, jak uvedeno výše, nelze přesně určit, jakého ekvivalentu hladiny FVIII je u konkrétního pacienta dosaženo. Klinickým podkladem jsou pak zkušenosti s provedením malých chirurgických výkonů (např. extrakce portu, zubní extrakce a pod), kde nebylo třeba konkomitantní léčby FVIII [63].
Nejasné zatím zůstává, zda u PUPs, u nichž byla primárně započata profylaxe emicizumabem, neaplikovat současně i koncentrát FVIII, případně EHL-rFVIII, jako formu imunotolerance (např. 1× za 7–14 dnů). Při dosažení efektivní profylaxe pomocí emicizumabu se nabízí možnost tuto formu imunotolerance posunout mimo časné dětství, a tím teoreticky snížit riziko rozvoje nepříznivé imunitní odpovědi. Podávání koncentrátu FVIII je doporučeno u pacientů s historií inhibitoru FVIII minimálně po dobu 1 roku po dosažení imunotolerance [47]. Jeví se tedy racionální takto postupovat i u PUPs.
Za současných znalostí lze shrnout, že emicizumab je indikován k profylaxi krvácení u osob s hemofilií A jak s inhibitorem (mimo i v rámci ITI), tak bez inhibitoru. Jeho použití u PUPs je možné, ale zatím není standardizováno. Konkomitantní použití emicizumabu a FVIII není spojeno se známým rizikem. Konkomitantní použití emicizumabu s by-passovými preparáty (zejména aPCC) se řídí zvláštními doporučeními. Emicizumab by měl být podáván pouze v rámci hemofilických center, pacient by měl být vždy pečlivě edukován a léčba komplikovaných krvácení či operací patří do rukou HCCC center, případně HTC center (osoby s hemofilií A bez inhibitoru), která disponují laboratoří, jež je schopna takovou léčbu spolehlivě monitorovat a hodnotit.
Genová terapie
I když v genové terapii s přenosem genu pro FIX a genu pro FVIII s delecí B domény pomocí adenovirus asociovaného vektoru (AAV) bylo dosaženo značného pokroku, genová terapie je dosud dostupná jen v rámci klinických studií 1.–3. fáze. Při použití genu pro hyperfunkční variantu Padua FIX bylo dlouhodobě dosaženo plazmatických hladin FIX: C nad 30 %. U hemofilie A byla popsána exprese FVIII s hladinou FVIII: C tři roky kolem 50 % [64]. Tato léčba v ČR zatím není v klinické praxi dostupná.
PRINCIPY TERAPIE KRVÁCIVÝCH EPIZOD
1. Léčba krvácení by měla být zahájena co nejdříve, čímž lze minimalizovat poškození tkání a předcházet pozdějším komplikacím. Výjimkou jsou pacienti léčení emicizumabem, kde je zahájení konkomitantní léčby doporučeno zvážit s časovým odstupem a po konzultaci s hematologem hemofilického centra. Níže uvedená doporučení jsou tedy platná zejména pro pacienty neléčené emicizumabem.
2. Je vhodné, aby u všech pacientů s vysokým rizikem krvácení (minimálně u těžkých hemofiliků) byla zavedena domácí léčba a pacient (případně rodiče) si byl schopen aplikovat koncentrát koagulačního faktoru sám, bezodkladně.
3. Začátek krvácení nejlépe pozná pacient sám a v ideálním případě je léčba zahájena při časných známkách krvácení ještě před manifestací krvácení dle fyzikálního vyšetření.
4. Pokud není do 12–24 h adekvátní léčebná odpověď na substituci koagulačního faktoru, je nutné vyšetření lékařem hematologem s ověřením aktivity FVIII, případně vyloučením inhibitoru.
5. Terapie musí být vedená pod dohledem centra typu HTC, resp. HCCC.
6. Při mírném a středně těžkém krvácení (nejčastěji se jedná o krvácení do kloubů, do svalů, epistaxe, krvácení z dásní, z povrchových ran) je vhodné dosáhnout hladiny FVIII 40–60 % a FIX 30–50 %, tedy aplikovat u těžké hemofilie FVIII 20–30 IU/kg a FIX 30–50 IU/kg.
7. Je-li podezření na život či končetinu ohrožující krvácení, je nutné nejprve substituovat koagulační faktor s cílem dosáhnout plazmatické hladiny 80–100 % a teprve potom provádět vyšetření k potvrzení diagnózy – zejména při podezření na krvácení do centrálního nervového systému (CNS).
8. Při závažném krvácení (intrakraniálním, do míchy, v oblasti krku, do hrudníku, břicha, pánve, musculus iliopsoas, jakémkoli rozsáhlém svalovém i kloubním krvácení, frakturách s dislokací, hlubokých poraněních, resp. jakémkoli masivním krvácení) je nutné dosáhnout hladiny FVIII 80–100 % a FIX 60–80 %, tedy u těžké hemofilie aplikovat FVIII 40–50 IU/kg a FIX 60–80 IU/kg.
DOPORUČENÝ POSTUP LÉČBY DLE LOKALIZACE KRVÁCENÍ [1,3,17,22,24–26, 65,66]
Krvácení do kloubu
- Při počínajícím krvácení do kloubu je většinou postačující dosáhnout požadovanou hladinu faktoru (FVIII 40–60 %, FIX 30–50 %) jednorázovou bezodkladnou aplikací faktoru. Při pokročilejším krvácení nebo i počínajícím krvácení do cílového kloubu podat druhou dávku faktoru za 12–24 h od první a třetí dávku přibližně 3. den od zahájení léčby.
- Jedná-li se o rozsáhlejší krvácení do velkého kloubu, musí se hemostatická hladina FVIII > 40 % či FIX > 30 % udržovat minimálně 2–3 dny i déle a iniciálně je vhodné dosáhnout hladiny FVIII > 80 % a FIX > 60 %.
- Vždy je vhodné kloub dle rozsahu krvácení minimálně 1 den imobilizovat elastickým/kompresním obinadlem v jeho „úlevové“ pozici a poté velmi pozvolně rozcvičovat a dalších 4–5 dnů plně nezatěžovat. Současně minimálně prvních 12–24 h kloub chladit, což zmírní prokrvení i bolest. Chlazení by mělo být intermitentní (opakovaně po dobu cca 20 min každé 2 h).
- Pokud do 12–48 h od zahájení substituce faktoru nedojde k ústupu potíží, lze po vyloučení inhibitoru (ověření hladiny faktoru) zvážit při velké náplni kloubu provedení odlehčovací aspirace kloubu za substituce FVIII/FIX minimálně nad 30–50 % a následně minimálně další 2–3 dny [3,67]. Tento postup je však alternativní a neexistuje literární pramen, který by tento postup u hemartros doporučoval standardně. U masivní náplně kloubu však artrocentéza může být prospěšná. Tento výkon může být proveden pouze v centru HTC/HCCC.
- Při recidivujícím krvácení do kloubu a rozvoji tzv. cílového kloubu (3 a více krvácení za 6 měsíců) je vhodné zavést (i u dospělého pacienta) alespoň krátkodobou profylaxi (2–3 měsíce), ideálně pak profylaxi dlouhodobou v minimální dávce FVIII 25 IU/kg 2× týdně až obden a FIX minimálně 25 IU/kg 2× týdně či každý 3. den, popřípadě využít EHL koncentrátů, jež mohou u individuálního pacienta pomoci nastavit vyhovující trough hladiny zabraňující opakovaným krvácením. V období mimo krvácení lze zkusit efekt selektivních COX-2 inhibitorů.
- Pokud tento postup situaci nezlepší a jsou známky chronické synovitidy (ověřit dle ultrazvukového vyšetření, případně dle magnetické rezonance), je vhodné zvážit provedení radiační synoviortézy s aplikací radionuklidu do kloubu. Náročnější je chirurgická synovektomie, která může být artroskopická či otevřená (viz další odstavec).
Léčba chronické synovitis
- Chronická synovitis je charakteristická nebolestivým otokem kloubu, který nereaguje na aplikaci koagulačního faktoru a který je současně provázen častým krvácením do kloubu.
- Jako první postup lze zvolit krátkodobou profylaxi koncentrátem FVIII/FIX, jejíž úspěšnost však nedosahuje ani 50 %.
- V období mimo krvácení lze využít i nesteroidní antiflogistika (NSAID), preferovány jsou selektivní COX-2 inhibitory.
- Individuálně lze zvážit i intraartikulární aplikaci kortikoidů, která krátkodobě zmírní symptomy [68].
- Radiační synoviortézu lze indikovat, pokud není zřejmý efekt profylaktické aplikace faktoru ani NSAID, ale i jako postup první volby vzhledem k většinou nedostatečnému efektu samotné profylaxe.
- Chirurgická synovektomie je vhodná až jako poslední možnost řešení chronické synovitis vzhledem k její náročnosti na substituci faktoru i riziku ztuhnutí kloubu.
- Uvedené postupy musí probíhat v gesci a na doporučení HTC/HCCC.
Radiační synovektomie (synoviortéza) [69–72]
- Indikací k zákroku je časté krvácení do kloubu bez reakce na krátkodobou profylaxi se známkami chronické synovitidy. Zákrok má největší efekt, pokud se provede ještě před destrukcí kloubní chrupavky, resp. ve stadiu ještě bez radiologických známek destrukce kloubu. Pokročilejší stupeň artropatie sice není kontraindikací výkonu, lze však očekávat jeho menší efekt. Výjimkou je destrukce kosti, kdy hrozí vlivem proniknutí radiofarmaka její nekróza.
- Synoviortézu je nevhodné provádět na kloubu po předchozím zakrvácení, proto při častém krvácení do kloubu před plánovaným termínem zákroku je vhodné vřadit cca na 2–4 týdny před zákrokem profylaxi koncentrátem FVIII/FIX.
- K zajištění zákroku je třeba dosáhnout fyziologické hladiny FVIII (80–100 %) a FIX (60–80 %) a po další 3 dny udržovat FVIII/FIX minimálně ≥ 30–40 %. Následně další 3–4 dny dávkování FVIII/FIX postupně snižovat a přejít na profylaxi minimálně na cca 3–6 týdnů i déle.
- První 2–3 dny po výkonu je nutné kloub imobilizovat.
- S rehabilitací lze začít až za týden od zákroku. Její délka (a tím i délka profylaktické aplikace koncentrátů) se odvíjí od klinického stavu – ztuhnutí kloubu vlivem přechodné imobilizace po zákroku.
- Zákrok lze na jednotlivém kloubu provést celkem až 3× s odstupem minimálně 3 měsíce mezi jednotlivými procedurami.
- Obvyklá dávka radionuklidu je 2–5 mCi, používán je radionuklid ytria *90, případně rhenia*186, dříve byl používán a v USA je dosud doporučován fosfor *32 (nevýhodou je dlouhý poločas rozpadu – 2 týdny, oproti zhruba 3 dnům u předchozích dvou radionuklidů).
- Zákrok lze provést po konzultaci s HCCC i v dětském věku. Dolní věková hranice není přesně stanovena; je však třeba adekvátně snížit dávku radionuklidu [72].
Chirurgická synovektomie
- Provádí se při selhání a/nebo nedostupnosti synoviortézy radiační.
- Substituce FVIII/FIX je jako pro operační zákrok (tab. 1).
- Důraz musí být kladen na řádnou rehabilitaci současně s profylaktickou aplikací FVIII/FIX jako prevence ztuhnutí kloubu, ke kterému je po tomto typu zákroku tendence.
Krvácení do svalů
- Cílová hladina FVIII/FIX při substituci je obdobná jako při krvácení do kloubů, většinou je však třeba delší doba její aplikace (minimálně 2–3 dny).
- Při menším rozsahu krvácení je cílová hladina FVIII 40–60 % a FIX 30–50 %, při rozsáhlých hematomech je nutno na úvod dosáhnout hladiny FVIII 80–100 % a FIX 60–80 %.
- Toto platí zejména při krvácení do musculus iliopsoas, kdy je doporučováno vysokou hladinu faktoru (60–100 %) udržovat 1–2 dny a následně minimálně dalších 5 dnů držet hladinu FVIII/FIX nad 40–60 % a v průběhu druhého týdne substituci postupně snižovat. Pacienta je nutno vždy hospitalizovat a imobilizovat.
- Při závažném krvácení s útlakem okolních struktur může edém svalu zmírnit krátkodobá aplikace kortikoidů (100 mg hydrocortisonu i.v.).
- Součástí terapie je i imobilizace postižené končetiny, v případě krvácení do m. iliopsoas klid na lůžku do ústupu bolesti, a dle dostupnosti i chlazení místa postiženého krvácením.
- Po krvácení do m. iliopsoas i po rozsáhlých hematomech na končetinách je vhodné přejít na několikatýdenní profylaktickou aplikaci koncentrátu FVIII/FIX, případně zintenzivnit dosavadní profylaxi chronickou
- Po odeznění příznaků provázejících krvácení je vhodná následná rehabilitace, většinou za současné profylaktické aplikace faktoru [3,73].
Hematurie
- Pokud není hematurie masivní a není provázena bolestí, je možno prvních 48 h léčit pouze klidem na lůžku a zvýšenou hydratací.
- Při bolesti a/nebo přetrvávající a/nebo masivní hematurii je nutná substituce faktoru FVIII > 50 % a FIX > 40 % po dobu 3–5 dnů.
- Při přetrvávající a/nebo recidivující hematurii může mít efekt podání prednisonu 0,5–1 mg/kg na 3–5 dnů [65]. Takovou léčbu lze pak naráz ukončit (bez postupného vysazování steroidů).
- Hematurie z proximální části močových cest je kontraindikací antifibrinolytik.
- Při přetrvávající a/nebo recidivující hematurii se doporučuje provést urologické došetření, resp. při každé hematurii je vhodné provést alespoň ultrazvukové vyšetření ledvin a močových cest a močový sediment (vyloučení litiázy a uroinfekce).
Epistaxe
- Před substitucí faktoru zkusit mírný tlak na nosní křídlo po dobu 10–20 min za současného ochlazování.
- Použít antifibrinolytika, obvykle tranexamová kyselina v dávce 15–25 mg/kg 3× denně.
- Je-li překrvení sliznice v rámci alergie, použít antihistaminikum.
- Při alergii i infekci dýchacích cest lze užít i lokální kapky s vazokonstrikčním účinkem.
- Při selhání výše doporučených postupů substituovat koagulační faktor > 30–40 % do zástavy krvácení.
- V případě nutnosti provést tamponádu za současné substituce faktoru a podávání antifibrinolytika, zejména při detamponádě (tampon je vhodné namočit do roztoku antifibrinolytika), po které výše uvedenou hladinu faktoru udržet alespoň 12–24 h a antifibrinolytikum podávat ještě několik (7–10) dnů.
Krvácení z dutiny ústní
- Mírné krvácení je často možno zvládnout jen pomocí antifibrinolytika formou opatrného výplachu 10% roztokem tranexamové kyseliny za následného spolknutí, do dávky 75–100 mg/kg/den.
- Není-li krvácení tímto způsobem zastaveno, je třeba substituovat faktor > 30–40 % do zástavy krvácení.
- V podávání antifibrinolytika celkově p. o. pokračovat ještě několik (7–10) dnů po zástavě krvácení.
- Dle lokalizace krvácení provést stomatologické vyšetření a zvážit možnost lokální aplikace fibrinového lepidla.
- Podávat studenou a měkkou stravu.
Poranění a/nebo krvácení do oka
- Nejdříve podat faktor a pak provést vyšetření oftalmologem.
- Faktor iniciálně substituovat na hladinu jako u závažného krvácení (FVIII na 80–100 % a FIX na 60–80 %) a následně udržovat > 40–50 %.
- Další terapie ve spolupráci s oftalmologem.
- Délka substituce koagulačního faktoru je individuální, u závažného krvácení lze doporučit substituci obdobnou jako při krvácení do CNS.
Intrakraniální (intraspinální) krvácení
- Při podezření nejprve substituovat faktor (FVIII > 80 %, FIX > 60 %) a teprve potom došetřovat.
- První týden substituovat FVIII na 80–100 %, FIX na 60–80 %, další 2 týdny FVIII > 50 % a FIX > 30 % a následně přejít na profylaktickou aplikaci na minimálně 3–6 měsíců.
Krvácení do měkkých tkání s rizikem útlaku dýchacích cest (krvácení retrofaryngeální, v oblasti krku, průdušnice, rozsáhlé krvácení do jazyka)
- První týden substituovat FVIII na 80–100 %, FIX na 60–80 %, druhý týden FVIII > 50 % a FIX > 30 %.
- Při těžké akutní tonzilitidě profylakticky substituovat i koagulační faktor.
Gastrointestinální krvácení
- Substituce FVIII na 80–100 % a FIX na 60–80 % 6 dnů a do 10.–14. dne držet hladinu FVIII > 50 % a FIX > 30 %.
- Vhodné je současně podávat antifibrinolytikum (tranexamová kyselina v dávce 15–25 mg/kg à 8 h).
- Současně provést vyšetření k objasnění zdroje krvácení.
- Obdobná substituce (jako u život ohrožujícího krvácení) je i při krvácení do dutiny břišní, do parenchymatózních orgánů, do stěny střeva.
Podkožní krvácení
- Menší podkožní hematomy nevyžadují substituci koagulačního faktoru a většinou je postačující mírný lokální tlak a chlazení.
- Ke zvážení je podat antifibrinolytikum.
- V případě masivního krvácení je však nutná substituční terapie a při rozsáhlém krvácení či při hrozbě kompartment syndromu může být nutná substituce jako u život ohrožujícího krvácení, tedy iniciálně FVIII > 80 % a FIX > 60 % a následně nad 30–50 %.
Tržné rány a eroze
- Povrchové eroze netřeba léčit substitucí koagulačního faktoru.
- Ke zvážení je podání antifibrinolytika.
- Hluboké tržné rány je třeba léčit substitucí FVIII > 50 % a FIX > 40 % po dobu 5–7 dnů; tam, kde to stav vyžaduje, je třeba spolupráce s chirurgem.
Zlomeniny
- Prvních 3–5 dnů substituovat FVIII > 50 % a FIX > 50 % a do stabilizace fraktury do 10.–14. dne udržovat hladinu koagulačního faktoru nad 20–50 %.
- Intenzivnější substituce je třeba při frakturách s dislokací, kdy může být nutná iniciální substituce jako při krvácení s ohrožením končetiny (FVIII 80–100 % a FIX 60–80 %) první týden a druhý týden udržovat hladinu FVIII > 50 % a FIX > 30 %.
CHIRURGICKÉ A ORTOPEDICKÉ VÝKONY
– viz samostatný doporučený postup
PROFYLAXE
Profylaxe primární či sekundární je indikována u všech těžkých forem (případně i středně těžkých forem s častými krvácivými projevy) hemofilie, aby se předešlo nevratnému poškození kloubů, které jsou v dětství více náchylné ke krvácení než v dospělosti. Profylaxe rovněž předchází život ohrožujícím krvácivým epizodám, vč. CNS krvácení. Cílem profylaxe je udržet hladinu FVIII/FIX > 1 %, lépe > 3 % [3,47,74,75].
Ze stávajících cílových minimálních hladin (trough level) 1–3 % vychází dnes doporučované dávky pro profylaxi SHL: 25–40 IU/kg 2–3× týdně až obden u hemofilie A a 2× týdně až každý třetí den 25–60 IU FIX/kg u hemofilie B [3]. Individuálně však dávka faktoru může být nižší a naopak i vyšší, dle dosahovaných hladin faktoru a klinického efektu. V ČR je v posledních letech nejčastěji používán tzv. režim Bremen/Munich, který má za cíl nejen předejít vzniku postižení pohybového aparátu, ale i předejít vzniku inhibitoru u dětí s hemofilií A. Profylaxe je zahájena ideálně mimo krvácení, nejčastěji kolem 12.–18. měsíce života a/nebo po prvním krvácení dávkou 25–35 IU/kg 1× týdně (nejčastěji paušální dávka 250 IU FVIII) a při prvním kloubním a/nebo opakovaných měkkotkáňových krváceních se zvyšuje frekvence aplikace FVIII. Maximální dávka, kterou lze v takovém režimu podat, je 50 IU/kg, doporučováno je však spíše zmíněných 25–35 IU/kg/ na dávku. Je žádoucí vyhnout se tzv. „peak treatment“ (tj. 50 a více IU/kg podávaných po dobu 5 a více za sebou následujících dní, resp. ED [35]. Podle některých studií tato léčba vede k signifikantnímu snížení rizika vzniku inhibitoru u PUPs [76]. Studie EPIC toto sice nepotvrdila, ale skutečných PUPs v ní bylo pouze 11 s rozvojem inhibitoru u tří pacientů, tedy počty malé na to, aby bylo možné je statisticky zhodnotit [77]. Právě tento způsob profylaxe je v současné době doporučeným režimem pro nově diagnostikované děti (PUPs) s těžkým fenotypem hemofilie A v České republice (doporučení PSDH a ČNHP). EHL koncentráty umožní při profylaxi aplikovat EHL-rFVIII v intervalech 3–5 dnů a EHL-rFIX 1× za 1–2 týdny a/nebo dosahovat trvale vyšších bazálních hladin chybějících faktorů. Profylaxe u dětí (vč. PUPs) může být vedena i emicizumabem. Data o takové léčbě jsou však zatím sporadická, a proto ji nelze v době publikace tohoto textu považovat za standarní doporučení.
Profylaxe všeobecně, a pro EHL koncentráty obvzvláště, by měla být dávkována s využitím znalosti farmakokinetických parametrů. Znalost IVR a nejnižší hladiny před aplikací další profylaktické dávky (trough level) je nezbytným minimem, které však především u dětských pacientů nemusí být dostačující. Hladina FVIII > 3 % eliminuje velkou část spontánních krvácení. Pacienti při hladině FVIII > 10–12 % mají minimum krvácivých epizod a při hladině FVIII > 15 % pak spontánně nekrvácí prakticky vůbec [23]. Farmakokinetické parametry vykazují velké interindividuální rozdíly i při použití stejného léčiva. Jejich stanovení (at již formou individuální, nebo tzv. „populační“ farmakokinetiky) poskytuje cenné údaje pro správné vedení léčby jak formou profylaxe, tak při léčbě krvácivých epizod či při zajištění chirurgických výkonů, a proto je doporučeno [23,43,46,78]. Na základě doporučení EDQM z roku 2019 je v rámci EU doporučeno při profylaxi EHL preparáty cílit na minimální hladinu 3% FVIII/FIX.
U převážné části pacientů, zejména s vyšší frekvencí krvácivých příhod, je vhodné pokračovat v profylaxi i v dospělém věku [79,80]. Většina adolescentů, nyní na primární či sekundární profylaxi, pokračuje v nějaké formě i v dospělosti za účelem celoživotní profylaxe. Je prokázáno, že i terciární profylaxe zavedená až při rozvinuté artropatii je pro dospělé pacienty přínosná výrazným poklesem nejen frekvence krvácení (studie SPINART) [81], ale i nižším počtem cílových kloubů a lepším ortopedickým i Petterssonovým skóre (studie POTTER) [82]. U dospělých pacientů léčených on demand je zavedení terciární profylaxe vhodné na základě individuálního posouzení, zejména pokud profylaxe přinese zvýšení kvality života pacienta. Prakticky nutná je terciární profylaxe u pacientů s cílovými klouby (pokud je nelze řešit jiným způsobem – např. radiační synoviortézou) a při život ohrožujícím a/nebo častém krvácení i bez rozvoje cílového kloubu – cca 2× a vícekrát měsíčně. Na rozdíl od dřívejších doporučení zmiňujících, že k dosažení klinického efektu (výraznému snížení frekvence krvácení) u dospělých pacientů mnohdy stačí i nižší dávkování koagulačního faktoru, než je běžně doporučované (25–40 IU/kg, v praxi většinou cca 15–30 IU/kg 3× týdně [83,84]), je nyní patrná snaha u pacientů s těžkou artropatií a s cílovými klouby udržovat hladinu FVIII/FIX i vyšší – ≥ 5 % (netřeba u pacientů bez krvácivých epizod) a u mladých pacientů s rizikovými fyzickými aktivitami v době jejich provozování ≥ 15 % [85].
Jak je uvedeno výše, k profylaxi lze u těžké formy hemofilie A použít i emicizumab, jehož výhodou je podkožní aplikace a dosažení hemostatického efektu srovnatelného s hladinou FVIII: C nad 10 %. Emicizumab se tedy jeví vhodným pro profylaxi i u pacientů se špatným žilním přístupem a u těch, kde je potřeba dosažení vyšších „trough“ hladin FVIII. Otázka profylaxe emicizumabem u PUPs je zmíněna výše. Mimo jiné by taková léčba eliminovala nutnost zavádění centrálního venózního přístupu (CVAD), kterým se někdy u PUPs nelze vyhnout.
DOMÁCÍ LÉČBA
Vždy, když je to možné, je koncentráty faktorů vhodné podávat formou tzv. domácí léčby, při které aplikaci provádí pacient sám nebo jeho rodina, případně praktický lékař či zdravotní sestra. Tento postup zaručí co nejmenší časové prodlení při léčbě krvácení a umožní profylaxi bez nutnosti docházet/dojíždět k aplikaci do zdravotnického zařízení. Domácí léčba je legislativně umožněna metodickým pokynem ministra zdravotnictví z roku 1992 [86]. Centra vydávající hemofilikům koncentráty koagulačních faktorů pro domácí léčbu musí nejprve pacienty seznámit s technikou aplikace koncentrátů a jejich skladováním a náležitě je poučit o způsobu léčby krvácivých epizod a možných rizicích této léčby, což musí být zaznamenáno ve zdravotnické dokumentaci a stvrzeno podpisem (doporučeno formou standardizovaného protokolu shrnujícího hlavní zásady domácí léčby) pacienta či jiné oprávněné osoby – zákonného zástupce (většinou rodičů). O realizaci domácí léčby je rovněž veden protokol a/nebo deník, do kterého je zaznamenáváno vydávání koncentrátů zdravotnickým zařízením a jejich aplikace pacientem. Formou domácí léčby lze podávat i emicizumab.
PODPŮRNÁ LÉČBA
Antifibrinolytika používáme především při krvácení z dutiny ústní au zubních extrakcí, kdy je doporučováno je podávat po dobu 7–10 dnů. V literatuře je zmiňována především tranexamová kyselina, doporučované dávkování je p. o. 25 mg/kg à 8 h nebo 15–20 mg/kg à 6 h nebo i.v. 10 mg/kg à 8 h [3,22,26,65,87]. Vhodná jsou i při epistaxi a podkožním krvácení. Kontraindikována je při hematurii z horní etáže močových cest (nevhodná je též při krvácení do kloubů) a při současné aplikaci aPCC (výrobce doporučuje minimálně 6hodinový odstup, vhodnější je však spíše delší interval mezi aplikací aPCC a antifibrinolytika). Důvodem je riziko rozvoje diseminované intravaskulární koagulace a trombózy.
DALŠÍ POSTUPY
Obecně jsou kontraindikovány nitrosvalové injekce, kdy hrozí obtížně stavitelné krvácení. Při podkožní aplikaci stačí komprese. Očkování je proto doporučováno místo i. m. provádět s.c. Tam, kde to není možné (vakcíny obsahující tetanus), je třeba i. m. injekci aplikovat šetrně, tenkou jehlou, místo vpichu komprimovat, případně i chladit. V současné době není při vakcinaci doporučována prevence krvácení pomocí aplikace faktorů krevního srážení. Podávání salicylátů, stejně jako jiných NSAID, je v době krvácení kontraindikováno. Při nutnosti jejich použití jsou preferovány selektivní COX-2 inhibitory.
Hemofilii lze vyléčit i transplantací jater, která se u hemofiliků provádí z důvodu terminálního stadia hepatopatie, nejčastěji v důsledku chronické hepatitidy C. Samotná hemofilie však pro rizika spojená s transplantací není její indikací.
Léčba virové hepatitidy C a B i HIV je realizována infektologem v rámci HTC/HCCC. Pokrokem je nyní i možnost léčby chronické hepatitidy C bezinterferonovým režimem novými antivirotiky s vysokou pravděpodobností dosažení setrvalé virologické odpovědi [88]. Sledování markerů virových hepatitid a HIV realizují rovněž pracoviště typu HTC/HCCC. Biopsie jater se pro riziko krvácení a nutnost náročné substituční léčby u pacientů s hemofilií standardně neprovádí.
Doporučení pro léčbu arteriální a žilní trombózy
Pacienti s hemofilií mají obdobné riziko aterosklerózy jako ostatní populace, riziko trombózy je pravděpodobně nižší, avšak tepenná i žilní trombóza u těchto pacientů může nastat. Neexistují zatím jednoznačná doporučení, touto otázkou se zabývala ADVANCE Working Group [89,90]. Dosavadní názory z literatury lze shrnout následovně:
Trombolýza
- Udržovat hladinu FVIII/FIX nad 80 %, ideálně 80–100 % během trombolýzy a následných 24–48 h [91,92].
Léčba terapeutickou dávkou (nízkomolekulárního) heparinu
- Úvodem dosáhnout „peak“ FVIII/FIX nad 80 % a následně pak „trough level“ nad 40–50 % [90].
Duální antiagregace
- Plazmatická hladina FVIII/FIX by neměla klesnout pod 25 %, individuálně lze zvažovat „trough level“ nad 15 % [89,90,93]. Preferován je clopidogrel pro nižší riziko krvácení oproti prasugrelu a ticagreloru [94]. V akutních případech po nezbytně krátkou dobu lze akceptovat hladinu FVIII/FIX ≥ 5 %, kdy však je již i zvýšené riziko krvácení [89].
Léčba acetylsalicylovou kyselinou
- Plazmatická hladina FVIII/FIX by neměla klesnout pod 5 %, individuálně lze zvažovat „trough level“ nad 1 % [89,93,95].
Koronární angiografie diagnostická
- K provedení výkonu je doporučena hladina FVIII/FIX nad 80 %, následně „trough level“ nad 50 % dalších 24 h [89,92].
Perkutánní koronární intervence (PCI)
- Upřednostnit přístup z a. radialis (lepší možnost komprese, prevence retroperitoneálního a tříselného krvácení vyžadujícího prolongovanou léčbu koncentráty faktorů).
- Původně bylo doporučováno použití „bare metal stentu“ (BMS) před „drug eluting stentem“ (DES) z důvodu kratšího zajištění duální antiagregační léčbou. V současnosti je doporučení upřednostnit DES druhé generace vyžadující jen měsíční duální antiagregaci [95].
- K provedení koronární intervence je nutná hladina FVIII/FIX nad 80 %, s udržováním této hladiny po dobu aplikace terapeutické dávky (nízkomolekulárního) heparinu – obvykle 48 h [96].
- Následně viz postup pro antikoagulační léčbu heparinem.
- Při duální antiagregační léčbě udržovat hladinu FVIII/FIX nad 25 % (15 %).
- Při antiagregační léčbě v monoterapii (obvykle acetylosalicylovou kyselinou – ASA) udržovat hladiny FVIII/FIX nad 1–5 %.
Léčba warfarinem
- Je možná při hladině FVIII/FIX nad 25 % [90], resp. dle novějšího doporučení je dostatečná hladina FVIII/FIX ≥ 20 % [95], při které lze použít nejen warfarin, ale i přímá antikoagulancia (DOAC), která mají výhodu u hemofilie B vzhledem k dependenci FIX na K vitamínu. Pro možnost zrušení efektu v současné době jen u inhibitoru anti-IIa je vhodné preferovat tento před přímými inhibitory anti-Xa.
Ke snaze o udržení dostatečné aktivity krevního srážení, nutné pro bezpečné podávání antiagregační či antikoagulační léčby, možná v budoucnu přispěje i emicizumab. Tato data však zatím nejsou k dispozici.
Prevence vzniku inhibitoru
Při hereditárním defektu a expozici alogennímu plazmatickému nebo rekombinantnímu FVIII/FIX u části hemofiliků dochází ke vzniku protilátek proti FVIII/FIX. Protilátka se váže na molekulu FVIII/FIX, a znemožňuje tak vykonávat jeho funkci v průběhu srážení krve, případně dochází ke zrychlení clearence komplexu faktor+inhibitor. Riziko vzniku inhibitoru je nejvyšší u těžké hemofilie A, incidence kolísá mezi 10–40 %, s prevalencí 12–13 % [97–99], u těžké hemofilie B je incidence inhibitoru kolem 3 % [97], u těžké formy 5–8 % [98,100,101]. Jen ojediněle vzniká inhibitor u středně těžké a lehké hemofilie B, zatímco při stejné tíži hemofilie A se objevuje u 3–13 % pacientů [102]. Celková prevalence inhibitoru u hemofilie A je 5–8 % [97,103]. Ke vzniku inhibitoru dochází většinou během prvních 50–75 dnů [14] podávání koncentrátu koagulačního faktoru, s mediánem mezi 10. a 16. ED [30,31,35,97,100,104], což bývá u těžkých hemofiliků již v předškolním věku. Zřídka dojde k jeho vývoji po sté aplikaci derivátu. V ČR je incidence inhibitoru u PUPs s těžkou hemofilií A v posledních 10 letech necelých 30 %. Nebyl pozorován rozdíl mezi PUPs léčenými pdFVIII a rFVIII, pouze trend k nižšímu výskytu u PUPs léčených rFVIII. Tento trend však nedosáhl statisticky významné hladiny. Všechny inhibitory vznikly v průběhu prvních 50 ED. Jeden inhibitor vznikl u PUPs se střední či lehkou hemofilií A [40]. V tab. 2 jsou uvedeny faktory mající vliv na vznik inhibitoru, jde o údaje platné pro inhibitor FVIII, který je mnohem častější a je o něm známo více informací než o inhibitoru FIX. V rámci regionu střední a východní Evropy se jako nejvyšší riziko jeví on-demand léčba a tzv. „peak-treatment“ v průběhu prvních 50 ED. Roli hrají i typ mutace a rodinná anamnéza (zatím nepublikovaná data).
Tab. 2. Faktory ovlivňující vznik inhibitoru (zejména) u dříve neléčených pacientů (PUPs) [14,29–42,44,45,76,77,100–111]. ![Faktory ovlivňující vznik inhibitoru (zejména) u dříve neléčených pacientů (PUPs)
[14,29–42,44,45,76,77,100–111].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/5fd8928ddbeaa6a120fb7ae4428f6185.png)
FVIII – faktor VIII, HLA – human leucocyte antigen, TNF α – tumor nekrotizující faktor alfa, VWF – von Willebrandův faktor, ED – expoziční den Z uvedeného vyplývají doporučení pro léčbu koncentráty FVIII, které lze převzít i pro FIX:
- Nově narozenému hemofilikovi doporučujeme aplikovat koncentráty FVIII/FIX pokud možno co nejpozději, ne dříve než mezi 6.–12. měsícem života (neprovokovat riziko krvácení následkem pádů batolete předčasnou vertikalizací a pokusy o chůzi, elektivní operace odložit minimálně po 6.–12. měsíci života).
- U těžkých hemofiliků doporučujeme zahájit profylaxi co nejdříve po první expozici koncentrátu koagulačního faktoru, ideálně do 5.–10. dne expozice (vzhledem k výše uvedenému mediánu vzniku inhibitoru u hemofilie A, u hemofilie B nejsou data). Žádoucí je vyhnout se podání dávky nad 50 IU/kg/den po dobu 5 a více po sobě jdoucích dnů.
- Ideální je s profylaxí začít v období mimo tzv. „nebezpečné signály“ stimulující imunitní odpověď jako vakcinace, infekce, probíhající akutní krvácení, operace.
- Doporučujeme proto u PUPs s těžkou hemofilií začít s profylaktickou aplikací koagulačního faktoru v dávce 25–35 IU/kg (250 IU) 1× týdně po opakovaném objevení prvních podkožních hematomů, které ještě nevyžadují substituci koncentrátem chybějícího faktoru, dříve než před ukončením druhého roku věku (podrobně viz doporučení v odstavci „Profylaxe“), optimálně po 12. měsíci věku.
- Obdobnou profylaxi a současně imunotoleranci je zřejmě vhodné aplikovat i u PUPs primárně léčených profylakticky emicizumabem, nicméně v tomto případě je pravděpodobně možné expocizi koncentrátu FVIII posunout mimo časný dětský věk. Pro toto tvrzení zatím však není dostatek dat.
- Nestřídat různé typy koncentrátů, není-li k tomu jednoznačný důvod.
- U jiné než těžké formy hemofilie perioperačně upřednostnit bolusovou aplikaci před kontinuální infuzí, zejména pokud je pacient nositelem mutace s vyšším rizikem pro vznik inhibitoru. Výhodné je použití DDAVP tam, kde je to možné a indikované (lehká hemofilie A s prokázaným vzestupem FVIII: C po jeho aplikaci).
- Nejsou důvody pro upřednostňování plazmatických koncentrátů před rekombinantními. Pro PUPs a MTPs jsou rekombinantní preparáty v ČR léčbou volby. Plazmatické koncentráty s obsahem VWF lze případně zvažovat během prvních 50 ED u pacientů s těžkou formou hemofilie A a s vysokým rizikem vzniku inhibitoru (rodinná anamnéza, typ mutace, způsob léčby při první expozici FVIII/FIX) [108].
- EHL FVIII/FIX s vazbou na Fc fragment imunoglobulinu nemají v SPC omezení pro použití u PUPs, ale v ČR je pro PUPs od 1. 11. 2020 hrazen prozatím pouze EHL FVIII s vazbou na Fc fragment imunoglobulinu. Data týkající se rizika rozvoje inhibitorů FVIII, vycházející z klinické studie s PUPs naznačují srovnatelný, ne-li nižší výskyt inhibitoru [48].
- Použití EHL FVIII/FIX může vést k prodloužení frekvence aplikací a snížení potřeby zavádění CVAD u malých dětí. Dávkovací režimy se pro EHL koncetráty FVIII pro profylaxi dle SPC pohybují kolem dávky 50 IU/kg à 3–5 dnů s možností individuální korekce dávky i intervalu aplikace dle dosažených hladin FVIII a krvácivých projevů (viz jejich SPC). Z EHL FIX je v současnosti v ČR registrován jen EHL s vazbou na fc fragment imunoglobulinu, u kterého je doporučení pro profylaxi 50 IU/kg 1× týdně s případnou úpravou dávky nebo 100 IU/kg à 10 dnů s případným prodloužením intervalu na dva týdny i delší.
Léčba pacientů s inhibitorem FVIII/FIX
– je obsažena v samostatném doporučeném postupu.
PROGNÓZA
Krvácivé projevy jsou celoživotní, většinou se objevují s počátkem chůze v batolecím věku. V období růstu mohou být častější než v dospělém věku. Tíže postižení závisí na tíži onemocnění, včasnosti a dostatečném dávkování koncentrátů chybějících koagulačních faktorů při léčbě každého krvácení a na správně vedené profylaxi. Opakovaná krvácení do kloubů mají za následek artropatii, která může vyústit až v ankylózu kloubu či nutnost implantace kloubní protézy.
AKTUÁLNÍ MOŽNOST PREVENCE
Jedinou současnou možností prevence hemofilie je prenatální diagnostika s následným ukončením gravidity v případě mužského plodu postiženého hemofilií nebo preimplantační diagnostika se selekcí embryí negativních na kauzální mutaci v genu FVIII/FIX [1]. Toto je možno zvážit zejména u těžké formy hemofilie, případně i u středně těžkých forem. Definitivní rozhodnutí o ukončení gravidity je však vždy rozhodnutím rodičů a neexistuje medicínský důvod na něm trvat či jej jednoznačně doporučovat. Oba nastávající rodiče by ale měli být důkladně informováni o všem, co souvisí s péčí o dítě s hemofilií. V užším slova smyslu lze pod pojmem prevence chápat prevenci artropatie a život ohrožujícího krvácení pomocí primární, sekundární, či terciární profylaxe koncentrátem faktoru FVIII/FIX či nesubstituční léčbou.
POSUDKOVÁ HLEDISKA
Choroba je dědičná a nevyléčitelná, tedy lze v průběhu života očekávat horšení postižení – především stavu pohybového aparátu, což bývá hlavní faktor pro přiznání pracovní neschopnosti a/nebo invalidního důchodu. Posouzení je přísně individuální. Z odborné stránky je žádoucí přiznání alespoň částečného invalidního důchodu ještě před invalidizací pacienta (a mnohdy i ztrátou soběstačnosti) následkem progrese kloubního poškození, jež lze zpomalit (nikoli zcela zastavit) včasným přizpůsobením pracovní zátěže.
ETICKÁ HLEDISKA
Onemocnění není vyléčitelné, je však léčitelné a cílem by mělo být dosažení co nejlepší kvality života po stránce fyzické i psychosociální, tedy vytvoření takových podmínek, aby pacienti s hemofilií nebyli ve společnosti hendikepováni a mohli žít normální osobní i společenský život.
PERSONÁLNÍ A TECHNICKÉ PŘEDPOKLADY
Péče o nemocné v České republice je vedena v síti center definovaných požadavky WFH [3] a Evropskými doporučeními [21]. Tato síť je tvořena centry komplexní hemofilické péče (HCCC) v rámci MZd ČR akreditovaných center vysoce specializované hematologické péče (CVSHP) a centry pro léčbu hemofilie (HTC) akreditovaných na principu čtyř kompetencí: kvalifikace, vybavení, sebehodnocení a komunikace. Periodicky probíhají opakované audity jednotlivých center v rámci ČNHP. Většina HCCC a některá HTC získaly navíc status evropského centra – EHCC a EHTC (certifikaci uděluje EUHANET [112]). S centry spolupracují pracoviště sdílené péče (spádová hematologická oddělení) dle vzájemné domluvy a potřeb zajištění péče o hemofiliky v daném spádu a v dané době. Pracoviště sdílené péče mají právo sama si vybrat jedno či více HTC/HCCC ke spolupráci. Vždy je nutné potvrzení diagnózy a pravidelná dispenzarizace v centru typu HCCC/HTC. Genetická vyšetření jsou pak v kompetenci center HCCC.
Terapii (substituci koncentráty koagulačních faktorů) lze v základní míře poskytovat regionálním/spádovým hematologickým pracovištěm, avšak pod dohledem a dle doporučení center typu HCCC/HTC, která tuto léčbu řídí a kde se realizují veškeré operační výkony a veškerá léčba pacientů s inhibitorem a/nebo léčba klinicky závažných krvácivých epizod a léčba emicizumabem. Centra HCCC/HTC jsou odpovědná i za péči poskytovanou regionálními pracovišti, která tuto péči nemohou poskytovat samostatně, ale jen za metodického vedení pracoviště HCCC/HTC.
Požadavky na centra a služby jimi poskytované vychází z deklarace ČNHP, kde jsou stratifikovány pro centra typu HCCC, HTC a pracoviště sdílené péče [19].
Stratifikace center
1. Hemofilici s inhibitorem
- k elektivním chirurgickým (vč. ortopedických) výkonům (HCCC);
- k imunotoleranční léčbě – HCCC;
- k profylaktické léčbě zahrnující i emicizumaba event. domácí léčbě – HCCC;
- k akutní péči – HCCC/HTC;
- k běžné péči – HCCC/HTC.
2. Hemofilici bez inhibitoru – těžcí a středně těžcí
- k elektivním ortopedickým výkonům (vč. synovektomie chirurgické i radiační) – HCCC. Radiační synoviortéza může být provedena i v HTC, je-li dostupné patřičné odborné a technické zázemí;
- k elektivním chirurgickým výkonům – HCCC/HTC;
- k akutním výkonům – HCCC/HTC;
- k profylaktické léčbě vč. emicizumabu – HCCC/HTC;
- k domácí péči – HCCC/HTC;
- k běžné péči – HCCC/HTC + spádová (regionální) pracoviště.
3. Hemofilici – lehcí, případně střední bez nutnosti (pravidelné) léčby
- dispenzarizováni v HCCC/HTC.
Stratifikace péče v České republice
- HCCC Praha – ÚHKT (dospělí) + FN Motol (děti) – spádová oblast Praha a střední Čechy, Vysočina; ve vybraných případech Čechy
- HCCC Brno (FN Brno Bohunice – dospělí, FN Brno Dětská nemocnice – děti) – spádová oblast jižní Morava, Zlínský kraj a část kraje Vysočina; ve vybraných případech Morava
- HCCC FN Ostrava (děti i dospělí) – spádová oblast severní Morava a Slezsko, ve vybraných případech Morava
- HTC FN Olomouc (děti i dospělí) – spádová oblast střední Morava
- HTC FN Hradec Králové (děti i dospělí) – spádová oblast východní Čechy
- HTC Krajská nemocnice Liberec (dospělí) – spádová oblast Liberecký kraj
- HTC Masarykova nemocnice Ústí n.L. (děti i dospělí) – spádová oblast Ústecký kraj
- HTC FN Plzeň (děti i dospělí) – Plzeňský kraj a Karlovarský kraj
- HTC Nemocnice České Budějovice (děti i dospělí) – Jihočeský kraj
POUŽITÉ POJMY A ZKRATKY
aPCC – aktivovaný koncentrát protrombinového komplexu
aPTT – aktivovaný parciální tromboplastinový test
ASA – acetylosalicylová kyselina (acetylsalicylic acid)
BMS – kovový stent (bare metal stent)
BU – Bethesda jednotka
CNS – centrální nervový systém
COX-2 – cyklooxygenáza 2
CVAD – centrální venózní přístup (central venous access devices)
CVSHP – Centrum vysoce specializované hematologické péče
ČNHP – Český národní hemofilický program
ČSH – Český svaz hemofiliků
DDAVP – 1-deamino-8-D-arginin vasopressin
DES – lékový stent (drug eluting stent)
DL – domácí léčba
DOAC – přímá orální antikoagulancia (direct oral anticoagulant)
ED – expoziční dny
EDQM – Evropský direktorát pro kvalitu zdravotní péče (European Directorate for the Quality of Medicine & HealthCare)
EHL – prodloužený poločas (extended half-life)
EMA – Evropská lékařská agentura (European Medicines Agency)
FDA – Úřad pro kontrolu potravin a léčiv v USA (U.S. Food ans Drug Administration)
FVII: C – koagulační aktivita FVII
FVIII – koagulační faktor VIII
FVIII: C – koagulační aktivita FVIII
FIX – koagulační faktor IX
FIX: C – koagulační aktivita FIX
HCCC – centrum komplexní péče pro hemofilii (hemophilia comprehensive care centre)
HJHS – hemofilické skóre kloubního zdraví (Haemophilia Joint Health Score)
HIV – virus lidské imunitní nedostatečnosti (human immunodeficiency virus)
HLA – lidský leukocytární antigen (human leucocyte antigen)
HTC – centrum pro léčbu hemofilie (hemophilia treatment centre)
i. m. – intramuskulárně
IU – mezinárodní jednotka (international unit)
i.v. – intravenózně
IVR – poměr mezi očekávaným a reálným vzestupem léčebně podaného faktoru (in vivo recovery)
MTP – minimálně léčený pacient (minimally treated patient)
MZd – Ministerstvo zdravotnictví
NSAID – nesteroidní antirevmatika (non-steroidal anti-inflammatory drug)
PCI – perkutánní koronární intervence
pd – plazmatický (plasma derived)
p. o. – per os
PSDH – pracovní skupina pro dětskou hematologii
PT – protrombinový test
PTP – dříve léčený pacient (previously treated patient)
PUP – dříve neléčený pacient (previously untreated patient)
r – rekombinantní
rFVIIa – rekombinantní aktivovaný faktor VII
s.c. – subkutánně
SHL – standardní poločas (standard half-life)
SPC – souhrn údajů o přípravku (summary of product characteristics)
t1/2 – plazmatický poločas
TFPI – inhibitor zevní koagulační cesty (tissue factor pathway inhibitor)
TNFa – tumor nekrotizující faktor alfa
ÚHKT – Ústav hematologie a krevní transfuze
VWF – von Willebrandův faktor
VWF: Ag – von Willebrandův faktor antigen
VWCH – von Willebrandova choroba
VWF: RCo – von Willebrandův faktor ristocetin kofaktor
WFH – Světová federace hemofilie (World Federation of Hemophilia)
WHO – Světová zdravotnická organizace (World Health Organization)
PODÍL AUTORŮ NA PŘÍPRAVĚ DOPORUČENÍ
Smejkal P – příprava rukopisu, Blatný J, Zápotocká E, kritická revize, doplnění, úpravy rukopisu a schválení konečné verze, Hajšmanová Z, Hluší A, Hrdličková R, Penka M, kritická revize a schválení konečné verze rukopisu. Výsledný rukopis pak prošel revizí a souhlasem zástupců všech center sdružených v Koordinační radě ČNHP (Český národní hemofilický program [19]).
PROHLÁŠENÍ O KONFLIKTU ZÁJMŮ
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Doručeno do redakce dne 1. 12. 2020.
MUDr. Petr Smejkal, Ph.D.
Oddělení klinické hematologie,
Fakultní nemocnice Brno
Jihlavská 20,
Brno, 625 00
e-mail: smejkal.petr@fnbrno.cz
Zdroje
1. Srivastava A, Brewer AK, Mauser-Bunschoten EP, et al. Guidelines for the management of hemophilia. Haemophilia. 2013; 19: e1–e47.
2. Annual Global Survey. 2018. World Federation of Hemophilia, October. 2019. http: //www1.wfh.org/publications/files/pdf-1731.pdf, přístup 27. 9. 2020.
3. Srivasta A, Santagostino E, Dougall A, et al. WFH Guidelines for the Management of Hemophilia 3rd edition. https: //onlinelibrary.wiley.com/doi/abs/10.1111/hae.14046, přístup 27. 9. 2020.
4. White GC, Rozendal F, Aledort L, et al. Definitions in hemophilia. Tromb Haemost. 2001; 85 : 560.
5. Maclean RM, Makris M. Hemophilia A and B. In: O’Shaughnessy D, Makris M, Lillicarp D. Practical Hemostasis and Thrombosis. 1st ed. Oxford, Blackwell Publishing. 2005 : 41–50.
6. Kemball-Cook G, Gomez K. Molecular basis of hemophilia A. In: Lee CA, Berntorp E, Hoots WK. Textbook of Hemophilia. 2nd ed. Oxford: Blackwell Publishing. 2010 : 24–32.
7. Gomez K. Hemophilia B – molecular basis. In: Lee CA, Berntorp E, Hoots WK. Textbook of Hemophilia. 2nd ed. Oxford, Blackwell Publishing. 2010 : 88-93.
8. Novotný J, Penka M, Matýšková M, Zavřelová J. Fyziologie krevního srážení. In: Penka M, Tesařová E et al. Hematologie a transfuzní lékařství I, 1. vyd. Praha: Grada Publishing. 2011 : 31–59.
9. Forbes CD, Aledort L, Madhok R. Hemophilia. London, Chapman & Hall. 1997.
10. Raffini L, Manno C. Modern management of haemophilic arthropathy. Br J Haematol. 2007; 136 : 777–787.
11. Kulkarni R, Lusher J. Perinatal management of newborns with haemophilia. Br J Haematol. 2001; 112 : 264–274.
12. Gray GR, Teasdale JM, Thomas JW. Hemophilia Bm. Canad Med Ass J 1968; 98 : 552–554.
13. Verbruggen B, Novakova I, Wessels H, et al. The Nijmegen modification of the Bethesda assay for factor VIII: C inhibitor. Improved specifity and reliability. Thromb Haemost 1995; 73 : 247–251.
14. Van den Berg, Fischer K, Carcao M, et al. Timing of inhibitor development in more than 1000 previously untreated patiens with severe hemophilia A. Blood. 2019; 134 : 317–320.
15. Gringeri A, Mannucci PM. Italian guidelines for the diagnosis and treatment of patiens with haemophilia and inhibitors. Haemophilia. 2005; 11 : 611–619.
16. Collins PW, Chlamers E, Hart DP, et al. Diagnosis and treatment of factor VIII and IX inhibitors in congenital haemophilia. 4th ed. Br J Haematol. 2013; 160 : 153–170.
17. Bátorová A, Jankovičová D, Žarnovičanová M, et al. Národné štandardné postupy pre liečbu hemofilie a iných vrodených koagulopatií v Slovenskej republike. Lek Obz. 2008; 56 : 330–340.
18. De Moerloose P, Fischer K, Lambert T, et al. Recommendations for assessment, monitoring and follow-up of patiens with haemophilia. Haemophilia. 2012; 18 : 319–325.
19. Český národní hemofilický program. http: //cnhp.registry.cz.
20. Věstník Ministerstva zdravotnictví České republiky. 2014, částka 3.
21. Colvin BT, Astermark J, Fischer K, et al. European principles of haemophilia care. Haemophilia. 2008; 14 : 361–374.
22. Armstrong E, Astermark J, Baghaei F, et al. Nordic Hemophilia Guidelines. Version 1. Printed 23 June. 2015. http: //www.nordhemophilia.org.
23. Den Uijl IE, Mauser-Bunschoten EP, Roosendaal G, et al. Clinical severity of haemophilia A: does the classification of the 1950s still stand? Haemophilia. 2011; 17 (6): 849–853.
24. United Kingdom Haemophilia Centre Doctors’ Organisation (UKHCDO). Guidelines on the selection and use of therapeutic products to treat haemophilia and other hereditary bleedings disorders. Haemophilia. 2003; 9 : 1–23.
25. Santagostino E, Mannucci PM, Bonomi Bianchi A. Guidelines on replacement therapy for haemophilia and inherited coagulation disorders in Italy. Haemophilia. 2000; 6 : 1–10.
26. Pabinger I, Heistinger M, Muntean W, et al. Hämophiliebehandlung in Österreich. Wien Klin Wochenschr. 2015; 127 (Suppl 3): 115–130.
27. Věstník Ministerstva zdravotnictví České republiky. 2016, částka 7.
28. Salaj P, Smejkal P, Komrska V, Blatný J, Penka M. Standardy péče o nemocné s hemofilií. Transfuze Hematol dnes. 2013; 13 : 96–98.
29. Astermark J, Altisent C, Batorova A, et al. Non-genetic risk factors and the development of inhibitors in haemophilia: a comprehensive review and consensus report. Haemophilia. 2010; 16 : 747–766.
30. Calvez T, Chambost H, Claeyssens-Donadel S, et al. Recombinant factor VIII products and inhibitor development in previously untreated boys with severe hemophilia A. Blood. 2014; 124 (23): 3398–3408.
31. Fischer K, Lassila R, Peyvandi F, et al. Inhibitor development in haemophilia according to concentrate. Four-year results from the European Haemophila Safety Surveilance (EUHASS) project. Thromb Haemost. 2015; 113 : 968–975.
32. Goudemand J, Rothschild C, Demiguel V, et al. Influence of the type of factor VIII concentrate on the incidence of factor VIII inhibitors in previously untreated patients with severe hemophila A. Blood. 2006; 107 : 46–51.
33. Goudemand J, Peyvandi F, Lacroix-Desmazes S. Key insights to understand the immunogenicity of FVIII products. Thromb Haemost. 2016; 116 (Suppl.1): 52–59.
34. Gouw SC, van der Bom JG, Auerswald G, et al. Recombinant versus plasma-derived factor VIII products and the development of inhibitors in previously untreated patients with severe hemophilia A: the CANAL cohort study. Blood. 2007; 109 : 4693–4697.
35. Gouw SC, van der Bom JG, van den Berg HM. Treatment-related risk factors of inhibitor development in previously untreated patiens with hemophilia A: the CANAL cohort study. Blood. 2007; 109 : 4648–4654.
36. Iorio A, Halimeh S, Holzhauer S, et al. Rate of inhibitor development in previously untreated hemophila A patiens treated with plasma-derived or recombinant factor VIII concentrates: a systematic review. J Thromb Haemost. 2010; 8 : 1256–1265.
37. Peerlinck K, Hermans C. Epidemiology of inhibitor formation with recombinant factor VIII replacement therapy. Haemophilia. 2006; 12 : 579–590.
38. Xi M, Makris M, Marcuci M, et al. Inhibitor dvelopment in previously treated hemophilia A patients: a systematic review, meta-analysis, and meta-regression. J Thromb Haemost. 2013; 11 : 1655–1662.
39. Peyvandi F, Mannucci PM, Garagiola I, et al. A randomized trial od factor VIII and neutralizing antibodies in hemophilia A. N Engl J Med. 2016; 374 : 2054–2064.
40. Blatny J, Komrska V, Blazek B, et al. Inhibitors incidence rate in Czech previously untreated patients with haemophilia A has not increased since introduction of recombinant factor VIII treatment in. 2003. Blood Coagul Fibrinolysis. 2015; 26 : 673–678.
41. Hay CRM, Palmer BP, Chalmers EA, et al. The incidence of factor VIII inhibitors in severe haemophilia A following a major switch from full-length to B-domain-deleted factor VIII: a prospective cohort comparison. Haemophilia. 2015; 21 : 219–226.
42. Giangrande P, Seitz R, Behr-Gross ME, et al. Kreuth III: European consensus proposal for treatment of haemophilia with coagulation factor concentrates. Haemophilia. 2014; 20 : 322–325.
43. Collins PW, Fischer K, Morfini M, Blanchette VS, Björkman S. Implications of coagulation factor VIII and IX pharmacokinetics in the prophylactic treatment of haemophilia. Haemophilia. 2011; 17 : 2–10.
44. Batorova A, Holme P, Gringeri A, et al. Continuous infusion in haemophilia: current practice in Europe. Haemophilia. 2012; 18 : 753–759.
45. Eckhardt EL, van Velzen AS, Peters M, et al. Factor VIII gene (F8) mutation risk of inhibitor development in nonsevere hemophilia A. Blood. 2013; 122 (11): 1954-1962.
46. Collins P, Chalmers E, Chowdary P, et al. The use of enhanced half-life coagulation factor concentrates in routine clinical practice: guidance from UKHCDO. Haemophilia. 2016; 22 : 487–498.
47. Rayment R, Chalmers E, Forsyth K, et al. Guidelines on the use of prophylactic factor replacement for children and adults with Haemophilia A and B. British Society for Haematology and John Wiley & Sons Ltd. 2020.
48. Königs C, Ozelo MC, Dunn A, et al. Final Results of PUPs A-LONG Study: Evaluating Safety and Efficacy of rFVIIIFc in Previously Untreated Patients with Haemophilia A. [abstract]. Res Pract Thromb Haemost. 2020; 4 (Suppl 1). https: //abstracts.isth.org/abstract/final-resultsof-pups-a-long-study-evaluating-safety-and-efficacy-of-rfviiifc-in-previously-untreated-patients-withhaemophilia-a/. Accessed July 19, 2020.
49. Dodt J, Hubbard AR, Wicks SJ, et al. Potency determination of factor VIII and factor IX for new product labelling and postinfusion testing: challenges for caregivers and regulators. Haemophilia. 2015; 21 : 543–549.
50. Hubbard AR, Didt J, Lee T, et al. Recommendations on the potency labelling of factor VIII and factor IX concetrates. J Thromb Haemost. 2013; 11 : 988–989.
51. Pruthi RK. Laboratory monitoring of new hemostatik agents for hemophilia. Semin Hematol. 2016; 53 : 28-34.
52. Workshop report: Characterisation of new clotting factor concentrates (FVIII, FIX) with respect to potency assays used for labelling and testing of post infusion samples. 26 June. 2014. http: //www.ema.europa.eu/docs/en_GB/document_library/Report/2014/07/WC500169760.pdf, přístup 22. 6. 2020
53. Young GA, Perry DJ and for The International Prophylaxis Studfy Group (IPSG). Laboratory assay measurement of modified clotting factor concetrates: a review of the literature and recommendations for practice. J Thromb Haemost. 2019; 17 : 567–573.
54. Gray E, Kitchen S, Bowyer A, et al. Laboratoty measurement of factor replacement therapies in the treatment of congenital haemophilia: A United Kingdom Haemophilia Centre Doctors’Organisation guideline. Haemophilia. 2020; 26 : 6–16.
55. Shima M, Hanabusa H, Taki M, et al. Factor VIII-mimetic function of humanized bispecific antibody in hemophilia A. N Engl J Med. 2016; 374 (21): 2044–2053.
56. Lenting PJ, Denis CV, Christophe OD. Emicizumab, a bispecific antibody recognizing coagulation factors IX and X: how does it actually compare to factor VIII? Blood. 2017; 130 (23): 2463–2468.
57. https: //www.ema.europa.eu/en/documents/product-information/hemlibra-epar-product-information_cs.pdf, přístup 22. 6. 2020
58. Oldenburg J, Mahlangu JN, Kim B, et al. Emicizumab prophylaxis in hemophilia A with inhibitors. N Engl J Med. 2017; 377 (9): 809–818.
59. Mahlangu J, Oldenburg J, Paz-Priel I, et al. Emicizumab prophylaxis in patients who have hemophilia a without inhibitors. N Engl J Med. 2018; 379 (9): 811–822.
60. Pipe SW, Shima M, Lehle M, et al. Efficacy, safety, and pharmacokinetics of emicizumab prophylaxis given every 4 weeks in people with haemophilia A (HAVEN 4): a multicentre, open-label, non-randomised phase 3 study. Lancet Haematol. 2019; 6 (6): e295–e305.
61. MASAC document #258. Recommendation on the use and management of emicizumab - KXWH (HEMLIBRA®) for hemophilia A with and without inhibitors. https: //www.hemophilia.org/sites/default/files/document/files/258_emicizumab.pdf, přístup 22. 6. 2020.
62. Müller J, Pekrul I, Pötzsch B, et al. Laboratory monitoring in emicizumab-treated persons with hemophilia A. Thromb Haemost. 2019; 119 : 1384–1393.
63. Kruse-Jarres R, Callaghan MU, Croteau SE, et al. Surgical experience in two multicenter, open-label phase 3 studies of Emicizumab in person with hemophilia A with inhibitors (HAVEN 1 and HAVEN 2). Blood. 2017; 130 (Supplement 1): 89.
64. Peyvandi F, Garagiola I. Clinical advances in gene therapy updates on clinical trials of gene therapy in haemophilia. Haemophilia. 2019; 25 : 738–746.
65. Hemophilia of Georgia, U.S.A. Protocol for the treatment of haemophilia and von Willebrand Disease. Haemophilia. 2000; 6 (Suppl. 1): 84–93.
66. Mahlangu JN, Gilham A. Guideline for the treatment of haemophilia in South Africa. S Afr Med J. 2008; 98 : 1296–1311.
67. Rodriguez-Merchan EC. Articular bleeding (hemarthrosis) in hemophilia. http: //www.wfh.org/2/docs/Publications/Musculoskeletal_Physiotherapy/TOH-23-Hermarthrosis-Revised2008.pdf, přístup 22. 6. 2020.
68. Hanley J, McKernan A, Greagh MD, et al. Guidelines for the management of acute joint bleeds and chronic synovitis in haemophilia. UKHCDO guideline. Haemophilia. 2017; 23 : 5121–520.
69. Fernandez-Palazzi F. Treatment of acute and chronic synovitis by non-surgical means. Haemophilia 1998; 4 : 518–523.
70. Dunn AL, Busch MT, Wyly JB, Abshire TC. Radionuclide synovectomy for hemophilic arthropathy: a comprehensive review of safety and efficacy and recommendation for a standardized treatment protocol. Thromb Haemost. 2002; 87 : 383–393.
71. Rodriguez-Merchan EC, Quintana M, de la Corte-Rodriguez H, Coyas J. Radioactive synoviorthesis for the treatment of haemophilic synovitis. Haemophilia. 2007; 13 (Suppl. 3): 32–37.
72. Rodrigez-Merchan EC, Valentino LA. Safety of radiation exposure after radiosynovectomy in paediatric patients with haemophilia. Haemophilia. 2015; 21 : 411–418.
73. Sorensen B, Benson GM, Bladen M, et al. Management of muscle haematoma in patiens with severe haemophilia in an evidence-poor world. Haemophila. 2012; 18 : 598–606.
74. Richards M, Williams M, Chalmers E, et al. A United Kingdom Haemophilia Centre Doctors’ Organization guidelines approved by the British Committee for Standards in Haematology: guideline on the use of prophylactic factor VIII concentrate in children and adults with severe haemophilia A. Br J Haematol. 2010; 149 : 498–507.
75. Pipe SW, Valentino LA. Optimizing outcomes for patients with severe haemophilia A. Haemophilia. 2007; 13 (Suppl. 4): 1–16.
76. Auerswald G, Bidlingmaier C, Kurnik K. Early prophylaxis/FVIII tolerization that avoids immunological ganger signals is still effective in minimizing FVIII inhibitor developments in previously untreated patients – long-term follow-up and continuing experience. Haemophilia. 2012; 18: e18–e20.
77. Auerswald G, Kutnik K, Aledort LM, et al. The EPIC study: a lesson to learn. Haemophilia. 2015; 21 : 622–628.
78. Ljung R, Auerswald G, Benson G, et al. Novel coagulation factor concentrates: Issues relating to their clinical implementation and pharmacokinetic assessment for optimal prophylaxis in haemophilia patients. Haemophilia. 2013; 19 : 481–486.
79. Hay CRM. Prophylaxis in adults with haemophilia. Haemophilia. 2007; 13 (Suppl. 2): 10–15.
80. Nijdam A, Foppen W, de Kleijn P, et al. Discontinuing early prophylaxis in severe haemophilia leads to deterioration of joint status despite low bleeding rates. Thromb Haemost. 2016; 115 : 931–938.
81. Manco-Johnson MJ, Kempton CL, Reding MT, et al. Randomized, controlled, parallel-group trial of routine prophylaxis vs on-demand treatment with sucrose-formulated recombinant factor VIII in adults with severe hemophilia A (SPINART). J Thromb Haemost. 2013; 11 : 1119–1127.
82. Tagliaferri A, Feola G, Molinari AC, et al. Benefits of prophylaxis versus on-demand treatment in adolescents and adulkts with severe haemophilia A: the POTTER study. Thromb Haemost. 2015; 114 : 35–45.
83. Fischer K, Collins P, Björkman S, et al. Trends in bleeding patterns during prophylaxis for severe haemophilia: observation from a series of prospective clinical trials. Haemophilia. 2011; 17 : 433–438.
84. Ljung R, Fischer K, Carcao M, et al. Practical considerations in choosing a factor VIII prophylaxis regimen: Role of clinical phenotype and trough levels. Thromb Haemost. 2016; 115 : 913–920.
85. Iorio A, Iserman E, Blanchette V, et al. Target plasma factor levels for personalized treatment in haemophilia: a Delphi consensus statement. Haemophilia. 2017; 23: e170–e179.
86. Bojar M. Metodický návod o komplexní péči o nemocné s hemofilií a dalšími poruchami hemostázy. Č.j.: PKP/2-2713-1.4. 92 (Věstník MZ ČR č. 3/1992).
87. Brewer A, Correa ME. Guidelines for dental treatment of patients with inherited bleeding disorders. World Federation of Hemophilia. 2006. http: //www.wfh.org/2/docs/Publications/Dental_Care/TOH-40_Dental_treatment.pdf, přístup 22. 6. 2020.
88. EASL Recommendations on Treatment of Hepatitis C. 2016 SUMMARY. Journal of Hepatology, September. 2016. http: //www.easl.eu/medias/cpg/HCV2016/Summary.pdf, přístup 22. 6. 2020.
89. Staritz P, De Moerloose P, Schutgens R, Dolans G. Applicability of the European Society of kardiology guidelines on management of acute coronary syndromes to people with haemophilia – an assessment by the ADVANCE Working Group. Haemophilia. 2013; 19 : 833–840.
90. Schutgens REG, Klamroth R, Pabinger I, et al. Management of atrial fibrilation in people with haemophilia – a concensus view by the ADVANCE Working Group. Haemophilia. 2014; 20: e399–e443.
91. Franchini M, Mannucci PM. Co-morbidities and quality of life in elderly persons with haemophilia. Br J Haematol. 2009; 148 : 522–533.
92. Mannucci PM, Schutgens REG, Santagostino E, Mauser-Bunschoten EP. How I treat age-related morbidities in elderly persons with hemophilia. Blood. 2009; 114 : 5256–5263.
93. Martin K and Key NS. How I treat patients with inherited bleeding disorders who need anticoagulant therapy. Blood. 2016; 128 (2): 178–184.
94. Jabbar AY, Baydoun H, Janbain M, Ferdinand KC. Current concepts in the management of stable ischemic heart disease and acute coronary syndrome in patients with hemophilia. Ann Transf Med. 2018; 6 (15): 299–305.
95. Schutgens REG, van der Heijden JF, Mauser-Bunschoten EP, Mannucci PM. New concept for anticoagulant therapy in persons with hemophilia. Blood. 2016; 128 : 2471–2474.
96. Mannucci PM, Mauser-Bunschoten EP. Cardiovascular disease in haemophilia patients: a contemporary issue. Haemophilia. 2010; 16 (Suppl. 3): 58–66.
97. Wight J, Paisley S. The epidemiology of inhibitors in haemophilia A: a systematic review. Haemophilia. 2003; 9 : 418–435.
98. Astermark J, Morado M, Rocino A, et al. Current European practise in immune tolerance induction therapy in patiens with haemophilia and inhibitors. Haemophilia. 2006; 12 : 363–371.
99. DiMichele DM, Hoots WK, Pipe SW, et al. International workshop on immune tolerance induction: consensus recommendations. Haemophilia. 2007; 13 (Suppl. 1): 1–22.
100. Astermark J. Overview of inhibitors. Semin Hematol. 2006; 43 (Suppl. 4): 3–7.
101. Darby SC, Keeling DM, Spooner RJD, et al. The incidence of factor VIII and factor IX inhibitors in the hemophilia population of the UK and their effect on subsequent mortality, 1977 -99. J Thromb Haemost. 2004; 2 : 1047–1054.
102. Peerlinck K, Jacquemin M. Characterictics of inhibitors in mild/moderate haemophilia A. Haemophilia. 2006; 12 (Suppl. 6): 43–47.
103. Abbonizio F, Giampaolo A, Coppola A, et al. Therapeutic management and cost of severe haemophilia A patients with inhibitors in Italy. Haemophilia. 2014; 20: e243–e250.
104. Hay CRM. The epidemiology of factor VIII inhibitors. Haemophilia. 2006; 12 (Suppl. 6): 23–29.
105. Astermark J. Why do inhibitors develop? Principles of and factors influencing the risk for inhibitor development in haemophilia. Haemophilia. 2006; 12 (Suppl. 3): 52–60.
106. Castaman G, Fijnvandraat K. Molecular and clinical predictors of inhibitor risk and its prevetion and treatment in mild hemophiliaA. Blood. 2014; 124 (15): 2333–2336.
107. Oldenburg J, Pavlova A. Genetic risk factors for inhibitors to factors VIII and IX. Haemophilia. 2006; 12 (Suppl. 6): 15–22.
108. EHC response to the Publication of the SIPPET Study. June 3, 2016. http: //static.ehc.eu/wp-content/uploads/EHC-SIPPET-Position-3-June-2016-WEB.pdf
109. Cormier M, Batty P, Tarrant J, Lillicrap D. Advances in knowledge of inhibitor formation in severe haemophilia A. Br J Haematol. 2020; 189 : 39–53.
110. Platokouki H, Fischer K, Gouw SC, et al. Vaccinations are not associated with inhibitor development in boys with severe haemophilia A. Haemophilia. 2018; 24 : 283–290.
111. Fischer K, Collins PW, Ozelo MC, et al. When and how to start prophylaxis in boys with severe hemophilia without inhibitors: Communication from SSc of the ISTH. J Thromb Haemost. 2016; 14 : 1105–1109.
112. http: //www.euhanet.org/, přístup 22. 6. 2020.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2021 Číslo 1- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- U pacientů s traumatem je častěji dosaženo adekvátních hladin anti-Xa při dávkování enoxaparinu podle hmotnosti
- Steroidní a nesteroidní inhibitory aromatázy v léčbě rakoviny prsu u postmenopauzálních žen
-
Všechny články tohoto čísla
- ZMĚNY V IMUNITNÍM SYSTÉMU U NELÉČENÝCH NEMOCNÝCH S CHRONICKOU LYMFOCYTÁRNÍ LEUKEMIÍ – ČÁST 2: NESPECIFICKÁ IMUNITA.
-
Doc. MUDr. Miroslav Tomíška, CSc.,
slaví sedmdesáté životní jubileum - Zemřel profesor Jan Evangelista Dyr
- Nově používané molekuly v cílené léčbě akutní myeloidní leukemie – jejich nežádoucí účinky, komplikace terapie a významné lékové interakce
- Jaké dávky inhibitorů tyrozinkináz jsou v léčbě pacientů s chronickou myeloidní leukemií optimální?
- EDITORIAL
- Von Willebrandova choroba – porovnanie dvoch metód analýzy multimérov von Willebrandovho faktora
- Nález dimorfní populace erytrocytů na analyzátorech krevních buněk
- Bolesti svalů jako vzácný autoimunitní projev při monoklonální IgM gamapatii – popis případu a přehled autoimunitních projevů monoklonálních imunoglobulinů
- Inhibítory faktora VIII – Výsledky imunotolerančnej indukcie v Národnom hemofi lickom centre a nové možnosti a prvé skúsenosti s liečbou bišpecifi ckou protilátkou (emicizumab) u pacientov s inhibítormi na Slovensku
- Konsenzuální doporučení Českého národního hemofilického programu (ČNHP) pro diagnostiku a léčbu pacientů s hemofilií, vydání 3., rok 2021
- Heparinem indukovaná trombocytopenie
- Doporučení pro diagnostiku a léčbu chronické lymfocytární leukemie 2021
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Heparinem indukovaná trombocytopenie
- Nález dimorfní populace erytrocytů na analyzátorech krevních buněk
- Doporučení pro diagnostiku a léčbu chronické lymfocytární leukemie 2021
- Bolesti svalů jako vzácný autoimunitní projev při monoklonální IgM gamapatii – popis případu a přehled autoimunitních projevů monoklonálních imunoglobulinů
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: MUDr. Petr Výborný, CSc., FEBO
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



