-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praxe
Deficit tyroxín viažúceho globulinu
Thyroxin binding globulin deficiency – a case study and literature review.
Abnormalities in the serum proteins that transport thyroid hormones do not alter the metabolic state and do not cause thyroid disease. However, they do alter total thyroid hormone concentrations in serum and, when unrecognized, may lead to inappropriate treatment. Therefore, estimation of TSH and fT4 concentrations is usually all that is required for evaluation of thyroid function. Measurement of TBG and total hormones is only appropriate for special targets, and is not common practice.
Key words:
total thyroxine, free thyroxine, TBG, deficiency TBG.
Autoři: A. Kreze jr. 1; M. Pura 2; M. Kosák 1; J. Koskuba 1
Působiště autorů: II . Interní oddělení Fakultní nemocnice Bulovka, Praha Primář: MUDr. Jiří Koskuba. 1; Národný endokrinologický a diabetologický ústav, Ľubochňa Primár: MUDr. Peter Vaňuga, Ph. D. 2
Vyšlo v časopise: Prakt. Lék. 2008; 88(7): 425-426
Kategorie: Kazuistika
Souhrn
Abnormality sérových proteínov, ktoré transportujú tyroidné hormóny, nealterujú metabolický stav a nezapríčiňujú tyroidné ochorenie. Vzniká ale porucha koncentrácií celkových sérových tyroidných hormónov, ktoré ak sú nepoznané, vedú k nenáležitej liečbe. Preto v bežnej praxi pre hodnotenie funkcie štítnej žľazy je dostatočné stanovenie koncentrácie TSH a fT4. Stanovovanie TBG a celkových hormónov je vhodné pre špeciálne ciele, nie pre bežnú dennú prax.
Kľúčové slová:
celkový tyroxín, voľný tyroxín, TBG, deficit TBG.Vlastné pozorovanie
Na našu endokrinologickú ambulanciu bol odoslaný 29 ročný „zdravý“ (negatívna anamnéza a fyziologický objektívny nález) muž, kde sa v rámci preventívnej prehliadky našli laboratórne hodnoty: tyreocyty stimulujúci hormón (TSH) 2,550 mU/l (norma 0,270–4,200 mU/l) a celkového tyroxínu (TT4) 35, 7 nmol/l (norma 66,0–181,0 nmol/l).
Doplnili sme vyšetrenie o voľné hormóny: voľný tyroxín (fT4) 17,6 pmol/l (norma 12,0–22,0 pmol/l), voľný trijódtyronín (fT3) 4,49 pmol/l (norma 3,95-6,8 pmol/l) a následne o stanovenie tyroxín viažúceho globulinu (TBG): 1,1 mg/l (norma 12,0–36, 0 mg/l).
Vyšetrenia sa vykonali komerčnými RIA kitmi (Immunotech, Česká republika). Jednalo sa o parciálny deficit TBG. Nakoľko je to geneticky podmienené ochorenie, vyšetrili sme rodičov s následovnými výsledkami:
matka: TSH 4,49 mU/l, TT4 72,7 nmol/l, TT3 0,97 nmol/l, fT4 17,5 pmol/l, fT3 3,66 pmol/l, TBG 5,1 mg/l,
otec: TSH 1,86 mU/l, TT4 100,1, nmol/l, TT3 1,63 nmol/l, fT4 16,4 pmol/l, fT3 5,01 pmol/l, TBG 15,5 mg/l.
Z uvedeného vyplýva, že sme potvrdili prenos defektného génu pre TBG z matky na syna.
Prehľad problematiky
Tyroidné hormóny v cirkulácii existujú vo voľnej a viazanej forme. Množstvo voľnej frakcii hormónu, ktorý je metabolicky aktívny komponent, predstavuje 0,03 % cirkulujúceho totálneho tyroxínu a 0,3 % cirkulujúceho trijódtyronínu. Hormóny sú naviazané na proteíny, z ktorých je najvýznamnejší TBG, ktorý viaže 75 % tyroidných hormónov. Ďaľšie viažúce proteíny sú thyroid binding prealbumin (TBPA), alebo transthyretin a albumín. Na tieto proteíny sa viaže asi 10–15 % celkového tyroxínu, kdežto trijódtyronín sa na tieto plazmatické komponenty neviaže.
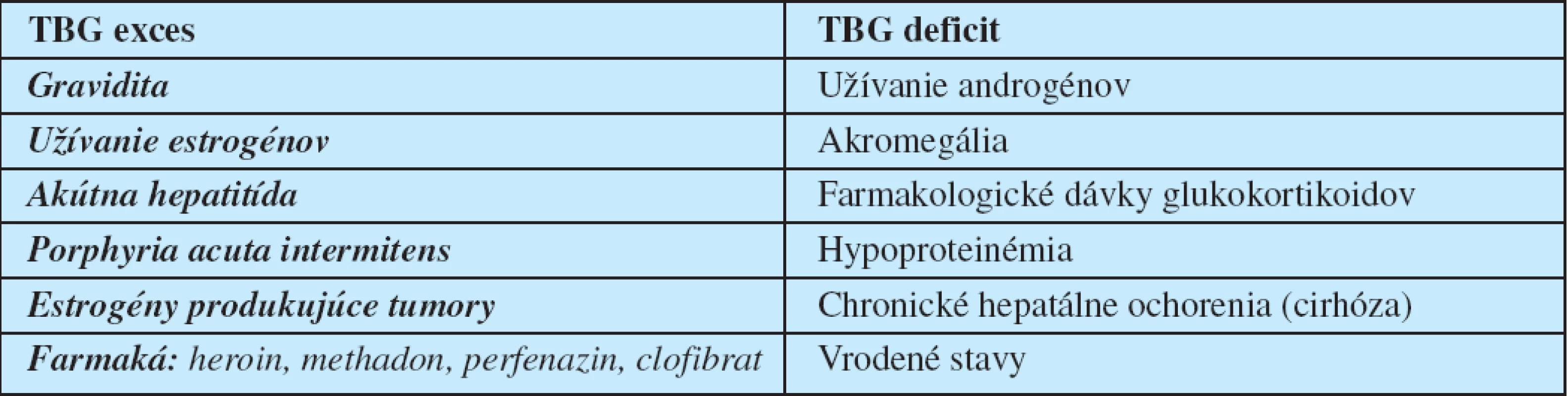
Porušenie koncentrácií thyroid binding proteínov, hlavne TBG, má za následok zmenu v hodnote celkových hormónov. Ale množstvo nenaviazaných, alebo voľ-ných (free) hormónov nie je narušené, takže tyreometabolický stav ostáva nezmenený. Stavy porušenej koncentrácie TBG a prealbumínu majú za následok alteráciu hodnôt celkových hormónov. Na koncentráciu TBG vplývajú rozličné faktory (10), ktoré sú uvedené v tabuľke 1.
TBG je 395 aminokyselinový, 54-kd polypeptid syntetizovaný v pečeni. Génový lokus u ľudí sa nachádza na dlhom ramene X chromozómu-Xq22.2 (7,12). TBG je člen serínovej proteázovej inhibítorovej (SERPIN) superrodiny. Do superrodiny patrí kortizol viažúci globulin, antitrombín III a angiotenzín.
Existenciu vrodených defektov sérových transportných proteínov pre tyroidné hormóny prvý krát popísali Beierwaltes a Robins (1).
Následne bolo identifikovaných 36 variant TBG deficitu a v 30 prípadov sa verifikovala genetická molekulárna báza génovou analýzou (4, 8). TBG deficit nezapríčiní tyroidné ochorenie.
Patofyziologický mechanizmus je následovný: zníženie TBG koncentrácie iniciuje zvýšenie koncentrácií voľných hormónov, čo zapríčiní tendenciu k hypertyroidnému stavu, a to vedie k zníženiu sekrécie TSH a následne tyroidných hormónov v štítnej žľaze. Finálne sa koncentrácia totálnych hormónov v sére zníži a koncentrácia voľných hormónov a TSH ostáva v norme.
Existuje kompletný a parciálny deficit TBG.
Kompletný deficit u mužov vedie k nedetekovateľnej koncentrácii TBG, u žien k asi polovičným (normálnym) koncentráciám TBG.
Parciálny deficit sa u mužov prejaví merateľnými koncentráciami TBG a u žien nadpolovičnými (normálnymi) koncentráciami TBG.
Prevalencia kompletného TBG deficitu je asi 1 : 15 000 mužských novorodencov a prevalencia parciálneho TBG deficitu 1 : 4000 novorodencov.
Z literárnych prehľadov (2, 3, 5 ,6, 11) a nakoniec aj našej kazuistiky vyplýva fakt, že k skríningovému vyšetreniu funkcie štítnej žľazy dostačuje TSH a fT4, ktoré sú citlivé markery jej funkcie. Tradične sa ale u neendokrinologickej populácie lekárov v praxi ešte aj dnes stretávame s vyšetrovaniami celkových hormónov. Na jednej strane to má význam, keď lekár može dedukovať na niektorý zo stavov uvedených v tabuľke 1, a v výskumných, alebo experimentálnych štúdiách na splnenie daného cieľa. Na druhej strane dostačuje podrobná anamnéza a klinický nález (k vylúčeniu, či potvrdeniu extratyroideálnych príčin nefyziologických koncentrácií celkových tyroidných hormónov), alebo vyšetrenie len TSH a frakcii voľných hormónov k posúdeniu funkcie štítnej žľazy, čím sa zjednodušuje, urýchľuje a finančne redukuje celý proces.
Najvýznamnejší klinický aspekt deficitu TBG je hrozba nesprávnej interpretácie laboratórnych výsledkov a vyhnutie sa nepotrebnej, nesprávnej a potenciálne ohrozujúcej liečbe tyroidnými hormónami (9).
MUDr. Alexander Kreze jr., Ph.D.
II. Interní oddělení FN Bulovka
Budínova 2
180 81 Praha 8
E-mail: krezejr@zoznam.sk
Zdroje
1. Beierwaltes, W.H., Robbins, J. Familial increase in the thyroxine–binding sites in serum alpha globulin. J. Clin. Incest. 1959, 38, p. 1683–1688.
2. Fleming, J.J., Rajaratnam, S., Seshadri M.S. et al. An audit of total and free thyroxine measurement in screening for hypo and hyperthyroidism in patients using chemiluminiscence immunoassay. Ind. J. Clin. Bioch. 2001, 16, p. 95-100.
3. Gharib, H., Tuttle, R.M., Baskin H.J. et al. Subclinical thyroid dysfunction: a joint statement on management from the American association of clinical endocrinologist, the American thyroid association, and the Endocrine society. JCEM 2005, 1, p. 581-585.
4. Hayashi, Y., Refetoff, S. Genetic abnormalities of thyroid hormone transport serum proteins. In: Weintraub, B. Molecular endocrinology. Basic concepts and clinical correlations. New York: Raven Press, 1995, p. 371–387.
5. Helfand, M. Screening for subclinical thyroid dysfunction in non pregnent adults. Summary and evidence. Ann. Intern. Med. 2004, 140, p. 128-141.
6. Larsen, P.R., Davies, T.F., Schlumberger, M.J. et al. Thyroid physiology and diagnostic evaluation of patients with thyroid disorders. In: Larsen, P.R., Kronenberg, H.M., Melmed, S., Polonsky K.S. Williams textbook of endocrinology. Philadelphia: Saunders, 2003. 1927 p.
7. Mori, Y., Miura, Y., Oiso, Y. et al. Precise localisation of the human thyroxine–binding globulin gene to chromozome Xq22.2 by flouroscence in situ hybridization. Hum. Genet. 1995, 96, p. 481-482.
8. Refetoff, S., Dumont, J.E., Vassart, G. Thyroid disorders. In: Scriver, C.R., Beaudet, A.L., Sly, W.S., Valle, D., Childs, B., Vogelstein, B. The metabolic and molecular basis of inherited disease (8 ed.). New York: McGraw-Hill, 2000. 4029–4075 p.
9. Sarlis, N.J., Hirshberg, B. Thyroxin-binding globulin deficiency [on line]. Dostupný na www.emedicine.com/med/topic2277.htm. Updated 12. 6. 2006. [cit. 2008-05-06].
10. Singer, P.A. Evaluation of thyroid function. In: Lavin, N.: Manual of endocrinology and metabolism. Philadelphia: Lippincott Williams Wilkins, 2002. 854 p.
11. Surks, M.I. Primary hypotyroidism. New issues and controversies. Endocrinologist 2006, 16, p. 203–207.
12. Trent, J.M., Flink, I.L., Morkin, E. et al. Localization of the human thyroxine-binding globuline gene to the long arm of the X chromozome(Xq21-22). Am. J. Hum. Genet. 1987, 41, p. 428–435.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek Perniciózní anémieČlánek Sladkovodní ryby ve výživěČlánek JubileaČlánek Chlamydiové pneumonieČlánek Žena v mrazáku
Článek vyšel v časopisePraktický lékař
Nejčtenější tento týden
2008 Číslo 7- Při preskripci inkontinenčních pomůcek je nezbytné hlídat limity
- Příznivý vliv Armolipidu Plus na hladinu cholesterolu a zánětlivé parametry u pacientů s chronickým subklinickým zánětem
- Když se ve střevech děje něco nepatřičného...
- Novinka s obsahem acikloviru dostupná na trhu ve více silách
- Pacient se bude cítit komfortně pouze při správně zvolené absorpční pomůcce
-
Všechny články tohoto čísla
- Laparoskopická kolorektální chirurgie pro karcinom – současný stav
- Perniciózní anémie
- Poranění hlezenního kloubu rostoucího skeletu
- Sladkovodní ryby ve výživě
- Sexuální rehabilitace po některých estetických operacích ženského genitálu
- Srdeční selhání se zachovalou ejekční frakcí levé komory srdeční
- Syndrom vyhoření a čeští praktičtí lékaři
- Hazardní hry a pracovní prostředí
- Obtížně diagnostikovatelné zlomeniny rostoucího dětského skeletu
- Tuberkulóza dýchacího ústrojí – diagnostický a léčebný přístup
- Jubilea
- V.A.C. terapie v léčbě traumatických defektů měkkých tkání
- Nový tomograf zařadil českou radiologii na světovou špičku
- Akutní exacerbace etylické cirhózy jater z méně obvyklých příčin
- Chlamydiové pneumonie
- Deficit tyroxín viažúceho globulinu
- Nová úskalí poskytování zdravotní péče
- Miniportréty slavných českých lékařů Profesor MUDr. Jan Baštecký, jeden ze zakladatelů české radiologie
- Žena v mrazáku
- Pozvání na XVIII. kongres ČLS JEP
- Antibiotika versus probiotika
- MUDr. Ljiljana Bojičová – úspěšných 15 let v čele lékařské posudkové služby
- Vladimír Wagner,jeden z prvních českých mikrobiologů a imunologů
- Praktický lékař
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Perniciózní anémie
- Obtížně diagnostikovatelné zlomeniny rostoucího dětského skeletu
- V.A.C. terapie v léčbě traumatických defektů měkkých tkání
- Chlamydiové pneumonie
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání