-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Závažný průběh autoimunitní encefalitidy u sedmnáctiletého chlapce
Severe autoimmune encephalitis in a seventeen-year-old boy – case report
Autoimmune encephalitis represent a heterogenous group of diseases which is based on an immune response against neuronal autoantigens with production of antibodies. Anti-N-methyl-D-aspartate receptor (anti-NMDAR) encephalitis is characterised by diffused involvement of cortical and subcorticale structures and represents the most frequent type of autoimmune encephalitis in adults which can manifest also in children and adolescents.
We present a case report of a seventeen-year-old boy with severe anti-NMDAR encephalitis and typical initial psychiatric symptomatology.
Keywords:
autoimmune encephalitis – anti-NMDAR encephalitis – children – Pediatrics
Autoři: A. Liptáková 1; J. David 1; J. Jonáš 2; N. Šimánková 1; V. Koukolská 3; R. Valkovičová 4
Působiště autorů: Pediatrická klinika 2. LF UK a FN Motol, Praha 1; Klinika anesteziologie, resuscitace a intenzivní medicíny 2. LF UK a FN Motol, Praha 2; Klinika zobrazovacích metod 2. LF UK a FN Motol, Praha 3; Klinika dětské neurologie 2. LF UK a FN Motol, Praha 4
Vyšlo v časopise: Čes-slov Pediat 2020; 75 (8): 474-478.
Kategorie: Kazuistika
Souhrn
Autoimunitní encefalitidy představují heterogenní skupinu nemocí, jejímž podkladem je postižení mozku imunitně zprostředkovanými mechanismy. Encefalitida s pozitivitou protilátek proti glutamátovým N-metyl-D-aspartát receptorům (tzv. anti-NMDAR encefalitida) je charakterizována difuzním postižením kortikálních i subkortikálních struktur. Představuje nejčastěji udávanou autoimunitní encefalitidu dospělých, která se může manifestovat i u dětí a mladistvých.
Prezentované sdělení formou kazuistiky se věnuje závažnému průběhu anti-NMDAR encefalitidy u sedm-náctiletého chlapce s typickou iniciální psychiatrickou symptomatologií.
Klíčová slova:
autoimunitní encefalitida – anti-NMDAR encefalitida – deti – pediatrie
ÚVOD
Autoimunitní encefalitidy představují heterogenní skupinu nemocí, jejímž podkladem je postižení mozku imunitně zprostředkovanými mechanismy (tab. 1) [1]. Jedná se o akutní či subakutní zánětlivá onemocnění mozku se širokým spektrem klinických projevů, od typických limbických encefalitid po syndromy s komplexní neuropsychiatrickou symptomatologií, jako je deficit paměti, kognitivní regres, psychóza, epileptické záchvaty, mimovolní pohyby a porucha vědomí charakteru stuporu až kómatu. Klinický obraz a prognóza se může u jednotlivých zástupců výrazně lišit [2].
Tab. 1. Klasifikace autoimunitních encefalitid (upraveno dle [1]). ![Klasifikace autoimunitních encefalitid (upraveno dle [1]).](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/a24990f52cdeca8bde55fa1899085410.png)
Encefalitida s pozitivitou protilátek proti glutamátovým N-metyl-D-aspartát receptorům (tzv. anti-NMDAR encefalitida) je charakterizována difuzním postižením kortikálních i subkortikálních struktur (hipokampus, bazální ganglia) a představuje nejčastěji udávanou autoimunitní encefalitidu. Poprvé byla popsána v roce 2007 autory Dalmau et al. na souboru dvanácti žen s ovariálním teratomem [3]. Onemocnění postihuje častěji mladé dospělé a dětské pacienty, přibližně 80 % tvoří ženy [4]. V dětském věku dominuje neparaneoplastická etiologie. Asociace s ovariálním teratomem je závislá na věku, přibližně 50 % žen starších osmnácti let má potvrzený ovariální teratom. Naopak u dívek mladších čtrnácti let je výskyt teratomu méně než 9%. Přítomnost nádorového onemocnění u mužů je vzácnější. Kromě ovariálního teratomu byly popsány případy anti-NMDAR encefalitidy asociované s testikulárním germinálním nádorem, teratomem mediastina, malobuněčným karcinomem plic, Hodgkinovým lymfomem a neuroblastomem [5].
Prezentované sdělení formou kazuistiky se věnuje závažnému průběhu anti-NMDAR encefalitidy u sedmnáctiletého chlapce s typickou iniciální psychiatrickou symptomatologií.
KAZUISTIKA
Sedmnáctiletý chlapec byl přijat na pediatrickou kliniku překladem z psychiatrické nemocnice pro proběhlou epizodu tonicko-klonických křečí a poruchu vědomí. Jednalo se o pacienta s anamnézou abúzu/experimentování s návykovými látkami (kanabinoidy, stimulancia), který byl recentně hospitalizován na dětském oddělení v místě bydliště pro poruchu vědomí s deviací bulbů vzhůru, progredující zmatenost, neklid a agresivitu s nutností opakovaného podání haloperidol-dekanoátu. Stav byl uzavřen jako akutní intoxikace diethylamidem kyseliny lysergové (LSD) a marihuany. Následně byl přeložen na pracoviště dětské psychiatrie, kde se v den překladu v ranních hodinách pětkrát objevil stav propnutí do opistotonu a symetrický třes končetin trvající do 30 s. Během této ataky byl pacient tachypnoický, tachykardický a febrilní s maximem 39 °C. Následně byl zajištěn rektálním diazepamem (10 mg), antipyretikem (paracetamol 500 mg), kapací infuzí s glukózou a ionty, jednou dávkou širokospektrého antibiotika (amoxicilin-klavulanát 1,2 g) a odeslán na naše pracoviště.
Nejprve uvádíme podrobné informace z pacientovy anamnézy. Jednalo se o původně eutrofické a donošené dítě z první fyziologické gravidity. Chlapec se narodil ve 41. gestačním týdnu plánovaně císařským řezem (pro kefalopelvický nepoměr) s porodní hmotností 3940 g a délkou 52 cm. Poporodní adaptace byla bez komplikací. Chlapec prospíval dobře a psychomotoricky se vyvíjel normálně. Očkován byl řádně podle očkovacího kalendáře. Žije v neúplné rodině s matkou, rodiče jsou rozvedeni. Studuje střední odbornou školu a přiznává příležitostné užívání LSD a marihuany. Je řádně dispenzarizován praktickým lékařem a alergologem pro atopickou dermatitidu a polinózu. Otec i matka pacienta jsou zdrávi, v širší rodině se neurologické onemocnění nevyskytuje. Chlapec má tři sourozence, desetiletou paternální sestru a dále pak maternální desetiletou a čtyřletou sestru, všechny jsou zdrávy.
Při vstupním fyzikálním vyšetření byl chlapec tachypnoický, afebrilní, somnolentní až soporózní s necílenou reakcí na algický podnět, výrazně slinil, poslechově bylo znatelné zhrubělé dýchání vpravo s ojedinělými chrůpky, s dechovou frekvencí 30/min, tepovou frekvencí 160/min, krevním tlakem 156/74 mmHg a saturací 98 % při oxygenoterapii. Dominoval též astenický habitus, ostatní somatický nález byl v mezích normy s následujícími antropometrickými parametry – výška 174 cm (18. percentil), hmotnost 56,7 kg (5. percentil), body mass index (BMI) 18,7 kg/m2 (7. percentil). Počátečním neurologickým vyšetřením byla konstatována porucha vědomí (Glasgow Coma Scale 9), pozitivní meningeální příznaky a omezená hybnost končetin pravděpodobně při nespolupráci a při celkovém stavu.
Vstupní laboratorní vyšetření prokázalo následující patologické nálezy: leukocytózu (20,8x109/l) a neutrofilii (86 %) v krevním obraze, elevaci alaninaminotransferázy (ALT, 1,32 μkat/l), kreatinkinázy (CK, 372 μkat/l) a myoglobinu (1 768 μg/l), kombinovanou poruchu acidobazické rovnováhy – metabolickou acidózu (aktivní HCO3 19,4 mmol/l, laktát 4,4 mmol/l) kompenzovanou mírnou respirační alkalózou (pH 7,45, pCO2 3,77 kPa), v moči proteinurie (2 jednotky) a pozitivní kanabinoidy (v rámci abúzu) a benzodiazepiny (iatrogenně). Mineralogram a koagulační parametry byly ve fyziologickém rozmezí, C-reaktivní protein (CRP) 0,5 mg/l. Vývoj vybraných laboratorních parametrů shrnuje tabulka 2.
Tab. 2. Vývoj vybraných laboratorních parametrů u prezentovaného pacienta, zdroj vlastní. 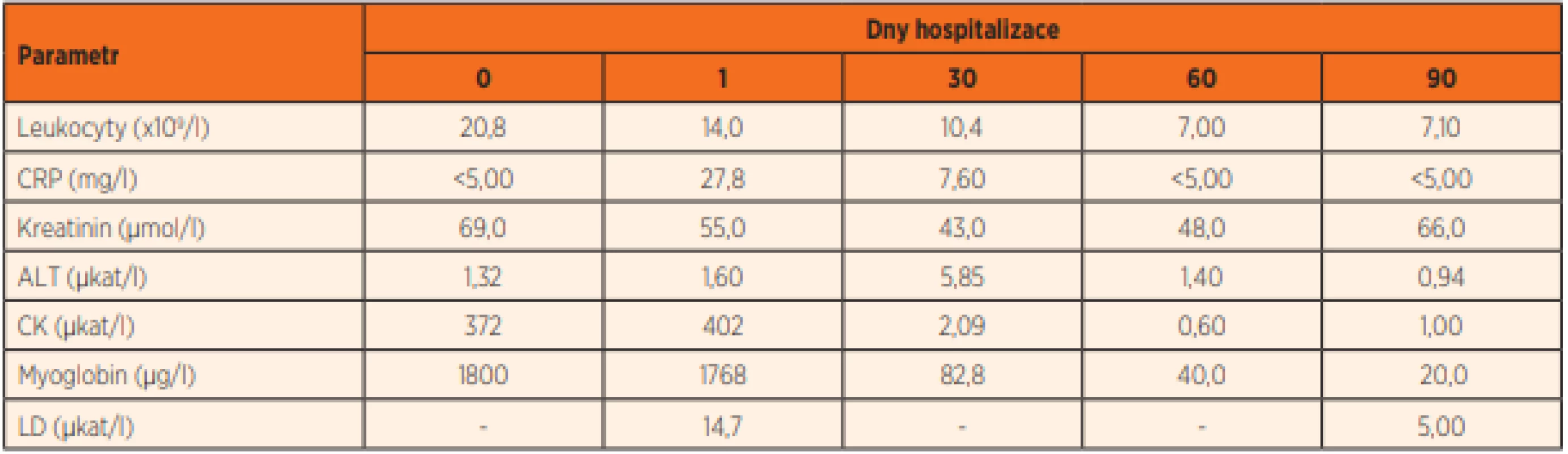
Vzhledem ke klinickému stavu bylo akutně provedeno vyšetření mozku výpočetní tomografií (CT), které však nepotvrdilo abnormality. V diferenciální diagnóze byla zvažována na prvním místě neuroinfekce, dále pak autoimunitní encefalitida. V likvorovém nálezu byla prokázána mírná lymfocytární pleiocytóza (leukocyty 17/3, lymfocyty 90 %), s normální proteinorachií a bez intratékální syntézy imunoglobulinů či průkazu infekčního agens. Diagnóza byla stanovena potvrzením výrazné pozitivity anti-NMDAR protilátek v likvoru i v séru (+++, metodou nepřímé imunofluorescence). Elektroencefalografické vyšetření (EEG) potvrdilo zpomalení bilaterálně frontotemporálně s iktálním vzorcem a s korelátem záchvatu, další záznam též prokázal specifické vlny, tzv. extreme delta brushes. Následující den bylo provedeno zobrazení magnetickou rezonancí (MRI) s nálezem změn lokalizovaných do kortexu frontomediálně a do oblasti pravé inzuly s možným podílem cytotoxického edému (obr. 1).
Obr. 1. Zobrazení mozku magnetickou rezonancí: FLAIR (Fluid-attenuated inversion recovery) a DWI (difuzně vážená sekvence).
a) FLAIR sekvence s nálezem mírného rozšíření a zvýšeného signálu kortexu oboustranně frontomediálně a inzulárně vpravo (fialové šipky);
b) DWI se známkami restrikce difuze inzulárně vpravo a frontomediálně oboustranně (modré šipky). Restrikce difuze může
být známkou cytotoxického edému v rámci neurotoxické encefalopatie.
Fig. 1. Brain magnetic resonance imaging: FLAIR (Fluid-attenuated inversion recovery) and DWI (Diffusion-weighted magnetic resonance imaging).
a) Cortical thickening and increased FLAIR signal intensity of insular cortex on the right and frontomedial cortex bilaterally (purple arrows);
b) Diffusion restriction involving right insular cortex and frontomedial cortex bilaterally (blue arrows). Diffusion restriction can be an indicative marker of cytotoxic edema as sign of neurotoxic encephalopathy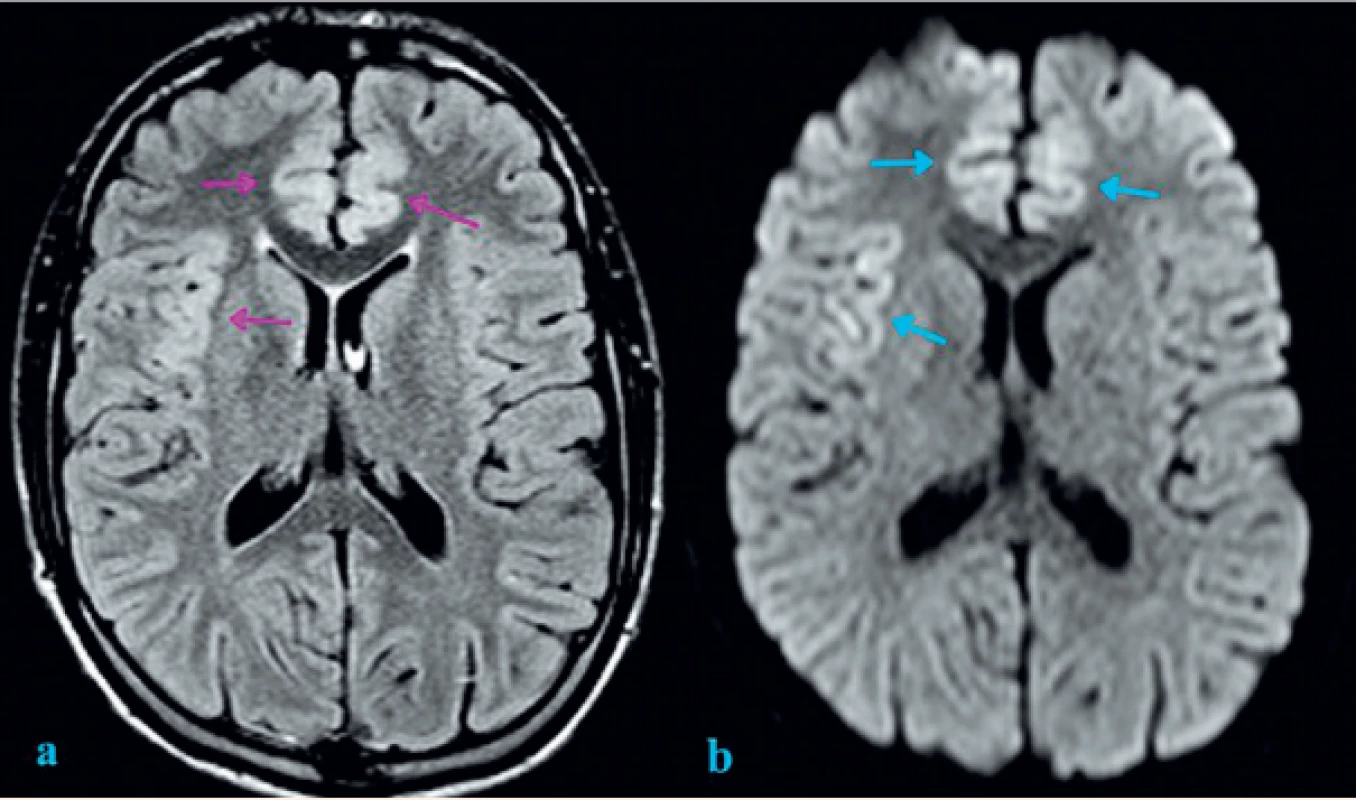
Po stanovení diagnózy byla zahájena imunosupresivní terapie cyklem plazmaferéz. Vzhledem ke klinickému (febrilie, rigidita, porucha vědomí) a laboratornímu obrazu (elevace CK, myoglobinu, leukocytóza) byla předpokládána kombinace diagnóz anti-NMDAR encefalitidy a neuroleptického maligního syndromu (NMS) po podání haloperidol-dekanoátu. Pro progresi kvalitativní poruchy vědomí s významným psychomotorickým neklidem a limitovaných možností tlumení následoval překlad pacienta na resuscitační oddělení. Byla dokončena série sedmi plazmaferéz, současně byl podán pulz natria-methylprednisolonu-sukcinátu v dávce 1 g denně pět následujících dní. K sedaci byla použita kombinace kontinuálně podávaného dexmedetomidinu a propofolu, zpočátku s dobrým efektem.
Z důvodu možného paraneoplastického původu anti-NMDAR protilátek bylo doplněno CT vyšetření hrudníku s nálezem patologické infiltrace thymu, zejména jeho pravého laloku. Provedené tumor markery (alfa-fetoprotein – AFP, lidský choriový gonadotropin – hCG, laktátdehydrogenáza – LDH, karcinoembryonální antigen – CEA) byly negativní. Pacient byl indikován k operačnímu výkonu. Z pravostranné torakotomie byla provedena exstirpace ohraničeného kulovitého tumoru horního mediastina. Dle histologického vyšetření se jednalo o diferencovaný zralý cystický teratom. Krátce po výkonu došlo k výraznému zhoršení psychomotorického neklidu, dávky analgosedace byly postupně významně navýšeny, což vedlo k nutnosti zajištění dýchacích cest tracheální intubací a k zahájení umělé plicní ventilace. I přes kombinovanou analgosedaci (sufentanil-citrát, dexmedetomidin-hydrochlorid, propofol) byl pacient neklidný, analgosedace byla v dalším průběhu postupně eskalována a doplněna o midazolam-hydrochlorid, fenobarbital, promethazin-hydrochlorid a myorelaxaci.
Po ukončení plazmaferéz byly dle indikace neurologa podány intravenózní imunoglobuliny (114 g, tj. 2 g/kg) se snížením dávky natrium-methylprednisolon-sukcinátu (na 0,8 mg/kg/den). V dalším průběhu byla pacientovi založena tracheostomie, což umožnilo deeskalaci analgosedace. Mladík se budil do částečného kontaktu a vyhověl jednoduché výzvě. Dále byla snižována ventilační podpora, což vedlo k odpojení od umělé plicní ventilace. Kontrolní CT hrudníku neprokázalo reziduum nádoru, další onkologická léčba nebyla indikována. Dle MRI mozku došlo k významné regresi signálových změn.
Hospitalizace byla komplikována přechodnou polékovou hepatopatií s elevací jaterních enzymů (maximální hodnoty gamaglutamyltransferázy 19,2 μkat/l, ALT 8,90 μkat/l, aspartátaminotransferázy 3,02 μkat/l) a bilirubinu (maximální hodnoty celkového bilirubinu 53,7 μmol/l a přímého bilirubinu 36,7 μmol/l) s úpravou hodnot po vysazení analgosedace. Rovněž došlo k rozvoji arteriální hypertenze nejspíše jako kombinace vegetativní dysfunkce v rámci základní diagnózy s možným podílem kortikoterapie. V léčbě byl podáván bolusově urapidil-hydrochlorid, poté kontinuálně s dobrým efektem esmolol-hydrochlorid. Následně byla terapie převedena na perorálně podávaný metoprolol-tartarát. Po stabilizaci stavu byl pacient k další péči přeložen na dětskou neurologickou kliniku.
Při překladu přetrvávala kvalitativní porucha vědomí s intermitentními krátkými lucidními intervaly a delšími epizodami halucinací, paranoidních verbálních projevů s agitovaností a brachiální agresí, stavy propnutí s třesem neepileptické etiologie. Proto byl v rámci druhé linie imunosupresivní terapie kromě prednisonu podán jednorázově monohydrát cyklofosfamidu v dávce 1200 mg (tj. 780 mg/m2), po němž došlo k významnému zlepšení stavu vědomí a spolupráce. Odezněly též halucinace a pozvolna i epizody psychomotorického neklidu, při kterých byl přechodně podáván midazolam intravenózně. Pro narušený cirkadiánní rytmus byl do terapie přidán melatonin, dále pro úzkostné a subdepresivní projevy navíc klonazepam a sertralin-hydrochlorid. Vzhledem k rozvoji kombinované spasticity a dystonie na dolních končetinách s levostrannou kontrakturou byla též zahájena terapie baklofenem a intenzivní fyzioterapie.
Během pokračující hospitalizace došlo k dalšímu významnému zlepšení klinického stavu, včetně normalizace stavu vědomí a korekce arteriální hypertenze. Kontrolní EEG nález odpovídal věku. Vyšetření anti-NMDAR protilátek v séru bylo po dvou měsících od vzniku onemocnění negativní. Pacient byl ponechán na perorální kortikoterapii s postupnou deeskalací dávky a na opakovaném podání intravenózních imunoglobulinů v měsíčních intervalech. Akutálně u pacienta přetrvává v behaviorálním projevu emoční labilita, pohotovost k afektivním výkyvům s negativismem, iritabilita, sociální dezinhibice, v kognitivním profilu pak převažně mnestický a exekutivní deficit, avšak pozvolně se upravující.
DISKUSE
Anti-NMDAR encefalitida je charakteristická psychiatrickou symptomatologií, která mívá subakutní rozvoj (v rámci 4–10 týdnů) od úzkosti, agitovanosti, dezorientace a poruch chování a spánku po nástup příznaků připomínajících psychotické onemocnění (sluchové i zrakové halucinace a bludy). Často bývají popisovány i nespecifické „chřipkovité“ příznaky, posléze se přidávají poruchy paměti, poruchy řeči (redukovaný řečový projev, mutismus, echolálie), epileptické záchvaty (ve formě generalizovaných tonicko-klonických či fokálních záchvatů s poruchou vědomí) a extrapyramidová symptomatika (facio-brachiální dystonie). Onemocnění v těžších případech progreduje do kvantitativní poruchy vědomí (stupor s katatonními rysy), časté jsou též projevy autonomní dysfunkce [4].
Patofyziologickým podkladem je vznik autoprotilátek proti NMDA receptorům mozku, které umožňují excitační neurotransmisi a podílejí se na plasticitě mozku a procesech paměti a učení. Nejvyšší denzita těchto receptorů je v amygdale, prefrontálním kortexu, hipokampu a hypotalamu. Snížení počtu povrchových receptorů je reverzibilní a závislé na titru NMDA protilátek. Protilátky mohou být vytvářeny v rámci zkřížené reaktivity proti nádorovým buňkám teratomu či jiného nádoru, který obsahuje různorodou tkáň včetně nervových buněk [2, 4]. Spouštěcí moment tvorby autoprotilátek u neparaneoplastických případů není zatím objasněn.
Diagnóza anti-NMDAR encefalitidy spočívá v průkazu specifických autoprotilátek imunofluorescenční metodou, a to jak ze séra, tak i likvoru. Senzitivita testování je však v likvoru vyšší. Dynamika titrů protilátek může sledovat klinický průběh onemocnění včetně relapsů, avšak pozitivita protilátek v séru i likvoru může přetrvávat roky po prodělaném onemocnění již u asymptomatických pacientů. Zánětlivý obraz mozkomíšního moku je přítomen u cca 95 %, obvykle v podobě lymfo-monocytární pleiocytózy [3].
V rámci diferenciální diagnostiky je indikováno zobrazení mozku. CT je však často negativní, MRI prokáže abnormní nálezy až u poloviny pacientů – kortikální hyperintenzity v oblasti mediálních temporálních laloků nebo subkortikálních struktur (hipokampus, bazální ganglia). Abnormální EEG záznam je přítomen u většiny pacientů. Nálezy bývají často nespecifické, s generalizovaným nebo lokalizovaným zpomalením a abnormální organizací základní aktivity. Normalizace EEG záznamu pak koreluje i se zlepšením klinického stavu. U každého pacienta s podezřením na anti-NMDAR encefalitidu je nutné provést kompletní onkologický screening. Nádor se u dospělých pacientů nalezne asi v polovině případů, v opačném případě by i přesto měli tito pacienti zůstat ve sledování [6].
V terapii je potřebné brát v úvahu věk pacienta, přítomnost či absenci nádoru a závažnost projevů. Základem terapie anti-NMDAR encefalitidy je případné odstranění nádoru a imunoterapie ve formě pulzů intravenózních kortikoidů (20–30 mg/kg/den, maximálně 1 g/den) podaných pět za sebou následujících dní, souběžně se zahájením plazmaferézy (pět až sedm cyklů) a/nebo podání imunoglobulinů (0,4 g/kg/den na pět dní). Při nedostatečném efektu léčby je pak v druhé linii indikováno podání rituximabu (schéma 375 mg/m2 týdně po dobu čtyř týdnů nebo 1 g dvakrát s odstupem dvou týdnů) nebo cyklofosfamidu (750 mg/m2 s možností měsíčního opakování při celkové délce léčby čtyři až šest měsíců dle stavu) [7, 8]. U těžších případů je nutná komplexní intenzivní péče zahrnující v případě nutnosti i umělou plicní ventilaci [6].
U výše prezentovaného pacienta lze vzhledem ke klinickým projevům charakteru horeček, poruchy vědomí, autonomní nestability, leukocytózy a elevace svalových parametrů (CK a myoglobinu) stav hodnotit jako kombinaci anti-NMDAR encefalitidy s velmi suspektním NMS. Spouštěčem byl pravděpodobně haloperidol-dekanoát opakovaně podávaný v úvodu onemocnění. NMS představuje antipsychotiky navozený život ohrožující stav, pro který je typická horečka, svalová rigidita, delirium a dysregulace autonomního nervového systému. Právě haloperidol je popisován jako nejčastější spouštěcí psychofarmakum [8]. Pro diagnostiku je nejdůležitější farmakologická anamnéza a laboratorní průkaz rabdomyolýzy s dominující elevací CK. Na druhou stranu, tzv. NMS-like syndrom bývá někdy považován za možný fenotypický projev anti-NMDAR encefalitidy.
ZÁVĚR
V této kazuistice předkládáme případ pacienta s autoimunitní encefalitidou s pozitivitou protilátek proti N-metyl-D-aspartát receptorům, který poukazuje na několik aspektů: (1) Autoimunitní encefalitidy by měly být zahrnuty do diferenciální diagnostiky u pacienta s nově zjištěnou psychózou. (2) Je potřeba myslet na paraneoplastickou etiologii a pátrat po možné nádorové příčině. (3) Prognóza autoimunitní encefalitidy je zásadně ovlivněna včasným stanovením diagnózy a zahájením adekvátní terapie. (4) Multioborová spolupráce mezi pediatrem, neurologem, intenzivistou, radiologem a psychiatrem je u takového pacienta v rámci diagnostického a léčebného procesu nezbytná.
Došlo: 28. 2. 2020
Přijato: 1. 7. 2020
Korespondující autor:
MUDr. Jan David, Ph.D.
Pediatrická klinika 2. LF UK
a FN Motol
V Úvalu 84
150 06 Praha
e-mail: jan.david@fnmotol.cz
Zdroje
1. Krýsl D, Marusič P. Autoimunitní limbické encefalitidy. Neurol Praxi 2012; 13 (3): 160–164.
2. Krýsl D, Elišák M. Autoimunitní encefalitidy. Cesk Slov Neurol N 2015; 78 (1): 7–23.
3. Dalmau J, Gleichman AJ, Hughes EG, et al. Anti-NMDA-receptor encephalitis: case series and analysis of the effects of antibodies. Lancet Neurol 2008; 7 : 1091–1098.
4. Kučerová J, Vališ M, Masopust J. Encefalitida s protilátkami proti NMDA receptorům. Cesk Slov Psychiatr 2014; 110 (5): 272–277.
5. Dalmau J, Rodenfeld M. Paraneoplastic and autoimmune encefalitis. Up to date 2020. http://www.uptodate.com.
6. Mikolášek P, Aulická Š, Homola L, et al. Anti-NMDAR encefalitida v dětském věku – kazuistika. Cesk Slov Neurol N 2017; 113 (2): 224–227.
7. Jakubčiaková V, Slonková J. Autoimunitní encefalitidy – kazuistiky. Cesk Slov Neurol N 2016; 79/112 (6): 707–714.
8. Češková E, Ustohal L. Neuroleptický maligní syndrom, přehledový článek a kazuistiky. Cesk Slov Psychiat 2019; 115 (1): 27–31.
Štítky
Neonatologie Pediatrie Praktické lékařství pro děti a dorost
Článek List redakcii
Článek vyšel v časopiseČesko-slovenská pediatrie
Nejčtenější tento týden
2020 Číslo 8- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- MUDr. Jiří Kornoušek: Program našich konferencí stavíme tak, aby reflektoval skutečně aktuální a praktická témata
- Aktuální postupy a role praktického lékaře v péči o pacienty s CHOPN
- Přínos perorálního semaglutidu pro pacienty s DM 2. typu v ordinaci praktického lékaře
-
Všechny články tohoto čísla
- Novorozenci matek s nemocí COVID-19 v České republice v průběhu první vlny pandemie (1. 3.–31. 8. 2020)
- Kumulativní efekt sociálních rizikových faktorů u kojenců zemřelých udušením
- Adherence u adolescentů s chronickým selháním ledvin a po transplantaci ledviny
- Závažný průběh autoimunitní encefalitidy u sedmnáctiletého chlapce
- Podání eculizumabu u dětského pacienta s hemolyticko-uremickým syndromem asociovaným s infekcí Escherichia coli
- Screening poruch jazykového vývoje v raném věku: přehled a představení dotazníku SDDS
- Spektrum autodestruktivního chování v adolescenci
- Zemřel prof. MUDr. František Stožický, DrSc.
- Zomrel doc. MUDr. Pavol Sýkora, CSc.
- List redakcii
- CENY PŘEDSEDNICTVA ČLS JEP ZA NEJLEPŠÍ VĚDECKÉ PUBLIKACE VYDANÉ V ROCE 2019
- OCENĚNÍ NEJLEPŠÍCH PRACÍ PUBLIKOVANÝCH V IMPAKTOVANÝCH ČASOPISECH V ROCE 2019
- Česko-slovenská pediatrie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Závažný průběh autoimunitní encefalitidy u sedmnáctiletého chlapce
- Screening poruch jazykového vývoje v raném věku: přehled a představení dotazníku SDDS
- Spektrum autodestruktivního chování v adolescenci
- Novorozenci matek s nemocí COVID-19 v České republice v průběhu první vlny pandemie (1. 3.–31. 8. 2020)
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



