-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaHormonálně senzitivní karcinom prostaty
Hormone sensitive prostate cancer
Prostate cancer is the second most common cancer in men worldwide and its incidence rises with age. Although most cases of prostate cancer are diagnosed and treated in early stage of disease, almost 10 % of patients have evidence of metastatic prostate cancer at presentation, and others develop disseminated disease after their definitive treatment. Contemporary research has led to the development of multiple active treatment modalities for men with advanced disease including combination of docetaxel or abiraterone with androgen deprivation therapy.
Keywords:
prostate cancer – androgen deprivation therapy – docetaxel – abiraterone
Autoři: Nikol Rušarová 1,2; Marie Bartoušková 1; Hana Študentová 1
Působiště autorů: Onkologická klinika, Fakultní nemocnice v Olomouci 1; Lékařská fakulta, Univerzita Palackého v Olomouci 2
Vyšlo v časopise: Ces Urol 2019; 23(4): 309-315
Kategorie: Přehledový článek
Souhrn
Karcinom prostaty patří celosvětově mezi druhé nejčastější onemocnění postihující muže a jeho incidence stoupá s věkem. Přestože je u většiny pacientů onemocnění diagnostikováno a léčeno v časných stadiích, přibližně 10 % pacientů stále přichází již v metastatickém stadiu nemoci a část pacientů po lokoregionální terapii dospěje k relapsu. Současný výzkum vedl k rozvoji více léčebných modalit pro muže s pokročilým hormonálně senzitivním onemocněním, zahrnující kombinaci docetaxelu nebo abirateronu s androgen deprivační terapií.
Klíčová slova:
karcinom prostaty – androgen- deprivační terapie – docetaxel – abirateron
ÚVOD
Karcinom prostaty patří mezi druhé nejčastější nádorové onemocnění postihující muže. V roce 2016 byla incidence karcinomu prostaty v České republice 141/100 000 mužů a mortalita v témže roce 30/100 000 mužů (1). V posledních několika letech lze pozorovat trend poklesu mortality a zvyšování incidence. Díky dostupnosti stanovení hladin PSA, možnostem léčby a průběhu se může karcinom prostaty řadit mezi chronická onemocnění. Klíčovým momentem v léčbě byl v roce 1941 objev Charlese Hugginse a Clarence Hodgese, kteří zjistili klíčovou souvislost mezi androgeny, bilaterální orchiektomií a později estrogenovou kastrací v léčbě karcinomu prostaty a v roce 1966 byl Charles Huggins za tento objev oceněn Nobelovou cenou (2, 3). Délka léčebné odpovědi na ADT je velmi variabilní a přibližně u 10–20 % pacientů během pěti let sledování dojde k progresi onemocnění do kastračně rezistentní fáze (4). V poslední době se v léčbě karcinomu prostaty změnilo mnohé. Může se zdát, že větší rozvoj se odehrál v léčbě CRPC, neboť nyní je k dispozici hned několik nových molekul, které rozšířily armamentárium léčebného ovlivnění této fáze onemocnění. Avšak pro hormonálně senzitivní onemocnění do nedávné doby byla jedinou možností androgen-deprivační terapie.
HORMONÁLNÍ LÉČBA
Karcinom prostaty patří mezi onemocnění, na jehož růstu se podílejí hormony a je tudíž ovlivnitelné hormonálními manipulacemi. Základním hormonem ovlivňujícím růst nádorových buněk prostaty je testosteron, který v téměř 90 % produkují Leydigovy buňky varlete. Minoritním podílem je testosteron produkován v kůře nadledvin (asi 5 %) a dále vzniká v periferní tukové tkáni konverzí z estradiolu. Vlastním účinným androgenem je dihydrotestosteron (DHT) vznikající z testosteronu působením enzymu 5α - reduktázy (5). V mnoha případech je jediným projevem metastatického rozsevu nemoci vzestup PSA. Ve většině případů platí, že karcinom prostaty, který dosud nebyl systémově léčený, je závislý na přítomnosti androgenů. Nedílnou součástí přístupu k systémové léčbě karcinomu prostaty je tedy snižování hladin testosteronu pomocí ADT či orchiektomií (OE). Stanovení hladin PSA v séru je nejjednodušší metoda monitorace od povědi na systémovou léčbu. Zahájení hormonální terapie je u pacientů individuální a řídí se přítomností symptomů, hodnotou PSA, stagingem a gradingem onemocnění. U pacientů se symptomatickým onemocněním by měla být ADT zahájena spíše dříve nežli později, naopak u pacientů s asymptomatickým onemocněním lze s léčbou vyčkat, neboť léčba by mohla negativně ovlivnit kvalitu života.
KOMBINOVANÁ TERAPIE V LÉČBĚ MHSPC
Přestože většina pacientů zpočátku velmi dobře reaguje na ADT, doba trvání léčby je omezená a u všech pacientů dojde k progresi onemocnění do kastračně rezistentní fáze. V poslední době prokázalo mnoho látek účinnost v léčbě CRPC, a proto se začaly tyto látky používat v léčbě mHSPC s potenciálním cílem zpomalit progresi onemocnění a zlepšit kvalitu života. Rezistence na ADT je do jisté míry zapříčiněna reaktivací androgenního receptoru v perzistující adrenální produkci androgenů, zvýšením intratumorózní produkce testosteronu a modifikací biologické charakteristiky androgenních receptorů.
Kombinace ADT s docetaxelem
Kombinace ADT s docetaxelem může poskytnout významné výhody u vybraných pacientů s metastatickým karcinomem prostaty. Docetaxel je standardně podáván v dávce 75 mg/m2 à tři týdny v léčbě metastatického kastračně rezistentního karcinomu prostaty (CRPC) již od roku 2004 (6, 7). První studií zkoumající přínos přidání docetaxelu k ADT byla studie GETUG-AFU 15, ve které bylo zařazeno necelých 400 pacientů s de novo diagnostikovaným CP nebo s CP po primární léčbě. Po mediánu sledování 50 měsíců byl OS prodloužen v rameni s kombinovanou terapií, nicméně nebylo dosaženo statistické významnosti (medián 58,9 měsíce vs. 54,2 měsíce, HR 1,01, 95 % CI 0,75–1,36, p = 0,955), lze tedy předpokládat, že soubor těchto pacientů byl poměrně malý (8).
Přínos kombinované terapie (ADT + docetaxel) byl poprvé prokázán u pacientů s vysokým podílem nemoci (high - volume disease), jak bylo definováno ve studii CHAARTED (přítomnost viscerálních metastáz a/nebo čtyř kostních metastáz, přičemž alespoň jedna z nich je umístěna mimo axiální skelet). Výsledky studie CHAARTED vzbudily velký rozruch. Toto tvrzení potvrdila později studie STAMPEDE. Ve studii CHAARTED bylo zařazeno 790 mužů s primárně diagnostikovaným CP, medián věku byl 64 let v kombinované skupině a 63 let v rameni s ADT, 65 % pacientů mělo high-volume disease. Pacienti byli léčeni kombinovanou terapií (ADT + docetaxel v dávce 75 mg/ m2 á tři týdny, šest cyklů, bez prednisonu) nebo samotnou ADT. Po mediánu sledování 28,9 měsíců se prokázalo, že kombinovaná terapie dosahuje o 13,6 měsíce delšího OS ve srovnání s ADT samotnou (57,6 měsíce vs. 44,0 měsíce, HR 0,61, 95 % CI 0,47–0,80, p < 0,001, graf 1). Průměrná doba do vývoje kastračně rezistentní formy onemocnění byla delší o 8,5 měsíce při kombinované terapii (20,2 měsíce vs. 11,7 měsíce, HR 0,61, 95 % CI 0,51–0,72, p < 0,001) a doba do klinické progrese byla prodloužena o 13,2 měsíce (HR 0,61, 95 % CI 0,50–0,75, p < 0,001). Z nežádoucích účinků se častěji při léčbě ADT a docetaxelem vyskytla febrilní neutropenie (6,1 % pacientů, tab. 1). Ohromný benefit z kombinované léčby docetaxelu s ADT ve smyslu významného prodloužení OS vedl k přepsání guidelines. Je doporučováno začínat s chemoterapií nejdříve po čtyřech měsících od zahájení ADT. Pacienti začínající s chemoterapií dříve než jeden měsíc od zahájení ADT měli častější výskyt nežádoucích účinků (9).
Tab. 1. Přehled nežádoucích účinků při léčbě ADT + docetaxel, studie CHAARTED
Tab. 1. Summary of side effects of treatment with ADT + docetaxel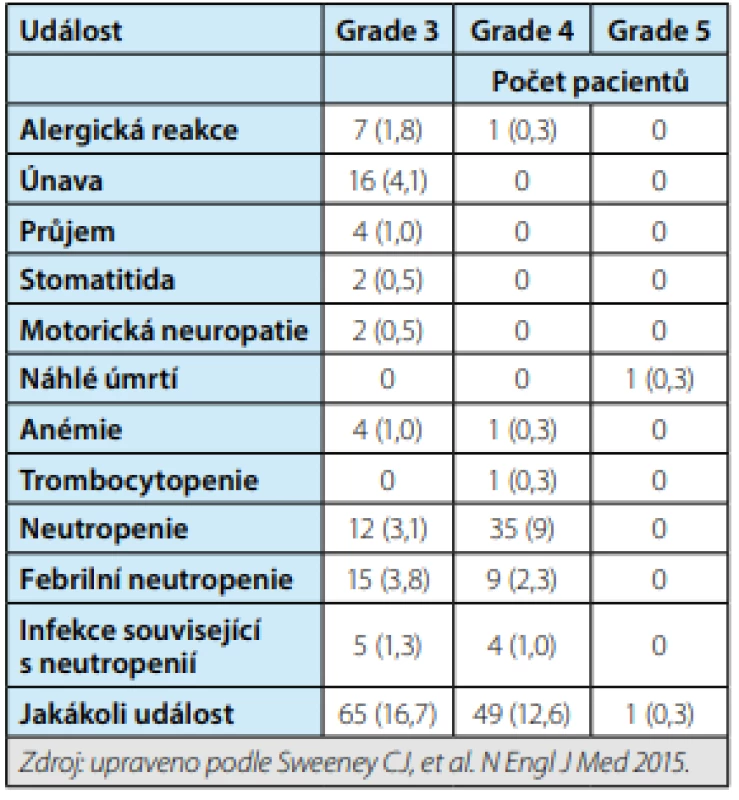
Graf 1. Kaplan-Meierova křivka celkového přežití u všech pacientů (CHAARTED)
Grapf 1. Kaplan-Meier estimate of overall survival – all pacient (CHAARTED trial)
Při následné analýze po 54 měsících bylo potvrzeno významné prodloužení OS u všech pacientů (medián 58 měsíců vs. 47 měsíců, HR 0,72, 95 % CI 0,59–0,89). Dále u 513 pacientů s high-volume disease byl prodloužen OS o celých 17 měsíců (49,2 měsíců vs. 32,2 měsíců, HR 0,60, 95 % CI 0,45–0,81, graf 2), na rozdíl u pacientů s low-volume disease, kde tento signifikantně významný rozdíl v OS prokázán nebyl (graf 3) (10).
Graf 2. Kaplan-Meierova křivka celkového přežití u pacientů s high-volume disease CHAARTED
Grapf 2. Kaplan-Meier estimate of overall survival – patients with high-volume disease (CHAARTED trial)
Graf 3. Kaplan-Meierova křivka přežití u pacientů s low-volume disease, CHAARTED
Grapf 3. Kaplan-Meier estimate of overall survival – patients with low-volume disease (CHAARTED trial)
Výsledky studie CHAARTED byly potvrzeny až studií STAMPEDE. Studie STAMPEDE je čtyřramenná studie porovnávající u 2 962 pacientů standardní léčbu HSPC s přidáním docetaxelu a kyseliny zoledronové. Zařazováni byli pacienti, kteří měli nově diagnostikovaný CP, metastatický či lokálně pokročilý, vysoce rizikový (T3–T4, Gleason skóre 9–10, PSA ≥ 40 ng/ml), nebo CP dříve léčený radikální prostatektomií či radioterapií. V rameni A pacienti dostávali ADT (1 184 pacientů), v rameni B byla ADT kombinovaná s kyselinou zoledronovou (4 mg á tři týdny šest cyklů, poté á čtyři týdny po dobu dvou let, 593 pacientů), ve třetím rameni C byla pacientům podávána ADT s přidáním šesti cyklů docetaxelu ve standardní dávce (75 mg/m2 á tři týdny šest cyklů, 592 pacientů) a v posledním čtvrtém rameni D byla podávána ADT s kyselinou zoledronovou a docetaxelem (593 pacientů). Po mediánu sledování 43 měsíců se opět prokázalo statisticky významné prodloužení mediánu OS (medián OS 81 měsíce pro rameno C vs. 71 měsíce pro rameno A, HR 0,78, 95 % CI 0,66–0,93, p = 0,006) a nebylo prokázáno zlepšení OS při přidání kyseliny zoledronové (medián OS 76 měsíce pro rameno D, HR 0,82, 95 % CI 0,69–0,97, p = 0,022). Významnější byl podíl toxicity u kombinované terapie (ADT + docetaxel 52 % vs. 32 % pro ADT samotné) (11). Docetaxel je poměrně výrazně toxické cytostatikum a vzhledem k populaci léčených pacientů (většinou starší muži s nezanedbatelnými komorbiditami) se může zdát docetaxel poněkud toxičtější variantou při výběru kombinované terapie. Největší prospěch z léčby docetaxelem měli pacienti s high-volume disase.
Kombinace ADT s abirateronem
Bylo prokázáno, že abirateron v kombinaci s prednisonem významně prodlužuje přežití u pacientů s metastatickým kastračně rezistentním karcinomem prostaty, kteří nebyli léčeni chemoterapií a u pacientů předléčených docetaxelem (12, 13). Standardní androgen-deprivační terapie byla také kombinována s abirateronem u mHSPC. Abirateron ireverzibilně inhibuje CYP 17, čímž dochází k blokování tvorby testosteronu jak v nadledvinách, tak ve varlatech a také v tumoru. Při blokování CYP 17 dochází rapidně k poklesu kortizolu s následným zvýšením ACTH, což může vést k projevům hypertenze a hypokalemie jako dvou nejčastějších nežádoucích účinků abirateronu. Z těchto důvodů se abirateron užívá v kombinaci s prednisonem, který zpětnou vazbou blokuje pokles kortizolu a ke zvýšení ACTH tedy nedochází. Přelomovým pro tuto kombinaci v indikaci mHSPC byl rok 2017, kdy byly na celosvětovém kongresu ASCO (American Society of Clinical Oncology) prezentovány a současně v prestižních časopisech publikovány výsledky studií LATITUDE a STAMPEDE, které prokázaly významný vliv na celkové přežití při přidání abirateronu k ADT.
V randomizované dvojitě zaslepené placebem kontrolované studii fáze III LATITUDE bylo 1 199 pacientů s nově diagnostikovaným HSPC náhodně přiděleno k podávání ADT + placeba či ADT + abirateronu (1 000 mg/den + prednison 5 mg/ den). Pacienti zařazeni do této studie měli vysoce rizikové onemocnění s přítomností nejméně dvou ze tří parametrů – Gleason skóre 8 nebo vyšší, alespoň tři kostní léze a měřitelné viscerální metastázy. Po mediánu sledování 30,4 měsíce (při plánované průběžné analýze, po 406 úmrtích) bylo prokázáno signifikantně významné prodloužení OS ve prospěch kombinované terapie. Medián OS nebyl v kombinované skupině dosažen, při terapii ADT byl medián OS 34,7 měsíce (HR 0,62, 95 % CI 0,51–0,76, p < 0,001, graf 4). Mimo prodloužení OS bylo také prokázáno zlepšení v přežití bez progrese (Progression - Free Survival – PFS) při přidání abirateronu k ADT, tedy o 53 % nižší relativní riziko radiografické progrese nebo úmrtí (medián 33,0 měsíce vs. 14,8 měsíce, HR 0,47, 95 % CI 0,39–0,55, p < 0,001, graf 5). Přidání abirateronu k ADT vede také ke snížení relativního rizika úmrtí o 38 %. Podobný stupeň přínosu byl zaznamenán i v sekundárních cílech (doba do progrese bolestí, doba do progrese PSA, doba do výskytu symptomatické kostní události, doba do zahájení chemoterapie), což přineslo významné zlepšení symptomů a zejména kvality života (14).
Graf 4. Kaplan-Meierova křivka celkového přežití, (LATITUDE)
Grapf 4. Kaplan-Meier estimate of overall survival (LATITUDE trial)
Graf 5. Kaplan-Meierova křivka doby progrese (LATITUDE)
Grapf 5. Kaplan-Meier estimate of progression-free surival (LATITUDE trial)
Druhou studií byla STAMPEDE, která randomizovala 1 917 mužů k podávání ADT v kombinaci s abirateronem. Populace pacientů ve studii byla heterogenní a zahrnovala pacienty jak s nově diagnostikovaným vysoce rizikovým karcinomem pro staty (94,9 % pacientů), tak pacienty s recidivou po radikální prostatektomii nebo radikální radioterapii (5,1 % pacientů). Medián sledování byl 40 měsíců se 184 úmrtími v kombinované skupině a 262 úmrtími ve skupině se samotnou ADT. Primárním cílem studie bylo OS, které bylo významně prodlouženo u kombinované terapie (třileté přežití 83 % vs. 76 %, HR 0,63, 95 % CI 0,52–0,76) (15). Z výsledků studií LATITUDE a STAMPEDE, které prokázaly významný vliv na OS při přidání abirateronu k ADT vyvstává otázka, jaká kombinovaná terapie by měla být považována za standardní léčbu. Abirateron má lepší profil nežádoucích účinků než docetaxel a je logisticky lepší pro svou perorální lékovou formu. Naopak doba trvání léčby abirateronem je delší, z čehož vyplývají dlouhodobé nežádoucí účinky glukokortikoidů (při nutnosti podávání prednisonu s abirateronem).
SOUČASNOST A BLÍZKÁ BUDOUCNOST
V současné době je v běhu několik klinických studií u pacientů s HSPC, které porovnávají ADT s přidáním enzalutamidu či apalutamidu. Za zmínku stojí studie ARCHES (NCT02677896), jejímž účelem je zhodnotit účinnost standardní ADT s přidáním enzalutamidu, primárním cílem bude radiografické PFS. Další v řadě probíhajících studií je studie ENZAMET (NCT02446405), která srovnává účinnost enzalutamidu s ADT oproti nesteroidnímu antiandgrogenu + ADT, primárním cílem bude OS. Ve studii TITAN (NCT02489318) je zkoumáno, zdali má přidání apalutamidu k ADT má vliv na prodloužení celkového přežití nebo doby do radiografické progrese. V rámci studie STAMPEDE probíhá v rameni J analýza s přidáním enzalutamidu ke kombinaci ADT s abirateronem, primárním cílem je OS. Probíhá i klinická studie PEACE-1 (NCT01957436), v této klinické studii jsou pacienti randomizováni do ramene A (ADT + docetaxel), ramene B (ADT + docetaxel + abirateron), do ramene C (ADT + docetaxel + lokální radioterapie) anebo do ramene D (ADT + docetaxel + abirateron + lokální radioterapie). Nicméně na výsledky těchto studií si prozatím budeme muset počkat (16).
ZÁVĚR
Díky velmi pozitivním výsledkům klinických studií (statisticky významné prodloužení OS) lze v současnosti považovat za nový standard léčby kombinovanou terapii ADT s docetaxelem či abirateronem, což je i součástí doporučení EAU a ESMO guidelines. Bohužel v České republice se prozatím jedná o off-label indikaci. Abirateron u nás má indikaci v léčbě vysoce rizikového metastatického HSPC, avšak úhrada v této indikaci k současnému datu nebyla plátci veřejného zdravotnictví stanovena. Podle současné úhradové vyhlášky je abirateron hrazen u pacientů s metastatickým kastračně rezistentním CP v kombinaci s prednisonem dříve léčených docetaxelem, nebo u asymptomatických či mírně symptomatických pacientů s metastatickým kastračně rezistentním karcinomem prostaty po selhání ADT před zahájením chemoterapie. Vzhledem k omezením úhradovými vyhláškami patří v České republice ke standardní a dostupné léčbě mHSPC stále pouze androgen-deprivační terapie.
Došlo: 24. 2. 2019
Přijato: 19. 5. 2019
Kontaktní adresa:
MUDr. Nikol Rušarová
Onkologická klinika,
Fakultní nemocnice v Olomouci
I. P. Pavlova 6,
779 00 Olomouc
e-mail: nikol.rusarova@fnol.cz
Střet zájmů: Žádný.
Prohlášení o podpoře: Tato práce vznikla za podpory grantového projektu Univerzity Palackého v Olomouci č. IGA_LF_2018_010.
Zdroje
1. Dušek L, Mužík J, Kubásek M, et al. Epidemiologie zhoubných nádorů v České republice [on - line]. Masarykova univerzita [2005] [cit. 2018–12–28]. Dostupný z URL: http://www.svod.cz.
2. Huggins C, Hodges CV. Studies on prostatic cancer: I. The effects of castration, of estrogen, and of androgen injection on serum phosphatases in metastatic carcinoma of the prostate. Cancer Res 1941; 1 : 293–297.
3. Huggins C, Stevens J, Hodges CV. Studies on prostatic cancer: II. The effects of castration on advanced carcinoma of the prostate gland. Arch Surg 1941; 43 : 209–223.
4. Kirby M, Hirst C, Crawford ED. Characterising the castration - resistant prostate cancer population: a systemic review. Int J Clin Pract. 2011; 65(11): 1180–1192.
5. Isaacs JT. The biology of hormone refraktory prostate cancer. Why does it develop? Clin North Am 1999; 26 : 263–273.
6. Petrylak DP, Tangen CM, Hussain MHA, et al. Docetaxel and estramustine compared with mitoxantrone and prednisone for advanced refractory prostate cancer. N Engl J Med 2004; 351(15): 1502–1512.
7. Berthold DR, Pond GR, Soban F, et al. Docetaxel plus prednisone or mitoxantrone plus prednisone for advanced prostate cancer: updated survival in the TAX 327 study. J Clin Oncol. 2008; 26(2): 242–245.
8. Gravis G, Fizazi K, Joly F, et al. Androgen - deprivation therapy alone or with docetaxel in non - castrate metastatic prostate cancer (GETUG - AFU 15): a randomised, open - label, phase 3 trial. Lancet Oncol 2013; 14(2): 149–158.
9. Sweeney CJ, Chen YH, Carducci M, et al. Chemohormonal Therapy in Metastatic Hormone -Sensitive Prostate Cancer. N Engl J Med 2015; 373(8): 737–746.
10. Kyriakopoulos CE, Chen YH, Carducci MA, et al. Chemohormonal Therapy in Metastatic Hormone-Sensitive Prostate Cancer: Long - Term Survival Analysis of the Randomized Phase III E3805 CHAARTED Trial. J Clin Oncol 2018; 36(11): 1080–1087.
11. James ND, Sydes MR, Clarke NW, et al. Addition of docetaxel, zoledronic acid, or both to first - line long - term hormone therapy in prostate cancer (STAMPEDE): survival results from an adaptive, multiarm, multistage, platform randomised controlled trial. Lancet 2016; 387(10024): 1163–1177.
12. Ryan CJ, Smith MR, Fizazi K, et al. Abiraterone acetate plus prednisone versus placebo plus prednisone in chemotherapy - naive men with metastatic castration - resistant prostate cancer (COU - AA-302): final overall survival analysis of a randomised, double - blind, placebo - controlled phase 3 study. Lancet Oncol 2015; 16 : 152–160.
13. Fizazi K, Scher HI, Molina A, et al. Abiraterone acetate for treatment of metastatic castration - resistant prostate cancer: fi nal overall survival analysis of the COU - AA-301 randomised, double - blind, placebo-controlled phase 3 study. Lancet Oncol. 2012; 13(10): 983–992.
14. Fizazi K, Tran N, Fein L, et al. Abiraterone plus Prednisone in Metastatic, Castration - Sensitive Prostate Cancer. N Engl J Med 2017; 377(4): 352–360.
15. James ND, de Bono JS, Spears MR, et al. Abiraterone for Prostate Cancer Not Previously Treated with Hormone Therapy. N Engl J Med 2017; 377(4): 338–351.
16. U.S. National Institutes of Health [online]. Home – ClinicalTrials.gov. [cit. 2018–12-20]. Dostupné z: https://clinicaltrials.gov/.
Štítky
Dětská urologie Nefrologie Urologie
Článek vyšel v časopiseČeská urologie
Nejčtenější tento týden
2019 Číslo 4- Inkontinence ovlivňuje duševní stav nemocného – nabízejte aktivně pomoc
- Na inkontinenční pomůcky nově dosáhne více pacientů
- Pacient se bude cítit komfortně pouze při správně zvolené absorpční pomůcce
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Probiotika snižují riziko průjmu spojeného s podáváním antibiotik
-
Všechny články tohoto čísla
- Editorial
- Laparoskopická transperitoneální rekonstrukce symptomatického retrokaválního močovodu - kazuistika
- Urogenitální tuberkulóza
- Hormonálně senzitivní karcinom prostaty
- Prevalence uropatogenů v moči a spektrum jejich rezistence – analýza dat z jednoho pracoviště
- Porovnání měření velikosti prostaty pomocí transrektálního ultrazvuku a magnetické rezonance a jejich vlivu na PSA denzitu
- Plastika tříselné kýly a laparoskopická radikální extraperitoneální prostatektomie
- Radiologická regrese metastatického renálního karcinomu po biologické léčbě sunitinibem – kazuistika a přehled literatury
- Emfyzematózní cystitida u 78leté ženy
- Možnost roboticky asistované augmentace močového měchýře typu „Patch“ pomocí daVinci XI®
- Zpráva z konání 17th European Urology Residents Education Programme (EUREP)
- V Praze je blaze aneb ohlédnutí za 65. ročníkem výroční konference ČUS
- Výsledky soutěže ČUS o nejlepší vědeckou publikaci za rok 2018
- Česká urologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Porovnání měření velikosti prostaty pomocí transrektálního ultrazvuku a magnetické rezonance a jejich vlivu na PSA denzitu
- Plastika tříselné kýly a laparoskopická radikální extraperitoneální prostatektomie
- Emfyzematózní cystitida u 78leté ženy
- Hormonálně senzitivní karcinom prostaty
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



