-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaVyplatí se bezpečná farmakoterapie?
Is safe pharmacotherapy worthwhile?
The safety of pharmacotherapy can be monitored at different levels of the health system and the quality of health care provided can be assessed from different points of view. The Ministry of Health, the health insurance companies, the State Institute for Drug Control, the Institute of Health Information and Statistics, and the health care facilities themselves fulfill their roles. Safety is assessed differently at each level. Based on current knowledge, it follows that the monitoring of adverse effects is not only of safety but also of economic importance for health care facilities. At this point the proactive way of working of clinical pharmacist can play a major role specifically when they get involved in direct care of the patient.
Keywords:
clinical pharmacist – safety of pharmacotherapy – Adverse reactions
Autoři: Kateřina Langmaierová 1,3; Jana Gregorová 2,3
Působiště autorů: Oddělení klinické farmacie, Krajská zdravotní, a. s., Ústí nad Labem, pracoviště Teplice 1; Oddělení klinické farmacie, Nemocnice Na Bulovce, Praha 2; Ústav aplikované farmacie, Farmaceutická fakulta VFU, Brno 3
Vyšlo v časopise: Čas. Lék. čes. 2019; 158: 270-272
Kategorie: Přehledový článek
Souhrn
Bezpečnost farmakoterapie může být sledována na různých úrovních zdravotního systému a kvalitu poskytované zdravotní péče je možné posuzovat z různých úhlů pohledu. Svou roli plní ministerstvo zdravotnictví, zdravotní pojišťovny, Státní ústav pro kontrolu léčiv, Ústav zdravotnických informací a statistiky i sama zdravotnická zařízení. Na každé úrovni je bezpečnost hodnocena jiným způsobem. Na základě současných poznatků se ukazuje, že pro zdravotnická zařízení má sledování nežádoucích účinků nejen bezpečnostní, ale i ekonomický význam. A právě v tomto bodě může hrát významnou roli proaktivní způsob práce klinického farmaceuta při jeho zapojení do přímé péče o pacienta.
Klíčová slova:
bezpečnost farmakoterapie – nežádoucí účinky – klinický farmaceut
RESORTNÍ BEZPEČNOSTNÍ CÍLE
Ministerstvo zdravotnictví stanovilo v roce 2012 v rámci resortních bezpečnostních cílů indikátory kvality poskytované zdravotní péče. Jedná se o minimální požadavky pro zajištění kvality poskytovaných zdravotních služeb. Jsou shrnuty ve Věstníku Ministerstva zdravotnictví ČR 5/2012 (1). Pro poskytovatele lůžkové péče platí 7 resortních bezpečnostních cílů (RBC), z nichž pouze jeden je věnován léčivům, konkrétně RBC2 Bezpečnost při používání léčivých přípravků s vyšší mírou rizikovosti. Pro poskytovatele ambulantní péče a zdravotniké záchranné služby platí dva RBC: RBC5 Zavedení optimálních postupů hygieny rukou při poskytování zdravotní péče a RBC7 Bezpečné předávání pacientů (2).
Resortní bezpečnostní cíle v oblasti léčiv se v rámci RBC2 zaměřují na přípravky s vyšší mírou rizikovosti – tedy návykové látky, hepariny, cytostatická léčiva, roztoky elektrolytů (zejména koncentrované roztoky kalia) a inzuliny. K naplnění tohoto cíle je důležité podchytit nejen proces logistiky a správného skladování léčiv, ale také moment preskripce a podání léčiva pacientovi. Bezpečné podání léčiva by se však nemělo týkat jen léčiv s vyšší mírou rizikovosti, nýbrž všech léčiv podávaných pacientovi v rámci jeho hospitalizace.
HODNOCENÍ KVALITY PÉČE
Zákonné normy definují rovněž proces externího hodnocení kvality a bezpečí poskytovaných zdravotních služeb. Požadavky na nastavení procesu hodnocení obsahuje § 98 zákona 372/2011 Sb., o poskytování zdravotních služeb (3), a prováděcí vyhláška 102/2012 Sb., o hodnocení kvality a bezpečí zdravotních služeb (4). Tento způsob hodnocení je pro zdravotnická zařízení dobrovolný, hodnocení provádí kompetentní osoba (fyzická či právnická), která získala oprávnění k provádění hodnocení kvality a bezpečí dle zákona č. 372/2011 Sb. (3). Po provedení auditu na základě předem definovaných a známých hodnoticích standardů a definovaných pravidel procesu hodnocení má taková osoba oprávnění vydat certifikát o komplexním hodnocení úrovně poskytovaných zdravotních služeb.
Zdravotní pojišťovna provádí hodnocení kvality poskytované péče v podstatě již v období vytváření smluvního vztahu s poskytovatelem, který musí doložit, že zdravotnické zařízení je řádně personálně i přístrojově vybaveno k poskytování příslušného typu zdravotní péče dle zákona. Z pohledu zdravotní pojišťovny – tedy toku financí z veřejného zdravotního pojištění – má největší význam sledovat péči poskytovanou složkou terapeutickou a diagnostickou, kterou je možné nazývat také složkou procesu vlastního provedení zdravotní péče (5). Jednu z komponent tohoto procesu představuje sledování spotřeb léčiv, jež dává přehled o toku financí vynaložených na terapii v obecném měřítku.
PROCES A ÚROVNĚ MONITOROVÁNÍ
Chyby v preskripci
Z úrovně plátce zdravotní péče je možné sledovat farmakoterapii konkrétního pacienta nebo výběrové skupiny pacientů. Výběr je možné v rámci revizního řízení předem definovat, vlastní hodnocení je pak poměrně časově náročné. Z tohoto důvodu také nebývá systematicky využíváno. V rámci těchto hodnocení je možné sledovat možnou obecnou systematickou chybu větší skupiny předepisujících (např. lékařů určité specializace) – např. neobvyklé kombinace lékových skupin nebo na základě sledování množství definovaných denních dávek neobvykle nižší dávkování některých léčiv, případně potenciálně rizikové lékové kombinace. Nežádoucí účinky či konkrétní manifestaci rizikové kombinace a z toho plynoucí nežádoucí ovlivnění pacienta je možné vysledovat tímto způsobem poměrně obtížně.
Nežádoucí účinky
Státní ústav pro kontrolu léčiv (SÚKL) dává přehled o výskytu nežádoucích účinků v rámci celé populace uživatelů prostřednictvím hlášení o nežádoucích účincích léčiv (6). Sledována jsou oznámení zdravotnických pracovníků, pacientů, ale i držitelů rozhodnutí o registraci a jsou zaměřena na podezření na závažný či neočekávaný nežádoucí účinek léčiva. Systém hlášení je součástí monitoringu, jenž v konečném důsledku dává vznik farmakovigilančnímu signálu, který je pak promítnut do textů, jež doprovázejí léčivý přípravek (SPC) (6). Toto sledování má význam pro globální úroveň bezpečnosti podání léčivého přípravku.
Závady v jakosti
SÚKL jsou hlášeny také informace, jež se vztahují k jakosti léčivého přípravku. Systém je nastaven na vyhodnocení možné závady v jakosti, včetně stanovení míry zdravotního rizika podezřelého léčivého přípravku pro pacienta a v nezbytném případě jsou nastavena opatření k minimalizaci rizika spojeného s používáním léčivého přípravku, včetně včasné informovanosti odborné i laické veřejnosti (6). Hlášení tohoto typu může podat opět farmaceut, lékař i jiný zdravotnický pracovník, ale i pacient. Tato úroveň monitorování má význam pro nastavení globálních opatření nejen na úrovni zdravotnického zařízení, ale i na úrovni výrobce či distributora tak, aby bylo zajištěno podání nezávadné medikace.
Nežádoucí události
Ústav zdravotnických informací a statistiky (ÚZIS) nastavuje systém hlášení nežádoucích událostí, který sleduje různé typy nežádoucích událostí včetně nežádoucích událostí spojených s medikací (7). Do systému jsou hlášeny pouze incidenty vzniklé v souvislosti s procesem podávání léku, nikoli s nežádoucím účinkem či vadnou šarží (v gesci SÚKL), nepředpokládá se tedy duplicita v hlášených událostech. Tato úroveň monitorování má význam pro sledování bezpečného procesu podání na úrovni zdravotnického zařízení. Povinnost sledovat nežádoucích událostí je dána zákonnými normami a zdravotnická zařízení mají vyvinut interní systém jejich sledování a vypořádání.
NÁKLADY SPOJENÉ S NEŽÁDOUCÍMI ÚČINKY LÉČIV
Přímý nežádoucí účinek léčiva může být příčinou neočekávaného zhoršení zdravotního stavu pacienta a může vést k prodloužení jeho hospitalizace. S tím souvisí i nárůst nákladů na poskytnutou péči (manifestace nežádoucím účinkem indukovaných nákladů na zdravotní péči). Analýza nákladů spojených s nežádoucími reakcemi spojenými s léčivy bývá rozdělena na náklady přímé a náklady nepřímé. Oba typy nákladů mohou být sledovány u hospitalizovaných i ambulantních pacientů. Pro jejich sledování však ze studií nevyplývá jednoznačně daná společná metodika.
Poznatky ze studií
Švédská studie Gyllenstenové et al. (8) porovnávala náklady na léčbu dospělých pacientů, kteří sami hlásili nežádoucí příhody, se skupinou dospělých pacientů, kteří je nehlásili.
Polská práce Szkultecké-Debek et al. (9) se zaměřila na analýzu dermatologických nežádoucích příhod spojených s léčbou vybraných onemocnění (revmatoidní artritidy, psoriázy, juvenilní revmatoidní artritidy). Autoři sledovali závažné kožní reakce s častým a velmi častým výskytem – výběr typu nežádoucích příhod byl proveden na základě souhrnu údajů o přípravku podávaných medikamentů. Pro analýzu nebylo podstatné, jaké léčivo bylo podáváno, ale zda manifestované nežádoucí příhody vedly k navýšení nákladů vynaložených pacientem či plátcem zdravotního pojištění v případě hospitalizace spojené s klinickou manifestací nežádoucího efektu (např. léky vyvolaný makulopapulozní exantém, léky vyvolaná toxoalergická dermatitida, alopecie, zhoršené hojení ran v důsledku podávané medikace). Analýza byla provedena s přispěním expertní skupiny dermatologů a z pohledu veřejného plátce. Závěrem hodnocení bylo, že při výskytu nežádoucích příhod dochází k navýšení nákladů na léčbu jak pro pacienta, tak pro zdravotní systém (zdravotní pojišťovny).
Dle práce, kterou publikovali Lagnaoui et al. (10), jsou nežádoucí reakce u hospitalizovaných pacientů očekávatelné – v tomto sledování je uváděna incidence 10,1 na 1000 pacientodnů. V jeho rámci byly vyčísleny náklady spojené s nežádoucími účinky na 11 357 euro na nemocniční lůžko a rok. Byly pozorovány u pacientů v rámci hospitalizace, byly pozorovatelné v okamžiku propouštění pacienta a dále i po jeho propuštění. Část pozorovaných nežádoucích příhod v okamžiku propouštění pak vedla k další hospitalizaci pacienta. Převážně byly povahy neurologické (např. zmatenost, aseptická meningitida, halucinace), kožní, gastrointestinální (průjem, nauzea), případně měly podobu horečky, hypotenze či anafylaktické reakce. Z práce je zřejmé, že je velmi důležité sledovat a průběžně přehodnocovat stav pacienta.
V italské studii FORWARD publikované v roce 2018 (11) se autoři zaměřili rovněž na výskyt nežádoucích reakcí – byly sledovány jak ty, které se objevily v průběhu hospitalizace, tak i ty, jež vedly k příjmu pacienta k hospitalizaci. Spektrum nežádoucích příhod, které byly pozorovány, bylo obdobné jako u výše uvedené francouzské práce. Významným závěrem studie bylo, že se ve většině případů jednalo o nežádoucí reakce, jimž bylo možné předejít.
Sledování nežádoucích účinků léčiv v rámci hospitalizace může mít na základě výše uvedeného dopad nejen na bezpečnost farmakoterapie pacienta, ale i na ekonomiku. Jak ukazují závěry metaanalýzy prospektivních studií z let 1966–1996, jež se zaměřily na výskyt nežádoucích příhod v rámci hospitalizace u pacientů v USA, jejich celkový výskyt dosahoval 6,7 %, z toho 0,32 % bylo označeno jako fatální. V databázové studii se záznamy o více než 8 milionech hospitalizací v USA z roku 1998 dosáhl výskyt nežádoucích příhod u hospitalizovaných pacientů 1,73 %. V dalších publikovaných pracích pohyboval až do 8 %, v závislosti na zemi původu, typu nemocničního oddělení nebo věkové struktuře sledované populace (12).
Systematickou práci klinického farmaceuta dokumentuje publikace Gregorové a kol. − ve zdravotnickém zařízení o cca 1000 lůžkách a 40 tisících příjmech k hospitalizaci za rok sledovali lékové problémy v letech 2016 a 2017, incidence nežádoucích účinků léčiv činila 3,84 % v roce 2016 a 3,22 % v roce 2017 (13, 14). Výsledky sledování (podíl výskytu nežádoucích účinků léčiv) v tomto zdravotnickém zařízení korelují s výsledky zmiňovaných zahraničních prací.
Tab. 1. Výskyt nežádoucích účinků vedoucích k vysazení léčiva nebo k úpravě jeho dávky. Nežádoucí účinky byly identifikovány 5 klinickými farmaceuty v období 2016−2017. 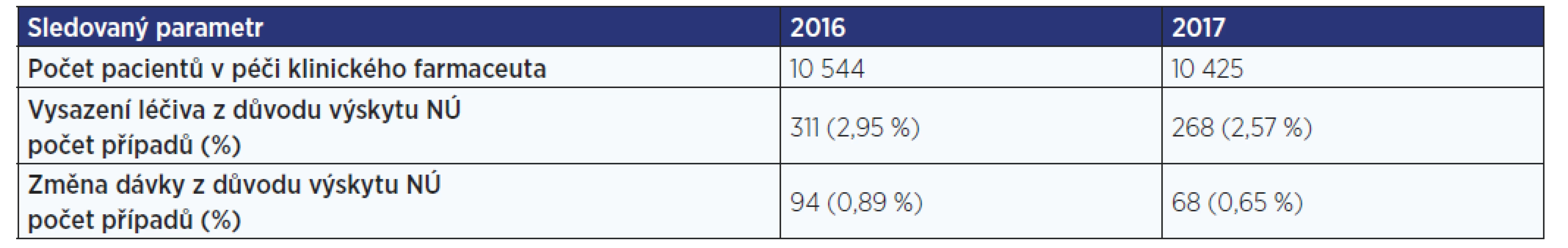
Na základě výše zmíněného se jeví jako účelné sledování nežádoucích účinků léčiv v procesu přímé péče o pacienta. Sledování nežádoucích projevů spojených s medikací má pro zdravotnické zařízení význam jak bezpečnostní, tak i ekonomický.
MOŽNOSTI ZAPOJENÍ KLINICKÉHO FARMACEUTA
V rámci zdravotnických zařízení v ČR se systematicky nežádoucí účinky neevidují a nevyhodnocují (nebo jen výjimečně). Právě v oblasti vyhodnocování nežádoucích účinků léčiv jsou možné dvě úrovně zapojení klinického farmaceuta (tab. 2).
Tab. 2. Úrovně zapojení klinického farmaceuta do sledování nežádoucích účinků 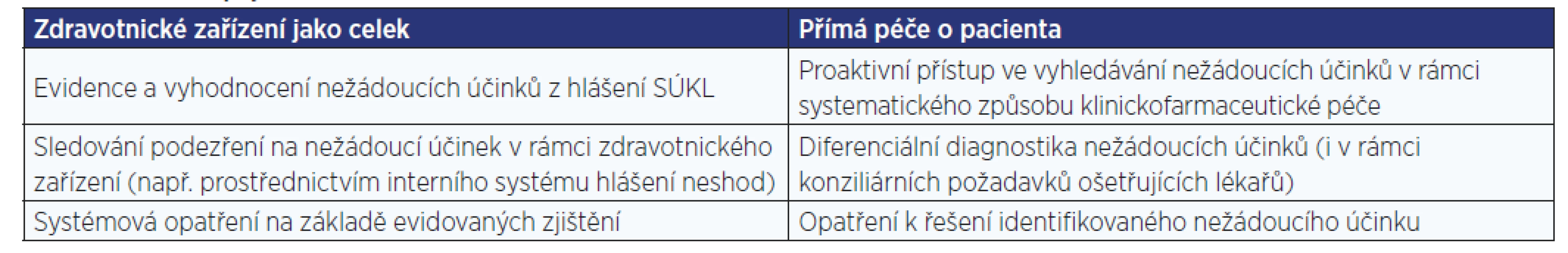
Monitorování nežádoucích příhod u hospitalizovaného pacienta vede k signálu o možném riziku, což dovoluje nastavit preventivní opatření, jež zabrání jeho projevu. Při klinické manifestaci nežádoucího účinku je pak možné nastavit taková opatření, která minimalizují riziko prodloužení hospitalizace právě v důsledku této manifestace. Systematické sledování nežádoucích účinků napříč zdravotnickým zařízením navíc umožňuje záchyt možné systematické chyby v medikačních zvyklostech lékařů (např. management interakčně bohaté medikace).
Klinický farmaceut by měl být do tohoto procesu intenzivně zapojen a měl by mít své pole působnosti v procesu diferenciální diagnostiky nežádoucích účinků léčiv. To umožňuje nastavit včas odpovídající opatření k řešení nežádoucího účinku již projeveného a minimalizovat tak jeho dopad, ale též identifikovat potenciální závažné nežádoucí účinky a předcházet jejich projevu. Tím se může podílet na redukci nákladů na zdravotní péči indukovaných nežádoucím účinkem.
Evidence nežádoucích účinků v rámci zdravotnického zařízení je neméně významná a měla by být v gesci klinického farmaceuta. Pokud se mu podaří dobře nastavit systém jejich sledování, má jedinečnou možnost (vzhledem k zapojení do procesu přímé péče o pacienta v rámci hospitalizace) zasáhnout do procesu medikace a systematickým sledováním farmakoterapie předcházet nežádoucím účinkům nebo nastavit efektivní management nežádoucích účinků již projevených.
Využití služby klinického farmaceuta v rámci našeho zdravotnického systému může při správném metodologicky podloženém způsobu práce podpořit racionalitu pacientovy farmakoterapie, bránit rozvoji preskripčních kaskád, a tím snižovat nežádoucími účinky indukované náklady na poskytnutou péči.
Adresa pro korespondenci:
PharmDr. Kateřina Langmaierová
Oddělení klinické farmacie
Krajská zdravotní, a. s. – Nemocnice Teplice, o. z.
Duchcovská 53, 415 29 Teplice
Tel.: 417 519 675
e-mail: klangmaierova@gmail.com
Zdroje
- Věstník MZ ČR 2012; 5.
- Ministerstvo zdravotnictví ČR. Resortní bezpečnostní cíle. MZ ČR, Praha, 2012.
- Zákon č. 372/2011 Sb., o zdravotních službách a podmínkách jejich poskytování.
- Vyhláška č. 102/2012 Sb., o hodnocení kvality a bezpečí lůžkové zdravotní péče.
- Prokeš M. Hodnocení kvality preskripce. Klinická farmakologie a farmacie 2008; 22 : 118–122.
- Státní ústav pro kontrolu léčiv. www.sukl.cz
- Pokorná A, Štrombachová V, Mužík J et al. Národní portál Systém hlášení nežádoucích událostí. Ústav zdravotnických informací ČR, Praha, 2016.
- Gyllensten H, Rehnberg C, Jonssön AK et al. Cost of illness of patient-reported adverse drug events: a population-based cross-sectional survey. BMJ Open 2013, 3(6), e002574.
- Szkultecka-Debek M, Drozd M, Kiepurska N et al. An adverse events potential costs analysis based on Drug Programs in Poland. Dermatology focus. Curr Issues Pharm Med Sci 2014; 27 : 183–186.
- Lagnaoui RN, Moore J, Fach M et al. Adverse drug reactions in a department of systemic diseases-oriented internal medicine: prevalence, incidence, direct costs and avoidability. Eur J Clin Pharmacol 2000; 56 : 181–186.
- Giardina C, Cutroneo PM, Moccario E et al. Adverse drug reactions in hospitalized patients: results of the FORWARD (Facilitation of Reporting in Hospital Ward) Study. Front Pharmacol 2018; 9 : 350.
- Mladá, J. Nežádoucí účinky léčivých přípravků – proč se jimi zabývat? Urologie pro praxi 2010; 11 : 108–109.
- Gregorová J et al. Význam klinickofarmaceutické péče. In: Gregorová J, Langmaierová K. Klinickofarmaceutická péče v České republice: Popis aktuálního stavu a stanovení cílů. Maxdorf, Praha, 2019 : 31–34.
- Rychlíčková J, Šaloun J, Gregorová J. Evaluation of clinical pharmacists' interventions in the Czech Republic. Pharmacotherapy 2016; 36 : 766–773.
Štítky
Adiktologie Alergologie a imunologie Angiologie Audiologie a foniatrie Biochemie Dermatologie Dětská gastroenterologie Dětská chirurgie Dětská kardiologie Dětská neurologie Dětská otorinolaryngologie Dětská psychiatrie Dětská revmatologie Diabetologie Farmacie Chirurgie cévní Algeziologie Dentální hygienistka
Článek Úvodem
Článek vyšel v časopiseČasopis lékařů českých
Nejčtenější tento týden
- Takrolimus v terapii atopické dermatitidy a analýza jeho nákladové efektivity ve srovnání s kortikosteroidní léčbou
- Efektivita kartáčku Sonicare For Kids u dětí předškolního věku
- Doc. Jitka Fricová: V USA nasazovali fentanyl poměrně nekriticky, v Česku je situace jiná
- Poškození plic mladé populace v souvislosti s vapováním − nová nozologická jednotka?
- Daivobet gel – lékový profil
-
Všechny články tohoto čísla
- Úvodem
- Klinická farmacie v České republice
- Vyplatí se bezpečná farmakoterapie?
- Specializační a kontinuální vzdělávání v oboru klinická farmacie
- Klinický farmaceut v pediatrii: možný přínos?
- Podání léčiv nutričními sondami: příklady, pracovní skupina
- Inhibitory protonové pumpy v praxi klinického farmaceuta
- Klinicky významné lékové interakce antiretrovirotik
- Altepláza v intrapleurální terapii: Co víme a nevíme?
- Management metabolických nežádoucích účinků everolimu u pacientů s renálním karcinomem
- Možnosti farmakologického ovlivnění singultu u pacientů v paliativní péči
- Kombinace mirtazapinu a paroxetinu: možná klinicky projevená interakce?
- Přednáškové večery spolku českých lékařů v Praze (BŘEZEN 2020)
- Fatální Stevensův-Johnsonův syndrom: komplikace při hospitalizaci pacienta na gerontopsychiatrii a prostor pro multioborovou spolupráci
- Spánek a jeho poruchy v neurologii
- Specifika spánku u žen a jeho poruch
- Význam spánkové medicíny v pediatrii
- Precizní psychiatrie – reálná možnost?
- Za docentem Václavem Jiráskem
- Princip posuzování a uznávání nemocí z povolání v České republice
- Časopis lékařů českých
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Možnosti farmakologického ovlivnění singultu u pacientů v paliativní péči
- Altepláza v intrapleurální terapii: Co víme a nevíme?
- Spánek a jeho poruchy v neurologii
- Inhibitory protonové pumpy v praxi klinického farmaceuta
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



