-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Point of care vyšetření krevní srážlivosti –
současné možnosti
Point of care examination of blood clotting –
current possibilitiesDetermination of platelet function and function of plasma coagulation system is one of the commonly performed examina tions in anesthesiology and intensive care. The reason for the examination of blood clotting may be planned or acute surgery, spontaneous bleeding, postoperative bleeding without a clear source, monitoring the effect of treatment with anticoagu lant and antiplatelet drugs, thromboembolism, etc. Very often these are urgent situations where it is advantageous if such examination can be performed directly at the patient’s bedside. Current medicine offers us the possibility of using several so-called point of care (POCT) devices that can be used for this purpose. In our article, we provide an overview of the most common methods and devices that are used to examine blood clotting at the patient’s bedside.
Keywords:
hemostasis – Platelets – aggregation – thromboelastometry
Autoři: J. Zatloukal 1; M. Horáková 1,2; L. Bultasová 3; J. Pouska 1; J. Kletečka 1; J. Beneš 1,2
Působiště autorů: Klinika anesteziologie a resuscitace, Lékařská fakulta v Plzni, Univerzita Karlova a Fakultní nemocnice Plzeň 1; Biomedicínské centrum, Lékařská fakulta v Plzni, Univerzita Karlova 2; Ústav klinické biochemie a hematologie, Lékařská fakulta v Plzni, Univerzita Karlova a Fakultní nemocnice Plzeň 3
Vyšlo v časopise: Anest. intenziv. Med., 32, 2021, č. 1, s. 14-24
Kategorie: Přehledové články
Souhrn
Stanovení funkce krevních destiček a plazmatického koagulačního systému patří v oborech anesteziologie a intenzivní péče mezi běžně prováděná vyšetření. Důvodem pro vyšetření krevní srážlivosti může být plánovaný či akutní operační výkon, spontánní krvácivé projevy, pooperační krvácení bez jasného zdroje, sledování efektu léčby antikoagulačních a protidestičkových léků, tromboembolie apod. Velmi často jde o situace naléhavé, kdy je s výhodou, pokud je možno tato vyšetření provést přímo u lůžka pacienta. Současná medicína nám nabízí několik tzv. point of care (POCT) přístrojů, které lze k tomuto účelu použít. V našem sdělení přinášíme přehled nejčastěji užívaných metod a přístrojů, které slouží k vyšetření krevní srážlivosti u lůžka pacienta.
Klíčová slova:
hemostáza – krevní destičky – agregace – tromboelastometrie
Úvod
Hemostáza patří mezi důležité procesy v organismu. Jedná se o řadu vzájemně propojených buněčných a humorálních interakcí složek krve a krevních cév. Jejich cílem je zabránit ztrátě krve při poranění cévní stěny tvorbou krevní sraženiny a zároveň zachovat funkční krevní tok uvnitř cévního systému. Toho je dosahováno vzájemnou interakcí pro - a antikoagulačních mechanismů.
Vyšetřování hemostázy prošlo v posledních několika letech významnou proměnou především díky řadě nových a dobře dostupných vyšetřovacích metod a analyzátorů. To umožnilo přenést interpretaci komplexních proa antikoagulačních dějů z laboratoří hematologie přímo do blízkosti lůžka pacientů v kritickém stavu. Vyšetřování funkce hemostázy je tak okamžitě k dispozici a stalo se již zcela rutinní součástí péče o pacienty na odděleních anesteziologie, intenzivní medicíny a urgentních příjmech.
Při péči o pacienty v perioperačním období a na lůžkách intenzivní péče se velmi často setkáváme se situacemi, kdy je důležitá včasná a přesná diagnostika stavu hemostázy.
Velká část pacientů v dnešní době užívá pravidelně léky ovlivňující krevní srážení – antikoagulancia a protidestičkové léky. Antikoagulancia – warfarin, či některé z tzv. nových orálních antikoagulancií – užívají především pacienti s fibrilací síní, anamnézou žilní trombózy a plicní embolie. Protidestičkové léky jsou podávány v rámci primární a sekundární prevence kardiovaskulárních chorob a při zajištění pacientů po proběhlých endovaskulárních intervenčních výkonech.
S těmito pacienty se setkáváme nejen při plánovaných operačních výkonech, ale také u akutních výkonů a traumatizovaných pacientů. Tehdy potřebujeme velmi rychlou diagnostiku, na kolik je hemokoagulační systém daným léčivem ovlivněn, nebo zdali již jeho vliv na hemostázu odezněl.
POCT diagnostiku hemostázy velmi často využíváme v případě časové tísně, kdy nelze čekat na výsledky standardních koagulačních testů, v případě život ohrožujícího perioperačního či peripartálního krvácení, závažných traumat apod. Výhodou některých POCT přístrojů je kromě rychlosti i to, že poskytují komplexní hodnocení hemostázy jako celku a současně umožňují hodnotit funkci jednotlivých jejích součástí. Na základě získaných výsledků můžeme vést cílenou léčbu poruchy srážlivosti a výsledky této léčby okamžitě kontrolovat. Jsme schopni vyhnout se zbytečné korekci poruchy koagulace např. před provedením invazivních výkonů (tracheostomie, kanylace centrálních žil apod.), na kterou můžeme mít podezření z výsledků některých standardních koagulačních testů. Vyšetření může odhalit i pacienty s vystupňovaným krevním srážením, kteří jsou ohroženi tromboembolií.
Tento text přináší čtenářům aktuální přehled diagnostických metod dostupných u lůžka, které mohou napomoci při péči o nemocné s poruchou krevní srážlivosti s hlavním zaměřením na POCT diagnostiku destičkových funkcí.
Aktuální pohled na hemostázu
Hemostáza patří mezi důležité funkce krve. Jedná se o řadu vzájemně propojených buněčných a humorálních interakcí, jejichž cílem je zabránit ztrátě krve při poranění cévní stěny tvorbou krevní sraženiny při zachování funkčního krevního toku uvnitř cévního systému. Toho je dosahováno vzájemnou interakcí pro - a antikoagulačních mechanismů.
Díky řadě nových poznatků o interakci cévních, celulárních a plazmatických faktorů při vzniku krevní zátky dnes opouštíme původní scholastické rozdělení hemostatických procesů. Dnes hovoříme spíše o komplexním procesu složeném z několika současně probíhajících a vzájemně provázaných dějů:
1. Reakce cév v místě poškození
2. Tvorba primární sraženiny
3. Stabilizace primární sraženiny fibrinovou sítí
4. Regulační funkce protisrážlivých mechanismů udržujících fluido‑koagulační rovnováhu (antitrombin, heparin, protein C a S)
5. Funkce fibrinolytického systému (plasmin).
Reakce cév v místě poškození
V procesu hemostázy se významnou měrou uplatňuje sama cévní stěna a především její endoteliální buňky, které produkují řadu vazoaktivních, antitrombogenních i protrombogenních látek. Za normálních okolností je endotel antitrombogenní, k čemuž přispívá jednak nesmáčivý povrch, normálně fungující glykokalyx (heparansulfáty glykokalyx váží antitrombin) a také produkce vazodilatačních a antiagregačních látek, trombomodulinu atd.
Při poranění cévní stěny dochází k reflexní vazokonstrikci. Na obnažený subendoteliální kolagen adherují krevní destičky a dochází k uvolnění tkáňového faktoru (TF). Lokální vazokonstrikce je dále podporována tromboxanem A2 (TXA2) a serotoninem uvolněným z aktivovaných destiček. Zahájení tvorby trombinu aktivuje endotelové buňky, které mění svůj fenotyp z vazodilatačního a antitrombogenního na vazokonstrikční a protrombogenní.
Aktivovaný endotel produkuje vazokonstrikční substance – endoteliny, exprimuje na svém povrchu adhezivní molekuly, produkuje von Willebrandův faktor (vWF), tkáňový faktor, a další protrombogenní substance, čímž napomáhá jak tvorbě primární hemostatické zátky, tak aktivaci koagulačního systému. Endotel taktéž reguluje fibrinolýzu díky produkci tkáňového aktivátoru plasminogenu, urokinázy a na druhé straně inhibitoru aktivátoru plasminogenu.
V současné době jsme i díky POCT přístrojům schopni poměrně detailně vyšetřovat proces hemostázy, bohužel s jedinou logickou výjimkou, kterou představuje právě funkce cévní stěny.
Tvorba primární sraženiny
Na tvorbě primární hemostatické zátky se podílejí především krevní destičky. Proces tvorby primární hemostatické zátky zahrnuje adhezi destiček k obnaženému kolagenu poškozené cévní stěny, na které se významnou měrou podílí i vWF. Adheze destiček vyvolá uvnitř trombocytu řadu metabolických pochodů, které vedou jednak k morfologickým změnám – změně tvaru tvorbou filopodií – dále uvolnění obsahu destičkových granulí, které obsahují významné proagregační a další působky: adenosindifosfát (ADP), Ca2+, serotonin, fibrinogen, platelet derived growth factor, vWF, destičkový faktor V a další, a v neposlední řadě také syntézu a uvolnění TXA2. TXA2 je produktem metabolismu kyseliny arachidonové (AA), která je v průběhu aktivace trombocytu uvolněna z jeho membrány. Výrazným adhezivním a proagregačním stimulem je také plazmatický trombin. Po vyplavení ADP, TXA2 a účinkem trombinu dochází ke zvýšení koncentrace a aktivaci receptorů GP IIb/ IIIa na povrchu destiček. GP IIb/IIIa zprostředkovávají vzájemnou vazbu destiček (agregaci) prostřednictvím fibrinogenu a vWF.
Proces tvorby primární hemostatické zátky ovlivňuje řada léčiv ze skupiny protidestičkových léků. Tyto léky dělíme do 4 skupin (tab. 1) podle mechanismu jejich účinku.
Tab. 1. Přehled protidestičkových léků 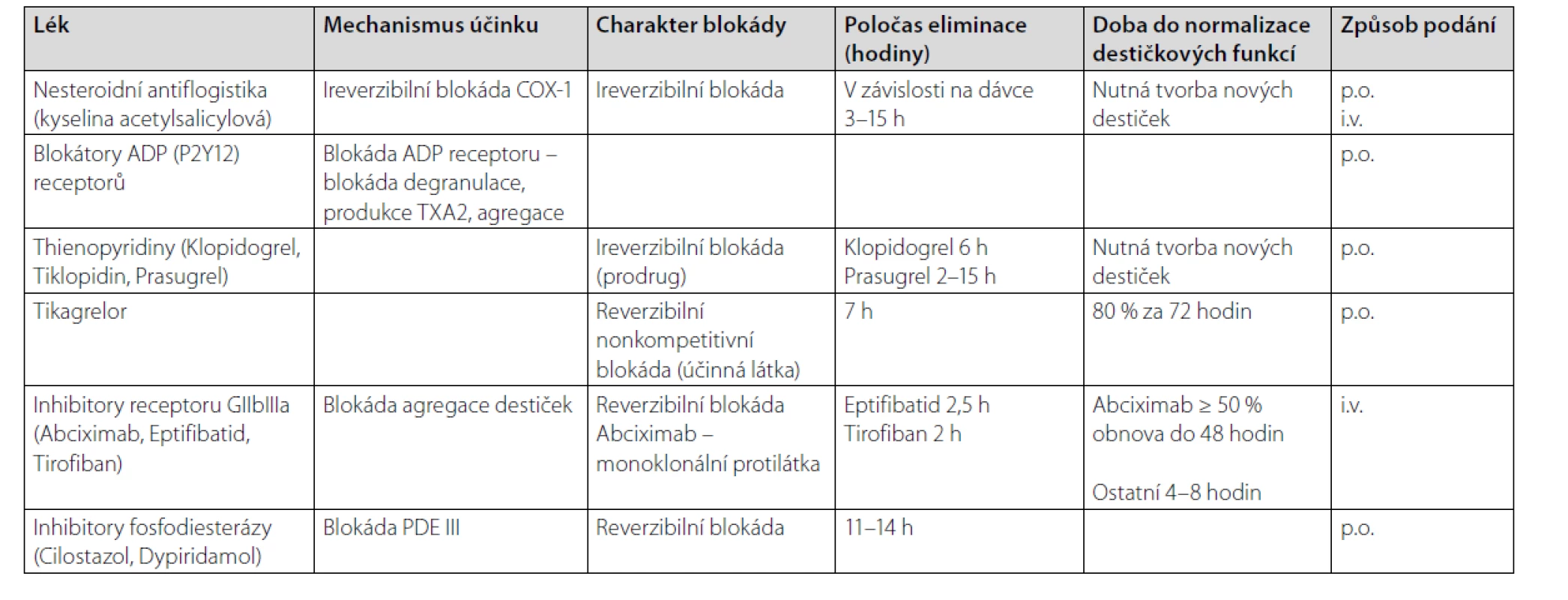
Vyšetření vlivu těchto léčiv na destičky patří mezi důležité indikace funkčního vyšetření destiček – agregometrie.
Plazmatický koagulační systém
Dalším důležitým hráčem v procesu hemostázy je plazmatický koagulační systém. Jedná se o systém vzájemně provázaných enzymatických reakcí, jejichž cílem je produkce trombinu a především nerozpustných fibrinových polymerů, které stabilizují primární hemostatickou zátku. Dříve používané členění na zevní a vnitřní koagulační systém je dnes bráno jako obsoletní. In vivo je pro spuštění koagulace zásadní uvolnění TF z poraněných tkání. Dochází k tvorbě komplexu TF (F VIIa + Ca2+ + TF), který aktivací faktoru X a následnou tvorbu protrombinázového komplexu (F Xa + F Va + Ca2+) vyvolá vytvoření malého množství trombinu (tzv. iniciační fáze). Tento trombin vede k aktivaci destiček, aktivaci faktorů XI, VIII a V a následně k tvorbě tenázového komplexu (F IXa + F VIIIa + Ca2+). Dochází k masivní produkci dalšího aktivního F Xa (fáze amplifikace) a excesivní produkci trombinu (fáze propagace). Trombin štěpí fibrinogen na fibrinové monomery, které spontánně polymerují v rozpustná fibrinová vlákna, která jsou dále stabilizována účinkem F XIIIa v nerozpustnou fibrinovou síť.
Tzv. vnitřní systém je důležitý především v amplifikaci. V aktivaci koagulace hraje roli pouze při in vitro vyšetření, ale v in vivo podmínkách má z tohoto pohledu zanedbatelnou úlohu.
K vyšetření plazmatického koagulačního systému jsou tradičně používány tzv. standardní koagulační testy: aktivovaný parciální tromboplastinový čas (aPTT), protrombinový čas (PT) a trombinový čas (TT). Nevýhodou těchto testů je nutnost předchozího zpracování krve centrifugací na pro vyšetření nezbytnou plazmu (eliminace buněčné složky), ohřátí na 37 °C a nutnost vyšetření v laboratoři. Čekání na výsledky vyšetření je z pohledu lékaře v akutní péči zdlouhavé a výsledky testů poskytují pouze omezenou informaci o funkci jednotlivých částí plazmatického koagulačního systému. Naproti tomu v rámci point of care diagnostiky jsou využívány přístroje přímo detašované na pracovištích, které jsou založené na měření komplexních změn viskoelastických vlastností plné krve při tvorbě koagula.
Regulační antikoagulační děje
Stejně tak jako je důležitý koagulační systém k zábraně krvácení, je neméně důležitý antikoagulační systém, který brání delokalizaci koagulační reakce, její nadměrné aktivaci a tím vzniku trombóz. Propagaci sraženiny omezuje do jisté míry sám o sobě proud krve a neporušený cévní endotel. Mezi hlavní faktory přirozeného antikoagulačního systému však patří inhibitor tkáňového faktoru (TFPI), antitrombin s heparinem jako kofaktorem a systém proteinu C a S. Aktivace těchto systémů je pomocí systému zpětných vazeb úzce spojena se systémem koagulačním. Detailnější popis těchto dějů však přesahuje rámec tohoto textu.
Fibrinolýza
Jedná se o finální děj hemostázy, při kterém dochází k rozpuštění vzniklého fibrinového koagula. Tento děj je žádoucí až ve chvíli, kdy krevní sraženina již splnila svou hemostatickou funkci. Vede k opětovnému plnému zprůchodnění cévy.
Základním faktorem tohoto systému je plasminogen, respektive jeho aktivovaná a enzymaticky aktivní forma plasmin. Plasmin vzniká aktivací plasminogenu navázaného na fibrinový povrch účinkem řady aktivátorů. Mezi nejdůležitější aktivátory patří tkáňový aktivátor plasminogenu (t‑PA) a urokináza, které jsou produkovány endotelem. Proces aktivace je dále akcelerován faktory koagulačního systému F XIIa, prekalikreinem, vysokomolekulárním kininogenem – zde je patrné vzájemné provázení koagulace a fibrinolýzy. Plasmin následně štěpí fibrin na jednotlivé fragmenty a rozpouští vzniklé koagulum. Celý systém je regulován celou řadou inhibitorů, ale jejich popis opět přesahuje obsah sdělení.
Jednotlivá dostupná POCT vyšetření krevní srážlivosti
1. Agregometrie
Agregometrie je metoda umožňující stanovení funkce destiček ex vivo. Její využití v klinické medicíně je široké. Jednak v rámci diferenciální diagnostiky krvácivých stavů, kde příčinou mohou být vrozené či získané poruchy funkce krevních destiček, dále pak ke sledování účinnosti protidestičkové terapie u pacientů s rizikem aterotrombotických uzávěrů [1, 2] a také za účelem vhodného načasování či hodnocení krvácivého rizika plánovaných chirurgických výkonů u pacientů léčených protidestičkovými léky [3].
Historicky nejstarší metodou (starou více než 100 let) a jedinou in vivo metodou sledování funkce destiček, respektive komplexního procesu tvorby primární hemostatické zátky, je test krvácivosti (bleeding time – např. dle Duka, Simplate…). Ve 20. století pak navázaly ex vivo laboratorní metody funkčního vyšetření krevních destiček – v 60. letech světelná transmisní agregometrie, v 80. letech impedanční agregometrie z plné krve, následně flowcytometrie, vyšetření sekrečních funkcí destiček a další metody. V současnosti stále roste poptávka po možnosti vyšetření funkce destiček u lůžka pacienta za využití POCT přístrojů, které jsou snadno použitelné a nevyžadují speciálně erudovaný personál pro práci v laboratoři. Při použití POCT jsou minimalizovány preanalytické chyby, které mohou nastat vlivem nevhodného transportu do laboratoře (starší typy potrubní pošty, otřesy, vysoká nebo naopak příliš nízká teplota), překročením doby stability vzorku při příliš dlouhém transportu apod. Přehled nejčastěji používaných metod a přístrojů pro POCT agregometrii ukazuje tabulka 2.
Tab. 2. Metody funkčního vyšetření trombocytů 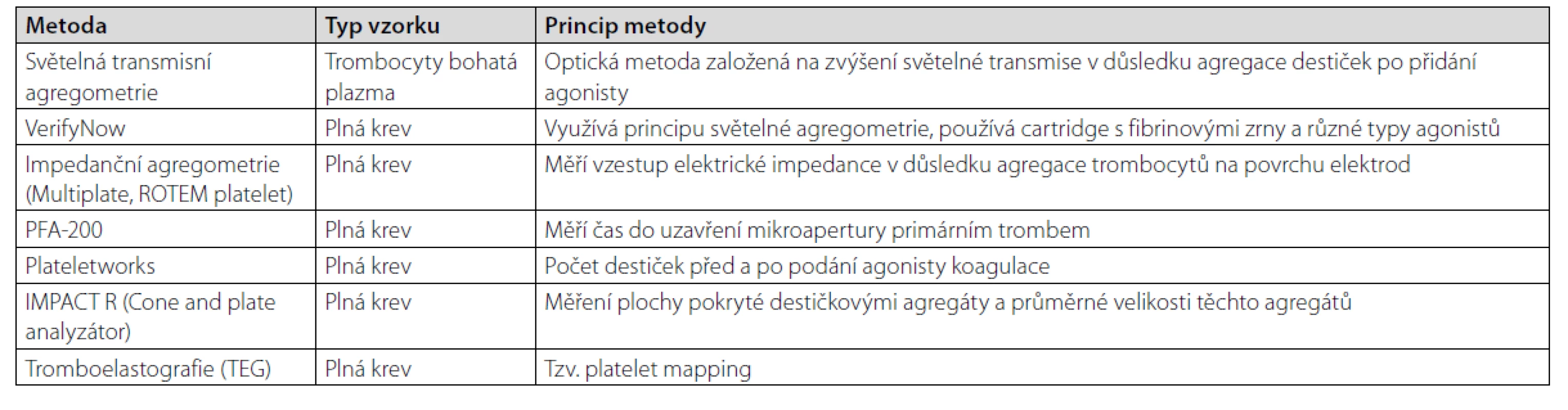
1.1 Světelná transmisní agregometrie
Historicky nejdéle používanou metodou, která je stále považována za zlatý standard, je tzv. světelná transmisní agregometrie (LTA z angl. light‑transmission aggregometry). Jedná se o spektrofotometrickou metodu založenou na hodnocení změny optické hustoty (absorbance) plazmy bohaté na trombocyty v průběhu agregačního děje vyvolaného přidáním induktorů.
Do citrátové plazmy bohaté na krevní destičky je přidán induktor – ADP, adrenalin, kolagen, ristocetin, arachidonová kyselina nebo trombin aktivující peptid (TRAP), který aktivuje proces agregace. Světlo o definované vlnové délce prochází měřící kyvetou a dopadá na detektor (obr. 1). V průběhu agregačního děje dochází k postupnému vzestupu intenzity dopadajícího světla. Naměřená hodnota intenzity světla je vyhodnocována jako procentuální rozdíl v porovnání s hodnotou intenzity světla prostupujícího plazmou bohatou na destičky (nulová agregace) a bezdestičkovou plazmou (100% agregace).
Obr. 1. Princip světelné transmisní agregometrie 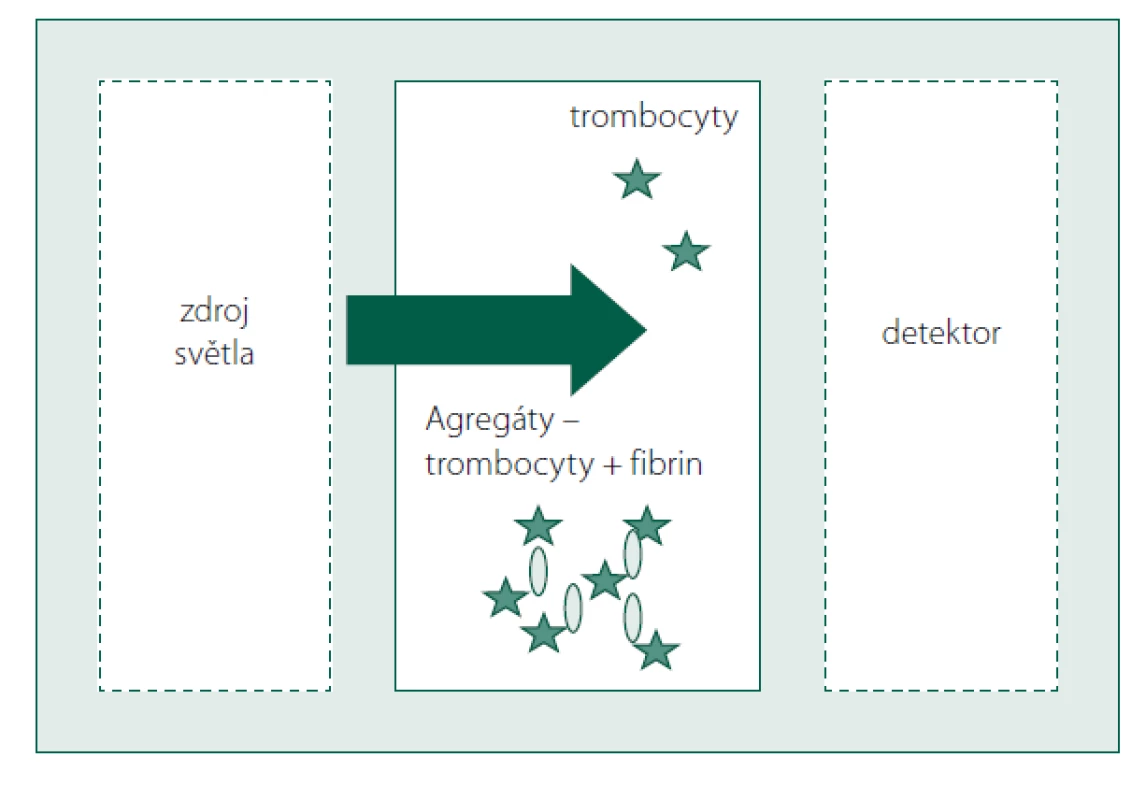
VerifyNow® (Accumetrics, San Diego, CA, USA)
Jedná se o POCT zařízení pracující na principu světelné agregometrie (obr. 2). Přístroj je určen primárně ke sledování účinnosti terapie kyselinou acetylsalicylovou a P2Y12 antagonistů (klopidogrel, prasugrel, tikagrelor), je však možné vyšetřit i efekt inhibitorů GIIb/IIIa.
Výhodou vyšetření je velmi snadná manipulace s krevním vzorkem. Vzorek plné krve antikoagulované citrátem sodným je přímo z odběrové zkumavky nasáván do speciální vyšetřovací kyvety vložené do přístroje. Zde se v zásobní části krev nejprve ohřeje na teplotu 37 °C a poté je distribuována do 4 měřících komor. V měřící komoře se nachází aktivátor a pelety potažené fibrinogenem. V závislosti na tvorbě destičkových agregátů dochází ke změně (snížení) absorbce emitovaného světla. Změna absorbance v čase je vyjádřena v tzv. reakčních jednotkách (viz níže).
Vyšetření je využíváno především k ověření účinku protidestičkových léků u pacientů před operačními výkony. Přístroj umožňuje měřit jak efekt protidestičkové léčby kyselinou acetylsalicylovou (VerifyNow Aspirin), kdy aktivátorem je AA a výsledek je udáván v tzv. aspirin reaction units (ARU), tak klopidogrelem (VerifyNow PRUTest). Zde je aktivátorem ADP + prostaglandin E1 (PGE1) a výsledek je v P2Y12 reaction units (PRU). Paralelně se v dalším kanálu měří transmise po přidání induktorů TRAP a PAR4-AP – toto vyšetření umožňuje odhadnout, jaká by byla agregace trombocytů bez účinku inhibitorů P2Y12 a následně pak stanovit procentuální míru inhibice navozenou inhibitory P2Y12.
Testování míry antiagregačního účinku léčiv před kardiochirurgickými operacemi je doporučeno i současnými doporučenými postupy [3, 4]. Existuje několik studií, které prokazují schopnost přístroje VerifyNow predikovat perioperační krvácení u pacientů podstupujících kardiochirurgické operační výkony nebo kardiologické implantační výkony [5, 6]. Další studie dokumentují využití VerifyNow k detekci účinnosti léčby kyselinou acetylsalicylovou a klopidogrelem u pacientů podstupujících perkutánní koronární intervenci (PCI) s implantací stentu. Přičemž za cut off hodnotu predikující zvýšené riziko krvácivých komplikací je většinou uváděna hodnota PRU ≥ 230, respektive ≥ 208 [7–9]. Určitou nevýhodu představuje nutnost delší inkubace vzorku před samotným vyšetřením, která činí u testu na aspirin 30 minut, u testu na P2Y12 10 minut. Samotné vyšetření pak trvá 2–5 minut.
1.2 Impedanční agregometrie
Metoda je založena na vzestupu elektrického odporu (poklesu průchodu elektrického proudu) mezi dvěma elektrodami v závislosti na tom, do jaké míry je jejich povrch pokryt agregujícími destičkami (obr. 3). Do měřící kyvety je pipetována plná krev antikoagulovaná citrátem sodným, heparinem nebo hirudinem. Přístroje založené na impedanční agregometrii umožňují použití celé běžné škály aktivátorů a tím stanovení efektu léčby všech běžně užívaných protidestičkových léků.
Obr. 3. Princip impedanční agregometrie 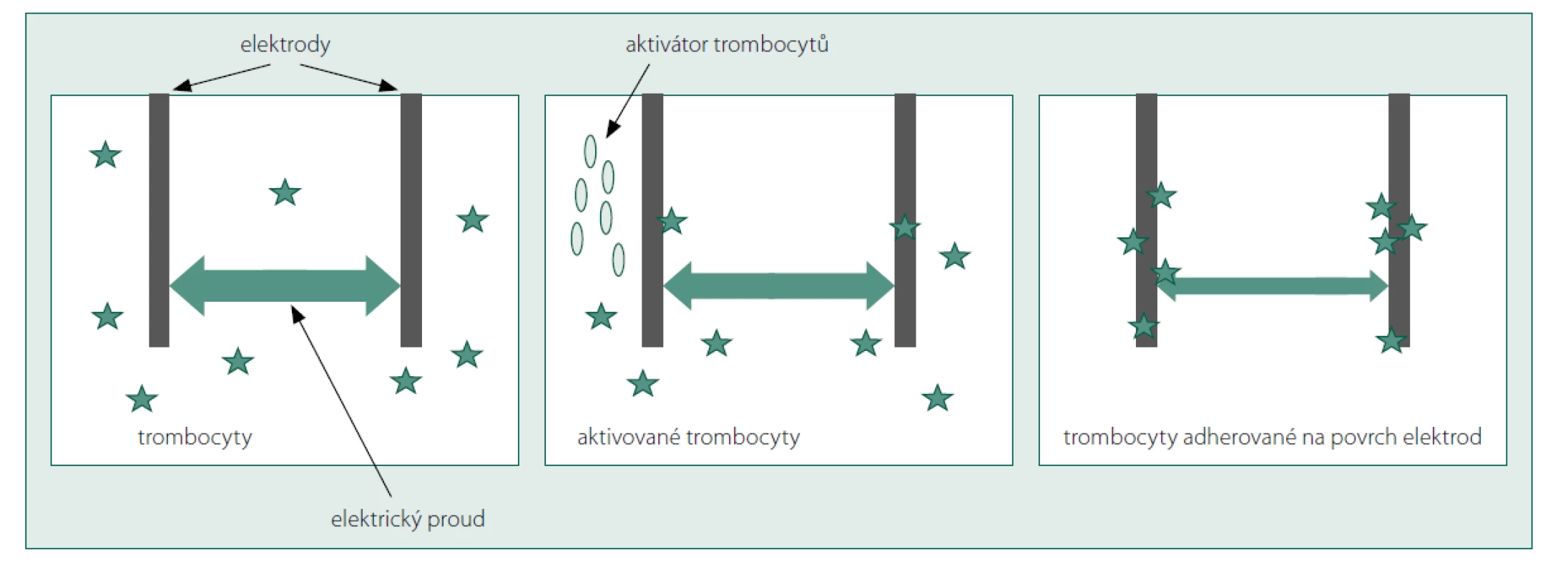
Multiplate® (Roche Diagnostics, Mannheim, Germany)
Je jedním z nejčastěji používaných přístrojů založených na principu impedanční agregometrie. Přístroj je určen jak pro laboratorní podmínky, tak pro POCT diagnostiku. Umožňuje současnou analýzu vzorků v pěti vyšetřovacích kanálech, jedno vyšetření trvá krátce, pouze necelých 10 minut. Pro analýzu je používána plná krev antikoagulovaná hirudinem. Aktivátorem agregace může být AA, ADP (+ PGE1), či TRAP.
Přístroj umožňuje diagnostiku zvýšené či snížené agregability destiček i stanovení účinku protidestičkových léků – kyseliny acetylsalicylové, ADP (P2Y12) antagonistů i inhibitorů GPIIb/IIIa. Přístroj kontinuálně měří postupný nárůst elektrického odporu mezi měřícími elektrodami v závislosti na množství aktivovaných destiček, které postupně agregují na povrchu elektrod. Výsledek měření je udáván v tzv. agregačních jednotkách (AU), rychlosti agregace (AU/min.) a celkovou hodnotou plochy pod agregační křivkou (AUC) (obr. 4), která má nejvyšší výpo - vědní hodnotu. Sibbigova studie, která hodnotila, zdali míra účinku klopidogrelu na krevní destičky hodnocená pomocí přístroje Multiplate koreluje s rizikem trombózy stentu implantovaného během PCI, prokázala silnou prediktivní hodnotu vyšetření [10]. Nevýhodou v porovnání s přístrojem VerifyNow nebo PFA-200 je složitější obsluha přístroje a také nutnost přípravy lyofilizovaných reagencí. Proto je spíše než pro POCT diagnostiku u lůžka pacienta využíván v laboratořích.
Obr. 4. Přístroj Multiplate + výsledek standardního testu 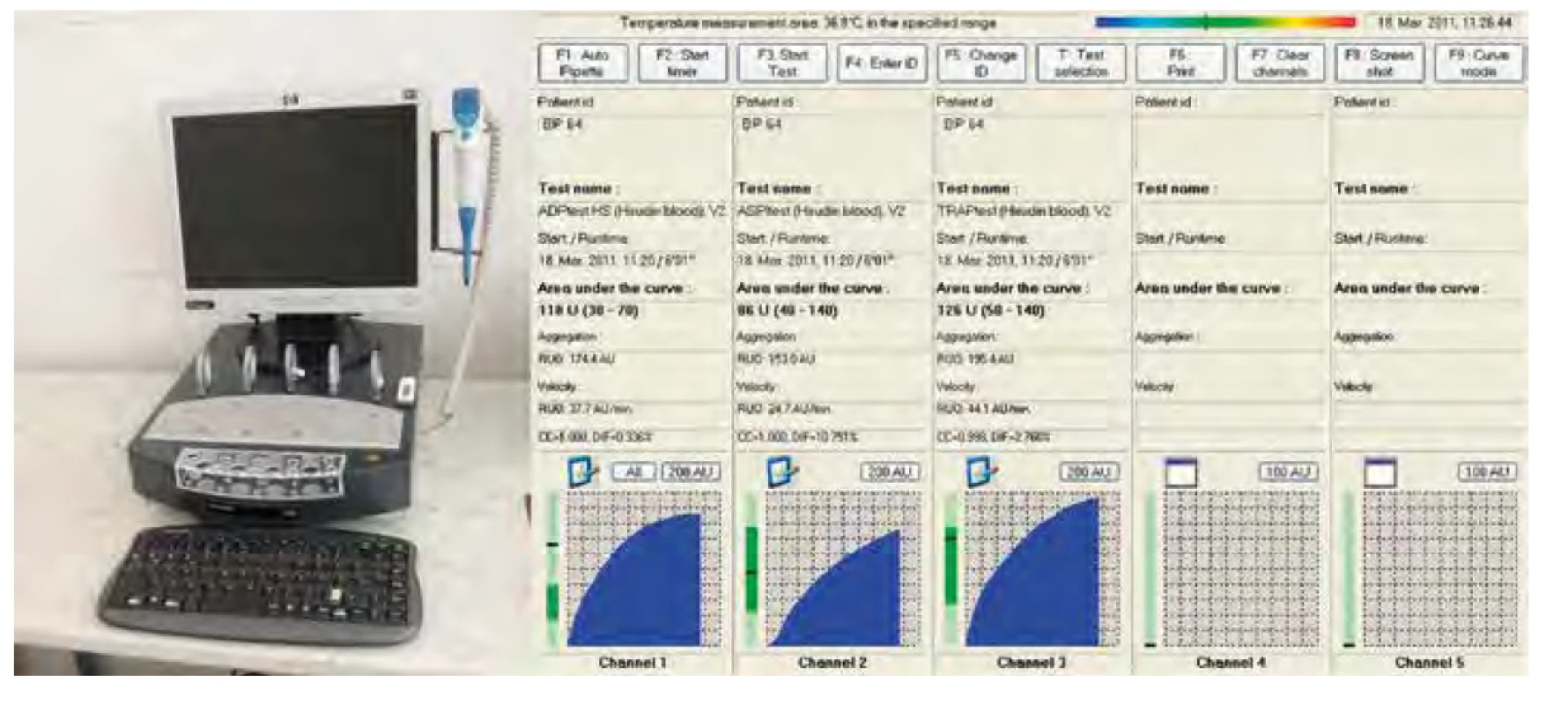
ROTEM Platelet (Instrumentation Laboratory, Werfen, Munich, Germany)
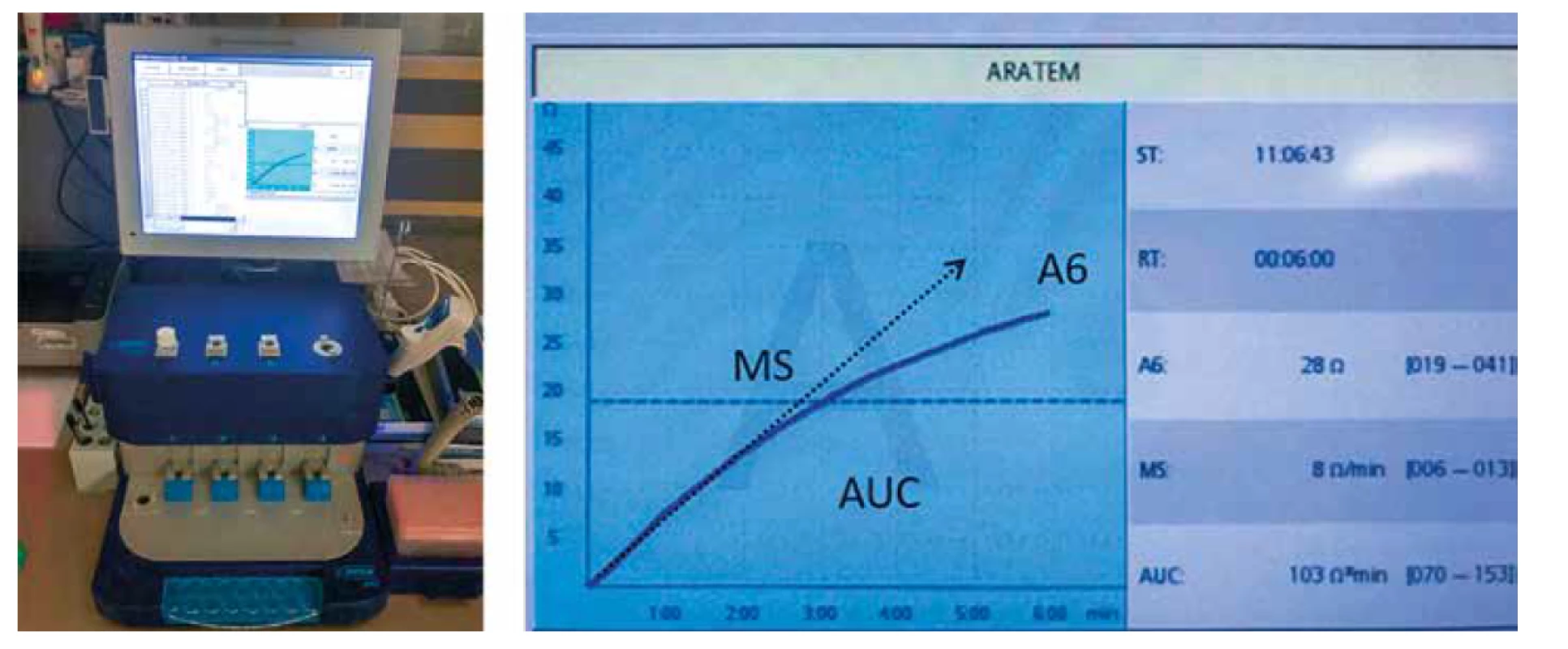
Přístroj ROTEM Delta disponuje speciálním přídavným modulem ROTEM Platelet, který umožňuje vyšetření trombocytů metodou impedanční agregometrie. Vyšetření je možno provádět současně ve dvou měřících kanálech. Příprava vzorku a vlastní vyšetření je velmi snadné a výsledky jsou k dispozici za 6 minut. Výhodou přístroje je možnost současně provádět i viskoelastické hemokoagulační vyšetření, a tak získat komplexní náhled na stav hemostázy. K dispozici jsou celkem 3 typy reagencií (testů): v testu ARA‑TEM reagencie obsahuje jako induktor AA a test je určen pro detekci účinku kyseliny acetylsalicylové, v ADP‑TEM je induktorem ADP a test zjišťuje efekt inhibitorů P2Y12 a v TRAP‑TEM je aktivátorem agregace trombin aktivující peptid a vyšetření je možno použít pro stanovení antiagregačního vlivu GPIIb/ IIIa inhibitorů.
Podobně jako u přístroje Multiplate získáváme křivku změny elektrického odporu v čase (obr. 5). Výsledkem měření jsou 3 parametry: A6 (amplituda v 6. minutě, tedy na konci měření), MS (maximal slope – sklon křivky) a AUC (plocha pod křivkou).
V současné době je k dispozici pouze omezené množství studií, které využívaly přístroj ROTEM Platelet. Kjellbergova studie z nedávné doby provedená na 23 kardiochirurgických pacientech prokázala všemi třemi testy ROTEM Platelet poruchu funkce destiček po ukončení mimotělního oběhu. Efekt destičkové transfuze vedl ke statisticky významnému zvýšení AUC u testu TRAP‑TEM [11]. Podobně studie Petricevice, která byla provedená na 101 pacientech po kardiochirurgickém výkonu v mimotělním oběhu [12], prokázala schopnost predikovat z výsledků přístrojů ROTEM Platelet a Multiplate velikost krevní ztráty 24 hodin po kardiochirurgickém výkonu a nutnost podání transfuzních přípravků.
1.3 Další metody vyšetření funkce destiček
Innovance PFA-200 (Siemens, Marburg, Germany)
Analyzátor umožňuje diagnostiku vrozených, získaných a léky navozených poruch destičkových funkcí. Umožňuje taktéž detekci funkce vWF a sledování efektu desmopresinu (DDAVP) [13].
Přístroj pracuje se speciální kyvetou, ve které krev prochází vysokou rychlostí mikroskopickým otvorem (velikost otvoru je 150 μm) v bioaktivní membráně potažené látkami aktivující trombocyty (kolagen + adrenalin, kolagen + ADP nebo ADP + PGE1). Rychlé proudění krve simuluje působení střižných sil, které za normálních okolností vznikají na povrchu endotelu in vivo. Celý proces tak vlastně simuluje adhezi a agregaci destiček v místě poranění cévy. Po aktivaci destiček induktory dochází postupně k uzavření otvoru v membráně (obr. 6). Přístrojem je měřen čas do uzavření této mikroapertury – „closure time = CT“, který je funkcí počtu a reaktivity destiček, aktivity vWF a hematokritu. Vyšetření nelze provádět, pokud je počet destiček nižší než 100 × 109/l. Výsledek měření může být zkreslen při nízkém hematokritu nebo trombocytopenii [14]. Měření má vysokou negativní prediktivní hodnotu, tedy je schopno dát s vysokou mírou přesnosti odpověď na otázku, zda je normální funkce destiček a vWF. Pokud je výsledek vyšetření patologicky prodloužený, je nutné pro samotnou detekci příčiny poruchy primární hemostázy využít některou z jiných metod (optickou agregometrii, stanovení aktivity a antigenu vWF). V tomto směru se tedy jedná spíše o kvalitativní screeningový test. Někteří autoři však toto vyšetření za vhodnou screeningovou metodou nepovažují v případě lehkých destičkových dysfunkcí [15] a je diskutabilní i jeho použití k předoperačnímu screeningu [14] a monitoraci účinku protidestičkových léků [16, 17]. Výhodou metody je snadné provedení a rychlost. Výsledek měření je k dispozici za 5–8 minut. Zařízení disponuje dvěma měřicími kanály, ale nelze je využít oba současně.
Obr. 6. Princip přístroje Innovance PFA-200 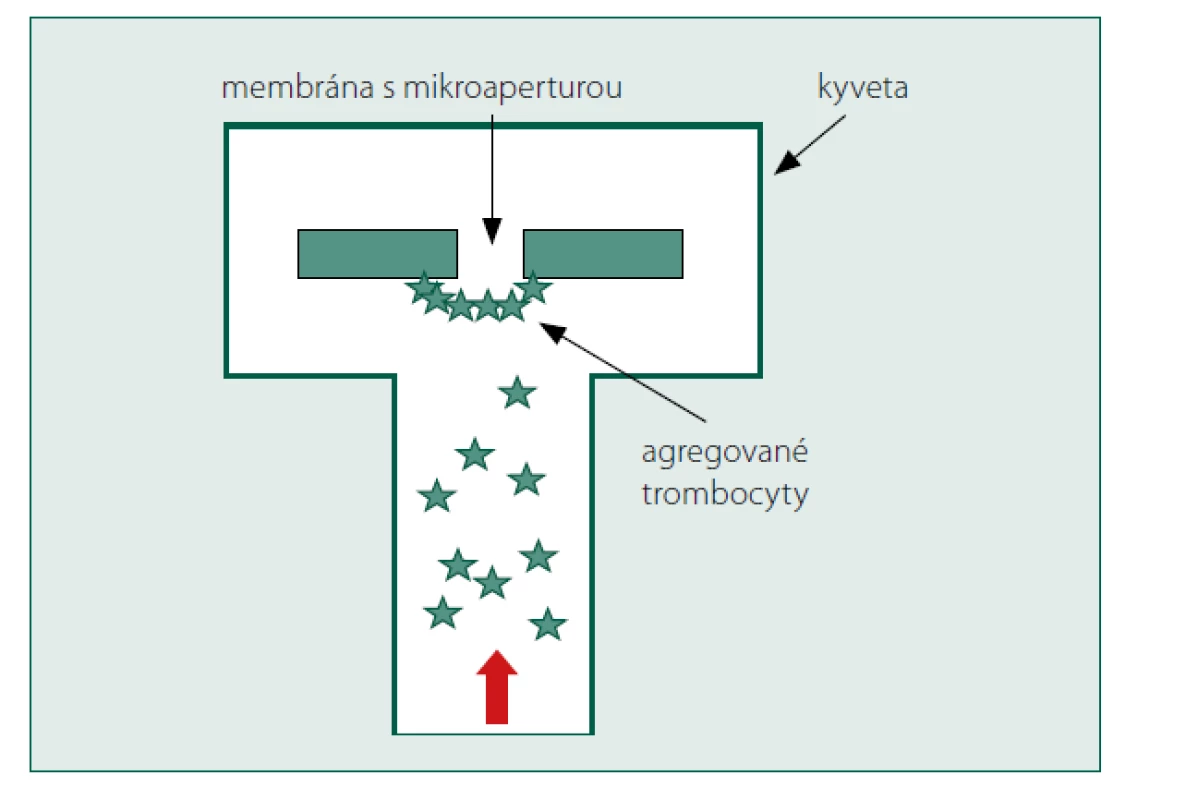
PlateletWorks (Helena Laboratories, Beaumont, Texas, USA)
Pro vyšetření je odebrána krev pacienta do zkumavky s kyselinou ethylendiamintetraoctovou (EDTA) a do speciálních zkumavek s aktivátory destiček (kolagenem, ADP, AA). Na hematologickém analyzátoru pracujícím na impedančním principu jsou pak následně v jednotlivých vzorcích vyšetřeny počty krevních destiček. Za referenční počet destiček je považován výsledek ve vzorku s EDTA, ve vzorcích s aktivátory agregace jejich počet klesá v závislosti na míře agregace. Pomocí vzorců obsahujících výsledek počtu destiček v EDTA a výsledek ve zkumavce s příslušným aktivátorem je kalkulován procentuální podíl agregace/inhibice destiček. Jedná se o vyšetření, které nelze zcela řadit do skupiny POCT přístrojů. Jeho použití není široce rozšířeno a je pouze omezené množství dat o jeho užití v klinické medicíně. Nicméně v Karkoutiho studii, která kombinuje vyšetření pomocí ROTEM EXTEM a PlateletWorks jako indikátorů k podání transfuzních přípravků u kardiochirurgických operantů, vedlo použití přístroje k 24% redukci množství transfuzí krevních destiček a ke snížení epizod závažného krvácení [18].
Impact R (Cone and plate analyzátor) (DiaMed, Cressier, Switzerland)
Jedná se o přístroj, který napodobuje fyziologický laminární tok krve tokem krve na povrchu tvořeném polystyrenem. Zde dochází k aktivaci destiček a jejich agregaci na povrch polystyrenové ploténky. Po promytí a obarvení destiček je následně zabudovaným speciálním zařízením analyzován procentuální podíl povrchu ploténky pokryté destičkovými agregáty a velikost jednotlivých agregátů. Měření je možné provádět i s přidáním stimulátorů agregace a vyšetřovat tak i účinek protidestičkových léků. Studií s využitím Impact R je pouze malé množství a přístroj zatím nezaznamenal větší rozšíření v klinické praxi.
PlateletMapping®
Určitou informaci o podílu krevních destiček na celkové hemostáze jsme schopni získat již ze základního vyšetření běžnou tromboelastometrií/ grafií, a to kombinací testů EXTEM + FIBTEM u přístroje ROTEM a Rapid TEG a CFF (functional fibrinogen) u přístroje TEG.
Nejmodernější verze přístroje TEG – TEG 6S (Haemonetics Corp., Braintree, MA, USA) je vybavena speciální kazetou (PlateletMapping® ADP and AA Cartridge), která umožňuje stanovit funkci destiček a vliv protidestičkových léků (kyseliny acetylsalicylové a ADP inhibitorů) metodou tzv. PlateletMapping. V rámci jedné kazety jsou prováděna 4 měření v oddělených měřicích komorách. První vyšetření využívá aktivátor kaolin, který plně aktivuje trombin a ten následně krevní destičky i plazmatický koagulační systém. Udává funkci destiček s 0% inhibicí (MAtrombin). V druhém testu je naopak trombin zcela inhibován a faktorem štěpícím fibrinogen je tzv. aktivátor F (firemní název výrobce). Destičky zde nejsou aktivovány vůbec, vyšetření tedy odpovídá 100% inhibici destičkových funkcí (MAfibrin). Ve třetím a čtvrtém vyšetření je opět plně inhibována funkce trombinu a použity jsou pouze induktory agregace destiček – ve třetím testu induktor ADP, který detekuje vliv inhibitorů ADP receptorů (MAADP), ve čtvrtém pak AA, která detekuje efekt kyseliny acetylsalicylové (MAAA). Z těchto parametrů je pak kalkulována agregace destiček, respektive jejich procentuální inhibice.
Sivapalan ve své studii prokazuje schopnost PlateletMapping predikovat podání transfuzních přípravků u pacientů podstupujících plánovaný aortokoronární bypass (CABG) [19], podobně byl PlateletMapping schopen predikovat pooperační krvácení u pacientů po CABG [20].
Klinický komentář k dostupným POCT agregometrům
V současné době je těžké říci, který z POCT přístrojů je pro funkční vyšetření krevních destiček nejpřesnější a nejspolehlivější. Studií srovnávajících jednotlivá zařízení je pouze omezené množství a POCT agregometrie stále ještě nepatří mezi běžně dostupná vyšetření v rámci intenzivní a perioperační péče. Studie Karona, která srovnávala přesnost a spolehlivost celkem 5 zařízení včetně 3 POCT, hodnotila PlateletMapping jako nevyhovující pro monitoraci léčby kyselinou acetylsalicylovou a klopidogrelem, naopak přístroj Multiplate vykazoval nejvyšší míru spolehlivosti [21]. Studie Ranucciho srovnávající vyšetření na Multiplate a ROTEM Platelet poukázala na nízkou míru shody u zařízení založených na principu impedanční agregometrie, přičemž ROTEM Platelet nebyl dostatečně citlivý detekovat změnu destičkových funkcí po vysazení klopidogrelu [22].
Z hlediska detekce účinnosti klopidogrelu se jako nejvhodnější jeví použití přístroje Multiplate a VerifyNow [23]. Srovnání je obtížné i vzhledem k tomu, že jednotlivá zařízení využívají jiný fyzikální princip měření. Diskutován je i jasně definovaný zlatý standard měření, přestože je za něj dlouhodobě považována světelná agregometrie. Tato metoda však pracuje s odlišným biologickým materiálem – plazmou bohatou na destičky – a nikoliv s plnou krví jako POCT analyzátory.
2. Viskoelastické POCT metody měření hemokoagulace
Metoda tromboelastografie byla popsána Herterem již v roce 1948. Je založena na monitorování změn viskoelastických vlastností plné krve v souvislosti s tvorbou koagula. Základem metody je převod mechanické energie, která je vynakládána na rotaci kovového hrotu v kyvetě s krví (v případě tromboelastometrie – přístroj ROTEM) nebo rotaci kyvety kolem kovového hrotu ve vzorku krve (v případě tromboelastografie – přístroj TEG). Mechanicko‑elektrickým převodníkem jsou změny pohybu trnu v průběhu procesu hemokoagulace přeměněny na elektrický signál, respektive do grafické podoby tromboelastografické křivky (obr. 7). Základní měřené parametry jsou uvedeny v tabulce 3 a obrázku 8.
Obr. 7. Princip funkce ROTEM a TEG 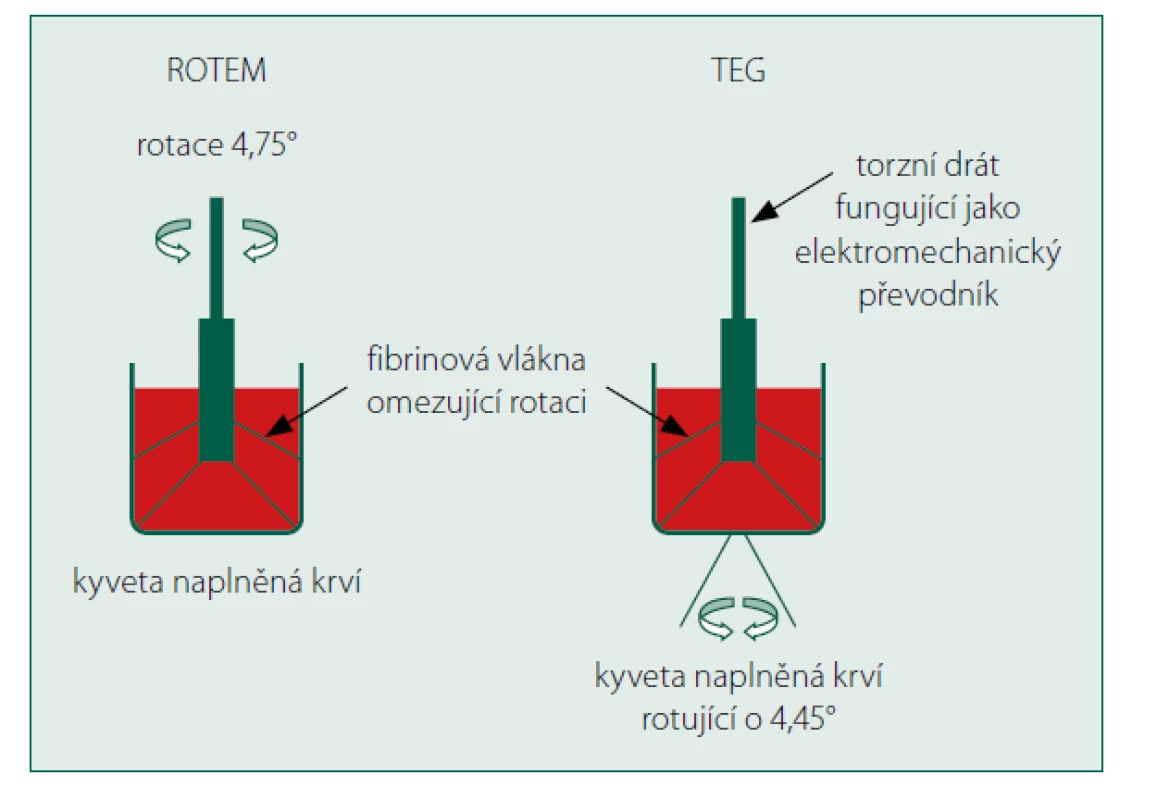
Tab. 3. Základní měřené parametry přístrojů ROTEM, TEG a ClotPro 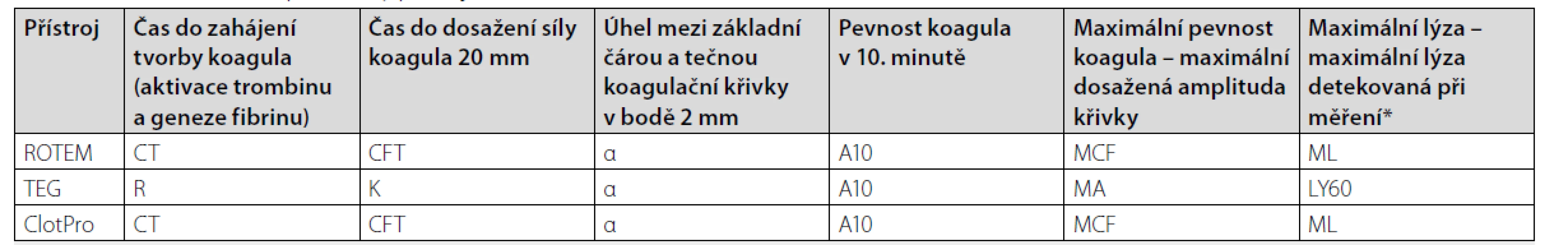
* jedná se o rozdíl mezi maximální a minimální amplitudou měření vyjádřený v % MCF, resp. MA. Zpravidla bývá měřen v 60. minutě od zahájení měření.
CT – clotting time, R – reaction time (čas od zahájení měření do chvíle kdy koagulum dosáhne síly 2 mm), CFT – clot formation time, K – coagulation time, A10 – amplituda křivky v čase 10 minut od začátku měření, MCF – maximum cloth firmness, MA – maximum amplitude, ML – maximum lysis, LY60 – lýza v 60. minutěObr. 8. Standardní tromboelasto-metrická (grafická) křivka apmlituda 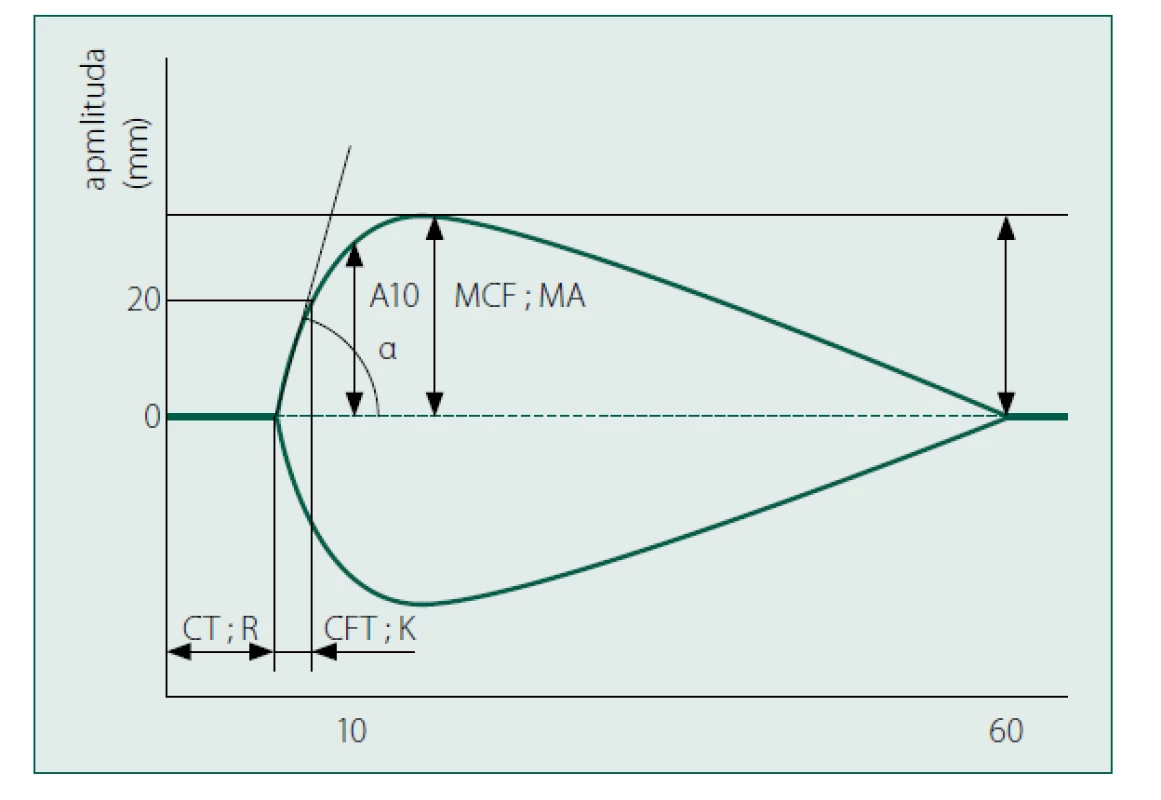
Nově ke dvěma výše uvedeným přístrojům přibyl přístroj ClotPro. U tohoto přístroje (podobně jako u přístroje TEG) dochází k rotaci nádobky a hrot zůstává během měření stacionární. Kromě výše uvedených přístrojů založených na rotační tromboelastometrii existuje i přístroj Sonoclot, který je založen na principu tromboelastometrie při lineárním pohybu. Nejnovějším přístrojem sloužícím k měření viskoelastických vlastností krve je přístroj Quantra, který k měření viskoelastických vlastností krve využívá ultrazvukového vlnění. Důležité je, že tyto POCT metody umožňují sledování vývoje koagula od jeho vzniku, přes dosažení maximální pevnosti až do jeho eventuální lýzy. Tím se liší od standardních hemokoagulačních testů, jako jsou aPTT, TT a PT, jelikož tyto monitorují koagulaci pouze do vzniku prvních fibrinových vláken. Navíc tyto metody pracují pouze s plazmou, která je zahřátá na 37 °C. Viskoelastické metody pracují s plnou krví a některé umožňují nastavením teploty vyšetření simulovat i vliv aktuální teploty pacienta na koagulaci. Další nespornou výhodou POCT vyšetření je jeho rychlost, která je především u akutních traumatických případů zcela zásadní. Výsledky standardního hemokoagulačního vyšetření bývají k dispozici za 30–60 minut, první výsledky POCT přístrojů získáme již za cca 20 minut [24], respektive již v 5.–10. minutě. To vede k rychlé cílené léčbě koagulační poruchy pomocí koncentrátů koagulačních faktorů a tím ke snížení spotřeby transfuzních přípravků [25]. Použití viskoelastických POCT metod v rámci perioperační péče u krvácejících pacientů s cílem redukovat množství podaných transfuzí doporučují i guidelines Evropské společnosti hrudní a srdeční chirurgie a anesteziologie [4].
V současné době je snaha všech výrobců o maximální automatizaci vyšetření a omezení nutnosti pipetování vzorků krve. Dále pak je patrná snaha minimalizovat rozměry přístrojů a zvýšit jejich odolnost a v neposlední řadě i možnost vzdáleného přístupu k výsledkům [26].
ROTEM (Instrumentation Laboratory, Werfen, Munich, Germany)
Tento přístroj v posledních letech prošel několika technickými inovacemi, nicméně jeho nejpoužívanější verzí je ROTEM delta. Jedná se o 4kanálový POCT přístroj měřící viskoelastické vlastnosti krve v průběhu procesu koagulace. Výhodou přístroje proti přístroji TEG (především starším variantám) je jednak možnost nastavení teploty měření v roz - mezí 30–40 °C, což umožňuje simulovat aktuální teplotní podmínky in vivo u kriticky nemocných pacientů (především vliv hypotermie na koagulaci), a dále pak jeho menší citlivost k otřesům oproti přístroji TEG. ROTEM disponuje baterií testů umožňujících vyšetřit funkčnost jednotlivých částí plazmatického koagulačního systému (tab. 4) a kombinace testů EXTEM/FIBTEM umožňuje i nepřímé zhodnocení funkce krevních destiček. Vyšetření lze provádět buď s použitím tekutých reagencií (výhodou je nižší cena, nevýhodou více pipetovacích kroků) nebo jednorázových předpřipravených reagencií. Nejnovější verze přístroje ROTEM Sigma poskytuje nejvyšší stupeň automatizace vyšetření s maximálně jednoduchou prací se vzorkem. Při vyšetření na tomto přístroji zcela odpadá pipetování krve a všechny testy jsou provedeny v rámci jedné univerzální kazety (cartridge), která obsahuje testy FIBTEM, EXTEM, INTEM a APTEM, eventuálně i HEPTEM.
Tab. 4. Testy ROTEM (+ClotPro) a TEG 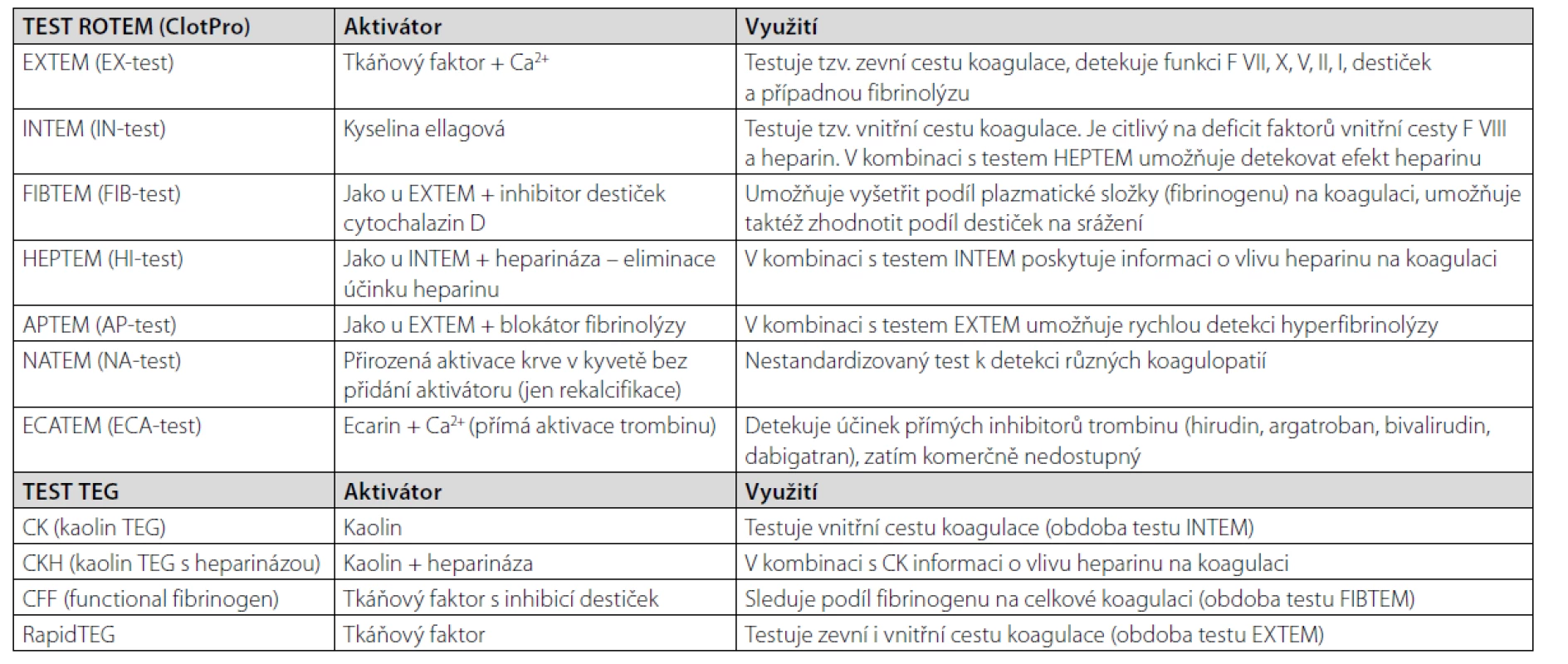
Přístroj je v současné době hojně využíván především v Rakousku a Německu a jeho používání se stále rozšiřuje i na našich pracovištích. Existuje řada studií prokazujících využitelnost přístroje v rychlé diagnostice koagulačních poruch a jejich rychlé a cílené léčbě spojené s redukcí podání alogenních transfuzí [27–29]. Přehledný algoritmus cílené léčby traumatem indukované koagulopatie byl vypracován Schöchlem [30] a v různých modifikacích je používán na celé řadě pracovišť. Cílená léčba koagulačních poruch představuje v současné době jistou alternativu, respektive doplnění masivního transfuzního protokolu (tedy léčebné strategie založené na frekventním podání transfuzních přípravků erytrocytů, krevních destiček a čerstvě zmražené plazmy často v poměru 1 : 1 : 1) v terapii masivního krvácení.
TEG (Haemonetics Corp., Braintree, MA, USA)
Jedná se také o POCT přístroj pro měření hemokoagulace na principu viskoelastometrie. K dispozici je v současné době starší verze přístroje TEG 5000 a novější varianta TEG 6S. Přístroj TEG 5000 je dvoukanálový a pracuje při standardní teplotě 37 °C. Jeho často popisovanou nevýhodou je citlivost k zevním otřesům. Novější verze TEG 6S pracuje podobně jako ROTEM sigma pouze s jednou kazetou (cartridge). Tato obsahuje kombinaci 4 testů, které jsou prováděny současně – kaolin TEG (CK), kaolin TEG s heparinázou (CKH), rapid TEG (CRT) a TEG functional fibrinogen (CFF). Přístroj má vysoký stupeň automatizace, výhodou jsou i jeho velmi malé rozměry. TEG 6S již nepracuje na principu převodu rotačních sil, ale měření probíhá na principu rezonance kombinované s fotodetektorem. Současné softwarové vybavení umožňuje i vzdálený přístup k výsledkům měření. Přehled testů a měřených veličin viz tabulky (tab. 4, tab. 3).
ClotPro (Enicor GmBH, Munich, Germany)
Jedná se o nejnovější rotační přístroj pro měření viskoelastických vlastností krve. U tohoto přístroje odpadá práce s aktivátory koagulace, jelikož ty jsou již obsaženy v suché houbičce, která se nachází uvnitř pipetovací špičky. Přístroj poskytuje celkem 6 měřicích kanálů. Přístroj disponuje jednak testy obdobnými jako přístroj ROTEM (tab. 4) navíc jsou k dispozici testy umožňující diagnostiku vlivu přímých inhibitorů trombinu (ECA-test) a přímých inhibitorů F Xa (RVV-test – aktivátorem je jed Russelovy zmije aktivující F X).
Součástí je i NA‑test, který sleduje tvorbu koagula po prosté rekalcifikaci vzorku (podobně jako NATEM). K dispozici je zatím pouze velmi málo dat, která by vypovídala o použitelnosti přístroje v klinické praxi.
Využití ROTEM a TEG v klinické praxi
Přístroj TEG podobně jako ROTEM nalezl široké využití v traumatologii [31, 32], v perioperační medicíně [33–35] i intenzivní péči. Oba přístroje slouží k rychlé diagnostice poruch koagulace a tím i jejich následné cílené léčbě. Lze je také využít k detekci pacientů se zvýšeným rizikem tromboembolie [36, 37] a k odhalení stavů, kdy prodloužení některého ze standardních hemokoagulačních časů není spojeno s alterací finální krevní srážlivosti [38, 39]. Dnes máme stále více důkazů, že cílená léčba poruchy koagulace s využitím koncentrátů koagulačních faktorů redukuje množství podaných transfuzních přípravků [27, 40]. Zatím není k dispozici velká randomizovaná studie, která by prokazovala, že tento přístup přináší mortalitní benefit v porovnání se standardním masivním transfuzním protokolem. O významu viskoelastických metod vypovídá i to, že jejich použití je zmiňováno v zásadních doporučeních pro management perioperačního krvácení [41] a krvácení u traumatu [42].
Sonoclot (Sienco Inc., Boulder, USA)
Je další z rodiny přístrojů pro měření změn viskoelastických vlastností krve. Byl konstruován von Kaullou již v roce 1975. Přístroj Sonoclot se liší od výše uvedených rotačních tromboelastometrů tím, že pohyb testovací sondy není rotační, ale lineární. Dutá sonda je připojena k elektromechanickému převodníku, který je generátorem vertikálního oscilačního pohybu a je ponořena do testovací kyvety s krví a příslušným aktivátorem koagulace (obr. 9). Aktivátorem koagulace je dle použitého testu kaolin, skleněné mikropartikule nebo minerál celit (česky slínek), některé testy jsou s přídavkem heparinázy a umožňují tak detekci efektu heparinu. Výrobce nabízí celkem 7 typů testu, jejich popis přesahuje obsah tohoto sdělení. Vznikající koagulum vytváří zvyšující se odpor vertikálnímu pohybu, který je měřen a zapisován formou křivky. Z té jsou potom odečítány základní měřené parametry: activated cloting time (ACT) – jedná se o čas od aktivace hemokoagulace do vzniku fibrinu. Tento parametr je podobný jako R a CT u přístroje TEG/ ROTEM, nicméně Sonoclot detekuje již časnější fázi tvorby fibrinu, clot rate (CR) – jedná se o maximální sklon křivky, který odpovídá rychlosti tvorby fibrinového gelu, Platelet function – jedná se o parametr, který je výsledkem softwarového zpracování vrcholu křivky, informuje o míře retrakce koagula. Tento parametr nabývá hodnoty 0–5 (0 = žádné známky destičkové funkce, 5 = vysoká funkčnost destiček). Přístroj pracuje při provozní teplotě 37 °C s plnou či citrátem ošetřenou krví. Přístroj není v našich podmínkách k dispozici a existuje limitované množství dat o jeho klinickém použití. Většina studií s přístrojem Sonoclot byla prováděna u pacientů podstupujících kardiochirurgické výkony. Ve studii Bischofa přístroj vykazoval schopnost predikce pooperačního krvácení u pacientů po kardiochirurgickém výkonu [43] a podobných výsledků dosáhl Rajkumar u pediatrických pacientů operovaných pro cyanotické srdeční vady [44]. Ve studii Espinosy byly výsledky přístroje v porovnání s rotačními tromboelastometry méně přesvědčivé [45].
Obr. 9. Schéma přístroje Sonoclot 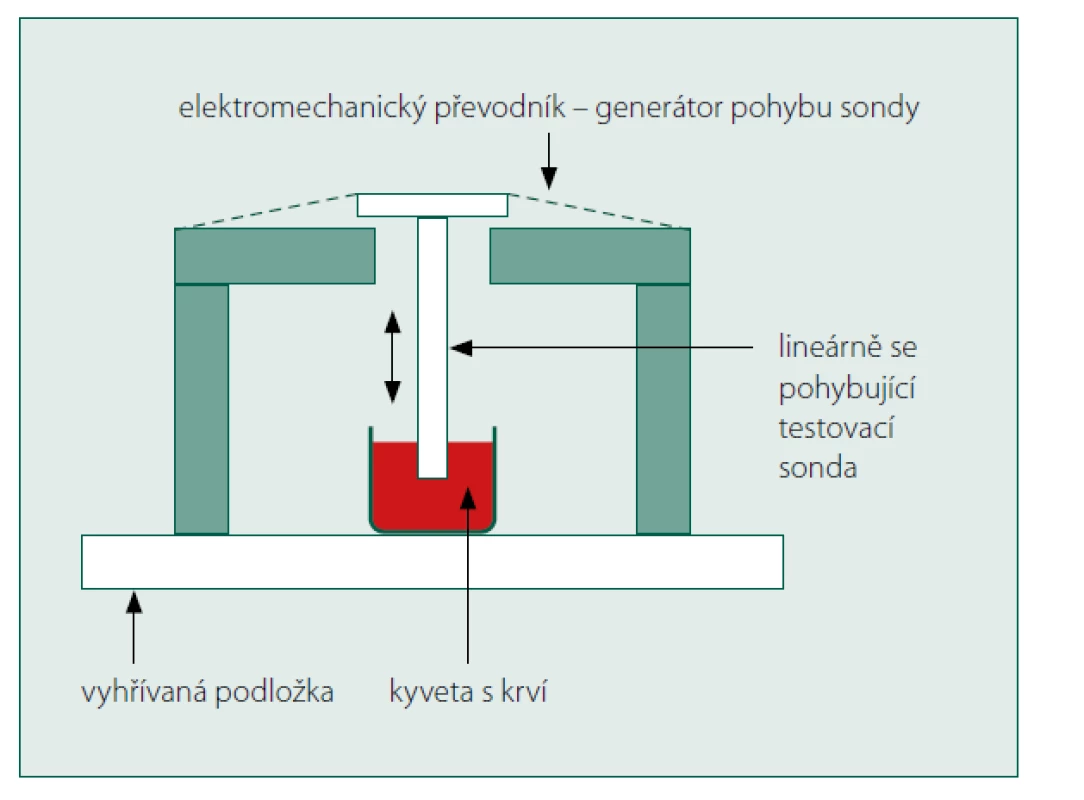
Quantra (Hemosonics, Charlottesville, USA)
Jde o novou generaci přístroje pro měření viskoelastických vlastností koagulující krve.
Přístroj využívá ultrazvukového vlnění prostřednictvím tzv. SEER (Sonic Estimation of Elasticity via Resonance) technologie. Krev v kyvetě je vystavena ultrazvukovému vlnění, které vede k rezonanci vzorku. S růstem pevnosti koagula dochází k nárůstu frekvence oscilací. Následně je konstruována křivka modulu pružnosti ve smyku a z ní jsou odečítány hodnoty tzv. clot time – čas do začátku tvorby koagula a clot stiffness – maximální síla koagula. Další měřené a kalkulované parametry jsou obdobné jako u ostatních přístrojů. Výrobce v současné době nabízí 2 multitestové cartridge Q plus určené pro vyšetření v kardiochirurgii a ortopedii a Q stat určenou pro traumatizované pacienty.
V současné době je k dispozici pouze omezené množství dat o klinické použitelnosti přístroje.
Recentní multicentrická studie Grovese prokázala velmi silnou korelaci výsledků přístroje Quantra s výsledky přístroje ROTEM u kardiochirurgických a velkých ortopedických operací [46].
Limitace viskoelastických metod
Viskoelastické metody nejsou schopny spolehlivě detekovat účinek warfarinu, nízkomolekulárního heparinu a tzv. nových orálních antikoagulancií, i když jak pro TEG, tak pro ROTEM jsou tyto testy vyvinuty či vyvíjeny, ale zatím nejsou komerčně dostupné. ClotPro tyto testy nabízí, ale zatím nejsou dostupná data o jejich spolehlivosti. Stejně tak není možná diagnostika efektu protidestičkových léků. V těchto případech je nutné vyšetření kombinovat se standardními hemokoagulačními testy, stanovením antiXa aktivity, dilutovaným trombinovým testem (dTT) nebo agregometrií. I když tyto přístroje pracují s plnou krví a tím se přiblížily fyziologickým podmínkám v organismu, stále chybí možnost zhodnotit funkci podstatné součásti krevního srážení in vivo, a to endotelu.
Závěr
POCT metody monitorace hemostázy se postupně stávají standardním vyšetřením na řadě pracovišť. Výrazným způsobem přispívají k rychlé a cílené diagnostice koagulačních poruch a tím i cílené léčbě koagulační poruchy. Umožňují rychlou detekci vlivu antikoagulancií a protidestičkových léků na hemostázu, pomáhají detekovat pacienty se zvýšeným rizikem trombózy.
Z těchto důvodů získávají stále větší oblibu v traumatologii, urgentní, perioperační a intenzivní medicíně. Současně poskytují anesteziologům a intenzivistům větší autonomii a detailnější pohled na hemostázu svých pacientů.
PROHLÁŠENÍ AUTORŮ: Prohlášení o původnosti: Práce je původní a nebyla publikována ani není zaslána k recenznímu řízení do jiného média. Práce ani její části nebyly prezentovány formou přednášky, posteru nebo abstraktu konference. Střet zájmů: Autoři prohlašují, že nemají střet zájmů v souvislosti s tématem práce. Podíl autorů: Všichni autoři rukopis četli, souhlasí s jeho zněním a zasláním do redakce časopisu Anesteziologie a intenzivní medicína. ZJ provedl literární rešerši, podílel se na sepsání rukopisu a finalizoval jeho verzi. BL se podílela na sepsání rukopisu, korekci kapitoly agregometrie a finální kontrole textu. PM, PJ, KJ se podíleli na sepsání rukopisu. BJ se podílel na přípravě a sepsání rukopisu a jeho finální kontrole. Financování: Podpořeno z projektu Q39 PROGRES.
KORESPONDENČNÍ ADRESA AUTORA:
Článek přijat redakcí: 28. 9. 2020; Článek přijat k tisku: 24. 11. 2020
MUDr. Jan Zatloukal, Ph.D.
Cit. zkr: Anest intenziv Med. 2021; 32(1): 14–24
Zdroje
1. Gurbel PA, Bliden KP, Butler K, Tantry US, Gesheff T, Wei C, et al. Randomized Double‑Blind Assessment of the ONSET and OFFSET of the Antiplatelet Effects of Ticagrelor Versus Clopidogrel in Patients With Stable Coronary Artery Disease. Circulation 2009; 120(25): 2577–2585.
2. Gurbel PA, Bliden KP, Butler K, Antonino MJ, Wei C, Teng R, et al. Response to Ticagrelor in Clopidogrel Nonresponders and Responders and Effect of Switching Therapies. Circulation 2010; 121(10): 1188–1199.
3. Ferraris VA, Saha SP, Oestreich JH, Song HK, Rosengart T, Reece TB, et al. 2012 Update to The Society of Thoracic Surgeons Guideline on Use of Antiplatelet Drugs in Patients Having Cardiac and Noncardiac Operations. Ann Thorac Surg. 2012; 94(5): 1761–1781.
4. Pagano D, Milojevic M, Meesters MI, Benedetto U, Bolliger D, Von Heymann C, et al. 2017 EACTS/EACTA Guidelines on patient blood management for adult cardiac surgery. European Journal of Cardio‑Thoracic Surgery 2018, 53(1): 79–111.
5. Reed GW, Kumar A, Guo J, Aranki S, Shekar P, Agnihotri A, et al. Point‑of‑Care Platelet Function Testing Predicts Bleeding in Patients Exposed to Clopidogrel Undergoing Coronary Artery Bypass Grafting: Verify Pre‑Op TIMI 45-A Pilot Study. Clin Cardiol. 2015; 38(2): 92–98.
6. Czerwińska‑Jelonkiewicz K, Witkowski A, Dąbrowski M, Piotrowski W, Hryniewiecki T, Stępińska J. The role of platelet reactivity assessment in dual antiplatelet prophylaxis after transcatheter aortic valve implantation. Arch Cardiovasc, DiS. 2018; 111(4): 233–245.
7. Marcucci R, Gori AM, Paniccia R, Giusti B, Valente S, Giglioli C, et al. Cardiovascular Death and Nonfatal Myocardial Infarction in Acute Coronary Syndrome Patients Receiving Coronary Stenting Are Predicted by Residual Platelet Reactivity to ADP Detected by a Point‑of‑Care Assay. Circulation. 2009; 119(2): 237–242.
8. Patti G, Nusca A, Mangiacapra F, Gatto L, D’Ambrosio A, Di Sciascio G. Point‑of‑Care Measurement of Clopidogrel Responsiveness Predicts Clinical Outcome in Patients Undergoing Percutaneous Coronary Intervention. Results of the ARMYDA‑PRO (Antiplatelet therapy for Reduction of MYocardial Damage during Angioplasty‑Platelet Rea. J Am Coll Cardiol. 2008; 52(14): 1128–1133.
9. Giustino G, Redfors B, Kirtane AJ, Mehran R, Dangas GD, Witzenbichler B, et al. Platelet Reactivity and Risk of Ischemic Stroke After Coronary Drug‑Eluting Stent Implantation. JACC Cardiovasc Interv. 2018; 11(13): 1277–1286.
10. Sibbing D, Braun S, Morath T, Mehilli J, Vogt W, Schömig A, et al. Platelet Reactivity After Clopidogrel Treatment Assessed With Point‑of‑Care Analysis and Early Drug‑Eluting Stent Thrombosis. J Am Coll Cardiol. 2009; 53(10): 849–856. doi: 10.1016/j.jacc.2008. 11. 030
11. Kjellberg G, Holm M, Lindvall G, Gryfelt G, van der Linden J, Wikman A. Platelet function analysed by ROTEM platelet in cardiac surgery after cardiopulmonary bypass and platelet transfusion. Transfus Med. 2020; (August 2018): 1–8.
12. Petricevic M, Konosic S, Biocina B, Dirkmann D, White A, Mihaljevic MZ, et al. Bleeding risk assessment in patients undergoing elective cardiac surgery using ROTEM® platelet and Multiplate® impedance aggregometry. Anaesthesia. 2016; 71(6): 636–647.
13. Favaloro EJ. Clinical utility of the PFA-100. Semin Thromb Hemost. 2008; 34(8): 709–733.
14. Favaloro EJ. Clinical utility of closure times using the platelet function analyzer-100/200. Am J Hematol. 2017; 92(4): 398–404.
15. Podda GM, Bucciarelli P, Lussana F, Lecchi A, Cattaneo M. Usefulness of PFA-100® testing in the diagnostic screening of patients with suspected abnormalities of hemostasis: comparison with the bleeding time. J Thromb Haemost. 2007; 5(12): 2393–2398.
16. Bartels A, Sarpong Y, Coberly J, Hughes N, Litt J, Quick J, et al. Failure of the Platelet Function Assay (PFA)-100 to detect antiplatelet agents. Surgery. 2015; 158(4): 1012–1019.
17. Orme R, Judge H, Storey R. Monitoring Antiplatelet Therapy. Semin Thromb Hemost. 2017; 43(03): 311–319.
18. Karkouti K, Callum J, Wijeysundera DN, Rao V, Crowther M, Grocott HP, et al. Point‑of‑Care Hemostatic Testing in Cardiac Surgery. Circulation. 2016; 134(16): 1152–1162.
19. Sivapalan P, Bäck AC, Ostrowski SR, Ravn HB, Johansson PI. Transfusion requirements in elective cardiopulmonary bypass surgery patients: predictive value of Multiplate and Thromboelastography (TEG) Platelet Mapping Assay. Scand J Clin Lab Invest. 2017; 77(5): 345–351.
20. Weitzel NS, Weitzel LB, Epperson LE, Karimpour‑Ford A, Tran ZV, Seres T. Platelet mapping as part of modified thromboelastography (TEG®) in patients undergoing cardiac surgery and cardiopulmonary bypass. Anaesthesia. 2012; 67(10): 1158–1165.
21. Karon BS, Tolan NV, Koch CD, Wockenfus AM, Miller RS, Lingineni RK, et al. Precision and Reliability of 5 Platelet Function Tests in Healthy Volunteers and Donors on Daily Antiplatelet Agent Therapy. Clin Chem. 2014; 60(12): 1524–1531.
22. Ranucci M, Baryshnikova E, Crapelli GB, Ranucci M, Meloni S, Pistuddi V. Electric impedance platelet aggregometry in cardiac surgery patients: A comparative study of two technologies. Platelets. 2016; 27(3): 185–190.
23. Le Quellec S, Bordet J‑C, Negrier C, Dargaud Y. Comparison of current platelet functional tests for the assessment of aspirin and clopidogrel response. A review of the literature. Thromb Haemost. 2016; 116(4): 638–650.
24. Haas T, Spielmann N, Mauch J, Madjdpour C, Speer O, Schmugge M, et al. Comparison of thromboelastometry (ROTEM®) with standard plasmatic coagulation testing in paediatric surgery. Br J Anaesth. 2012; 108(1): 36–41.
25. Deppe AC, Weber C, Zimmermann J, Kuhn EW, Slottosch I, Liakopoulos OJ, et al. Point‑of‑care thromboelastography/thromboelastometry‑based coagulation management in cardiac surgery: a meta‑analysis of 8332 patients. Journal of Surgical Research 2016; 203(2): 424–433.
26. Hartmann J, Murphy M, Dias JD. Viscoelastic Hemostatic Assays: Moving from the Laboratory to the Site of Care – A Review of Established and Emerging Technologies. Diagnostics 2020; 10(2): 118.
27. Görlinger K, Dirkmann D, Hanke AA, Kamler M, Kottenberg E, Thielmann M, et al. First‑line Therapy with Coagulation Factor Concentrates Combined with Point‑of‑Care Coagulation Testing Is Associated with Decreased Allogeneic Blood Transfusion in Cardiovascular Surgery. Anesthesiology. 2011; 115(6): 1.
28. Girdauskas E, Kempfert J, Kuntze T, Borger MA, Enders J, Fassl J, et al. Thromboelastometrically guided transfusion protocol during aortic surgery with circulatory arrest: A prospective, randomized trial. J Thorac Cardiovasc Surg. 2010; 140(5): 1117–1124.e2.
29. Schöchl H, Nienaber U, Hofer G, Voelckel W, Jambor C, Scharbert G, et al. Goal‑directed coagulation management of major trauma patients using thromboelastometry (ROTEM®)-guided administration of fibrinogen concentrate and prothrombin complex concentrate. Crit Care. 2010; 14(2): R55.
30. Schöchl H, Maegele M, Solomon C, Görlinger K, Voelckel W. Early and individualized goal‑directed therapy for trauma ‑ induced coagulopathy. Scand J Trauma Resusc Emerg Med. 2012; 20(1): 15.
31. Gonzalez E, Moore EE, Moore HB, Chapman MP, Chin TL, Ghasabyan A, et al. Goal‑directed hemostatic resuscitation of trauma ‑ induced coagulopathy a pragmatic randomized clinical trial comparing a viscoelastic assay to conventional coagulation assays. Ann Surg. 2016; 263(6): 1051–1059.
32. Moore HB, Moore EE, Chin TL, Gonzalez E, Chapman MP, Walker CB, et al. Activated clotting time of thrombelastography (T‑ACT) predicts early postinjury blood component transfusion beyond plasma. Surgery. 2014; 156(3): 564–569.
33. Bolliger D, Tanaka KA. Roles of Thrombelastography and Thromboelastometry for Patient Blood Management in Cardiac Surgery. Transfus Med Rev. 2013; 27(4): 213–220.
34. Nakayama Y, Nakajima Y, Tanaka KA, Sessler DI, Maeda S, Iida J, et al. Thromboelastometry‑guided intraoperative haemostatic management reduces bleeding and red cell transfusion after paediatric cardiac surgery. Br J Anaesth. 2015; 114(1): 91–102.
35. Clevenger B. Transfusion and coagulation management in liver transplantation. World J Gastroenterol. 2014; 20(20): 6146.
36. Hincker A, Feit J, Sladen RN, Wagener G. Rotational thromboelastometry predicts thromboembolic complications after major non‑cardiac surgery. Crit Care. 2014; 18(5): 549.
37. McCrath DJ, Cerboni E, Frumento RJ, Hirsh AL, Bennett‑Guerrero E. Thromboelastography Maximum Amplitude Predicts Postoperative Thrombotic Complications Including Myocardial Infarction. Anesth Analg. 2005; 100(6): 1576–1583.
38. Luckner G, Mayr VD, Fries DR, Innerhofer P, Jochberger S, Hasibeder WR, et al. Uncovering Hypercoagulability in Sepsis Using ROTEM® Thromboelastometry: A Case Series. Open Crit Care Med J. 2008; 1(1): 1–6.
39. Mallett SV, Sugavanam A, Krzanicki DA, Patel S, Broomhead RH, Davidson BR, et al. Alterations in coagulation following major liver resection. Anaesthesia. 2016; 71(6): 657–668.
40. Görlinger K, Fries D, Dirkmann D, Weber CF, Hanke AA, Schöchl H. Reduction of Fresh Frozen Plasma Requirements by Perioperative Point‑of‑Care Coagulation Management with Early Calculated Goal‑Directed Therapy. Transfus Med Hemotherapy. 2012; 39(2): 104–113.
41. Kozek‑Langenecker SA, Ahmed AB, Afshari A, Albaladejo P, Aldecoa C, Barauskas G, et al. Management of severe perioperative bleeding. Eur J Anaesthesiol. 2017; 34(6): 332–395.
42. Spahn DR, Bouillon B, Cerny V, Duranteau J, Filipescu D, Hunt BJ, et al. The European guideline on management of major bleeding and coagulopathy following trauma: fifth edition. Crit Care. 2019; 23(1): 98.
43. Bischof DB, Ganter MT, Shore‑Lesserson L, Hartnack S, Klaghofer R, Graves K, et al. Viscoelastic Blood Coagulation Measurement With Sonoclot Predicts Postoperative Bleeding in Cardiac Surgery After Heparin Reversal. J Cardiothorac Vasc Anesth. 2015; 29(3): 715–722.
44. Rajkumar V, Kumar B, Dutta V, Mishra AK, Puri GD. Utility of Sonoclot in Prediction of Postoperative Bleeding in Pediatric Patients Undergoing Cardiac Surgery for Congenital Cyanotic Heart Disease: A Prospective Observational Study. J Cardiothorac Vasc Anesth. 2017; 31(3): 901–908.
45. Espinosa A, Stenseth R, Videm V, Pleym H. Comparison of three point‑of ‑ care testing devices to detect hemostatic changes in adult elective cardiac surgery: A prospective observational study. BMC Anesthesiol. 2014; 14(1): 1–7.
46. Groves DS, Welsby IJ, Naik BI, Tanaka K, Hauck JN, Greenberg CS, et al. Multicenter Evaluation of the Quantra QPlus System in Adult Patients Undergoing Major Surgical Procedures. Anesth Analg. 2020; 130(4): 899–909.
Štítky
Anesteziologie a resuscitace Intenzivní medicína
Článek Perorální dexmedetomidin?
Článek vyšel v časopiseAnesteziologie a intenzivní medicína
Nejčtenější tento týden
2021 Číslo 1- Bezpečnostní profil metamizolu – systematický přehled
- Aktuální pohled na využití myorelaxancií a jejich antidot v moderní anesteziologii a intenzivní medicíně
- Perorální antivirotika jako vysoce efektivní nástroj prevence hospitalizací kvůli COVID-19 − otázky a odpovědi pro praxi
- Neodolpasse účinně snižuje pooperační bolest
- Neodolpasse jako ideální volba tam, kde je bolest provázena spasmem kosterního svalstva
-
Všechny články tohoto čísla
- Mezinárodní konsenzuální doporučení k postintenzívnímu syndromu
-
Point of care vyšetření krevní srážlivosti –
současné možnosti - Gabapentinoidy v perioperačním období
- Ketamin – nezávislost disociativní a analgetické působnosti
- Perorální dexmedetomidin?
- Vzdělávání mladých lékařů v době COVIDu
- Sto devadesát let od objevu chloroformu – historie inhalačních anestetik. Část 1
- Peroperační maligní hypertermie – bude vhodný předoperační genetický skríning?
- Fasciální prostory dolních končetin ve vztahu k regionální anestezii
- Raritná komplikácia zavedenia centrálneho venózneho katétra
- Pneumotorax, který nebyl pneumotoraxem
- Posttraumatická stresová porucha – až znepokojivý postintezivní výskyt
- Předejde umělá inteligence peroperační hypotenzi?
- Shaken adult syndrom nebo neurologická komplikace epidurální anestezie?
-
Biochemické vyšetření moči v intenzivní péči –
naučme se ho používat častěji - Mimotělní eliminace CO2 u pacientů v intenzivní péči – konsenzus evropského kulatého stolu
- Doporučení pro anestezii a sedaci u kojících žen
-
Stanovisko výboru ČSARIM 14/2021
Aktuální stav dostupnosti a poskytování intenzivní péče v rámci pandemie onemocnění COVID-19 -
MEZIOBOROVÉ STANOVISKO (evidenční číslo ČSARIM: 15/2021)
K POUŽITÍ BAMLANIVIMABU U PACIENTŮ S COVID-19 - Zajímavosti, tipy a triky, informace z jiných oborů
-
Přetlaková aplikace kyslíku pomocí Venturiho trysky Corovalve vyrobené na 3D tiskárně
Jednoduchá a levná metoda použitelná v nouzových podmínkách v masovém měřítku
- Anesteziologie a intenzivní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Doporučení pro anestezii a sedaci u kojících žen
-
Point of care vyšetření krevní srážlivosti –
současné možnosti - Ketamin – nezávislost disociativní a analgetické působnosti
- Fasciální prostory dolních končetin ve vztahu k regionální anestezii
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání