-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Centrální žilní porty a jejich využití k zajištění dlouhodobého cévního přístupu
Autoři: Renc Ondřej; Chovanec Vendelín; Raupach Jan
Působiště autorů: Radiologická klinika Lékařské fakulty a Fakultní nemocnice v Hradci Králové
Vyšlo v časopise: Anest. intenziv. Med., 25, 2014, č. 3, s. 235-238
Kategorie: Postgraduální vzdělávání - Didaktická radiologie
ÚVOD
V posledních letech se neustále zvyšuje počet nemocných, kteří vyžadují dlouhodobou intermitentní intravenózní léčbu. Nejčastěji se jedná o onkologické pacienty, u kterých je plánována protinádorová chemoterapie, nebo o nemocné s chronickým onemocněním jiné etiologie, kteří jsou závislí na dlouhodobé antibiotické léčbě či podávání protizánětlivých látek (cystická fibróza, asthma bronchiale a další). Nitrožilní léčba se běžně uskutečňuje u 90 % hospitalizovaných, ovšem opakované punkce povrchových žil, podávání látek s vysokou osmolalitou (> 500 mosmol/l) nebo nevhodným pH (pH < 5 nebo pH > 9) mohou postupně vést k poškození endotelu a insuficienci periferního žilního řečiště, která může být navíc přítomna již primárně. Pro dlouhodobou terapii je tak vhodnější podávání takových látek přímo do centrálního řečiště. Na trhu v současnosti existuje celá řada zařízení, v anglosaské literatuře označovaných jako „venous access devices“ (VAD), která zajištění dlouhodobého centrálního žilního přístupu umožňují [1, 2].
Nejběžnějším z těchto zařízení je jistě standardní netunelizovaný centrální žilní katétr, který se jednoduše zavádí a velmi snadno používá, nespornou nevýhodou je však jeho omezená životnost s nutností výměny po 10–12 dnech vzhledem k riziku rozvoje infekce. Periferně zaváděný centrální žilní katétr (PICC) je dobrou alternativou k centrální žilní kanyle, jelikož vzhledem k jeho délce je riziko bakteriální kolonizace významně nižší a lze jej používat po dobu 3–6 měsíců [1]. Je-li však nitrožilní léčba plánována na dobu delší než půl roku, ideálním řešením se zdá být implantace centrálního žilního portu, který nemocného nijak neomezuje při běžných denních činnostech, umožňuje odebírání krve a podávání látek s jakoukoli osmolalitou a jakýmkoli pH, umožňuje podávání vysokotlakých injekcí (tzv. power - nebo CT-port), a to vše při současné minimalizaci infekčních komplikací vzhledem k podkožní lokalizaci systému [3].
KONSTRUKCE ŽILNÍHO PORTU
Centrální žilní port sestává ze tří základních částí: komůrky, portové cévky a zámku. Komůrka (rezervoár) je vyrobena z kovu, plastu nebo keramiky a její nedílnou součástí je centrálně umístěná silikonová membrána, která slouží k zavedení speciální tzv. Huberovy jehly. Při správném používání by měla membrána vydržet 2000–3000 vpichů. Portová cévka je vyrobena z polyuretanu nebo silikonu a po spojení s komůrkou umístěnou v podkoží slouží jako centrální žilní katétr k podání léčiva do krevního oběhu. Zatímco polyuretanové katétry mají pevnější stěnu, a tudíž umožňují vyrobení tenčí cévky se širším vnitřním lumen, výhodou měkčích silikonových katétrů je naproti tomu lepší ohebnost a přizpůsobení se anatomickým podmínkám v místě implantace. Zámek – ať již kovový nebo plastový – potom slouží k vlastnímu spojení komůrky portu a portové cévky [2, 3].
INDIKACE A KONTRAINDIKACE
Jak již bylo zmíněno výše, hlavní indikací k zavedení centrálního žilního portu je nutnost dlouhodobé intermitentní intravenózní léčby u nemocných s insuficiencí periferního žilního řečiště. Téměř 95 % těchto indikací představují pacienti s nádorovým onemocněním. Z dalších skupin se potom jedná o nemocné vyžadující parenterální výživu, opakované krevní odběry či transfuze, dlouhodobou infuzní, analgetickou či antibiotickou léčbu nebo o nemocné s koagulopatií [2].
Absolutní kontraindikací k implantaci portu je známý septický stav nebo prokázaná bakterémie, jelikož zavedení systému u takového pacienta by vedlo ke kolonizaci zařízení mikroorganismy s nutností následné časné extrakce. Rovněž nemocní s krvácivým stavem, těžkou koagulopatií (INR > 1,5) nebo trombocytopenií (trombocyty < 80.109/l) jsou k výkonu kontraindikováni z důvodu rizika závažného krvácení při kanylaci centrální žíly nebo během preparace podkožní kapsy pro komůrku portu. Výkon je však možno provést po normalizaci koagulačních parametrů, např. podáním plazmy nebo trombocytárních náplavů. Jinou relativní kontraindikací je monstrózní obezita (BMI > 35 kg/m2), psychická intolerance cizího materiálu v těle nebo předpokládaná alergie na materiál žilního portu [2].
TECHNIKA IMPLANTACE
Před provedením vlastního výkonu je nezbytné provést některá režimová opatření, která zajistí bezproblémový průběh výkonu a další spolupráci pacienta. Je třeba nemocného poučit o povaze výkonu, jeho výhodách a rizicích a získat pacientův informovaný souhlas. Anamnéza a znalost základního onemocnění jsou velmi důležité např. u žen s karcinomem prsu, u kterých je z důvodu případného následného chirurgického výkonu, axilární lymfadenektomie či radioterapie doporučováno zavedení žilního portu na kontralaterální stranu, než je místo nádorového postižení. Nutností je rovněž hematologické vyšetření se zvláštním zřetelem na množství trombocytů a parametry koagulace (INR, APTT). Ultrasongrafické vyšetření centrálních žil před výkonem potom významně usnadní konečný výběr místa punkce a místa implantace portového zařízení.
Vlastní výkon probíhá v několika krocích a všeobecně je doporučováno jeho provedení pod kontrolou zobrazovacích metod:
- Příprava operačního pole: Za aseptických kautel ve spolupráci s asistující sestrou je připraveno operační pole včetně sterilního krytí ultrasonografické sondy a zesilovače rentgenového přístroje (obr. 1). Současně je možno připravit rizikové pacienty k výkonu podáním sedativ.
- Punkce centrální žíly: Pod ultrasonografickou kontrolou v místní anestezii provádíme punkci v. jugularis interna (VJI) nebo v. subclavia (VS) ze supraklavikulárního či infraklavikulárního přístupu (obr. 2). Po punkci následuje zavedení vodiče pod skiaskopickou kontrolou do horní duté žíly (HDŽ) a umístění portového katétru koncem do úrovně kavoatriální junkce.
- Vytvoření podkožní kapsy: Opět v místním znecitlivění provádíme incizi kůže v místě plánovaném pro zavedení komůrky žilního portu, nejčastěji na přední stěně hrudní v podklíčkové krajině. Místo incize by mělo být vzdáleno nejméně 3 cm od místa punkce centrální žíly. Vlastní příprava podkožní kapsy se provádí tupou preparací v hloubce 5–20 mm pod kožním povrchem, abychom předešli případným nekrózám kůže nad rezervoárem portu po jeho implantaci (obr. 3).
- Zavedení portu: Umístění komůrky žilního portu do připravené podkožní kapsy a její spojení se zavedeným tunelizovaným katétrem pomocí zámku (obr. 4). Je možné fixovat komůrku ke spodině rány několika vstřebatelnými stehy.
- Proplach systému: Stříkačkou s fyziologickým roztokem nejprve aspirujeme malé množství krve a následně systém proplachujeme, aspirace i proplach musí být zcela volné, bez odporu. Není-li plánováno časné použití, je možno systém uzavřít heparinovou zátkou.
- Uzávěr rány: Provádíme ve vrstvách podkoží vstřebatelnými stehy, uzávěr kůže nevstřebatelnými jednotlivými stehy či stehem intradermálním.Po výkonu následuje observace nemocného na dospávacím oddělení po dobu 2–3 hodin. Je-li následně plánováno propuštění do ambulantní péče, je vhodné před odchodem pacienta provést skiagram hrudníku k ozřejmení polohy žilního portu a vyloučení komplikací, zejména pneumothoraxu [2, 3] – obrázek 5.
Obr. 1. Instrumentárium potřebné k zavedení centrálního žilního portu 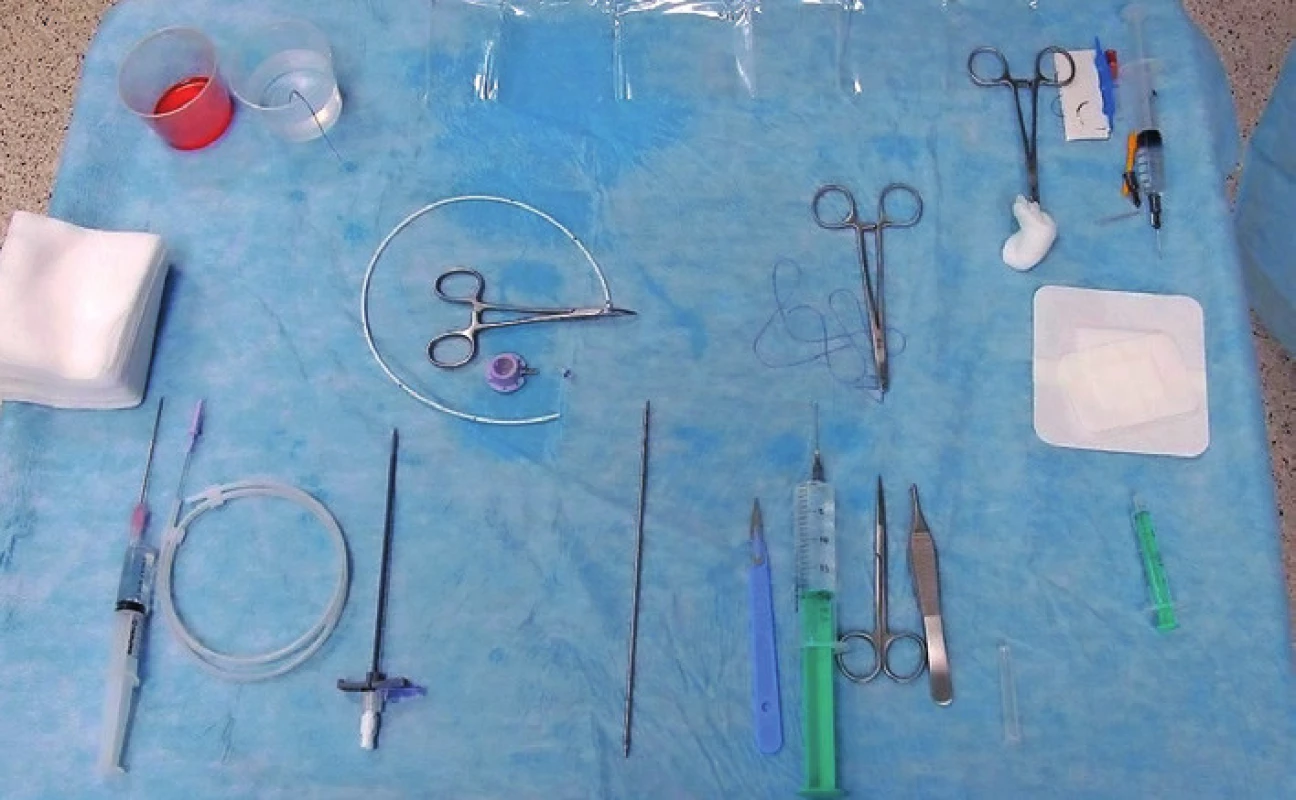
Obr. 2. Punkce centrální žíly pod ultrasonografickou kontrolou 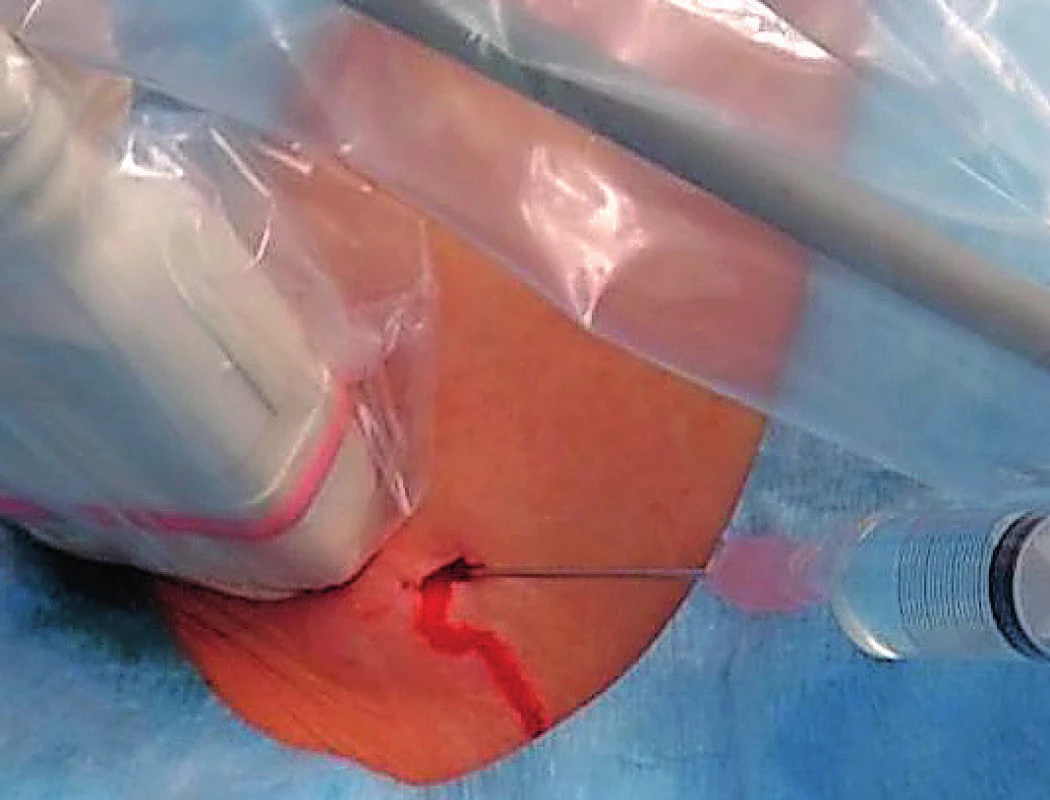
Obr. 3. Vytvoření podkožní kapsy a tunelizace katétru z místa vpichu 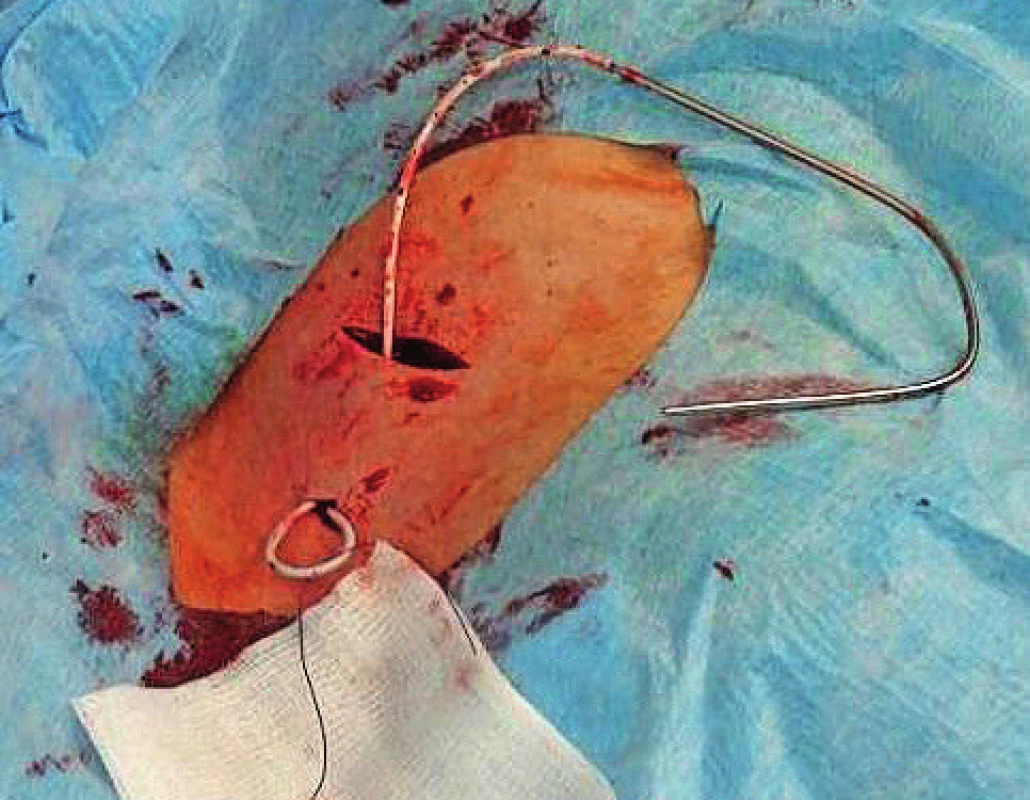
Obr. 4. Napojení portové cévky na komůrku žilního portu 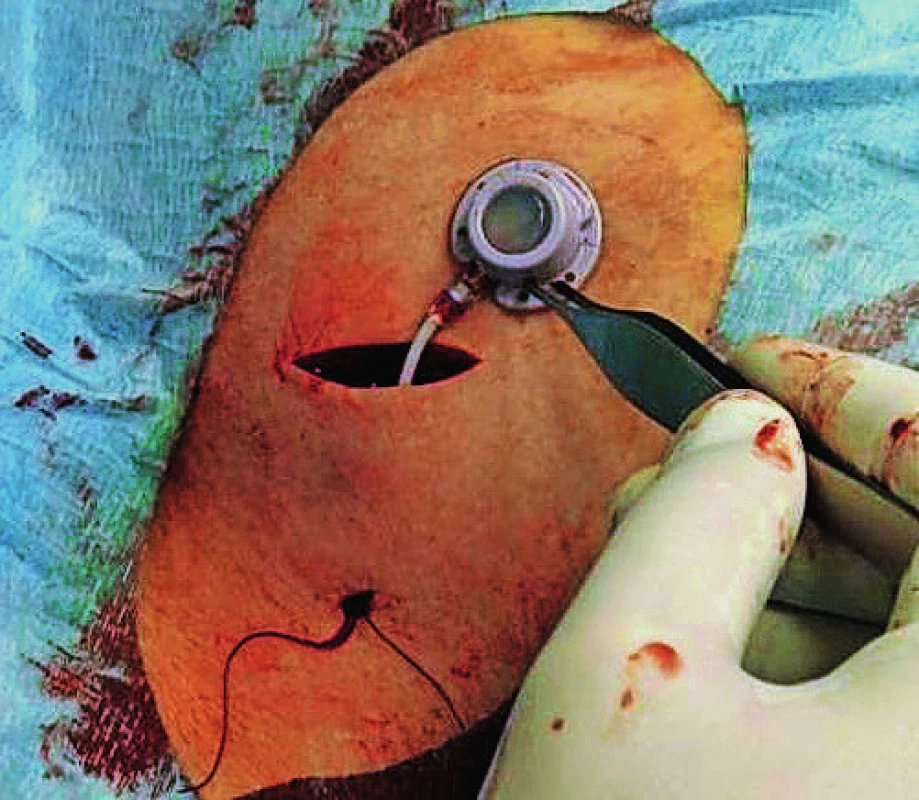
Obr. 5. Správná pozice centrálního žilního portu s koncem portové cévky v úrovni kavoatriální junkce na kontrolním skiagramu hrudníku po výkonu 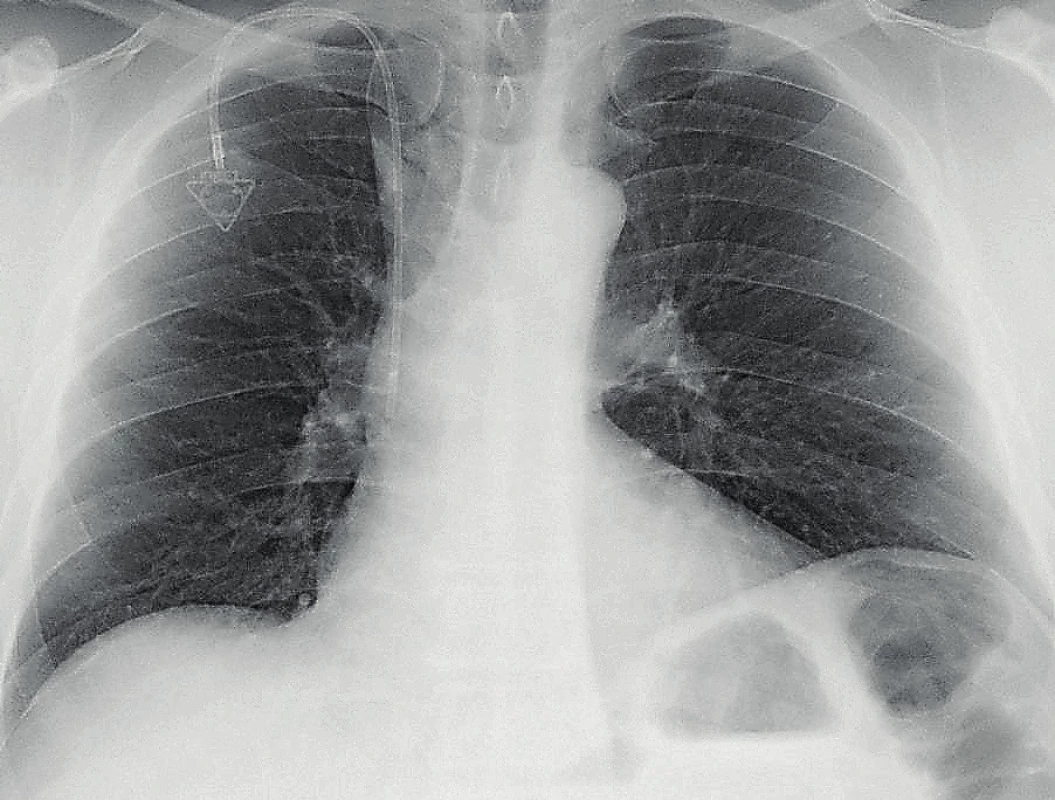
PÉČE O CENTRÁLNÍ ŽILNÍ PORT
Vzhledem k tomu, že po implantaci je zařízení již plně funkční, je možné jej okamžitě začít používat. Po každém použití je však doporučeno provedení proplachu fyziologickým roztokem s případnou aplikací heparinové zátky. Není-li žilní port používán delší dobu, je vhodné provedení proplachu systému jednou za 1–3 měsíce. Po zhojení rány v místě zavedení není pacient ničím omezen a může se věnovat až na ojedinělé výjimky veškerým svým denním aktivitám [2].
KOMPLIKACE PO ZAVEDENÍ ŽILNÍHO PORTU
Komplikace po zavedení žilního portu je možno rozdělit na časné (do 30 dnů od implantace) a na komplikace pozdní (déle než 30 dní po zavedení). Časné komplikace jsou popisovány v 7–11,6 % případů, pozdní u 0,6–27 % nemocných [2, 3].
Z časných komplikací připadá v úvahu nechtěná punkce doprovázející tepny (krkavice, podklíčková tepna) s následným možným vznikem hematomu v okolí místa vpichu, případně i hemothoraxu s rozvojem hemoragického šoku. Poranění plíce během punkce centrální žíly může vést k rozvoji pneumothoraxu, který může být zcela asymptomatický, ovšem může vést i k rozvoji tenzní formy se závažným ohrožením zdraví nemocného (obr. 6). Při provádění punkce centrální žíly pod ultrasonografickou a skiaskopickou kontrolou je však riziko poranění tepny nebo poranění plicního parenchymu velmi malé (0,5 %). Významná vzduchová embolie je vzácná, přesto je třeba důsledně bránit nasátí vzduchu do žilního systému při manipulaci s instrumentáriem, zejména u nemocných s negativním tlakem v pravé srdeční síni. Jinou možnou časnou komplikací je vznik hematomu v místě vytvořené podkožní kapsy pro komůrku portu vlivem nedostatečné hemostázy – není-li hematom evakuován, může vést k obtížnému hojení rány s možností následné infekce. Špatné umístění konce portové cévky může vést k rozvoji poruch srdečního rytmu nebo ke vzniku trombózy [2].
Obr. 6. Skiagram hrudníku prokazuje parciální pneumothorax vpravo s jasně viditelnou linií viscerální pleury částečně kolabované pravé plíce (šipky) 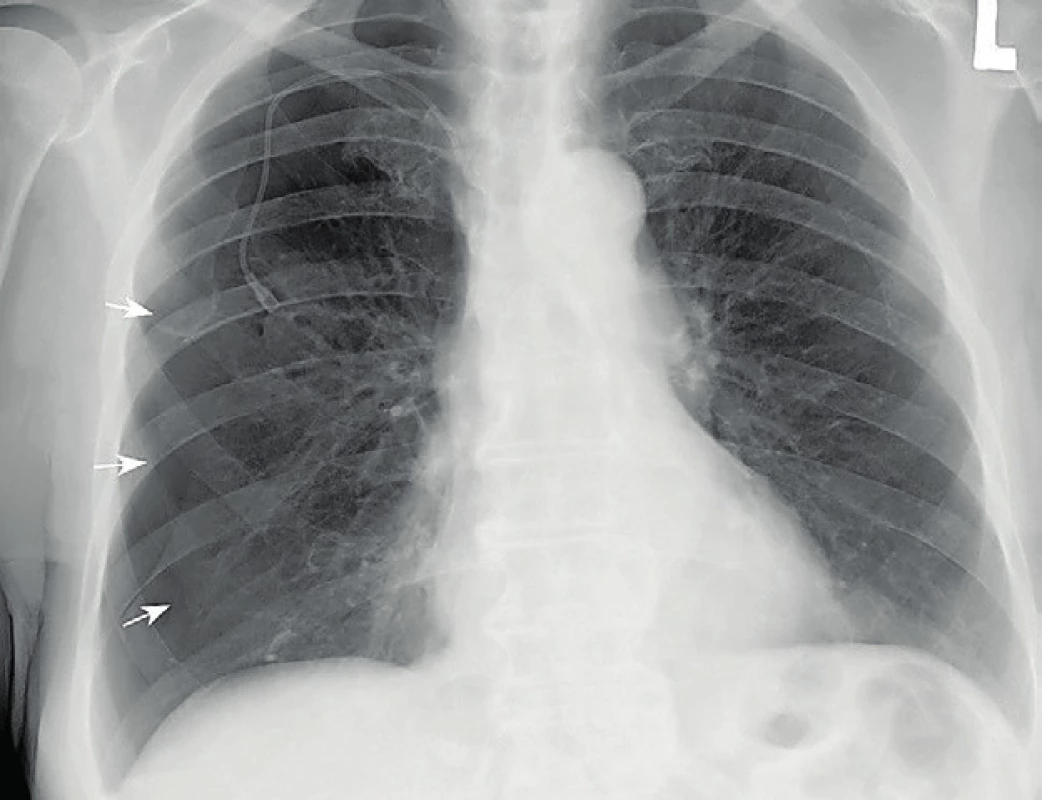
Nejčastějšími pozdními komplikacemi po zavedení žilního portu jsou trombóza a infekce. Trombóza je popisována u 0–16 % nemocných, přičemž se může manifestovat jako krevní sraženina pouze v okolí hrotu portové cévky, jako fibrinová pochva postihující delší úsek katétru od jeho konce, jako krevní sraženina v komůrce portu a nebo jako trombóza mateřské žíly na podkladě jejího poranění v místě punkce. Klinické projevy trombózy vlastního portu se obvykle projeví nemožností provést proplach systému a stav je možno řešit podáním malého množství trombolytika, což obvykle vede k jeho zprůchodnění. Trombóza mateřské žíly se obvykle projeví otokem končetiny a bolestivostí krku či ramene na postižené straně. Metodou volby k jejímu potvrzení je ultrasonografické vyšetření, a pokud se trombóza prokáže, je indikována dlouhodobá antikoagulační léčba. Žilní port není nutno ve většině případů odstranit, extrakce je však nutná při neúspěchu antikoagulační léčby a progresi trombózy do horní duté žíly či k bazi lební [2, 4, 5].
Infekční komplikace jsou udávány u 2,6–27 % nemocných se zavedeným žilním portem. Infekce může být buď lokální, nebo systémová. Lokální infekce postihuje okolí portové komůrky a jejím zdrojem je nejčastěji Staphylococcus epidermidis. Klinicky se projeví bolestivostí, zarudnutím a otokem v oblasti komůrky portu. Jsou-li známky přítomnosti hnisu (vytékání hnisu z rány, fluktuace, ultrasonograficky potvrzená tekutinová kolekce), je nutno systém extrahovat. Systémová infekce se může projevit epizodami febrilií, zimnice a třesavky následujícími vždy po proplachu žilního portu a definitivně je potvrzena pozitivitou hemokultur. Odstranění portu je doporučováno, pokud bakterémie trvá déle než 72 hodin po zahájení antibakteriální léčby [2, 4, 5].
Fragmentace katétru je pozdní komplikací, která se může projevit třemi způsoby. Tzv. pinch-off syndrom znamená dlouhodobou kompresi cévky mezi 1. žebrem a klíční kostí v případě infraklavikulárního přístupu a může vést k uzávěru, perforaci, nebo dokonce k úplnému odtržení části katétru a její embolizaci do plicního řečiště. Rozpojení portové cévky s komůrkou může vzniknout při chybě v napojení těchto dvou částí a projeví se intenzivní bolestivostí během používání systému. Ruptura katétru je velmi vzácná, příčinou může být vada materiálu, nevhodné umístění nebo uzávěr katétru s následným vysokotlakým proplachem (např. při CT vyšetření, není-li port na vysokotlakou injekci dedikován) [4, 5].
Konec katétru může rovněž migrovat retrográdně z obvyklého umístění na hranici HDŽ a pravé srdeční síně do stejnostranné jugulární žíly nebo kontralaterální brachiocefalické žíly, což může vést k poruše jeho funkce a trombózám. Mechanismus migrace je nejspíše multifaktoriální, častěji je tato komplikace pozorována u kratších katétrů, které nebyly svým koncem zavedeny až do úrovně kavoatriální junkce, dalším rizikovým faktorem je obezita s možností dislokace cévky do měkkých tkání podkoží. V případě potvrzení tohoto jevu je indikován pokus o endovaskulární repozici [4, 5] – obrázky 7 a 8.
Obr. 7. Dislokace konce portové cévky do levé brachiocefalické žíly (šipky) 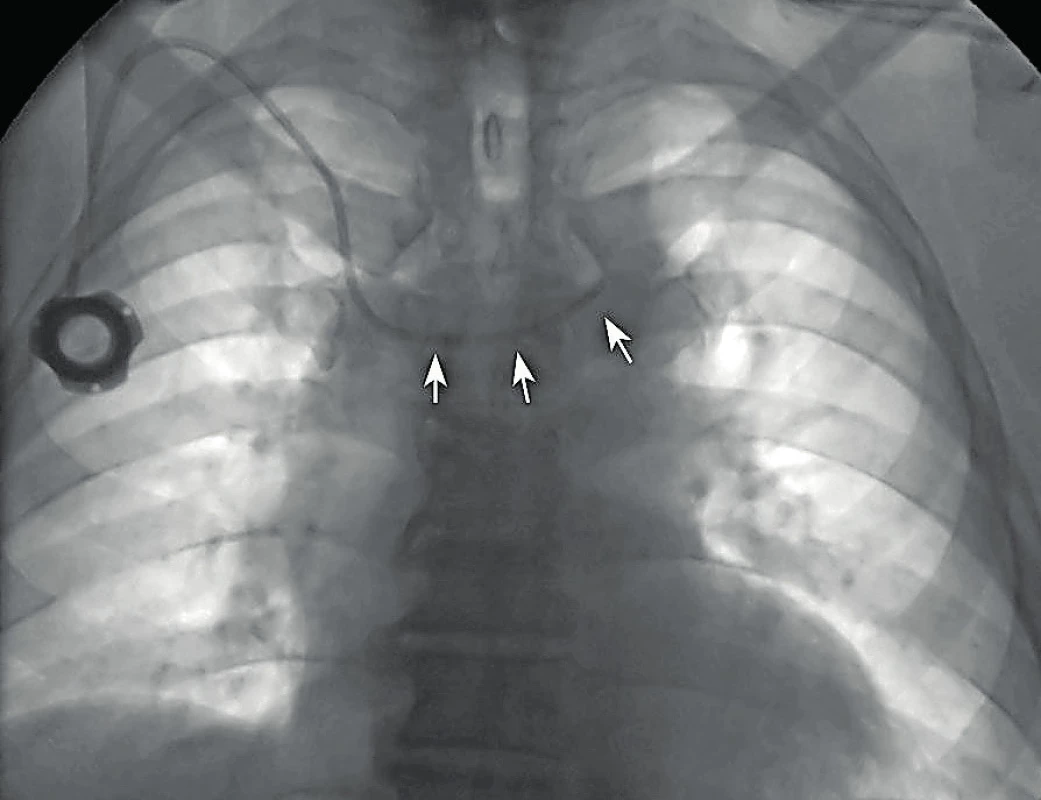
Obr. 8. Endovaskulární repozice konce dislokované cévky zpět do horní duté žíly pomoc katétru typu „pigtail“ zavedeného cestou pravé femorální žíly 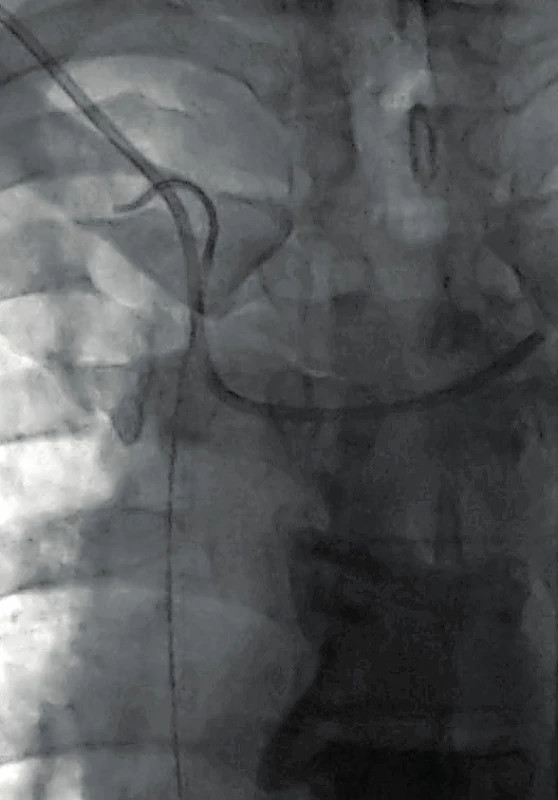
Defekt portové komůrky znamená riziko extravazace léčiva do okolních tkání, což zejména při podávání chemoterapeutik může vést k rozsáhlým nekrózám (obr. 9). Příčinou může být vysokotlaká injekce, při průkazu defektu je nutná explantace žilního portu. K extravazaci léčiva může však dojít i u nepoškozené komůrky, a to v případě špatného zavedení portové jehly. Prevencí této komplikace je důsledná aspirace krve a proplach systému při každém použití ještě před začátkem podávání vlastní léčby [4, 5].
Obr. 9. Extravazace kontrastní látky z komůrky portu jako známka jejího poškození (šipky) 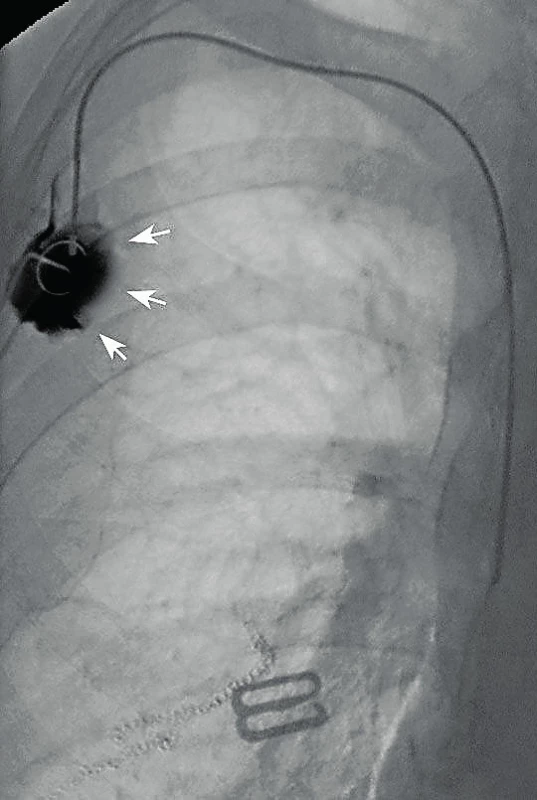
ZÁVĚR
Centrální žilní port představuje adekvátní zařízení k zajištění dlouhodobého cévního přístupu s nízkým rizikem komplikací. Upřednostňováno je jeho zavádění pod kontrolou zobrazovacích metod – ultrasonografie a skiaskopie. Venózní port umožňuje nemocným plně aktivní život bez významných omezení.
Adresa pro korespondenci:
MUDr. Ondřej Renc, Ph.D.
Radiologická klinika FNHK
Sokolská 581
500 05 Hradec Králové
e-mail: ondej.renc@seznam.cz
Zdroje
1. Maňásek, V., Soumarová, R., Kociánová, I., et al. Žilní vstupy v onkologii. Klin. Onkol., 2012, 25 (1), s. 9–16.
2. Walser, E. M. Venous Acess Ports: Indications, Implantation Technique, Follow-Up, and Complications. Cardiovasc. Intervent. Radiol., 2012, 35, p. 751–764.
3. Teichgräber, U. K. M., Kausche, S., Nagel, S. N. et al. Outcome analysis in 3,160 implantationsof radiologically guided placements of totally implantable central venous port systems. Eur. Radiol., 2011, 21 (6), p. 1224–1232.
4. Jordan, K., Behlendorf, T., Surov, A. et al. Venous Access Ports: Frequency and Management of Complications in Oncology Patients. Onkologie, 2008, 31, p. 404–410.
5. Surov, A., Jordan, K., Buerke, M. et al. Port Catheter Insufficiency: Incidence and Clinical-Radiological Correlations. Onkologie, 2008, 31, p. 2–8.
Štítky
Anesteziologie a resuscitace Intenzivní medicína
Článek vyšel v časopiseAnesteziologie a intenzivní medicína
Nejčtenější tento týden
2014 Číslo 3- Bezpečnostní profil metamizolu – systematický přehled
- Aktuální pohled na využití myorelaxancií a jejich antidot v moderní anesteziologii a intenzivní medicíně
- Perorální antivirotika jako vysoce efektivní nástroj prevence hospitalizací kvůli COVID-19 − otázky a odpovědi pro praxi
- Neodolpasse účinně snižuje pooperační bolest
- Neodolpasse jako ideální volba tam, kde je bolest provázena spasmem kosterního svalstva
-
Všechny články tohoto čísla
- Terapeutická hypotermie po zástavě oběhu - máme přestat? Ani náhodou!
- Bužií asistovaná koniotomie (BACT) na prasečím modelu – pilotní studie
- Kontinuální kaudální epidurální analgezie extrémně nedonošeného dítěte – kazuistika
- Postpunkční cefalea v porodnictví
- Úloha krátkodobých betablokátorů v anestezii a intenzivní péči
- Kandidová sepse jako komplikace u pacienta s polytraumatem
- Význam tromboelastografie (TEG) a tromboelastometrie (ROTEM) na jednotke intenzívnej starostlivosti
- Současné možnosti kontinuálního neinvazivního monitorování arteriálního tlaku
- Možnosti využití ultrazvuku u neuroaxiálních blokád
- Centrální žilní porty a jejich využití k zajištění dlouhodobého cévního přístupu
- Premedikace a lačnění
- Valsalvův manévr
- Consensus guidelines for the management of postoperative nausea and vomiting
- Mezioborové stanovisko k používání terapeutické hypotermie u pacientů po zástavě oběhu
- Použití vysokofrekvenční ventilace/oscilace u pacientů s ARDS: jen jako rescue postup!
- Souhlas k pitvě – právní a etický problém?
- Vladimír Lemon a hudba v korespondenci z let 2009–2010
- Anesteziologie a intenzivní medicína
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Postpunkční cefalea v porodnictví
- Valsalvův manévr
- Centrální žilní porty a jejich využití k zajištění dlouhodobého cévního přístupu
- Význam tromboelastografie (TEG) a tromboelastometrie (ROTEM) na jednotke intenzívnej starostlivosti
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



