-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Aktuální pohled na léčbu nově diagnostikovaných nemocných s periferními T-lymfomy a novinky v této oblasti s důrazem na využití brentuximab vedotinu
Current treatment approaches in patients with newly diagnosed peripheral T-cell lymphoma and novel therapies-focusing on brentuximab vedotin
Peripheral T-cell lymphoma (PTCL) is a rare disease with unfavourable prognosis except for low-risk patients with ALK (anaplastic lymphoma kinase)-positive anaplastic large T-cell lymphoma (ALCL). CHOP (cyclophosphamide, doxorubicin, vincristine and prednisone) was for many years the standard first line regimen. Addition of etoposide to the CHOP (CHOEP) resulted in better progression-free survival (PFS) but did not confer any overall survival (OS) benefit. The role of autologous stem cell transplantation as consolidation therapy of first line treatment remains unclear in the absence of randomised phase 3 studies. Prognosis of patients failing first line therapy is extremely poor. Apart from a small cohort of young patients who can benefit from salvage therapy with allogeneic stem cell transplantation, there is no standard therapy showing adequate results in the relapse/refractory setting. A recently published phase 3, randomised, double-blind, double dummy study (ECHELON-2) for newly diagnosed CD30-positive patients with PTCL has shown remarkable benefit of brentuximab vedotin (BV, chimeric anti-CD30 antibody with monomethyl auristatin E) when added to CHP chemotherapy in terms of significantly improved PFS as well as OS compared to standard therapy with CHOP, especially in ALCL patients. In other histological subtypes, benefit of BV was difficult to assess given the small numbers of patients and will have to be studied further. Combination of BV and CHP is considered to be a very potent therapy for CD30 positive treatment-naïve PTCL patients. Brentuximab vedotin is newly reimbursed from 01-AUG-2020 in Czech Republic for newly diagnosed patients with CD30-positive T-cell lymphoma, in combination with cyclophosphamid, doxorubicin and prednison.
Keywords:
T-cell lymphoma – Prognosis – brentuximab vedotin – Transplantation
Autoři: D. Belada
Působiště autorů: IV. interní hematologická klinika, FN a LF UK v Hradci Králové
Vyšlo v časopise: Transfuze Hematol. dnes,26, 2020, No. 3, p. 177-185.
Kategorie: Souhrnné/edukační práce
Souhrn
Periferní T-lymfomy (PTCL) jsou vzácným nádorovým onemocněním se špatnou prognózou s výjimkou nemocných s ALK (anaplastická lymfomová kináza) pozitivním anaplastickým velkobuněčným lymfomem (ALCL) nízkého rizika. Za standardní terapii 1. linie byl mnoho let považován režim CHOP (cyklofosfamid, doxorubicin, vinkristin a prednison). Přidání etoposidu k režimu CHOP (CHOEP) vedlo u mladších nemocných k prodloužení doby do progrese, ale neprokázalo vliv na celkové přežití. Význam konsolidační terapie autologní transplantací po 1. linii léčby je stále nejasný z důvodu chybějící prospektivní randomizované studie fáze 3. Osud nemocných po selhání terapie 1. linie je extrémně nepříznivý. S výjimkou malé části mladších nemocných, kteří mohou profitovat ze záchranné terapie a provedení alogenní transplantace, neexistuje žádná standardní terapie, která by prokazatelně dosahovala uspokojivých dlouhodobých výsledků u relabujících nebo refrakterních pacientů. Nedávno byly publikovány výsledky randomizované, dvojitě zaslepené, dvojitě maskované studie fáze 3 (ECHELON-2), které prokazují, že u nemocných s nově diagnostikovaným CD30 pozitivním PTCL podání brentuximab vedotinu (chimérické monoklonální protilátky anti-CD30 s monometyl auristatinem E) s režimem CHP vedlo nejen k významně delší době do progrese oproti standardnímu režimu CHOP, ale i k delšímu celkovému přežití, a to zejména u nemocných s ALCL. U ostatních histologických subtypů nebyl přínos BV tak dobře hodnotitelný díky menšímu zastoupení a vyžaduje další studium. V současné době tak lze režim BV-CHP považovat za velmi účinnou terapii 1. linie u pacientů s CD30+ PTCL. V České republice má BV nově úhradu od 1. 8. 2020 v 1. linii léčby dospělých pacientů s CD30-pozitivním periferním T-lymfomem v kombinaci s cyklofosfamidem, doxorubicinem a prednisonem.
Klíčová slova:
T-lymfom – prognóza – brentuximab vedotin – transplantace
ÚVOD
Periferní T-lymfomy (PTCL) představují poměrně vzácný typ lymfoproliferací – zaujímají jen cca 10 % všech nehodgkinských lymfomů (NHL) v naší populaci [1]. Odlišná je incidence v Asii, kde PTCL tvoří až 24 % všech NHL [2]. Jedná se o poměrně heterogenní skupinu onemocnění, která se liší svojí biologií, klinickým průběhem a prognózou. S výjimkou několika forem kožních lymfomů se jedná vesměs o klinicky agresivní nádorová onemocnění s nepříznivou prognózou.
Podle aktuálně platné WHO klasifikace jsou v našich podmínkách nejčastějšími podtypy:
- periferní T-lymfom, blíže nespecifikovaný (PTCL-NOS),
- angioimunoblastický lymfom (AITL),
- anaplastický velkobuněčný lymfom (ALCL) – ALK pozitivní nebo ALK negativní.
Ostatní podtypy, jako například hepatosplenický T-lymfom, enteropatický T-lymfom (EATL), podkožní panikulitidě podobný T-lymfom a další, jsou extrémně raritní onemocnění, která se ročně v České republice vyskytují v řádu jednotek případů. I proto léčebná doporučení pro terapii těchto vzácných jednotek se buď extrapolují z výsledků klinických hodnocení léčby ostatních, častějších podtypů, nebo se doporučení odkazují na retrospektivní analýzy z registrů či jen malé sestavy nebo jednotlivé kazuistické případy.
Prognóza nemocných s PTCL byla dosud velmi neuspokojivá. S výjimkou nemocných s ALK pozitivním ALCL nízkého rizika podle mezinárodního prognostického indexu (IPI 0–1), kde je prognóza dokonce o něco lepší než u B-lymfomů, ve všech ostatních případech se jedná o onemocnění se špatnou prognózou, s pravděpodobností přežití v 5 letech mezi 10–30 % – záleží na subtypu lymfomu [3].
Standardem léčby 1. linie u PTCL je po několik desítek let režim CHOP (cyklofosfamid, doxorubicin, vinkristin, prednison). Přidáním etoposidu k režimu CHOP (režim CHOEP) bylo dosaženo lepších výsledků u mladších nemocných, bohužel jen z hlediska delší doby do progrese (progression free survival – PFS), nikoliv ale celkového přežití (overal survival – OS), kde nebyl shledán signifikantní rozdíl [4, 5]. Starší nemocní navíc nejsou schopni režim CHOEP tolerovat z důvodu vysoké hematologické toxicity. Přidání alemtuzumabu (monoklonální protilátky anti-CD52) k režimu CHOP vedlo ke zvýšení celkové léčebné odpovědi, ale za cenu neakceptovatelně vysoké hematologické toxicity, proto výzkum tímto směrem byl ukončen [6]. Romidepsin (histon deacetylázový inhibitor) v kombinaci s režimem CHOP byl také testován v 1. linii v rámci studie fáze 1b/2 – problémem byla také poměrně významná hematologická toxicita [7].
Snaha zlepšit osud nemocných s PTCL v 1. linii použitím některé konsolidační terapie přinesla rovněž rozporuplné výsledky. Radioterapie je smysluplná jen v případě iniciální léčby extranodálního NK/T lymfomu, nazálního typu – tam je nezbytnou součástí léčby 1. linie s velmi dobrými výsledky díky lokální kontrole onemocnění ozářením. V ostatních případech je její význam velmi omezený. Role konsolidační terapie vysokodávkovanou chemoterapií s autologní transplantací (ASCT) je v současné době také nejasná. Data ze studie fáze 2 ukazují na velmi dobré výsledky tohoto postupu, některé další práce ale význam ASCT nepotvrdily, včetně analýzy z dat registru NIHiL české Kooperativní lymfomové skupiny [8–10]. Zásadním problémem je, že neexistuje žádná prospektivní randomizovaná studie fáze 3 studující význam autologní transplantace jako konsolidační terapie 1. linie. Malá část mladších nemocných může být léčena alogenní transplantací – buď jako konsolidační terapie 1. linie při nedosažení kompletní remise, nebo v relapsu onemocnění.
IMUNOTERAPIE U PTCL
Antigen CD30 je univerzálně exprimován na povrchu nádorových T-lymfocytů u všech nemocných s ALCL. U ostatních subtypů PTCL je jeho exprese variabilní, cca mezi 58–64 % u PTCL-NOS, u 43–63 % nemocných s AITL, u cca 55 % pacientů s T-buněčnou leukemií/lymfomem a velmi variabilní u EATL [11, 12]. Snaha o terapii PTCL pomocí monoklonální protilátky proti antigenu CD30 byla zpočátku neúspěšná. Podání samotné anti-CD30 protilátky vedlo ke zcela minimální léčebné odpovědi u nemocných s relabujícími/refrakterními PTCL [13]. Z klinického pohledu jako průlomový krok nutno vnímat vytvoření molekuly brentuximab vedotinu (BV) – konjugátu monoklonální protilátky anti-CD30 a toxinu – monometyl auristatinu E, který je kovalentně na ni navázán. Po vazbě BV na nádorovou buňku dochází k uvolnění toxinu (silný inhibitor mikrotubulů), který vede k usmrcení nádorové buňky. Po průkazu významné klinické efektivity tohoto léku u nemocných s relabujícím/refrakterním ALCL se klinický vývoj přesunul do oblasti léčby 1. linie PTCL [14]. Vývoj byl zahájen standardně studií fáze 1 a byl vytvořen režim BV-CHP, tedy kombinací BV a režimu CHP – záměrně bez vinkristinu, aby nedocházelo k potenciaci neurotoxického efektu BV [15]. Na základě velmi dobrých výsledků studie fáze 1 byla následně iniciována studie fáze 3 s označením ECHELON-2.
ECHELON-2 STUDIE
Charakteristika studie
ECHELON-2 je mezinárodní, dvojitě zaslepená, dvojitě maskovaná, randomizovaná, placebem kontrolovaná studie fáze 3 srovnávající standardní terapii CHOP s režimem BV-CHP, a to na 132 centrech v 17 zemích celého světa. Studie se zúčastnilo i několik center a pacientů z České republiky.
Do studie byli zařazeni dospělí nemocní s nově diagnostikovanými CD30 pozitivními PTCL. Podmínkou byla minimálně 10% pozitivita CD30 podle imunohistochemického (IHCH) vyšetření vzorku nádorové tkáně. Z histologických subtypů PTCL byli vhodní nemocní s ALCL (v případě pacientů s ALK pozitivním ALCL jen vyššího rizika s IPI 2 a více), PTCL-NOS, AITL, T-buněčnou leukemií/lymfomem dospělých, EATL a hepatosplenickým T-lymfomem. Podmínkou regulatorních úřadů bylo zařazení minimálně 75 % (± 5 %) případů nemocných s ALCL k ověření efektivity a bezpečnosti BV u tohoto typu PTCL. Všechny histologické vzorky byly následně podrobeny centrálnímu čtení. Nemocní byli randomizováni 1 : 1 mezi CHOP a BV-CHP, stratifikace probíhala podle histologického subtypu (ALK pozitivní ALCL vs. ostatní histologie) a IPI (0–1 vs. 2–3 vs. 4–5).
Léčba se skládala z 6–8 cyklů (podle rozhodnutí řešitele) a byla složena z cyklofosfamidu 750 mg/m2 v den 1 (D1), doxorubicinu 50 mg/m2 D1, prednisonu 100 mg D1–5 a vinkristinu 1,4 mg/m2 (maximum 2 mg) D1 nebo brentuximab vedotinu 1,8 mg/kg D1. Rozhodnutí o podání konsolidační radioterapie nebo vysokodávkované terapie s autologní transplantací muselo být provedeno před zahájením léčby u každého nemocného. Primárním cílem studie byla doba do progrese podle nezávislé hodnotící komise, která byla definována jako doba od randomizace do selhání terapie, relapsu/progrese, úmrtí nebo zahájení další protilymfomové léčby, která nebyla v úvodu definována. Použití předem definované radioterapie nebo autologní transplantace v případě, že nebyla přítomna progrese lymfomu, nebylo považováno za událost. Sekundárními cíli byly zejména celkové přežití, procento dosažených kompletních remisí a PFS u skupiny pacientů s ALCL. Léčebná odpověď byla hodnocena podle standardních kritérií Lugano 2007.
Výsledky studie
V období mezi roky 2013 a 2016 bylo do studie zařazeno celkem 601 nemocných, z toho 452 bylo následně randomizováno 1 : 1 mezi CHOP (n = 226) a BV-CHP (n = 226). Medián věku nemocných byl 58 let (45–67 let). Obě skupiny byly srovnatelné stran základních prognostických charakteristik (věk, IPI, stadium, performance status, histologické subtypy). Nejpočetněji zastoupenou skupinou byli nemocní s ALCL (48 % ALK negativních, 22 % ALK pozitivních). Přehledně jsou základní charakteristiky obou skupin uvedeny v tabulce 1.
Tab. 1. Základní charakteristiky pacientů ve studii Echelon-2 (adaptováno podle Horwitz S et al., Lancet, 2019) 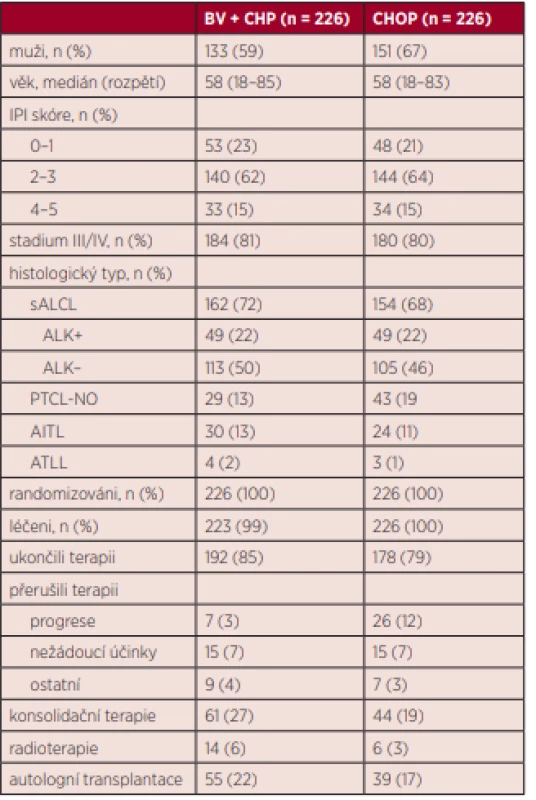
Podání režimu BV-CHP vedlo k 29% redukci rizika progrese oproti CHOP (HR 0,71; 95 % CI 0,54–0,93). Při mediánu sledování 36,2 měsíce byl medián doby do progrese u skupiny BV-CHP 48,2 měsíce vs. 20,8 měsíce u CHOP (p = 0,011) (obr. 1). Primární cíl studie byl tedy naplněn. Subanalýzou podle jednotlivých histologických podtypů byl zjištěn největší benefit u ALCL (ALK+ i ALK–) a PTCL-NOS. U nemocných s AITL byl přínos BV v následné subanalýze statisticky nevýznamný, což mohlo být způsobeno malým počtem nemocných s tímto histologickým typem. Nutno konstatovat, že studie nebyla primárně designována na tento typ subanalýzy podle histologických typů.
Obr. 1. Studie Echelon-2: Graf doby do progrese podle nezávislé hodnotící komise 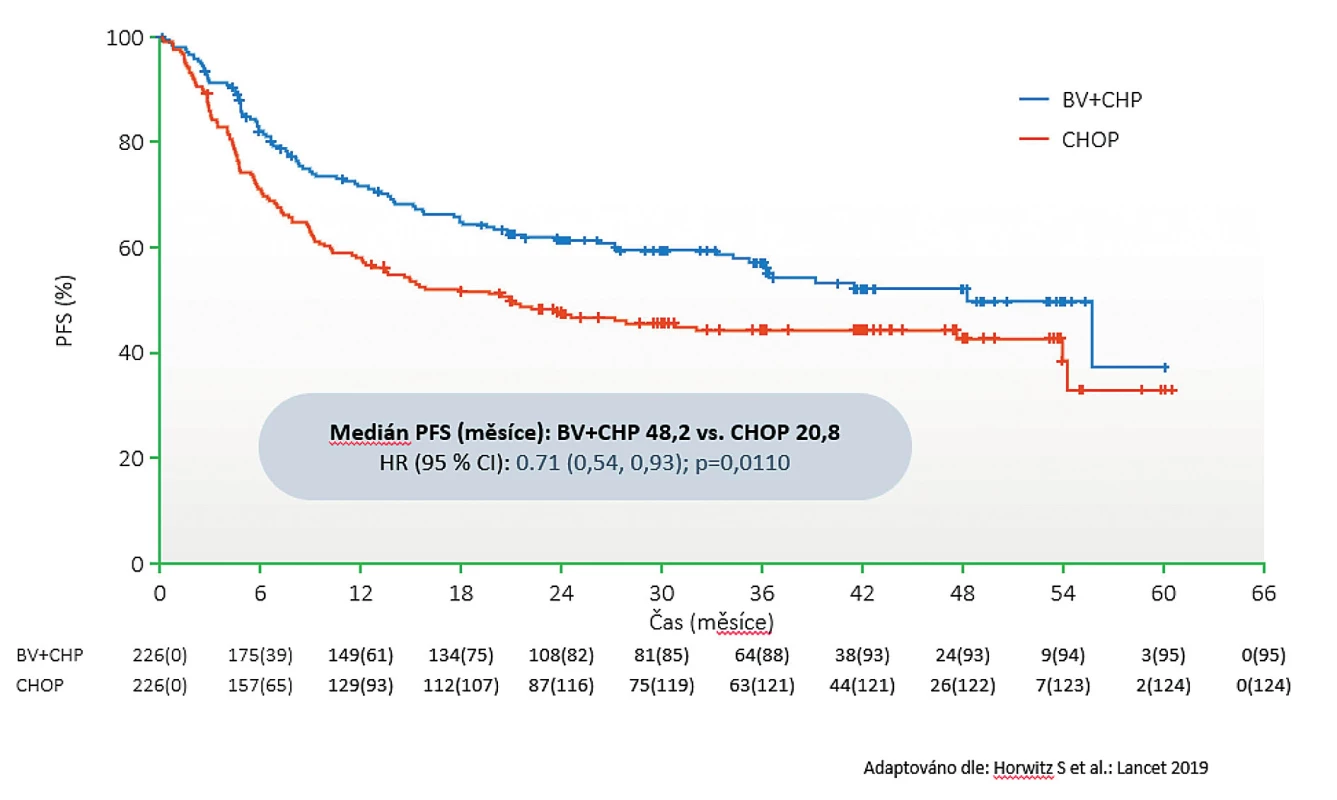
Z hlediska celkového přežití podání režimu BV - -CHP vedlo k 34% redukci rizika úmrtí oproti režimu CHOP (HR 0,66; 95 % CI 0,46–0,95), p = 0,0244. Medián celkového přežití nebyl dosažen u obou ramen (obr. 2). Benefit BV-CHP byl z hlediska histologických subtypů srovnatelný jako při analýze PFS. Relativně největší benefit byl zaznamenán u nejpočetněji zastoupené podskupiny nemocných s ALCL, kde redukce rizika progrese byla celkově 41 % (HR 0,59; 95 % CI 0,42–0,84), p = 0,0031. Vyšší efektivita z hlediska základních parametrů účinnosti (PFS a OS) byla provázena i významně vyšším procentem dosažených kompletních remisí v rameni BV-CHP vs. CHOP (68 % vs. 56 %, p = 0,0066) i vyššího procenta celkových léčebných odpovědí (overall response rate – ORR) ve prospěch režimu BV-CHP oproti CHOP (83 % vs. 72 %, p = 0,0032) (obr. 3). Celkem 59 nemocných v rameni BV-CHP (26 %) a 94 nemocných v rameni CHOP (42 %) vyžadovalo následnou terapii pro relaps, progresi nebo zbytkovou aktivitu lymfomu [16].
Obr. 2. Studie Echelon-2: Graf celkového přežití podle nezávislé hodnotící komise 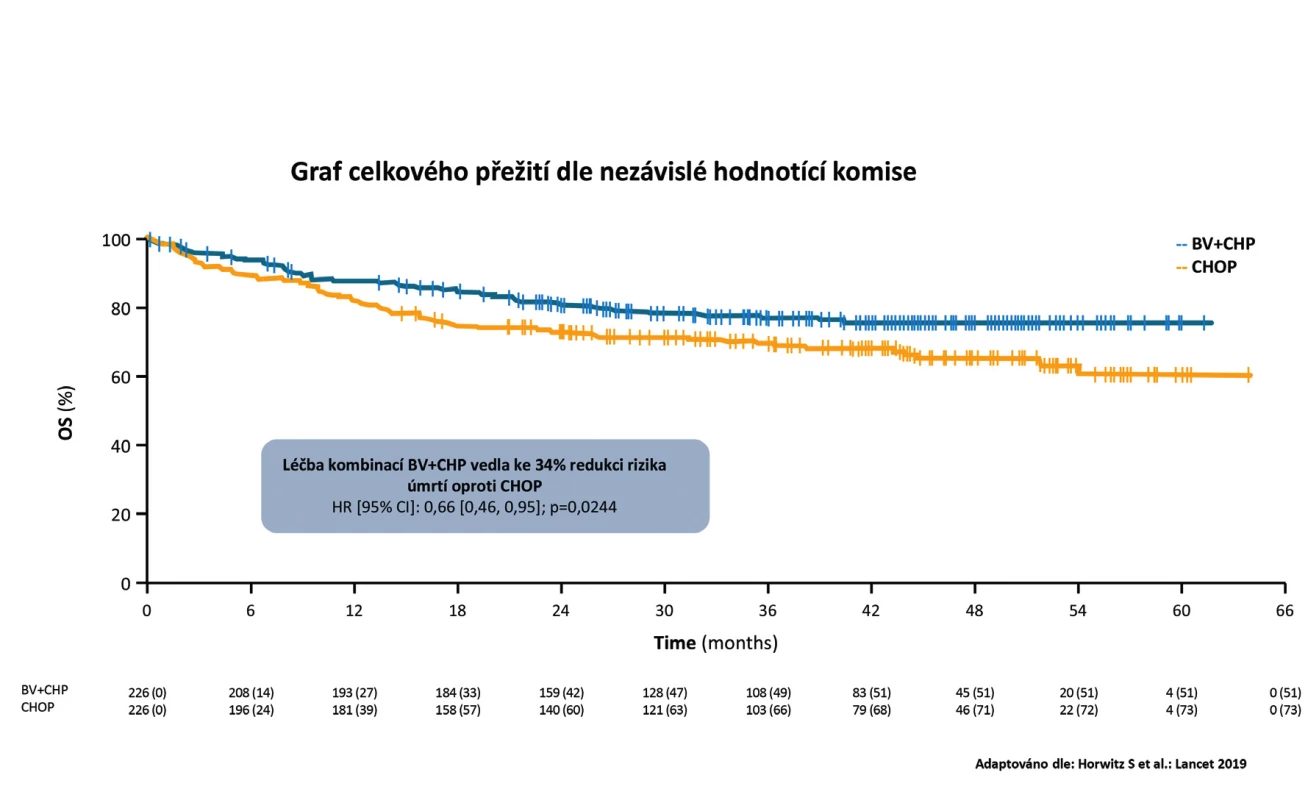
Obr. 3. Studie Echelon-2: Souhrn celkové léčebné odpovědi na konci léčby podle nezávislé hodnotící komise 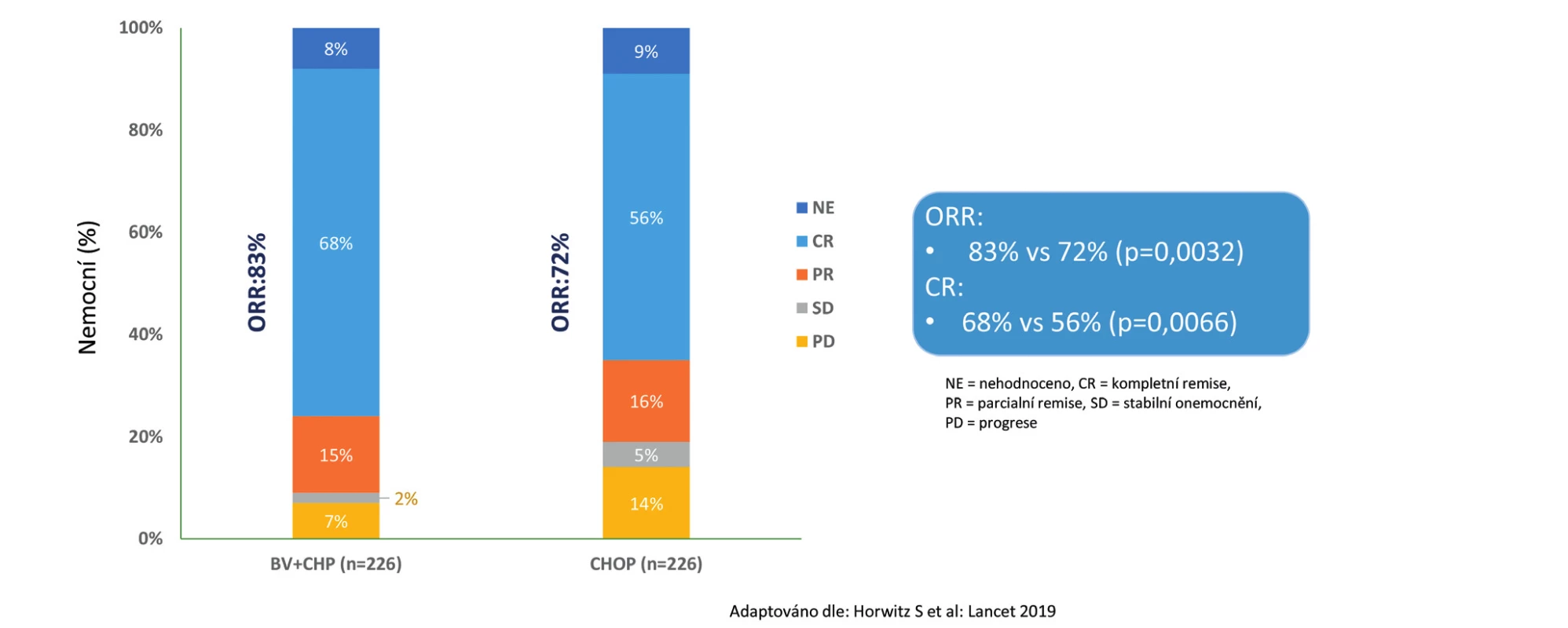
Zajímavé výsledky byly prezentovány stran korelace mezi expresí CD30 a efektivitou léčby. Ze závěrů této subanalýzy vyplývá, že neexistuje žádná korelace mezi stupněm exprese CD30 a účinností režimu BV-CHP [17]. Druhá subanalýza se týká významu autologní transplantace (ASCT) na základě výsledků studie ECHELON-2 u pacientů léčených BV. Z výsledků vyplývá, že vysokodávkovaná terapie s ASCT je výhodnější z hlediska PFS, na druhou stranu nejednalo se o prospektivní, randomizované sledování, ale až následnou post-hoc subanalýzu, která je tak zatížena jistě selekčním bias při volbě daného postupu [18]. Ani z této práce tedy nelze udělat jednoznačný závěr ohledně významu ASCT jako konsolidační terapie 1. linie léčby nemocných s PTCL.
Nežádoucí účinky
Výskyt a závažnost sledovaných nežádoucích účinků byly celkově srovnatelné mezi oběma rameny. O něco vyšší výskyt průjmů (většinou stupně 1) byl zaznamenán v rameni BV-CHP. Procento zaznamenané hematologické toxicity terapie, stejně jako očekávané neuropatie, bylo srovnatelné mezi oběma režimy (obr. 4).
Obr. 4. Studie Echelon-2: Přehled hlavních nežádoucích účinků 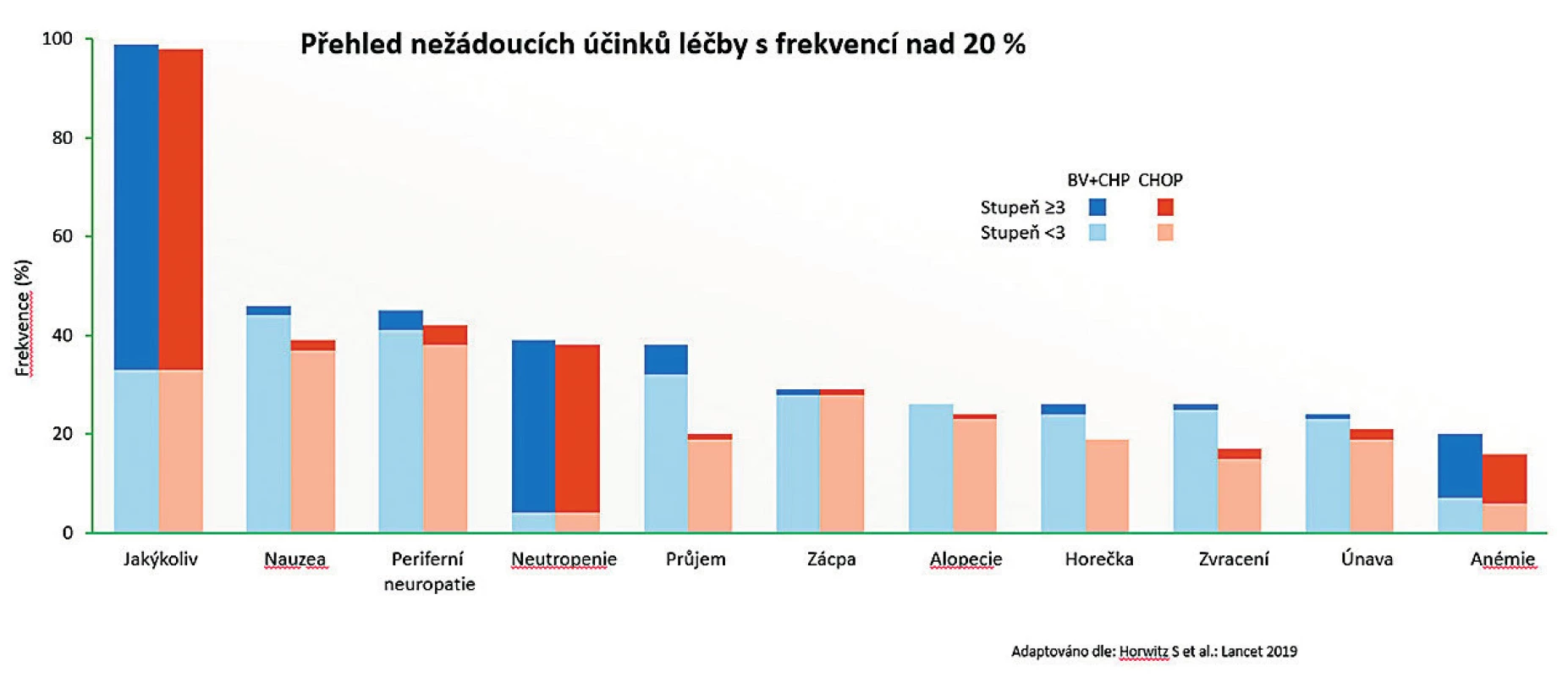
Periferní neuropatie byla velmi pečlivě sledovaným ukazatelem během studie, protože podání vinkristinu i BV je spojeno s tímto nežádoucím účinkem. Celkově byla zaznamenána u 52 % nemocných léčených BV-CHP a u 55 % nemocných léčených CHOP. Zajímavé bylo i sledování dynamiky následné úpravy této neuropatie po ukončení léčby. K úpravě neuropatie na vstupní úroveň před léčbou došlo u 50 % nemocných léčených BV-CHP při mediánu 17 týdnů; u režimu CHOP k tomu došlo u 64 % nemocných s mediánem úpravy 11,4 týdne. Pouze u 2 nemocných léčených BV-CHP došlo ke vzniku neuropatie stupně 3 (u CHOP jen v jednom případě). Nežádoucí účinky vedly k ukončení léčby pouze v 6 % případů v rameni BV-CHP, resp. v 7 % v rameni CHOP [16].
Diskuse k výsledkům studie
Studie ECHELON-2 představuje první prospektivní, randomizovanou studii fáze 3, která prokazuje benefit režimu BV-CHP oproti dosud standardnímu režimu CHOP, a to jak z hlediska redukce rizika progrese (o 29 %), tak zejména prodloužení celkového přežití (redukce rizika úmrtí o 34 %). Nutno poznamenat, že největší benefit této terapie byl zaznamenán u nemocných s ALCL. Důležitým zjištěním bylo, že toxicita (a zejména periferní neuropatie) je srovnatelná mezi oběma režimy. Předchozí pokusy zlepšit výsledky léčby 1. line nemocných s PTCL byly vesměs neúspěšné. Kombinace režimu CHOP s novými léky, jako například romidepsin, alemtuzumab nebo pralatrexate, nevedla ke zlepšení výsledků, a to většinou z důvodu nepřijatelné toxicity [6, 7, 19]. Ani přidání etoposidu v rámci režimu CHOEP v první linii nevedlo k průkazu statisticky významného prodloužení OS v žádné z randomizovaných studií. Největší význam byl shledán u skupiny mladších nemocných do 60 let věku, ale jen z hlediska PFS [5]. Následně byla publikována data z retrospektivních analýz některých registrů (například z českého registru Kooperativní lymfomové skupiny NIHiL), které poukazují na možný benefit přidání etoposidu stran PFS i OS. Bohužel, tyto výsledky jsou zatíženy rizikem selekčního bias – nejedná se o prospektivní randomizované srovnání [10]. Ani v rámci analýzy ze švédského lymfomového registru nebyl v rámci multivariantní analýzy prokázán význam etoposidu na zlepšení celkového přežití v rámci režimu CHOEP [21]. Přehledně jsou srovnány výsledky studie ECHELON-2 s daty z českého a švédského registru v tabulce 2.
Tab. 2. Srovnání výsledků studie Echelon-2 s retrospektivními analýzami z národních registrů. 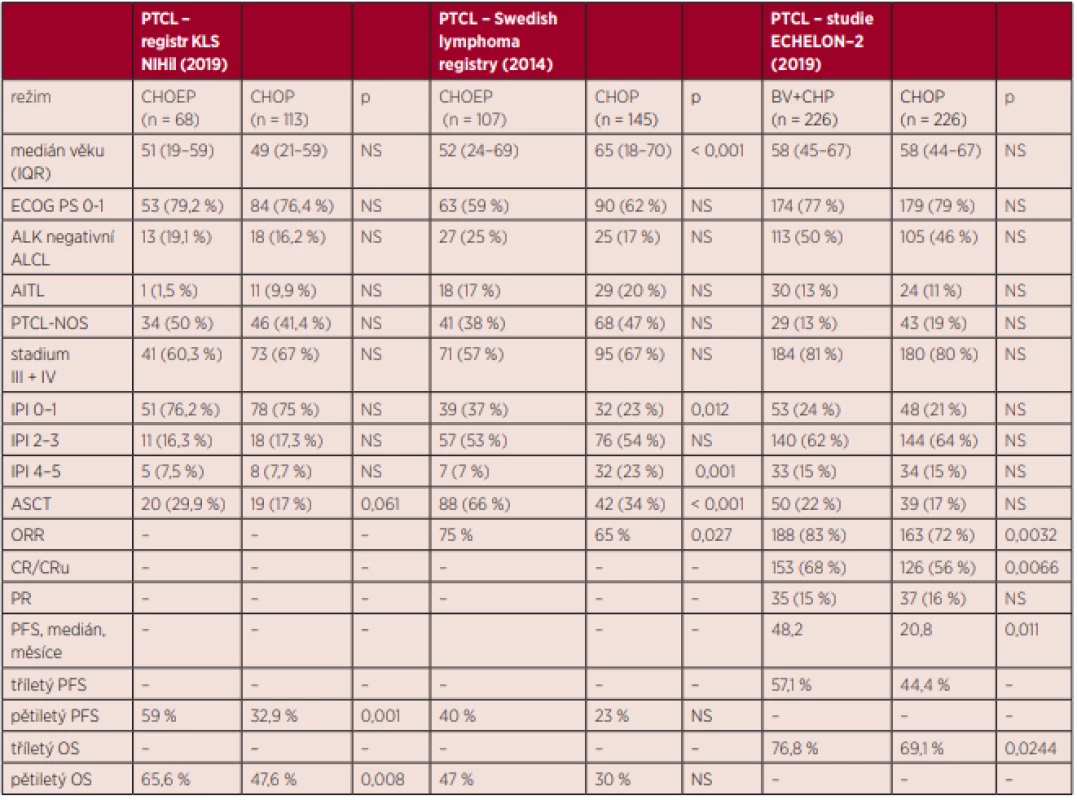
PTCL – periferní T-lymfomy, KLS – Kooperativní lymfomová skupina, IQR – interkvartilové rozdělení, ECOG PS – Eastern Cooperative Oncology Group pefrormance status, ALK – anaplastická lymfomová kináza, ALCL – anaplastický velkobuněčný lymfom, PTCL-NOS – periferní T-lymfom blíže nespecifikovaný, AITL – angioimunoblastický lymfom, IPI – mezinárodní prognostický index, CR – kompletní remise, CRu – nepotvrzená kompletní remise, PR – parciální remise, PFS – období do progrese, OS – celkové přežití, ASCT – autologní transplantace, ORR – celková léčebná odpověď, NS - nesignifikantní Konsolidační léčba 1. linie pomocí ASCT také neprokázala jednoznačný benefit OS. V rámci analýzy švédského registru byl sice shledán PFS i OS benefit ASCT, bohužel se jednalo o retrospektivní analýzu a nikoliv randomizované srovnání, a analýza je tím pádem zatížena rizikem selekčního bias. Navíc mezi oběma skupinami (ASCT a no-ASCT) byly poměrně významné rozdíly z hlediska vstupních charakteristik: věku (nemocní s ASCT byli významně mladší – 57 let vs. 65 let), použité indukční terapie (režim CHOEP byl použit u 66 % skupiny s ASCT vs. 20 % u skupiny no-ASCT) a vstupního IPI – nízké riziko bylo shledáno u 35 % transplantovaných oproti jen 22 % ve skupině no-ASCT [21]. Otázkou významu ASCT se zabývala i analýza z dat registru NIHiL české Kooperativní lymfomové skupiny. V rámci retrospektivní analýzy bohužel nelze jednoznačně význam ASCT zhodnotit z důvodu malého počtu nemocných, kteří byli k této terapii indikováni [10]. V současné době neexistuje žádná randomizovaná studie zkoumající význam ASCT jako konsolidační terapie 1. linie. I přes absenci této studie některé výše uvedené práce ukazují na její benefit, proto je tato terapie považována za možnost konsolidační léčby 1. linie a takto je uvedena v doporučeních pro léčbu nemocných do 65 let s PTCL v České republice [21].
V léčbě nemocných s relapsem PTCL jsou k dispozici data o velmi dobré efektivitě BV v terapii nemocných s relabujícím nebo refrakterním ALCL, kde léčebnou odpověď dosáhlo celkem 86 % nemocných, z toho u 57 % bylo dosaženo CR [14]. Tyto výsledky byly potvrzeny i při dlouhodobém sledování [22]. Účinnost BV v léčbě ostatních podtypů PTCL v relapsu onemocnění je výrazně nižší – léčebná odpověď byla zaznamenána u 41 % s mediánem doby do progrese 6,7 měsíce [23].
Kromě naplnění primárního cíle studie, kterým bylo prodloužení PFS pro celou studijní populaci, se podařilo splnit i klíčový sekundární cíl studie, kterým bylo zlepšení PFS v nejvíce zastoupené populaci, a to u nemocných s ALCL. Požadavek regulatorních autorit na zařazení minimálně 70 % (± 5 %) nemocných s touto diagnózou ale současně způsobil, že zastoupení ostatních histologických subtypů bylo výrazně nižší. Z tohoto důvodu je interpretace výsledků u nemocných s PTCL-NOS a AITL obtížná. Hlavní limitací bylo, že studie nebyla designována na porovnání účinnosti mezi jednotlivými histologickými subtypy. Zatímco u nemocných s PTCL-NOS se v rámci multivariantní analýzy intervaly spolehlivosti stran benefitu PFS i OS pohybovaly na straně BV-CHP, u AITL jsou výsledky léčby z důvodu malého počtu nemocných nejednoznačné a přínos BV je sporný. Dalším důležitým aspektem z hlediska správné interpretace výsledků této studie je pozitivní skutečnost, že medián PFS u kontrolního ramene (20,8 měsíce) je v porovnání s některými jinými kohortami historicky lepším výsledkem. To ale může být způsobeno relativně vysokým zastoupením skupiny nemocných s ALCL (přestože podmínkou pro ALK pozitivní nemocné bylo IPI 2 a více).
I přes pozitivní výsledky studie v této oblasti zůstává celá řada otazníků. Prvním je benefit BV u méně zastoupených histologických podskupin – PTCL-NOS a AITL. Z důvodu malého počtu zařazených nemocných s těmito histologickými subtypy nebyl eventuální přínos BV tak dobře hodnotitelný jako u nemocných s ALCL a vyžaduje další studium. Druhým otazníkem je absence korelace mezi expresí CD30 a účinností léčby BV [17]. Podmínkou zařazení do studie ECHELON-2 byla minimálně 10% exprese antigenu CD30 pomocí IHCH vyšetření. Nelze vyloučit, že efektivita BV může být přítomna i u nemocných s nižší expresí CD30 – toto bude předmětem dalšího výzkumu. Nadále nejasný je bohužel význam konsolidace autologní transplantací. Z výsledků post hoc analýzy vyplývá, že nemocní, kteří byli konsolidováni v rámci studie ECHELON-2 pomocí ASCT po léčbě 1. linie, dosáhli lepších výsledků z hlediska PFS. Nutno ale upozornit, že rozhodnutí o provedení ASCT muselo být provedeno před zahájením léčby. Nejednalo se tedy o randomizované srovnání, proto výsledky mohou být zatíženy významným selekčním bias a těžko z nich lze stanovit nějaké jednoznačné závěry. Další oblastí je otázka přidání etoposidu k režimu CHOP a kombinace s BV, a to zejména u mladších nemocných. Je možné, že tato kombinace by dosahovala ještě lepších výsledků, studie ale nebyla takto designována a pro eventuální průkaz je nutno vyčkat na výsledky dalších klinických studií. I přes zlepšení výsledků léčby nemocných s PTCL vstupem BV do léčby 1. linie jsou výsledky nemocných (zejména při selhání indukční léčby) neuspokojivé. V současné době probíhá celá řada klinických hodnocení testujících nové léky v léčbě PTCL, a to jak v první linii léčby, tak zejména v relapsu onemocnění. Jedná se například o monoklonální protilátku mogamulizumab proti chemokinovému receptoru CCR4, inhibitory histondeacetylázy belinostat a romidepsin, imunitu modulující lék lenalidomid, inhibitor kontrolních bodů nivolumab a další. Významná výzkumná aktivita je zaměřena i na testování léčby pomocí CAR-T (geneticky modifikované T-lymfocyty a chimérickým antigenním receptorem [23].
ZÁVĚR
Studie ECHELON-2 představuje po delší době průlomovou studii v terapii 1. linie nemocných s CD30 pozitivními PTCL. Největší benefit přidání BV byl pozorován u nemocných s ALCL, u ostatních subtypů nebyl benefit BV tak přesvědčivý, což mohlo být způsobeno malým zastoupením v rámci studie – zde nutno vyčkat výsledků dalšího výzkumu v této oblasti. BV v kombinaci s režimem CHP byl 16. listopadu 2018 schválen FDA (US Food and Drug Administration) pro léčbu první linie u ALCL a ostatních CD30 pozitivních PTCL. V rámci EMA (European Medicines Agency) je indikační omezení na ALCL nemocné. V České republice má BV nově od 1. 8. 2020 úhradu v 1. linii léčby dospělých pacientů s CD30-pozitivním periferním T-lymfomem v kombinaci s cyklofosfamidem, doxorubicinem a prednisonem. Jedná se o pacienty o stavu výkonnosti 0–1 podle ECOG. Brentuximab je hrazen do progrese onemocnění, projevů nepřijatelné toxicity nebo do vyčerpání maximálního počtu 8 cyklů kombinační chemoterapie podle toho, co nastane dříve.
Čestné prohlášení
Autor deklaruje tento potenciální konflikt zájmů: Takeda – konzultační činnost, podpora výzkumu, podpora vzdělávání.
Autor práce prohlašuje, že vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Poděkování
Tato práce byla podpořena projektem PROGRES Q40/08.
Do redakce doručeno dne 21. 3. 2020.
Přijato po recenzi dne 16. 4. 2020.
MUDr. David Belada, Ph.D.
4. interní hematologická klinika
Fakultní nemocnice Hradec Králové a Univerzita Karlova,
Lékařská fakulta v Hradci Králové
Sokolská 581
500 05 Hradec Králové 5
e-mail: david.belada@seznam.cz
Zdroje
1. Trněný M. Non-Hodgkinův lymfom v České republice. Transfuze Hematol Dnes. 2019;25(1):81–86.
2. Anderson JR, Armitage JO, Weisenburger DD. Epidemiology of the non-Hodgkin‘s lymphomas: distributions of the major subtypes differ by geographic locations. Non-Hodgkin‘s Lymphoma Classification Project. Ann Oncol. 1998;9(7):717–720.
3. Foss FM, Zinzani PL, Vose JM. Peripheral T-cell lymphoma. Blood. 2011;117(25):6756–6767.
4. Schmitz N, Trümper L, Ziepert M, et al. Treatment and prognosis of mature T-cell and NK-cell lymphoma: an analysis of patients with T-cell lymphoma treated in studies of the German High-Grade NonHodgkin Lymphoma Study Group. Blood. 2010;116(18):3418–3425.
5. Pfreundschuh M, Trümper L, Kloess M, et al. Two-weekly or 3-weekly CHOP chemotherapy with or without etoposide for the treatment of elderly patients with aggressive lymphomas: results of the NHL-B2 trial of the DSHNHL. Blood. 2004;104(3):634–641.
6. Trumper H, Wuff G, Ziepert M, et al. Alemtuzumab added to CHOP for treatment of peripheral T-cell lymphoma (pTNHL) of the elderly: Final results of 116 patients treated in the international ACT-2 phase III trial. J Clin Oncol. 2016;34(15suppl):7500.
7. Dupuis J, Morschhauser F, Ghesquières H, et al. Combination of romidepsin with cyclophosphamide, doxorubicin, vincristine, and prednisone in previously untreated patients with peripheral T-cell lymphoma: a non-randomised, phase 1b/2 study. Lancet Haematol. 2015;2(4):e160–165.
8. Válková V, Trněný M. Současné postavení transplantace krvetvorných buněk v léčbě lymfomů – přehled. Klin Onkol. 2010;23(3):155–164.
9. d’Amore F, Relander T, Lauritzsen GF, et al. Up-front autologous stem-cell transplantation in peripheral T-cell lymphoma: NLG-T-01. J Clin Oncol. 2012;30(25):3093–3099.
10. Janikova A, Chloupkova R, Campr V, et al. First-line therapy for T cell lymphomas: a retrospective population-based analysis of 906 T cell lymphoma patients. Ann Hematol. 2019;98(8):1961–1972.
11. Bossard C, Dobay MP, Parrens M, et al. Immunohistochemistry as a valuable tool to assess CD30 expression in peripheral T-cell lymphomas: high correlation with mRNA levels. Blood. 2014;124(19):2983–2986.
12. Sabattini E, Pizzi M, Tabanelli V, et al. CD30 expression in peripheral T-cell lymphomas. Haematologica. 2013;98(8):e81–e82.
13. Forero-Torres A, Leonard JP, Younes A, et al. A Phase II study of SGN-30 (anti-CD30 mAb) in Hodgkin lymphoma or systemic anaplastic large cell lymphoma. Br J Haematol. 2009;146(2):171–179.
14. Pro B, Advani R, Brice P, et al. Brentuximab vedotin (SGN-35) in patients with relapsed or refractory systemic anaplastic large-cell lymphoma: results of a phase II study. J Clin Oncol. 2012;30(18):2190–2196.
15. Fanale MA, Horwitz SM, Forero-Torres A, et al. Brentuximab vedotin in the front-line treatment of patients with CD30+ peripheral T-cell lymphomas: results of a phase I study. J Clin Oncol. 2014;32(28):3137–3143.
16. Horwitz S, O’Connor OA, Pro B, et al. Brentuximab vedotin with chemotherapy for CD30-positive peripheral T-cell lymphoma (ECHELON-2): a global, double-blind, randomised, phase 3 trial. Lancet. 2019;393(10168):229–240.
17. Illidge T, Horwitz S, Iver S, et al. Response to A+CHP by CD30 expression in the ECHELON-2 trial. Hematol Oncol. 2019;37(S2):abstract 228.
18. Savage K, Radvani A, Horwitz S, et al. An exploratory analysis of brentuximab vedotin plus CHP (A+CHP) in the frontline treatment of patients with CD30+ peripheral T-cell lymphomas (ECHELON-2): impact of consolidative stem cell transplant. Blood. 2019;134(Supplement 1):464.
19. Advani RH, Ansell SM, Lechowicz MJ, et al. A phase II study of cyclophosphamide, etoposide, vincristine and prednisone (CEOP) alternating with pralatrexate (P) as front line therapy for patients with peripheral T-cell lymphoma (PTCL): final results from the T-cell consortium trial. Br J Haematol. 2016;172(4):535–544.
20. Ellin F, Landström J, Jerkeman M, et al. Real-world data on prognostic factors and treatment in peripheral T-cell lymphomas: a study from the Swedish Lymphoma Registry. Blood. 2014;124(10):1570–1577.
21. Belada D, Trněný M a kol. Diagnostické a léčebné postupy u nemocných s maligními lymfomy. X. vydání [on-line]. Praha: Czech Lymproma Study group, Kooperativní lymfomová skupian, Česká hematologická společnost ČLS JEP, 2018 Dostupné na: https://www.lymphoma.cz/_uploads/attachments/KLS_guidelines_10_2018.pdf
22. Pro B, Advani R, Brice P, et al. Five-year results of brentuximab vedotin in patients with relapsed or refractory systemic anaplastic large cell lymphoma. Blood. 2017;130(25):2709–2717.
23. Horwitz SM, Advani RH, Bartlett NL, et al. Objective responses in relapsed T-cell lymphomas with single-agent brentuximab vedotin. Blood. 2014;123(20):3095–3100.
24. https://www.clinicaltrials.gov.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2020 Číslo 3- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Ibrance® – nová šance pro pacientky s HR+/HER2– karcinomem prsu
-
Všechny články tohoto čísla
- COVID-19 a transfuzní služba v ČR
- Regenerující krvetvorba se podobá embryonální krvetvorbě nezávislé na kmenových buňkách
- Příznaky a projevy Erdheimovy-Chesterovy choroby
- Aktuální pohled na léčbu nově diagnostikovaných nemocných s periferními T-lymfomy a novinky v této oblasti s důrazem na využití brentuximab vedotinu
- Léčba multicentrické a unicentrické formy Castlemanovy nemoci
- Tematizace problémů komplexní péče z perspektivy osob s hemofilií
- Hodnocení znalosti transfuzního lékařství u lékařů po promoci v Turecku
- Charakteristika a výsledky léčby mladších nemocných s akutní myeloidní leukemií pod 60 let: Analýza reálných dat z české databáze DATOOL-AML
- Vzácné kožní změny asociované s monoklonální gamapatií: skleredém, skleromyxedém a IgA pemfigus – popis pěti případů a přehled léčebných možností
- Doporučený postup pro použití rekonvalescentní plazmy v léčbě dospělých pacientů s COVID-19
- Doporučený postup při řešení a vyšetřování potransfuzních reakcí
- Konsenzuální doporučení Českého národního hemofilického programu (ČNHP) pro zajištění chirurgických a invazivních výkonů u pacientů s hemofilií, vydání 2., rok 2020
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Příznaky a projevy Erdheimovy-Chesterovy choroby
- Doporučený postup při řešení a vyšetřování potransfuzních reakcí
- Charakteristika a výsledky léčby mladších nemocných s akutní myeloidní leukemií pod 60 let: Analýza reálných dat z české databáze DATOOL-AML
- Aktuální pohled na léčbu nově diagnostikovaných nemocných s periferními T-lymfomy a novinky v této oblasti s důrazem na využití brentuximab vedotinu
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



