-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Závěr života nemocných s nehodgkinským lymfomem, analýza souboru zemřelých během šesti let (2012–2017) na jednom pracovišti, integrace paliativní péče
The last days of patients with non-Hodgkin’s lymphoma - analysis of a sample of deceased patients over a period of 6 years (2012-2017) at one institution and the role of integrating palliative care
Background: Despite the achievements of modern haemato-oncology, non-Hodgkin´s lymphoma remains a potentially life-threatening disease. Population aging and the prolonged survival of patients with haematological malignancy place increasing demands on health care, including decisions as to the type of treatment and care. In haemato-oncology, palliative care is the subject of much discussion, both in literature and practice. This discussion is affected by the difficulties in determining prognosis, the many treatment options available including targeted treatment, the personal standpoints of haematologists themselves, patient transfusion dependence and the limited experience of hospices with haematologically ill patients. There is a lack of studies showing the benefits of palliative care in these patients compared to patents with solid tumours.
Methods: We analysed the last 6 months, 3 months and 1 month of life of 72 treated and deceased patients with non-Hodgkin's lymphoma at the Haemato-oncology Clinic of the University Hospital Olomouc over 6 years (2012–2017).
Results: The place of death was in 90% the hospital, 47% of the patients died directly at the clinic. 43% of the patients died during curative treatment, 57% died during palliative treatment. 29% of the patients had relapsed disease and 29% of the patients were refractory to chemotherapy at the time of death, while 27% died during first-line treatment. In the last 30 days of life, 25 (37%) patients received chemotherapy, 15 patients were in curative and 10 in palliative care. In the last 7 days of life, only 5 (7%) patients were receiving curative chemotherapy. The median number of hospitalizations in the last 6 months of life was 3 (range 0–7). The median days of hospitalization in the last 6 months of life were 32 days (range 0–118), 25 days (range 0–90) in the last 3 months of life, and 11 days (range 0–31) in the last month of life. The median overall survival from diagnosis was 9.2 months.
Conclusion: Despite all the successes of modern haemato-oncology, Non-Hodgkin's lymphoma remains a potentially life-threatening disease. Its treatment is associated with a significant symptom burden and intensive end-of-life care. Some patients receive chemotherapy at the end of their lives, frequent hospitalization is needed, some patients die as a direct result of the disease or its complications, most often in hospital. We believe that comprehensive care for patients with non-Hodgkin's lymphomas should include palliative care, both end-of-life care and early palliative care, in addition to modern anti-cancer therapy.
Keywords:
haemato-oncology – palliative care integration – non-Hodgkin’s lymphoma – end-of-life care (EoLC)
Autoři: R. Urbanová 1; R. Machová 1; R. Szotkowská 1; V. Procházka 1
; M. Labudíková 1; M. Hošťálková 2; A. Hluší 1; T. Papajík 1; O. Sláma 3
Působiště autorů: Hemato-onkologická klinika Fakultní nemocnice Olomouc a Lékařská fakulta, Univerzita Palackého v Olomouci, Olomouc 1; Jsme blízko vám – Institut klinické pastorační péče, z. ú., Olomouc 2; Klinika komplexní onkologické péče, Masarykův onkologický ústav, Brno 3
Vyšlo v časopise: Transfuze Hematol. dnes,26, 2020, No. 2, p. 113-123.
Kategorie: Původní práce
Souhrn
Východiska: Přes úspěchy moderní hemato-onkologie zůstává nehodgkinský lymfom potenciálně život ohrožujícím onemocněním. Stárnoucí populace a prodlužující se přežití nemocných s hematologickou malignitou kladou zvyšující se nároky na zdravotní péči včetně rozhodování o typu léčby a péče. V hemato-onkologii se paliativní péče v literatuře i praxi diskutuje, a to s ohledem na obtíže při stanovení prognózy krevních onemocnění, vzhledem k současným možnostem mnoha linií léčby včetně léčby cílené, postojům samotných hematologů k léčbě, transfuzní závislosti nemocných a malým zkušenostem hospiců s péčí o hematologicky nemocné. Prací, které prokazují přínos paliativní péče u těchto nemocných, je ve srovnání s nemocnými se solidními tumory výrazně méně.
Metody: Analyzovali jsme posledních 6 měsíců, 3 a 1 měsíc života 72 léčených a zemřelých nemocných s nehodgkinským lymfomem na Hemato-onkologické klinice Fakultní nemocnice Olomouc v průběhu 6 let (2012–2017).
Výsledky: Místem úmrtí byla v 90 % nemocnice, přímo na HOK zemřelo 47 % nemocných. 43 % nemocných souboru zemřelo v průběhu kurativní léčby, 57 % zemřelo v průběhu léčby paliativní. 29 % úmrtí bylo v relapsu nemoci, 29 % úmrtí bylo ve stadiu refrakterity na chemoterapii, 27 % úmrtí bylo během léčby první linie. V posledním měsíci života dostávalo chemoterapii 25 (37 %) pacientů, 15 pacientů bylo v léčbě kurativní a 10 v léčbě paliativní. V posledních 7 dnech života bylo chemoterapií léčeno 5 (7 %) pacientů, všichni v léčbě kurativní. Medián počtu hospitalizací v posledních 6 měsících života byl 3 (rozmezí 0–7). Medián počtu dnů hospitalizace v posledních 6 měsících života byl 32 dnů (rozmezí 0–118), 25 dnů (rozmezí 0–90) v posledních 3 měsících života a 11 dnů (rozmezí 0–31) v posledním měsíci života. Medián celkového přežití zemřelých nemocných od stanovení diagnózy onemocnění byl 9,2 měsíce.
Závěr: Přes všechny úspěchy moderní hemato-onkologie zůstává nehodginský lymfom nadále potenciálně život ohrožujícím onemocněním, jeho léčba je spojena s výraznou symptomovou zátěží a intenzivní léčbou na konci života. Část nemocných dostává na konci života chemoterapii, častá je potřeba hospitalizací, část pacientů v přímém důsledku onemocnění nebo jeho komplikací umírá, nejčastěji v nemocnici. Domníváme se, že součástí komplexní péče o nemocné s nehodgkinskými lymfomy by vedle moderní protinádorové terapie měla být také paliativní péče, a to jak terminální péče (end-of-life care), tak časná paliativní péče.
Klíčová slova:
hematoonkologie – nehodgkinský lymfom – integrace paliativní péče – End of life care
Úvod
Incidence i prevalence nehodgkinského lymfomu (NHL) v České republice roste. Podle publikovaných údajů Ústavu zdravotnických informací a statistiky České republiky (ÚZIS) byla v letech 2011–2015 incidence nově diagnostikovaných NHL 14 nemocných na 100 000 obyvatel, s mediánem věku 67 let. NHL je potenciálně život ohrožující onemocnění. Péče o narůstající počty nemocných je náročná po stránce organizační i finanční.
Paliativní péče je podle definice Světové zdravotnické organizace z roku 2002 komplexní, multidisciplinární péče směřující k udržení či zvýšení kvality života nemocných s nevyléčitelnou, život ohrožující chorobou nebo souborem chorob. Nabízí podporu nemocným, ale i jejich blízkým. Zabývá se včasným vyhledáváním a léčbou závažných symptomů – tělesných, psychických, sociálních a spirituálních. Paliativní péče může být poskytována v různých fázích nemoci, nejefektivnější se ukazuje její poskytování v závěru života, jako tzv. péče na konci života (end-of-life-care, EoLC), která se týká zdravotní péče nejen v posledních hodinách a dnech života, ale obecněji v terminální fázi nemoci, která se stala pokročilou, progresivní a nevyléčitelnou. Zabývá se etikou a účinností prováděných lékařských zákroků, práv nemocných na rozhodování a také přidělováním zdrojů v nemocnicích a systémech zdravotní péče. Pokud je paliativní péče poskytována současně s kurativní léčbou (model tzv. časné integrace paliativní péče), pak může znamenat významný přínos pro nemocné, pečovatele a zdravotní systém [1]. Několik kontrolovaných randomizovaných studií provedených u solidních nádorů potvrzuje její efekt na kvalitu života a zvládání symptomů nemoci [2, 3], lepší pochopení prognózy nemoci [4], redukci užívání náročné chemoterapie v posledních týdnech života a obecně užívání méně agresivní péče na konci života [5, 6]. V souvislosti s tím je popsáno i prodloužení přežití onkologicky nemocných [7]. Jsou totiž důkazy o tom, že horší kvalita života a depresivní nálada zkracují přežití nemocných [8–10]. Pacienti pak častěji využili péči hospicovou a byli více spokojeni s péčí na konci života, lépe na tom byly rodiny [4, 7, 11, 12]. Studie vyvrátily mylné představy a obavy, že paliativní péče vede k beznaději a předčasné smrti. Americká společnost klinické onkologie (ASCO) od roku 2012 proto doporučuje u všech nemocných s metastatickým nádorovým onemocněním a nemocných s vysokou symptomovou zátěží souběžnou paliativní péči od stanovení diagnózy [13].
Nemocnice hrají v ošetřování nemocných s nádorovým onemocněním nebo obecně závažným onemocněním důležitou roli. Ze studie Ramireze vyplývá, že v posledním roce života je hospitalizováno až 90 % nemocných a kolem 55 % úmrtí ve Velké Británii je právě v nemocnici [14]. Z podrobnějších analýz Institutu biostatistiky a analýz Lékařské fakulty Univerzity Masarykovy (IBA) pro národní datovou základu paliativní péče, provedených z údajů ÚZIS Polívkou a Švancarou v roce 2017, vyplývá, že v letech 2007–2015 zemřelo v nemocnici 66,9–79,6 % nemocných s hematologickými malignitami (lymfom, mnohočetný myelom, akutní leukemie, myelodysplastický syndrom a myeloproliferativní nemoci), u nemocných s lymfomem to bylo 69,6 %, 6,4 % zemřelo v léčebnách pro dlouhodobě nemocné, 13,5 % doma, na ulici nebo při převozu, v hospicích zemřelo pouze 1,1–5,5 % nemocných s hematologickými malignitami (3,7 % nemocných s lymfomy). Z celkového počtu zemřelých nemocných s lymfomem zemřelo na akutních lůžkách 81,3 %, na lůžkách následné péče 18,2 %.
Výzkum provedený v osmdesátých letech ve Velké Británii přitom zdokumentoval nedostatky v péči o umírající pacienty v nemocnicích. Studie Rogerse z roku 2000, čerpající ze zkušeností pozůstalých, hodnotila zkušenosti s péčí v posledním roce života. Ačkoliv přístup lékařů a ošetřovatelů byl výborný nebo dobrý, dotázaní vyjadřovali nespokojenost s dehumanizací, cítili, že na jejich individuální potřeby a přání nebyl brán zřetel [15]. Ošetřovatelé se vyhýbali setkání se smrtí [16]. Dunneová a Sullivanová v roce 2000 popsaly názory rodin na prostředí nemocnic. Rodiny poukazovaly na nedostatek soukromí, na nedostatečnou komunikaci, stěžovaly si, že nebyly přizvány k péči o své příbuzné [17]. V nemocniční paliativní péči byla i v dalších studiích shledána řada nedostatků, tj. kvůli aspektům lidskosti, schopnosti mírnit úzkost. Sláma uvádí, že paliativní péči na náležité odborné úrovni (lege artis) nelze v České republice v roce 2016 považovat za běžně dostupnou a garantovanou zdravotní a sociální službu. Z toho podle něj vyplývá naléhavá potřeba koncepčního rozvoje obecné a specializované paliativní péče [18].
Earle a kolektiv ve své studii uváděj, že nemocní s nádorovým onemocněním na konci života si přejí mít pohodlí, důstojnost a soukromí [19]. V roce 2004 stejný autor s kolektivem identifikovali ukazatele potenciálně příliš agresivní péče u nádorových onemocnění na konci života. Ta zahrnovala vícečetné návštěvy pohotovosti, vysoký počet dnů strávených v nemocnici, úmrtí v nemocnici a nedostatečné využití hospicových služeb [20]. Temel a kolektiv v randomizované kontrolované studii časné paliativní péče u nemocných s pokročilým metastazujícím nemalobuněčným karcinomem plic zjistili, že příliš agresivní péče na konci života může přežití zkrátit. Jako agresivní péči na konci života autoři definují takovou péči, která zahrnuje chemoterapii v posledních 14 dnech života, nevyužívání péče hospicové a přijetí k hospicové péči v čase kratším než 3 dny [7]. Další studie Wrighta a kolektivu poukazovala na vztah agresivní péče na konci života a snížení kvality života nemocných spolu se zvýšeným výskytem psychických poruch u pozůstalých pečujících [21]. Práce Gonsalvese prokazuje efekt včasné konzultace paliativního týmu na snížení míry agresivní péče u nádorových onemocnění v posledních 30 dnech života [22]. K podobným závěrům dospěli také Barbera a kolektiv, kteří posuzují EoLC v kratším čase než předchozí autoři, v posledních 14 dnech života [23].
Nemocní s hematologickými malignitami výrazně méně využívají specializované paliativní péče včetně péče hospicové [24] a naopak častěji podstupují agresivní péči na konci života [25]. Přitom mají symptomovou zátěž (fyzickou i psychickou) srovnatelnou nebo dokonce vyšší než pacienti s pokročilými solidními tumory [26–28]. Paliativní péči poskytují hematologové sami v rámci obecné paliativní péče, a to zcela nezávisle na specialistech v paliativní péči. Specialisté na paliativní péči by přitom mohli a měli poskytovat péči nemocným s vysokým stupněm zátěže, s velkou prognostickou nejistotou, s relativně špatnou prognózou. Jejich role spočívá v tom, že pomáhají v dobré kontrole symptomů nemoci, pomáhají v komunikaci, slouží jako komunikační most mezi hematologem a nemocným [29, 30]. Roste množství literárních dat o tom, že hematologicky nemocným se nedostává paliativní péče [24, 25, 31, 32]. Hematologové nemají zkušenost ze spolupráce se specialisty na paliativní péči, mohou tak mít nedůvěru nebo mylné představy o paliativní péči [33]. Paliativní péče není buď, anebo, ale doplněk péče hematologa. Hematolog doporučením paliativní péče nechce vzít naději [34]. Pokud jsou sami nemocní dotazováni na preference, říkají, že chtějí být informováni otevřeně, i když je prognóza špatná [35, 36]. Nemocní zpochybňují myšlenku nepodání nepříznivé informace [37]. Nemocní, kteří se dostávají k paliativní péči, jsou schopni nasměrovat svoje naděje z úplného vyléčení k dobré kontrole příznaků, prodloužení života při jeho dobré kvalitě se svými blízkými. Touha zachovat naději je tak slučitelná s paliativní péčí. Studie naznačují, že časná paliativní péče může skutečně existovat, usnadnit pochopení prognózy nemoci a nevede k větší úzkosti nebo depresi [4, 7]. Hematolog pracuje nezávisle na dalších medicínských profesích, což může vést ve vztahu k nemocnému k silnému pocitu vlastnictví a pocitu, že musí uspokojit všechny potřeby svého nemocného, ale současně tak může bránit větší míře zapojení specialistů na paliativní péči [33].
Henson na souboru 681 nemocných s nádorovým onemocněním včetně 54 nemocných s hematologickou malignitou studoval EoLC v posledních 3 měsících života, která je v takto daném období považována za agresivní péči, tj. 2 a více návštěv na pohotovosti, více než 30 dnů hospitalizace a úmrtí v nemocnici. Taková péče byla častěji poskytována právě u hematologických malignit ve srovnání se solidními tumory. Její poskytování se v celém souboru zmenšilo v případě dobře dostupné komunitní paliativní a ošetřovatelské péče a v případě pravidelných návštěv praktického lékaře v domácím prostředí [38].
Chybí ale větší výzkumy, které by definovaly jedinečné potřeby hematologicky nemocných v průběhu léčby stejně jako na konci života [39–41]. Do současnosti neexistuje žádné formální doporučení zapojení paliativní péče do péče o nemocné s hematologickou malignitou.
Cíle práce
- Popsat soubor zemřelých nemocných s NHL na Hemato-onkologické klinice Fakultní nemocnice Olomouc (HOK FNOL) v průběhu 6 let (2012–2017) s ohledem na věk, pohlaví, podtyp onemocnění, stav nemoci, předchozí léčbu, cíl, intenzitu léčby (kurativní nebo paliativní) a výskyt refrakterity na chemoterapii v době úmrtí.
- Zdokumentovat počet nově diagnostikovaných nemocných s NHL, všech hospitalizovaných nemocných s NHL a nemocných léčených chemoterapií pro NHL na HOK FNOL v průběhu 6 let (2012–2017).
- Popsat na sledovaném souboru zemřelých nemocných výskyt faktorů považovaných v EoLC za ukazatele agresivní léčby (počet dnů hospitalizace v nemocnici v posledních 3 a jednom měsíci života, podané chemoterapie v posledním měsíci a 7 dnech života), popsat místo a příčinu úmrtí. Dále analyzovat počty hospitalizací a počty dnů hospitalizace v posledních 6 měsících života, charakterizovat výkonnostní stav nemocného (Karnofského skóre) v posledním měsíci života.
- Diskutovat problémy a překážky v poskytování paliativní péče u hemato-onkologicky nemocných a zamyslet se nad možnostmi řešení.
Soubor a metody
Na HOK FNOL zemřelo s diagnózou NHL od 1. 1. 2012 do 31. 12. 2017, tedy v průběhu 6 let, 72 nemocných, 51 mužů a 21 žen, medián věku v době úmrtí byl 70 let, věkové rozmezí 27–96 let. Celkem 39 nemocných (54 %) bylo ve věku nad 70 let (tab. 1).
Tab. 1. Charakteristika souboru zemřelých nemocných s NHL na HOK 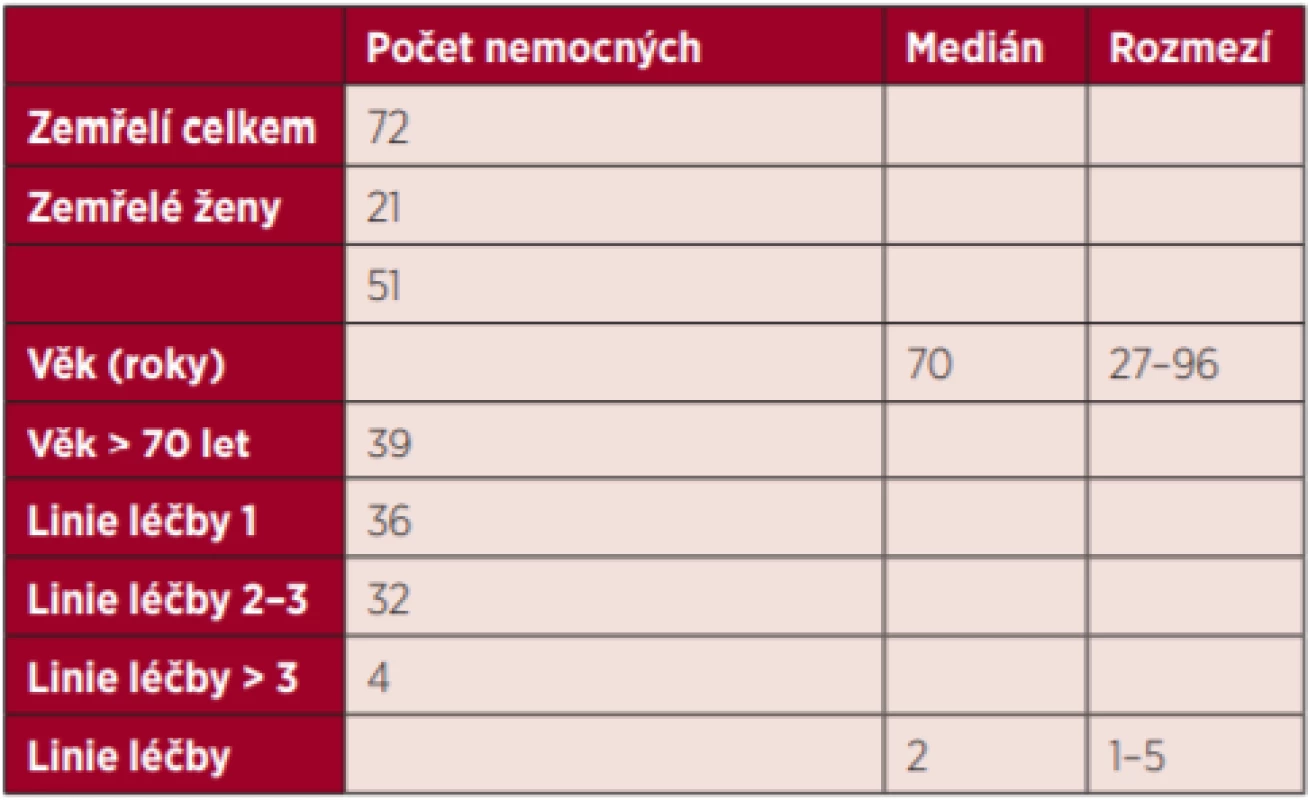
Zastoupení jednotlivých histologických podtypů lymfomů souboru zemřelých nemocných uvádí graf 1. Relativně častěji byly v souboru zemřelých nemocných zastoupeny histologicky agresivní formy NHL, tj. difuzní velkobuněčný lymfom (DLBCL) (26 nemocných, 36 %), lymfom z plášťových buněk (MCL) (7 nemocných, 10 %), lymfom centrálního nervového systému (CNS) (5 nemocných, 7 %), Burkittův lymfom (4 nemocní, 6 %), T nehodgkinský lymfom (7 nemocných, 10 %).
Graf 1. Rozdělení souboru zemřelých nemocných podle typu NHL 
Celkem 36 nemocných absolvovalo 1 linii léčby, 32 nemocných absolvovalo 2–3 linie léčby a 4 nemocní absolvovali více než 3 linie léčby (tab. 1). Pokud budeme blíže analyzovat typ podané léčby, potom 64 nemocných (89 %) bylo léčeno chemoterapií, 12 nemocných bylo léčeno současně chemoterapií i radioterapií, 15 nemocných chemoterapií a následně autologní transplantací krvetvorných buněk, jeden nemocný chemoterapií a alogenní transplantací, chemoterapii a následně biologickou léčbu absolvovali 4 nemocní. Pouze radioterapií byli léčeni 3 nemocní a další 3 nemocní byli léčeni pouze kortikoterapií.
V uvedeném období 6 let bylo na HOK nově diagnostikováno celkem 549 nemocných s NHL (data získaná z registru Kooperativní lymfomové skupiny). U celkem 727 nemocných s NHL ve stadiu nově diagnostikované nemoci a v době relapsu nemoci proběhlo 2 290 hospitalizací (data získaná z nemocničního informačního systému). Celkem 702 nemocných bylo léčeno chemoterapií v léčbě první linie nebo v relapsu, ambulantně byla podána chemoterapie 220 nemocným a 540 nemocným byla podána chemoterapie za hospitalizace, u 68 nemocných byla chemoterapie podávána ambulantně i za hospitalizace. Tato data byla získána ze systému Computer aided Therapy for Oncology (CATO).
Ke statistickému hodnocení byly použity metody popisné statistiky a Kaplanova Meirova analýza. Sledovanou veličinou bylo celkové přežití zemřelých nemocných a celkové přežití nově diagnostikovaných nemocných s NHL z let 2012–2017. Křivka přežívání byla odhadována Kaplanovou Meierovou metodou. K analýzám byla využita data nemocných HOK FNOL z registru nemocných Kooperativní lymfomové skupiny, dále data z nemocničního informačního systému FNOL a data ze systému CATO pro přípravu chemoterapií.
Výsledky
Protinádorová léčba v posledních 6 měsících života: V posledních 6 měsících života dostávalo chemoterapii 61 nemocných (85 %) všech zemřelých nemocných sledovaného souboru.
Protinádorová léčba v posledních 30 dnech života a Karnofského skóre hodnocení celkového stavu: V posledních 30 dnech života bylo chemoterapií léčeno 25 nemocných (37 %). Z nich bylo 15 nemocných v léčbě kurativní, 10 nemocných v péči paliativní. Celkový stav nemocných v posledních 30 dnech života byl hodnocen podle Karnofského skóre. Data bylo možno dohledat u 44 nemocných, z nich 14 (32 %) mělo skóre 50 a méně, 15 (34 %) mělo Karnofského skóre 60–70 % a 15 (34 %) mělo Karnofského skóre 80–100 %.
Protinádorová léčba v posledních 7 dnech života: 5 nemocných dostávalo chemoterapii v posledních 7 dnech života, jednalo se ve všech případech o nemocné v kurativní léčbě. Žádný nemocný v paliativní léčbě nebyl chemoterapií léčen v posledních 7 dnech života.
Pokud jsme analyzovali typ léčby, v průběhu které nemocní zemřeli, potom 30 nemocných (43 %) zemřelo v průběhu kurativní léčby, 20 (29 %) zemřelo v léčbě paliativní, ale primárně byli léčeni s kurativním záměrem, a 19 (28 %) zemřelo v paliativní léčbě, která byla léčbou paliativní od okamžiku stanovení diagnózy. Paliativní terapií rozumíme nízce dávkovanou chemoterapii, kortikoterapii, paliativní radioterapii a léčbu symptomovou (graf 2).
Graf 2. Rozdělení souboru zemřelých nemocných podle typu léčby v době úmrtí 
Počet hospitalizací v posledních 6 měsících života: Medián počtu hospitalizací v posledních 6 měsících života je v souboru nemocných 3 (rozmezí 0–7).
Délka hospitalizace v posledních 6 měsících (resp. ve 3 a 1 měsíci) života: Medián počtu dnů hospitalizace v posledních 6 měsících života je 32 (rozmezí 0–118 dnů), medián počtu dnů hospitalizace v posledních 3 měsících života je 25 (rozmezí 0–90 dnů) a medián počtu dnů hospitalizace v posledním 1 měsíci života je 11 (rozmezí 0–31 dnů) (tab. 2).
Tab. 2. Charakteristika péče EoLC v posledních 6, 3 a 1 měsíci života nemocných s NHL na HOK 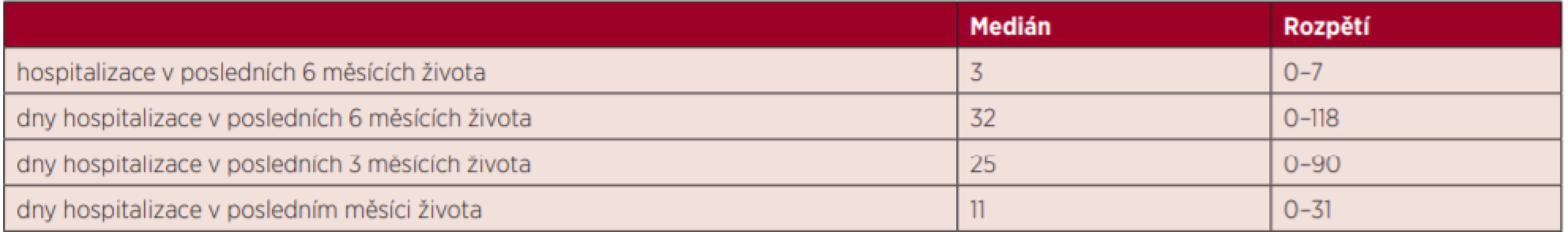
Stav onemocnění v době úmrtí: 61 nemocných (85 %) mělo aktivní nádorové onemocnění, 6 (8 %) zemřelo v remisi nemoci, u 5 (7 %) nebyl znám stav nemoci v době úmrtí. Ve skupině nemocných s aktivním onemocněním v době úmrtí 19 (27 %) zemřelo v léčbě první linie, 21 (29 %) zemřelo v relapsu a 21 (29 %) bylo refrakterních na chemoterapii (graf 3).
Graf 3. Rozdělení souboru zemřelých nemocných podle stavu nemoci v době úmrtí 
Místo úmrtí: Místem úmrtí byla v 34 případech oddělení HOK (standardní oddělení a jednotka intenzivní péče), dalších 5 nemocných zemřelo po překladu z HOK na Klinice anesteziologie, resuscitace a intenzivní medicíny (KARIM) FNOL, na jiných odděleních FNOL zemřelo 7 nemocných. V ostatních nemocnicích mimo FNOL zemřelo 12 nemocných. U 8 nemocných není místo úmrtí známo. Pouze 3 nemocní zemřeli v péči hospicové a 3 v léčebně pro dlouhodobě nemocné (LDN). Celkem 90 % nemocných léčených s NHL v období let 2012–2017 zemřelo v nemocniční péči, 47 % přímo na odděleních HOK, 4,2 % těchto nemocných zemřelo v péči hospicové a 4,2 % na LDN (graf 4).
Graf 4. Rozdělení souboru zemřelých nemocných podle místa úmrtí 
Příčiny úmrtí: U 24 nemocných byl příčinou úmrtí nehodgkinský lymfom, u 25 byla příčinou infekce v souvislosti s NHL, 10 zemřelo na projevy orgánového selhávání v souvislosti s NHL, 4 zemřeli na sekundární tumor bez přímé příčinné souvislosti s NHL, 1 zemřel v remisi nemoci na cévní mozkovou příhodu a u 8 není příčina úmrtí známa, resp. přesně zjistitelná (graf 5). Padesát devět nemocných (92 %) zemřelo v příčinné souvislosti s NHL (progrese NHL, komplikace infekční nebo orgánové v průběhu léčby NHL), 5 (8 %) zemřelo bez přímé příčinné souvislosti s NHL.
Graf 5. Rozdělení souboru zemřelých nemocných podle příčiny úmrtí 
Celkové přežití zemřelých nemocných: Medián celkového přežití (OS) zemřelých nemocných byl 9,2 měsíce (95 % CI 7,1–14,9) (graf 6).
Graf 6. Kaplanova Meierova křivka celkového přežití souboru zemřelých nemocných s NHL na HOK FNOL v letech 2012–2017 
Pravděpodobnost celkového přežití všech nemocných s NHL nově diagnostikovaných a léčených na HOK FNOL v letech 2012–2017 je v 5 letech 68,0 % (95% CI 0,64–0,72) (graf 7).
Graf 7. Kaplanova Meierova křivka celkového přežití souboru nemocných s nově diagnostikovaným NHL na HOK v letech 2012–2017 
Diskuse
Z naší retrospektivní analýzy zemřelých s diagnózou NHL vyplývá vysoký podíl úmrtí na lůžkách HOK (celkem 47 % zemřelých), 90 % nemocných zemře v některé z nemocnic. 4,2 % nemocných zemřelo na LDN. To odpovídá datům ÚZIS o 69,6 % úmrtí na lymfom v nemocnicích a 6,4 % úmrtí v léčebnách pro dlouhodobě nemocné. Přitom podle údajů ÚZIS na lůžkách akutní péče zemře více než 80 % nemocných s lymfomy. Ať už je podíl nemocniční péče na konci života jakkoliv velký, vždy se jedná o velký objem EoLC péče poskytovaný v nemocnicích.
V hospicové péči zemřeli 4,2 % nemocných souboru, stejné údaje pro nemocné s lymfomem uvádí také ÚZIS (3,7 %). Hospice mají největší zkušenosti s poskytováním specializované paliativní péče v závěru života. Určitou překážkou v širším využití hospicové péče v hemato-onkologii jsou menší zkušenosti hospiců s péčí o hematologicky nemocné [24]. Profesor LeBlanc referuje nedůvěru hematologů ve specialisty v paliativní péči. To vyplývá z četných hloubkových rozhovorů, kde hematologové poukazovali na to, že hematologicky nemocní nedostávali od specialistů na paliativní péči přesné prognostické informace nebo dostávali nevhodná doporučení [33, 42].
Z našich zkušeností vyplývá intenzivní léčba NHL v posledních 6 měsících života, chemoterapií bylo léčeno v tomto období 86 % nemocných. Léčba zahrnovala imunochemoterapii, radioterapii, autologní i alogenní transplantaci, léčbu biologickou. V posledních 30 dnech života bylo chemoterapií léčeno 25 nemocných (37 %), přičemž se u 57 % jednalo o léčbu paliativní. Naše pozorování odpovídá publikovaným zkušenostem Odejide a kolektivu. Nemocní s lymfomy reagují na opakovaně podávanou chemoterapii, léčba je tak možná i ve fázi pokročilého, relabovaného onemocnění. Taková léčba může délku života prodlužovat, bývá ale často nejasné, kdy je nemoc skutečně refrakterní a který relaps nemoci je poslední. Kvůli této vysoké míře nejistoty v prognóze se hematologové spolu s nemocným rozhodují často pro další linii léčby na úkor plánování péče na konci života. Zahájení paliativní péče je tak zpožděno [41]. Ve sledovaném souboru byla chemoterapie v posledních 30 dnech života podána 37 % nemocným, což je relativně vysoké procento, odpovídající datům z práce autorů Hui a kolektiv z MD Anderson Cancer Center, která porovnávala kvalitu péče na konci života nemocných s pokročilou hematologickou malignitou a pokročilým solidním tumorem. V posledních 30 dnech života bylo u hematologicky nemocných trojnásobné podávání chemoterapie (43 % vs. 14 %) a trojnásobné podávání cílené léčby (34 % vs. 11 %). Častější byla u hematologicky nemocných potřeba hospitalizací (81 % vs. 47 %), častější opakované hospitalizace (23 % vs. 10 %), častější úmrtí v klinických studiích a častější úmrtí v intenzivní péči. Naopak méně časté byly paliativní konzultace (22 % vs. 48 %) oproti nemocným se solidními tumory. Ve shodě s uvedenými autory prokazujeme časté hospitalizace.
V posledních 30 dnech (1 měsíci) života nemocných námi sledovaného souboru byl medián délky hospitalizace 11 dní (rozmezí 0–31 dní), v posledních 3 měsících života byl medián délky hospitalizace 25 dní (rozmezí 0–90 dnů). Délku hospitalizací v nemocnici v posledních 3 a jednom měsíci života délku uvádíme jako ukazatel kvality poskytované EoLC, jako ukazatel agresivní léčby na konci života. Část autorů vztahuje tento ukazatel k posledním 14 dnům nebo poslednímu jednomu měsíci života [7, 20, 22, 23]. Henson a kolektiv ve své studii zahrnující hematologicky nemocné uvádí poslední 3 měsíce života jako období, ve kterém posuzuje kvalitu EoLC.
V časovém období naší retrospektivní studie u nemocných s NHL probíhala obecná paliativní péče poskytovaná lékaři hematology, všeobecnými sestrami, psychologem a dalšími zdravotníky v rámci jejich odbornosti s cílem zajistit nemocným dobrou kvalitu života (empatická komunikace o nemoci, léčba symptomů nemoci, zajišťování domácí péče, rozhovory s rodinnými příslušníky.) Specializovaná paliativní péče chápaná jako péče poskytovaná nemocným a jejich rodinám týmem odborníků, kteří absolvovali vzdělání v oboru paliativní péče, v uvedeném období poskytována nebyla.
Autorský kolektiv pod vedením Hui si v roce 2013 položil otázku, proč mají hematologičtí nemocní v posledních 30 dnech života vyšší pravděpodobnost systémové cílené protinádorové léčby. Naznačují, že podstatnou roli hrají také sami hematologové a nemocní [43]. Hematologům a onkologům byl předložen případ nemocného s pokročilým neléčitelným nádorovým onemocněním s minimální pravděpodobností léčebné odpovědi, pravděpodobným přežitím jeden měsíc bez prodloužení přežití léčbou. Hematologové mnohem pravděpodobněji nabídnou nemocnému léčbu ve srovnání s onkology, jejich přesvědčení a postoje tak mohou přispívat k intenzivnější péči na konci života.
Významnou roli v rozhodování o další péči hrají také preference nemocného. Ti upřednostňují léčbu s výhledem prodloužení života. Tato je ale spojena s riziky intenzivní péče, protože léčba krevních onemocnění u oslabených, vyčerpaných a předléčených nemocných s sebou přináší četné komplikace, často s nutností hospitalizace [44, 45]. V našem sledovaném souboru značná část nemocných zemřela na komplikující infekce v průběhu léčby, celkem 25 nemocných a dalších 10 nemocných zemřelo na orgánové selhání. Proto je třeba při plánování další péče a léčby o prospěchu a rizicích podané chemoterapie s nemocnými otevřeně hovořit. Může to být jedna z indikací paliativní intervence.
Medián celkového přežití souboru zemřelých nemocných byl krátký, 9,2 měsíce, s intervalem 7,1–14,9 měsíce. Krátké celkové přežití je dáno spektrem nemocných v pokročilém věku, s rizikovými formami NHL s vysokou pravděpodobností relapsu nemoci nebo nedostatečné odpovědi na léčbu. 29 % nemocných souboru zemřelo v relapsu nemoci, 29 % mělo nemoc refrakterní na podávanou chemoterapii. Ne vždy lze vývoj nemoci předvídat, k úmrtí může dojít již v průběhu léčby první linie, což byl případ 19 nemocných sledovaného souboru.
Časná intervence paliativní péče by měla být indikována u nemocných s rizikovým lymfomem s nejistým průběhem onemocnění. Tato intervence by se měla týkat také jinak rizikových nemocných, starších nebo komorbidních, u nichž je vyšší riziko komplikací. Indikace paliativní intervence nejsou dosud u nemocných s hematologickou malignitou stanoveny oproti indikacím u nemocných se solidními nádory. Příjemce specializované paliativní péče v hematologii se pokusil definovat profesor LeBlanc. Navrhl pro tuto péči nemocné s vysokým stupněm symptomové zátěže, na terapii refrakterní nemocné, nemocné indikované k náročným výkonům, jako je alogenní transplantace, nemocné s psychickou nepohodou nebo ty, kteří nemají správnou představu a náhled stavu své nemoci, nemocné se špatnou prognózou a omezenou délkou života [42].
Paliativní péče by měla zahrnovat komunikaci s nemocným a jeho rodinou v celém průběhu péče, komunikaci o prognóze včetně prognózy nejisté, o předpokládaném vývoji onemocnění. Je třeba dostatek času na plánování závěru života, stanovení plánů péče, které musí zohledňovat přání nemocných. Práce prokázala vysokou míru hospitalizací v posledních 3 měsících života. Tento čas lze chápat také jako příležitost pro komunikaci o cílech léčby a plánech péče s nemocným i rodinou pro případ, že přes léčbu nedochází ke zlepšení stavu. Předpokladem je v komunikaci vzdělaný personál. Nutná je práce v multidisciplinárním týmu a intenzivní spolupráce s ostatními poskytovateli paliativní péče, např. domácími hospici. Ze studií v onkologii vyplývá, že si nemocní přes integraci paliativní péče udrží stálou vazbu na ošetřujícího onkologa a péči vůbec nevnímají jako roztříštěnou [46]. Lze tak předpokládat prospěch zapojení paliativní péče do hematologie, zejména s ohledem na intenzitu léčby a nejasnou prognózu krevních nemocí [26, 27]. Bude třeba vyvinout cílené paliativní intervence také v průběhu kurativní léčby, tzv. časnou paliativní péči [47]. Určitým problémem, který může bránit např. většímu využití hospicové péče, je transfuzní závislost nemocných [27]. V článku, který se týká závěru života hemato-onkologických pacientů v České republice a paliativní péče o ně v roce 2020 dochází Kouba a Rusinová k závěru, že hematologické a paliativní týmy včetně týmů hospicových se mohou v péči o nemocné vhodně doplňovat ve prospěch pacienta [48].
Závěr
Článek potvrzuje i v podmínkách České republiky vysokou míru hospitalizací a intenzivní terapii krátce před úmrtím, tedy proměnné, které nemusí být vždy přiměřené v EoLC. Z našich klinických zkušeností vyplývá potřeba zapojení paliativní péče, a to jak časné, tak EoLC u nemocných s NHL, onemocnění potenciálně život ohrožujícího s prognostickou nejistotou. Od roku 2017 proto probíhá na HOK FNOL vzdělávání ošetřujících v paliativní medicíně, nemocným a ošetřujícím lékařům, hematologům je k dispozici konzultace lékaře se zvláštní specializovanou způsobilostí v oboru paliativní medicína. Paliativní péče vyžaduje spolupráci ošetřujícího lékaře, paliatra, sestry, psychologa, kaplana, sociální sestry, nutričního terapeuta a klinického farmakologa. Úzce spolupracujeme s dalšími poskytovateli paliativní péče, zejména s domácími hospici, a to nejen při předávání nemocných, ale i v předávání zkušeností. To se v praxi ukázalo oboustranně zvláště cenné.
Podíl autorů na přípravě rukopisu
UR – léčba nemocných, příprava rukopisu, závěrečná kontrola rukopisu
MR – léčba nemocných
SR – léčba nemocných a kontrola rukopisu
PV – léčba nemocných, příprava rukopisu
LM – léčba nemocných
HM – kontrola a revize rukopisu
HA – léčba nemocných a kontrola rukopisu
PT – léčba nemocných a kontrola rukopisu
SO – příprava studie, kontrola a revize rukopisu
Poděkování
Příprava rukopisu byla podpořena grantem Nadačního fondu AVAST, Stipendium pro paliativní péči 2018/19.
Čestné prohlášení
Autoři práce prohlašují, že vznik a publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Do redakce doručeno dne 28. 6. 2019.
Přijato po recenzi dne 30. 3. 2020.
Závěr života nemocných s NHL
MUDr. Renata Urbanová, Ph.D.
Hemato-onkologická klinika FNOL a LF UP v Olomouci
I. P. Pavlova 6
779 00 Olomouc
e-mail: renata.urbanova@fnol.cz
Zdroje
1. Hearn J, Higginson IJ. Do specialist palliative care teams improve outcomes for cancer patients? A systematic literature review. Palliat Med. 1998;12 : 317–332.
2. Bakitas M, Lyons KD, Hegel MT, et al. Effects of a palliative care intervention on clinical outcomes in patients with advanced cancer: the Project ENABLE II randomized controlled trial. JAMA. 2009;302 : 741–749.
3. Jacobsen J, Jackson V, Dahlin C, et al. Components of early outpatient palliative care consultation in patients with metastatic nonsmall cell lung cancer. J Palliat Med. 2011;14 : 459–464.
4. Temel JS, Greer JA, Admane S, et al. Longitudinal perceptions of prognosis and goals of therapy in patients with metastatic non-small-cell lung cancer: results of a randomized study of early palliative care. J Clin Oncol. 2011;29 : 2319–2326.
5. Greer JA, Pirl WF, Jackson VA, et al. Effect of early palliative care on chemotherapy use and end-of-life care in patients with metastatic non-small-cell lung cancer. J Clin Oncol. 2012;30 : 394–400.
6. Morrison RS, Penrod JD, Cassel JB, et al. Cost savings associated with US hospital palliative care consultation programs. Arch Intern Med. 2008;168 : 1783–1790.
7. Temel JS, Greer JA, Muzikansky A, et al. Early palliative care for patients with metastatic non-small-cell lung cancer. N Engl J Med. 2010;363 : 733–742.
8. Pirl WF, Temel JS, Billings A, et al. Depression after diagnosis of advanced non-small cell lung cancer and survival: a pilot study. Psychosomatics. 2008;49 : 218–224.
9. Maione P, Perrone F, Gallo C, et al. Pretreatment quality of life and functional status assessment significantly predict survival of elderly patients with advanced non-small-cell lung cancer receiving chemotherapy: a prognostic analysis of the multicenter Italian lung cancer in the elderly study. J Clin Oncol. 2005;23 : 6865–6872.
10. Movsas B, Moughan J, Sarna L, et al. Quality of life supersedes the classic prognosticators for long-term survival in locally advanced non-small-cell lung cancer: an analysis of RTOG 9801. J Clin Oncol. 2009;27 : 5816–5822.
11. Zimmermann C, Swami N, Krzyzanowska M, et al. Early palliative care for patients with advanced cancer: a cluster-randomised controlled trial. Lancet. 2014;383 : 1721–1730.
12. Dionne-Odom JN, Azuero A, Lyons KD, et al. Benefits of early versus delayed palliative care to informal family caregivers of patients with advanced cancer: outcomes from the ENABLE III randomized controlled trial. J Clin Oncol. 2015;33 : 1446–1452.
13. Smith TJ, Temin S, Alesi ER, et al. American Society of Clinical Oncology provisional clinical opinion: the integration of palliative care into standard oncology care. J Clin Oncol. 2012;30 : 880–887.
14. Ramirez A, Addington-Hall J, Richards M. ABC of palliative care. The carers. Br Med J. 1998;316 : 208–211.
15. Rogers A, Karlsen S, Addington-Hall J. All the services were excellent. It is when the human element comes in that things go wrong’: dis-satisfaction with hospital care in the last year of life. J Adv Nurs. 2000;31 : 768–774.
16. Morris E. A pain of separation. Nurs Times. 1988;84 : 54–56.
17. Dunne K, Sullivan K. Family experiences of palliative care in the acute hospital setting. Int J Palliat Nurs. 2000;6 : 170–178.
18. Slama O, Kabelka L, Loucka M. Palliative care in Czech Republic in 2016. Čas Lék Čes. 2016;155 : 445–450.
19. Earle CC, Park ER, Lai B, et al. Identifying potential indicators of the quality of end-of-life cancer care from administrative data. J Clin Oncol. 2003;21 : 1133–1138.
20. Earle CC, Neville BA, Landrum MB, et al. Trends in the aggressiveness of cancer care near the end of life. J Clin Oncol. 2004;22 : 315–321.
21. Wright AA, Keating NL, Balboni TA, et al. Place of death: correlations with quality of life of patients with cancer and predictors of bereaved caregivers’ mental health. J Clin Oncol. 2010;28 : 4457–4464.
22. Gonsalves WI, Tashi T, Krishnamurthy J, et al. Effect of palliative care services on the aggressiveness of end-of-life care in the Veteran´s Affairs cancer population. J Palliat Med. 2011;14 : 1231–1235.
23. Barbera L, Paszat L, Chartier C. Indicators of poor quality end-of-life cancer care in Ontario. J Palliat Care. 2006;22 : 12–17.
24. Howell DA, Shellens R, Roman E, et al. Haematological malignancy: are patients appropriately referred for specialist palliative and hospice care? A systematic review and meta-analysis of published data. Palliat Med. 2011;25 : 630–641.
25. Hui D, Didwaniya N, Vidal M, et al. Quality of end-of-life care in patients with hematologic malignancies: a retrospective cohort study. Cancer. 2014;120 : 1572–1578.
26. Epstein AS, Goldberg GR, Meier DE. Palliative care and hematologic oncology: the promise of collaboration. Blood Rev. 2012;26 : 233–239.
27. Manitta VJ, Philip JA, Cole-Sinclair MF. Palliative care and the hemato-oncological patient: can we live together? A review of the literature. J Palliat Med. 2010;13 : 1021–1025.
28. Fadul NA, El Osta B, Dalal S, et al. Comparison of symptom burden among patients referred to palliative care with hematologic malignancies versus those with solid tumors. J Palliat Med. 2008;11 : 422–427.
29. Quill TE, Abernethy AP. Generalist plus specialist palliative care-creating a more sustainable model. N Engl J Med. 2013;368 : 1173–1175.
30. Lupu D, American Academy of Health, Palliative Medicine Workforce Task F. Estimate of current hospice and palliative medicine physician workforce shortage. J Pain Symptom Manage. 2010;40 : 899–911.
31. LeBlanc TW, Abernethy AP, Casarett DJ. What is different about patients with hematologic malignancies? A retrospective cohort study of cancer patients referred to a hospice research network. J Pain Symptom Manage. 2015;49 : 505–512.
32. Howell DA, Roman E, Cox H, et al. Destined to die in hospital? Systematic review and meta-analysis of place of death in haematological malignancy. BMC Palliat Care. 2010;9 : 9.
33. LeBlanc TW, O´Donnell JD, Crowley-Matoka M, et al. Perceptions of palliative care among hematologic malignancy specialists: a mixed-methods study. J Oncol Pract. 2015;11:e230–e238.
34. Bernacki RE, Block SD, American College of Physicians High Value Care Task F. Communication about serious illness care goals: a review and synthesis of best practices. JAMA Intern Med. 2014;174 : 1994–2003.
35. El-Jawahri A, Traeger L, Park ER. Associations among prognostic understanding, quality of life, and mood in patients with advanced cancer. Cancer. 2014;120 : 278–285.
36. El-Jawahri A, Traeger L, Kuzmuk K, et al. Prognostic understanding, quality of life and mood in patients undergoing hematopoietic stem cell transplantation. Bone Marrow Transplant. 2015;50 : 1119–1124.
37. Apatira L, Boyd EA, Malvar G, et al. Hope, truth, and preparing for death: perspectives of surrogate decision makers. Ann Intern Med. 2008;149 : 861–868.
38. Henson LA, Gomes B, Koffman J, et al. Factors associated with aggressive end of life cancer care. Support Care Cancer. 2016;24 : 1079–1089.
39. LeBlanc TW. Palliative care and hematologic malignancies: old dog, new tricks? J Oncol Pract. 2014;10:e404–e407.
40. LeBlanc TW. In the sandbox: palliative care and hematologic malignancies. J Community Support Oncol. 2014;12 : 44–45.
41. Odejide OO, Salas Coronado DY, Watts CD, et al. End-of-life care for blood cancers: a series of focus groups with hematologic oncologists. J Oncol Pract. 2014;10:e396–e403.
42. LeBlanc TW, El-Jawahri A. When and why should patients with hematologic malignancies see a palliative care specialist? Hematology Am Soc Hematol Educ Program. 2015;2015 : 471–478.
43. Hui D, Karuturi MS, Tanco KC, et al. Targeted agent use in cancer patients at the end of life. J Pain Symptom Manage. 2013;46 : 1–8.
44. Hui D, Bansal S, Park M, et al. Differences in attitudes and beliefs toward end-of-life care between hematologic and solid tumor oncology specialists. Ann Oncol. 2015;26 : 1440–1446.
45. Wright AA, Zhang B, Keating NL, et al. Associations between palliative chemotherapy and adult cancer patients’ end of life care and place of death: prospective cohort study. Br Med J. 2014;348:g1219.
46. Schenker Y, Crowley-Matoka M, Dohan D, et al. Oncologist factors that influence referrals to subspecialty palliative care clinics. J Oncol Pract. 2014;10:e37–e44.
47. El-Jawahri AR, Traeger LN, Kuzmuk K, et al. Quality of life and mood of patients and family caregivers during hospitalization for hematopoietic stem cell transplantation. Cancer. 2015;121 : 951–959.
48. Kouba M, Rusinová K. Závěr života hematoonkologických pacientů v České republice a paliativní péče o ně v roce 2020. Postgrad Med. 2020;1 : 74–80.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2020 Číslo 2- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Ibrance® – nová šance pro pacientky s HR+/HER2– karcinomem prsu
-
Všechny články tohoto čísla
- Léčba histiocytózy z Langerhansových buněk u dospělých osob
- Závěr života nemocných s nehodgkinským lymfomem, analýza souboru zemřelých během šesti let (2012–2017) na jednom pracovišti, integrace paliativní péče
- Skladování erytrocytů při nestandardní teplotě
- Theralite a mnohočetný myelom – známe už odpověď na efektivitu léčby nefrologa s hematologem?
- Překvapivý nález v kostní dřeni: co za ním je?
- Životní jubileum pana profesora Jiřího Mayera
- Editorial
- Trombotické mikroangiopatie
- Castlemanova nemoc, jedna z příčin chronické systémové zánětlivé reakce, někdy i retence tekutin, vaskulitid a poruch imunity – Mezinárodní diagnostická kritéria z roku 2017
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Castlemanova nemoc, jedna z příčin chronické systémové zánětlivé reakce, někdy i retence tekutin, vaskulitid a poruch imunity – Mezinárodní diagnostická kritéria z roku 2017
- Trombotické mikroangiopatie
- Léčba histiocytózy z Langerhansových buněk u dospělých osob
- Překvapivý nález v kostní dřeni: co za ním je?
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



