-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Současný přístup ke krvácení do horní části trávicího traktu
Contemporary management of the upper gastrointestinal bleeding
Background: Upper gastrointestinal bleeding is a relatively common but potentially fatal medical emergency. Many medical disciplines are involved in the diagnosis and treatment of this condition. The patients are usually admitted primarily to surgical wards and the attending surgeon is responsible for management of the patients. Surgery may also be an ultimatum refugium when less invasive treatments fail.
Objective: The aim of this study is to review the current practice in the management of patients with upper gastrointestinal bleeding based on a literature review and our own experience in the management of these patients.
Conclusions: Upper gastrointestinal bleeding is a relatively common emergency. It is a hemorrhage whose the source is proximal to the ligament of Treitz. The diagnosis and treatment require a multidisciplinary approach. Today, endoscopy plays a key role in the diagnosis and treatment. The correct timing of each step is essential for patient survival. This article provides a clear summary of the current recommended procedures from initial resuscitation, fluid therapy, administration of blood substitutes, adjustment of coagulation parameters in patients on anticoagulant and antithrombotic therapy, endoscopic diagnostic and therapeutic options, and procedures for recurrent bleeding, including angiointervention and surgical treatment, with a main focus on nonvariceal bleeding.
Keywords:
endoscopy – peptic ulcer – proton pump inhibitors – upper gastrointestinal bleeding
Autoři: D. Hoskovec
Působiště autorů: I. chirurgická klinika – břišní, hrudní a úrazové chirurgie 1. LF UK a VFN v Praze
Vyšlo v časopise: Rozhl. Chir., 2025, roč. 104, č. 7, s. 300-308.
Kategorie: Souhrnné sdělení
doi: https://doi.org/10.48095/ccrvch2025300Souhrn
Východiska: Krvácení do horní části gastrointestinálního traktu je relativně častou, ale potenciálně fatální náhlou příhodou břišní. Na diagnostice a léčbě tohoto onemocnění se podílí řada odborností, ale nemocní jsou obvykle primárně hospitalizováni na lůžkách chirurgických oddělení. Ošetřující lékař, tj. chirurg je tedy zodpovědný za léčbu pacienta a indikaci konzilií spolupracujících specialistů. Operace může být také ultimum refugium postupem při selhání méně invazivních léčebných postupů.
Cíl: Cílem práce je přehled současných postupů a metod užívaných v léčbě pacientů s krvácením do horní části trávicího traktu na základě literární rešerše i vlastních zkušeností s léčbou těchto nemocných.
Závěr: Krvácení do horní části gastrointestinalniho traktu je relativně častou náhlou příhodou. Jde o krvácení, jehož zdroj je proximálně od Treitzova ligamenta. Diagnostika a léčba vyžaduje multioborovou spolupráci více oborů. Klíčovou roli v diagnostice a terapii dnes představuje endoskopie. Správné načasování jednotlivých kroků je zásadní pro přežití pacienta. Článek v přehledné formě shrnuje současné doporučené postupy od iniciální resuscitace, tekutinové léčby, podání krevních náhrad přes úpravu koagulačních parametrů u pacientů s antikoagulační a antitrombotickou léčbou, možnosti endoskopické diagnostiky a terapie a také postupy při recidivě krvácení, vč. angiointervenční a chirurgické léčby s hlavním zaměřením na nevariceální krvácení.
Klíčová slova:
endoskopie – inhibitory protonové pumpy – peptický vřed – krvácení do horní části GIT
Krvácení do horní části gastrointestinálního traktu (GIT) je jednou z nejčastějších gastroenterologických diagnóz vedoucích k hospitalizaci. Incidence krvácení do horní části GIT se pohybuje kolem 40–160 pacientů na 100 000 obyvatel za rok [1,2]. V USA je ročně hospitalizováno 500 000 pacientů s touto diagnózou [3]. Letalita krvácení do horní části GIT je 2–11 % a dlouhodobě se nemění [4,5]. Za krvácení do horní části GIT je považováno krvácení, jehož zdroj je v jícnu, žaludku a duodenu. Za hranici je považováno Treitzovo ligamentum.
Krvácení do horní části trávicího traktu se manifestuje hematemézou (zvracení čerstvé či natrávené krve charakteru kávové sedliny), melenou (odchod černé mazlavé asfaltové stolice s typickým zápachem) nebo hematochezií (odchod tmavě červené krve konečníkem).
Krvácení do horní části GIT lze rozdělit etiologicky do dvou skupin (tab. 1) [1,6–8]:
- nevarikózní krvácení do horní části GIT (cca 80 % krvácení do horního GIT);
- varikózní krvácení při portální hypertenzi.
Nicméně i u pacientů se známou portální hypertenzí může být jiný zdroj krvácení než jícnové (nebo žaludeční) varixy. Následující text se bude týkat především nevarikózního krvácení do horního GIT.
Péči o pacienta s akutním krvácením do horního GIT lze rozdělit do několika fází, které se v praxi ale částečně překrývají.
Stanovení diagnózy
Iniciální je stanovení diagnózy krvácení do horní části GIT, kde v podstatě stačí anamnéza a klinické vyšetření. V anamnéze nás kromě údaje o zvracení čerstvé či natrávené krve, případně odchodu černé nebo krvavé stolice budou zajímat časové údaje a frekvence těchto příznaků. Specificky nás budou zajímat údaje o onemocnění trávicího traktu a jater, případně předchozí ataky krvácení, operace na horním GIT a také farmakologická anamnéza se zaměřením na mediaci ovlivňující koagulační parametry, případně ochrannou bariéru sliznice GIT (nesteroidní analgetika, antikoagulancia, vč. NOAK). Nesmíme zapomínat, že preparáty železa mohou zbarvovat stolici do černa a vést k falešnému podezření na krvácení.
Při klinickém vyšetření jsou důležité vstupní oběhové parametry, dále známky krvácení do GIT (nezapomínat na vyšetření per rectum!), přítomnost jizev, ascitu, hepatosplenomegalie apod. Při jasných známkách krvácení do GIT je celkem zbytečné stolici zkoumat testy na okultní krvácení (jak bohužel někdy v praxi vidíme).
Paralelně s odběrem anamnézy a klinickým vyšetřením probíhá zajištění intravenózního vstupu (min. dvě i.v. linky) a odběr krve pro laboratorní vyšetření (za minimum je možné považovat krevní obraz, křížový test, koagulační testy, jaterní soubor, urea, kreatinin, minerály). Zavedení nazogastrické sondy není nutné a nemění prognózu nemocných a v současné době se rutinně nedoporučuje [3].
Již při tomto prvním kontaktu s pacientem lze orientačně vytipovat skupinu nemocných ve vysokém riziku – jsou to pacienti s krátkou anamnézou krvácení, tachykardií, hypotenzí, poklesem hemoglobinu pod 80 g/l. Dále sem patří starší polymorbidní nemocní. U těchto nemocných je nejvyšší riziko selhání terapie a recidivy krvácení.
V zahraniční literatuře je poměrně velký důraz na stanovení rizika krvácení skórovacími systémy s cílem identifikovat skupinu nemocných, kteří nevyžadují hospitalizaci ani časné endoskopické vyšetření. Evropská společnost pro gastrointestinální endoskopii (European Society of Gastrointestinal Endoscopy – ESGE) doporučuje použití Glasgow- -Blatchfordova skóre (GBS) pro předendoskopickou stratifikaci nemocných. Skóre se počítá při prvním kontaktu s pacientem a nemocní s hodnotou 0–1 se považují za pacienty v nízkém riziku, kteří nevyžadují hospitalizaci ani časné endoskopické vyšetření (tab. 2). Dalšími skórovacími systémy jsou Rockallovo skóre, které ale ke svému výpočtu už potřebuje endoskopický nález, a systém AIMS65. Využití skórovacích systémů v rutinní praxi je ale v České republice minimální.
Tab. 1. Etiologie krvácení do horní části GIT [1,6–8]. Tab. 1. Upper GI bleeding – etiology [1,6–8]. ![Etiologie krvácení do horní části GIT [1,6–8]. Tab. 1. Upper GI bleeding – etiology [1,6–8].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/423f4c136bec86a0280211fd43921a2d.png)
Tab. 2. Glasgow-Blatchfordovo skóre [1]. Tab. 2. Glasgow-Blatchford score [1]. ![Glasgow-Blatchfordovo skóre [1]. Tab. 2. Glasgow-Blatchford score [1].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/a78dd976add31698b4510ac46c28acb4.png)
Iniciální léčba
Po stanovení diagnózy krvácení následuje stabilizace stavu nemocného – korekce intravaskulární hypovolemie, obnovení adekvátní tkáňové perfuze a prevence orgánového selhání. Dále doplnění ztracených součástí krve, především červených krvinek. V současné době se doporučuje restriktivní přístup k podávání transfuzních přípravků s cílovou hladinou hemoglobinu 70–90 g/l, u pacientů se závažnými kardiálními komorbiditami by měla být cílová hladina hemoglobinu na horní hranici tohoto rozmezí. Tento přístup vede ke zlepšení přežití oproti liberálnějšímu přístupu k transfuzní politice (95 vs. 91 %) i nižšímu výskytu recidiv krvácení (10 vs. 16 %) [1]. Kromě náhrady červených krvinek je třeba korigovat také případnou koagulopatii. Při masivních krevních náhradách je doporučený poměr suplementovaných částí krve (červené krvinky, plazma, destičky) 1 : 1 : 1 [9]. Vyšší mezinárodní normalizovaný poměr (international normalised ratio – INR) (nad 1,5) zvyšuje letalitu, nicméně se neprokázalo, že by vyšší INR zvyšoval procento recidiv krvácení. Množství krevních destiček je dostačující na hladině 50 × 109/l, pouze u pacientů s dysfunkcí destiček je doporučována hladina vyšší (100 × 109/l).
Ze specifických léků se podávají blokátory protonové pumpy (inhibitory protonové pumpy – PPI). V současné době se doporučuje zahájení intravenózní terapie blokátorem protonové pumpy ještě před endoskopickým vyšetřením. Doporučené dávkování je 80 mg jako iniciální bolus a následná kontinuální infuze 8 mg/hod.
Na druhou stranu u nevarikózního krvácení do horního GIT se v současné době nedoporučuje rutinní podání kyseliny tranexenové a somatostatinu, vč. jeho derivátů.
ESGE doporučuje před endoskopickým vyšetřením podání i.v. Erytromycinu s cílem zlepšit přehlednost v horní části GIT, ale v České republice tč. není preparát pro nitrožilní podání registrován.
Tab. 3. Přehled antikoagulační a antitrombotické terapie [10,11]. Tab. 3. Anticoagulation and antithrombtic therapy [10,11]. ![Přehled antikoagulační a antitrombotické terapie [10,11]. Tab. 3. Anticoagulation and antithrombtic therapy [10,11].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/6df816939e606b1c334e1675f90523fc.png)
Tab. 4. Postup u život ohrožujícího krvácení a užívání léků ovlivňujících srážlivost [11]. Tab. 4. Reversal strategy in cases of the anticoagulated patients [11]. ![Postup u život ohrožujícího krvácení a užívání léků ovlivňujících srážlivost [11]. Tab. 4. Reversal strategy in cases of the anticoagulated patients [11].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/0fcb9bc0f287354f958a7dcf315d5187.png)
Tab. 5. Forrestova klasifikace [8,14,15]. Tab. 5. Forrest classification [8,14,15]. ![Forrestova klasifikace [8,14,15]. Tab. 5. Forrest classification [8,14,15].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image/03e5d6e0b8bf0b0d63334d83e7af2c5c.png)
Iniciální léčba u pacientů užívajících antikoagulační léčbu
Incidence krvácení do GIT u pacientů užívajících antagonisty K vitaminu (warfarin) je cca 1–4 % ročně. Při příznacích krvácení do GIT je třeba aplikaci těchto preparátů přerušit a korigovat koagulopatii. U stabilizovaných nemocných je dostatečné podání K vitaminu, u pacientů oběhově nestabilních, případně s nadhraničními hodnotami INR se doporučuje podání koncentrátů protrombinu, případně čerstvě zmražené plazmy. Normalizaci INR při podání protrombinových koncentrátů lze očekávat cca do 2 hod (při vstupním INR nad 2,1), při podání plazmy se efekt projeví cca do 6 hod [1].
Nové perorální antikoagulační léky (NOAK či DOAK) mají přibližně stejnou incidenci krvácení jako antagonisté K vitaminu. Při krvácení se léčba přerušuje a v podstatě se nechá účinek těchto léků spontánně vyprchat (u pacientů bez hepatálního a renálního selhání je efekt těchto léků po 12–24 hod minimální) (tab. 3,4) [1,12].
Protidestičková léčba – dle současných doporučení ESGE antitrombotická léčba (kyselina acetylsalicylová), pokud je indikována v rámci primární prevence kardiovaskulárních onemocnění, může být podávání aminosalicylové kyseliny (ASA) přerušeno, naproti tomu při indikaci z důvodu sekundární prevence kardiovaskulárních onemocnění může být nízká dávka ASA ponechána i v případě krvácení do GIT. Pokud pacient užívá duální antiagregační léčbu, ASA se i v případě krvácení může ponechat, druhý preparát má být vysazen. Je prokázáno, že úplné přerušení léčby podávané v rámci sekundární prevence vede k trombotickým komplikacím (už po několik dnech od vysazení) [12].
Endoskopické vyšetření
Endoskopické vyšetření horní části trávicího traktu je klíčovým diagnostickým a často i terapeutickým postupem. Podle časového faktoru se rozlišuje urgentní endoskopie (do 12 hod), časná (do 24 hod) a odložená (po 24 hod). ESGE doporučuje provedení endoskopie do 24 hod po přijetí [1,12]. Podmínkou je oběhová stabilita nemocného. Nicméně jsou studie dokazující, že rizikoví pacienti (vyšší věk, oběhová nestabilita při příjmu nebo během hospitalizace, pacienti s cirhózou) mohou profitovat z časnějšího vyšetření (do 12 hod) [4]. Naproti tomu endoskopické vyšetření v pozdějším intervalu než 24 hod je spojeno s vyšším rizikem recidivy krvácení [13].
Endoskopické vyšetření stanoví diagnózu a současně je možné provést terapeutický zákrok během jednoho vyšetření. Pokud je příčinou krvácení peptická léze, nález se hodnotí podle Forrestovy klasifikace (tab. 4).
Za rizikové nálezy se považují nálezy Forrest Ia, Ib a IIa, kde je nejvyšší pravděpodobnost recidivy krvácení. U lézí krytých koagulem (Forrest IIb) je možné koagulum odstranit a přesněji klasifikovat lézi, kterou kryje. Léze Forrest I (a, b) a IIa jsou indikované k endoskopické terapii.
Kromě Forrestovy klasifikace je důležitá také lokalizace a velikost vředu. Především vředy na zadní straně bulbu duodena (v blízkosti a. gastroduodenalis) a dále vředy subkardiální na malé kurvatuře a prepylorické na malé kurvatuře mají vysoké riziko vzniku recidivy krvácení. Stejně tak velikost vředu nad 2 cm zvyšuje riziko vzniku recidivy krvácení. Z tohoto pohledu je nejrizikovější nález velkého vředu na zadní stěně bulbu duodena Forrest Ia a IIa [16].
Obr. 1. 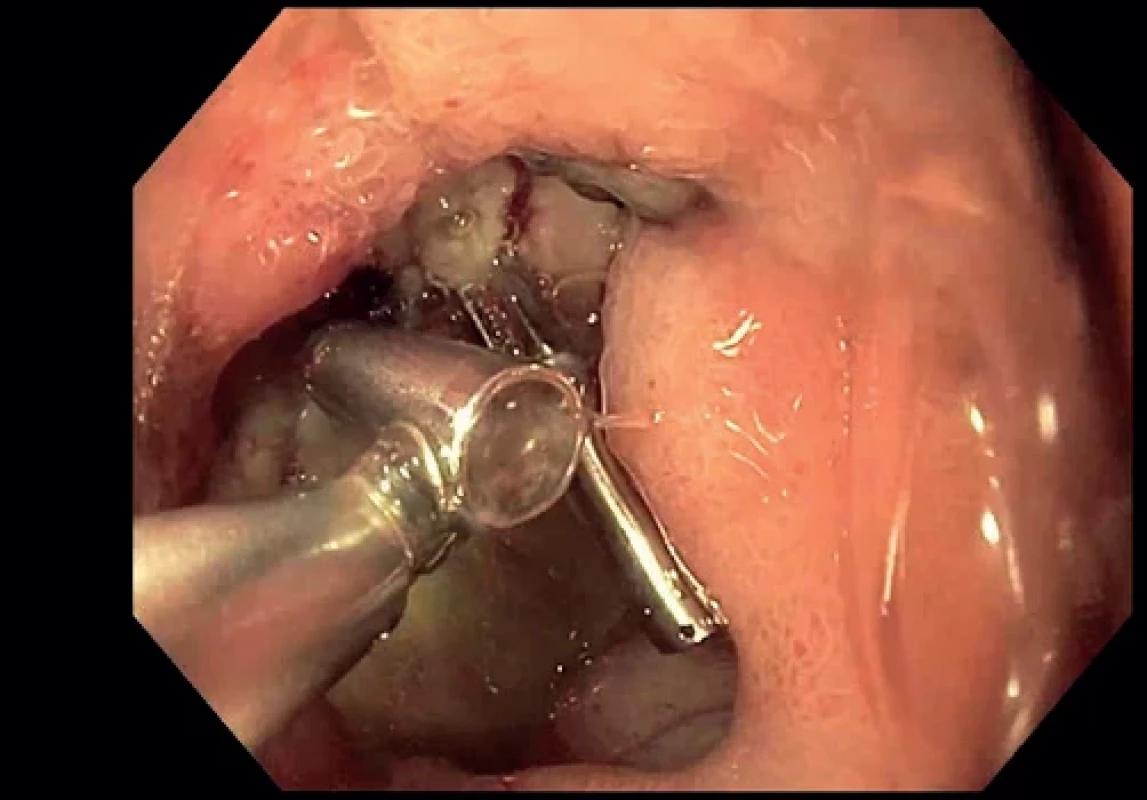
Krvácející vřed ošetřený klipy. Zdroj: IV. interní klinika 1. LF UK a VFN v Praze, MUDr. Pavel Hrabák.
Bleeding peptic ulcer treated by clips. Source: IVth Department of Internal Medicine, 1st Faculty of Medicine, Charles University, and General Hospital in Prague, Pavel Hrabák, MD.Obr. 2. 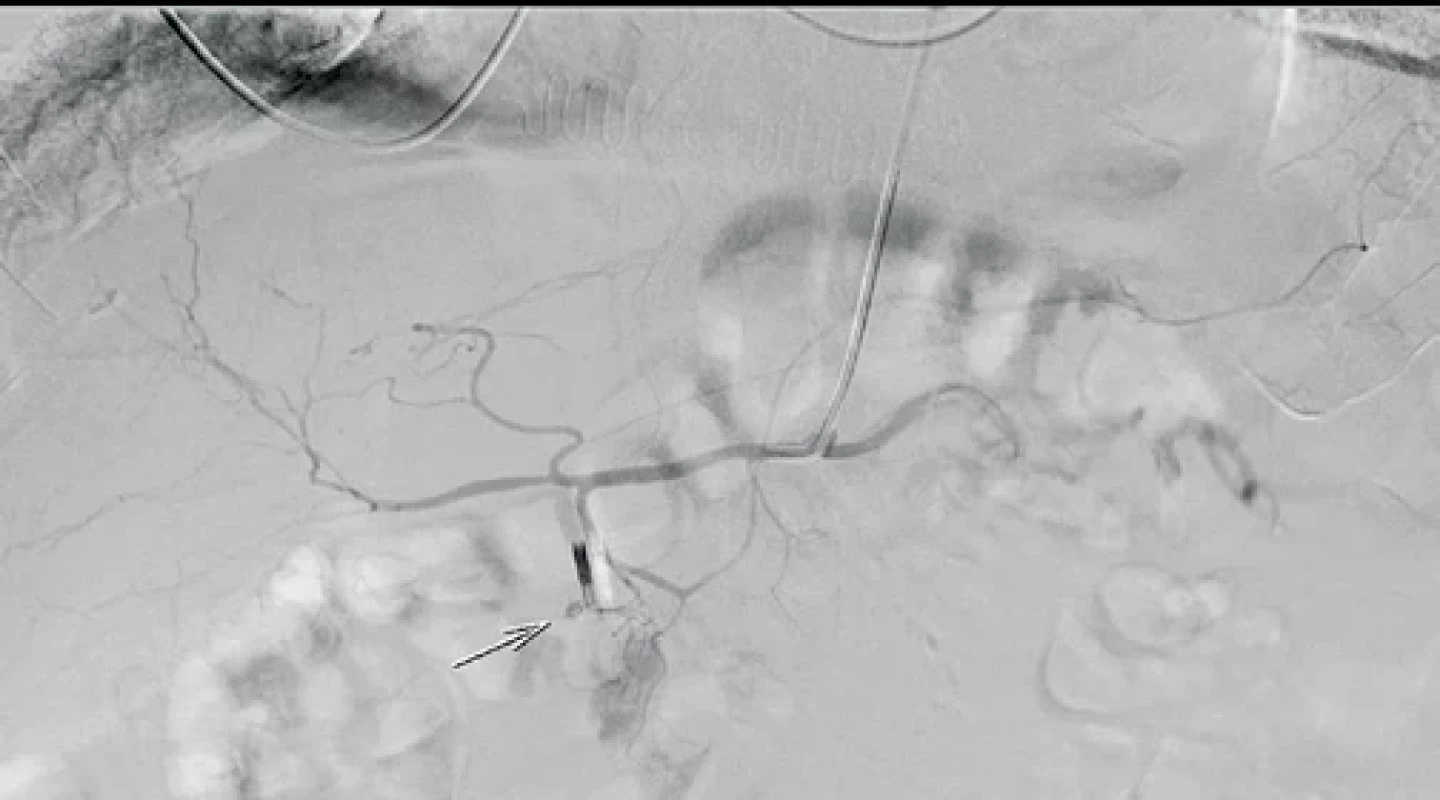
Angiografie truncus coeliacus, šipkou označeno krvácení z a. gastroduodenalis v blízkosti endoskopického klipu. Zdroj: Radiodiagnostická klinika 1. LF UK a VFN v Praze, MUDr. Artem Leščinskij, MUDr. Josef Hořejš, CSc.
Arteriography of the celiac trunk, bleeding site from gastroduodenal artery near the endoscopic clip signed by an arrow. Source: Department of Radiodiagnostics, 1st Faculty of Medicine, Charles University, and General Hospital in Prague, Artem Leščinskij, MD, Josef Hořejš, MD, PhD.Obr. 3. 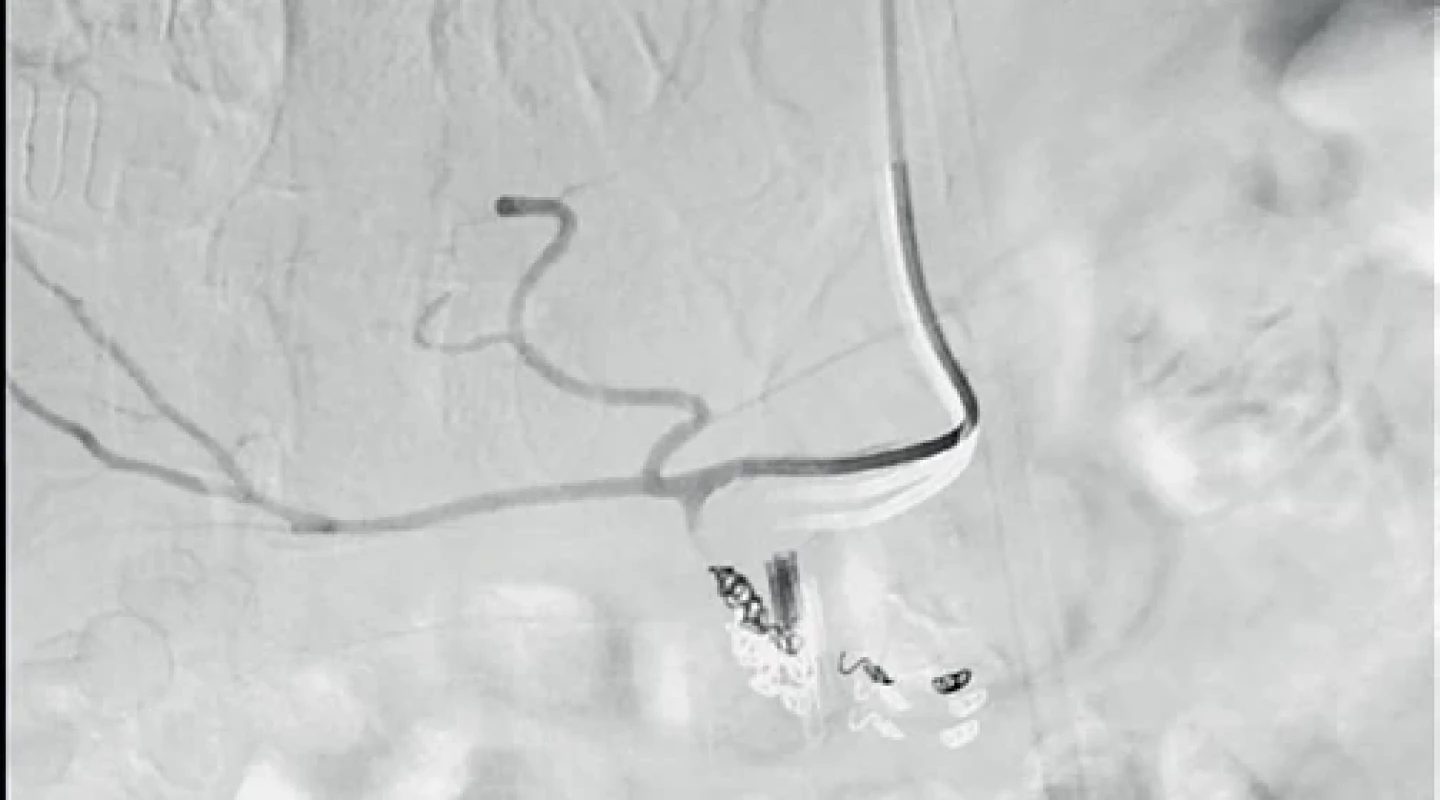
Gastroduodenální arterie uzavřená endovaskulárními spirálkami (stejný pacient jako na obr. 2). Zdroj: Radiodiagnostická klinika 1. LF UK a VFN v Praze, MUDr. Artem Leščinskij, MUDr. Josef Hořejš, CSc.
Gastroduodenal artery obturated by the endovascular coils (the same patient as in Fig. 2). Source: Department of Radiodiagnostics, 1st Faculty of Medicine, Charles University, and General Hospital in Prague, Artem Leščinskij, MD, Josef Hořejš, MD, PhD.Endoskopická terapie
K endoskopickému ošetření krvácení jsou k dispozici čtyři metody – injekční, termální, mechanické a lokální [5]. Jednotlivé metody je možné kombinovat. V rámci injekční terapie se nejčastěji užívá ředěný adrenalin (ředění 1 : 10 000 nebo 1 : 20 000), případně ethanol, nově i fibrin a trombin. Termální metody používají bipolární koagulaci nebo tzv. heater-probe, případně argon plazma koagulaci. K mechanickému ošetření jsou k dispozici různé typy klipů (obr. 1). Lokální prostředky jsou ve formě gelu nebo prášků. V případě ošetření rizikových vředů (Forrest Ia, Ib, IIa) je doporučováno současné použití dvou z výše uvedených metod – nejčastěji opich s adrenalinem (který zmírní krvácení, a tím zlepší přehlednost) doplněný klipy nebo termální metodou [12].
Pokud je zdrojem krvácení nevředová léze, u vzácných příčin jako Mallory Weiss syndrom, M Dieulafoy a angiektázií, doporučuje se endoskopické ošetření léze. V případě nálezu hemoragické gastropatie, ezofagitidy a duodenitidy se za dostatečný považuje konzervativní postup s PPI. Při nálezu krvácející maligní léze se doporučuje pokus o endoskopickou zástavu krvácení, ale obvykle jde pouze o dočasné řešení.
Obr. 4. 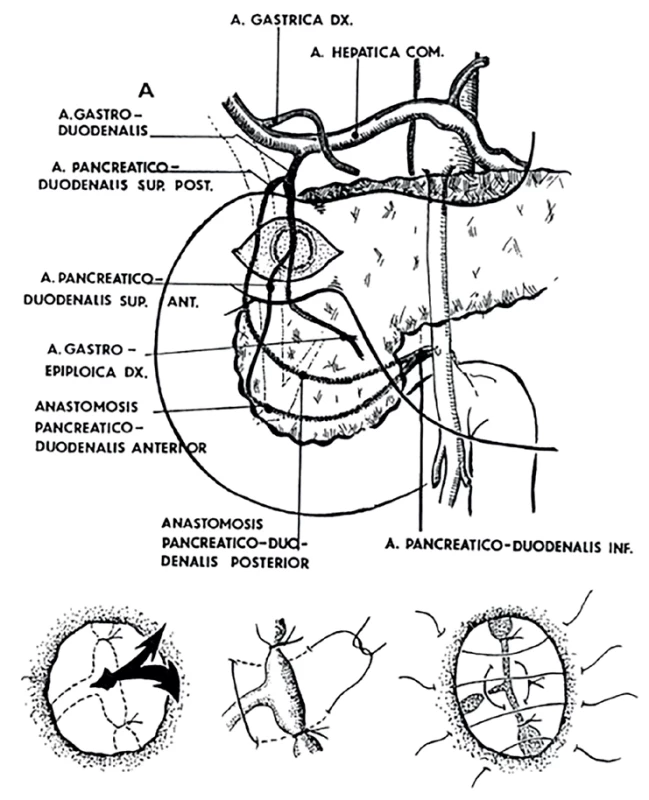
Ošetření krvácejícího vředu zadní stěny bulbu duodena. Zdroj: archiv autora.
Surgical approach to the bleeding peptic ulcer in the duodenum. Source: author's archive.Péče po endoskopické diagnostice/terapii
U rizikových pacientů Forrest I (a, b) a Forrest IIa po úspěšném ošetření krvácení pokračujeme v aplikaci PPI v dávce 8 mg/hod po dobu 72 hod, poté je možný přechod na standardní terapeutické dávky. U nemocných s nízkým rizikem dle Forresta (nebylo nutné endoskopické ošetření) je možné přejít ihned na standardní antisekreční léčbu [3]. V případě pozitivního testu na Helicobacter pylori (Hp) je indikována eradikační terapie. V rámci emergentní situace ale odběr na diagnózu infekce Hp není nutný, protože je zde vyšší riziko falešně negativních výsledků. Rutinní endoskopická kontrola po úspěšném ošetření krvácení se obvykle neindikuje, nicméně u rizikových pacientů může být zvažována kontrolní endoskopie (24 hod po endoskopickém ošetření krvácející léze). Za rizikový faktor se považuje i méně zkušený endoskopický tým.
U rizikových pacientů, především s velkým vředem na zadní stěně bulbu duodena a vysoko na malé kurvatuře, je ke zvážení preventivní transarteriální embolizace přívodné cévy (a gastroduodenalis a gastrica sin.). Tento postup snižuje počet recidiv krvácení a reintervencí, nutnosti chirurgické terapie a podle některých studií i snižuje celkovou letalitu [17,18].
V případě úspěšné léčby akutního nevariceálního krvácení do GIT u antikoagulovaných nemocných je indikováno opětné zahájení antikoagulační léčby co nejdříve (v horizontu dní), ale vždy po konzultaci s kardiologem a za pokračující léčby blokátory protonové pumpy.
Recidiva krvácení
Recidiva krvácení do GIT se objeví cca u 5–20 % nemocných [9]. Za klinické známky recidivy krvácení se považuje znovuobjevení hematemézy a meleny, tachykardie, hypotenze a pokles hemoglobinu o 20 g/l [16].
Při podezření na recidivu krvácení je indikováno nové endoskopické vyšetření a ošetření zdroje. Při neúspěchu je ke zvážení selektivní transarteriální embolizace pod radiodiagnostickou kontrolou. Pokud není pacient stabilní nebo není k dispozici transarteriální embolizace, je nutné recidivu řešit chirurgicky.
Transarteriání embolizace
Transarteriální embolizace je radiointervenční metoda, kdy po selektivní katetrizaci cévy je tato embolizována. Jako přístup se nejčastěji používá arteria femoralis. Jako embolizační materiál se nejčastěji užívá n-butyl kyanoakrylát nebo různé druhy spirálek (coilů).
Technická úspěšnost se blíží 100 %, klinický efekt je u 65–90 % nemocných. Indikací je především recidiva krvácení po endoskopické terapii, případně profylaktická aplikace u rizikových vředů (Forrest I (a, b) a IIa a vředů větších než 15 mm) (obr. 2, 3) [19]. Embolizace aktivně krvácející léze nebo embolizace „na slepo“ bez průkazu aktivního krvácení má obdobné výsledky [6]. V průběhu angiografie aktivně krvácí asi polovina pacientů [14].
Transarteriální embolizace je také efektivní u krvácejících maligních lézí [20].
Chirurgická léčba
Operační intervence je nutná asi u 4 % nemocných s krvácením do horní části GIT. Téměř vždy jde o peptické léze. Největší skupinu operovaných nemocných představují duodenální vředy (75 %) [15]. Skupina nemocných, kde je vyšší riziko chirurgické intervence, je charakterizována vyšším věkem, velkými vředy (2 cm a výše) s rizikovou lokalizací a krátkou anamnézou krvácení s příznaky šoku při přijetí [16].
Důležitým faktorem chirurgické léčby je její správné načasování. Dříve uváděné pomůcky jako podání 5–6 transfuzí za 24 hod apod. nelze dnes brát jako jasné dogma, nicméně u rizikových nálezů, recidivy krvácení a vyčerpání endoskopické a radiologické terapie může být správně indikovaná operace pro nemocného život zachraňující.
Hlavní indikací chirurgické léčby je selhání dosavadní terapie (ať endoskopické, nebo radiologické) nebo její nedostupnost. Dále masivní krvácení s oběhovou nestabilitou nemocného, která nereaguje na léčbu a neumožňuje provedení méně invazivní intervence. Také u recidivy krvácení, především s rychlým zhoršením oběhových parametrů, je třeba zvažovat operační léčbu. Zkušenosti ošetřujícího lékaře, pečlivé monitorování nemocného a případná včasná indikace k operaci zabrání vyčerpání homeostatikých mechanizmů organizmu a vzniku refrakterní fáze šokového stavu.
U duodenálních vředů (na zadní stěně bulbu duodena) je indikována duodenotomie, propichová ligatura vředu a podvaz a. gastroduodenalis (obr. 4). Pouhé prošití vředu má vysoké riziko recidivy krvácení (uvádí se až 50 %). V případě, že se během operace nepodaří ošetřit a. gastroduodenalis, je možné doplnění transarteriální embolizace této cévy v druhé době. Někdy může vřed penetrující do hlavy pankreatu způsobit tak velkou destrukci stěny duodena, že je nutná vynucená resekce, obvykle druhého typu dle Billrotha. V těchto případech může být obtížné bezpečné uzavření pahýlu duodena. Pak je indikována dekomprese duodenálního pahýlu T drénem nebo jiným slabým katetrem (obr. 5). Vynucená resekce je nutná asi u 10 % operovaných nemocných. U žaludečních vředů je obvykle postačujícím výkonem excize vředu a sutura žaludeční stěny. Při technicky obtížné situaci může pomoci gastrotomie, propich vředu a ideálně devaskularizace této části (nejčastěji opich a gastrica sin). V současné době, kdy jsou k dispozici blokátory protonové pumpy, není třeba připojovat definitivní antisekreční výkon [16,21].
Urgentní operace jsou zatíženy vysokou letalitou kolem 25–30 %. Jde ale o skupinu vysoce rizikových nemocných, u kterých selhaly všechny méně invazivní přístupy.
Obr. 5. 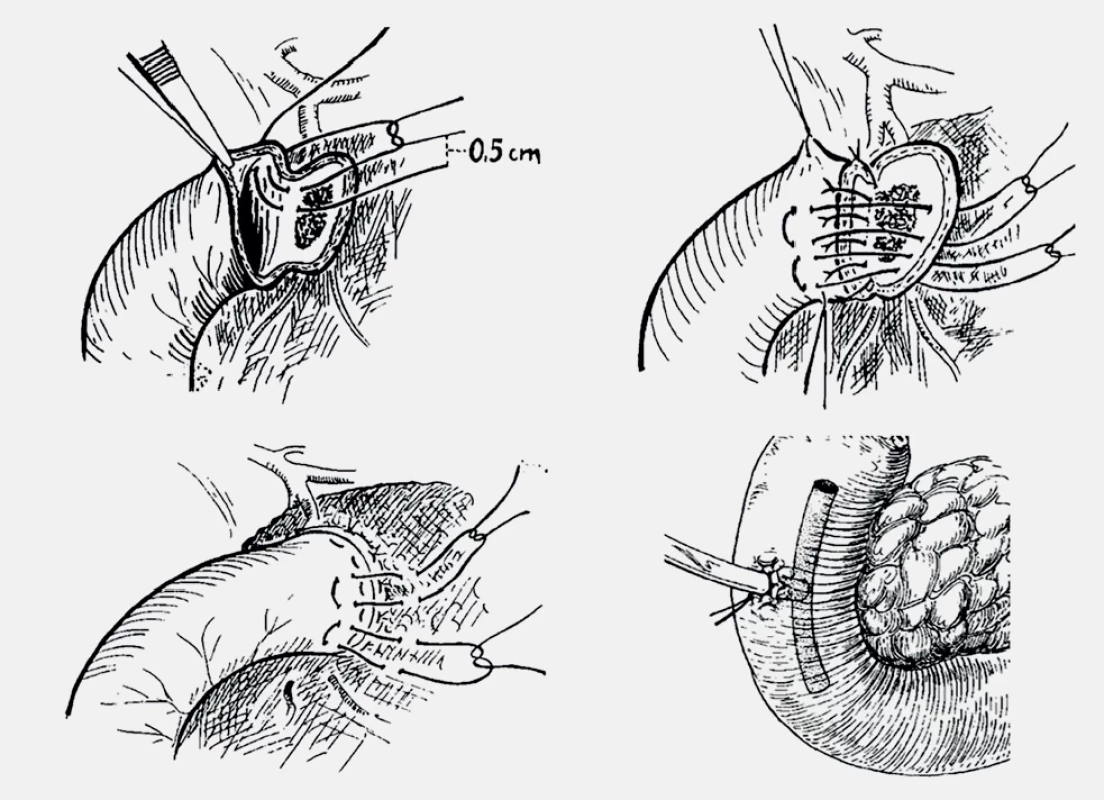
Uzávěr duodena dle Bsteha s pojistnou duodenostomií – možné řešení při destrukci zadní stěny bulbu duodena. Zdroj: archiv autora.
Closure of the duodenal stump according to Bsteh and duodenostomy. Source: author's archive.Vzácné zdroje krvácení do GIT
Aortoenterická píštěl – buď je primární, nejčastěji z aneuryzmatu aorty, nebo při infekci. Sekundární vzniká jako komplikace cévní náhrady – ať chirurgicky, nebo endovaskulárně založené. Diagnóza je potvrzena CT vyšetřením a léčba je buď chirurgická, nebo endovaskulární.
Ruptura aneuryzmatu viscerální tepny je potenciálně fatální komplikace. Nejčastěji se aneuryzma nachází na lienální tepně. Diagnóza je potvrzena CT, metodou volby v léčbě je endovaskulární embolizace.
Žaludeční submukozní arteriální kolaterála – extrémně vzácná příčina krvácení do GIT. Diagnóza a léčba je endoskopická.
M. Dieulafoy – vzácná léze, která může být příčinou 2–4 % krvácení do GIT. Jde o rozšířenu submukózní cévu. Patofyziologie vzniku onemocnění není známa. Léze je obvykle malá, 2–5 mm. Častěji se vyskytuje u starších mužů. V rámci léčby by mělo být dostatečné endoskopické ošetření, při neúspěchu je možné uvažovat o embolizaci. V případě refrakterního krvácení je poslední možností chirurgické řešení, kdy je dostatečná excize léze. Při operaci ale může být problém rozšířenou cévu správně lokalizovat.
Cameronova léze – slizniční trhlina v místě krčku hiátové hernie. Podkladem je opakovaná traumatizace stěny žaludku v místě hiátu. Iniciální diagnostika a léčba je endoskopická, jako prevenci recidivy lze zvažovat fundoplikaci.
Hemosuccus pancreaticus – jde o krvácení do d. Wirsungi a následně přes papilu do duodena. Letalita je kolem 10 %. Nejčastější příčinou je ruptura aneuryzmatu viscerálních tepen. Diagnóza i terapie vyžaduje kombinovaný endoskopický a radiologický přístup.
Hemobilie – krvácení do biliárního traktu. Nejčastěji jde o venobiliární píštěl. Etiologicky jde nejčastěji o iatrogenní komplikaci po intervencích v podjaterní krajině. Klinicky se projevuje jako tzv. Quinckeho trias (krvácení do GIT, bolesti v pravém podžebří a intermitentní obstrukční ikterus). Léčba je endoskopická nebo radiointervenční.
Syndrom Mallory Weiss – trhlina v oblasti kardie vznikající při opakovaném zvracení. Anamnéza je typická, nejprve pacient zvrací žaludeční obsah, později se objevuje příměs čerstvé krve. Většinu se krvácení zastaví spontánně a primární diagnostika i terapie je endoskopická [9,22,23].
Krvácení z jícnových varixů – rozdíly proti nevarikóznímu krvácení
Problematiku krvácení při portální hypertenzi řeší doporučený postup České hepatologické společnosti ČLS JEP [24].
Hlavní rozdíly proti nevarikóznímu krvácení do GIT jsou:
- Podání antibiotik už v předendoskopické fázi (chinolony nebo cefalosporiny 3. generace).
- Podání vazoaktivních léků ovlivňujících splachnickou perfuzi: terlipresin 1–2 mg každé 4 hod i.v. nebo somatostatin 250 μg bolus i.v., dále kontinuálně 250–500 μg/hod i.v., případně octreotid 50 μg bolus i.v., dále kontinuálně 25–50 μg/hod i.v.
- V případě vzniku jaterní encefalopatie se podává laktulóza 15–30 ml každých 8–12 hod k dosažení 2–3 stolic denně, event. v kombinaci s rifaximinem.
- Endoskopická diagnostika a léčba by měla být provedena do 12 hod od přijetí.
- Za metodu volby v endoskopické léčbě je považována ligace varixů.
- Balonková sonda je indikována pouze při selhání léčby.
- Alternativními metodami léčby jsou jícnový stent a TIPS.
- V rámci prevence krvácení, případně recidivy krvácení se podávají neselektivní beta blokátory a současně je indikována endoskopická eradikace varixů. U nemocných s vysokým portosystémovým gradientem je ke zvážení TIPS.
Závěr
Krvácení do horní části GIT stále patří mezi potenciálně fatální náhlé příhody břišní. Přes pokroky v diagnostice a terapii se letalita tohoto onemocnění dlouhodobě nemění. Je to dáno změnou skladby nemocných, kdy jsou častěji postiženi starší polymorbidní nemocní s bohatou farmakologickou anamnézou a omezenými rezervami organizmu. Správný postup diagnostiky a léčby, především načasování jednotlivých kroků, je v rukou ošetřujícího lékaře, který je stále nejčastěji z chirurgického oboru. V článku jsou shrnuty současné poznatky a doporučené postupy léčby tohoto onemocnění. I když jednotlivé modality nemusí být vždy všude dostupné, jejich znalost, společně s relativně krátkými vzdálenostmi mezi zdravotnickými zařízeními v České republice, může vést k jejich širšímu použití. Na druhé straně rozhodnutí ošetřujícího lékaře, tj. chirurga o včasné operaci u nemocného s hraniční oběhovou stabilitou při nedostupnosti méně invazivních metod může být pro nemocného život zachraňující.
Konflikt zájmů
Autor článku prohlašuje, že není v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů
Zdroje
1. Gralnek IM, Dumonceau JM, Kuipers EJ et al. Diagnosis and management of nonvariceal upper gastrointestinal hemorrhage: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy 2015; 47(10): a1–a46. doi: 10.1055/s-0034-1393172.2. Al Dhahab H, McNabb-Baltar J, Al-Taweel T et al. State-of-the-art management of acute bleeding peptic ulcer disease. Saudi J Gastroenterol 2013; 19(5): 195–204. doi: 10.4103/1319-3767.118116.3. Laine L, Barkun AN, Saltzman JR et al. ACG Clinical Guideline: Upper gastrointestinal and ulcer bleeding. Am J Gastroenterol 2021; 116(5): 899–917. doi: 10.14309/ajg.0000000000001245.4. Ejtehadi F, Sivandzadeh GR, Hormati A et al Timing of emergency endoscopy for acute upper gastrointestinal bleeding: a literature review. Middle East J Dig Dis 2021; 13(3): 177–185. doi: 10.34172/mejdd.2021.223.5. Li XJ, Fung BM. Advancements in endoscopic hemostasis for non-variceal upper gastrointestinal bleeding. World J Gastrointest Endosc 2024; 16(7): 376–384. doi: 10.4253/wjge.v16.i7.376.6. Samuel R, Bilal M, Tayyem O et al. Evaluation and management of non-variceal upper gastrointestinal bleeding. Dis Mon 2018; 64(7): 333–343. doi: 10.1016/j.disamonth.2018.02.003.7. Wasserman RD, Abel W, Monkemuller K et al. Non-variceal upper gastrointestinal bleeding and its endoscopic management. Turk J Gastroenterol 2024; 35(8): 599–608. doi: 10.5152/tjg.2024.23507.8. Szura M, Pasternak A. Upper gastrointestinal bleeding – state of the art. Folia Med Cracov 2014; 54(4): 59–78.9. Nelms DW, Pelaez CA. The acute upper gastrointestinal bleed. Surg Clin North Am 2018; 98(5): 1047–1057. doi: 10.1016/j.suc.2018.05.004.10. Menichelli D, Gazzaniga G, Del Sole F et al. Acute upper and lower gastrointestinal bleeding management in older people taking or not taking anticoagulants: a literature review. Front Med (Lausanne) 2024; 11 : 1399429. doi: 10.3389/fmed.2024.1399429.11. Stolow E, Moreau C, Sayana H et al. Management of non-variceal upper gi bleeding in the geriatric population: an update. Curr Gastroenterol Rep 2021; 23(4): 5. doi: 10.1007/s11894-021-00805-6.12. Gralnek IM, Stanley AJ, Morris AJ et al: Endoscopic diagnosis and management of nonvariceal upper gastrointestinal hemorrhage (NVUGIH): European Society of Gastrointestinal Endoscopy (ESGE) Guideline – Update 2021. Endoscopy 2021; 53(3): 300–332. doi: 10.1055/ a-1369-5274.13. Cagir Y, Durak MB, Yuksel I. Optimal endoscopy timing in elderly patients presenting with acute non-variceal upper gastrointestinal bleeding. BMC Gastroenterol 2024; 24(1): 444. doi: 10.1186/s12876-024-03541-z.14. Wang A, Yerxa J, Agarwal S et al. Surgical management of peptic ulcer disease. Curr Probl Surg 2020; 57(2): 100728. doi: 10.1016/j.cpsurg.2019.100728.15. Zittel TT, Jehle EC, Becker HD. Surgical management of peptic ulcer disease today – indication, technique and outcome. Langenbecks Arch Surg 2000; 385(2): 84–96. doi: 10.1007/s004230050250.16. Hoskovec David (ed.). Onemocnění žaludku. 1. vydání. Praha: We Make Media, s.r.o. 2020. 502 stran.17. Chang JH, Lye TJ, Zhu HZ et al. Systematic review and meta-analysis of prophylactic transarterial embolization for high-risk bleeding peptic ulcer disease. J Vasc Interv Radiol 2021; 32(4): 576–584. doi: 10.1016/j.jvir.2020.12.005.18. Roost I, Zetner D, Rosenberg J et al. Prophylactic arterial embolization in patients with bleeding peptic ulcers following endoscopic control of bleeding. Cochrane Database Syst Rev 2022; 2022(6): CD014999. doi: 10.1002/14651858.CD014999.19. Ini‘ C, Distefano G, Sanfilippo F et al. Embolization for acute nonvariceal bleeding of upper and lower gastrointestinal tract: a systematic review. CVIR Endovasc 2023; 6(1): 18. doi: 10.1186/s42155-023-00360-3.20. Hall T, Temperley HC, Mac Curtain BM et al. Transcatheter arterial embolisation (TAE) to treat acute upper gastrointestinal bleeding secondary to gastric cancer: a systematic review and meta-analysis. Surgeon 2024; 22(6): e213–e220. doi: 10.1016/j.surge.2024.09.009.21. Charvát D, Leffler J, Hoch J. Chirurgické léčení krvácení z gastroduodenálního vředu. Rozhl Chir 2007; 86(4): 166–169.22. Martino A, Di Serafino M, Orsini L et al. Rare causes of acute non-variceal upper gastrointestinal bleeding: a comprehensive review. World J Gastroenterol 2023; 29(27): 4222–4235. doi: 10.3748/wjg.v29.i27.4222.23. Abdoh Q, Samara E, Zayed A et al. Dieulafoy lesion with rare vascular complications: diagnostic and therapeutic approach. J Surg Case Rep 2024; 2024(12): rjae750. doi: 10.1093/jscr/rjae750.24. Fejfar T, Vaňásek T, Brůha R et al. Léčba krvácení v důsledku portální hypertenze při jaterní cirhóze – aktualizace doporučených postupů ČHS ČLS JEP. Gastroent Hepatol 2017; 71(2): 105–116. doi: 10.14735/amgh2017105.doc. MUDr. David Hoskovec, Ph.D.I. chirurgická klinika – břišní, hrudní a úrazové chirurgie1. LF UK a VFN v PrazeU Nemocnice 499/2128 08 Praha 2david.hoskovec@vfn.czORCID autoraD. Hoskovec 0000-0003-2948-8989Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2025 Číslo 7- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Riziko rozvoje závažné infekce po císařském řezu lze snížit provedením antiseptického výplachu vaginy
- Úloha růstového faktoru TGF-β v procesu hojení ran
- Topicky aplikovaný propolis může urychlovat hojení diabetických bércových vředů
-
Všechny články tohoto čísla
- K významnému životnímu jubileu prof. MUDr. Ivana Čapova, CSc.
- Ad gloriam medicinae – k jubileu 70 let prof. MUDr. Ivana Čapova, CSc.
- Chirurg, profesor a také gurmet
- Role dynamické MR defekografie v diagnostickém algoritmu u pacientek s anorektální dysfunkcí
- Základy laparoskopie na boxových a virtuálních simulátorech I: zhodnocení po 10 letech (2014–2024) kurzů z pohledu jejich absolventů
- SSI – analýza vlastních dat a ekonomický dopad
- Akutní vyšetření k vyloučení poranění krční páteře u dospělých
- Současný přístup ke krvácení do horní části trávicího traktu
- Prof. MUDr. Josef Stingl, CSc., doyen klinické anatomie a chirurg, pětaosmdesátiletý
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Současný přístup ke krvácení do horní části trávicího traktu
- Role dynamické MR defekografie v diagnostickém algoritmu u pacientek s anorektální dysfunkcí
- Akutní vyšetření k vyloučení poranění krční páteře u dospělých
- Prof. MUDr. Josef Stingl, CSc., doyen klinické anatomie a chirurg, pětaosmdesátiletý
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



