-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Efektivita a bezpečnost budesonidu MMX (Cortiment®) v dlouhodobé udržovací léčbě ulcerózní kolitidy
The efficacy and safety of budesonide MMX (Cortiment®) for long-term maintenance therapy of ulcerative colitis
Background:
The role of budesonide-MMX (Cortiment®) in the induction of remission in mild to moderate active ulcerative colitis (UC) is already well established; however, data on maintenance treatment are limited.
Aim:
To assess the efficacy and safety of this medication as a long-term maintenance treatment.
Methods:
Forty patients, corresponding to responders in a previous 8-weeks induction study on continuing medication, were included in this multicentric (10 Czech centers were involved) retrospective 12-month study. Partial Mayo score and endoscopic Mayo score were assessed at 6 and 12 months, adverse events of special interest were recorded, and tolerability and compliance data were collected.
Results:
Significant maintenance of decreased clinical and endoscopic activity of UC were observed; the mean partial resp. endoscopic Mayo scores were 2.2 resp. 0.96 at week 8, 2.33 resp. 1.09 at 6 months, and 1.03 resp. 0.86 at 12 months. Complete mucosal healing (Mayo 0) was found in 19 (48%) patients at month 12. Clinical remission was achieved in 63% resp. (month 6) 66% (month 12) patients. A clinical response was observed even in 80% resp. 85% patients. The incidence of adverse events (AE) was very low. No patient interrupted or discontinued the maintenance medication because of the risk of experiencing AE.
Conclusion:
Our results demonstrate good efficacy and safety of Cortiment® use in the long-term maintenance treatment of mild to moderate UC.
Key words:
ulcerative colitis – maintenance therapy – glucocorticoids – budesonide-MMX
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.
Submitted: 4. 6. 2018
Accepted: 13. 6. 2018
Autoři: Luděk Hrdlička 1; M. Bortlík 2; T. Douda 3; P. Drastich 4
; Přemysl Falt 5
; P. Matějková 6; J. Koželuhová 7; M. Liberda 8; L. Nedbalová 9; A. Novotný 10; M. Kolář 2
; M. Lukáš 2
Působiště autorů: Gastroenterologie, Medicon, a. s., Poliklinika Budějovická, Praha 1; Klinické a výzkumné centrum pro střevní záněty ISCARE I. V. F. a. s., Praha 2; II. interní gastroenterologická klinika LF UK a FN Hradec Králové 3; Klinika hepatogastroenterologie, Transplantcentrum, IKEM, Praha 4; Centrum péče o zažívací trakt, Vítkovická nemocnice a. s., Ostrava 5; Gastroenterologické oddělení, EGK s. r. o., Sanatorium sv. Anny, Praha 6; Gastroenterologie, I. interní klinika FN Plzeň 7; Gastroenterologická ambulance, Nemocnice Valašské Meziříčí, a. s. 8; IBD centrum Turnov, Krajská nemocnice Liberec, a. s. 9; IV. interní klinika – klinika gastroenterologie a hepatologie, 1. LF UK a VFN v Praze 10
Vyšlo v časopise: Gastroent Hepatol 2018; 72(4): 329-333
Kategorie: IBD: původní práce
doi: https://doi.org/10.14735/amgh2018329Souhrn
Úvod:
Úloha budesonidu MMX (Cortiment®) v indukční léčbě mírně až středně aktivní ulcerózní kolitidy (UC) je již dobře dokumentována, literární data o podávání preparátu v udržovací terapii chybějí.
Cíl:
Zhodnotit efektivitu a bezpečnost podávání léku Cortiment® v dlouhodobé udržovací léčbě pacientů s UC.
Metodika:
Do multicentrického (10 pracovišť) retrospektivního ročního sledování bylo zařazeno celkem 40 pacientů s mírně a středně aktivní UC, kteří po ukončení předchozího 8týdenního projektu zaměřeného na indukční léčbu pokračovali v dlouhodobé medikaci. Efektivita léčby byla sledována pomocí klinického i endoskopického Mayo skóre, bezpečnost, tolerance léčby a adherence k ní byly monitorovány dotazníkovou metodou (vizity po 6 a 12 měsících).
Výsledky:
Při dlouhodobé terapii lékem Cortiment® bylo prokázáno významné přetrvávání efektu léčby na klinickou a endoskopickou aktivitu UC, průměrná hodnota parciálního Mayo skóre byla 2,2 v týdnu 8 a 2,33, resp. 1,03 po 6 a 12 měsících. Průměrná hodnota endoskopického Mayo skóre v našem souboru činila 0,96 v týdnu 8 a 1,09 a 0,86 po 6 a 12 měsících léčby. Makroskopické známky kompletního slizničního hojení (endoskopické subskóre Mayo 0) vykazovalo při ukončení sledování 19 (48 %) nemocných. V klinické remisi (parciální Mayo skóre ≤ 1) se nacházelo 63, resp. 66 % nemocných po 6 a 12 měsících, klinickou odpověď jsme zaznamenali dokonce u 80, resp. 85 % pacientů. Výskyt nežádoucích účinků byl relativně velmi nízký, žádný z nemocných kvůli nim neukončil nebo nepřerušil dlouhodobou léčbu.
Závěr:
Zjištěné výsledky dlouhodobé udržovací léčby lékem Cortiment® prokazují velmi dobrou efektivitu a výborný bezpečnostní profil v léčbě nemocných s mírnou až středně závažnou formou UC.
Klíčová slova:
ulcerózní kolitida – udržovací léčba – glukokortikoidy – budesonid MMX
Úvod
Cortiment® 9 mg je relativně novým lékem určeným pro léčbu mírně až středně aktivní ulcerózní kolitidy (UC). Účinnou látkou je syntetický topický glukokortikoid budesonid, který má vysokou afinitu ke glukokortikoidním receptorům. Jeho významnou předností je vysoký „first-pass effect“ umožňující odbourání cca 90 % budesonidu vstřebaného ze střeva při prvním průchodu játry. Tím je v podstatné míře eliminována frekvence a intenzita nežádoucích účinků glukokortikoidové medikace. Unikátní vazebný systém, označovaný jako MMX (multi-matrix), pak zajišťuje uvolnění účinné látky až v tlustém střevě.
Účinnost a bezpečnost terapie přípravkem Cortiment® 9 mg v indukční léčbě je dobře dokumentována velkými registračními studiemi 3. fáze nazvanými CORE I a CORE II [1,2]. Obou studií se zúčastnilo více než 1 000 pacientů s mírně až středně aktivní UC a na základě jejich výsledků byl preparát registrován k použití v klinické praxi. Autoři tohoto sdělení publikovali v roce 2016 výsledky své práce [3], ve které sledovali v 10 centrech celkem 81 pacientů, u kterých byl Cortiment® 9 mg použit v indukci remise u mírně a středně aktivních UC pacientů. Data z tohoto retrospektivního sledování potvrdila výbornou efektivitu a velmi dobrý bezpečnostní profil léku.
Všechny zmíněné uveřejněné práce byly zaměřeny na aktivní pacienty a krátkodobou (8týdenní) indukční léčbu. Vedlejším výstupem analýzy dat ze sledování české kohorty bylo zjištění, že téměř u poloviny pacientů byla medikace podávána i po ukončení 8týdenního období sledování, a to i u pacientů, kteří se na konci krátkodobého sledování nacházeli v klinické remisi [3]. O dlouhodobé léčbě přípravkem Cortiment® není dostatek informací, data jsou dostupná v podstatě pouze z analýzy 12měsíčního klinického hodnocení zaměřeného zejména na bezpečnost podávání léku Cortiment® v dávce 6 mg/den (62 pacientů na účinné látce vs. 61 na placebu). Výsledky studie potvrzují přetrvávající benefit léčby při zachování dobrého bezpečnostního profilu podávané medikace [4–6]. Cílem této práce je zhodnotit účinnost a bezpečnost dlouhodobého podávání budesonidu MMX (Cortiment®) v udržovací léčbě v reálné klinické praxi u pacientů s mírnou až středně aktivní UC.
Metodika a soubor pacientů
Jedná se o retrospektivní multicentrické sledování, do kterého bylo zařazeno celkem 40 pacientů s mírně nebo středně aktivní UC z celkem 10 českých pracovišť. Tito nemocní absolvovali v rámci již zmiňované studie (původně 81 aktivních UC pacientů) [3] indukční 8týdenní léčbu budesonidem MMX v dávce 9 mg/den a dále pokračovali v udržovací léčbě. Indikací pro pokračování v udržovací léčbě právě preparátem budesonid MMX bylo nejčastěji selhání jiné udržovací léčby v minulosti, kortikodependence nebo jen parciální terapeutická odpověď indukčního režimu. Iniciálně 35 pacientů pokračovalo na dávce 9 mg/den, 5 pacientů užívalo nadále 9 mg ob den. Během trvání studie docházelo u některých pacientů ke snižování dávky na 9 mg ob den, podíl pacientů na redukované dávce činil na konci studie 50 % (14 z 28 sledovaných nemocných).
K analýze byla u dlouhodobě léčených pacientů převzata data z projektu sledování indukční léčby (týdny 0, 4 a 8) [3] a dále byli tito pacienti monitorováni po 6 a 12 měsících. Sledování bylo realizováno pomocí elektronických kazuistických formulářů, monitorována byla klinická aktivita choroby (parciální Mayo skóre), endoskopická aktivita (endoskopické Mayo subskóre), zaznamenávány byly případné změny v konkomitantní medikaci, výskyt nežádoucích účinků a komplikací léčby, snášenlivost terapie a pacientovo subjektivní vyjádření adherence k medikaci.
Za klinickou odpověď bylo považováno snížení parciálního Mayo skóre ≥ 2 bodů proti výchozí hodnotě v týdnu 0. Klinická remise onemocnění byla definována hodnotou parciálního Mayo skóre 1 nebo 0. Endoskopická hodnocení byla provedena při sigmoideoskopickém vyšetření nebo koloskopii podle klasifikačního systému endoskopického subskóre Mayo indexu [7,8]. Klinická a demografická data sledovaných pacientů jsou uvedena v tab. 1.
Tab. 1. Klinické a demografické charakteristiky souboru – týden 8, začátek udržovací terapie.
Tab. 1. Clinical and demographic chracteristics of the cohort – week 8, start of the maintenance therapy.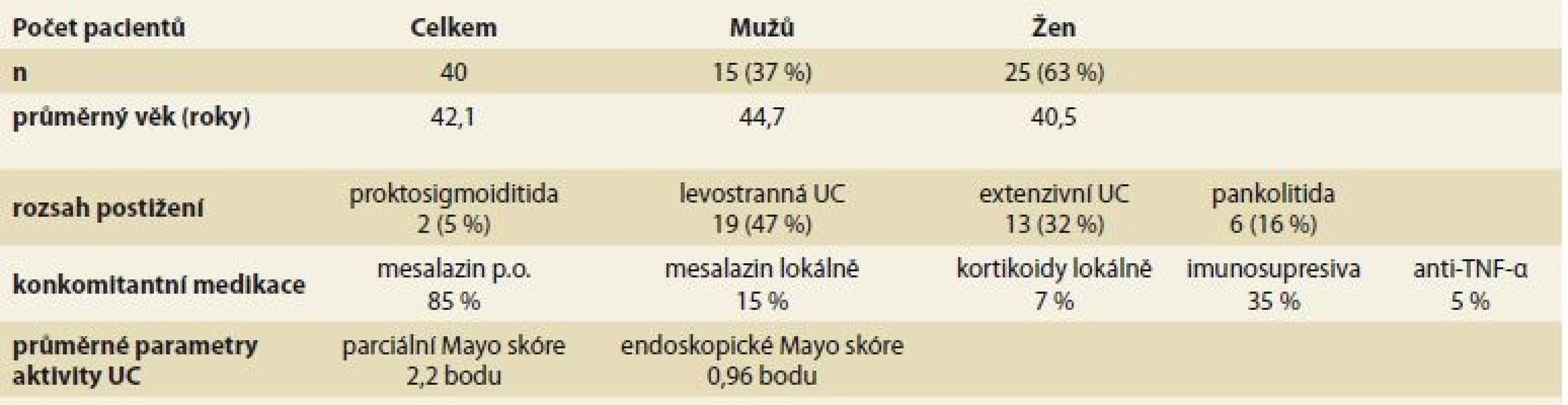
UC – ulcerózní kolitida, anti-TNF-α – anti-tumor nekrotizující faktor α Výsledky
Klinický efekt
Do ročního sledování vstoupilo celkem 40 pacientů, po 1 roce bylo stále na medikaci preparátem Cortiment® 28 pacientů (70 %), 7 pacientů ukončilo léčbu po 6 měsících pro dlouhodobou hlubokou remisi, 5 pacientů (12,5 %) ukončilo účast v projektu pro sekundární selhání. Během dlouhodobé léčby preparátem Cortiment® přetrvávala u 35 nemocných z našeho souboru (87,5 %) terapeutická odpověď – průměrná hodnota parciálního Mayo skóre byla 2,2 v týdnu 8 a 2,33, resp. 1,03 po 6 a 12 měsících. Přetrvávala zásadní regrese nebo úplné vymizení krvácení, průměrná hodnota subskóre krvácení byla 0,43 a 0,43, resp. 0,18 v týdnu 8 a po 6 a 12 měsících.
V klinické remisi se nacházelo 58, resp. 63 % a 66 % nemocných v týdnu 8 a po 6 a 12 měsících, klinickou odpověď jsme zaznamenali dokonce u 85, resp. 80 % a 85 % pacientů. Po dokončení ročního sledování pokračovalo v medikaci Cortiment® 19 (48 %) sledovaných pacientů.
Slizniční hojení
Naše výsledky dokumentují i přetrvávající benefit dlouhodobé léčby na zlepšení endoskopického nálezu, průměrná hodnota endoskopického Mayo skóre v našem souboru činila 0,96 v týdnu 8, 1,09 a 0,86 po 6 a 12 měsících léčby. Makroskopické známky kompletního slizničního hojení (endoskopické subskóre Mayo 0) vykazovalo při ukončení sledování 19 (48 %) nemocných (graf 1 a 2).
Graf 1. Parciální Mayo skóre a subskóre krvácení.
Graph 1. Partial Mayo score and bleeding subscore
Graf 2. Endoskopické Mayo skóre, klinická odpověď a klinická remise.
Graph 2. Endoscopic Mayo score, clinical response and clinical remission.
Vedlejší účinky, snášenlivost medikace, adherence
Podávaná léčba vykazovala po celou dobu sledování velmi dobrý bezpečnostní profil, vč. cíleně sledované potenciální glukokortikoidové toxicity, výskyt jednotlivých nežádoucích účinků po 6 i 12 měsících sledování byl relativně nízký, nejčastěji se objevovaly bolesti hlavy (u 7,5 % nemocných) a akné (12,5 %), vždy s maximem v 6. měsíci a poklesem výskytu ve 12. měsíci. Alespoň 1 nežádoucí účinek udržovací terapie referovalo 10 (25 %) pacientů, u žádného z nich nebyla z těchto důvodů dlouhodobá léčba přerušena nebo ukončena. Pacienti reportovali velmi dobrou subjektivní snášenlivost podávané medikace a adherenci k ní, hodnoty bodovacích skóre subjektivního hodnocení léčby byly stabilní po celou dobu trvání studie (graf 3 a 4).
Graf 3. Nežádoucí účinky léčby.
Graph 3. Adverse effects of medication.
Graf 4. Subjektivní snášenlivost a compliance k léčbě.
Graph 4. Subjective tolerance and compliance.
Diskuze
Účinnost a zejména bezpečnost udržovací léčby budesonidem MMX byla zkoumána ve12měsíční studii, do níž bylo zařazeno 123 pacientů v endoskopické remisi po absolvování indukční fáze léčby ve studiích CORE I a CORE II [1,2]. Pacienti byli zařazeni bez ohledu na to, zda byli původně ve větvi s účinnou látkou, placebem nebo srovnávací medikací, non-respondéři indukční léčby se mohli ještě dodatečně kvalifikovat dosaženou endoskopickou remisí po absolvování open-label vmezeřené 8týdenní studie s přípravkem Cortiment® v dávce 9 mg/den. Zařazení nemocní byli randomizováni v poměru 1 : 1 do skupiny placebové a skupiny užívající Cortiment® v dávce 6 mg (toto dávkování preparátu není v současné době komerčně dostupné). Primárním cílem, co se účinnosti týče, byla klinická remise po 1, 3, 6, 9 a 12 měsících. Střední čas do klinického relapsu byl 181 dní v placebové skupině, ve skupině s lékem Cortiment® přesahoval 12měsíční dobu trvání studie (statisticky signifikantní rozdíl; p = 0,02). Pravděpodobnost klinického relapsu byla 59,7 % (placebová větev) oproti 40,7 % u nemocných na účinné léčbě [4]. Rozdíl v procentu pacientů v klinické remisi naproti tomu nebyl statisticky signifikantní, nejspíše kvůli nízké statistické síle souboru [9]. Naše výsledky z reálné klinické praxe jsou ještě příznivější, k sekundárnímu selhání léčby během ročního sledování došlo jen u 12,5 % nemocných, důvodem budou nejspíše méně ambiciózní vstupní kritéria, která umožnila sledovat i pacienty s mírnou aktivitou po indukční fázi projektu, kteří byli v uspokojivém klinickém stavu i při mírně aktivním endoskopickém nálezu (citovaná studie požadovala úplnou endoskopickou remisi) a z pokračování terapie dlouhodobě profitovali. Druhou skutečností, která mohla příznivě ovlivnit výsledky dosažené v našem souboru, je fakt, že se nejednalo o monoterapii, naprostá většina našich pacientů byla kromě MMX budesonidu léčena i další protizánětlivou léčbou, zejména aminosalicyláty, zatímco v uvedené práci tato medikace byla vyloučena. Klinická charakteristika našich nemocných jistě daleko lépe kopíruje běžnou klinickou praxi, uplatňuje se zde také synergický efekt s konkomitantní medikací a podávání MMX budesonidu je další možností dlouhodobé léčby mírnější aktivity onemocnění i u nemocných s UC již na imunosupresivní (v našem souboru 35 %) a dokonce i biologické léčbě (5 %). Oprávněnost kombinace s perorální medikací aminosalicyláty (85 % v našem souboru) byla ověřena například studií CONTRIBUTE [10].
Preparáty s obsahem účinné látky budesonid mají obecně v porovnání se systémovými steroidy zásadně nižší výskyt a intenzitu nežádoucích účinků [11]. Bezpečnost MMX budesonidu při krátkodobém podávání během indukční léčby jednoznačně potvrdila podrobná bezpečnostní analýza provedená v rámci studií CORE I a CORE II [1,2]. Jedinečný bezpečnostní profil při podávání 6 mg Cortiment®/den po dobu 12 měsíců ověřila již opakovaně zmiňovaná dlouhodobá klinická zkouška [4–6]. Kromě standardních klinických bezpečnostních kontrol v jejím rámci probíhaly i podrobné cílené laboratorní testy k ověření možného negativního vlivu na produkci vlastních glukokortikoidů (ranní kortizolemie, ACTH stimulační test), glukózový metabolizmus a kvalitu kostní matrix (denzitometrie). Provedené testy neprokázaly signifikantní rozdíly mezi skupinou placebovou a nemocnými na účinné medikaci MMX budesonidem ani po 12 měsících terapie. Tato data potvrzují i naše výsledky – v našem sledování jsme neprováděli sofistikované laboratorní testy, zaměřili jsme se na cílené vyhledávání klinických symptomů potenciální glukokortikoidové toxicity. Jejich záchyt byl nízký a žádný z pacientů nemusel z těchto důvodů přerušit nebo dokonce ukončit udržovací léčbu MMX budesonidem.
Závěr
Získaná data prokazují velmi dobrou efektivitu i bezpečnost udržovací léčby budesonidem MMX (Cortiment®) u pacientů s mírnou až středně těžkou UC. Dlouhodobé podávání léku vede nejen k přetrvávání pozitivního efektu ve smyslu udržení klinické remise, ale i ke zlepšení endoskopického nálezu při zachování výborného bezpečnostního profilu.
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 4. 6. 2018
Přijato: 13. 6. 2018
MUDr. Luděk Hrdlička
Gastroenterologie, Medicon, a.s.
Poliklinika Budějovická
Antala Staška 1670/ 80 140 46 Praha 4
Zdroje
1. Travis SP, Danese S, Kupcinskas L et al. Once-daily budesonide MMX in active, mild-to-moderate ulcerative colitis: results from the randomised CORE II study. Gut 2014; 63 (3): 433–441. doi: 10.1136/gutjnl-2012-304258.
2. Sandborn WJ, Travis S, Moro L et al. Once-daily budesonide MMX® extended-release tablets induce remission in patients with mild to moderate ulcerative colitis: results from the CORE I study. Gastroenterology 2012; 143 (5): 1218–1226. doi: 0.1053/j.gastro.2012.08.003.
3. Hrdlicka L, Bortlik M, Douda T et al. Budesonid MMX (Cortiment® 9 mg) v léčbě ulcerózní kolitidy v reálné klinické praxi. Gastroent Hepatol 2016; 70 (6): 509–513. doi: 10.14735/amgh2016509.
4. Sandborn WJ, Danese S, Ballard ED et al. Efficacy of Budesonide MMX® 6 mg QD for the maintenance of remission in patients with ulcerative colitis: results from a phase III, 12 month safety and extended use study. Gastroenterology 2012; 142 (5 Suppl 1): 564. doi: 10.1016/S0016-5085 (12) 62168-4.
5. Travis S, Danese S, Ballard ED et al. Safety analysis of Budesonide MMX 6 mg used for the maintenance of remission in patients with ulcerative colitis: results from a phase III, 12 month safety and extended use study. Gastroenterology 2012; 142 (5 Suppl 1): 566–567. doi: 10.1016/S0016-5085 (12) 62176-3.
6. Lichtenstein GR, Danese S, Ballard ED et al. Effect of Budesonide MMX 6 mg on the hypothalamic-pituitary-adrenal (HPA) axis in patients with ulcerative colitis: results from a phase III, 12 month safety and extended use study. Gastroenterology 2012; 142 (5) (Spuul 1): 785. doi: 10.1016/S00165085 (12) 63046-7.
7. Schroeder KW, Tremaine WJ, Ilstrup DM. Coated oral 5-aminosalicylic acid therapy for mildly to moderately active ulcerative colitis. A randomized study. N Engl J Med 1987; 317 (26): 1625–1629.
8. Rutgeerts P, Sandborn WJ, Feagan BG et al. Infliximab for induction and maintenance therapy for ulcerative colitis. N Engl J Med 2005; 353 (23): 2462–2476. doi: 10.1056/NEJMoa050516.
9. Lichteinstein GR. Budesonide multi-matrix for the treatment of patients with ulcerative colitis. Dig Dis Sci 2016; 61 (2): 358–370. doi: 10.1007/s10620-015-3897-0.
10. Rubin DT, Cohen RD, Sanborn WJ et al. Budesonide Multimatrix is efficacious for Mesalamine-refractory, mild to moderate ulcerative colitis: a randomised, placebo-controlled trial. J Crohns Colitis 2017; 11 (7): 785–791. doi: 10.1093/ecco-jcc/jjx032.
11. Rutgeerts P, Löfberg R, Malchow H et al. A comparison of budesonide with prednisolone for active Crohn’s disease. N Engl J Med 1994; 331 (13): 842–845. doi: 10.1056/NEJM199409293311304.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek Kvíz z klinické praxe
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2018 Číslo 4- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Itoprid v léčbě funkční dyspepsie
- Vliv podávání prokinetik na riziko syndromu bakteriálního přerůstání u pacientů užívajících inhibitory protonové pumpy
- Úloha růstového faktoru TGF-β v procesu hojení ran
-
Všechny články tohoto čísla
- Klinická a experimentální gastroenterologie
- Kvíz z klinické praxe
- Alveolární echinokokóza – vzácné onemocnění vyžadující multidisciplinární přístup
- Prevalencia a asociované faktory ovariálnych cýst u pacientiek s Crohnovou chorobou
- Porovnání účinnosti kolonické kapslové endoskopie a optické koloskopie u osob s pozitivním imunochemickým testem na okultní krvácení do stolice – multicentrická, prospektivní studie
- Experimentální enteroskopie s využitím kapsle s boční optikou
- Endosonograficky navigované drenážní výkony novými metalickými apozičními stenty s elektrokauterizační jednotkou (stent Hot AXIOS) – vlastní soubor 20 pacientů
- Mastocytární enterokolitida jako možná příčina chronického průjmového onemocnění
- Personalizovaná terapie pacientů s gastroezofageální refluxní chorobou – metodika stanovení genového profilu CYP2C19
- Efektivita a bezpečnost budesonidu MMX (Cortiment®) v dlouhodobé udržovací léčbě ulcerózní kolitidy
- Modulace signálních drah IL-12/IL-23 ustekinumabem tlumí poškozující zánět u pacientů s Crohnovou nemocí
- Klinický případ jaterního a pleuropulmonálního abscesu amébového původu u pacienta s chronickou hepatitidou B v Cotonou
- Hyponatremie v souvislosti s chorobami gastrointestinálního traktu
- 40th Czech and Slovak Endoscopic Days and 19th Endoscopic Day IKEM
- XLVI. májové hepatologické dny
-
Gastroenterologie a hepatologie nebude registrována v PubMed a co z toho plyne
Odpověď předsedovi České gastroenterologické společnosti - Zpráva o činnosti výboru ČGS ČLS JEP za období 2014–2018
- Výběr z mezinárodních časopisů
-
Správná odpověď na kvíz
Pneumatosis cystoides intestinalis (coli) - Kreditovaný autodidaktický test: klinická a experimentální gastroenterologie
- Metotrexát – znovu objevený lék pro Crohnovu nemoc
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Hyponatremie v souvislosti s chorobami gastrointestinálního traktu
- Mastocytární enterokolitida jako možná příčina chronického průjmového onemocnění
- Endosonograficky navigované drenážní výkony novými metalickými apozičními stenty s elektrokauterizační jednotkou (stent Hot AXIOS) – vlastní soubor 20 pacientů
- Metotrexát – znovu objevený lék pro Crohnovu nemoc
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



