-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Syndrom solitárního rektálního vředu
Solitary rectal ulcer syndrome
The authors summarise the basic facts about and personal experience with a rare nosological disorder – solitary rectal ulcer syndrome (SRUS). In the first part, the pathophysiology and the diagnostics of SRUS are mentioned. The generally accepted theory of the development of SRUS is supported by the relevant citations. The symptoms and the endoscopic picture and in uncertain cases also the biopsy are the basis for the diagnosis of SRUS. In diagnostics, evacuation proctography is crucial especially with regard to SRUS therapy planning. In the second part, all the possible SRUS therapies are described. First in the line is conservative therapy. If conservative therapy fails, endoscopic therapy can be indicated but with limited options. The most causal is surgical therapy, which also offers the most options. Finally, the authors share their clinical experience with patients suffering from solitary rectal ulcer syndrome.
Key words:
rectal prolapse – solitary rectal ulcer – evacuation proctography
The authors declare they have no potential conflicts of interest concerning drugs, products, or services used in the study.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.Submitted:
1. 6. 2012Accepted:
26. 7. 2012
Autoři: R. Procházka; P. Srna; J. Frydrych
Působiště autorů: Oddělení gastroenterologie Nemocnice Jablonec nad Nisou
Vyšlo v časopise: Gastroent Hepatol 2012; 66(4): 259-264
Kategorie: Klinická a experimentální gastroenterologie: přehledová práce
Souhrn
Autoři shrnují základní poznatky a zmiňují své zkušenosti se vzácnou nosologickou jednotkou – syndromem solitárního rektálního vředu (SRUS). V první části je zmíněna patofyziologie a diagnostika SRUS. Obecně uznávaná teorie vzniku SRUS je doložena citacemi relevantních studií. Diagnóza SRUS je stanovena z klinického a endoskopického obrazu a v případě nejasností i z biopsie. V diagnostice je nezastupitelná defekografie, především s ohledem na volbu terapie SRUS. Ve druhé části jsou popsány možnosti léčby SRUS. Vždy začínáme terapií konzervativní. V případě jejího selhání je možná endoskopická terapie, nicméně její efektivita je rovněž omezená. Nejkauzálnější je chirurgická léčba, která také nabízí i nejvíce možností. V závěru jsou zmíněny vlastní zkušenosti autorů se SRUS.
Klíčová slova:
rektální prolaps – solitární rektální vřed – defekografieDefinice
Syndrom solitárního rektálního vředu (SRUS) je vzácná a často zaměňovaná chronická benigní choroba provázející poruchu defekace. Nehledě na označení je endoskopický obraz velmi rozmanitý od erytému přes polypoidní změny až k typickému rektálnímu vředu. Vředy a polypy mohou být mnohočetné a vzácněji postihovat i sigma. První zmínka o SRUS je připisována francouzskému anatomovi a patologovi Jaenu Cruveilhieru, který v r. 1829 popsal čtyři případy nenádorových vředů rekta. Termín solitární rektální vřed byl poprvé použit v roce 1939 v nemocnici Sv. Marka v Londýně. Klinicko-patologické znaky nemoci byly podrobně popsány Madigenem a Morsonem na 68 pacientech v r. 1969 [1].
Epidemiologie
Prevalence SRUS je nízká 1 : 100 000 [2], částečně ovlivněna také neznalostí rozmanitých endoskopických a klinických projevů. Většina odborných sdělení až na výjimky počítá s jednotkami pacientů. Choroba je nejčastěji diagnostikována u pacientů středního věku, ale vyskytuje se také u pediatrických pacientů. Většina studií uvádí větší prevalenci v ženské populaci, ale jsou některé, které naopak uvádějí větší výskyt v populaci mužské.
Patofyziologie
SRUS vzniká v důsledku prolapsu rekta, který vede k ischemii sliznice. Tato teorie byla poprvé navržena již v r. 1975 Rutterem a Riddellem a opírá se o to, že rektální prolaps je častým nálezem na defekogramu pacientů se SRUS, a také, že SRUS má společné klinicko-patologické znaky s obstrukčním defekačním syndromem (ODS), s proctitis cystica profunda, s kloakogeními polypy a také s prolabujícími mukózními polypy. Ve všech případech se velmi pravděpodobně jedná pouze o jiné projevy rektálního prolapsu. Proto byl navržen termín „syndrom slizničního prolapsu (mucosal prolaps syndrom)“, který tyto chorobné jednotky sdružuje [3]. Oporu ischemické etiopatogenezi SRUS pak nabízejí studie měřící průtok krve v rektální sliznici pomocí laserové dopplerometrie. U pacientů se SRUS, stejně jako u pacientů s ODS, je zjišťován snížený klidový krevní průtok oproti kontrolám. Nižší prokrvení rektální sliznice je vysvětlováno horší autonomní cholinergní střevní regulací [4]. Navíc se po terapii biofeedbackem toto prokrvení normalizuje a u části pacientů se upravuje slizniční nález a mizí klinické obtíže [5]. Londsdale ve své práci podporuje ischemickou etiologii SRUS popisem mikrovaskulární patologie. Na základě histopatologických nálezů u pacientů se SRUS navrhnul následující posloupnost změn vedoucích až k ulceraci. A) Prolaps rekta vede k přetažení slizničních a podslizničních cév s následným zduřením poškozeného endotelu a zúžením cévního lumen. B) K těmto změnám v aferentní cirkulaci se navíc přidávají i změny v cirkulaci eferentní. Zhoršený venózní odtok vede ke kongesci v kapilární síti se zpomalením mikrocirkulace [6]. Na druhou stranu ne každý pacient s rektálním prolapsem vyvine SRUS a pouze u části pacientů s tímto syndromem nacházíme typickou ulcerózní formu. Bylo postulováno, že ke vzniku SRUS je nutný ještě další přídatný faktor, kterým je abnormálně vysoký transrektální tlak. Vysoký transrektální tlak vzniká při defekaci pacientů s intususcepcí a s hyperaktivními análními svěrači a také u pacientů s overtním rektálním prolapsem [7]. Overtní rektální prolaps neboli zevní rektální prolaps je detekovatelný fyzikálním vyšetřením. Okultní rektální prolaps neboli skrytý rektální prolaps, spíše známý pod pojmem intususcepce, je prokazatelný pouze defekograficky.
Obr. 1. Erytematozní forma. Fig. 1. Erythemathous type. 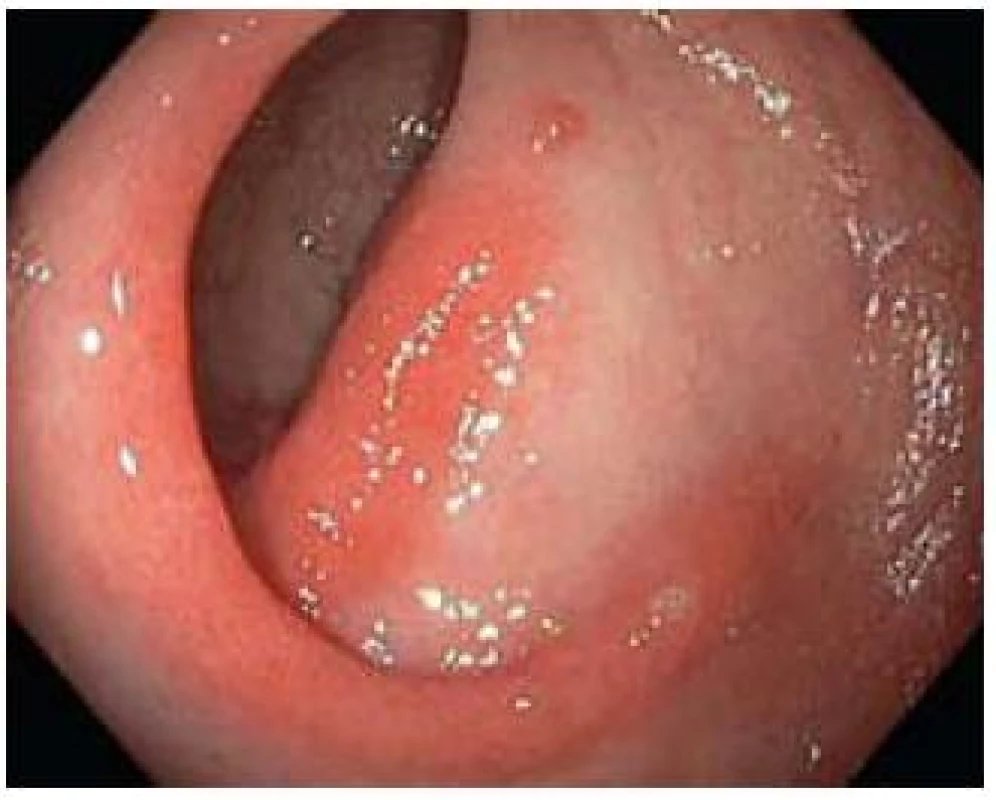
Obr. 2. Polypoidní forma. Fig. 2. Polypoid type. 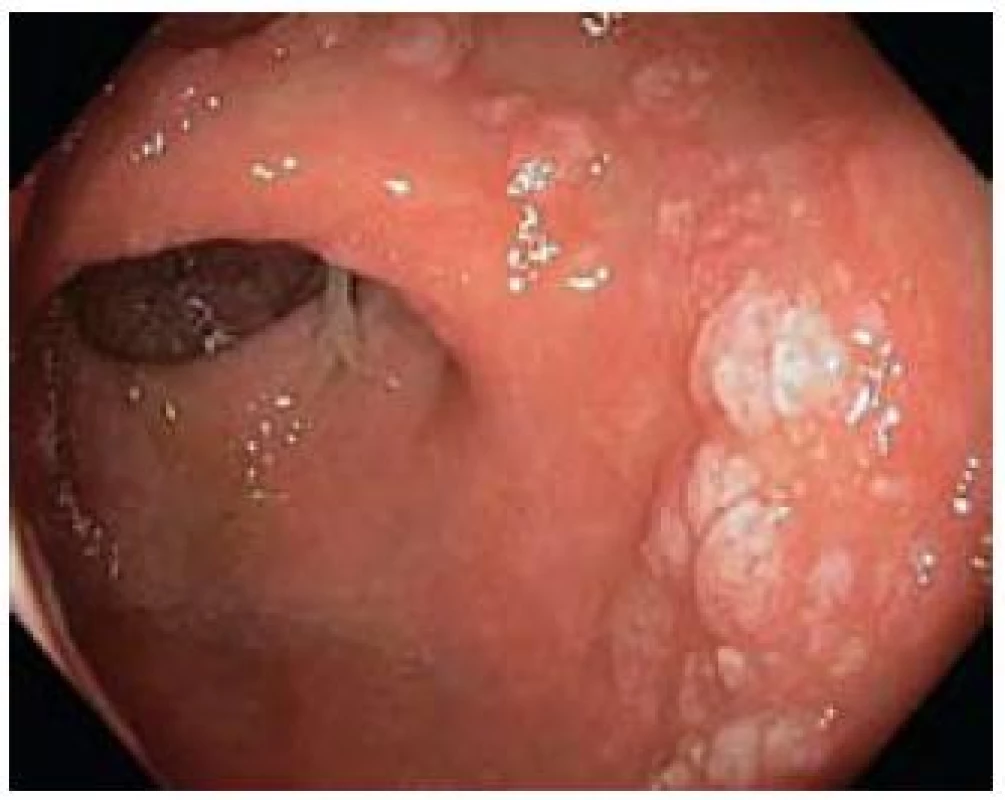
Obr. 3. Ulcerózní forma. Fig. 3. Ulcerous type. 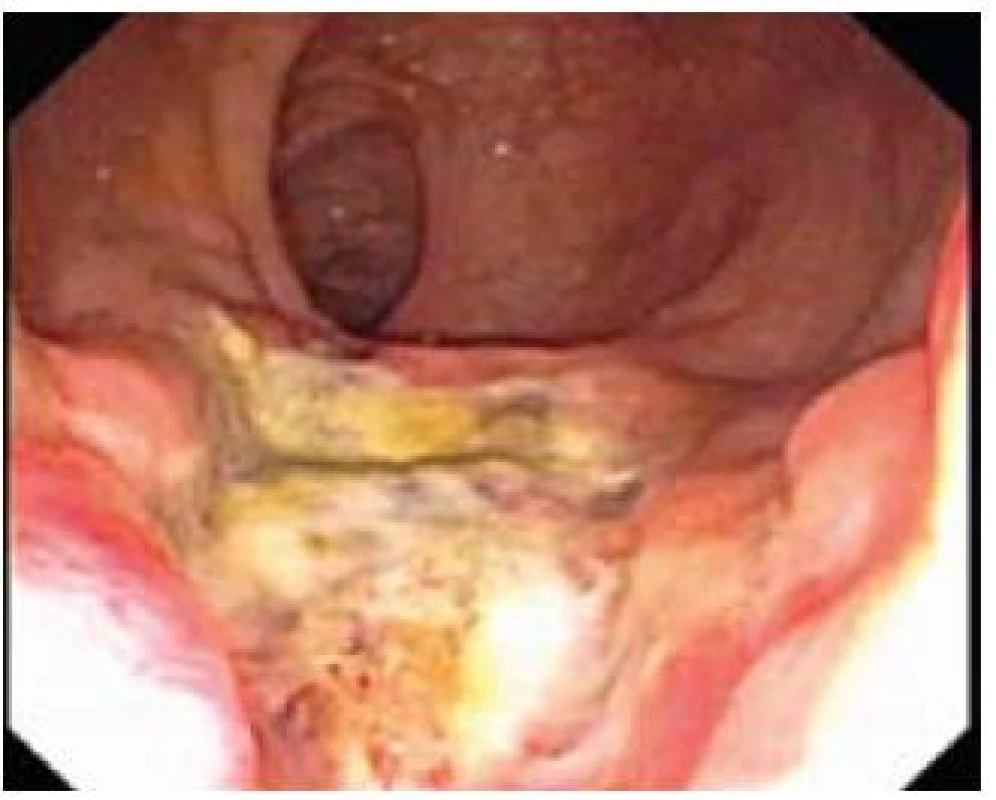
Obr. 4. Hyperplastická elongovaná krypta. Fig. 4. Hyperplastic and prolonged crypt of Lieberkühn. 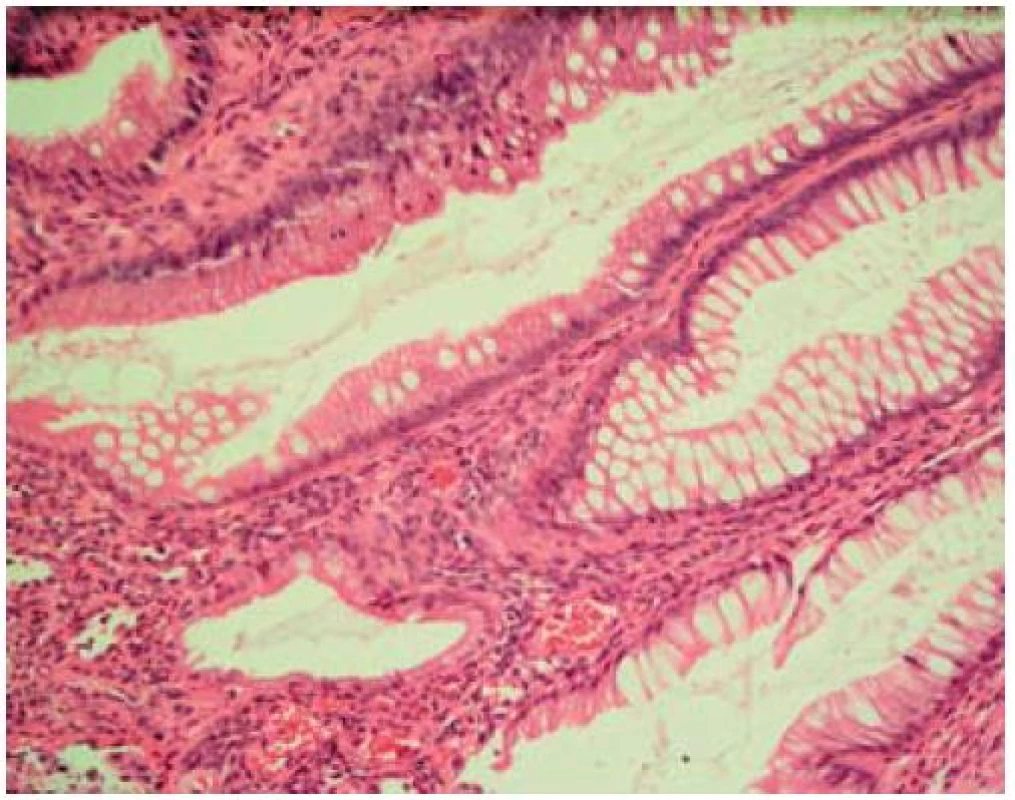
Obr. 5. Fibromusculární obliterace. Fig. 5. Fibro-muscular mucosal obliteration. 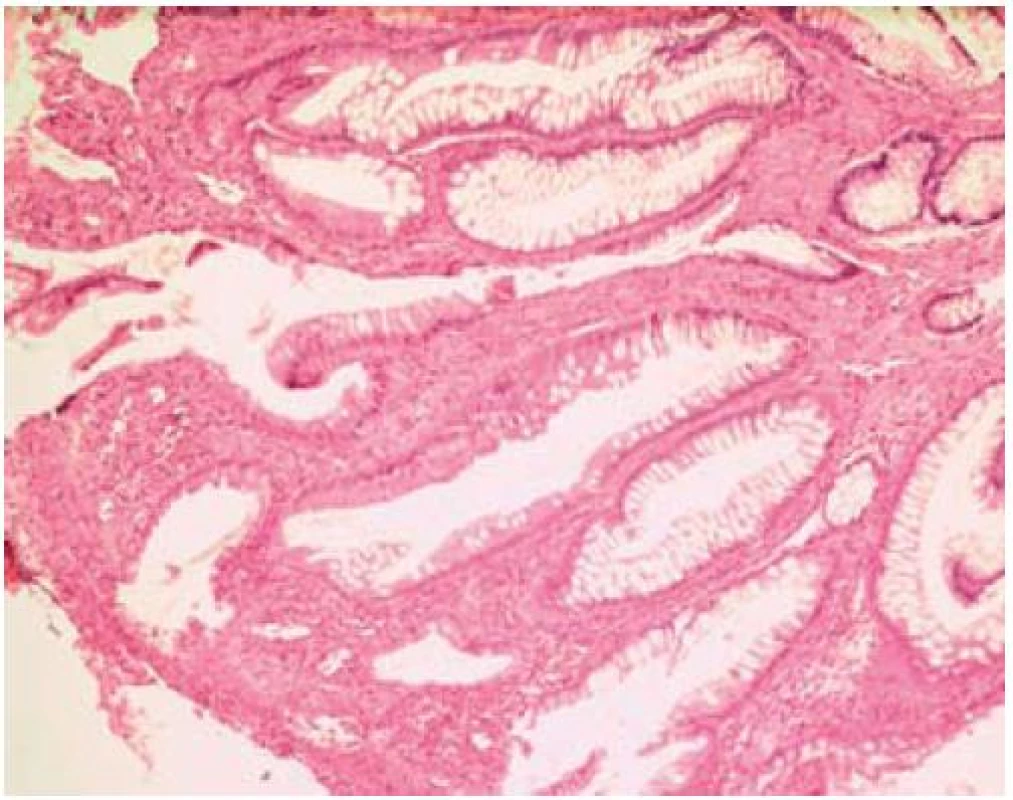
Klinika
SRUS se nejčastěji projevuje hematochezií a defekací hlenu, tzv. mucorrheou. Další uváděné projevy jako je pocit neúplného vyprázdnění, tenesmy, namáhavá defekace či proktalgie, jsou spíše projevy okultního rektálního prolapsu/intususcepce. Pacient s overtním rektálním prolapsem i přes obtížnou defekaci a zácpu může být paradoxně inkontinentní. Je zajímavé, že velká část pacientů bývá asymptomatická a rektální léze jsou zjištěny incidentálně.
Diagnostika
Endoskopický obraz
Jak již bylo zmíněno, endoskopický obraz SRUS je velmi rozmanitý a může se i v čase měnit. Někdy velmi nenápadná erytematozní forma často přechází ve výraznější formu polypoidní. To, zda je nejznámější ulcerózní forma SRUS přirozenou progresí dvou předchozích forem nebo vzniká de novo, je otázkou. Ulcerózní léze se typicky nachází na přední stěně rekta, a to do 12 cm od anokutáního přechodu a má velikost mezi 0,5 a 4 cm. Uložení polypoidní formy je méně typické. Erytematózní forma často postihuje mapovitě celý rektální obvod. Nejčastější variantou je forma ulcerózní, následovaná formou polypoidní a nejméně častá je forma erytematózní [8]. Lze spekulovat, že poměr jednotlivých forem, spíše než jejich skutečnou prevalenci, reflektuje spektrum pacientů se SURS vyhledávajících lékařskou péči.
Histologie
Histologický obraz je velmi podobný pro všechny formy SRUS. Nejtypičtějším bioptickým nálezem je obliterace lamina propria mucosae vlákny hladkého svalu, fibroblasty a kolagenem. Tuto tzv. fibromuskulární obliteraci však také nacházíme i u dalších chorobných jednotek patřících k syndromu slizničního prolapsu. Velmi často popisovanými nálezy jsou hyperplazie epitelu vedoucí k elongaci krypt a chudá chronická celulizace. Některými patology pak bývají popisované i atypické diamantovité krypty. V biopsii z okrajů vředu pak můžeme najít v submukóze ektopické ostrůvky mukózy, někdy cysticky dilatované a s retencí hlenu. Tento obraz může být milně interpretován jako obraz adenokarcinomu [1]. V případě resekátu nacházíme zesílení muscularis propria na podkladě její hypertrofie, a to nejvíce ve vnitřní cirkulární vrstvě. Velmi zajímavé je i oddělení této cirkulární vrstvy od vrstvy longitudinální připomínající vnitřní anální svěrač [9]. Nabízí se, že toto může být zóna vyššího rektálního tlaku hrající roli v patogenezi SRUS.
Obr. 6. Defekografické vyšetření rektoanální intususcepce, enterokéla. Fig. 6. Defecography of rectoanal intussusception, enterocele. 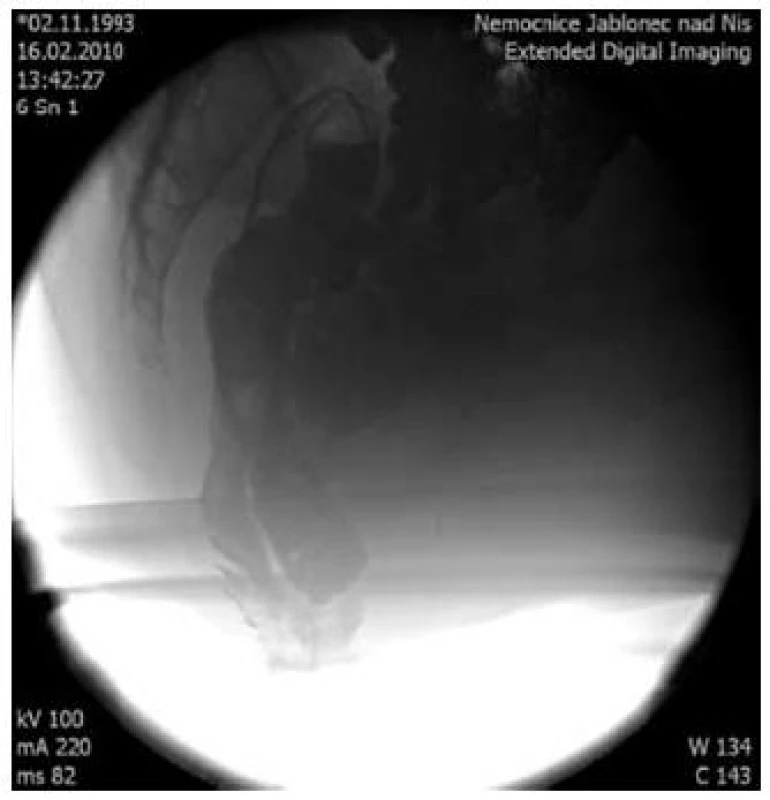
Obr. 7. Defekografické vyšetření – overtní rektální prolaps. Fig. 7. Defecography – overt rectal prolapse. 
Defekografie
Dynamická rentgenová, nověji magnetická rezonanční defekografie jsou metody, které mají nezastupitelnou roli v posouzení anatomie malé pánve u pacientů s problematickou defekací. Vzhledem k asociaci SRUS a obtížné defekaci jsou obě tyto metody používány pro potvrzení diagnózy SRUS a zvláště významná jsou pro plánování terapie SRUS. Na defekogramu u pacientů se SRUS nacházíme nejčastěji okultní rektální prolaps neboli intususcepci, někdy overtní rektální prolaps a někdy prodlouženou defekaci nebo její neúplnost. Intususcepce se u pacientů se SRUS liší od intususcepce, kterou lze nalézt u zdravých dobrovolníků. U zdravých dobrovolníků má intususcepce anální směr a nenarušuje rychlost a kompletnost vyprázdnění. U pacientů se SRUS má intususcepce rektální, tj. opačný směr, a může být příčinou obstrukce lumen. Druhým zásadním rozdílem je šíře prolabující řasy, která má u zdravých pacientů do 3 mm, a jedná se tudíž pouze o prolabující sliznici. U pacientů se SRUS je prolabující řasa širší v důsledku prolapsu celé rektální stěny. Existuje i skupina pacientů se SRUS, kde není na defekogramu rektální prolaps patrný, a zjišťujeme pouze prodlouženou či neúplnou defekaci. Jedná se o pacienty s pelvianální dysynergií. Je otázkou, jakým mechanizmem vzniká SRUS u této skupiny pacientů [10].
Endoskopická ultrasonografie (EUS)
EUS je metodou spíše doplňkovou, výjimečně sloužící k potvrzení diagnózy. U pacientů se SRUS zjišťujeme oproti zdravým pacientům rozšíření stěny rekta, a to hlavně díky rozšíření muscularis propria. U části pacientů pak nalézáme i rozšíření sliznice [11]. EUS může být použita i k potvrzení pelvianální dysynergie, tj. nerelaxující puborektální kličky.
Anorektální manometrie
Tato funkční vyšetřovací metoda má doplňující význam ve zhodnocení přítomnosti pelvianální dysynergie.
Diferenciální diagnostika
Vzhledem k vážnosti prognózy je nutné na prvním místě u ulcerózní a polypoidní formy vyloučit malignitu nebo neoplastický polyp. Velmi častá je záměna ulcerózní a erytematozní formy SRUS s Crohnovou chorobu, resp. ulcerózní kolitidou. Nutné je i odlišení infekčních příčin proktitid, amébové, chlamydiové či syfylitické. U neulcerózních forem SRUS nesmíme v diferenciální diagnostice opominout endometriózu.
Terapie
Přístup k pacientovi se SURS záleží především na tíži jeho příznaků. Vzhledem k minimálnímu počtu kontrolovaných studií není efekt jednotlivých terapeutických modalit zcela jasný a neexistují jasná doporučení. Vždy začínáme konzervativní léčbou a až po jejím selhání saháme k léčbě endoskopické a ve finále k léčbě chirurgické.
Konzervativní léčba
Vzhledem k těsné vazbě SRUS na problematické vyprazdňování je základem léčby navýšení dietní vlákniny nebo přímé užití objemových projímadel, jako je např. psyllium [12]. Většinou se tato terapie kombinuje s behaviorální terapií, tzv. biofeedbackem. Biofeedback ovlivňuje vyprazdňování dvojím způsobem. Jednak psychologicky snížením počtu návštěv na toaletě, času stráveného na toaletě, námahy při defekaci, frekvenci užívání laxativ a snížením nutnosti indigace. Za druhé působí na fyziologii defekace úpravou koordinace pánevního dna a svěračů a zlepšuje slizniční prokrvení rekta. Jarett ve své práci dokládá subjektivní zlepšení u 2/3 pacientů se SRUS, přičemž u třetiny došlo k vyhojení rektálního vředu [5]. Krátkodobému i dlouhodobému efektu biofeedbacku na pacienty se SRUS se věnuje ve své práci Malouf [13]. V malém souboru 12 pacientu polovina pozorovala krátkodobý efekt biofeedbacku. Dlouhodobý efekt pak pozorovala pouze třetina pacientů. Ke zhojení vředu nedošlo u žádného z vyšetřovaných pacientů. Menší terapeutický efekt oproti souboru Jaretta lze vysvětli výběrem pacientů, kdy byli do studie zahrnuti i pacienti po selhání chirurgické léčby. Pokles efektu biofeedbacku s časovým odstupem lze vysvětlit postupným poklesem psychologického efektu této léčby. Dle některých studií lze pozitivní efekt biofeedbacku predikovat na základě anorektální manometrie. Lépe reagují pacienti s nálezem pelvianální dysynergie [14].
Ke konzervativní léčbě patří i lokální léčba 5-ASA, kortikoidy a sukrálfátem. Efekt této léčby je velmi variabilní a není podpořen prospektivními studiemi. Z těchto topických léků se zdá nejefektivnější terapie sukralfátem [15,16].
Endoskopická terapie
K endoskopické léčbě řadíme termoablaci APC a topickou aplikaci fibrinu. APC léčba vede u některých pacientů k zástavě krvácení s možností vyhojení vředů [17]. Většinou je nutné několik sezení. Topická aplikace fibrinu byla popsána na šesti pacientech s promptním zhojením vředů a dlouhodobým efektem [18]. Efekt je vysvětlován stimulací fibroblastů a vaskulární proliferací. Přes popisovaný 100% efekt nejsou další studie, které by se zabývaly účinkem fibrinu v terapii SURS.
Chirurgická léčba
Chirurgická terapie je rezervována pro pacienty nereagující na konzervativní terapii nebo na případnou terapii endoskopickou. Pacienty se solitárním vředem či fokální polypoidní lézí je možno léčit transanální excizí za pomocí operačního rektoskopu (TEM). Pro pacienty s overtním rektálním prolapsem je metodou volby rektopexe bez přední resekce nebo v kombinací s ní. Alternativou pro starší či polymorbidní pacienty je mukózní resekce podle Delorma nebo perineální proktektomie podle Altemeiera. U pacientů s intususcepcí lze volit mezi rektopexí a staplerovou transanální rektální resekcí (STARR). STARR je efektivní metodou v terapii pacientů se SRUS a intususcepcí i v dlouhodobém horizontu, a to s minimální morbiditou [14].
Tab. 1. Klinická symptomatologie u 11 pacientů. Tab. 1. Clinical symptomatology in 11 patients. 
Tab. 2. Endoskopický obraz SURS u 13 pacientů. Tab. 2. Endoscopic findings in 13 patients with SRUS. 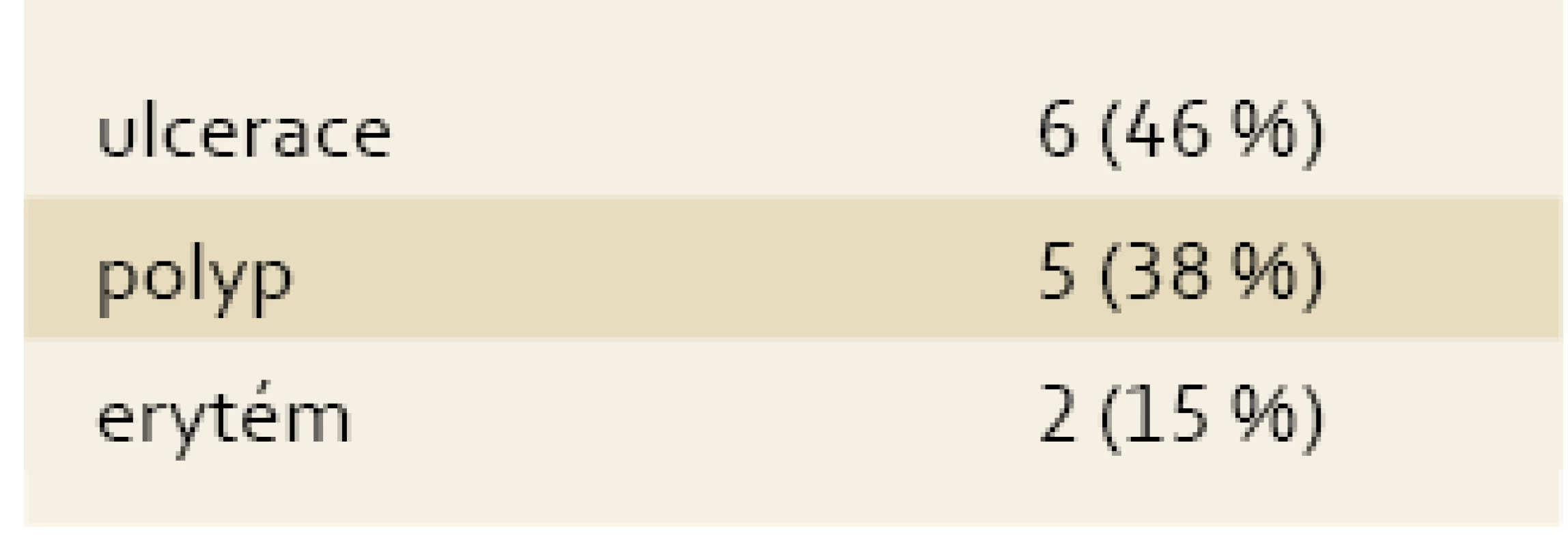
Tab. 3. Histopatologické nálezy 11 pacientů se SRUS. Tab. 3. Histopathological findings in 11 patients with SRUS. 
Tab. 4. Defekografické nálezy u 13 pacientů se SRUS. Tab. 4. Defecographic findings in 13 patients with SRUS. 
Tab. 5. Terapeutické výsledky u 11 pacientů se SRUS. Tab. 5. Therapeutic results in 11 patients with SRUS. 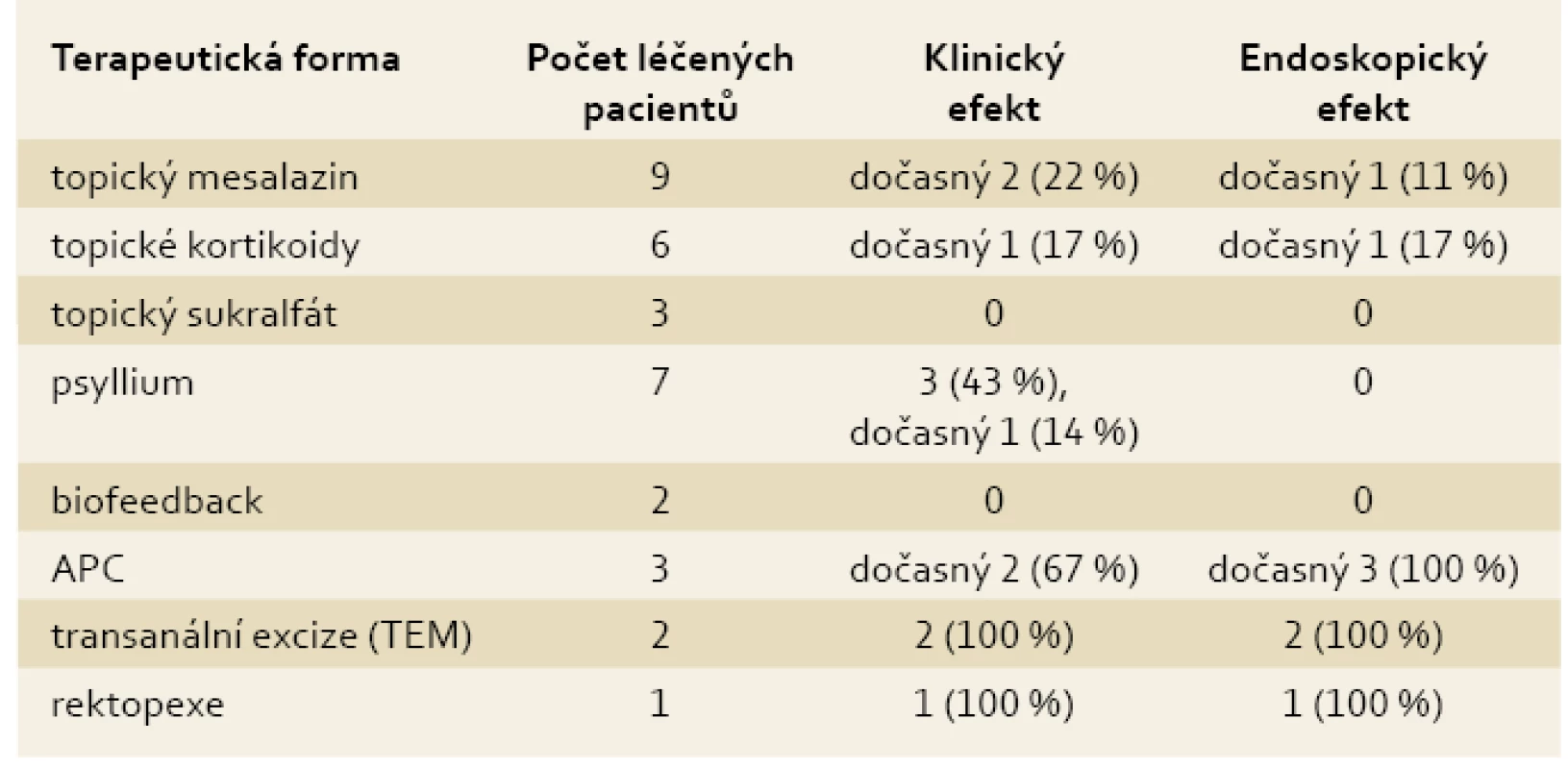
Vlastní zkušenosti
Náš soubor čítá celkem 13 pacientů diagnostikovaných 2008–2011. Průměrný věk pacientů byl 47 let s nejmladším 17letým pacientem a nejstarší 69letou pacientkou. Žen bylo v našem souboru výrazně více, a to deset oproti třem mužům. Nejčastějším klinickým projevem přivádějícím pacienta k lékaři bylo krvácení po stolici (tab. 1). Při endoskopickém vyšetření byla zjištěna ulcerózní forma u šesti pacientů a u třech z nich byly vředy četné. Ulcerace byly u pěti pacientů uloženy dominantně na přední stěně a u jednoho pacienta byla ulcerace uložena na stěně zadní. Polypoidní forma byla zjištěna u pěti pacientů a u zbývajících dvou pacientů šlo o formu erytematózní. Stranová predilekce těchto dvou forem byla oproti ulcerózní formě mnohem méně vyhraněná. Zvláště erytematózní forma byla pak spíše difuzní. V histopatologii byla srovnatelně popisována fibromuskulární obliterace lamina propria mucosae a hyperplastická elongace krypt, méně pak specifické diamantovité krypty. Na dynamické defekografii byla nejčastějším obrazem intususcepce, častěji vyšší rektorektální a méně často nižší rektoanální. Overtní rektální prolaps byl zjištěn u dvou pacientek.
V terapii jsme vyzkoušeli všechny popisované modality vyjma topické aplikace fibrinu. Procentuálně nejefektivnější byla chirurgická léčba. Dva pacienti s fokální polypoidní lézí byli úspěšně léčeni transanální excizí s pomocí operačního rektoskopu (TEM). Jedna pacientka podstoupila ventrální rektopexi s výborným efektem. Trvalý klinický účinek pak měla ještě léčba psylliem u dvou pacientek s erytematozní formou a u jedné s ulcerózní formou SURS. Velmi dobrý, ale pouze dočasný klinický a endoskopický účinek měla léčba argon plazmakoagulací (APC). Jednalo se o pacienty s polypoidní a erytematozní formou, ale všichni absolvovali pouze jedno léčebné sezení. Překvapivě nulový klinický i endoskopický efekt byl pozorován u léčby biofeedbackem a topické léčby sukralfátem. Je nutno podotknout, že léčba biofeedbackem nebyla standardizována. Sukralfát byl podáván v doporučované dávce 2 mg 2× denně [15], ale pouze krátkodobě. Dočasný efekt byl ještě patrný u dvou pacientek léčených topickým mesalazinem a u jednoho pacienta léčeného topickým budesonidem.
Závěr
SRUS je chronická benigní choroba postihující rektum pacientů středního věku s problematickou defekací. Diagnostika SRUS je ve většině případů možná na základě subjektivních obtíží a endoskopického obrazu. V případě diagnostických rozpaků pak diagnózu potvrdí biopsie zhodnocená patologem obeznámeným s histologickým obrazem této nosologické jednotky. Pro toto hovoří i naše zkušenosti. V plánování chirurgické léčby má nezastupitelnou úlohu dynamická defekografie. Anorektální manometrie může naopak predikovat efekt behaviorální terapie biofeedbackem. Pozitivním prognostickým faktorem pro její účinnost je přítomnost pelvianální dysynergie. Nicméně i při absenci pelvianální dysynergie je vzhledem k patofyziologii choroby biofeedback, nejlépe v kombinaci s psylliem, na prvním místě terapeutického algoritmu. Přes nízkou efektivitu je v rámci konzervativní terapie možná i zkouška s topickým mesalazinem, kortikoidy či sukralfátem. Klinickou neefektivnost biofeedbacku v našem souboru, oproti literárním údajům, je nutno brát kriticky vzhledem k nestandardizovanému postupu pouze na dvou pacientech. V případě selhání konzervativní léčby je možné zkusit endoskopickou APC léčbu. Vhodné jsou krvácející ulcerózní či polypoidní léze. K jejímu efektu je nutné více sezení. V případě selhání endoskopické léčby nebo její alternativou je excize ohraničené rektální léze operačním rektoskopem. Symptomatické SRUS pacienty s intususcepcí můžeme řešit méně invazivní staplerovou transanální resekcí rekta (STARR) nebo invazivnější rektopexí. U overtního rektálního prolapsu je pro větší efekt metodou volby rectopexe. Perineální přístup (sec Delorme nebo Altemaier) pak volíme u méně zdatných pacientů [8].
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
Doručeno: 1. 6. 2012
Přijato: 26. 7. 2012
MUDr. Robert Procházka
Oddělení gastroenterologie Nemocnice Jablonec nad Nisou, p.o.
Nemocniční 15
466 60 Jablonec nad Nisou
prochazka@nemjbc.cz
Zdroje
1. Madigan MR, Morson BC. Solitary ulcer of the rectum. Gut 1969; 10(11): 871–881.
2. Martin CJ, Parks TG, Biggart JD. Solitary rectal ulcer syndrom in Northern Ireland, 1971–1980. Br J Surg 1981; 68(10): 744–757.
3. Clair Eh Du Boulay, Fairbrother J, Isaacson PK. Mucosal prolaps syndrome – a unifying concept for solitary ulcer syndrom and related disorders, J Clin Pathol 1983; 36(11): 1264–1268.
4. Emmanuel AV, Kamm MA. Response to a behavioural treatment, biofeedback, in constipated patients is associated with improved gut transit and autonomic innervation. Gut 2001; 49(2): 214–219.
5. Jarrett MED, Emmanuel AV, Vaizey CJ et al. Behavioural therapy (biofeedback) for solitary rectal ulcer syndrom improves symptoms a mucosal blood flow. Gut 2004; 53(3): 368–370.
6. Lonsdale RN. Microvascular abnormalities in the mucosal prolapse syndrom. Gut 1993; 34(1): 106–109.
7. Womack NR, Williams NS, Holmfield JHM et al. Pressure and prolaps-the cause of solitary rectal ulceration. Gut 1987; 28(10): 1228–1233.
8. Sharara AI, Azar C, Amr SS et al. Solitary rectal ulcer syndrome: endoscopic spectrum and review of the literature. Gastrointest Endosc 2005; 62(5): 755–762.
9. Kang YS, Kamm MA, Engel AF et al. Pathology of the rectal wall in solitary rectal ulcer syndrom and complete rectal prolaps, Gut 1996; 38(4): 587–590.
10. Halligan S, Nicholls RJ, Bartram CI. Evacuation Proctography in Patiens with Solitary Rectal Ulcer Syndrom. Am J Roentgenol 1995; 164(1): 91–95.
11. Van Outryve MJV, Pelckmans PA, Fierens H et al. Transrectal ultrasound study of the pathogenesis of solitary rectal ulcer syndrome. Gut 1993; 34(10): 1422–1426.
12. van den Brandt-Grädel V, Huibregtse K, Tytgat GNJ. Treatment of solitary rectal ulcer syndrome with high-fiber diet and abstention of straining at defecation. Dig Dis Sci 1984; 29(11): 1005–1008.
13. Malouf AJ, Vaizey CJ, Kamm MA. Results of Behavioral Treatment (Biofeedback) for Solitary Rectal Ulcer Syndrom. Dis Colon Rectum 2001; 44(1): 72–76.
14. Boccasanta P, Ventura M, Calabro G et al. Stapled Transanal Rectal Resection in Solitary Rectal. Dis Colon Rectum 2008; 51(3): 348–354.
15. Zargar SA, Khuroo MS, Mahajan R. Sucralfate retention enemas in solitary rectal ulcer. Dis Colon Rectum 1991; 34(6): 455–457.
16. Kochhar R, Mehta SK, Aggarwal R et al. Sucralfate enema in ulcerative rectosigmoid lesions. Dis Colon Rectum 1990; 33(1): 49–51.
17. Somani SK, Ghosh A, Avasthi G et al. Healing of solitary rectal ulcers with multiple sessions of argon plasma coagulation. Dig Endosc 2010; 22(2): 107–111.
18. Ederle A, Bulighin G, Orlandi PG et al. Endoscopic application of human fibrin sealant in the treatment of solitary rectal ulcer syndrome. Endoscopy 1992; 24(8): 736–737.
19. Simsek A, Yagci G, Gorgulu S et al. Diagnostic Features and Treatment Modalities in Solitary Rectal Ulcer Syndrome, Acta Chir Belg 2004; 104(1): 92–96.
20. Abid S, Khawaja A, Bhimani SA et al. The clinical, endoscopic and histological spectrum of the solitary rectal ulcer syndrome: a single-center experience of 116 cases. BMC Gastroenterol 2012; 12(1): 72.
21. Stoppino V, Cuomo R, Tonti P et al. Argon plasma coagulation of hemorrhagic solitary rectal ulcer syndrome, J Clin Gastroenterol 2003; 37(5): 392–394.
22. Chong VH, Jalihal A. Solitary rectal ulcer syndrom: characteristic, outcomes and predictive profiles for persistent bleeding per rectum. Singapore Med J 2006; 42(12): 1063–1068.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2012 Číslo 4- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Riziko rozvoje závažné infekce po císařském řezu lze snížit provedením antiseptického výplachu vaginy
- Spolehlivý systém skórování jizev k hodnocení fotografií popálenin
- Nedostatečné dávkování enoxaparinu je u pacientů po ortopedickém výkonu časté a zvyšuje riziko tromboembolické nemoci
- Spasmolytický účinek metamizolu
-
Všechny články tohoto čísla
- Zácpa na okraji?
- Zácpa a přežívající mýty. Laxativa
- Neobvyklá příčina anémie a střevní obstrukce u mladého pacienta
- Zácpa a hypofunkce štítné žlázy. Mýtus nebo skutečnost?
- Syndrom solitárního rektálního vředu
- Defekografie
- Radioizotopové vyšetření segmentální pasáže tlustým střevem pomocí 67Ga-citrátu
- Úspěšná léčba pacientky s obstrukčním defekačním syndromem
- Mezenteriálna fibromatóza ako príčina náhlej príhody brušnej
- Doporučený postup pro diagnostiku a léčbu anémie u IBD
-
Dlouhodobé výsledky terapie infliximabem u pacientů s ulcerózní kolitidou
Pokračování studií ACT-1 a ACT-2 - Flexibilní ezofagogastroskopie – jakých nálezů si má všímat gastroenterolog v hypofaryngu a hrtanu?
- Endoskopická polypektomie – jak dosáhnout standardu kvality v roce 2012?
- Liečba spontánnej baktériovej peritonitídy
-
Kvalita života je důležitým faktorem indikační rozvahy u nemocných s karcinomem pankreatu
Multicentrická prospektivní studie - Nová sekce Diskuzní fórum
- Vleklé dyspepsie: co a jak v běžné praxi
- Správná odpověď na kvíz
- 44th congress of the European Pancreatic Club (EPC) and PROMED symposium in 2012
- Dulcolax® čípky
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Defekografie
- Zácpa a hypofunkce štítné žlázy. Mýtus nebo skutečnost?
- Syndrom solitárního rektálního vředu
- Liečba spontánnej baktériovej peritonitídy
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



