-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Rotorův syndrom podmiňuje porucha jaterního vychytávání konjugovaného bilirubinu
Autoři: M. Jirsa 1; S. Kmoch 2
Působiště autorů: Centrum experimentální medicíny IKEM, Praha 1; Ústav dědičných metabolických poruch VFN a 1. LF UK v Praze 2
Vyšlo v časopise: Gastroent Hepatol 2012; 66(2): 99-100
Kategorie: Hepatologie: komentář
Komentář ke studii: van de Steeg E, Stránecký V, Hartmannová H et al. Complete OATP1B1 and OATP1B3 deficiency causes human Rotor syndrome by interrupting conjugated bilirubin reuptake into the liver. J Clin Invest 2012; 122(2): 519–528.Commentary on the study: van de Steeg E, Stránecký V, Hartmannová H et al. Complete OATP1B1 and OATP1B3 deficiency causes human Rotor syndrome by interrupting conjugated bilirubin reuptake into the liver. J Clin Invest 2012; 122(2): 519–528.
Předmětem práce jsou nizozemská experimentální a česká genetická studie, které paralelně a nezávisle vyústily v odhalení molekulární podstaty a mechanizmu žloutenky Rotorova typu.
Bilirubin jakožto koncový produkt degradace hemu je detoxikován konjugací s kyselinou glukuronovou a poté vyloučen do žluče. Donedávna se mělo za to, že konjugace bilirubinu probíhá pouze v játrech a veškerý konjugovaný bilirubin je vylučován do žluče prostřednictvím kanalikulárního transportéru pro multivalentní organické anionty MRP2. Teprve při blokádě odtoku žluče, a to na kterékoli úrovni, dochází v sinusoidální membráně hepatocytů ke zvýšení exprese proteinu MRP3, strukturou i funkcí blízkého MRP2, a k následnému přesměrování sekrece konjugovaného bilirubinu do krve. K tomu se může přidružit regurgitace konjugovaného bilirubinu z poškozených žlučových cest. Konjugovaná složka parenchymové žloutenky při onemocnění jater byla přičítána neschopnosti hepatocytů vylučovat konjugovaný bilirubin do žluče.
Zatímco mechanizmus jaterní konjugace a sekrece konjugovaného bilirubinu do žluče byl již v 90. letech objasněn studiem Crigler-Najjarova a Gilbertova syndromu vyvolaném úplným, resp. částečným deficitem UDP bilirubin glukuronosyltransferázy a Dubin-Johnsonova syndromu podmíněného deficitem MRP2, podstata a mechanizmus Rotorova syndromu (autozomálně recesivně dědičná žloutenka charakterizovaná konjugovanou hyperbilirubinemií, absencí jaterního vychytávání aniontových diagnostických barviv i radiofarmak a porfyrinurií) zůstával nevysvětlen.
V publikované práci jsme kombinací genového mapování provedeného v pěti rodinách s výskytem Rotorova syndromu a mutační analýzy kandidátních genů v lokusu 12p12 u jedenácti probandů z celkem osmi rodin ukázali, že molekulární podstatu Rotorova syndromu tvoří současně přítomné mutace v obou alelách dvojice homologních genů SLCO1A1 a SLCO1B3, jejichž důsledkem je současné a úplné chybění proteinů OATP1B1 a OATP1B3 (Organic Anion Transporting Polypeptides). Tyto známé proteiny odpovídají za vychytávání a transport přes cévní pól hepatocytů, a tudíž i za clearance a detoxikaci řady látek, např. konjugovaného i nekonjugovaného bilirubinu, nekonjugovaných žlučových kyselin, porfyrinů, steroidních hormonů, hormonů štítné žlázy, radiofarmak i běžně užívaných léků, jako jsou penicilinová antibiotika, statiny, rifampicin či metotrexát. Polymorfizmy v SLCO1B1 a SLCO1B3 byly již před naším objevem asociovány s nežádoucími účinky, popř. toxicitou některých léků.
V experimentech s myšími kmeny deficitními pro Oatp1a/1b a multispecifický sinusoidální exportér Mrp3 dokázali naši nizozemští partneři z Nederlands Kanker Instituut a Academisch Medich Centrum v Amsterodamu, že Mrp3 zprostředkovává sekreci konjugátů bilirubinu do krve, zatímco Oatp1a/1b odpovídají za jejich zpětné vychytávání v jaterních buňkách. Transgenní exprese lidského OATP1B1 nebo OATP1B3 u „rotorovských“ Oatp1a/1b-/ - myší vedla k obnovení chybějící funkce a k potlačení žloutenky. To ukazuje, že lidské proteiny OATP1B1 a OATP1B3 tvoří spolu s ABCC3 sekrečně resorpční smyčku sestávající z vylučování konjugovaného bilirubinu do krve periportálními hepatocyty a jeho následným vychytáním v centrální zóně jaterních lalůčků. Tato smyčka vyznačená na obr. 1 červenými šipkami zvyšuje detoxikační a sekreční kapacitu jater pro endogenní látky, xenobiotika a jejich konjugáty přiváděné do jater z portálního řečiště a brání přetížení jaterních buněk v periportální zóně. Jaterní vychytáváni konjugovaného bilirubinu dále slouží k odstranění bilirubinu konjugovaného mimo játra, např. ve střevě (obr. 1). Molekulární mechanizmus Rotorova syndromu vyvolaného deficitem obou transportérů OATP1B1 a OATP1B3 spočívá v přerušení zpětného vychytávání konjugovaného bilirubinu z krve.
Obr. 1. Porucha jaterního vychytávání konjugovaného bilirubinu vyvolaná deficitem OATP1B1 a OATP1B3 je příčinou Rotorova syndromu. Fig. 1. Impaired liver uptake of conjugated bilirubin caused by OATP1B1 and OATP1B3 deficiency is the molecular basis of Rotor syndrome. 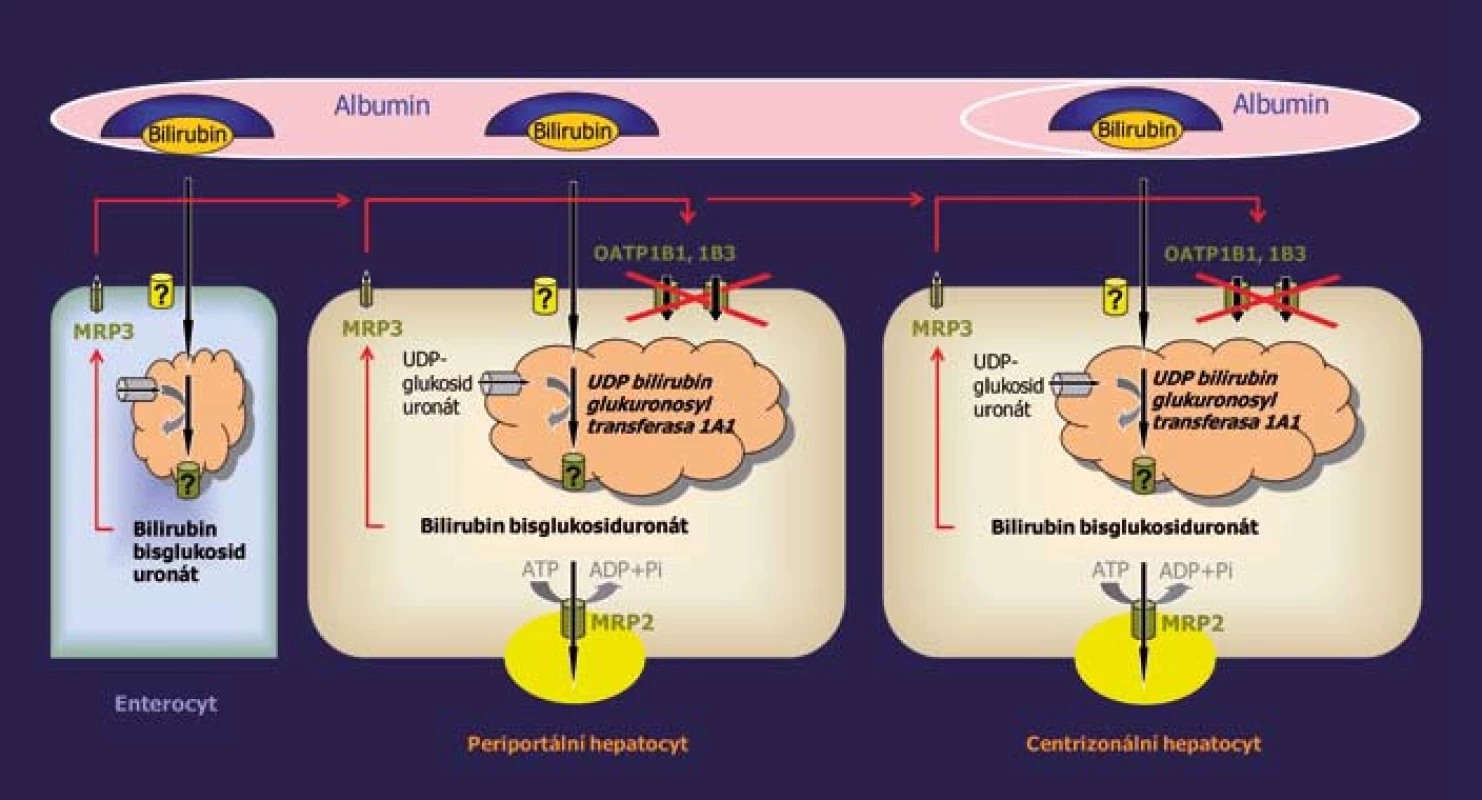
Uvedené poznatky v kombinaci s popisovaným snížením exprese „rotorovských“ proteinů u parenchymových a cholestatických nemocí jater naznačují, že porucha jaterního vychytávání konjugovaného bilirubinu se nejspíš podílí i na mechanizmu konjugované hyperbilirubinemie u těchto chorob. Bezprostředním praktickým výstupem práce je možnost potvrdit diagnózu Rotorova syndromu na molekulární úrovni genetickým vyšetřením doplněným imunohistologickým vyšetřením exprese „rotorovských“ proteinů v archivních vzorcích jaterních biopsií.
Zásadní význam má práce pro farmakogenetiku, neboť v literatuře udávaný výskyt nosičství závažných mutací v alespoň jedné alele některého z genů SLCO1B1 a SLCO1B3 odhadovaný na 1 : 100–1 : 1000 je podstatně vyšší než výskyt extrémně vzácného Rotorova syndromu vyžadujícího současnou přítomnost mutací v obou alelách obou „rotorovských“ genů (odhadovaná frekvence pod 1 : 106). Je příznačné, že zatímco české grantové agentury naše žádosti o podporu mapovacího projektu zamítly s odkazem na okrajový a čistě teoretický medicínský význam studia raritní metabolické odchylky, nizozemské grantové agentury a farmaceutická společnost GlaxoSmithKline vývoj myšího modelu Rotorova syndromu a experimentální studium jeho molekulárního mechanizmu podpořily několika granty.
doc. MUDr. Mgr. Milan Jirsa, CSc.
Centrum experimentální medicíny IKEM
Vídeňská 1958/9
140 21 Praha 4
milan.jirsa@ikem.cz
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek Dobré zprávyČlánek Správná odpověď na kvíz
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2012 Číslo 2- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Itoprid v léčbě funkční dyspepsie
- Farmakokinetika a tolerance pantoprazolu v dětském věku
- Vliv podávání prokinetik na riziko syndromu bakteriálního přerůstání u pacientů užívajících inhibitory protonové pumpy
-
Všechny články tohoto čísla
- Hepatorenálny syndróm u pacientov s akútnou alkoholovou hepatitídou
- Správná odpověď na kvíz
- Graft vs host disease jako neobvyklá komplikace po transplantaci jater
- Liečba achalázie – súčasný prístup a vlastné skúsenosti
- Analýza těkavých plynů ve vydechovaném vzduchu u nemocných s idiopatickými střevními záněty
- Súčasný prístup k anémii u pacientov s nešpecifickými črevnými zápalmi
- Mezinárodní konsenzus ke sledování aktivity nemoci u pacientů s Crohnovou chorobou: Výsledky projektu IBD AHEAD 2011
- XVIst Hradec days of gastroenterology and hepatology
- Prof. Jiří Nevoral on the occasion of his 70th birthday
- 20 let členem výboru České gastroenterologické společnosti (ČGS)
- Esomeprazol – první inhibitor protonové pumpy „druhé“ generace
- Dobré zprávy
- Doporučený postup pro léčbu a diagnostiku hepatocelulárního karcinomu
- Histopatologická diagnóza hepatocelulárního karcinomu
- Nález v distálnom duodene, ktorý by nemal prekvapiť
- Rotorův syndrom podmiňuje porucha jaterního vychytávání konjugovaného bilirubinu
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Hepatorenálny syndróm u pacientov s akútnou alkoholovou hepatitídou
- Súčasný prístup k anémii u pacientov s nešpecifickými črevnými zápalmi
- Liečba achalázie – súčasný prístup a vlastné skúsenosti
- Prof. Jiří Nevoral on the occasion of his 70th birthday
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



