-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Účinnost a bezpečnost vildagliptinu jako léku druhé volby ve srovnání s jinými perorálními antidiabetiky u pacientů s diabetes mellitus 2. typu: české výsledky v rámci celosvětové prospektivní kohortové studie EDGE
Efficacy and safety of vildagliptin as a second-line therapy vs other oral antidiabetic agents in patients with type 2 diabetes: Czech results within the worldwide prospective cohort EDGE study
Introduction:
Metformin monotherapy is recommended as initial treatment of type 2 diabetes. The selection of optimal second-line therapy that is often necessary due to the progressive nature of the disease is still a subject of ongoing discussions.Aim of the study:
The aim of the international EDGE (Effectiveness of Diabetes control with vildaGliptin and vildagliptin/mEtformin) study was to prospectively compare the efficacy and safety of vildagliptin vs other oral antidiabetic agents in patients with type 2 diabetes not adequately controlled on monotherapy in a real-life clinical setting. In this paper, we present the data of patients participating in the EDGE study in the Czech Republic.Material and methods:
Patients with type 2 diabetes not adequately controlled on monotherapy were enrolled into the study, and randomised into either the vildagliptin arm or control arm with another OAD at the discretion of the treating physician. Patients with the addition of other incretin-based medications were not enrolled into the study. The efficiency was evaluated as a proportion of patients reaching the combined endpoint of decreasing HbA1c> 3 mmol/mol without hypoglycaemia, peripheral oedema or treatment termination due to gastrointestinal side effects during the 12 months of treatment.Results:
654 patients were enrolled into the study in the Czech Republic. The mean age of the patients when enrolled into the study (vildagliptin group vs control group) was 59.5 ± 10.6 vs 63.7 ± 8.5 years, mean body mass index was 32.4 ± 5.7 vs 31.7 ± 6.5 kg/m2, mean HbA1c was 62 ± 12 vs 64 ± 11 mmol/mol. The probability of reaching the combined primary endpoint (calculated using a binary logistic regression model to calculate the odds ratios with 95% confidence intervals) was higher for vildagliptin regardless of baseline HbA1c or type of medication added in the control group. Primary endpoint was reached by 60.6 % of patients in the vildagliptin group vs 51.3 % of patients in the control group, odds ratio 1.46 (1.06, 1.99); p< 0.019. The proportion of patients reaching secondary endpoint (HbA1c< 54 mmol/mol without hypoglycemic event or weight gain ≥ 3 % with baseline glycated hemoglobin > 54 mmol/mol was higher for vildagliptin 45.7 % vs 31.4 % in the control arm, odds ratio 1.84 (1.26, 2.68), p< 0.001. The rate of adverse events was comparable in both groups.Conclusion:
In a real-life clinical setting, the percentage of patients reaching the combined endpoint of decreasing HbA1c> 3 mmol/mol, without hypoglycaemia, peripheral oedema or treatment termination due to gastrointestinal side effects was higher after the addition of vildagliptin as compared to other antidiabetic agents with comparable rate of side effects.Key words:
type 2 diabetes mellitus – vildagliptin – combination therapy
Autoři: M. Haluzík 1
; V. Veselá 2; J. Gerle 3; M. Brada 4; L. Dohnalová 5; T. Edelsberger 6; J. Houdová 7
Působiště autorů: III. interní klinika 1. lékařské fakulty UK a VFN Praha, přednosta prof. MUDr. Štěpán Svačina, DrSc., MBA 1; Novartis s. r. o., Praha, vedoucí pracovník MUDr. Richard Vonka 2; Polymedica Praha, vedoucí pracovník MUDr. Jan Gerle 3; Privátní diabetologická ambulance Břeclav, vedoucí pracovník MUDr. Michal Brada 4; Interní oddělení Nemocnice České Budějovice, přednosta prim. MUDr. Pavel Havránek 5; Privátní diabetologická ambulance Krnov, vedoucí pracovník MUDr. Tomáš Edelsberger 6; Diabetologická ambulance Praha, vedoucí pracovník MUDr. Jana Houdová 7
Vyšlo v časopise: Vnitř Lék 2013; 59(12): 1049-1056
Kategorie: Původní práce
Souhrn
Úvod:
Monoterapie metforminem je doporučenou iniciální léčbou diabetu 2. typu. Výběr optimálního léku druhé volby, jehož přidání je vzhledem k progresi onemocnění postupně nutné, je však stále předmětem intenzivních diskuzí.Cíle studie:
Cílem mezinárodní studie EDGE (Effectiveness of Diabetes control with vildaGliptin and vildagliptin/mEtformin) bylo prospektivně srovnat účinnost a bezpečnost vildagliptinu s jinými antidiabetiky u pacientů s diabetem 2. typu neuspokojivě kompenzovaným monoterapií v podmínkách běžné klinické praxe. V tomto článku prezentujeme výsledky pacientů účastnících se studie v České republice.Materiál a metody:
Pacienti s diabetem 2. typu byli zařazeni do studie v případě neuspokojivé kompenzace na monoterapii a randomizováni buď do skupiny s přidáním vildagliptinu, nebo do kontrolní skupiny s přidáním jiného antidiabetika do dvojkombinace dle rozhodnutí ošetřujícího lékaře. Pacienti, kterým byla přidána jiná inkretinová léčba, nebyli do studie zařazeni. Účinnost léčby byla hodnocena jako procento pacientů dosahujících kombinovaného cíle poklesu glykovaného hemoglobinu > 3 mmol/mol bez výskytu periferního edému, hypoglykemie nebo ukončení léčby z důvodu gastrointestinálních nežádoucích účinků během 12 měsíců léčby.Výsledky:
V rámci České republiky bylo do studie zařazeno 654 pacientů. Průměrný věk pacientů při zařazení do studie (skupina s vildagliptinem vs kontrolní skupina) byl 59,5 ± 10,6 vs 63,7 ± 8,5 roku, průměrný body mass index 32,4 ± 5,7 vs 31,7 ± 6,5 kg/m2, průměrný vstupní glykovaný hemoglobin 62 ± 12 vs 64 ± 11 mmol/mol. Pravděpodobnost dosažení kombinovaného cíle (vypočítaná pomocí binárního logistického regresního modelu jako poměr pravděpodobností po adjustaci na rozdíly v bazálních parametrech s 95% intervaly spolehlivosti (CI)) byla vyšší pro vildagliptin nezávisle na vstupní hodnotě glykovaného hemoglobinu či typu přidaného léku v kontrolní skupině. Ve skupině s přidáním vildagliptinu dosáhlo primárního cíle 60,6 % pacientů ve srovnání s 51,3 % v kontrolní skupině, poměr pravděpodobností (OR) 1,46 (1,06; 1,99); p < 0,019. Podíl pacientů, kteří dosáhli sekundárního kombinovaného cíle definovaného jako pokles glykovaného hemoglobinu pod 54 mmol/mol bez výskytu hypoglykemie nebo váhového přírůstku ≥ 3 % při vstupních hodnotách glykovaného hemoglobinu > 54 mmol/mol, byl vyšší ve skupině s přidáním vildagliptinu, a to 45,7 % oproti 31,4 % v kontrolní skupině, poměr pravděpodobností (OR) 1,84 (1,26; 2,68), p < 0,001. Výskyt nežádoucích účinků byl v obou skupinách srovnatelný.Závěr:
V podmínkách běžné klinické praxe bylo procento pacientů dosahujících kombinovaného cíle (poklesu glykovaného hemoglobinu > 3 mmol/mol bez výskytu periferního edému, hypoglykemie nebo ukončení léčby z důvodu gastrointestinálních nežádoucích účinků) vyšší při přidání vildagliptinu než jiných antidiabetických léků při srovnatelném výskytu nežádoucích účinků.Klíčová slova:
diabetes mellitus 2. typu – vildagliptin – kombinační léčbaÚvod
Výskyt diabetes mellitus 2. typu stoupá ve všech vyspělých zemích světa včetně České republiky [1]. Uspokojivá kompenzace diabetu je z dlouhodobého hlediska zásadní podmínkou snížení výskytu chronických diabetických komplikací, jejichž přítomnost výrazně zvyšuje náklady na léčbu diabetiků a snižuje kvalitu jejich života [2]. Diabetici 2. typu mají několikanásobně zvýšené riziko kardiovaskulární morbidity a mortality a při dlouhodobě neuspokojivé kompenzaci též trpí mikrovaskulárními komplikacemi (diabetickou retinopatií, neuropatií a nefropatií) [3–5].
Prospektivní studie prokázaly, že těsná kompenzace diabetu vede ke snížení jak makro-, tak i mikrovaskulárních komplikací [6]. Zatímco zlepšení kompenzace pozitivně ovlivní incidenci i progresi mikrovaskulárních komplikací jak u pacientů s krátkým, tak i delším trváním diabetu [7], ke snížení makrovaskulárních komplikací je zřejmě nutné dosažení těsné kompenzace co nejdříve po diagnóze [8]. Studie zaměřené na ovlivnění výskytu kardiovaskulárních komplikací těsnou kompenzací diabetu u předtím dlouhodobě neuspokojivě kompenzovaných diabetiků neprokázaly signifikantní snížení výskytu těchto komplikací [9–11]. V jednom případě (studie ACCORD) byla dokonce mortalita překvapivě zvýšena ve skupině s intenzivnější antidiabetickou léčbou a těsnou kompenzací, což mohlo být důsledkem příliš intenzivní léčby zvyšující nadměrně riziko hypoglykemie [11].
Vzhledem k úzké provázanosti diabetu a kardiovaskulárních komplikací je v poslední době intenzivně sledován vliv jednotlivých antidiabetických léků na kardiovaskulární komplikace. Z léků v současné době používaných má prokázaný pozitivní vliv na kardiovaskulární morbiditu a mortalitu pouze metformin a u některých typů komplikací též pioglitazon, zatímco vliv ostatních léků se zdá být spíše neutrální a v některých případech až negativní [12,13]. K negativnímu vlivu na kardiovaskulární komplikace mohou jistě přispívat též nežádoucí účinky antidiabetických léků, zejména zvýšení hmotnosti a výskyt hypoglykemie.
Vildagliptin je představitelem relativně nové skupiny antidiabetik, jejichž mechanizmus účinku je vysvětlován tzv. inkretinovým efektem [14]. Tento lék inhibuje ubikvitérní enzym dipeptidyl peptidázu-4 (DPP-4), a tak zvyšuje hladiny inkretinového hormonu glukagon-like peptidu-1 (GLP-1) [15]. Zvýšení endogenních hladin GLP-1 stimuluje glukózo-dependentní sekreci inzulinu a snižuje hladiny glukagonu, který za normálních okolností hladiny glykemie zvyšuje [16]. Velkou výhodou vildagliptinu a dalších inhibitorů DPP-4 je skutečnost, že jejich podávání nevede ke vzniku hypoglykemie a zvýšení hmotnosti [17–19]. Tyto vlastnosti je odlišují od jiných klasicky používaných antidiabetik včetně derivátů sulfonylurey, glitazonů i inzulinu. Experimentální studie navíc naznačují, že zvýšení hladin GLP-1 by mohlo mít i kardioprotektivní a neuroprotektivní účinky a mohlo by též chránit β buňky pankreatu před apoptózou a zpomalit tak progresi diabetu [20].
Současný algoritmus léčby diabetu 2. typu jednoznačně preferuje metformin jako lék první volby [21]. Progresivní charakter tohoto onemocnění však vede k nutnosti postupné kombinační léčby, přičemž optimální lék druhé volby dosud není jednoznačně stanoven. Vzhledem k výše popsaným komplexním pozitivním účinkům se inhibitory DPP-4 jeví v tomto ohledu jako velmi výhodná možnost s řadou potenciálních výhod oproti v současné době nejčastěji používaným derivátům sulfonylurey.
Dosud není k dispozici dostatek studií zaměřených na srovnání účinnosti a bezpečnosti DPP-4 inhibitorů s jinými perorálními antidiabetiky v podmínkách běžné klinické praxe, které se mohou často dosti lišit od podmínek v rámci klinických studií. Cílem studie EDGE (Effectiveness of Diabetes control with vildaGliptin and vildagliptin/ /mEtformin) bylo prospektivně srovnat účinnost a bezpečnost vildagliptinu s jinými antidiabetiky u pacientů s diabetem 2. typu neuspokojivě kompenzovaným monoterapií v podmínkách běžné klinické praxe. Studie EDGE probíhala celosvětově a bylo do ní zařazeno celkem více než 45 000 pacientů ve 27 zemích světa. V tomto článku prezentujeme výsledky analýzy podskupiny pacientů zařazených do studie EDGE v rámci ČR. Zaměřujeme se jednak na výsledky primárního cíle studie, tedy procento pacientů dosahujících kombinovaného cíle poklesu glykovaného hemoglobinu > 3 mmol/mol bez výskytu periferního edému, hypoglykemie nebo ukončení léčby z důvodu gastrointestinálních nežádoucích účinků. Dále zde prezentujeme a diskutujeme výsledky třetího sekundárního cíle studie, tedy procento pacientů s glykovaným hemoglobinem ≥ 54 mmol/mol na počátku studie, kteří dosáhli glykovaného hemoglobinu < 54 mmol/mol, bez výskytu hypoglykemie nebo vzestupu hmotnosti ≥ 3 % po 12 měsících léčby.
Materiál a metody
Design studie
Studie EDGE byla roční, prospektivní, observační, kohortová studie, do níž bylo zařazeno 45 868 pacientů z 2 957 center ve 27 zemích Evropy, Střední a Latinské Ameriky, Asie a Středního východu. Z těchto pacientů bylo 654 z 39 center zařazeno v ČR. Do studie byli zařazováni dospělí pacienti s diabetem 2. typu (věk > 18 let) neuspokojivě kompenzovaní na monoterapii derivátem sulfonylurey, metforminem, glitazonem (thiazolidindionem), glinidem nebo inhibitorem α-glukozidázy, u kterých bylo ošetřujícím lékařem zvažováno přidání druhého antidiabetika do kombinace. Pacienti, u kterých bylo plánováno přidání jiného DPP-4 inhibitoru než vildagliptinu, případně GLP-1 mimetika, nebo kteří vyžadovali trojkombinaci perorálních antidiabetik, byli ze studie vyloučeni. Podobně nemohli být zařazeni pacienti léčení v době zahájení studie inzulinem a pacienti se známou alergií na některý ze studijních léků či léků z podobné lékové skupiny. Podrobnosti o vstupních a vylučovacích kritériích studie jsou uvedeny v nedávno přijaté publikaci kompletních výsledků studie [22].
Studie byla schválena lokálními etickými komisemi a byla provedena v souladu s pravidly Helsinské deklarace. Všem pacientům byly na počátku podrobně vysvětleny cíle studie a byl jim dán k podpisu informovaný souhlas.
Sledované parametry
Na počátku studie byly zaznamenány demografické charakteristiky pacientů (věk, pohlaví, rasa, výška, etnický původ), hladina kreatininu nutná k výpočtu odhadované glomerulární filtrace (eGFR) dle rovnice MDRD, délka trvání diabetu, přehled antidiabetické léčby užívané před začátkem studie, informace o nově nasazované léčbě při vstupu do studie a výsledek posledního měření glykovaného hemoglobinu. Stejné charakteristiky byly zaznamenány po 12 měsících účasti ve studii spolu s výskytem nežádoucích příhod, závažných nežádoucích příhod a stavem pacienta při ukončení studie. Kontroly mezi zahájením a ukončením studie a případná další vyšetření byla provedena dle indikace ošetřujícího lékaře a potřeb pacienta.
Parametry účinnosti a bezpečnosti
Primární cíl byl definován jako procento pacientů dosahujících kombinovaného endpointu poklesu glykovaného hemoglobinu > 3 mmol/mol bez vzestupu hmotnosti ≥ 5 %, bez výskytu periferního edému, hypoglykemie nebo ukončení léčby z důvodu gastrointestinálních nežádoucích příhod během 12 měsíců léčby. Pacienti, jejichž kategorizace nemohla být provedena z důvodu chybějících dat, nebyli do konečného hodnocení zařazeni. Hlavní analýza primárního cíle byla provedena pouze u pacientů s dodržením protokolu v průběhu celého trvání studie (tzv. per protocol analysis). Hypoglykemie byla definována jako výskyt symptomů hypoglykemie, které pominuly po požití sacharidů.
Sekundární parametry účinnosti
- pokles glykovaného hemoglobinu > 3 mmol/mol bez výskytu periferních otoků, hypoglykemie, vysazení léčby pro gastrointestinální nežádoucí příhody nebo vzestupu hmotnosti ≥ 3 % po 12 měsících léčby;
- pokles glykovaného hemoglobinu > 3 mmol/mol bez výskytu hypoglykemie nebo vzestupu hmotnosti ≥ 3 % po 12 měsících léčby;
- u pacientů s glykovaným hemoglobinem ≥ 54 mmol/mol na počátku studie – glykovaný hemoglobin < 54 mmol/mol výskytu hypoglykemie nebo vzestupu hmotnosti ≥ 3 % po 12 měsících léčby.
Sekundární parametry bezpečnosti
Jedním z cílů studie bylo sledovat bezpečnost vildagliptinu jako přídavné léčby ve srovnání s přidáním jiných typů antidiabetik v reálné klinické praxi a identifikovat případná rizika této léčby. Zvláštní pozornost byla věnována bezpečnosti stran jaterních nežádoucích příhod. Ta byla hodnocena nezávislou komisí expertů (Hepatic Adjudication Committee). Zaměření na jaterní nežádoucí příhody vychází z výsledků iniciálních studií s vildagliptinem, kdy při jeho podávání v dávce 100 mg 1krát denně byly ojediněle zaznamenány případy zvýšení jaterních testů. Při podávání v dávce 50 mg 2krát denně se tyto případy již vyskytovaly ve frekvenci srovnatelné s placebem a ostatními antidiabetiky, jak bylo potvrzeno řadou studií i kombinovaných analýz [23].
Analýza primárních a sekundárních cílů účinnosti a tolerability
Pravděpodobnost dosažení primárních a sekundárních cílů byla analyzována pomocí binárního logistického regresního modelu s výpočtem poměrů pravděpodobnosti (OR) s 95% intervaly spolehlivosti (CI). Jako parametry kovariance byly do modelu zařazeny: bazální glykovaný hemoglobin, BMI, rasa, věk, pohlaví, region, trvání diabetu, antidiabetické léčba a typ pacienta (dle přítomnosti komorbidit). OR vyjadřuje poměr pravděpodobnosti úspěšné léčby ve prospěch vildagliptinu či kombinace vildagliptin/ /metformin oproti pravděpodobnosti úspěšné léčby s kontrolními antidiabetiky. K adjustaci možné nerovnováhy v distribuci parametrů kovariance mezi srovnávanými skupinami bylo použito metodiky propensity score. Provedené statistické testy a analýzy byly předem definovány v protokolu studie.
Výsledky
V rámci ČR bylo do studie zařazeno celkem 654 pacientů (343 do skupiny s přidáním vildagliptinu a 311 do kontrolní skupiny). Studii dokončilo celkem 615 pacientů (324 ve skupině s vildagliptinem a 291 v kontrolní skupině) (obr. 1).
Obr. 1. Pacienti zařazení do studie a počty pacientů, kteří studii nedokončili. 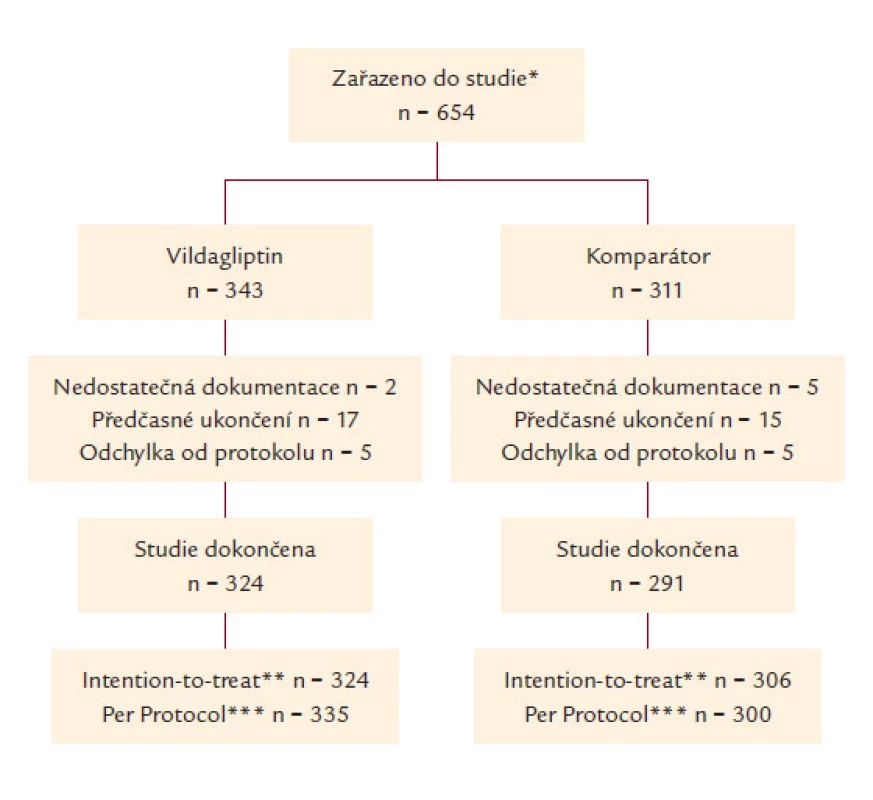
*Všichni pacienti, kteří podepsali informovaný souhlas s účastí ve studii. **Intent-to-treat (ITT) populace – všichni pacienti, kterým byla nasazena nová medikace při vstupu do studie. Centra nebo pacienti s identifikovanými kvalitativními i kvantitativními nedostatky v zadaných datech byli vyloučeni z ITT analýzy. ***Per Protocol (PP) populace byla použita pro analýzu účinnostních endpointů. Pacienti s následujícími odchylkami od protokolu byli vyřazeni z PP populace: • pacienti užívající DPP-4 inhibitor během 1 měsíce před vstupem do studie • pacienti užívající GLP-1 mimetika během 1 měsíce před vstupem do studie • pacienti užívající inzulin při vstupu do studie • pacienti užívající pouze nově zahájenou monoterapii nebo 2 a více PAD při vstupu do studie • pacienti doposud farmakologicky antidiabeticky neléčení při vstupu do studie • pacienti se změnou antidiabetické medikace při vstupu do studie • pacienti užívající studijní medikaci během 30 dnů před vstupem do studie a 5násobkem eliminačního poločasu před vstupem do studie • pacienti užívající více než 1 PAD před vstupem do studie Demografické údaje pacientů, hodnota glykovaného hemoglobinu a doba trvání diabetu jsou uvedeny v tab. 1. Skupiny se v těchto charakteristikách signifikantně nelišily.
Tab. 1. Demografické údaje a vstupní charakteristiky pacientů (ITT populace). 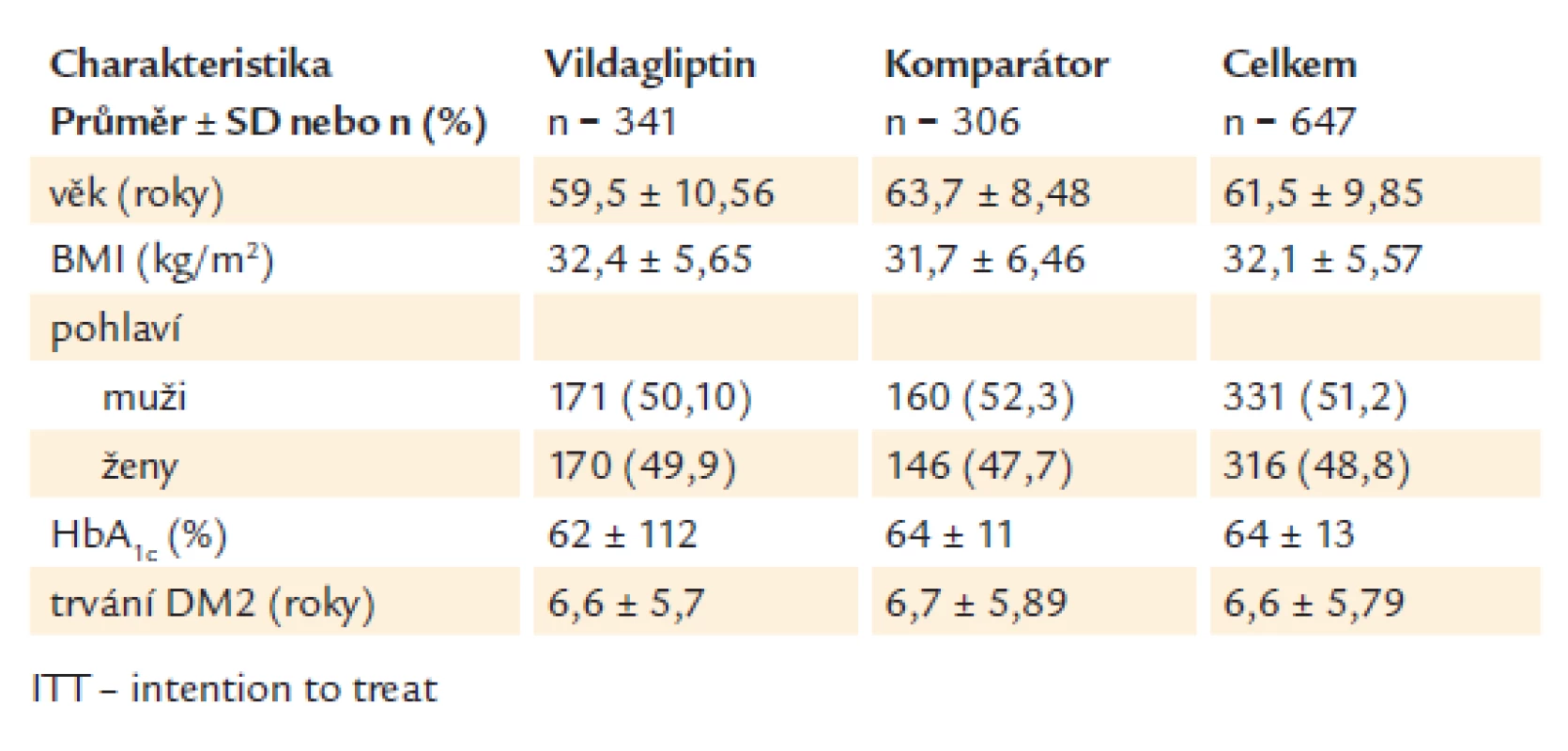
V tab. 2 jsou uvedeny kombinace antidiabetik, kterými byli pacienti v průběhu studie léčeni. Ve skupině s přidáním vildagliptinu byla nejčastější kombinace vildagliptin/metformin (87 % pacientů), v kontrolní skupině pak kombinace derivát sulfonylurey//metformin (83 % pacientů).
Tab. 2. Léčba při vstupu do studie (ITT populace). 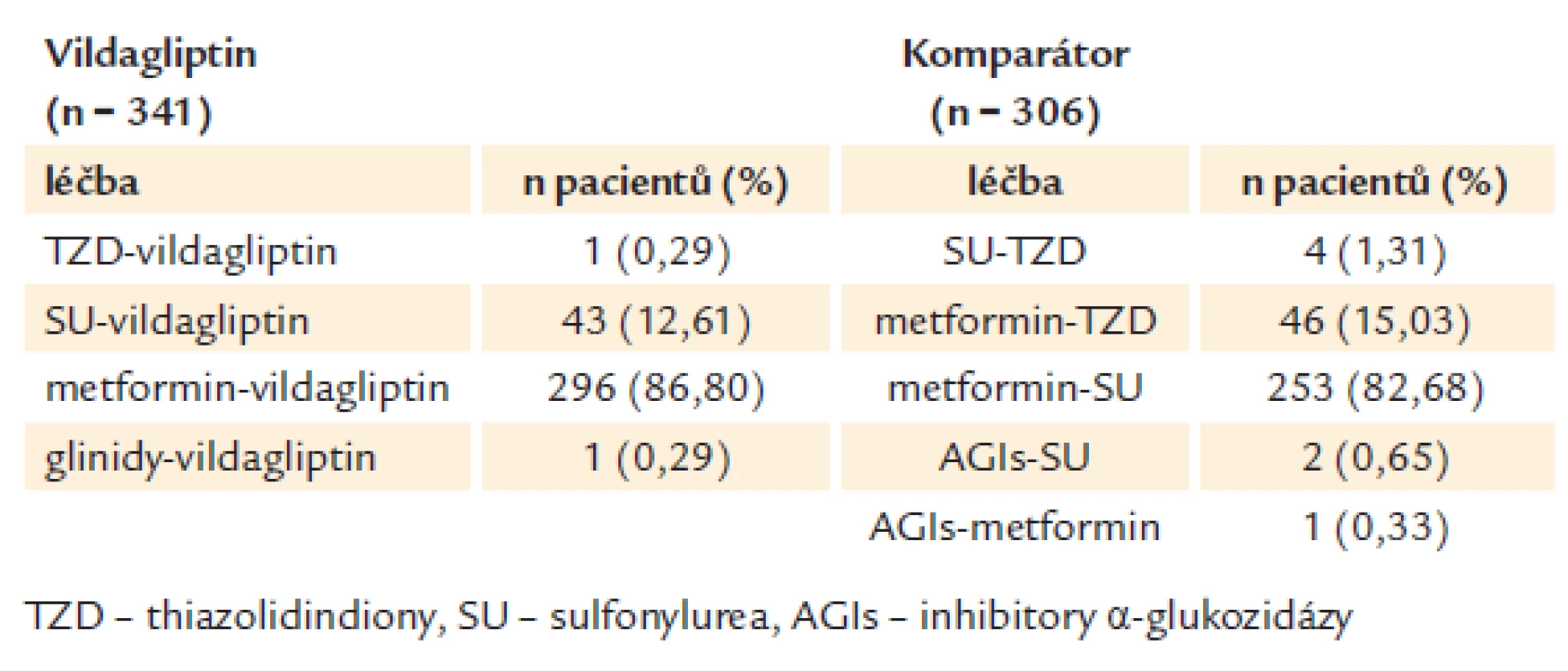
V tab. 3 jsou výsledky hodnocení primárního a sekundárního cíle. Primárního cíle (poklesu glykovaného hemoglobinu > 3 mmol/mol bez vzestupu hmotnosti ≥ 5 %, bez výskytu periferního edému, hypoglykemie nebo ukončení léčby z důvodu gastrointestinálních nežádoucích příhod během 12 měsíců léčby) dosáhlo 60,6 % pacientů ve skupině s přidáním vildagliptinu, což bylo signifikantně více než v kontrolní skupině (51,3 % pacientů, p < 0,019).
Tab. 3. Primární a sekundární endpointy účinnosti a bezpečnosti. 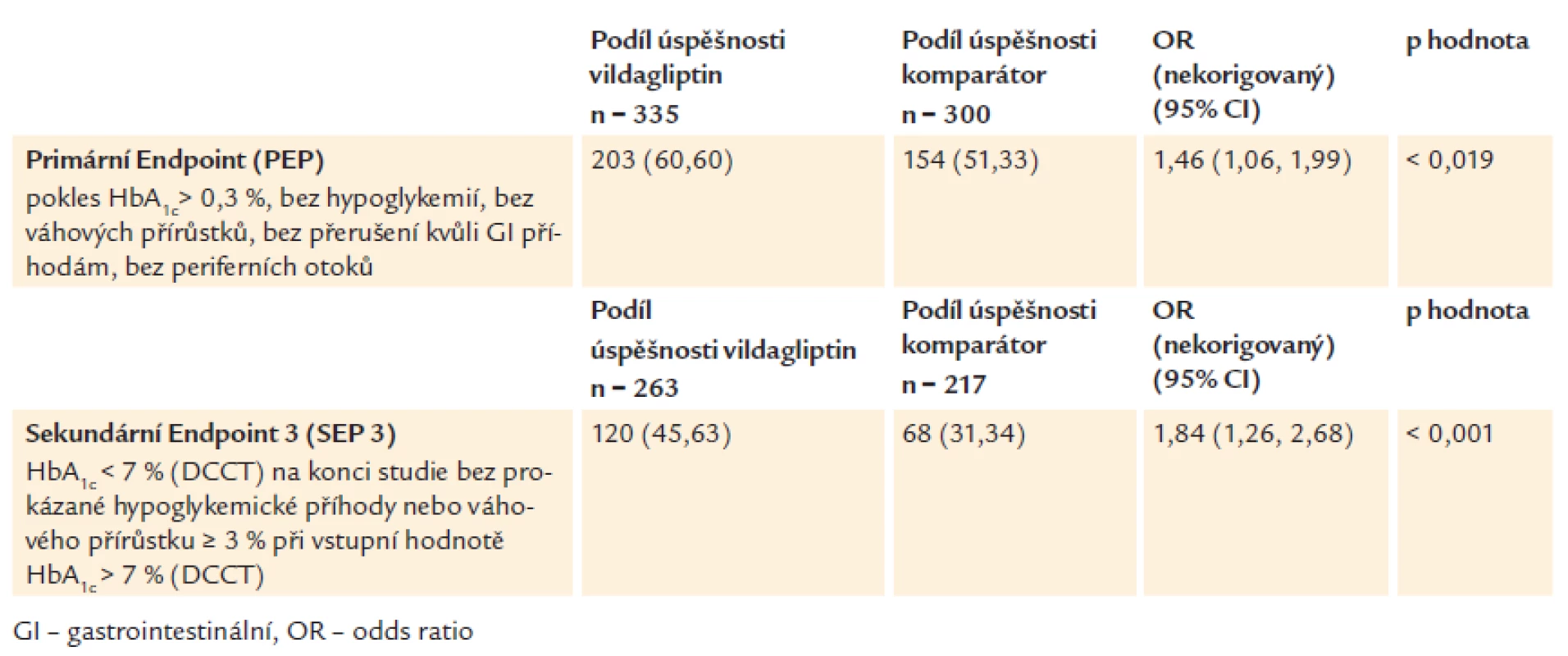
Sekundárního cíle (glykovaný hemoglobin < 54 mmol/mol bez výskytu hypoglykemie nebo vzestupu hmotnosti ≥ 3 % po 12 měsících léčby při vstupní hodnotě glykovaného hemoglobinu > 53 mmol/mol) dosáhlo 45,7 % pacientů ve skupině s vildagliptinem ve srovnání s 31,4 % pacientů v kontrolní skupině (p < 0,001).
Celkový výskyt nežádoucích příhod byl v obou skupinách nízký (27 vs 27) a signifikantně se nelišil (tab. 4).
Tab. 4. Nežádoucí příhody podle primární třídy orgánového systému (SOC) a léčené skupiny (ITT populace) 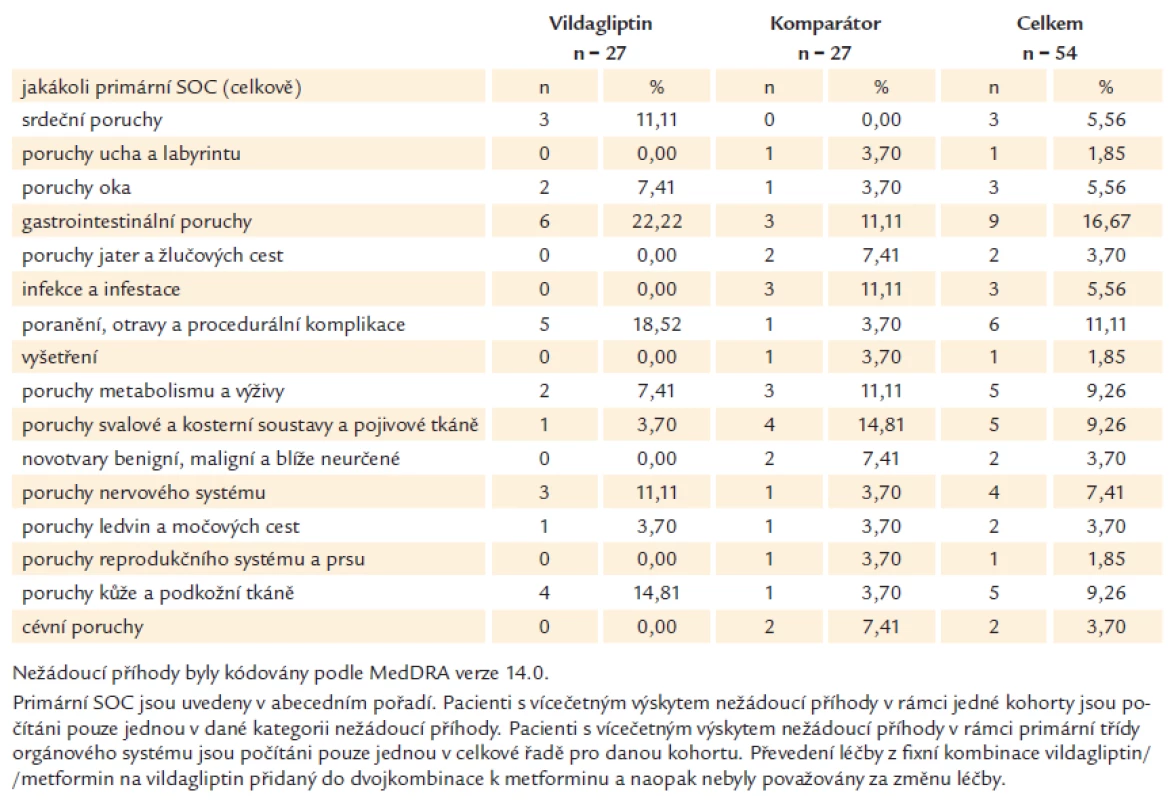
Diskuze
Diabetes mellitus 2. typu je progresivní onemocnění vyžadující postupnou intenzifikaci léčby přidáním dalších léků [24]. V současné době stále není k dispozici dostatek výsledků z rozsáhlejších studií provedených v podmínkách běžné klinické praxe, které by odpověděly na otázku optimálního algoritmu léčby diabetu 2. typu. Jednoznačná shoda nepanuje především v otázce léku druhé volby, který je obvykle přidáván při neuspokojivé kompenzaci na monoterapii metforminem. Výsledky studie EDGE tak mohou přispět k přesnější charakterizaci výhod a nevýhod nasazení jednotlivých typů perorálních antidiabetik.
Přestože současná doporučení jasně stanovují, že již při hodnotě glykovaného hemoglobinu nad 53 mmol/mol by měla být posílena léčba a do kombinace přidán další antidiabetický lék [21], v reálné praxi je intenzifikace léčby mnohdy i výrazně opožděna [8,25]. Rovněž cílů optimální kompenzace diabetu není u většiny pacientů dosahováno, což potvrdila v českých podmínkách i studie publikovaná prof. Škrhou [26].
K tomuto stavu přispívají mimo jiné i nežádoucí účinky antidiabetických léků a obavy lékařů i pacientů z možnosti vyvolání hypoglykemie (při nasazení derivátů sulfonylurey, glinidů, či inzulinu) nebo váhového přírůstku (při nasazení inzulinu či glitazonů) [27,28]. Opožděná intenzifikace léčby tak vede k prodlužování období neuspokojivé kompenzace pacientů a zvyšuje riziko vzniku chronických diabetických komplikací. Právě inkretinová léčba, a to zejména využití DPP-4 inhibitorů, by mohla díky nízkému výskytu nežádoucích účinků při zachování dobré účinnosti tento stav zlepšit.
Studie EDGE provedená celosvětově na více než 45 000 pacientech přináší řadu zajímavých poznatků, které by mohly přispět k optimální volbě léčby u diabetiků 2. typu neuspokojivě kompenzovaných na monoterapii. Výsledky pacientů zařazených do studie v rámci ČR jsou podobné jako celkové výsledky studie, které byly nedávno publikovány [22]. Nejdůležitějším výsledkem je fakt, že přidání vildagliptinu vedlo k dosažení primárního kombinovaného cíle u signifikantně vyššího počtu pacientů než přidání jiného antidiabetika k monoterapii. Z hlediska konkrétní léčby bylo nejvíce pacientů ve vildagliptinové skupině léčeno kombinací vildagliptin/metformin a v kontrolní skupině kombinací derivát sulfonylurey/metformin, což reálně odráží současnou klinickou praxi. Podobně bylo přidání vildagliptinu účinnější i v dosažení sekundárního kombinovaného cíle, tedy hodnoty glykovaného hemoglobinu pod 54 mmol/mol. Podíváme-li se podrobněji na parametry zodpovědné za rozdíly v dosažení primárního i sekundárního kombinovaného cíle, vidíme, že vildagliptin byl numericky, byť statisticky nesignifikantně mírně účinnější ve snížení procenta glykovaného hemoglobinu. Hypoglykemie se vyskytly pouze v kontrolní skupině, zatímco ve skupině s přidáním vildagliptinu nebyly zaznamenány.
Nepochybnou výhodou studie je její provedení v podmínkách reálné klinické praxe i fakt, že výběr antidiabetika do kombinace v kontrolní skupině byl ponechán na konkrétním ošetřujícím diabetologovi. Srovnání přidání vildagliptinu s kontrolním lékem tak reálně odpovídá zvyklostem v dané zemi. V rámci ČR i celosvětově je typickým lékem druhé volby u pacientů neuspokojivě kompenzovaných na monoterapii metforminem některý z derivátů sulfonylurey [29]. Tyto léky mají výhodu dobré účinnosti a mnoholetých zkušeností s jejich podáváním. Nevýhodou však zůstává zvýšené riziko hypoglykemie a hmotnostního přírůstku. Výsledky studie EDGE ukazují, že přidáním vildagliptinu pacientům neuspokojivě kompenzovaným na monoterapii je možné dosáhnout účinného zlepšení kompenzace diabetu, které je zcela srovnatelné nebo mírně lepší než u starších antidiabetik. Hodnotíme-li výsledky komplexně v rámci kombinovaného cíle tak, jak byl definován v této studii, léčba vildagliptinem umožňuje dosáhnout zlepšení kompenzace bez nejobávanějších nežádoucích účinků typu hypoglykemie, vzestupu hmotnosti či periferního edému.
Dosažení uspokojivé kompenzace diabetu bez přítomnosti nežádoucích účinků je z pohledu reálné klinické praxe zásadně důležité, protože jednoznačně ovlivňuje compliance pacientů k léčbě [30]. V praxi se typicky setkáváme s tím, že pacienti velmi nelibě nesou vzestup hmotnosti, zatímco vlastní kompenzace diabetu pro ně často nepředstavuje příliš reálný parametr, který by při svém hodnocení léčby brali v potaz. Výskyt hypoglykemií je nejen velmi nepříjemný pro pacienta, ale významně také zvyšuje riziko kardiovaskulárních komplikací [31]. U aktivních pacientů navíc často vede k omezování fyzické aktivity právě v důsledku obavy z možného vyvolání hypoglykemie. Při suboptimálním výběru léčby se pak často setkáváme s vynecháváním léků, které nežádoucí účinky způsobují. Konkrétní přínos studie EDGE tak spočívá v potvrzení skutečnosti, že léčba vildagliptinem je nejen účinná, ale také dobře akceptovatelná z hlediska pacientů, kterým přináší výhodu nízkého výskytu nežádoucích účinků. Tento nález potvrzuje zjištění z dříve publikovaných studií [32–34].
V souvislosti s léčbou DPP-4 inhibitory byly v poslední době diskutovány i možnosti výskytu některých nežádoucích účinků, především zvýšení rizika infekcí dýchacích cest a v širším kontextu inkretinové léčby též zvýšení rizika pankreatitidy a nádorů pankreatu [35,36]. Řada z těchto podezření byla založena převážně na výsledcích experimentálních studií na hlodavcích, které pochopitelně nelze přímo interpolovat do klinické praxe. V rámci studie EDGE byl výskyt nežádoucích příhod zcela srovnatelný s kontrolní skupinou léčenou jinými antidiabetickými léky podobně jako při analýze celosvětových výsledků [22]. Celkově jsou výsledky analýzy bezpečnosti a snášenlivosti ve studii EDGE v souladu s výsledky randomizovaných klinických studií s vildagliptinem. Ve studii nebyly prokázány žádné bezpečnostní signály v souvislosti se zvýšenými kardiovaskulárními nebo cerebrovaskulárními riziky, zvýšeným výskytem pankreatitid, jaterních příhod nebo s poruchami kůže či imunitního systému.
Zatímco design i vysoký počet pacientů sledovaných ve studii EDGE přináší řadu výhod, považujeme za nutné zmínit i limity studie, které musejí být při interpretaci jejích výsledků brány v potaz. Jednalo se o studii umožňující ošetřujícímu lékaři vybrat, zda bude pacient zařazen do skupiny s vildagliptinem nebo komparátorem, což vedlo k mírně vyššímu počtu pacientů s nasazením vildagliptinu. Tento rozdíl byl patrný i v rámci pacientů zařazených v ČR. Rovněž celkový počet hypoglykemií zaznamenaný během studie je o něco nižší, než by odpovídalo předpokladům u pacientů léčených deriváty sulfonylurey [37]. Je však dobře známo, že pacienti velmi často klinické příznaky hypoglykemie přisuzují jiným onemocněním či obtížím, a proto je lékaři ani nenahlásí. I tento stav do značné míry odpovídá běžné klinické praxi, kdy řada pacientů léčených pouze perorálními antidiabetiky nemá k dispozici glukometr, a výskyt hypoglykemie tak nemůže objektivně verifikovat. Ve skupině s vildagliptinem pak nebyly hypoglykemie zaznamenány vůbec, což prakticky odpovídá jejich minimálnímu výskytu v dalších studiích s vildagliptinem a jinými inkretinovými léky [17,38].
Závěr
Závěrem konstatujeme, že v rámci studie EDGE provedené v podmínkách běžné klinické praxe bylo procento pacientů dosahujících kombinovaného cíle poklesu glykovaného hemoglobinu > 3 mmol/mol bez výskytu periferního edému, hypoglykemie nebo ukončení léčby z důvodu gastrointestinálních nežádoucích příhod vyšší při přidání vildagliptinu než jiných antidiabetických léků při srovnatelném výskytu nežádoucích příhod. Tato studie potvrzuje, že vildagliptin může být velmi výhodnou možností léku druhé volby pro pacienty s diabetes mellitus 2. typu neuspokojivě kompenzovaných na monoterapii.
prof. MUDr. Martin Haluzík, DrSc.
www.lf1.cuni.cz
e-mail: mhalu@lf1.cuni.cz
Doručeno do redakce: 6. 11. 2013
Přijato po recenzi: 22. 11. 2013
Zdroje
1. O‘Rahilly S. Science, medicine, and the future. Non-insulin dependent diabetes mellitus: the gathering storm. BMJ 1997; 314 : 955–959.
2. CDC Diabetes Cost-effectiveness Group. Cost-effectiveness of intensive glycemic control, intensified hypertension control, and serum cholesterol level reduction for type 2 diabetes. JAMA 2002; 287 : 2542–2551.
3. Adler AI, Stevens RJ, Neil A et al. UKPDS 59: hyperglycemia and other potentially modifiable risk factors for peripheral vascular disease in type 2 diabetes. Diabetes care 2002; 25 : 894–899.
4. Adler AI, Stratton IM, Neil HA et al. Association of systolic blood pressure with macrovascular and microvascular complications of type 2 diabetes (UKPDS 36): prospective observational study. BMJ 2000; 321 : 412–419.
5. Haffner SM, Lehto S, Ronnemaa T et al. Mortality from coronary heart disease in subjects with type 2 diabetes and in nondiabetic subjects with and without prior myocardial infarction. N Engl J Med 1998; 339 : 229–234.
6. Skyler JS, Bergenstal R, Bonow RO et al. Intensive glycemic control and the prevention of cardiovascular events: implications of the ACCORD, ADVANCE, and VA Diabetes Trials: a position statement of the American Diabetes Association and a Scientific Statement of the American College of Cardiology Foundation and the American Heart Association. J Am Coll Cardiol 2009; 53 : 298–304.
7. Lachin JM, Genuth S, Nathan DM et al. Effect of glycemic exposure on the risk of microvascular complications in the diabetes control and complications trial – revisited. Diabetes 2008; 57 : 995–1001.
8. Holman RR, Paul SK, Bethel MA et al. 10-year follow-up of intensive glucose control in type 2 diabetes. N Engl J Med 2008; 359 : 1577-1589.
9. Duckworth W, Abraira C, Moritz T et al. Glucose control and vascular complications in veterans with type 2 diabetes. N Engl J Med 2009; 360 : 129–139.
10. Patel A, Chalmers J, Poulter N. ADVANCE: action in diabetes and vascular disease. J Hum Hypertens 2005; 19 (Suppl 1): S27–S32.
11. Turnbull FM, Abraira C, Anderson RJ et al. Intensive glucose control and macrovascular outcomes in type 2 diabetes. Diabetologia 2009; 52 : 2288–2298.
12. Baldeweg SE, Yudkin JS. Implications of the United Kingdom prospective diabetes study. Prim care 1999; 26 : 809–827.
13. Dormandy JA, Charbonel B, Eckland DJ et al. Secondary prevention of macrovascular events in patients with type 2 diabetes in the PROactive Study (PROspective pioglitAzone Clinical Trial In macroVascular Events): a randomised controlled trial. Lancet 2005; 366 : 1279–1289.
14. Martin JH, Deacon CF, Gorell MD et al. Incretin-based therapies--review of the physiology, pharmacology and emerging clinical experience. Intern Med J 2011; 41 : 299–307.
15. Ahren B et al. Mechanisms of action of the dipeptidyl peptidase-4 inhibitor vildagliptin in humans. Diabetes Obes Metab 2011; 13: 775–783.
16. Henness S, Keam SJ. Vildagliptin. Drugs 2006; 66 : 1989–2001; discussion 2002–2004.
17. Ahren B Clinical results of treating type 2 diabetic patients with sitagliptin, vildagliptin or saxagliptin – diabetes control and potential adverse events. Best Pract Res Clin Endocrinol Metab 2009; 23 : 487–498.
18. Foley JE, Jordan J. Weight neutrality with the DPP-4 inhibitor, vildagliptin: mechanistic basis and clinical experience. Vasc Health Risk Manag 2010; 6 : 541–548.
19. Foley JE, Sreenan S. Efficacy and safety comparison between the DPP-4 inhibitor vildagliptin and the sulfonylurea gliclazide after two years of monotherapy in drug-naive patients with type 2 diabetes. Horm Metab Res 2009; 41 : 905–909.
20. Abu-Hamdah R, Rabiee A, Meneilly GS et al. Clinical review: The extrapancreatic effects of glucagon-like peptide-1 and related peptides. Journal Clin Endocrinol Metab 2009; 94: 1843–1852.
21. Inzucchi SE et al. Management of Hyperglycemia in Type 2 Diabetes: A Patient-Centered Approach: Position Statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes care 2012; 35 : 1364–1379.
22. Mathieu C, Barnett AH, Brath H et al. Effectiveness and tolerability of second-line therapy with vildagliptin vs. other oral agents in type 2 diabetes: A real-life worldwide observational study (EDGE). Int J Clin Pract 2013; 67: 947–956.
23. Ligueros-Saylan M, Foley JE, Schweizer A et al. An assessment of adverse effects of vildagliptin versus comparators on the liver, the pancreas, the immune system, the skin and in patients with impaired renal function from a large pooled database of Phase II and III clinical trials. Diabetes Obes Metab 2010; 12 : 495–509.
24. Bell D. Pathophysiology of type 2 diabetes and its relationship to new therapeutic approaches. Diabetes Educ 2000; 26 (Suppl): 4–7.
25. Grant RW, Pirraglia PA, Meigs JB et al. Trends in complexity of diabetes care in the United States from 1991 to 2000. Arch Intern Med 2004; 164 : 1134–1139.
26. Škrha J et al. Diabetes mellitus 2002 v České republice – epidemiologická studie. DMEV 2005; 8 : 5–12.
27. Peyrot M, Barnett AH, Meneghini LF et al. Factors associated with injection omission/non-adherence in the Global Attitudes of Patients and Physicians in Insulin Therapy study. Diabetes Obes Metab 2012; doi: 10.1111/j.1463–1326.2012.01636.x.
28. Peyrot M, Barnett AH, Meneghini LF et al. Insulin adherence behaviours and barriers in the multinational Global Attitudes of Patients and Physicians in Insulin Therapy study. Diabet Med 2012; 29 : 682–689.
29. Škrha J et al. Diabetologie. Praha: Galén 2009.
30. Blonde L. Current challenges in diabetes management. Clin Cornerstone 2005; 7 (Suppl 3): S6–S17.
31. Mellbin LG, Malmberg K, Waldenstrom A et al. Prognostic implications of hypoglycaemic episodes during hospitalisation for myocardial infarction in patients with type 2 diabetes: a report from the DIGAMI 2 trial. Heart 2009; 95 : 721–727.
32. Fonseca V, Baron M, Shao Q et al. Sustained efficacy and reduced hypoglycemia during one year of treatment with vildagliptin added to insulin in patients with type 2 diabetes mellitus. Horm Metab Res 2008; 40 : 427–430.
33. Lukashevich V, Del Prato S, Araga M et al: Efficacy and safety of vildagliptin in patients with type 2 diabetes mellitus inadequately controlled with dual combination of metformin and sulphonylurea. Diabetes Obes Metab 2013. doi: 10.1111/dom.12229. In press 2013.
34. Schweizer A, Dejager S, Foley JE. Impact of insulin resistance, body mass index, disease duration, and duration of metformin use on the efficacy of vildagliptin. Diabetes Ther 2012; 3 : 8.
35. Butler PC, Elashoff M, Elashoff R et al. A critical analysis of the clinical use of incretin-based therapies: Are the GLP-1 therapies safe? Diabetes care 2013; 36 : 2118–2125.
36. Matveyenko AV, Dry S, Cox HI et al. Beneficial endocrine but adverse exocrine effects of sitagliptin in the human islet amyloid polypeptide transgenic rat model of type 2 diabetes: interactions with metformin. Diabetes 2009; 58 : 1604–1615.
37. Lundkvist J, Berne C, Bolinder B et al. The economic and quality of life impact of hypoglycemia. Eur J Health Econ 2005; 6 : 197–202.
38. Dejager S, Schweizer A. Minimizing the risk of hypoglycemia with vildagliptin: Clinical experience, mechanistic basis, and importance in type 2 diabetes management. Diabetes Ther 2011; 2 : 51–66.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2013 Číslo 12- U pacientů s traumatem je častěji dosaženo adekvátních hladin anti-Xa při dávkování enoxaparinu podle hmotnosti
- Přínos perorálního semaglutidu pro pacienty s DM 2. typu v ordinaci praktického lékaře
- Rizikové období v léčbě růstovým hormonem: přechod mladých pacientů k lékařům pro dospělé
- Prognostický význam hladiny natriuretických peptidů při léčbě empagliflozinem
- Levothyroxin a zaměnitelnost přípravků s jeho obsahem
-
Všechny články tohoto čísla
- Indikátory zánětu u pacientů s koronární aterosklerózou – editorial
- Komentář ke studii EDGE – editorial
- Pozice tiotropia v nových léčebných doporučeních pro chronickou obstrukční plicní nemoc – editorial
- Prospektivní, multicentrická, neintervenční studie na zhodnocení současné léčby pacientů s diabetes mellitus 2. typu, nedostatečně kompenzovaných monoterapií metforminem – KOMETA CZ
- Účinnost a bezpečnost vildagliptinu jako léku druhé volby ve srovnání s jinými perorálními antidiabetiky u pacientů s diabetes mellitus 2. typu: české výsledky v rámci celosvětové prospektivní kohortové studie EDGE
- Indikátory zápalu u pacientov s koronárnou aterosklerózou – úloha usCRP v diagnostike a predikcii prognózy ochorenia
- Současný pohled na onemocnění jater u srdečního selhání
- Pozice tiotropia v nových léčebných doporučeních pro chronickou obstrukční plicní nemoc
- Súčasnosť a budúcnosť farmako-artériotromboprofylaxie v klinickej praxi. Odporúčania Angiologickej sekcie Slovenskej lekárskej komory
- Doporučené postupy v léčbě starších pacientů s diabetes mellitus v ČR
- Doporučení KDIGO pro léčbu zvýšeného krevního tlaku u chronického onemocnění ledvin
- Zánětlivá borreliová dilatační kardiomyopatie
- Závažná rizika spojená s užíváním natrium-fosfátových projímadel
- Histiocytární sarkom
- Effects of the angiotensin receptor blocker Valsartan (Valsacor®) on arterial pressure, indices of myocardial diastolic function and global longitudinal strain in patients with uncontrolled arterial hypertension
- Mechanizmus pleiotropního účinku sulodexidu
- Rifaximin v léčbě jaterní encefalopatie
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Současný pohled na onemocnění jater u srdečního selhání
- Rifaximin v léčbě jaterní encefalopatie
- Histiocytární sarkom
- Závažná rizika spojená s užíváním natrium-fosfátových projímadel
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: MUDr. Petr Výborný, CSc., FEBO
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



