-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Globální hodnocení funkce hemostázy – část II. Vlastní zkušenosti s použitím trombin generačního testu u pacientů s trombofilií
Global assessment of haemostatic function - part II. Our experience with thrombin generation test using in thrombophilia patients
Generally used haemostatic tests do not cover the complexity of clotting system. Estimation of the potential to generate thrombin, which is the central enzyme in the blood coagulation, may correlate with thrombophilic fenotype. In our study we used thrombin generation test to evaluate the parameters of thrombin generation curve in thrombophilic patients and healthy blood donors groups. We compare results in asymptomatic and symptomatic subgroups of thrombophilic mutation carriers and also an influence of acquired risk factor on thrombin generation is assessed. The results show higher generation of thrombin in carriers of thrombophilic mutation which is statistically significant.
Key words:
thrombophilia, thrombin generation test, acquired risk factors
Autoři: A. Hluší 1; L. Slavík 1; J. Úlehlová 1; V. Krčová 1; J. Zapletalová 1; K. Indrák 1
Působiště autorů: Hemato-onkologická klinika FN LF UP Olomouc, 2Ústav lékařské biofyziky, pracoviště biometrie Lékařská fakulta UP Olomouc 1
Vyšlo v časopise: Transfuze Hematol. dnes,16, 2010, No. 3, p. 121-125.
Kategorie: Souhrnné práce, původní práce, kazuistiky
Souhrn
Běžně užívaná vyšetření hemostatického systému dostatečně nepostihují komplexitu procesu krevního srážení. Dosavadní zkušenosti se stanovením generace trombinu, centrálního enzymu koagulačního systému, naznačují možnou korelaci s trombofilním fenotypem. V našem souboru pacientů hodnotíme parametry trombin generační křivky u pacientů s trombofilií a zdravých dárců krve. Rovněž srovnáváme výsledky u symptomatických a asymptomatických nosičů trombofilní mutace a hodnotíme vliv získaných rizikových faktorů na generaci trombinu. Získané výsledky prokazují statisticky signifikantně vyšší generaci trombinu u nosičů trombofilní mutace.
Klíčová slova:
trombofilie, trombin generační test, získané rizikové faktoryÚvod
Trombin představuje centrální enzym v hemostatickém systému. Jednoduchý test sledující tvorbu trombinu byl navržen před více než 50 lety (1, 2). Posledních deset let při nových technických možnostech metoda sledování generace trombinu zažívá renesanci. Objevuje se celá řada klinických možností využití této metody jak u hypo-, tak u hyperkoagulačních stavů. Sledování generace trombinu umožňuje posouzení kapacity koagulačního systému v tvorbě fibrinové krevní sraženiny a tím posouzení globální funkce hemostázy. V řadě případů potenciál monitorování generace trombinu překonává možnosti konvenčních testů (např. sledování účinnosti bypassové léčby u hemofiliků, monitorování efektu nových antitrombotických léků).
V současnosti jsou komerčně dostupné dvě varianty trombin generačního testu (TGT), obě založené na principu štěpení fluorogenního substrátu vznikajícím trombinem (3–11). Konečným výsledkem měření je softwarově zpracovaná křivka charakterizovaná třemi základními parametry: dobou do nástupu generace trombinu (lag fáze), maximální koncentrací vznikajícího trombinu (Cmax) a celkovým množstvím vzniklého trombinu (ETP, plocha pod křivkou) (obr. 1).
Obr. 1. Trombin generační křivka. (Lag time – doba do nástupu generace trombinu, Cmax – maximum generace trombinu, ETP – plocha pod křivkou odpovídá celkovému množství generovaného trombinu) 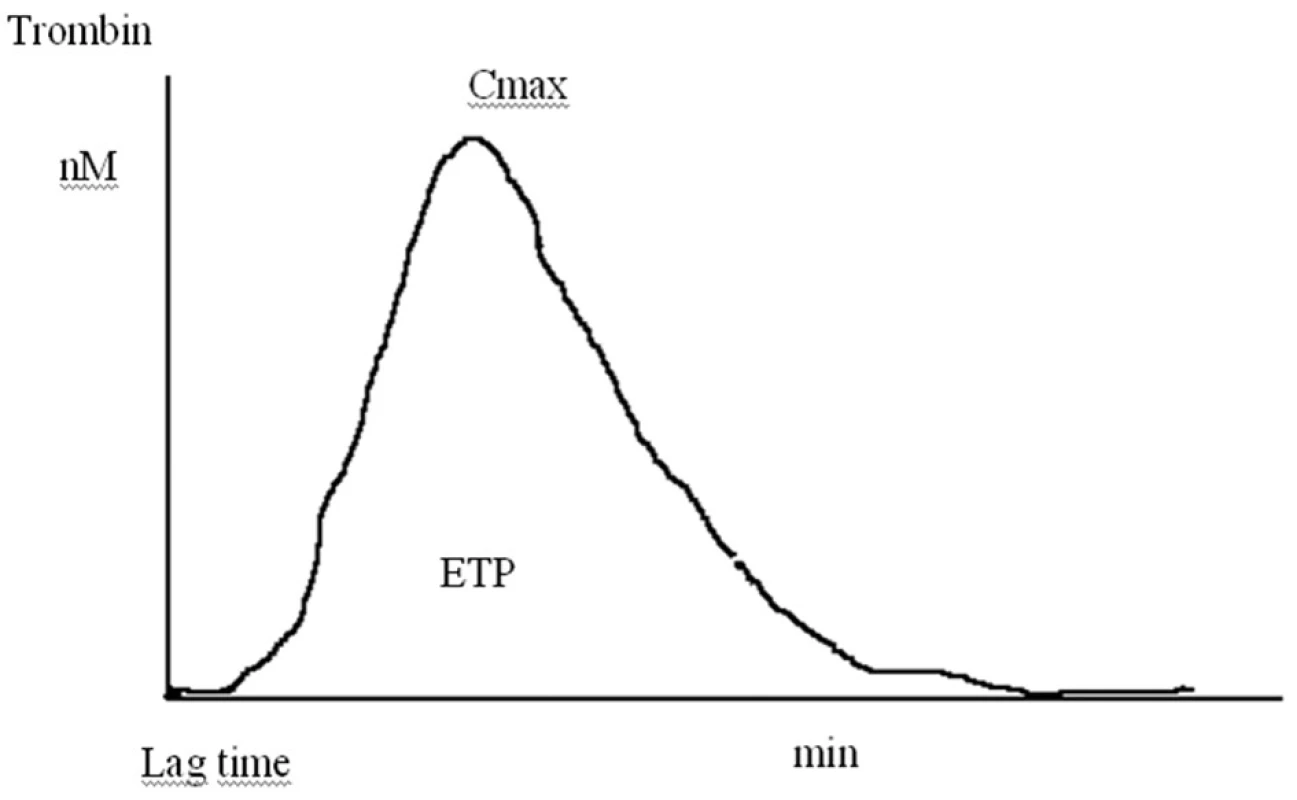
TGT může být potenciálně přínosný i v problematice hyperkoagulačních stavů, v posouzení zvýšeného rizika žilních tromboembolických komplikací či v hodnocení rizika rekurence těchto příhod (10–12). Dále uvádíme vlastní zkušenosti s použitím TGT u pacientů s geneticky podmíněným trombofilním stavem.
Vlastní zkušenosti
Cíl práce
Stanovení generace trombinu u zdravých jedinců a nosičů trombofilní mutace. Posouzení závislosti parametrů TGT na pohlaví a věku. Zhodnocení přínosu jednotlivých parametrů trombogramu a jejich korelace. Statistické zhodnocení rozdílů v jednotlivých parametrech TGT mezi kontrolní a trombofilní skupinou. U pacientů s trombofilií zhodnocení jednotlivých parametrů v podskupinách s/bez prodělané tromboembolické komplikace a s/bez přítomnosti získaného rizikového faktoru v době odběru vzorku.
Metodika
Odběr krve – periferní žilní krev byla odebrána do zkumavek s 3,2% citrátem sodným. Vzorek byl následně za laboratorní teploty centrifugován 10 min. při 3000xg. Získaná horní frakce (plazma chudá na destičky – PPP) byla rozdělena do stejných dávek a uchovávána při -70 °C do doby analýzy.
Trombin generační test – použit kit TECHNOTHROMBIN® TGA (Technoclone, Rakousko) na plně automatickém analyzátoru Ceveron® Alpha (Technoclone, Rakousko). Popisovaná laboratorní metodika vychází z četných literárních zkušeností (8, 13–16). Generace trombinu v měřeném vzorku byla iniciována 7,16 pM rekombinantního tkáňového faktoru (rTF) resuspendovaného v 0,32 μM fosfolipidových micel (obsah fosfatidylcholinu 2,56 μM a fosfatidylserinu 0,64 μM). Vlastní stanovení bylo prováděno následovně: Ke 40 μl vzorku PPP bylo přidáno 20 μl TRIS pufru a 15 μl 71,6 pM rTF s 3,2 μM fosfolipidových micel. Následně bylo přidáno 25 μl fluorogenního substrátu Z-G-G-RAMC a vlastní reakce byla zahájena 35 μl 25 mM CaCl2. Kalibrace stanovení byla prováděna na standard trombinu ~800 nmol. Z tohoto standardu byly připraveny kalibrační body s koncentrací ~200, ~400 a ~800 nmol. Z těchto ředění byla provedena měření dle následujícího protokolu. Do reakce bylo pipetováno 90 μl příslušně naředěného standardu trombinu. Další postup byl identický jako v případě vzorku. Vlastní integrovaný fluorescenční reader pracuje s excitační vlnovou délkou 360 nm a emisní vlnovou délkou 465 nm. Detekci fluorescence provádí v minutových intervalech po dobu 60 min. při 37 °C.
Vyhodnocení výsledků bylo automaticky prováděno pomocí software Ceveron PC-SW ver. 1.4., kdy primárně měřené referenční fluorescenční jednotky (RFU) byly pomocí kalibrační křivky převedeny na aktuální koncentraci trombinu ve vzorku. Jednotlivé parametry TGT (lag fáze – TGTt, max. generace trombinu – TGTm, plocha pod křivkou TGTe) byly získány derivací z naměřené křivky.
TGT test byl proveden u skupiny pacientů s vrozenou trombofilií, u kterých byl rutinními metodami vyloučen deficit antitrombinu, PC, PS, či přítomnost antifosfolipidových protilátek. Z vyšetření byli vyloučeni pacienti se stávající nebo nedávno (< 4 týdny) ukončenou antikoagulační terapií. K potvrzení vrozené trombofilní mutace byly použity standardizované PCR metodiky. Srovnávací soubor tvořili zdraví dárci krve. U nosičů trombofilní mutace jsme anamnesticky hodnotili přítomnost zevního rizikového faktoru v době odběru vzorku.
Soubory nosičů trombofilní mutace a kontrol – popisné charakteristiky
Hodnocený soubor nosičů trombofilní mutace tvořilo celkem 71 probandů s geneticky potvrzeným významným trombofilním stavem (Leidenská mutace G1691A, mutace FII G20210A). Výběr trombofilního souboru byl omezen pouze na uvedené genetické mutace vzhledem k jejich četnosti v populaci, dostatečně potvrzeným rizikům tromboembolických komplikací a s ohledem dobrou definovatelnost stran statistického hodnocení. K hodnocení byly zařazeny pouze vzorky od probandů vyšetřených v naší ambulanci, u kterých byla známa anamnéza případných prodělaných žilních tromboembolických komplikací (TEN+ – hluboká žilní trombóza, plicní embolie) a byl zjištěn výskyt přídatných rizikových faktorů v době odběru (RF+; v souboru zastoupeny: gravidita, hormonální antikoncepce, hormonální substituční léčba, chronické zánětlivé onemocnění, renální insuficience, maligní nádorové onemocnění). U hodnocených případů neprobíhala antikoagulační léčba, případně byla ukončena více než 4 týdny před odběrem vzorku. V podskupině trombofilních pacientů s mutací FII G20210A byla hodnocena i hladina koagulačního FII pro její možný výraznější vliv na generaci trombinu. Zvýšená hladina FII byla prokázána pouze u dvou nosičů této mutace. Popisné charakteristiky trombofilního souboru jsou uvedeny v tabulce 1.
Tab. 1. Charakteristika trombofilního souboru. 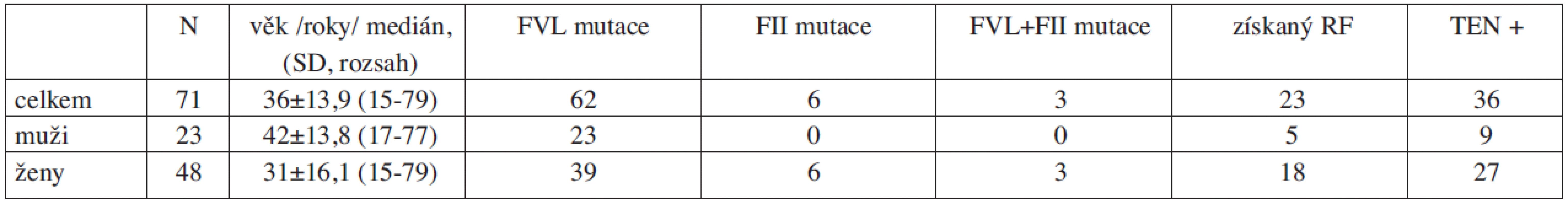
(RF = získané rizikové faktory – gravidita, hormonální antikoncepce, hormonální substituční léčba, chronické zánětlivé onemocnění, renální insuficience, maligní nádorové onemocnění, TEN+ = manifestní hluboká žilní trombóza či plicní embolie v anamnéze, SD = standardní odchylka) Srovnávací soubor tvořilo 66 vzorků plazmy získaných od zdravých dárců krve při venepunkci předcházející dárcovskému odběru. Medián věku činil v této skupině 32,5 roku, podíl zastoupení mužů a žen byl 41 ku 25.
Statistické hodnocení
Statistické hodnocení získaných dat provedlo pracoviště biometrie Ústavu lékařské biofyziky, LF UP v Olomouci. Pro posouzení závislosti parametrů TGT na sledovaných proměnných (pohlaví, věk, anamnéza TEN, přítomnost RF) byly použity neparametrické statistické metody: Mann-Whitney U-test resp. Spearmanova korelační analýza. Posouzení možnosti predikce žilní TEN ze získaných dat bylo postaveno na ROC analýze.
Výsledky
Kontrolní soubor
Získané výsledky jednotlivých parametrů TGT u zdravých dárců krve jsou uvedeny v tabulce 2. Při statistickém zpracování Spearmanova korelační analýza neprokázala závislost mezi hodnotami TGT parametrů a věkem (r = - 0,037 až 0,042), Mann-Whitney U-test neprokázal závislost mezi hodnotami TGT parametrů a pohlavím (p = 0,42–0,475).
Tab. 2. Výsledky TGT – kontrolní skupina. 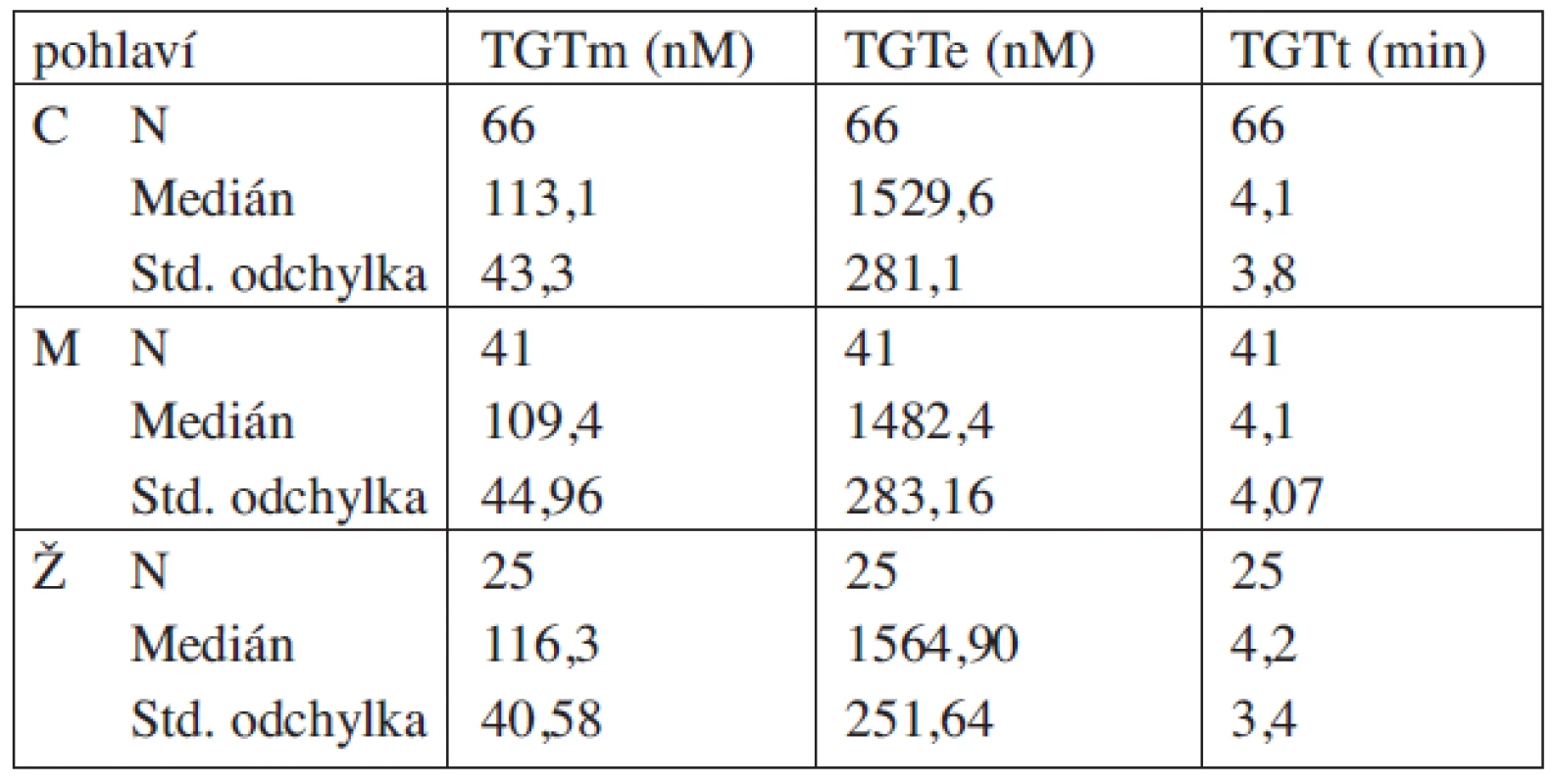
(C-celý soubor, M-muži, Ž-ženy) Trombofilní soubor
Výsledky parametrů TGT u nosičů s trombofilní mutace sumarizuje tabulka 3. Ani v tomto souboru neprokázala korelační analýza závislost mezi hodnotami parametrů TGT a věkem (r = 0,123 až 0,190). Z hlediska pohlaví byly zjištěny signifikantně vyšší hodnoty TGTe u žen ve srovnání s muži (p = 0,044).
Tab. 3. Výsledky TGT – trombofilní soubor. 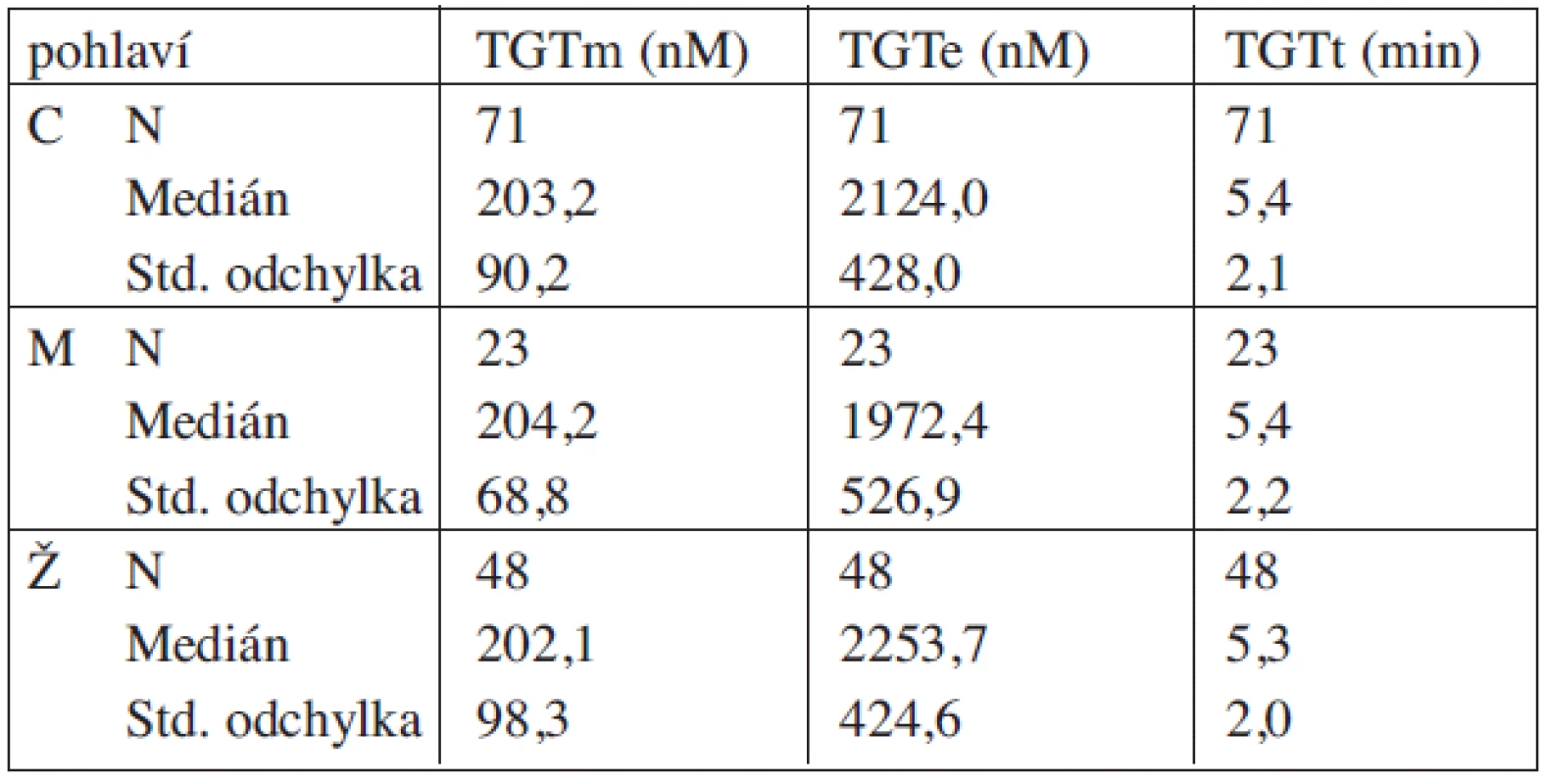
(C-celý soubor, M-muži, Ž-ženy) Srovnání jednotlivých souborů, analýza podskupin v rámci trombofilie
Při srovnání výsledků parametrů TGT kontrolního a trombofilního souboru byly prokázány signifikantně vyšší hodnoty TGTm a TGTe u pacientů s trombofilní mutací (p < 0,0001 v obou případech, box grafy 1, 2). V době do nástupu generace trombinu TGTt nebyl významný rozdíl prokázán (p = 0,714).
Graf 1 a 2. Srovnání parametrů TGT v kontrolním a trombofilním souboru. 
Subanalýza parametrů v rámci jednotlivých podskupin v trombofilním souboru (s/bez prodělané TEN příhody) prokázala vyšší medián hodnot v parametru TGTe (2253,7 nM v.s. 2039 nM) u pacientů s prodělanou komplikací. Při srovnání podskupin bez a s přítomností získaného rizikového faktoru byl prokázán vyšší medián hodnot v parametrech TGTm a TGTe (200 nM vs 218,9 nM, resp. 2107 v.s. 2157,6 nM) při přítomnosti RF. Statisticky nebyl ovšem tento rozdíl významný pro žádný z parametrů (p = 0,16 až 0,42). Výsledky shrnuje tabulka 4.
Tab. 4. Výsledky parametrů TGT v podskupinách pacientů s trombofilní mutací. 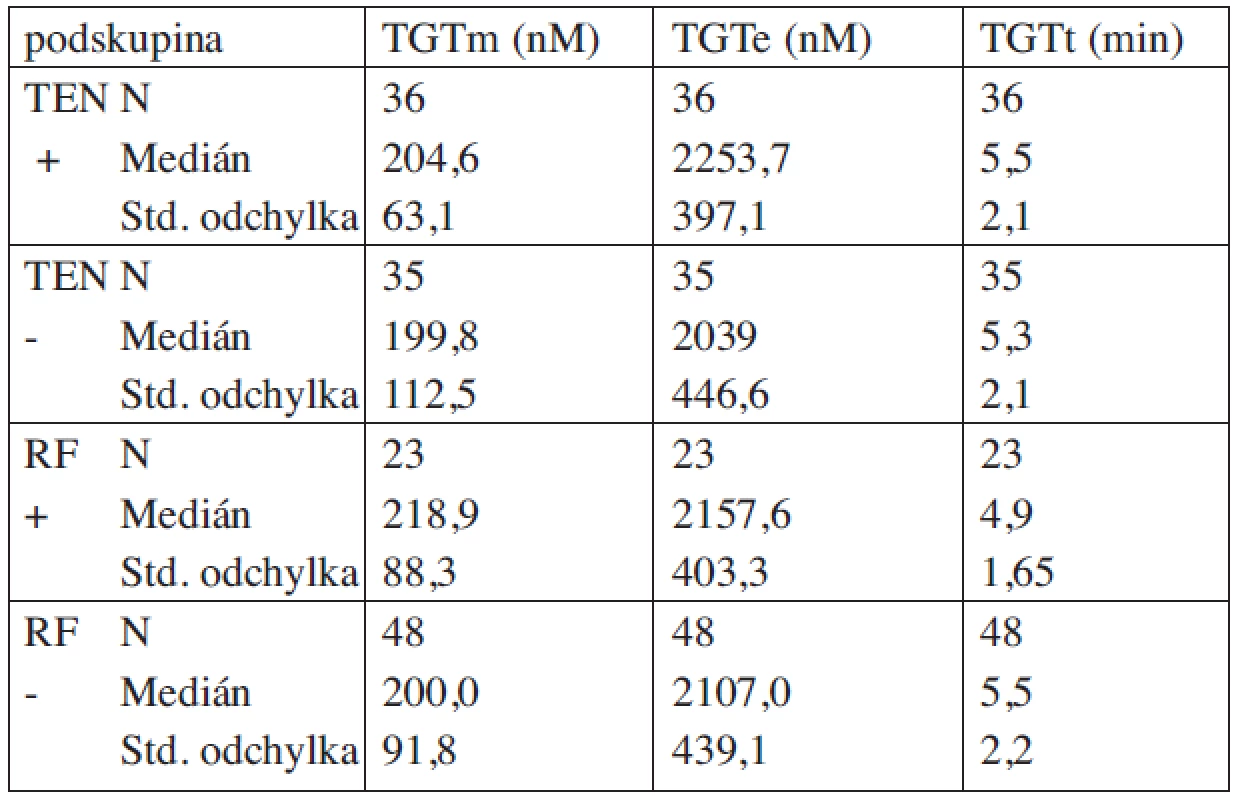
(TEN +/- = prodělaná/neprodělaná žilní tromboembolická příhoda, RF +/- = přítomen/nepřítomen získaný rizikový faktor v době odběru) Korelační analýza parametrů, posouzení možnosti predikce TEN
Zhodnocení vzájemné závislosti jednotlivých parametrů TGT pomocí Spearmanovy korelační analýzy prokázalo korelaci pouze mezi parametry TGTm a TGTe (r = 0,653, středně pozitivní korelace, graf 3), doba do nástupu generace trombinu TGTt ani s jedním z ostatních parametrů významně nekorelovala.
Graf 1. Korelace mezi parametry TGTm a TGTe. 
V rámci posouzení vhodného parametru pro predikci TEN byla provedena ROC analýza (graf 4). Statisticky nebyl ani jeden z hodnocených parametrů TGT shledán jako vhodný prediktor pro odhad rizika vzniku TEN komplikace (plocha pod ROC křivkou AUC je menší než 0,75). Hranici významnosti se nejvíce blíží celkové množství generovaného trombinu TGTe (AUC = 0,624).
Graf 2. ROC analýza – odhad rizika TEN. 
Shrnutí, diskuse
Z analýzy vlastních výsledků vyplývá, že generace trombinu není u mladších zdravých jedinců statisticky významně ovlivněna pohlavím ani věkem. Tento závěr nelze vztahovat na všechny věkové kategorie. Uvedená srovnávací skupina představuje soubor selektovaný, dárci krve jsou průměrně nižšího věku.
U nosičů trombofilní mutace byla generace trombinu statisticky významně zvýšená v porovnání se zdravou skupinou (parametry TGTm, TGTe). V rámci této skupiny byla prokázána vyšší celková generace trombinu (TGTe) u žen. Toto zjištění lze vysvětlit frekventnější přítomností přídatných protrombogenních rizik v době měření ve srovnání s muži (užívání hormonálních přípravků, gravidita).
Při subanalýze souboru nebyl prokázán signifikantní rozdíl mezi asymptomatickými nosiči trombofilní mutace a pacienty s prodělanou TEN komplikací v anamnéze. Tento nález podporuje teorii multifaktoriální etiologie tromboembolismu, kdy vlastní manifestaci TEN příhod většinou předchází působení dalšího nebo kombinace více přidružených získaných rizikových faktorů.
U probandů s trombofilním stavem a přítomným získaným rizikovým faktorem jsme prokázali generaci trombinu vyšší v porovnání se zbytkem skupiny, rozdíl ale překvapivě nebyl statisticky významný. Vzhledem k velikosti souboru nebyla z tohoto pohledu možná další podrobnější stratifikace dle typu rizikového faktoru.
V rámci analýzy možností TGT jsme prokázali středně pozitivní korelaci mezi parametry TGTm a TGTe. Dle našich zkušeností se doba do nástupu generace trombinu TGTt jeví jako klinicky nejméně použitelný parametr při hodnocení trombofilních stavů. Klinický potenciál TGT pro odhad rizika TEN komplikací byl hodnocen podrobnou statickou analýzou. Ani jeden z parametrů TGT nebyl shledán jako vhodný prediktor TEN.
Ve shodě s řadou literárních zkušeností byl i v našich souborech pozorován výrazný interindividuální rozptyl v TGT parametrech, který může být vedle omezeného počtu hodnocených subjektů, jednou z příčin některých nesignifikantních statistických závěrů. Pro zkvalitnění naší analýzy je do budoucna potřebné rozšíření obou souborů.
Trombin generační test představuje určitě slibnou možnost v posuzování globální hemostatické funkce. Nejen naše zkušenosti, ale i výsledky dosud publikovaných prací zatím neumožňují zavedení této metody do rutinní klinické praxe. Brání tomu mimo jiné velká mezilaboratorní variabilita testu, nedostatečná standardizace a v neposlední řadě i vyšší ekonomická náročnost vyšetření. TGT tak zatím v oblasti vyšetřování trombofilních stavů stále zůstává hlavně experimentálním laboratorní metodou.
Práce byla podpořena granty NS 10319-3/2009 86-14 a NR 9282-3/2007 86-12.
Doručeno do redakce: 27. 10. 2009
Přijato po recenzi: 20. 1. 2010
MUDr. Antonín Hluší
751 05 Kokory 401
e-mail: hlusian@fnol.cz
Zdroje
1. Macfarlane R, Biggs R. A thrombin generation test; the application in haemophilia and thrombocytopenia. Journal of Clinical Pathology 1953; 6 : 3–8.
2. Pitney WR, Dacie JV. A simple method of studying the generation of thrombin in recalcified plasma; application in the investigation of haemophilia. Journal of Clinical Pathology 1953; 6 : 9–14.
3. Hemker HC, Beguin S. Thrombin generation in plasma: its assessment via the endogenous thrombin potential. Thrombosis and Haemostasis 1995; 74 : 134-138.
4. Hemker HC, Giesen P, Al Dieri R, Regnault V, de Smedt E, Wagenvoord R, Lecompte T, Beguin S. Calibrated automated thrombin generation measurement in clotting plasma. Pathophysiology of Haemostasis and Thrombosis 2003; 33 : 4-15.
5. Hemker HC, Willems GM, Beguin S. A computer assisted method to obtain the prothrombin activation velocity in whole plasma independent of thrombin decay processes. Thrombosis and Haemostasis 1986; 56 : 9-17.
6. Hemker HC, Wielders S, Kessels H, Beguin S. Continuous registration of thrombin generation in plasma, its use for the determination of the thrombin potential. Thrombosis and Haemostasis 1993; 70 : 617-624.
7. Hemker HC, Giesen PL, Ramjee M, Wagenvoord R, Beguin S. The thrombogram: monitoring thrombin generation in platelet-rich plasma. Thrombosis and Haemostasis 2000; 83 : 589-591.
8. Hemker HC, et al. Thrombin generation, a function test of the haemostatic-thrombotic system. J Thromb Haemost 2006; 96 : 553-561.
9. Váradi K, Turecek PL, Schwarz HP. Thrombin generation assay and other universal tests for monitoring haemophilia therapy. 2004; 10: s2, 17-21.
10. Hron G, Kollars M, Binder BR, Eichinger S, Kyrle P.A. Identification of patients at low risk for recurrent venous thromboembolism by measuring thrombin generation. JAMA: The Journal of the American Medical Association 2006; 296 : 397-402.
11. Tripodi A, Legnani C, Chantarangkul V, Cosmi B, Palareti G, Mannucci PM. High thrombin generation measured in the presence of thrombomodulin is associated with an increased risk of recurrent venous thromboembolism. J Thromb Haemost 2008; 6 : 1327–33.
12. Besser M, Baglin C, Luddington R, van Hylckama Vlieg A, Baglin T. High rate of unprovoked recurrent venous thrombosis is associated with high thrombin-generating potential in a prospective cohort study. J Thromb Haemost 2008; 6 : 1720–5.
13. Devreese K, Wijns W, Combes I, et al. Thrombin generation in plasma of healthy adults and children: chromogenic versus fluorogenic thrombogram analysis. Thromb Haemost 2007; 98 : 600-613.
14. Baglin T. The measurement and application of thrombin generation. Br J Haematol 2005; 130 : 653-661.
15. Dargaud Y, Luddington R, Gray E, et al. Effect of standardization and normalization on imprecision of calibrated automated thrombography: an international multicentre study. Br J Haematol 2007; 139 : 303-309.
16. Chandler WL, Roshal M. Optimization of Plasma Fluorogenic Thrombin-Generation Assays. 2009; 132(2):169-79.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek Výběr z tisku
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2010 Číslo 3- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Ibrance® – nová šance pro pacientky s HR+/HER2– karcinomem prsu
-
Všechny články tohoto čísla
- Globální hodnocení funkce hemostázy – část II. Vlastní zkušenosti s použitím trombin generačního testu u pacientů s trombofilií
- Přínos režimu CTD (cyklofosfamid, thalidomid, dexametazon) v léčbě relabujících a refrakterních forem mnohočetného myelomu
- Odlišné hladiny asparagin syntetázy nejsou zodpovědné za rozdílnou senzitivitu leukemických blastů k L-Asparagináze
- Cytomegalovirus-specifická buněčná imunita: stanovení profilu imunitní funkce přináší klinicky relevantní odpověď
- Folikulární lymfom a význam nádorového mikroprostředí
- Vlasatobunková leukémia – diagnostika, liečba a monoklonové protilátky
- Imunofenotypizace a diagnostika obtížně klasifikovatelných akutních leukemií – nová diagnostická skupina dle WHO klasifikace 2008
- XXIV. Olomoucké hematologické dny s mezinárodní účastí
- Výběr z tisku a zprávy o knihách
- Autotransfuze v České republice v roce 2009
- Produkce transfuzní služby ČR za rok 2009
- Informace o volbách do výboru České hematologické společnosti, revizní komise, výboru zdravotních laborantů a výboru sester.
- Komentář k článku: Novinky v klasifikaci MDS a stanovení prognózy dle WPSS Žídková M., Voglová J., Bělohlávková P., Vrbacký F. Transfuze a Hematologie dnes 2010, 16: 42-46
- Odpověď na komentář Doc. Neuwirtové
- Výběr z tisku
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Vlasatobunková leukémia – diagnostika, liečba a monoklonové protilátky
- Folikulární lymfom a význam nádorového mikroprostředí
- Cytomegalovirus-specifická buněčná imunita: stanovení profilu imunitní funkce přináší klinicky relevantní odpověď
- Imunofenotypizace a diagnostika obtížně klasifikovatelných akutních leukemií – nová diagnostická skupina dle WHO klasifikace 2008
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




