-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Karotická endarterektomie z pohledu neurochirurga
Carotid endarterectomy from the neurosurgeon’s perspective
Introduction: Carotid endarterectomy (CEA) is performed by surgeons, vascular surgeons and neurosurgeons. This article aims to familiarize the reader with the neurosurgical principles of CEA.
Results: CEA anesthesia can be locoregional or general. In neurosurgical departments, both techniques are utilized according to standard practices. Both techniques are used in our department, with general anesthesia predominating. A microscope is always used during surgery. The advantages are magnification, perfect illumination and precise disobliteration. The gentle running suture allows minimal prevention of the vessel wall and substantially reduces the risk of residual stenosis/restenosis. The use of shunts is strictly selective. We use dominantly somatosensory evoked potentials in combination with EEG to monitor the need for shunt. We rarely use the eversion endarterectomy technique in carotid artery kinking with an abundant vessel wall.
Conclusion: The neurosurgical principles of carotid endarterectomy are characterized by a microscope/exoscope, microsurgical technique, and selective use of shunt. The dominant neurosurgical technique remains microendarterectomy with primo suture of the artery.
Keywords:
carotid endarterectomy – shunt – microscope – microsurgical technique – eversion carotid endarterectomy
Autoři: V. Přibáň; J. Dostál; J. Mork; J. Mraček
Působiště autorů: Neurochirurgická klinika LF UK a FN Plzeň
Vyšlo v časopise: Rozhl. Chir., 2025, roč. 104, č. 6, s. 242-246.
Kategorie: Souhrnné sdělení
doi: https://doi.org/10.48095/ccrvch2025242Souhrn
Úvod: Karotická endarterektomie (carotid endarterectomy – CEA) je prováděna cévními chirurgy a neurochirurgy. Cílem článku je seznámit čtenáře s neurochirurgickými principy CEA.
Výsledky: Anestezie CEA může být lokoregionální nebo celková. Na neurochirurgických pracovištích jsou užívány obě techniky dle zvyklosti. Na našem pracovišti jsou využívány obě techniky, dominuje anestezie celková. Při operaci je vždy využíván mikroskop. Výhodou je magnifikace, dokonalá iluminace a precizní dezobliterace. Jemná pokračující sutura umožní minimální zabrání cévní stěny a zásadně snižuje riziko reziduální stenózy/restenózy. Užití shuntu je přísně selektivní. Pro monitoraci potřeby shuntu využíváme dominantně somatosenzorické evokované potenciály v kombinaci s EEG. Techniku everzní endarterektomie využíváme vzácně při kinkinku karotidy s abudndantní cévní stěnou.
Závěr: Neurochirurgické principy karotické endarterektomie jsou charakterizovány využitím mikroskopu/exoskopu, mikrochirurgickou technikou a selektivním užitím shuntu. Dominantní neurochirurgickou technikou zůstává mikroendarterektomie s primosuturou tepny.
Klíčová slova:
karotická endarterektomie – shunt – mikroskop – mikrochirurgická technika – everzní karotická endarterektomie
Úvod
Ischemická cévní mozkové příhoda je problémem nejen medicínským, ale vzhledem k významné četnosti úmrtí a invalidity i celospolečenským. Stenóza vnitřní krkavice (arteria carotis interna – ACI) coby zdroj distální embolizace je velmi častou příčinou vzniku iktu. Karotická endarterektomie (carotid endarterectomy – CEA) hraje proto v primární a sekundární prevenci významnou roli již 70 let. I když v posledních 30 letech je karotický stenting alternativní metodou, je nadále role CEA významná a nezpochybnitelná. Další role CEA přichází stále častěji v akutní indikaci při karotické stenóze extrakraniální v kombinaci s okluzí magistrální mozkové tepny nebo v případě akutního uzávěru ACI. Tyto situace se řeší přísně individuálně v mezioborové spolupráci s intervenčními radiology.
Obr. 1. Uzávěr karotidy. Společná karotida uzavřená turniketem, ostatní tepny aneuryzmatickými svorkami. 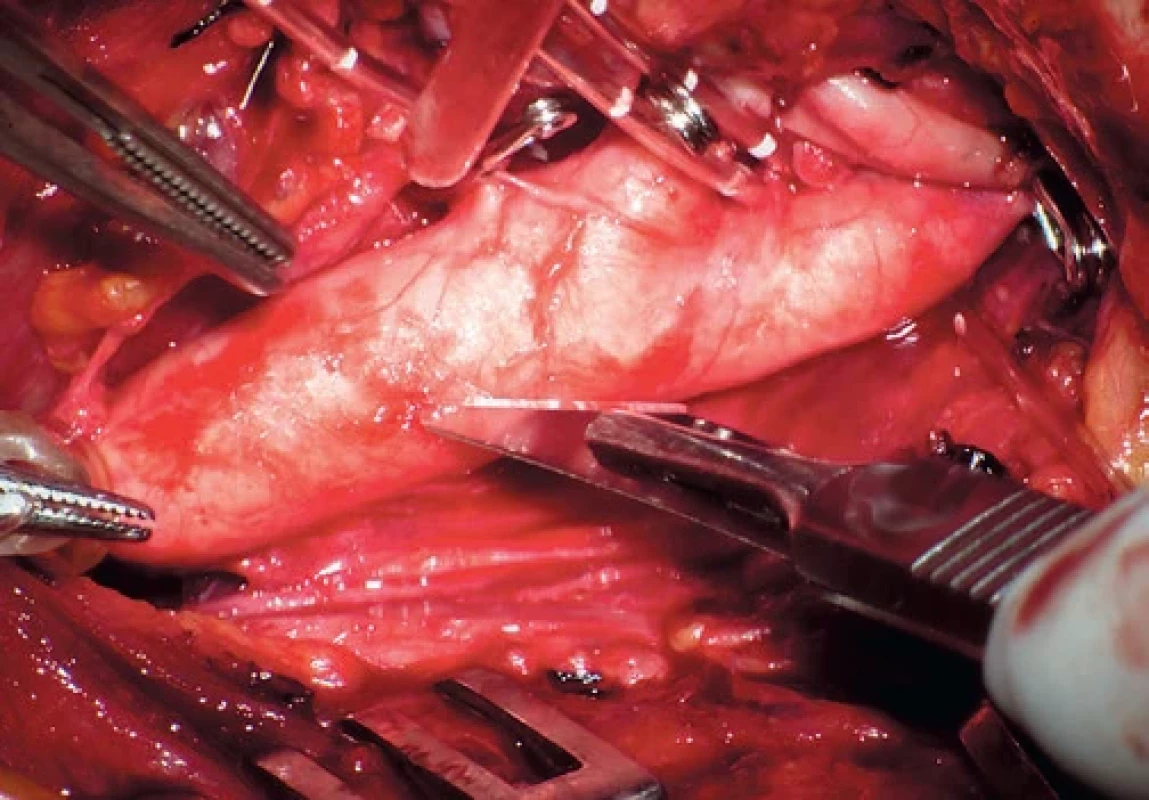
Closure of the carotid artery. The common carotid artery was
closed using a tourniquet, while other arteries were closed
with aneurysmal clips.Obr. 2. Stav po desobliteraci karotidy. 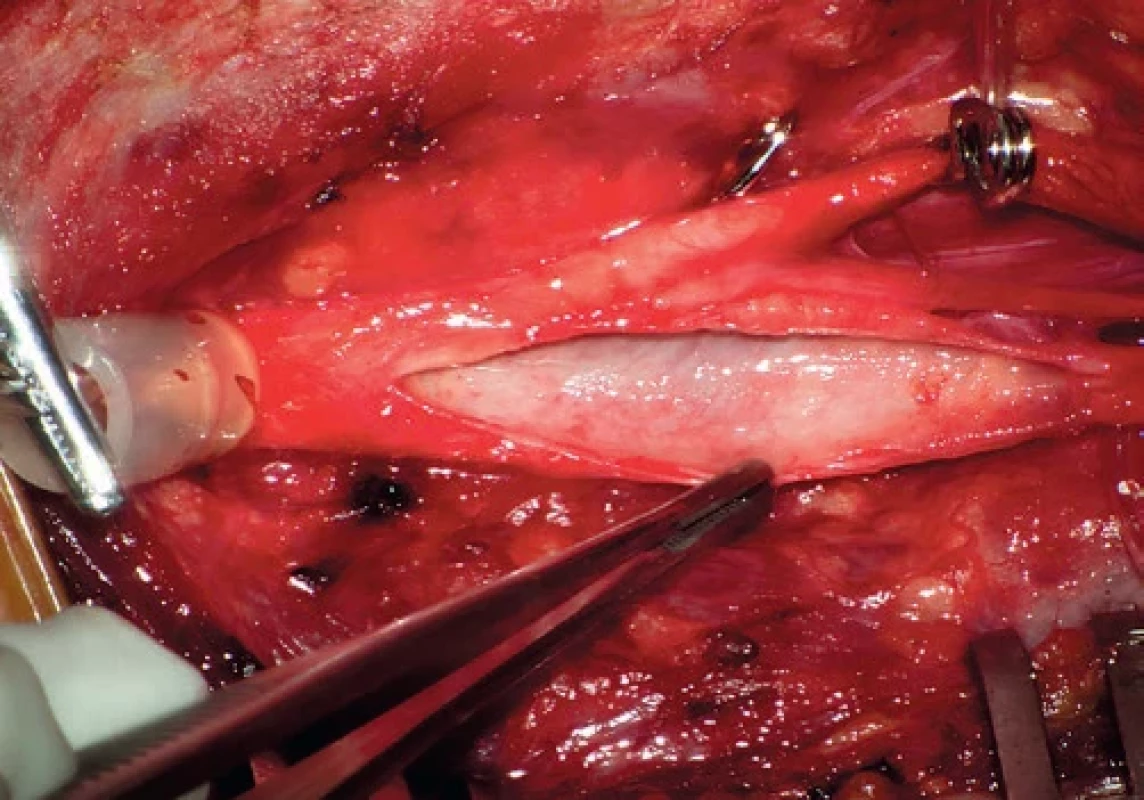
Condition after carotid artery desobliteration. Obr. 3. Primosutura tepny. 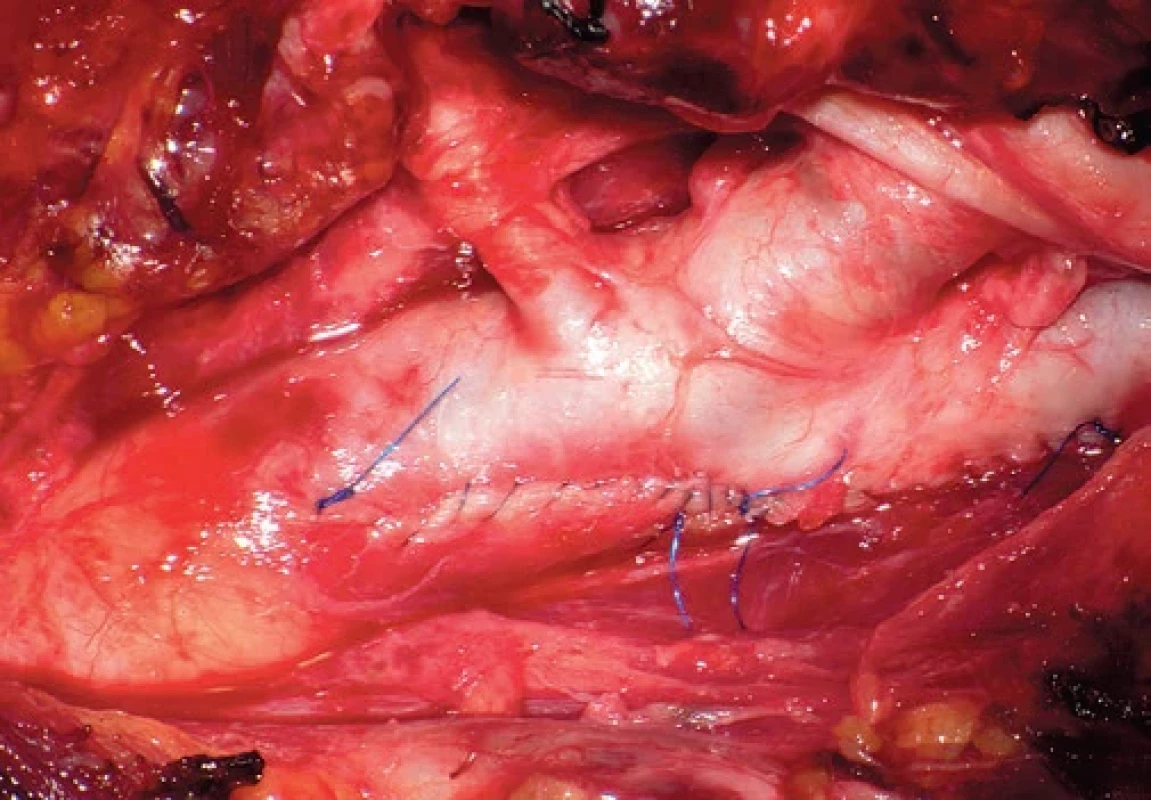
Primary arterial suture. Obr. 4. Stenóza a kinking ACI. 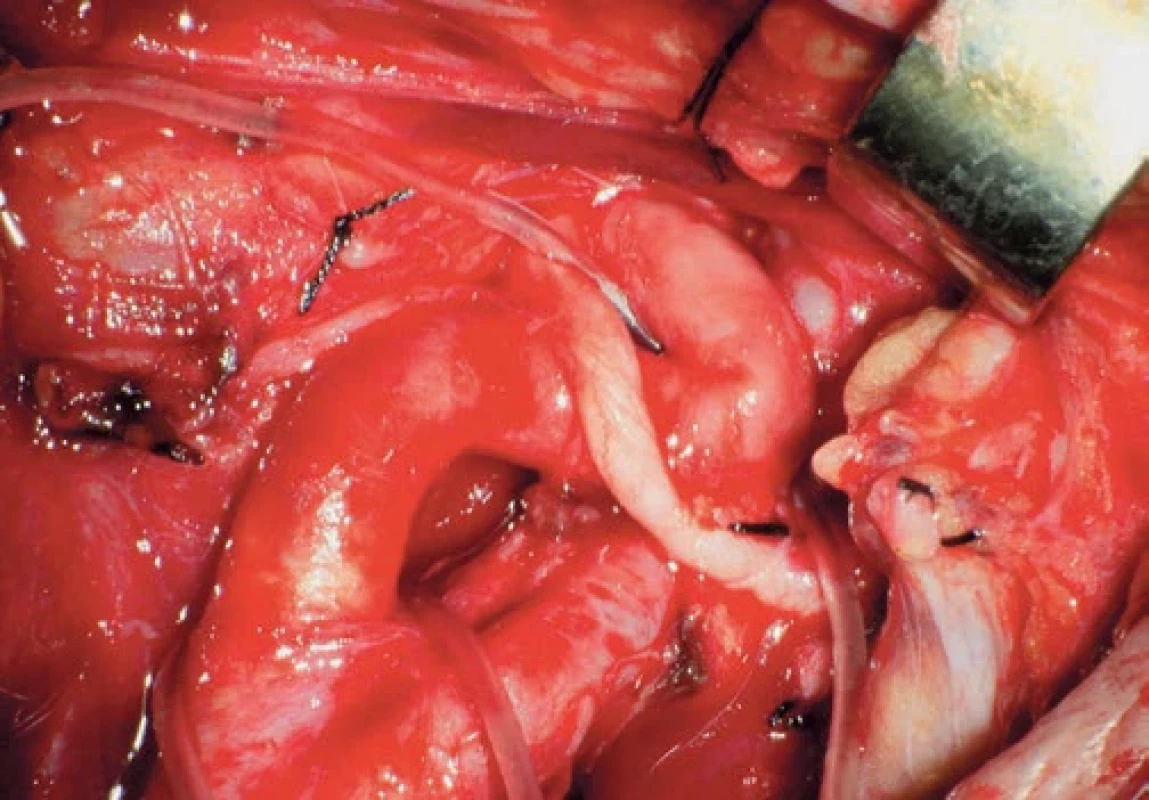
ICA stenosis and kinking. První CEA byla provedena na počátku 50. let 20. století [1]. V českých zemích byla první endarterektomie provedena profesorem Lhotkou. V roce 1963 publikovali své zkušenosti plzeňští neurochirurgové Ledinský a Mraček.
Problematice operací karotid se na počátku věnovali především cévní chirurgové. Renezanci zájmu o problematiku operací karotid v neurochirurgické obci můžeme datovat do 90. let 20. století. Tehdy se vrátil Vladimír Beneš z ročního pobytu ve Phoenixu u Roberta Spetzlera, kde zažil techniku karotické mikroendarterektomie v barbiturátové anestezii. Neustále tuto techniku propagoval, a zásadně tak přispěl k rozvoji operací karotid v rámci neurochirurgie. Dnes se těmto operacím věnuje 11 z 15 neurochirurgických pracovišť [2].
Mikrochirurgická technika s využitím mikroskopu je pravděpodobně nejvýznamnější charakteristikou filozofie operace z pohledu neurochirurga. Dalším společným bodem je přísně selektivní užití shuntu. Pokud jde o anestezii, zde je situace více heterogenní. Jsou pracoviště, která přísahají na lokoregionální anestezii (LA), další pak využívají anestezii celkovou (general anesthesia – GA) s monitorací potřeby shuntu. Na naší klinice operujeme symptomatické pacienty se stenózou ≥ 50 % dle metodiky NASCET a asymptomatické pacienty se stenózou ≥ 60 %. Symptomatické pacienty operujeme dle současných doporučení do 2 týdnů od příhody. U asymptomatických pacientů vyžadujeme přítomnost alespoň jednoho z rizikových faktorů – němý infarkt na MR nebo CT, progrese karotické stenózy, juxtaluminální „black area“, hemoragie uvnitř plátu na MR MRI, vyčerpaná cerebrovaskulární rezervní kapacita, lucentní plát na SONO, ≥ 1 mikroemboly na TCD za hodinu, kontralaterální karotická TIA/iktus. Indikace je přísně selektivní. Postupujeme podle aktuálních guidelines, a proto je v našem souboru četnost operací asymptomatických stenóz nízká [3]. Kritérium neurologické morbidity/mortality do 3 % je striktní podmínkou operativy asymptomatické karotické stenózy. V naší práci z roku 2011 jsme zaznamenali u 387 operovaných morbiditu 1,8 %, ischemickou mozkovou příhodu pak v 1,3 % [4].
Obr. 5. Dokončená everzní endarterektomie. 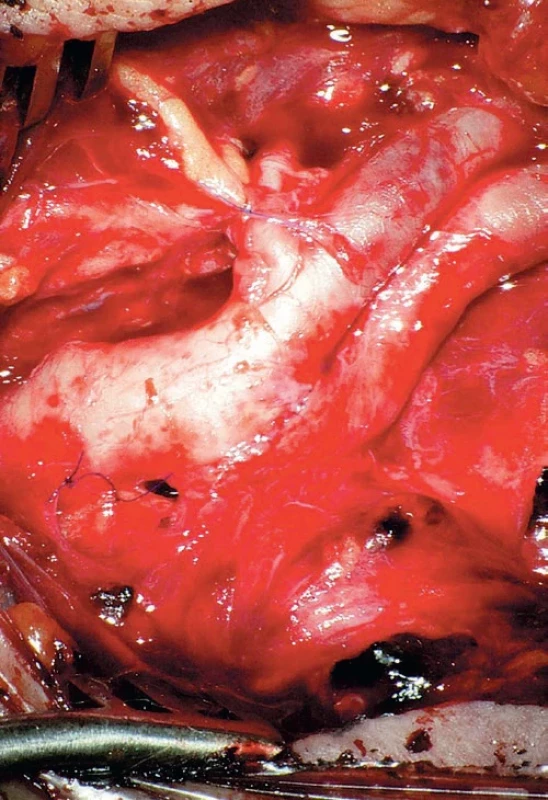
Eversion endarterectomy completed. Anestezie
První autor začínal operace CEA v LA. Soubor 1 000 pacientů mu umožňuje jisté subjektivní shrnutí problematiky. LA je šetrná vůči pacientům, kteří jsou obvykle zatíženi dalšími komorbiditami. Pokud však pacient netoleruje uzávěr tepny, může se to projevit nejen hemiparézou a event. ztrátou vědomí, ale i výrazným motorickým neklidem, obtížně zvladatelným. Verze v GA je pak někdy nevyhnutelná. Doba do návratu vědomí a úpravy hemiparézy po inzerci shuntu při pokračování výkonu v LA je pro operatéra nekonečná, byť se jedná o minuty. Nicméně je pravdou, že velká randomizovaná studie neprokázala rozdíly mezi GA a LA [5]. I s ohledem na tuto skutečnost na naší klinice necháváme pacienta zvolit si způsob anestezie. GA volí majorita operantů [6]. Poměr ve prospěch GA je na našem pracovišti 3 : 1. Důvody jsou heterogenní. Rozhodnutí pro GA může být na podkladě užívání clopidogrelu (komplikující krvácení při hlubokém cervikálním bloku), z důvodů preference pacienta, při vysoké pravděpodobnosti nutnosti užití shuntu u insuficientního Willisova okruhu a v neposlední řadě při nepříznivých anatomických poměrech na krku (hlavohruď, vysoko uložená bifurkace). Preference pro LA je v případě interních komorbidit, na přání pacienta, při technických problémech snímání evokovaných potenciálů, při zavedeném pacemakeru [7]. Orlický et al. provedli prospektivní randomizovanou studii, v níž hodnotili vznik čerstvých infarktů na MR při využití LA a GA po endarterektomii. Pacienti operovaní v LA měli významně nižší četnost ischemických lézí. Nicméně tyto nálezy neměly klinický dopad na výsledný stav pacientů [8]. Naše studie vyvrátila domněnku, že GA poškozuje kognitivní funkce. Zhoršení kognitivních potenciálů P 300 bylo detekováno pouze v bezprostředním pooperačním období, po 6 dnech byly kognitivní parametry identické v LA i GA [9]. Otázka dopadu CEA na změnu (potenciální zlepšení) kognitivních funkcí není dosud vyřešena. Výsledky studií jsou nejednoznačné. Nicméně v prospektivně hodnoceném souboru asymptomatických stenóz bylo prokázáno zlepšení kognitivních funkcí po CEA [10] Vyšší věk pacientů není pro nás zásadním omezujícím prvkem při indikaci CEA. Naše zkušenosti prokázaly, že se morbidita/mortalita zásadně neodlišuje od ostatní populace [11]. Naopak v indikaci stentu u pacientů nad 70 let jsme zdrženliví [3].
Karotická mikroendarterektomie
Využití mikroskopu považujeme za zásadní z několika důvodů:
Magnifikace
Zvětšení umožňuje velmi šetrnou preparaci a zejména primosuturu s minimálním, leč adekvátním zabráním cévní stěny. Tato technika podle našeho názoru prakticky eliminuje užití záplaty. Výskyt restenóz v našem souboru je zanedbatelný. Jsme si vědomi, že naše zkušenosti jsou v rozporu s doporučeními ESVS (European Society for Vascular Surgery) [3,12]. Mimo jiné i proto probíhá v současnosti napříč neurochirurgickými pracovišti studie na výskyt restenóz po CEA.
Iluminace
Užití mikroskopu poskytuje dokonalé nasvícení a přiblížení operačního pole, což umožňuje provádět CEA i při nepříznivých anatomických poměrech nebo na hypoplastické tepně. Toto je podle nás zásadní předností ve srovnání s užitím lupových brýlí.
Exaktní desobliterace
Patřičné zvětšení s dokonalým nasvícením umožní precizní odstranění plátu nejen distálně, ale také „dobrání“ vlajících cárů plátu „do hladka“ s čistou rannou plochou zbytku tunica media a adventicie. Čistá plocha je nesmírně důležitá, protože rezidua plátu zásadně zvyšují trombogenitu ranné plochy. Pokud distální ukončení odstraněného plátu nemá hladký přechod a je tendence k odchlípení intimy, pak neváháme užít tři fixační stehy Prolenem 7/0 k eliminaci potenciální disekce [2,13–15]. Ostatní technické aspekty s výjimkou uzávěru vnitřní karotidy (ACI) nejsou ničím pozoruhodné. Operujeme při trvající antiagregaci – anopyrin v LA a clopidogrel v GA. Kožní řez vedeme longitudinálně podél m. sternocleidomastoideus. Faciální žílu podvazujeme prakticky vždy. Heparin je aplikován v dávce 100 jednotek/kg intravenózně a pooperačně není antagonizován protaminem. Společnou karotidu uzavíráme DeBakeyho svorkou, resp. turniketem, ostatní tepny pomocí aneuryzmatických Yasargilových svorek (obr. 1).
Podélná arteriotomie probíhá ze společné do vnitřní karotidy distálně za stenózu. Uzávěr tepny po desobliteraci provádíme standardně technikou primosutury Prolenem 6/0 pokračujícím stehem (obr. 2, 3).
Pro dočasnou okluzi vnitřní karotidy užíváme dvě rozdílné techniky. V případě příznivě uložené bifurkace je ACI první uzavřenou tepnou [16]. Následuje test tolerance okluze v trvání 3 min. Pokud jsou somatosenzorické evokované potenciály (SSEP) stabilní, pokračujeme v operaci bez shuntu. Je-li bifurkace vysoko uložená nebo je stenóza velmi dlouhá, volíme odlišnou techniku. Nejprve uzavřeme společnou karotidu, zevní karotidu a a. thyroidea superior. Poté následuje preparace ACI a její uzávěr svorkou. Tato technika preparace při zástavě toku snižuje riziko distální embolizace z plátu v nepříznivých anatomických podmínkách [17,18].
V současnosti je nově využíván v mikrochirurgické operativě exoskop. Budoucnost ukáže, zda tato technologie nahradí mikroskop [19].
Selektivní shunting
Otázka užití shuntu se táhne do pravěku CEA. DeBakey shunt při první endarterektomii nepoužil a výsledek CEA byl excelentní. Cooley shunt spolu s lokální hypotermií využil a výsledkem byl těžký neurologický deficit s následnou významnou úpravou. Užití shuntu při operaci CEA můžeme rozdělit do tří skupin:
1. Operace paušálně bez užití shuntu
V současnosti prakticky opuštěný postoj.
2. Paušální užití shuntu
Rutinní užití má mnoho oponentů. Důvody jsou logické – 95 % operovaných nepotřebuje shunt vzhledem k patentnímu Willisovu okruhu. Selhání shuntu v důsledku mechanického uzávěru toku distálně nebo periferní embolizace při manipulaci se shuntem mohou vyústit v iatrogenní mozkovou ischemii. Na druhou stranu paušální užití shuntu přináší tvrdou rutinu, a tím i minimalizaci technických chyb při inzerci [20].
3. Selektivní užití shuntu
Základní postulát neurochirurgického přístupu. Možnost monitorace nabízí měření zpětného tlaku [21,22]. Tento monitoring nedává přesná spolehlivá data a není prakticky využíván. Transkraniální doppler [23,24] je metodou, která poskytuje relevantní data, spolehlivost ve srovnání s hodnocením somatosenzorických evokovaných potenciálů je nižší. SSEP jsou v kombinací s EEG aktuálně standardem identifikace potřeby užití shuntu. Detekce hypoperfuze je nejvyšší. Pokles amplitudy vln o 50 % a více je indikací inzerce shuntu [25,26]. V současnosti se i NIRS (near-infrared spektroskopie) monitorace jeví jako slibná technika určení selektivního užití shuntu [27].
Everzní CEA
Everzní karotická endarterektomie je nepochybně legitimní technikou, která má své kořeny v historii operativy CEA [28]. V současnosti je tato technika vnímána zejména cévními chirurgy jako základní pilíř CEA [29,30]. V našem pojetí užíváme everzní CEA v případě stenózy ACI a kinkingu nad stenózou stěny ACI, kdy po everzním odstranění plátu všijeme nadbytečnou ACI proximálně do společné karotidy tak, abychom narovnali patologický kinking cévní stěny. Druhou variantou je resekce tepny a její reimplantace do fyziologického místa odstupu (obr. 4, 5) [30,31].
Závěr
Od počátku se na chirurgickém řešení problematiky stenóz karotických tepen podíleli cévní chirurgové a neurochirurgové. Neurochirurgický přístup je charakterizován mikrochirurgickou technikou s využitím mikroskopu/exoskopu a selektivním užitím shuntu. Dominantní neurochirurgickou technikou zůstává mikroendarterektomie s primosuturou tepny.
Konflikt zájmů
Autoři článku prohlašují, že nejsou v souvislosti se vznikem tohoto článku ve střetu zájmů a že tento článek nebyl publikován v žádném jiném časopise, s výjimkou kongresových abstrakt a doporučených postupů.
Zdroje
1. DeBakey ME. Successful carotid endarterectomy for cerebrovascular insufficiency. Nineteen-year follow-up. JAMA 1975; 233(10): 1083–1085.
2. Spetzler RF, Martin N, Hadley MN et al. Microsurgical endarterectomy under barbiturate protection: a prospective study. J Neurosurg 1986; 65(1): 63–73. doi: 10.3171/jns.1986.65.1.0063.
3. Naylor R, Rantner B, Ancetti S et al. Editor’s choice – European Society for Vascular Surgery (ESVS) 2023 Clinical Practice Guidelines on the Management of Atherosclerotic Carotid and Vertebral Artery Disease. Eur J Vasc Endovasc Surg 2023; 65(1): 7–111. doi: 10.1016/j.ejvs.2022.04.011.
4. Sokol D, Fiedler J, Chlouba V et al. Endarterectomy for asymptomatic carotid artery stenosis under local anaesthesia. Acta Neurochir (Wien) 2011; 153(2): 363–369. doi: 10.1007/s00701-010-0806-3.
5. Lewis SC, Warlow CP, Bodenham AR et al. General anaesthesia versus local anaesthesia for carotid surgery (GALA): a multicentre, randomised controlled trial. Lancet 2008; 372(9656): 2132–2142. doi: 10.1016/S0140-6736(08)61699-2.
6. Mracek J, Kletecka J, Holeckova I et al. Patient satisfaction with general versus local anesthesia during carotid endarterectomy. J Neurol Surg A Cent Eur Neurosurg 2019; 80(5): 341–344. doi: 10.1055/s-0039-1688692.
7. Mracek J, Kletecka J, Mork J et al. Indications for general versus local anesthesia during carotid endarterectomy. J Neurol Surg A Cent Eur Neurosurg 2019; 80(4): 250–254. doi: 10.1055/s-0039-1678601.
8. Orlický M, Hrbáč T, Sameš M et al. Anesthesia type determines risk of cerebral infarction after carotid endarterectomy. J Vasc Surg 2019; 70(1): 138–147. doi: 10.1016/j.jvs.2018.10.066.
9. Mracek J, Holeckova I, Chytra I et al. The impact of general versus local anesthesia on early subclinical cognitive function following carotid endarterectomy evaluated using P3 event-related potentials. Acta Neurochir (Wien) 2012; 154(3): 433–438. doi: 10.1007/s00701-011-1270-4.
10. Košťál P, Mrhálek T, Kajanová A et al. Changes in cognition and hemodynamics 1 year after carotid endarterectomy for asymptomatic stenosis. J Neurol Surg A Cent Eur Neurosurg 2021; 82(6): 505–511. doi: 10.1055/s-0040-1720985.
11. Pribán V, Tesarík R. Carotid microendarterectomy in the aged. Rozhl Chir 2002; 81(1): 30–33.
12. De Letter JA, Moll FL, Welten RJ et al. Benefits of carotid patching: a prospective randomized study with long-term follow-up. Ann Vasc Surg 1994; 8(1): 54–58. doi: 10.1007/BF02133406.
13. Benes V, Mohapl M. Carotid microendarterectomy – surgical technique. Rozhl Chir 1999; 78(11): 556–561.
14. Findlay JM, Lougheed WM. Carotid microendarterectomy. Neurosurgery 1993; 32(5): 792–797. doi: 10.1227/00006123-199305000-00012.
15. Uno M, Takai H, Yagi K et al. Surgical technique for carotid endarterectomy: current methods and problems. Neurol Med Chir (Tokyo) 2020; 60(9): 419–428. doi: 10.2176/nmc.ra.2020-0111.
16. Pratesi C, Dorigo W, Alessi Innocenti A et al. Reducing the risk of intraoperative neurological complications during carotid endarterectomy with early distal control of the internal carotid artery. Eur J Vasc Endovasc Surg 2004; 28(6): 670–673. doi: 10.1016/j.ejvs.2004.09.015.
17. Yoshida K, Kurosaki Y, Funaki T et al. Surgical dissection of the internal carotid artery under flow control by proximal vessel clamping reduces embolic infarcts during carotid endarterectomy. World Neurosurg 2014; 82(1–2): e229–e234. doi: 10.1016/j.wneu.2013.06.018.
18. Yoshida K, Fukumitsu R, Kurosaki Y et al. The association between expansive arterial remodeling detected by high-resolution MRI in carotid artery stenosis and clinical presentation. J Neurosurg 2015; 123(2): 434–440. doi: 10.3171/2014.12.JNS14185.
19. Izumo T, Ujifuku K, Baba S et al. Initial experience of ORBEYE™ surgical microscope for carotid endarterectomy. Asian J Neurosurg 2019; 14(3): 839–842. doi: 10.4103/ajns.AJNS_242_18.
20. Javid H, Julian OC, Dye WS et al. Seventeen-year experience with routine shunting in carotid artery surgery. World J Surg 1979; 3(2): 167–177. doi: 10.1007/BF01561267.
21. Kwaan JH, Peterson GJ, Connolly JE. Stump pressure: an unreliable guide for shunting during carotid endarterectomy. Arch Surg 1980; 115(9): 1083–1086. doi: 10.1001/archsurg.1980.01380090051012.
22. Moore WS, Yee JM, Hall AD. Collateral cerebral blood pressure. An index of tolerance to temporary carotid occlusion. Arch Surg 1973; 106(4): 521–523. doi: 10.1001/archsurg.1973.01350160134022.
23. Jørgensen LG, Schroeder TV. Transcranial Doppler for carotid endarterectomy. Eur J Vasc Endovasc Surg 1996; 12(1): 1–2. doi: 10.1016/s1078-5884(96)80266-8.
24. Halsey JH. Risks and benefits of shunting in carotid endarterectomy. The International Transcranial Doppler Collaborators. Stroke 1992; 23(11): 1583–1587. doi: 10.1161/01.str.23.11.1583.
25. Loftus CM, Quest DO. Technical issues in carotid artery surgery 1995. Neurosurgery 1995; 36(4): 629–647. doi: 10.1227/00006123-199504000-00001.
26. Kearse LA, Brown EN, McPeck K. Somatosensory evoked potentials sensitivity relative to electroencephalography for cerebral ischemia during carotid endarterectomy. Stroke 1992; 23(4): 498–505. doi: 10.1161/01.str.23.4.498.
27. Pennekamp CW, Immink RV, den Ruijter HM et al. Near-infrared spectroscopy to indicate selective shunt use during carotid endarterectomy. Eur J Vasc Endovasc Surg 2013; 46(4): 397–403. doi: 10.1016/j.ejvs.2013.07.007.
28. De Bakey ME, Crawford ES, Cooley DA et al. Surgical considerations of occlusive disease of innominate, carotid, subclavian, and vertebral arteries. Ann Surg 1959; 149(5): 690–710. doi: 10.1097/00000658-195905000-00010.
29. Etheredge SN. A simple technic for carotid endarterectomy. Am J Surg 1970; 120(2): 275–278. doi: 10.1016/s0002-9610(70)80124-6.
30. Certík B, Treska V, Molácek J. Modified eversion carotid endarterectomy. Rozhl Chir 2004; 83(3): 140–143.
31. Priban V, Bombic M, Fiedler J. Comments on eversion technique of carotid endarterectomy. Rozhl Chir 2005; 84(9): 448–451.
Štítky
Chirurgie všeobecná Ortopedie Urgentní medicína
Článek vyšel v časopiseRozhledy v chirurgii
Nejčtenější tento týden
2025 Číslo 6- U pacientů s traumatem je častěji dosaženo adekvátních hladin anti-Xa při dávkování enoxaparinu podle hmotnosti
- Spolehlivý systém skórování jizev k hodnocení fotografií popálenin
- Nedostatečné dávkování enoxaparinu je u pacientů po ortopedickém výkonu časté a zvyšuje riziko tromboembolické nemoci
- Spasmolytický účinek metamizolu
-
Všechny články tohoto čísla
- Chirurgie karotid
- Workshop: Je čas na robotické kýly u nás?
- Workshop: Ultrazvuk v chirurgii s hands-on nácvikem
- Workshop: ERAS téměř na dosah, a přece tak daleko – jak na to?
- Ženy v chirurgii na Národním chirurgickém kongresu 2025: věda, zkušenosti i odvaha mluvit nahlas
- Výsledky on-line dotazníku spokojenosti účastníků 2. národního chirurgického kongresu 2025
- Historické poznámky k onemocnění karotid a karotické endarterektomii
- Chirurgie karotid z pohledu cévního chirurga
- Karotická endarterektomie z pohledu neurochirurga
- Extra-intrakraniální bypass
- Pohled současné cévní chirurgie na asymptomatické stenózy krkavic
- Populační pilotní program screeningu aneuryzmatu abdominální aorty v České republice
- Karotický web – vzácná příčina ischemické cévní mozkové příhody
- Rozhledy v chirurgii
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Karotická endarterektomie z pohledu neurochirurga
- Chirurgie karotid z pohledu cévního chirurga
- Historické poznámky k onemocnění karotid a karotické endarterektomii
- Populační pilotní program screeningu aneuryzmatu abdominální aorty v České republice
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: MUDr. Petr Výborný, CSc., FEBO
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



