-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Terapeutická role ambroxolu v léčebném ovlivňování mukociliární clearance u „bronchitického fenotypu“ CHOPN
Role of ambroxol in therapeutic interaction of mucociliary clearance in the “bronchitic phenotype” of COPD
Chronic obstructive pulmonary disease (COPD) is one of the leading causes of morbidity and mortality in the world. In addition, the prevalence of this syndrome is continually growing. The majority of COPD subjects suffer from the expectoration phenotype of this condition. The cornerstone of the expectoration phenotype is chronic mucus hypersecretion, which is a physiologically protective process that occurs in connection with non-infectious chronic inflammation of the airways and lung parenchyma. This prolonged and excess mucus secretion can usually lead to mucus retention inside the airways. This retention can often contribute to chronic expiratory airflow limitation. Therefore any pharmacotherapy that is able to reduce mucus secretion may play a considerable role in the management of the expectoration (bronchitic) phenotype of COPD.
Mucus over-secretion could be normalized with multiple mucoactive drugs that decrease inflammation, produce antioxidant activity, block secretion, break down the molecular structure of mucus and generally reduce the amount or viscosity of mucus. There are many mucoactive medications on the market and more are being clinically evaluated in the field of COPD. Presently we have several safe and effective drugs, which we can recommend for day-to-day clinical practice (ambroxol, erdosteine, N-acetylcysteine and bromhexine).
This article describes the realistic role of ambroxol in mucoactive therapy of COPD. Overall beneficial effects of mucoactive pharmaceutics appear to be in the treatment of acute exacerbations and presumably during chronic therapy of long-term mucus expectoration (bronchitic phenotype of COPD).Key words:
mucociliary clearance, mucociliary pathology, COPD, mucoactive substances, ambroxol, treatment.
Autoři: V. Koblížek; T. Dobešová; P. Papoušek; Š. Prachařová
Působiště autorů: Přednosta: doc. MUDr. František Salajka, CSc. ; Plicní klinika FN Hradec Králové
Vyšlo v časopise: Prakt. Lék. 2009; 89(10): 570-574
Kategorie: Z různých oborů
Souhrn
Chronická obstrukční nemoc (CHOPN) je celosvětově považována za jednu z hlavních příčin nemocnosti a úmrtnosti. Navíc její výskyt stále stoupá. Většina nemocných s CHOPN trpí expektoračním (bronchitickým) fenotypem onemocnění. Za hlavní rys tohoto fenotypu považujeme chronickou hypersekreci hlenu spojenou s neinfekčním chronickým perzistujícím zánětem v dýchacích cestách a plicním parenchymu. Hypersekrece může vést k retenci tohoto respiračního sekretu a přispívat tak ke zhoršování bronchiální obstrukce. Z tohoto důvodu přepokládáme přínos léků snižujících či dokonce normalizujících množství a charakter hlenu v léčbě tohoto typu CHOPN.
Mechanismy působení mukoaktivní medikace jsou velmi rozmanité (od protizánětlivého působení, přes antioxidační a mukolytické efekty, po inhibici tvorby hlenu či modifikaci jeho složení). Z bezpečných a efektivních preparátů u nás dostupných pro léčbu CHOPN lze vyjmenovat ambroxol, bromhexin, erdostein a N-acetylcystein. Zejména na prvně jmenovaný preparát je zaměřen náš přehledný článek.
Obecná role mukoaktivně působící látek na poli CHOPN je dosud ne zcela jasná. Jako chronická medikace mají prokázaný benefit u chronicky expektorujících nemocných se středně těžkou či těžkou CHOPN, pokud trpí recidivujícími či opakovanými akutními exacerbacemi, a to zejména v nepřítomnosti konkomitantní medikace inhalačními steroidy. Dále nejspíše najdou místo v léčbě většiny akutních exacerbací. Výsledky nových studií jistě náš léčebný postup zpřesní a upraví.Klíčová slova:
mukociliární clearance, mukociliární patologie, CHOPN, mukoaktivní látky, ambroxol, léčba.Úvod
Multikomponentní hlenový sekret, cylindrický respirační epitel, bronchiální i bronchiolární svalovina spolu s efektivním kašlacím reflexem a s rozmanitými prvky slizniční imunity představují důležité součásti adekvátní očisty dolních dýchacích cest – tzv. mukociliární clearance (1). Léky zasahující do tvorby hlenu, případně modifikující jeho složení či působící na funkci hlenové dvojvrstvy (ostrůvkový vazký gel + kontinuální řidší sol) jsou předmětem neustálého zájmu plicních i všeobecných lékařů (2, 3). Důvod je prostý. Značný počet nemocných navštěvujících naše ordinace přichází právě z důvodu respiračních obtíží souvisejících s mukociliární patologií (produktivní kašel, obtížná či nadměrná expektorace, dušnost způsobená retencí respiračních sekretů).
Mukociliární postižení může být spojeno s řadou respiračních chorob:
- CHOPN - chronickou obstrukční plicní nemocí (nejčastěji),
- pneumonií,
- tumorózním postižením plic,
- intersticiální plicními procesy nebo pooperační stavy,
- pneumopatií.
Zejména u pacientů s CHOPN je porucha mukociliární clearance a s ní asociovaný produktivní kašel frekventovaným problémem (4, 5, 6).
Fyziologická a patologická produkce hlenu
Samotný fakt výraznější hlenoprodukce není vždy patologií. Jedná se o obecnou pozitivní snahu organismu ochránit slizniční povrch dýchacích cest před inhalovanými pevnými či plynnými škodlivinami, případně před slizniční infekcí (7). Pokud denní tvorba hlenu překročí 100 ml – pacient trpí expektorací (2,3).
U průduškových onemocnění se dosti často setkáváme se skutečně výraznou (až excesivní) a/nebo protrahovanou nadprodukcí hlenového sekretu. Jak akutní, tak chronická zánětlivá onemocnění dýchacích cest (akutní tracheobronchitida, CHOPN, bronchiektázie, cystická fibróza, některé varianty bronchiálního astmatu) bývají asociovány s fenotypově různě vyjádřenými poruchami mukociliární clearance. Velmi často dochází ke změnám ve složení hlenu, například u CHOPN roste zejména obsah mucinu 5B (MUC5B) a poněkud méně i mucinu 5AC (MUC5AC) a dochází k tvorbě mucinu 2 (MUC2), u zdravých osob nepřítomného. Je zajímavé, že vznikají zejména jejich méně glykosylované formy (tzv. nízce nabité glykoformy mucinů).
Spolu se změnou typu se u některých pacientů s CHOPN zvyšuje i množství vytvořeného respiračního sekretu (2, 3, 8–11). Zmnožují se pohárkové slizniční buňky a hypertrofují podslizniční žlázy, ve kterých navíc dochází ke změně dříve vyrovnaného poměru mezi serózními a mucinózními buňkami ve prospěch mucinózních. Hlen se stává více hustým, zhoršuje průchodnost bronchů, stává se místem bakteriální či mykotické kolonizace, případně příčinou vzniku atelektáz různého rozsahu.
Mechanismus působení mukoaktivních látek
Teoreticky nejvýhodnějším postupem v terapii patologické hlenové nadprodukce je ukončit zánět vedoucí k jejímu vzniku, případně přímo zablokovat procesy stimulující hlenovou tvorbu. V případě CHOPN pak redukovat velikost hypertrofovaných submukosních žlázek, upravit poměr serózních a mucinózních žlázových buněk, snížit počet pohárkových buněk a normalizovat složení hlenu (2, 3).
Léky s takovým působením v klinické praxi bohužel nemáme. Proto používáme různá alternativní řešení, jejichž podstatou je necílené ovlivňování složení a množství respiračního hlenu. V praxi k tomu využíváme tzv. mukoaktivních farmak.
Mechanismy současné mukoaktivní medikace spočívají v redukci hypersekrece respirační sliznice (pohárkových buněk a submukózních žlázek), případně ve změně složení nebo zlepšení odstraňování již vzniklého respiračního sekretu. Většina aktuálních klasifikací dělí léky ovlivňující respirační sekret (mukoaktivní léčiva) na
- expektorancia,
- mukolytika,
- modifikátory iontového transportu,
- mukokinetika, a
- mukoregulační látky (12–15).
Mnohé preparáty mají kombinovaný efekt (například mukolytický + mukoregulační + expektorační či mukolytický + mukokinetický), některé účinkují i jinde než v dýchacích cestách (v plicním parenchymu, mimo respirační systém), případně je jejich aktivita antioxidační, eventuálně protizánětlivá. Proto tab. 1 popisující mechanismus účinku jednotlivých skupin je pouze určitým zjednodušením (15-17).
Tab. 1. Mukoaktivní léky (základní rozdělení dle Rubina 2007, Koblížka 2007 a Janssense 2009) 
Zkratky CF – cystická fibróza; CHOPN – chronická obstrukční plicní nemoc; KFA – kryptogenní fibrotizující alveolitida (idiopatická plicní fibróza); NAC – N-acetylcystein; Bronchitický fenotyp CHOPN
CHOPN patří mezi nejvíce frekventovaná chronická respirační onemocnění. Dle kvalifikovaných odhadů zůstává téměř polovina všech pacientů nediagnostikována. Celkem předpokládáme přítomnost CHOPN u 9–10 % dospělých (³40 let) (18–20). Nemalá část nemocných s CHOPN má více či méně vyjádřenou poruchu mukociliární clearance v oblasti dýchacích cest. Tato mukociliární dysfunkce patofyziologicky vede k hlenové nadprodukci a retenci. Klinicky se pak většinou projevuje jako chronický produktivní kašel. Takový fenotyp CHOPN můžeme nazvat bronchitickým – neboť splňuje klasickou britskou definici chronické bronchitidy (10, 20–22). V anglosaské literatuře se s tímto pojmem setkáváme nejvíce u anglických autorů, tzv. „mucus hypersecretory COPD phenotype“ (2, 3).
Léčebná role mukoaktivní medikace je značně důležitá zejména u této skupiny nemocných, neboť hlenová nadprodukce má negativní vliv na morbiditu a mortalitu nemocných (21, 23). Nadměrně tvořený a hůře odstraňovaný respirační hlenový sekret retinuje na mnoha místech dýchacích cest, kde snížením ventilace vede k nepoměru ventilace/perfúze, což může negativně ovlivňovat výměnu krevních plynů (O2 a CO2). Navíc lokální stáza hlenového sekretu sekundárně negativně ovlivňuje kinetiku cilií a celkovou mukociliární clearanci. To dále prohlubuje hlenovou retenci a navíc v místě nepohybujícího se hlenu dochází ke snadnější bakteriální kolonizaci. Bakteriální kolonizace pak bývá nezřídka příčinnou exacerbace, jež dále zvyšuje tvorbu hlenu (2, 3).
Kromě expektoračního (bronchitického) fenotypu CHOPN se u našich nemocných setkáváme také s fenotypem bronchiolitickým (převažující zánětlivé onemocnění malých bronchů s průměrem menším než 2 mm) klinicky charakterizovaným časným vznikem dušnosti, emfyzematickým fenotypem (s přítomností destrukce stěny alveolů, duktulů a sakulů, vedoucí k výrazné plicní hyperinflaci a značné limitaci námahy) a v neposlední řadě i s cévním fenotypem (s přítomností plicní arteriální hypertenze převyšující tíži ventilační poruchy při dominantním postižení plicní vaskulatury), případně s různě vyjádřenými kombinacemi všech výše uvedených typů onemocnění.
Obr. 1. Excesivní hlenová nadprodukce provází většinu pacientů s akutní exacerbací CHOPN, bronchiektaziemi, případně osoby s pneumonií (archiv autorů) 
Použití mukoaktivních léků v terapii CHOPN
Mukoaktivní medikace by teoreticky měla představovat benefit pro nemocné ve stabilní fázi, pokud trpí bronchitickým fenotypem CHOPN (2, 3). Dle některých studií totiž (v rozporu se staršími daty) je hlenová nadprodukce v těsné korelaci s poklesem plicních funkcí a koreluje také s rizikem infekční mortality (5). Také většina případů akutní exacerbace bývá asociována s akcentací hlenové produkce, se zvýšením viskozity hlenu a s tím související progresí retence respiračního sekretu v dýchacích cestách (24). Otázka přechodného (při akutních exacerbacích) či dlouhodobého (u stabilní fáze onemocnění) podávání léků ovlivňujících respirační hlenový sekret sekret je proto neustále diskutována a testována v mnoha klinických studiích (2, 3, 14, 23, 25).
Zatím musíme konstatovat, že v mnoha aspektech týkajících se mukoaktivní léčby nemocných s CHOPN stále nemáme jasno. Obecnou snahou terapie bronchitické (hlenotvorné) komponenty CHOPN by totiž měla být úplná normalizace hlenové produkce, redukce velikosti submukózních žlázek, normalizace poměru mezi serózními a mucinózními buňkami těchto žlázek, pokles počtu pohárkových buněk ve sliznici, úprava funkce „poškozeného mukociliárního eskalátoru“a případně s tím související zpomalení úbytku (deklinace) plicních funkcí. V současnosti bohužel neexistuje žádný lék, který by tyto maximalistické požadavky splňoval (ani v pestré paletě mukoaktivních farmak ani v jiné lékové skupině). Proto lze pochopit současně platná mezinárodní léčebná doporučení (20, 26), jež pravidelnou mukoaktivní léčbu všech nemocných s CHOPN nedoporučují.
Obr. 2. Rozšířená hlenová podslizniční žláza u nemocného s CHOPN (stabilní fáze) – obraz v bílém světle a pomocí autofluorescenčního modu bronchoskopu (archiv autorů) 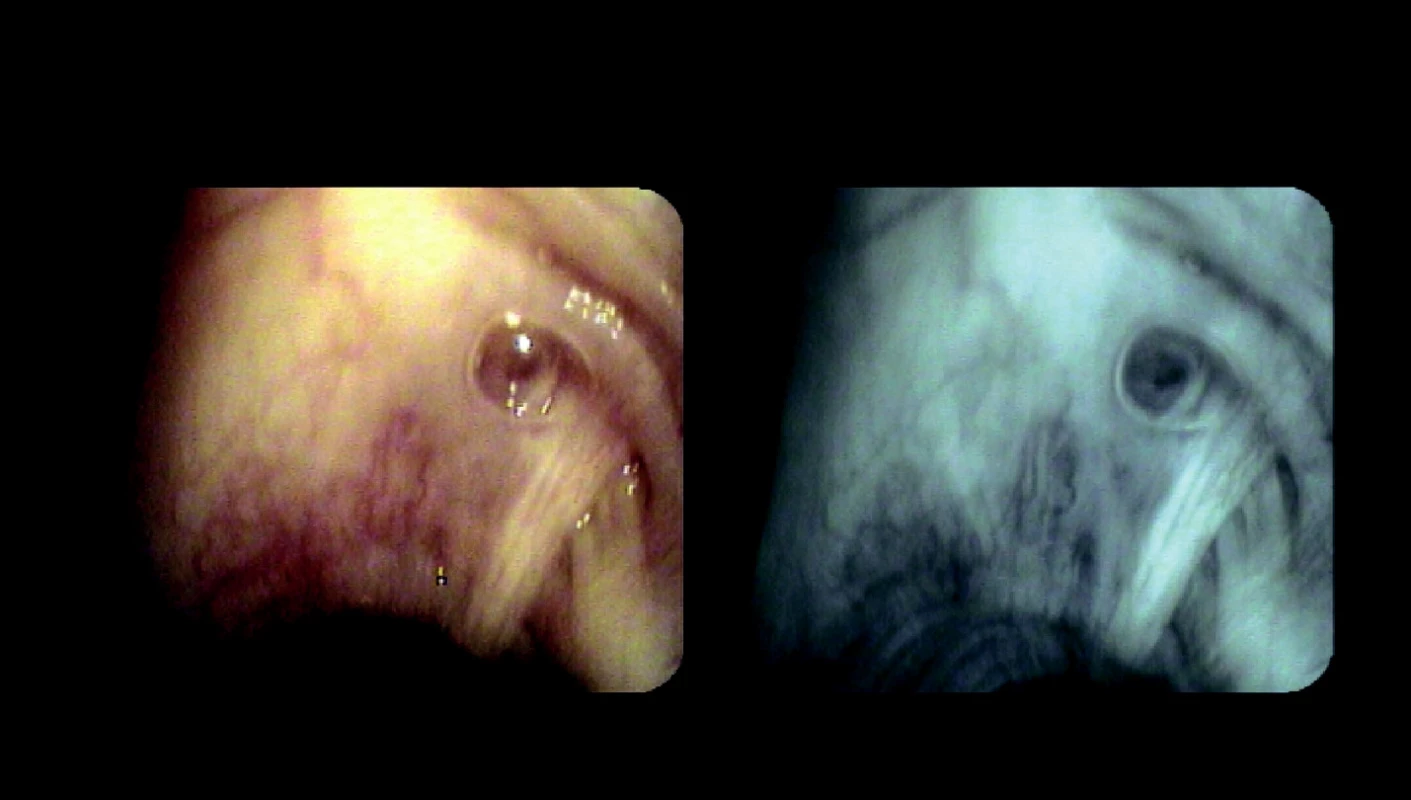
Dle pravidelně aktualizovaného mezinárodního léčebného standardu (GOLD) se doporučení mukolytik (zejména NAC) vymezuje na osoby se středně těžkou či těžkou CHOPN, současně trpící recidivujícími či opakovanými akutními exacerbacemi, a to v nepřítomnosti konkomitantní medikace inhalačními steroidy (26). Jindy velmi střízlivá britská léčebná doporučení však mukoaktivní terapii považují za vhodnou u poněkud méně selektované skupiny nemocných s CHOPN, u všech osob se symptomatickou chronickou hlenovou expektorací (12, 27). V této skupině je možné v již zahájené mukoaktivní terapii pokračovat dlouhodobě, pokud její přidání ke stávající medikaci vedlo k příznivému klinickému efektu (tj. poklesu frekvence kašle a/nebo redukci množství expektorovaného hlenového sekretu). Přechodně podávaná mukoaktivní léčba je dále vhodná u všech nemocných s obtížnou expektorací během akutní exacerbace onemocnění (2, 3, 12, 14, 25).
Tato doporučení byla podpořena některými recentními metaanalýzami (28, 29). U dlouhodobé léčby byl prokázán příznivý efekt na výskyt a klinickou závažnost exacerbací (s redukcí počtu exacerbací, snížením počtu hospitalizačních dnů, poklesem spotřeby antibiotik a snížením celkových výdajů na léčbu) a na kvalitu života (30–32) zejména u nemocných bez chronické inhalační léčby topickými steroidy. U akutních exacerbací pak pozorujeme zlepšení mukociliární clearance, zrychlení eradikace bakterií, redukci zánětlivých markerů a subjektivní redukci symptomů při podávání různých preparátů s mukolytickou, mukokinetickou či mukoregulační povahou (viz tab. 1) (14, 15, 33–36).
Obr. 3. Sliznice zdravého pacienta (A) a pacienta (B) s CHOPN (povšechná retence vazkého hlenu) – obraz v bílém světle a pomocí autofluorescenčního modu bronchoskopu (archiv autorů) 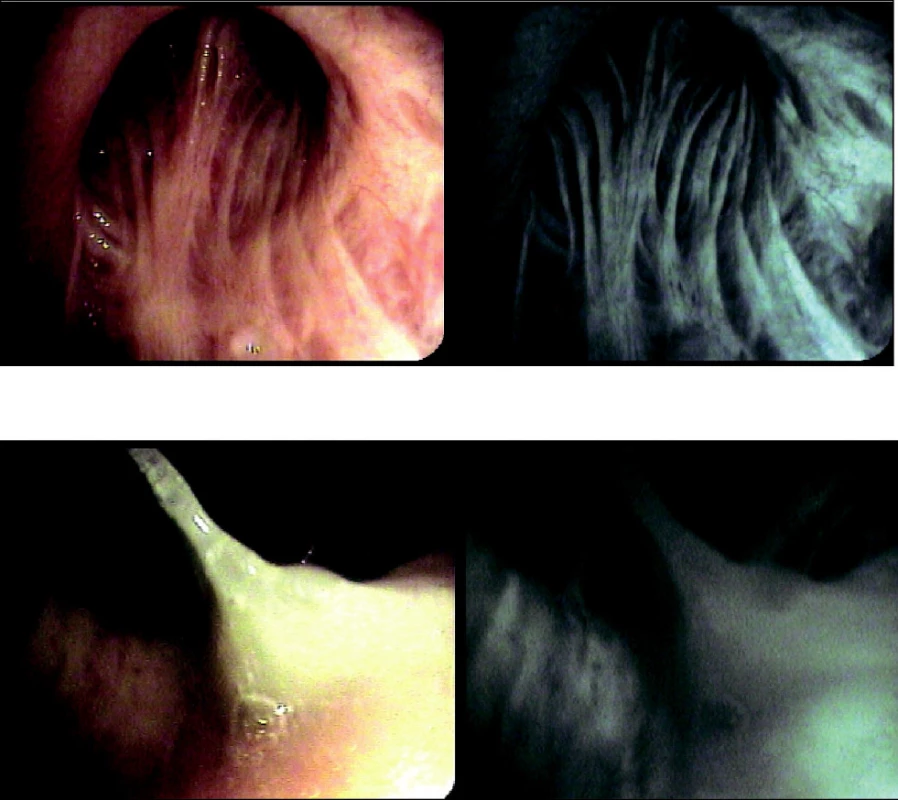
Reálná role ambroxolu v rámci mukoaktivní lékové skupiny
Spektrum mukoaktivních léků je široké. Doporučení GOLD v abecedním pořadí zmiňují:
- ambroxol,
- erdostein,
- karbocystein,
- jodovaný glycerol, a
- NAC.
Ambroxol – hydrochlorid ambroxolu (lék s kombinovanou mukokinetickou a mukolytickou aktivitou) patří v EU stále mezi nejčastěji podáváná mukoaktivní farmaka (spolu s NAC, erdosteinem a bromhexinem). Jedná se o derivát vasicinu (alkaloidu z asijského keře Adhatoda vasica), jehož plný chemický název zní: trans-4-[(2-amino-3,5-dibromo-benzyl)amino] cyklohexanol hydrochlorid. Jeho indikace (spolu s ostatními výše uvedenými farmaky) zahrnuje expektorační fenotyp CHOPN ve středním či těžkém stádiu s opakovanými či prolongovanými exacerbacemi, dále pak akutní exacerbace s obtížnou expektorací vazkého hlenu, stavy retence respiračního sekretu asociované s hrudní chirurgií (resekce) či pneumoniemi. Vzhledem k příznivému působení na pneumocyty II. typu se s podáváním ambroxolu můžeme setkat také při terapii syndromu dechové nedostatečnosti předčasně narozených dětí (zde má však prioritu intratracheálně podávaný animální surfaktant), dále pak jako s aditivním lékem při ARDS dospělých a jako s profylaxí postoperačních atelektáz.
Ambroxol dále zvyšuje antibakteriální efekt současně podávaných antibiotik, například chinolonů v terapií gram-negativních respiračních infekcí (37–38). Relativně novější informací je jeho lokálně znecitlivující (anestetický) efekt při působení na iontové (sodíkové a vápníkové) kanály respirační sliznice (například trachey) a komplexní protizánětlivé působení, jež může býti využitelné například při terapii akutní tracheitidy (16). Standardní dávkování perorálně (tablety či sirup) aplikovaného ambroxolu v péči o dospělé (nad 12 let věku) je
- 30 mg 3x denně,
- 60 mg 2x denně, nebo
- 75 mg v retardované formě 1x denně.
V případě inhalačního ambroxolu doporučujeme 30 mg (4 ml tj.100 kapek roztoku) 3x denně.
Pro intravenózní aplikaci ambroxolu z důvodu ARDS nejsou jasná doporučení. Doba podávání se liší dle indikací:
- cca 5 dnů při akutní tracheitidě,
- 1–2 týdny léčby akutní exacerbaci CHOPN,
- měsíce léčby pacientů s bronchitickým fenotypem CHOPN a s příznivou klinickou reakcí na iniciální podání ambroxolu.
Kontraindikace podávání ambroxolu jsou zcela ojedinělé. Absolutní jsou pouze alergie na látky obsažené v preparátu. Vzhledem ke třem desítkám let používání ambroxolu můžeme zodpovědně říci, že je bezpečný, neboť výskyt nežádoucích účinků je zcela zanedbatelný, a pokud se nějaké vyskytují, jsou klinicky méně závažné a postihují zažívací systém (dyspepsie). Naprosto raritně se můžeme setkat s kontaktní dermatitidou, výskytem anémie, xerostomií či rhinorheou. Nejsou známy žádné farmakokinetické interakce s dalšími konkomitantně podávanými léčivy (35–36, 39–42).
Obr. 4. Řasinkový epitel a zmnožené pohárkové buňky u nemocného s lehčím stádiem CHOPN (A) a těžké destrukční změny povrchu řasinkového epitelu pacienta s těžkým stupněm onemocnění (B) (archiv autorů) 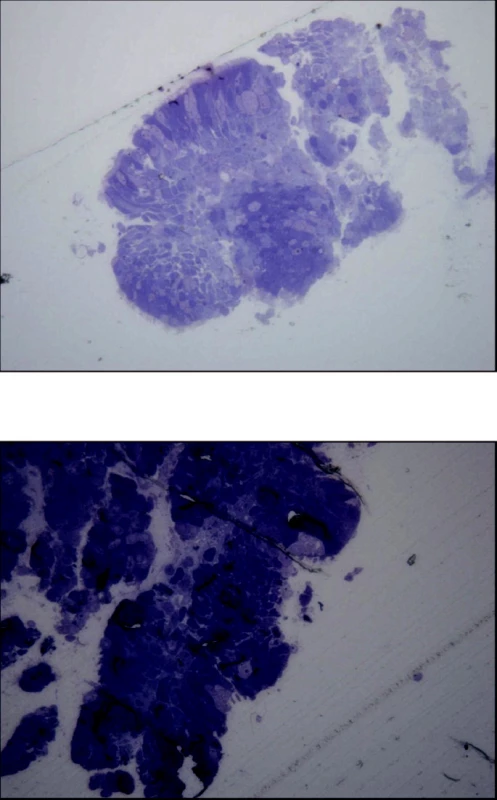
Závěr
Každý případ chronického produktivního kašle u osoby v inhalačním riziku (nejen kouření cigaret, ale i dopravní, profesní a interiérové znečištění ovzduší) je suspektní z přítomnosti prosté chronické bronchitidy, případně bronchitického fenotypu CHOPN. Existuje také řada akutních onemocnění (akutní tracheitida, akutní exacerbace CHOPN, pneumonie) s produktivní expektorací.
V případě nutnosti léčebně ovlivňovat tvorbu a odstraňování respiračního hlenu máme v současnosti k dispozici řadu inhalačních, intravenózních či perorálně aplikovaných léčiv (viz výše). Jejich efektivní používání vyžaduje cílenou indikaci a pečlivé monitorování efektu.
I když je stran indikací mukoaktivní medikace stále více otázek než odpovědí, můžeme ji doporučit jako aditivní medikaci u expektoračního (bronchitického) fenotypu CHOPN pro jedince se středně těžkou či těžkou formou onemocnění, pokud současně trpí recidivujícími či opakovanými akutními exacerbacemi, a to zejména v nepřítomnosti konkomitantní medikace inhalačními steroidy, u symptomatických bronchiektázií, během akutních respiračních infektů (akutní tracheitida či tracheobronchitida) s obtížnou expektorací, případně v pooperačním období (po resekcích plic, případně jiných operacích hrudníku a horní části břicha). Ve všech těchto indikacích v ČR používáme nejčastěji následující preparáty:
- ambroxol,
- bromhexin,
- erdostein, a
- N-acetylcystein.
Jejich benefit je srovnatelný.
Zcela nezastupitelnou roli ve skupině mukoaktivních léčiv mají modifikátory iontového transportu a peptidová mukolytika (a-dornáza) u pacientů s plicním postižením při cystické fibróze.
V klinické praxi se v rámci mukoaktivní farmakoterapie bohužel běžně setkáváme s mnoha chybami: tj. s nedostatečnou, nadměrnou či neadekvátní indikací mukoaktivní medikace, někdy i se zcela iracionální kombinaci antitusik a mukoaktivních léků.
Pokud náš stručný přehled (zaměřený nejenom na v titulu uvedený ambroxol) bude pro někoho určitým vodítkem, budeme velmi rádi. Na závěr je třeba konstatovat, že další klinické studie se současnými mukoaktivními léky i s jejich potenciálními nástupci stále probíhají a jejich závěry možná výrazně ovlivní naše budoucí léčebná doporučení.
MUDr. Vladimír Koblížek
Pneumologická klinika FN
Hradec Králové
Sokolská 581
500 12 Hradec Králové
E-mail: koblivla@fnhk.cz
Zdroje
1. Houtmeyers, E. Gosselink, R., Gayan-Ramirez, G. et al. Regulation of mucociliary clearance in health and disease. ERJ 1999, 13, p. 1177-1188.
2. Rogers, D.F. The role of airway secretions in COPD: pathophysiology, epidemiology and pharmacotherapeutic options. COPD 2005,; 2, p. 341-353.
3. Rogers, D.F. Airway Mucus Secretion. In: Barnes PJ. Chronic Obstructive Pulmonary Disease (Cellular and Molecular Machanisms). Boca Raton: Taylor & Francis 2005, p. 83-111.
4. Agnew, J.E., Little, F., Pavia, D., Clarke, S.W. Mucus clearance from the airways in chronic bronchitis – smokers and ex-smokers. Bull. Eur. Phsiopathol. Respir. 1982, 18, p. 473-484.
5. Prescott, E., Lange, P., Vestbo, J. Chronic mucus hypersecretion in COPD and death from pulmonary infection. ERJ 1995, 8, p. 1333-1338.
6. Wanner, A., Salathe, M., O´Riordan, T.G. Mucociliary clearance in the airways. AJRCCM 1996,; 154, p. 1868-1902.
7. Giembytcz, M.A. Mucolytics pharmacotherapy for COPD. In: Rennard SI et al. Clinical management of chronic obstructive pulmonary disease. 2nd ed. New York: Informa Healthcare 2007, p. 339-341.
8. Davies, J.R., Hermann, A., Russell, W. et al. Respiratory tract mucins: structure and expression patterns. In: Mucus hypersecretion in respiratory disease, No. 248. Chichester: John Wiley & Sons 2002, p. 76-88.
9. Kirkham, S., Sheehan, J.K., Knight, D. et al. Heterogenity of airways mucus: variations in the amounts and glycoforms of the major oligomeric mucins MUC5AC ad MUC5B. Biochem. J. 2002, 361, p. 542-553.
10. Hogg, J.C. Pathophysilogy of airflow limitation in COPD. Lancet 2004, 364, p. 709-721.
11. Caramori, G., Di, G.C., Carlstedt, I. et al. Mucin expression in peripheral airways of patiens with chronic obstructive ulmonary disease. Histopathology 2004, 45, p. 477-484.
12. Rogers, D.F., Barnes, P.J. Treatment of airway mucus hyper-sectretion. Ann. Med. 2006, 38, p. 116-125.
13. Henke, M.O., Shah, S.A., Rubin, B.K. The role of airway secretion in COPD – clinical applications. COPD 2005, 2, p. 377-390.
14. Rubin, B.K. Mucolytics, expectorants and mucokinetics medications. Respir. Care 2007, 52, p. 859-865.
15. Koblížek, V., Tomšová, M. a kol. Mukoaktivní léky. Stud. Pneumol. Phthiseol. 2007, 67, s. 18-23.
16. Beeh, K.M., Beier, J., Esperester, A., Paul, L.D. Antiinflammatory properties of ambroxol. Eur. J. Med. Res. 2008, 13, p. 557-562.
17. Janssens, W., Decramer, M. Use of bronchodilators and mucolytics at COPD exacerbations. In: Wedzicha JA, Martinez FJ. Chronic obstructive pulmonary disease exacerbations. New York: Informa Healthcare 2009, p. 203-238.
18. Halbert, R.J., Natoli, J.L., Gano, A. et al. Global burden of COPD: systematic review and meta-analysis. ERJ 2006, 28, 523-532.
19. World Health Organization. Chronic respiratory disease: Burden (2007) [on line]. Dostupné na http://who.int/respiratory/copd/burden/en/index.html.
20. The Global Initiative for Chronic Obstructive Lung Disease (GOLD). Global strategy for diagnosis, management, and prevention of COPD [on line]. Dostupné na http://www.goldcopd.com/ Guidelineitem.asp?l1=2&l2=1&intId=2003.
21. Vestbo, J. Epidemiological studies in mucus hypersecretion. Novartis Found Symp. 2002, 248, p. 3-12.
22. Koblížek, V., Salajka, F., Čermáková, E. a kol. Vztah mezi kvalitou života a BODE indexem u bývalých kuřáků ve stabilní fázi chronické obstrukční plicní nemoci (Ciliární studie). Vnitřní lékařství 2009, 10 (v tisku).
23. Rogers, D.F. Mucus pathophysiology in COPD: differences to astma, and pharmacotherapy. Monaldi Arch. Chest. Dis. 2000, 55, p. 324-332.
24. Anthonisen, N.R. Bacteria and exacerbation of COPD. NEJM 2002, 347, p. 526-527.
25. Rogers, D.F. Mucoactive drugs for astma and COPD: any place in therapy? Expert Opin. Investig. Drugs 2002, 11, p. 15-35.
26. Rabe, K.F., Hurd, S., Anzueto, A. et al. Global strategy for the diagnosis, management and prevention of chronic obstructive pulmonary disease: GOLD executive summary. AJRCCM 2007, 176, p. 532-555.
27. National Institute for Clinical Excellence (NICE). Chronic obstructive pulmonary disease. National clinical guideline on management of chronic obstructive pulmonary disease in adults in primary and secondary care – Managing stable COPD. Thorax 2004, 59,, p. 139-130.
28. Poole, P.J. Black, P.N. Mucolytic agents for chronic bronchitis or chronic obstructive pulmonary disease. Cochrane Database Syst, Rev. 2003, CD001287.
29. Poole, P.J., Black, P.N. Mucolytic agents for chronic bronchitis or chronic obstructive pulmonary disease. Cochrane Database Syst. Rev. 2006, CD001287.
30. Gerrits, C.M., Herings, R.M., Leufkens, H.G. et al. N-acetylcysteine reduces the risk of re - hospitalisation among patients with chronic obstructive pulmonary disease. ERJ 2003, 21, p. 795-798.
Štítky
Praktické lékařství pro děti a dorost Praktické lékařství pro dospělé
Článek Jmenování nových profesorůČlánek Velký mezonČlánek NÁZORČlánek NÁZORČlánek Co píše o alkoholu LancetČlánek Jubilea
Článek vyšel v časopisePraktický lékař
Nejčtenější tento týden
2009 Číslo 10- Na inkontinenční pomůcky nově dosáhne více pacientů
- Naděje budí časná diagnostika Parkinsonovy choroby založená na pachu kůže
- Pacient se bude cítit komfortně pouze při správně zvolené absorpční pomůcce
- Úloha praktického lékaře v péči o inkontinentní pacienty
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
-
Všechny články tohoto čísla
- Posuzování zdravotního stavu a pracovní schopnosti u onkologicky nemocných
- Ambulantní flebektomie u trombofilních pacientů
- Dříve vyslovená přání (advance directives) v USA
- Patofyziologie, symptomatologie a diagnostika hyperaktivního močového měchýře
- Jmenování nových profesorů
- Vrozené poruchy sexuálního vývoje (DSD) a jejich následky
- Skupinová kognitivně behaviorální terapie obezity v primární prevenci metabolického syndromu
- Terapeutická role ambroxolu v léčebném ovlivňování mukociliární clearance u „bronchitického fenotypu“ CHOPN
- Léčba rekombinantním humánním erytropoetinem
- Zpráva WHO o úmrtích při dopravních nehodách
- Akreditace ordinací všeobecných praktických lékařů v České republice
- Mikrometastáza v sentinelové uzlině – nutnost disekce axilárních uzlin?
- Neobvyklý případ závislosti na více psychoaktivních látkách
- Občanský průkaz při poskytování zdravotní péče
- Miniportréty slavných českých lékařů
- Velký mezon
- Enzym ozdobený Nobelovou cenou
- Ceny Josefa Hlávky za rok 2008
- NÁZOR
- NÁZOR
- Co píše o alkoholu Lancet
- Jubilea
- Praktický lékař
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Občanský průkaz při poskytování zdravotní péče
- Léčba rekombinantním humánním erytropoetinem
- Vrozené poruchy sexuálního vývoje (DSD) a jejich následky
- Akreditace ordinací všeobecných praktických lékařů v České republice
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



