-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaMožnosti terapie onychomykózy nízkoteplotním plazmatem
Therapy of Onychomycosis Using the Non-thermal Plasma
Inactivation of fungi including dermatophytes by the action of non-thermal plasma has already been verified by numerous in vitro and in vivo studies. Feasibility of this simple and cheap method for therapy of human onychomycosis is documented here on clinical case reports.
Keywords:
dermatophytes – cometary discharge – nonthermal plasma – tinea unguium
Autoři: J. Lux 1,2; R. Dobiáš 3,4; V. Scholtz 5; J. Khun 5; H. Soušková 6; E. Mrázková 1; J. Julák 7
Působiště autorů: Ústav epidemiologie a ochrany veřejného zdraví, Lékařská fakulta Ostravské univerzity, Ostrava, Vedoucí ústavu doc. MUDr. Rastislav Maďar, Ph. D., MBA, FRCPS 1; Podiatrické centrum Medicia Ostrava, Ostrava, vedoucí pracoviště MUDr. Jaroslav Lux 2; Oddělení bakteriologie a mykologie, Centrum klinických laboratoří, Zdravotní ústav se sídlem v Ostravě, Ostrava, vedoucí oddělení RNDr. Vladislav Holec 3; Ústav mikrobiologie, Lékařská fakulta Univerzity Palackého v Olomouci, Olomouc, přednosta ústavu prof. MUDr. Milan Kolář, Ph. D. 4; Ústav fyziky a měřicí techniky Fakulty chemicko-inženýrské, VŠCHT Praha, vedoucí ústavu doc. Ing. Jaroslav Hofmann, CSc. 5; Ústav počítačové a řídicí techniky Fakulty chemicko-inženýrské, VŠCHT Praha, vedoucí ústavu doc. Ing. Jan Mareš, Ph. D. 6; Ústav imunologie a mikrobiologie, 1. lékařská fakulta, Univerzita Karlova a Všeobecná fakultní nemocnice, Praha, přednostka ústavu prof. RNDr. Libuše Kolářová, CSc. 7
Vyšlo v časopise: Čes-slov Derm, 93, 2018, No. 6, p. 266-271
Kategorie: Novinky v medicíně
Souhrn
Inaktivace vláknitých hub včetně dermatofytů aplikací nízkoteplotního plazmatu byla již dříve prokázána řadou experimetálních in vitro i in vivo studií. V tomto příspěvku je na klinických případech doložena použitelnost této jednoduché a levné metody pro léčbu lidské onychomykózy.
Klíčová slova:
dermatofyty – kometární výboj – nízkoteplotní plazma
ÚVOD
Onychomykóza (tinea unguium) je mykotické postižení nehtů, nehtových plotének nebo nehtových lůžek. Vyskytuje se téměř u 10 % populace (podle některých průzkumů i více než 20 % populace). Jedná se sice o méně nebezpečné onemocnění, které je ovšem nepříjemné, život komplikující a s možnými psychosociálními důsledky. Možné jsou též komplikace, zejména u diabetiků a imunokompromitovaných pacientů, vzácnou komplikací může být osteomyelitida (viz např. Scher et al. [29]). Nejčastějšími původci onychomykóz jsou mikroskopické vláknité houby řazené mezi dermatofyty, zejména Trichophyton rubrum, méně často též T. interdigitale, T. violaceum, Epidermophyton floccosum, Nannizzia gypsea (dříve Microsporum gypseum) a řada dalších. Častá jsou podobná postižení způsobená kvasinkami, hlavně v tropických oblastech pak i nedermatofytickými vláknitými houbami.
Pro terapii lehčích forem onychomykózy se obvykle používá lokální aplikace preparátů jako terbinafin, itrakonazol, efinakonazol, ciclopirox, amorolfin nebo polyhexamethylen biguanid. Možné je i perorální podávání antimykotik, např. terbinafinu nebo flukonazolu. Musí být aplikovány v krátkých, typicky každodenních intervalech a po dlouhou dobu až 1 roku; přesto je účinnost těchto preparátů nejistá, za úspěch bývá považován terapeutický efekt ve více než 50 % případů. Podrobnější přehledy uvádějí např. Roberts et al. [15], Elewski [4], Ghannoum a Isham [5] nebo Gupta et al. [6]. Pomocnou terapií bývá i pedikérský zákrok spočívající v odstranění postižených částí nehtu.
Kromě klasické terapie antimykotiky se objevily i pokusy o aplikaci různých fyzikálních metod, např. ohřevu nehtového lůžka na cca 40–50 °C Nd:YAG laserem. Tato nadějná metoda se ovšem ukázala jako málo účinná a spolehlivá [1]. Možnosti dalších metod (fotodynamická terapie, iontoforéza, ultrazvuk) uvádějí Ghannoum a Isham [5], jejich praktické použití je ovšem hodnoceno spíše skepticky. Fotodynamická terapie se ovšem ukázala jako poměrně úspěšná (v 60 % případů) v kombinaci s nanoemulzemi [14]. Nověji se objevují i zprávy o aplikaci nízkoteplotního plazmatu.
Nízkoteplotní plazma (NTP, non-thermal plasma, low--temperature plasma či cold plasma) je částečně ionizovaný plyn, v němž jsou přítomny volné ionty o teplotě okolí a vysokoteplotní volné elektrony, které díky své malé hmotnosti nezvyšují teplotu celého plazmatu. Toto plazma je poměrně snadno připravitelné působením elektrických výbojů stejnosměrného, střídavého a vysokofrekvenčního vysokého napětí. Obvyklými zdroji plazmatu jsou koronové výboje, dielektrický bariérový výboj (DBD), klouzavý výboj, elektrospray, tzv. plasma jet zvaný též plazmatická tužka atd. Přehled uvádí např. Tendero et al. [27]. Nízkoteplotní plazma se používá nejen v řadě inženýrských oborů, ale i v biologických aplikacích, kde je podstatou jeho účinku tvorba reaktivních částic (iontů, radikálů, atomárního a singletového kyslíku aj.) i stabilních molekul (peroxidu vodíku, ozonu aj.), shrnovaných pod názvy reactive oxygen species (ROS) a reactive nitrogen species (RNS). Na jejich přítomnosti je založeno použití plazmatu v biotechnologiích (přehled viz [22]), kde je využívána hlavně jeho schopnost dezinfekce a sterilizace [3]. V lékařských oborech se plazma využívá k urychlování hojení ran [7, 13], v dermatologii [8], v zubním lékařství [9], jakož i v onkologii [16]. Různé zdroje plazmatu (plasma jet, surface microdischarge a dielektrický bariérový výboj) pro eradikaci T. rubrum jako původce onychomykózy studovali na modelu kravského kopyta Xiong et al. [28]. Citlivost řady dalších původců testovali pomocí plasma jet také Daeschlein et al. [2]. V současné době probíhá několik klinických studií terapie humánní onychomykózy pomocí nízkoteplotního plazmatu (odkazy viz Literatura, Klinické studie). Jejich výsledky nebyly v době vzniku tohoto sdělení ještě známy. Metodicky je zajímavý rozdílný přístup k frekvenci terapeutických aplikací plazmatu. V jednotlivých studiích jsou uváděna dávkování:
- 20 minut jednou týdně po dobu tří týdnů;
- tři dávky týdně po dobu 14 dnů, pak jednou měsíčně (doba expozice nespecifikována);
- tři expozice trvající 45 minut během jednoho týdne.
Nověji byl popsán též tzv. kometární výboj s některými výhodnými vlastnostmi [20, 21]. Jeho mikrobicidní účinek může být zlepšen vložením kovové mřížky do hlavice jeho zdroje [17]. Jedná se o stejnosměrný vysokonapěťový výboj typu koronového výboje, projevující se směrovaným proudem aktivních částic tryskajícím z kladné elektrody. Vzhledem i účinky připomíná často používaný plasma jet, oproti němu však nepotřebuje přídavný zdroj nosného plynu. Kromě baktericidního účinku je též významný jeho účinek fungicidní, srovnatelný s jinými zdroji plazmatu [24, 11]. Schematické uspořádání ručního přístroje produkujícího kometární výboj je uvedeno na obrázku 1, skutečná situace při jeho použití pak na obrázku 2.
Obr. 1. Schéma aparatury pro generaci kometárního výboje 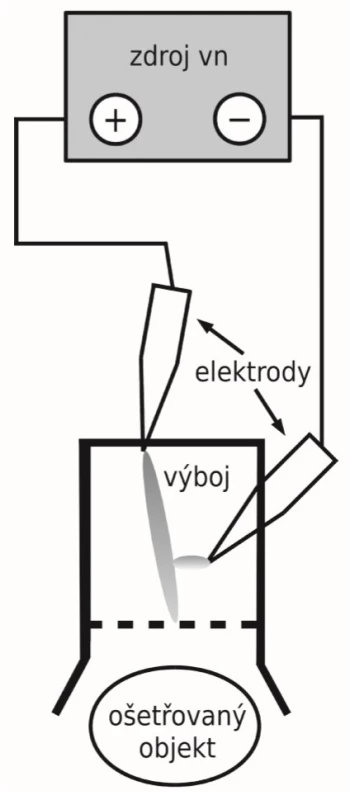
Obr. 2. Fotografie přístroje při expozici postižené končetiny nízkoteplotním plazmatem 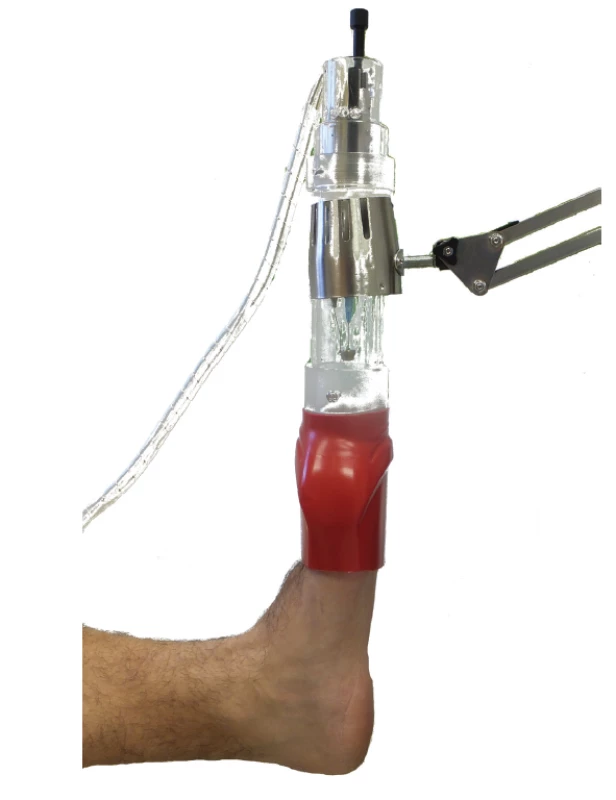
Zdroj plazmatu, schematicky znázorněný na obrázku 1, je uzavřen v plexisklovém pouzdře a upevněn v teleskopickém držáku. Prsty exponované nohy jsou uzavřeny v plastovém obalu. Naše in vitro studie dezinfekčních účinků plazmatu prokázaly obecně menší citlivost vláknitých hub: jejich inaktivace bylo dosaženo po expozici v řádu desítek minut, zatímco bakterie bývají inaktivovány někdy i po expozici kratší než jedna minuta. Významné jsou rozdíly v citlivosti různých rodů a druhů, kdy některé jsou inaktivovány již po několika minutách, zatímco jiné přežívají i expozice delší než 40 minut. Tak např. byly za srovnatelných podmínek kompletně inaktivovány všechny kmeny druhů T. rubrum a T. interdigitale po 25 minutách expozice, zatímco u druhů T. benhamiae (dříve Arthroderma benhamiae) a Nannizzia gypsea byl kompletně inaktivován jen jeden ze tří testovaných kmenů. Podrobněji uvádějí výsledky těchto in vitro studií Soušková et al. [23, 25] a Scholtz et al. [18].
Ve studiích in vivo byla mj. prokázána schopnost kometárního výboje dezinfikovat fyziologickou bakteriální mikroflóru lidské pokožky během jednorázové desetiminutové expozice [10]. Možnost terapie kožní dermatofytózy byla prokázána na morčatech experimentálně infikovaných T. mentagrophytes: po desetiminutových expozicích kometárním výbojem, aplikovaných ve dvou - až třídenních intervalech, bylo zjištěno vymizení objektivních příznaků, v kožních stěrech pak byl nalezen významný pokles infekčních zárodků a jejich úplné vymizení o týden dříve než u neléčených zvířat. Nebyly zjištěny žádné vedlejší účinky této terapie [19, 12]. Terapeutický účinek plazmatu byl ověřen i na klinickém případu dvacetileté studentky, postižené kožním onemocněním v levém horním kvadrantu hrudníku: kruhová léze o průměru cca 7 cm byla poseta drobnými pustulkami a měla typický vzhled tiney corporis. Z léze byl izolován T. interdigitale, pacientka se na vlastní riziko rozhodla pro autoléčbu kometárním výbojem. Na exponované polovině léze se každodenní desetiminutovou expozicí podařilo potlačit jak objektivní příznaky, tak i svědění. Množství infekčních šupin bylo mnohem menší v ošetřované části léze a patogen dříve vymizel v porovnání s neexponovanou polovinou léze použité jako kontrola (podrobněji viz [26]).
POPISY PŘÍPADŮ
V současné době probíhá klinická studie na pacientech postižených onychomykózou a léčených v Podiatrickém centru Medicia Ostrava. Z deseti prozatím léčených pacientů uvádíme dále kazuistiky dvou pacientů, u nichž je již možno léčebný efekt hodnotit. V obou případech bylo aplikováno nízkoteplotní plazma produkované na bázi kometárního výboje popsaného v Úvodu. V jednom případě předcházela aplikaci plazmatu neúspěšná konvenční léčba. Schematické znázornění aparatury pro generaci kometárního výboje a fotografie přístroje při expozici postižené končetiny jsou uvedeny na obrázcích 1 a 2.
Případ 1
Pacientka (žena, 68 let) se poprvé dostavila do ambulance kožního lékaře v lednu 2015 se suspektní onychomykózou dolních končetin. V anamnéze se vyskytoval diabetes mellitus prvního typu, ischemická choroba dolních končetin, hypertenze a hypercholesterémie. Při vyšetření byly nehtové ploténky palců nohou žlutě diskolorované, patrné mohutné hyperkeratózy (tinea hyperkeratotica), v meziprstí nohou se nacházely deskvamace a ve čtvrtém meziprstí vlevo ragáda. Mikroskopické vyšetření podnehtové drti bylo pozitivní na dermatofytická vlákna, kultivačně byl identifikován původce T. rubrum. Pacientce byla indikována terapie mytí nohou roztokem hexamidini diisetionas, chlorhexidini digluconatis, chlorcresolum, 1krát 250 ml a v meziprstí krémem cyclopiroxum olaminum 2krát denně, dále byla indikována chemická ablace nehtů 40% ureou a následné ošetření změklých nehtů na pedikúře.
Po roce, v lednu 2016, se lokální nález pouze mírně zlepšil. Meziprstí bylo bez ragád. Terapie nehtů pokračovala krémem cyclopiroxum olaminum 2krát denně a pro změkčení nehtů byla indikována 40% urea mast 2krát týdně. Celková antimykotická terapie nebyla použita kvůli rizikům interakcí s dalšími užívanými léky (metoprololi tartras). Po šesti týdnech vykazovaly nehtové ploténky podnehtové hyperkeratózy a žlutou diskoloraci, v proximální třetině nehtová ploténka slabě odrůstala. Terapie byla eskalována aplikací laku amorolfini hydrochloridum na postižené nehty obou palců 2krát týdně, na ostatní nehty byl aplikován 2krát denně krém cyclopiroxum olaminum a také bylo doporučeno ztenčovat nehty pilováním.
Po následujících sedmi týdnech se stav postižených nehtů nezměnil, ale terapie zůstávala beze změny. Po dalších osmi týdnech zůstával stav stále nezměněn, navíc se vyskytovala hyperkeratóza s drolením. Vzhledem k dlouhodobé lokální terapii onychomykózy i s rizikem možných lékových interakcí byla indikována terapie terbinafinem v redukované dávce 125 mg každé 2 dny po dobu dvou týdnů, pak 125 mg jedenkrát denně.
Ke kontrole se pacientka dostavila po 4 týdnech. Terapii terbinafinem snášela dobře. Proximálně, na nehtových ploténkách obou palců byl patrný odrůst cca 2 mm. Terapie zůstávala nezměněna, po dalších šesti týdnech odrůstaly nehtové ploténky palců do poloviny a u ostatních nehtů docházelo ke zhrubění distálních okrajů. Následovala stejná terapie, ale po šesti týdnech byly vzorky nehtů stále pozitivní na dermatofytická vlákna.
Pacientka souhlasila s aplikací nízkoteplotního plazmatu (NTP) na postižené nehty. Těsně před první aplikací NTP v říjnu 2016 vykazovaly distální části nehtových plotének drolení a proximálně odrůst zdravé části o cca 3 až 4 mm. Nehtové ploténky ostatních prstů byly distálně rovněž postiženy onychomykózou v různém rozsahu. Tento stav je demonstrován na obrázku 3a.
Obr. 3. a. Palce obou dolních končetin před aplikací NTP: hyperkeratóza distálních částí nehtových plotének s drolením, zdravá proximální část ploténky cca 3–4 mm
Nehtové ploténky ostatních prstů distálně rovněž postiženy onychomykózou v různém rozsahu.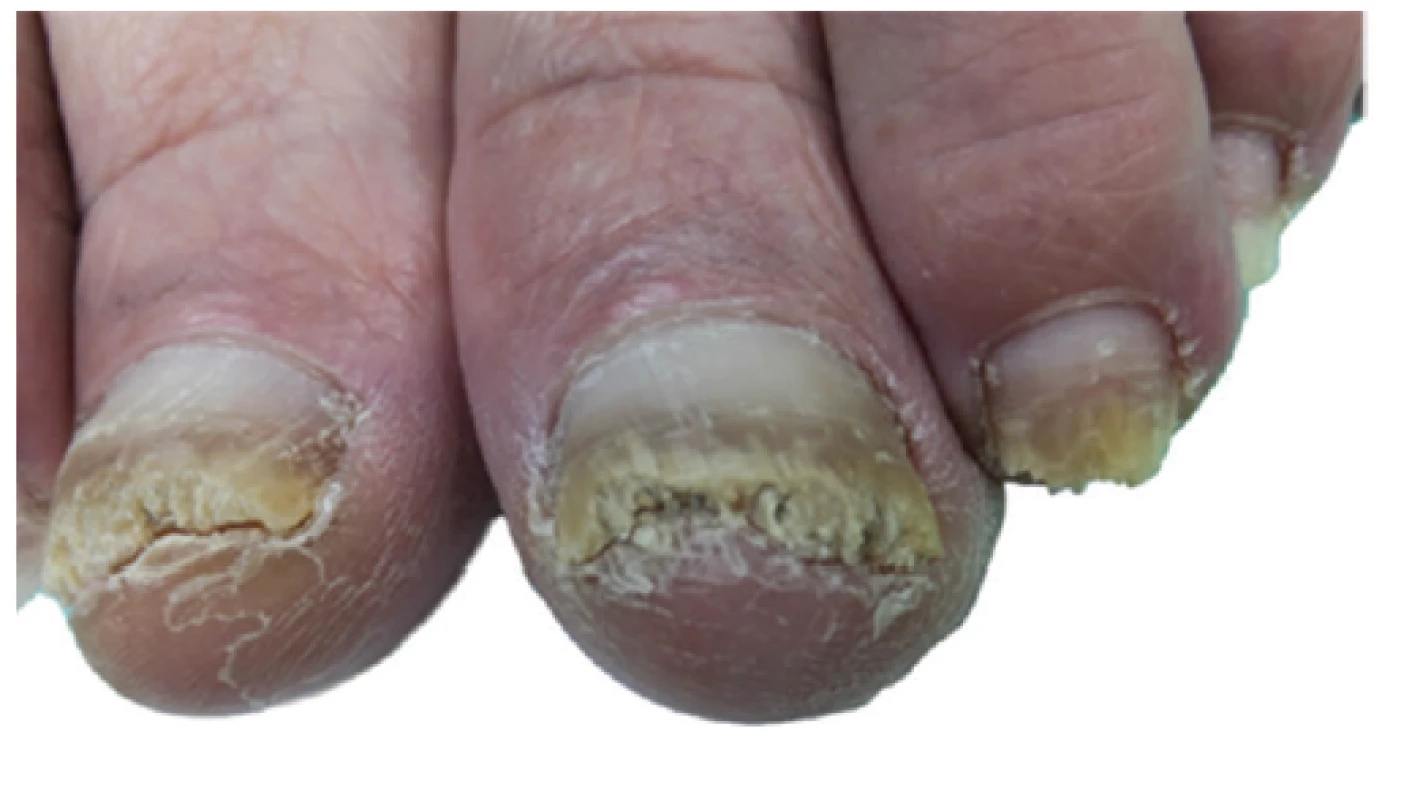
Od tohoto stavu do konce března 2017 absolvovala pacientka 16 aplikací NTP s expozicí vždy dvacet minut. Při kontrole v červnu 2017 byly nehtové ploténky obou palců dolních končetin na distálních stranách bez hyperkeratóz s odrůstáním nehtové ploténky do půl až dvou třetin délky. Ostatní nehty nevykazovaly mykotické změny (obr. 3b). Odebrané vzorky nehtů byly negativní na přítomnost původce dermatomykózy stanovované mikroskopicky, přímou detekcí ribozomální DNA a kultivačně.
Obr. 3b. Nehtové ploténky palců obou dolních končetin po sedmi měsících od první aplikace NTP: bez hyperkeratóz na distálních stranách, odrůst nehtové ploténky do půl až dvou třetin délky
Ostatní nehty bez mykotických změn.
Případ 2
Pacient (74 let) se poprvé dostavil v listopadu 2015 do podiatrické ambulance na doporučení diabetologa pro zarůstání mediální hrany nehtové ploténky palce levé nohy. V anamnéze se vyskytoval diabetes mellitus prvního typu, před 50 lety podstoupil ablaci nehtu palce levé dolní končetiny pro zarůstání. Při vyšetření byly na distální hraně nehtové ploténky patrné nerovné okraje se známkami hyperkeratózy mykotického vzhledu. Na mediální straně nehtové ploténky se vyskytovaly známky rozštěpu, pravděpodobně jako důsledek dřívějšího chirurgického ošetření (obr. 4a). Pacient nepodstoupil před tímto vyšetřením žádnou konvenční terapii onychomykózy.
Obr. 4. a. Nehty dolní končetiny před aplikací NTP: postižení nehtové ploténky v celém rozsahu, volný okraj nehtu nerovný, se známkami hyperkeratózy a drolení, na mediální straně nehtové ploténky se vyskytují známky rozštěpu a zarůstání 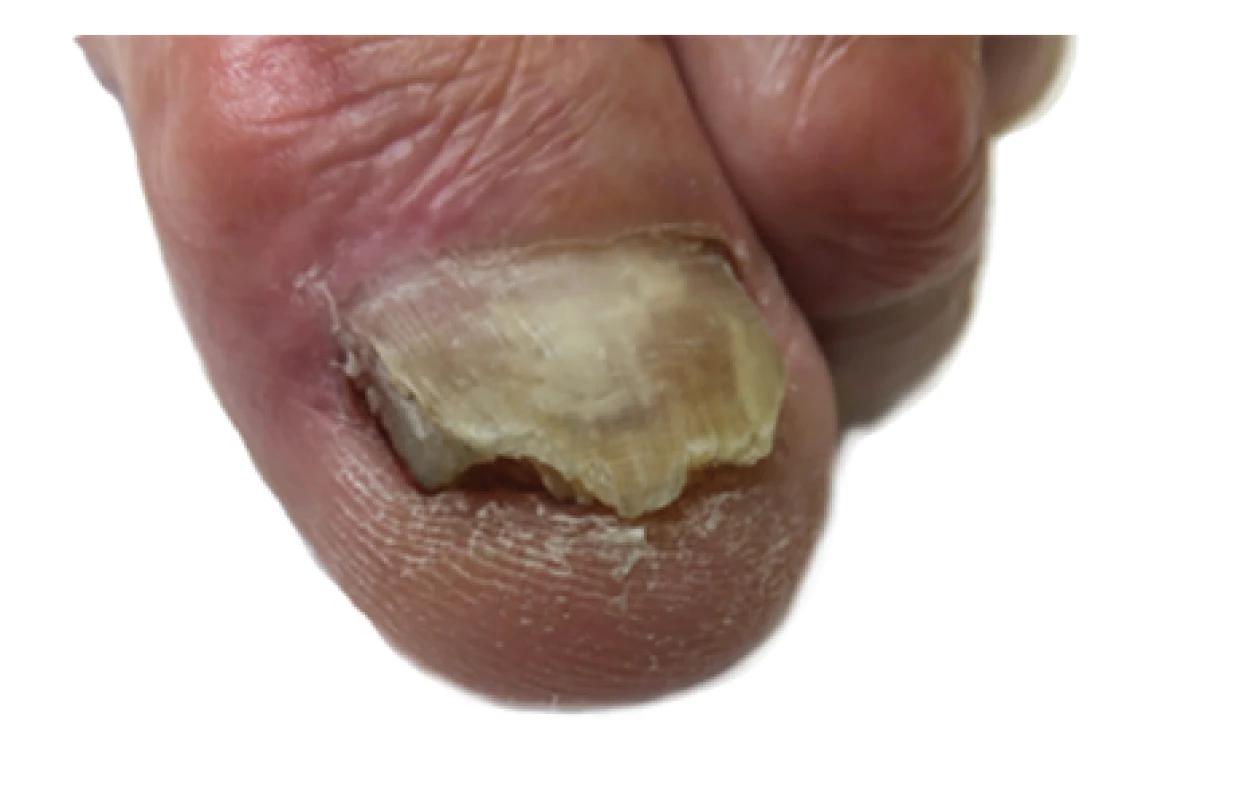
V říjnu 2016 bylo mikroskopické vyšetření vzorku nehtů pozitivní na dermatofytická vlákna, kultivačně byl identifikován původce T. interdigitale.
V listopadu 2016 byla zahájena aplikace NTP a do března 2017 pacient absolvoval 16 aplikací NTP s expozicí vždy po 20 minutách. Zarůstající pahýl nehtové ploténky na mediální straně byl zároveň ošetřen, elevován a zpevněn speciálním akrylem.
Při kontrole po šesti měsících od první aplikace NTP byly odebrané vzorky nehtů negativní na přítomnost původce dermatomykózy stanovované mikroskopicky, přímou detekcí ribozomální DNA i kultivačně. Odrůstající nehtová ploténka byla patrná z proximální strany po celé bázi v délce cca 5–6 mm. Nehet měl v distální části rovné okraje bez hyperkeratóz (obr. 4b).
Obr. 4b. Nehty dolní končetiny při kontrole po šesti měsících od první aplikace NTP
Proximálně je po celé bázi patrná odrůstající zdravá nehtová ploténka v délce cca 5–6 mm. Nehet má v distální části rovné okraje bez hyperkeratóz. Mediální hrana nehtu je elevována korekcí zarůstajícího nehtu a shora fixována speciálním akrylem.
DISKUSE
Studie in vitro [18, 23, 25], citované v Úvodu, ukázaly poměrně dobrou citlivost hub k nízkoteplotnímu plazmatu, jehož aplikace způsobovala jejich inaktivaci jak ve vodné suspenzi, tak i na polotuhých kultivačních půdách. Tato inaktivace ovšem není bez problémů: na rozdíl od dobře citlivých bakterií vyžadují např. kvasinky k inaktivaci obecně delší dobu expozice, tato doba je ještě delší v případě vláknitých hub. Přestože se aplikací NTP dařilo koncentraci spor některých druhů, respektive kmenů snížit, nedařilo se je v rozumné době kompletně inaktivovat. Pro zde uváděnou aplikaci je příznivé, že původci dermatomykóz vykazovali v experimentálních studiích zpravidla dobrou citlivost na NTP. To platí i pro studie in vivo provedené na zvířecím modelu i na lidských pacientech [12, 19, 26].
Předložené výsledky jsou jen dílčí etapou v dlouhodobém sledování účinnosti aplikace nízkoteplotního plazmatu na terapii onychomykózy, nicméně je považujeme za nadějné, v čemž nás podporují i dílčí výsledky terapie zde dosud neuvedených pacientů. Terapeutický efekt NTP považujeme za prokázaný jak u pacienta po neúspěšné konvenční terapii, tak i u pacienta dosud neléčeného. Další výsledky této klinické studie budou publikovány po skončení její další etapy.
Předmětem dalšího studia budou jak optimalizace jeho fyzikálních parametrů, tak i jeho aplikační schéma. Terapeutický efekt by se mohl zlepšit při častější aplikaci plazmatu, neumožňující regeneraci infekčního agens v době mezi jednotlivými expozicemi. V předchozím terapeutickém experimentu [26] se osvědčila každodenně opakovaná aplikace; toto schéma ovšem v našem případě naráží na organizační a technické potíže. Dávkování plazmatu je dosud nevyřešený problém, jak dokládají výrazné rozdíly v aplikačních schématech výše citovaných klinických studií.
Klinické studie
Pilot Study to Evaluate Plasma Treatment of Onychomycosis. US National Library of Medicine, ClinicalTrials.gov identifier: NCT01819051. First Posted 2013. Dostupné na www: https://clinicaltrials.gov/ct2/show/NCT01819051.
Evaluating the Safety, Tolerability and Preliminary Efficacy of Plasma in Improving the Appearance of Onychomycosis. US National Library of Medicine, ClinicalTrials.gov Identifier: NCT02724384. First Posted 2016.
Dostupné na www: https://clinicaltrials.gov/ct2/show/NCT02724384?recrs=ab&cond=Onychomycosis&cntry1=NA%3AUS&draw=1&rank=10.
Early Feasibility Study to Evaluate the Efficacy of the RenewalNail™ Plasma Treatment System in Patients With Onychomycosis (Fungal Nail). US National Library of Medicine, ClinicalTrials.gov Identifier: NCT03216200. First Posted 2017.
Dostupné na www: https://clinicaltrials.gov/ct2/show/NCT03216200?recrs=ab&cond=Onychomycosis&cntry1=NA%3AUS&draw=1&rank=3.
Poděkování
Studie byla podpořena projektem Ministerstva zdravotnictví České republiky AZV 17-31269A a programem Univerzity Karlovy Progres Q25.
Do redakce došlo dne 13. 9. 2018.
Adresa pro korespondenci:
doc. RNDr. Jaroslav Julák, CSc.
Ústav imunologie a mikrobiologie, 1. LF UK a VFN
Studničkova 7
128 00 Praha 2
e-mail jaroslav.julak@lf1.cuni.cz
Zdroje
1. BRISTOW, I. R. The effectiveness of lasers in the treatment of onychomycosis: A systematic review. J Foot Ankle Res, 2014, 7, p. 34–44. DOI: 10.1186/1757-1146-7-34.
2. DAESCHLEIN, G., SCHOLZ, S., VON WOEDTKE, T., NIGGEMEIER, M., KINDEL, E., BRANDENBURG, R., WELTMANN, K.-D., JUNGER, M. In vitro killing of clinical fungal strains by low-temperature atmospheric-pressure plasma jet. IEEE Trans. Plasma Sci., 2011, 39, p. 815–821. DOI: 10.1109/TPS.2010.2063441.
3. EHLBECK, J., SCHNABEL, U., POLAK, M., WINTER, J., VON WOEDTKE, T., BRANDENBURG, R., VON DEM HAGEN, T., WELTMANN, K.-D. Low temperature atmospheric pressure plasma sources for microbial decontamination. J Phys D: Applied Physics, 2010, 44, p. 13002. DOI:10.1088/0022-3727/44/1/013002.
4. ELEWSKI, B. E. Onychomycosis: Pathogenesis, diagnosis, and management. Clin Microbiol Rev, 1998, 11, p. 415–429.
5. GHANNOUM, M., ISHAM, N. Fungal nail infections (onychomycosis): A never-ending story? PLoS Pathog, 2014, 10, p. e1004105. DOI: 10.1371/journal.ppat.1004105.
6. GUPTA, A. K., FOLEY, K. A., VERSTEEG, S. G. New antifungal agents and new formulations against dermatophytes. Mycopathologia, 2017, 182, p. 127–141. DOI:10.1007/s11046-016-0045-0.
7. HAERTEL, B., VON WOEDTKE, T., WELTMANN, K.-D., LINDEQUIST, U. Non-thermal atmospheric pressure plasma possible application in wound healing. Biomol Therapeut, 2014, 22, p. 477–490. DOI:10.4062/biomolther.2014.105.
8. HEINLIN, J., MORFILL, G., LANDTHALER, M., STOLZ, W., ISBARY, G., ZIMMERMANN, J. L., SHIMIZU, T., KARRER, S. Plasma medicine: possible applications in dermatology. J German Soc Dermatol, 2010, 8, p. 968–976. DOI:10.1111/j.1610-0387.2010.07495.x.
9. CHA, S., PARK, Y. S. Plasma in dentistry. Clin Plasma Med, 2014, 2, p. 4–10. DOI:10.1016/j.cpme.2014.04.002.
10. JULÁK, J., SCHOLTZ, V. Decontamination of human skin by low-temperature plasma produced by cometary discharge. Clin Plasma Med, 2013, 1, p. 31–34. DOI:10.1016/j.cpme.2013.09.002.
11. JULÁK, J., SOUŠKOVÁ, H., SCHOLTZ, V., KVASNIČKOVÁ, E., SAVICKÁ, D., KŘÍHA V. Comparison of fungicidal properties of non-thermal plasma produced by corona discharge and dielectric barrier discharge. Folia Microbiol, 2018, 63, p. 63–68. DOI:10.1007/s12223-017-0535-6.
12. JULÁK, J., SOUŠKOVÁ, H., ŽIVNÁ, H., SCHOLTZ, V. Možnosti využití nízkoteplotního plazmatu v léčbě plísňových onemocnění. Veterinární lékař, 2016, 14, p. 199–204.
13. LLOYD, G., FRIEDMAN, G. JAFRI, S., SCHULTZ, G., FRIDMAN, A., HARDING, K. Gas plasma: medical uses and developments in wound care. Plasma Process Polym, 2010, 7, p. 194–211. DOI:10.1002/ppap.200900097.
14. MORGADO, L. F., TRÁVOLO, A. R. F., MUEHLMANN, L. A., NARCIZO, P. S., NUNES, R. B., PEREIRA, P. A. G., PY-DANIEL, K. R., JIANG, C. S., GU, J., AZEVED, R. B., LONGO, J. P. F. Photodynamic therapy treatment of onychomycosis with aluminium-phthalocyanine chloride nanoemulsions: A proof of concept clinical trial. J Photochem Photobiol B, 2017, 173 p. 266–270. DOI:10.1016/j.jphotobiol.2017.06.010.
15. ROBERTS, D. T., TAYLOR, W. D., BOYLE, J. Guidelines for treatment of onychomycosis. Brit J Dermatol, 2003, 148, p. 402–410. DOI: 10.1046/j.1365-2133.2003.05242.x.
16. SCHLEGEL, J., KÖRITZER, J. BOXHAMMER, V. Plasma in cancer treatment. Clin Plasma Med, 2013, 1, p. 2–7. DOI:10.1016/j.cpme.2013.08.001.
17. SCHOLTZ, V., KVASNIČKOVÁ, E., JULÁK, J. Microbial inactivation by electric discharge with metallic grid. Acta Phys Pol A, 2013, 124, p. 62–65.
18. SCHOLTZ, V., SOUŠKOVÁ, H., HUBKA, V., ŠVARCOVÁ, M., JULÁK, J. Inactivation of human pathogenic dermatophytes by non-thermal plasma. J Microbiol Methods, 2015, 119, p. 53–58. DOI:10.1016/j.mimet.2015.09.017.
19. SCHOLTZ, V., SOUŠKOVÁ, H., ŠVARCOVÁ, M., KŘÍHA, V., ŽIVNÁ, H., JULÁK, J. Inactivation of dermatophyte infection by nonthermal plasma on animal model. Med Mycol, 2017, 55, p. 422–428. DOI:10.1093/mmy/myw094.
20. SCHOLTZ, V., JULÁK, J. Plasma jet-like point-to-point electrical discharge in air and its bactericidal properties. IEEE Trans Plasma Sci, 2010, 38, p. 1978–1980. DOI:10.1109/TPS.2010.2051461.
21. SCHOLTZ, V., JULÁK, J. The “cometary” discharge, a possible new type of DC electric discharge in air at atmospheric pressure, and its bactericidal properties. J Phys Conf Ser, 2010, 223, p. 012005.
22. SCHOLTZ, V., PAZLAROVÁ, J., SOUŠKOVÁ, H., KHUN, J., JULÁK, J. Nonthermal plasma – a tool for decontamination and disinfection. Biotechnol Adv, 2015, 33, p. 1108–1119. DOI:10.1016/j.biotechadv.2015.01.002.
23. SOUŠKOVÁ, H., SCHOLTZ, V., JULÁK, J., KOMMOVÁ, L., SAVICKÁ, D., PAZLAROVÁ, J. The survival of micromycetes and yeasts under the low-temperature plasma generated in electrical discharge. Folia Microbiol, 2011, 56, p. 77–79.
24. SOUŠKOVÁ, H., SCHOLTZ, V., JULÁK, J., KŘÍHA, V., SAVICKÁ, D. Srovnání fungicidních vlastností koronového výboje a dielektrického bariérového výboje. Mykol Listy, 2013, 123, p. 48–50.
25. SOUŠKOVÁ, H., SCHOLTZ, V., JULÁK, J., SAVICKÁ, D. The fungal spores survival under the low-temperature plasma. In Hensel, K., Machala, Z., Akishev Y. (eds), Plasma for bio-decontamination, medicine and food security. Springer, Dordrecht, 2012, p. 57–66. DOI 10.1007/978-94-007-2852-3.
26. ŠVARCOVÁ, M., JULÁK, J., HUBKA, V., SOUŠKOVÁ, H., SCHOLTZ, V. Treatment of a superficial mycosis by low-temperature plasma: Case report. Prague Med Rep, 2014, 115, p. 73–78.
27. TENDERO, C., TIXIER, C., TRISTANT, P., DESMAISON, J., LEPRINCE, P. Atmospheric pressure plasmas: A review. Spectrochim Acta B: Atomic Spectroscopy, 2006, 61, p. 2–30. DOI:10.1016/j.sab.2005.10.003.
28. XIONG, Z., ROE, J., GRAMMER, T. C., GRAVES D. B. Plasma treatment of onychomycosis. Plasma Process Polym, 2016, 13, p. 588–597. DOI: 10.1002/ppap.201600010.
29. SCHER R. K., JOSEPH W., ROBBINS J. Progression and Recurrence of Onychomycosis. Medscape, April 10, 2018. Dostupné na www: https://www.medscape.org/viewarticle/452687.
Štítky
Dermatologie Dětská dermatologie
Článek vyšel v časopiseČesko-slovenská dermatologie
Nejčtenější tento týden
2018 Číslo 6- Takrolimus v terapii atopické dermatitidy a analýza jeho nákladové efektivity ve srovnání s kortikosteroidní léčbou
- Daivobet gel – lékový profil
- Fixní kombinace kalcipotriol/betamethason v topické léčbě psoriázy
- Psoriáza a kouření – vzájemně se potencující rizika?
-
Všechny články tohoto čísla
- Zoonotické dermatofytózy: klinický obraz, diagnostika, etiologie, léčba, epidemiologická situace u nás
- Kontrolní test
- Pět případů lidských dermatofytóz vyvolaných zoofilním druhem Trichophyton erinacei přeneseným z ježků
- Efektivní léčebná modulace poškozujícího zánětu u nemocných s psoriázou guselkumabem cílícím na specifickou podjednotku p19 IL-23 regulační osy IL-23/Th17
- Identifikace dermatofytů pomocí MALDI-TOF hmotnostní spektrometrie
- Využití PCR-HRMA při přímé detekci a identifikaci původců dermatofytóz z klinických vzorků
- Možnosti terapie onychomykózy nízkoteplotním plazmatem
- Klinický případ: Shluk žlutavých papul u kojence – stručný přehled
- Mykózy nohou a nehtů
- Zápisnica zo zasadania výboru Slovenskej dermatovenerologickej spoločnosti SLS Bratislava 7. 4. 2018
- Zápis ze schůze výboru ČDS Praha 27. 9. 2018
- 12. KONFERENCE AKNÉ A OBLIČEJOVÉ DERMATÓZY
- Odborné akce 2019
- Česko-slovenská dermatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Zoonotické dermatofytózy: klinický obraz, diagnostika, etiologie, léčba, epidemiologická situace u nás
- Klinický případ: Shluk žlutavých papul u kojence – stručný přehled
- Pět případů lidských dermatofytóz vyvolaných zoofilním druhem Trichophyton erinacei přeneseným z ježků
- Mykózy nohou a nehtů
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



