-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariérní portál
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaPotvrzuje cenobamát v anglické reálné praxi výsledky dosažené v regulačních studiích?
Cenobamát je nové protizáchvatové léčivo (ASM) s dlouhým poločasem užívané 1× denně. Je indikované jako přídatná terapie u dospělých s fokálními záchvaty (FOS) s přechodem do bilaterálních tonicko-klonických záchvatů (FBTCS) nebo bez něj, kteří splňují definici ILAE pro farmakorezistenci. Regulační studie předpovídají, že větší část pacientů dosáhne úplného vymizení nebo téměř vymizení záchvatů s cenobamátem ve srovnání s podobně navrženými studiemi komparátorů. Co ukazuje anglická reálná praxe? O tom hovořil dr. Rhys Thomas z Newcastleské univerzity.
Nevýhody regulačních studií – nákladnost a výběr populace
Regulační studie jsou nákladné a obecně je snahou zapojit do nich nemocné, kteří mají velkou četnost záchvatů; musejí to však zároveň být pacienti, kteří nebudou poškozeni případnou randomizací do placebové skupiny. Titrace je obvykle tak rychlá, aby bylo ještě možné provádět ji bezpečně, a standardním cílovým ukazatelem stanoveným Evropskou lékovou agenturou (EMA) a americkým Úřadem pro kontrolu potravin a léčiv (FDA) bývá redukce záchvatů po krátkém sledování (např. 12 týdnů) o 50 %.
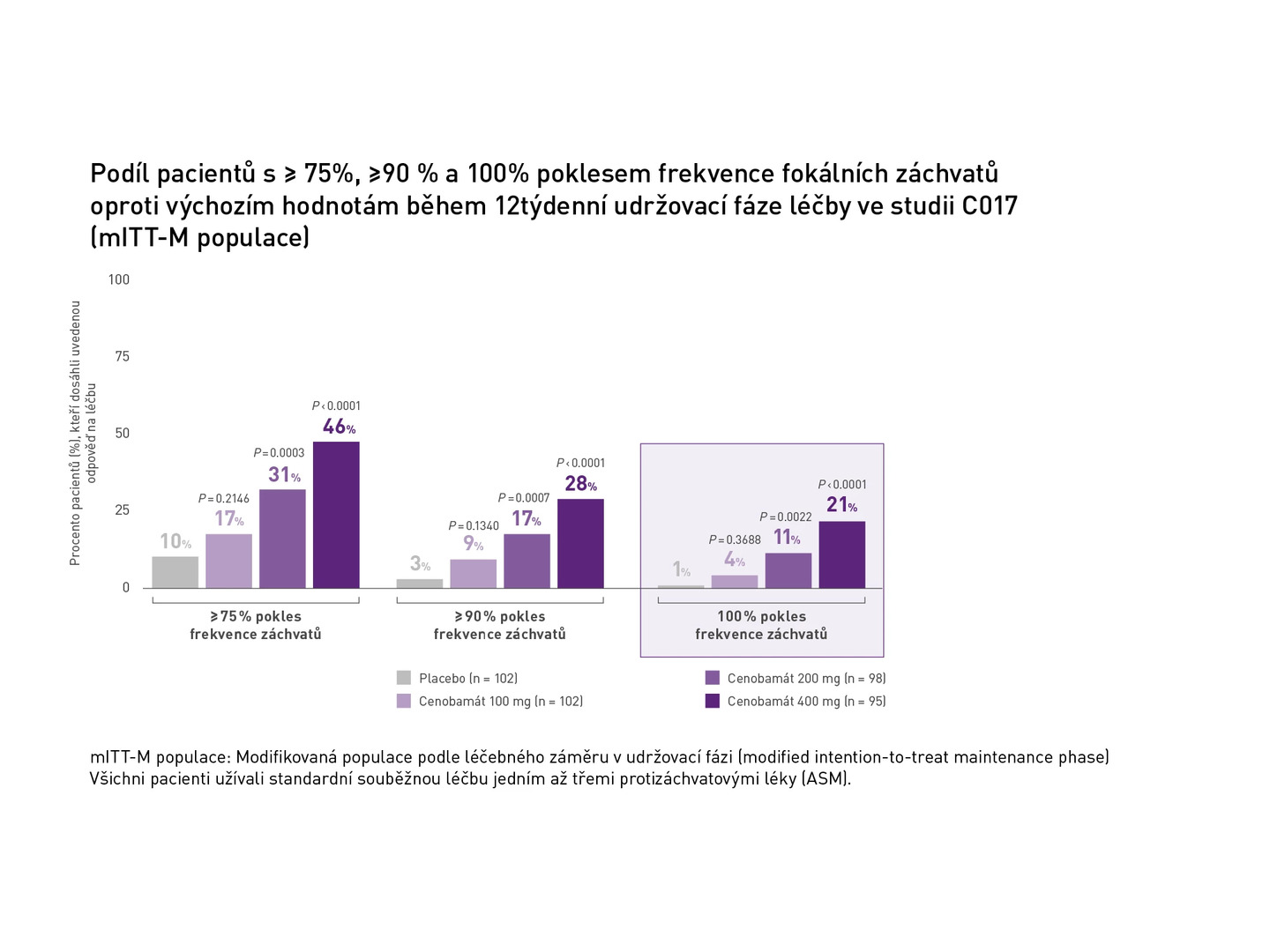
Krauss et al. provedli multicentrickou randomizovanou dvojitě zaslepenou placebem kontrolovanou studii, v níž zkoumali odpověď na různou dávku cenobamátu nebo placebo u 437 pacientů s nekontrolovanými fokálními záchvaty, kteří současně dostávali 1–3 ASMs. Pacienti byli náhodně přiřazeni do kohorty s cenobamátem v dávce 100, 200 či 400 mg nebo placebem přidaným ke standardní péči (SoC). Cílový ukazatel účinnosti tvořila změna od výchozí hodnoty frekvence fokálních záchvatů za 28 dní a podíl pacientů, kteří dosáhli alespoň 50% úbytku frekvence záchvatů v udržovací fázi léčby. V tomto uspořádání by bylo dosažení 75% snížení záchvatů neobvyklé a neočekávané pro tak rezistentní nemocné. Proto jsou výsledky této studie překvapivé − pokud je 75% redukce záchvatů za 12 týdnů neobvyklá, pak 90% úbytek je překvapivý. Jedná se však o regulační studii ve vybrané populaci.
Obr. 1 Účinnost cenobamátu v přídatné léčbě po 12 týdnech u pacientů s nekontrolovanými fokálními záchvaty (dle: Krauss et al., 2020)
Reálná praxe: program včasného přístupu k léčbě a ilustrativní kazuistika
Schválení použití cenobamátu v Anglii bylo založeno nejen na údajích o účinnosti, ale také na metodice, která hodnotí potenciální dopad extrapolace výsledků účinnosti z regulačních studií na efektivitu v reálné praxi, a na porovnání cenobamátu v tomto modelu s příslušnými komparátory (tj. v tomto případě s brivaracetamem, eslikarbazepinem, lakosamidem, perampanelem). Výsledky předpovídaly méně medikačních pokusů, hospitalizací, možnost vyhnout se stimulaci n. vagus (VNS) a chirurgickému zákroku, což by mimo jiné znamenalo podstatnou úsporu nákladů při volbě cenobamátu.
Přednášející popsal zkušenosti svého týmu s použitím cenobamátu v reálné praxi v programu časného přístupu (early access), k němuž byl jeho skupině udělen přístup v říjnu 2020. V této souvislosti přiblížil kazuistiku pacienta Adama – jednoho z prvních, kteří byli léčeni cenobamátem ve Velké Británii. Epilepsie mu byla diagnostikována ve věku 10 let, kdy mu pravidelné záchvaty způsobovaly pravostranné ochromení těla až 10× denně. Do svých 20 let zažil až 50 záchvatů denně. Po přidání cenobamátu do terapie prožil 8 měsíců bez jediného záchvatu, a přestože se nyní někdy vyskytují, jsou mnohem méně časté. Navíc dokázal přestat užívat téměř veškerou ostatní medikaci. Nyní pracuje na plný úvazek a podle vlastních slov má více energie na trávení času se svou rodinou.
Důležitost dodržování schématu a milníky titrace
Ze studie fáze III C021 vyplynulo optimální a bezpečné dávkovací schéma, obnášející zahájení nízkou dávkou a její pomalé zvyšování (start low, go-slow), tedy startovací dávkou 12,5 mg 1× denně a titrací každých 14 dní. Bezpečnost tohoto titračního schématu byla potvrzena v údajích získaných od 1339 pacientů léčených cenobamátem, u kterých nedošlo k žádným případům syndromu DRESS. Titrace dávky má dle přednášejícího dva zásadní milníky – 100 mg, kdy je důležité se ujistit, že od pacienta pravidelně přichází zpětná vazba s ohledem na tolerabilitu a možné farmakokinetické interakce vzhledem k souběžné léčbě, a poté cílovou dávku, kdy může být zapotřebí ještě úprava na dávku udržovací. U pacientů s komunikačními obtížemi může být titrace pomalejší.
Cenobamát lze použít spíše k nahrazení jedné z konkomitantně užívaných medikací než pouze přidat jako další protizáchvatové léčivo.
Nežádoucí příhody (AEs) hlášené v klinických studiích a následně shrnuté v SPC souvisejí s mechanismy účinku CNB. Ty nejběžnější jsou ovšem předvídatelné a zvládnutelné, protože se jedná hlavně o ty, s nimiž se pacienti setkávají a které řeší při užívání jiných ASMs nebo kombinací zaměřených na jeden či více těchto mechanismů.
Nejnovější data z Newcastlu
Zásadním bodem je potvrdit, že účinnost léčby v regulačních studiích následně odpovídá její účinnosti v reálné praxi. Tu vedle retrospektivní 2leté studie u pacientů s ultrarefrakterní epilepsií publikované Peña-Ceballosem et al. podle všeho ukazují také předběžné výsledky probíhající prospektivní studie s cenobamátem v reálné praxi u pacientů s farmakorezistentní refrakterní fokální epilepsií na pracovišti přednášejícího.
Od května 2023 bylo do newcastleské studie zahrnuto 151 dospělých (60 % mužů, střední věk přibližně 40 let). Fokální epilepsii se strukturálními lézemi na MRI jich trpělo 68, z toho 11 s fokální kortikální dysplazií, 6 s poruchami migrace neuronů, 5 s autoimunitní encefalitidou, 2 s Rasmussenovou encefalitidou a 1 s Alpersovým syndromem (mitochondriální poruchou spojenou s mutací genu POLG). Střední dávka cenobamátu dosáhla 204 mg, ačkoliv 37 pacientů bylo stále ve fázi titrace. Při střední době sledování 367 dnů přibližně 45 % pacientů hlásilo některé nežádoucí příhody související s léčbou a 24 pacientů (16,3 %) užívání přerušilo kvůli nízké tolerabilitě. V podstatě byl 1 z 10 pacientů bez záchvatů a další čtvrtina zaznamenala snížení míry záchvatů o 75−99 %. Méně než 5 % pacientů se zhoršením záchvatů bylo připisováno pravděpodobně lékovým interakcím a u některých se zkrátka nejednalo o vhodně zvolené léčivo. Většina jich však z podání cenobamátu těží, přestože trpí refrakterní epilepsii.
Obr. 2 Výsledky účinnosti cenobamátu v reálné praxi v Newcastlu (dle: Thomas, 2023)

(esr)
Zdroje:
1. Thomas R. From an Early Access program to real-world cenobamate use. 35th International Epilepsy Congress, Dublin, 2023 Sep 4.
2. Krauss G. L. et al. Safety and efficacy of adjunctive cenobamate (YKP3089) in patients with uncontrolled focal seizures: a multicentre, double-blind, randomised, placebo-controlled, dose-response trial. Lancet Neurol 2020; 19 (1): 38–48, doi: 10.1016/S1474-4422(19)30399-0.
3. Peña-Ceballos J. et al. Adjunctive cenobamate in highly active and ultra-refractory focal epilepsy: a "real-world" retrospective study. Epilepsia 2023 May; 64 (5): 1225–1235, doi: 10.1111/epi.17549.
3. The impact of time lost to achieving meaningful seizure control. Congress report. Angelini Pharma satellite symposium at ILAE 2023, Dublin, 2023 Sep 4. Dostupné na: www.librarycontent.net/documenti/624_f672dad87b2586b8d89fa25471d8c72b.pdfZáznam Péči o pacienty s epilepsií může usnadnit zájem o jejich subjektivní zkušenosti s touto nemocíZáznam Čas u epilepsie znamená život... aneb dopad ztráty času na dosažení smysluplné kontroly záchvatů
- Péči o pacienty s epilepsií může usnadnit zájem o jejich subjektivní zkušenosti s touto nemocí
- Cílem léčby epilepsie je vrátit pacienty do normálního života
- Čas u epilepsie znamená život... aneb dopad ztráty času na dosažení smysluplné kontroly záchvatů
- U farmakorezistentní epilepsie hrozí náhlé neočekávané úmrtí. Jaké jsou hlavní rizikové faktory?
- Je na obzoru změna klinických výsledků u osob s farmakorezistentní epilepsií?
- Potvrzuje cenobamát v anglické reálné praxi výsledky dosažené v regulačních studiích?
Přihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




