-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Kariérní portál
Doporučené pozice
Reklama- Praxe
Top novinky
ReklamaCílem léčby epilepsie je vrátit pacienty do normálního života
Podíl lidí s epilepsií, kteří mají nekontrolované onemocnění (více než třetina), a těch, kteří přerušili léčbu v důsledku nežádoucích účinků, se v průběhu posledních 30 let nezměnil, přestože byly postupně zavedeny četná protizáchvatová léčiva (ASMs) 1., 2. a 3. generace s různými mechanismy účinku. Mezi nové možnosti, jež pomáhají pacientům obnovit normalitu jejich života, patří cenobamát (CNB). Výsledky jeho podávání jsou velmi slibné, jak ve svém sdělení upozornil přednosta neurologické kliniky v Alfred Health v australském Melbourne profesor Patrick Kwan.
Účinnost léčby je ovlivněná i tolerabilitou
Schopnost léčiva snížit výskyt záchvatů a současně jeho snášenlivost představují „dvě strany téže mince“ – obě mají významný vliv na účinnost léčby, neboť vysoce účinná terapie může být pacientovi prospěšná jen tehdy, nemusí-li kvůli jejím nežádoucím účinkům léčbu přerušit. U nemocných s nově diagnostikovanou epilepsií je zřejmé, že za selháním prvních ASMs stály právě nežádoucí účinky – míra vysazení v jejich důsledku se v uplynulých 3 dekádách nezměnila.
Role a potenciál cenobamátu
Cenobamát byl nedávno zaveden jako přídatná léčba fokálních záchvatů, se sekundární generalizací i bez ní, u dospělých pacientů s epilepsií, kteří nedosáhli adekvátní kontroly navzdory léčbě alespoň 2 ASMs. Účinnost a bezpečnost potvrdil ve dvou multicentrických randomizovaných dvojitě zaslepených a placebem kontrolovaných studiích – fáze IIB C017 (klíčové hodnocení) a fáze II C013.
Studie C017
C017 testovala odpovědi na různé dávky cenobamátu a zahrnovala 4 studijní ramena: CNB 100 mg (n = 108), CNB 200 mg (n = 110), CNB 400 mg (n = 111), placebo (n = 108).
V exploratorní post hoc analýze byla vstupní konkomitantní protizáchvatová medikace rozdělena na blokátory sodíkových kanálů (SCBs) a ASMs s jiným mechanismem účinku (non-SCBs).
Obr. 1 Míra odpovědi na léčbu CNB: graf vlevo − v kombinaci s blokátory sodíkových kanálů (SCBs); graf vpravo − v kombinaci s jinými ASMs než blokátory sodíkových kanálů (non-SCBs) (post hoc analýza studie C017)
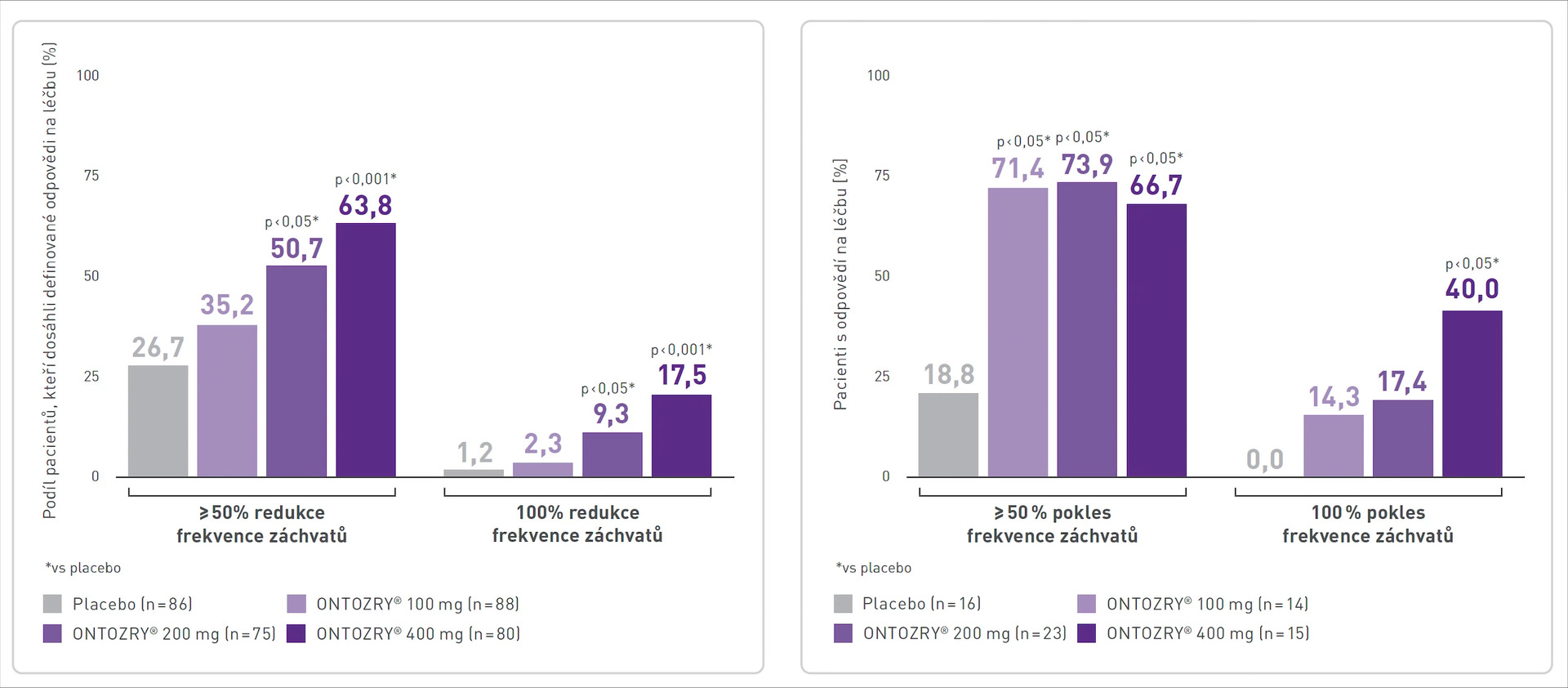
Ukázalo se, že ať byl cenobamát v dávce 200 či 400 mg denně podán s ASM ze skupiny SCBs nebo non-SCBs, významně větší podíl pacientů s nekontrolovanými fokálními záchvaty dosáhl míry odpovědi ≥ 50 %, ≥ 75 % a ≥ 90 %, (tj. úbytku záchvatů o ≥ 50, ≥ 75 a ≥ 90 %) oproti placebové větvi. Navíc významně větší část pacientů, kteří dostávali CNB 400 mg, v porovnání s placebovou větví docílila bezzáchvatovosti (při užívání SCBs 17,5 vs. 1,2 %; ve skupině non-SCBs 40,0 vs. 0,0 %). Pacienti užívající dávku 200 a 400 mg denně a souběžně SCB a všichni, kteří dostávali cenobamát v kombinaci s non-SCB ASM, měli významně větší medián procentuálního snížení frekvence fokálních záchvatů oproti placebovému ramenu. Nežádoucí příhody související s léčbou (TEAEs) byly podobné napříč skupinami, závrať byla častěji hlášena u pacientů užívajících SCBs.
Studie C013
Studie C013 prokázala, že přídatná léčba cenobamátem v dávce 200 mg denně významně zlepšila kontrolu záchvatů u dospělých s nekontrolovanými fokálními záchvaty a byla dobře tolerována. Studie měla 8týdenní úvodní fázi a 12týdenní dvojitě zaslepenou, přičemž prvních 6 týdnů probíhala titrace a dalších 6 týdnů představovalo udržovací fázi léčby. Primární cílový ukazatel představovala procentuální změna frekvence záchvatů za 28 dní z výchozího stavu během dvojitě slepé fáze.
Obr. 2 Design studie C013
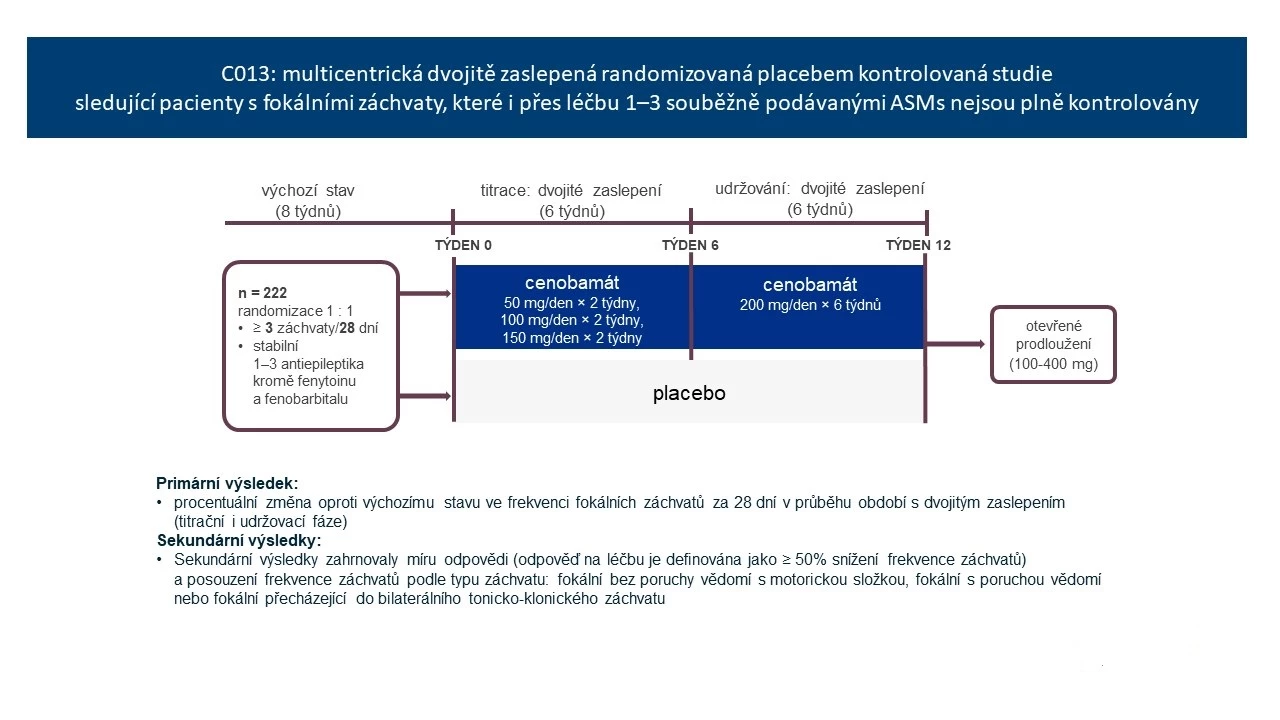
Randomizováno bylo 222 dospělých pacientů ve věku 18−65 let, z nich 113 užívalo cenobamát a 109 placebo; dvojitě zaslepenou fázi dokončilo 90,3 a 90,8 %.
Obr. 3 Distribuce pacientů ve studii C013

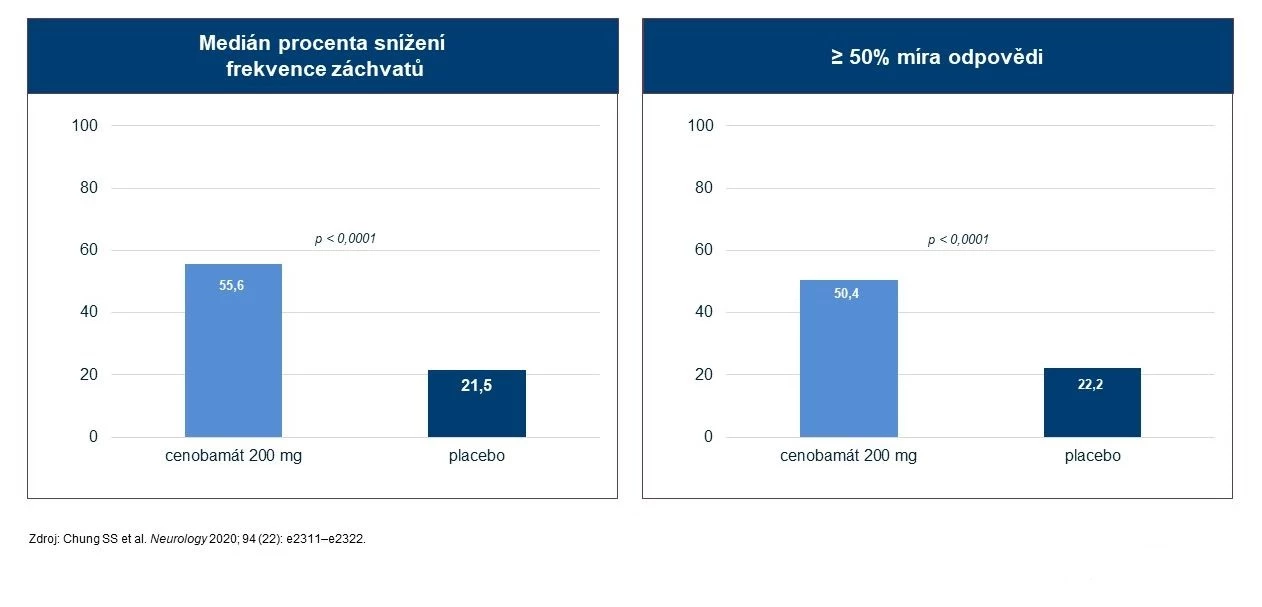
Střední hodnota výchozí frekvence výskytu záchvatů byla 6,5 (0–237) za 28 dní. Ve srovnání s placebem byla s cenobamátem spojena větší střední hodnota procentuálního úbytku záchvatů (55,6 vs. 21,5 %; p < 0,0001) i míra odpovědi (≥ 50% snížení frekvence záchvatů u 50,4 vs. 22,2 % pacientů pro placebo; p < 0,0001).
Obr. 4 Hodnocení účinnosti CNB v přídatné léčbě oproti placebu ve studii C013
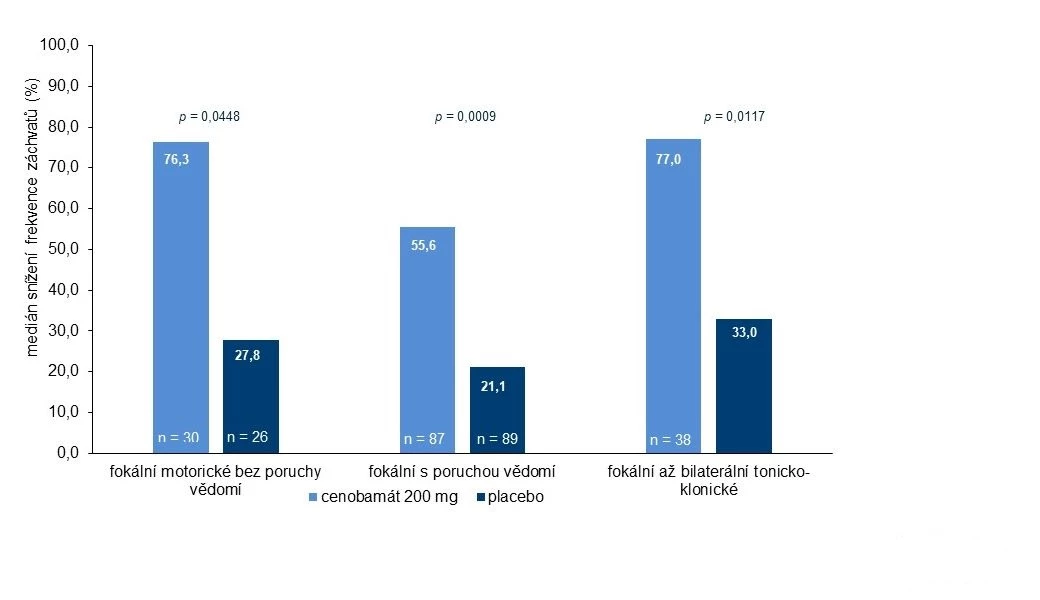
Významně redukovány při podávání cenobamátu 200 mg v porovnání s placebem byly fokální záchvaty s motorickou komponentou bez poruchy vědomí, fokální záchvaty s poruchou vědomí i fokální záchvaty přecházející do bilaterálních tonicko-klonických záchvatů. Během udržovací fáze bylo zcela bez záchvatů 28,3 % léčených cenobamátem a 8,8 % pacientů, kteří dostávali placebo. TEAEs hlášené v některé skupině v > 10 % případů představovaly somnolence (cenobamát vs. placebo 22,1 vs. 11,9 %), závratě (22,1 vs. 16,5 %), bolest hlavy (12,4 vs. 12,8 %), nauzea (11,5 vs. 4,6 %) a únava (10,6 vs. 6,4 %).
Obr. 5 Účinnost (snížení frekvence záchvatů) podle typu záchvatu
OLE C013
Další důležitá data z hlediska tolerability léčby cenobamátem poskytla otevřená extenze studie C013 (OLE C013), která obnášela dlouhodobé hodnocení bezpečnosti užívané terapie. Bylo v ní dosaženo dlouhodobé retence, která prokázala trvalou bezpečnost a snášenlivost přídatné léčby cenobamátem až 7,8 roku u dospělých pacientů s fokálními záchvaty rezistentními na léčbu 1−3 ASMs.
Do OLE C013 vstoupilo 149 pacientů, kteří dokončili 12týdenní dvojitě zaslepenou fázi studie C013. Během OLE byly povoleny úpravy dávky cenobamátu i konkomitantních ASMs. Hodnocení bezpečnosti zahrnovala frekvenci TEAEs a závažných TEAEs, závažnost TEAEs a TEAEs vedoucích k přerušení terapie.
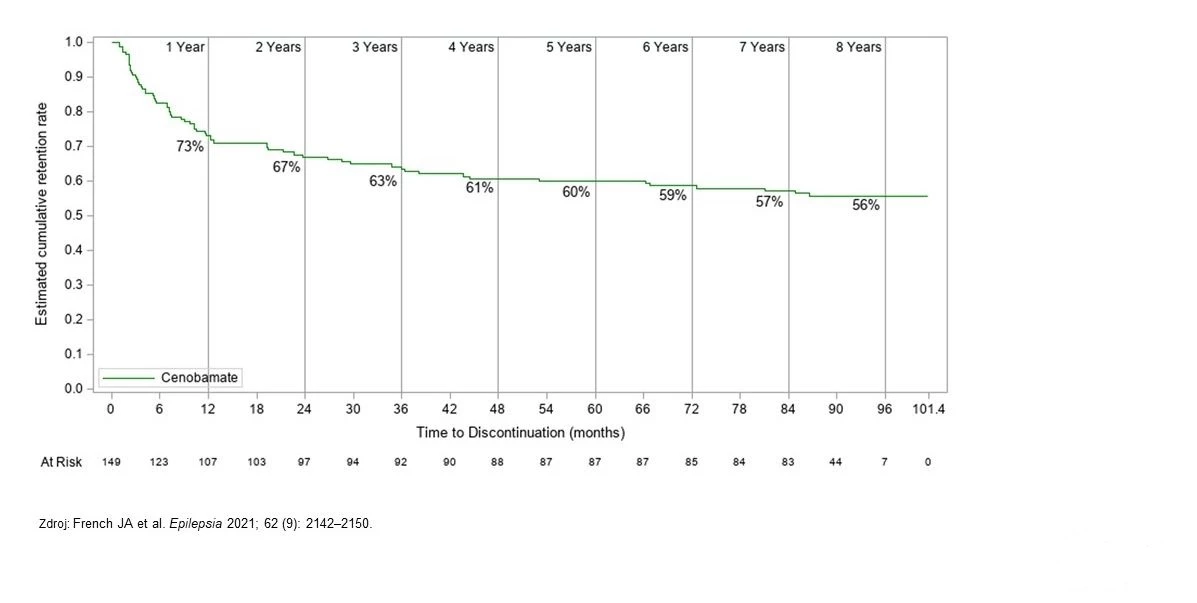
Medián doby léčby cenobamátem činil 6,25 roku. V době hodnocení dat (data cut off) zůstávalo v OLE C013 57 % účastníků (85 z 149), medián doby léčby u nich činil 6,8 roku (6,4–7,8). Medián modální denní dávky cenobamátu byl 200 mg (50–400). Pravděpodobnost pokračování léčby po 1−6 letech léčby cenobamátem činila 59−73 %. U pacientů, kteří pokračovali po 1 roce (n = 107), byla pravděpodobnost pokračování po 2 letech 92 %, po 5 letech 82 %. Nejběžnějšími důvody přerušení byly vysazení pacientem (19,5 %; 29 z 149), nežádoucí účinky (10,1 %; 15 z 149) a nedostatečná účinnost (5,4 %; 8 z 149). TEAEs vedoucí k přerušení aspoň u 1 % pacientů představovaly únava (1,3 %; 2 z 149), ataxie (1,3 %; 2 z 149) a poruchy paměti nebo amnézie (1,3 %; 2 z 149). Nejčastěji hlášené TEAEs tvořily závratě (32,9 %; 49 z 149), bolest hlavy (26,8 %; 40 z 149) a somnolence (21,5 %; 32 z 149), primárně byly mírné či střední závažnosti.
Obr. 6 Doba do přerušení účasti v otevřeném prodloužení (OLE) studie C013
(esr)
Zdroje:
1. Kwan P. Experience of people with epilepsy while waiting for seizure freedom: Has the treatment outcomes landscape changed in 30 years? 35th International Epilepsy Congress, Dublin, 2023 Sep 4.
2. Brandt C. et al. Efficacy and safety of adjunctive cenobamate: Post-hoc analysis of study C017 in patients grouped by mechanism of action of concomitant antiseizure medications. Seizure 2022; 96 : 86–93, doi: 10.1016/j.seizure.2022.02.003.
3. Chung S. S. et al. Randomized phase 2 study of adjunctive cenobamate in patients with uncontrolled focal seizures. Neurology 2020; 94 (22): e2311−e2322, doi: 10.1212/WNL.0000000000009530.
4. French J. A. et al. Long-term safety of adjunctive cenobamate in patients with uncontrolled focal seizures: open-label extension of a randomized clinical study. Epilepsia 2021; 62 (9): 2142–2150, doi: 10.1111/epi.17007.
5. The impact of time lost to achieving meaningful seizure control. Congress report. Angelini Pharma satellite symposium at ILAE 2023, Dublin, 2023 Sep 4. Dostupné na: www.librarycontent.net/documenti/624_f672dad87b2586b8d89fa25471d8c72b.pdfZáznam Péči o pacienty s epilepsií může usnadnit zájem o jejich subjektivní zkušenosti s touto nemocíZáznam Čas u epilepsie znamená život... aneb dopad ztráty času na dosažení smysluplné kontroly záchvatů
- Péči o pacienty s epilepsií může usnadnit zájem o jejich subjektivní zkušenosti s touto nemocí
- Cílem léčby epilepsie je vrátit pacienty do normálního života
- Čas u epilepsie znamená život... aneb dopad ztráty času na dosažení smysluplné kontroly záchvatů
- U farmakorezistentní epilepsie hrozí náhlé neočekávané úmrtí. Jaké jsou hlavní rizikové faktory?
- Je na obzoru změna klinických výsledků u osob s farmakorezistentní epilepsií?
- Potvrzuje cenobamát v anglické reálné praxi výsledky dosažené v regulačních studiích?
Přihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání




