-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaÚskalia stanovenia vitamínu D
“Snags” connected with establishing the vitamin D
Objective:
The aim of proposed paper was to compare a three total 25-hydroxy-vitamin D immunoassays to that of HPLC with UV detection.Material and methods:
Serum 25-(OH) D levels were measured from blood samples of 109 patients with different immunoassays (ABBOTT, ROCHE, SIEMENS) and method of HPLC which was chosen as the reference. In the first step immunoassays were compared to HPLC. In the second step immunoassays were compared to each other. Further purpose of methods comparison the Passing-Bablok regression and Bland-Altman analysis were used. The limits of maximum acceptable differences were set at 21.5 %, according to Vitamin D Standardization-Certification Program (VDSCP). In the last step, the concordance in the interpretation of measured results was evaluated.Results:
None of the examined 25-(OH) D immunoassays was comparable to HPLC and to each other. Bland-Altman analysis revealed, in comparison to HPLC, that ROCHE showed positive bias +28.0 %, ABBOTT +0.2 % and SIEMENS –23.4 %. Although average bias of ABBOTT immunoassay is insignificant, particular results do deviate significantly (-89.4 % to 89.0 %). The concordance in the interpretation of measured results, in comparison to HPLC, was highest with ABBOTT (65.21 %), then with ROCHE (59.63 %) and lowest with SIEMENS (47.79 %).Conclusion:
The results of the proposed papers suggest low levels of 25-(OH) D immunoassays standardization and an alternative to use assay-specific decision limits.Keywords:
25-hydroxy-vitamin D – interpretation – method comparison – standardization
Autoři: Anton Vaňuga 1,2; Peter Huba 1; Ivana Ságová 3; Pavel Blažíček 1; Jarmila Melegová 5; Juraj Payer 4; Peter; Vaňuga 2
Působiště autorů: Alphamedical s. r. o., Slovenská republika 1; Národný endokrinologický a diabetologický ústav, n. o., Ľubochňa, Slovenská republika 2; I. interná klinika JLF UK a UNM, Martin, Slovenská republika 3; V. interná klinika LF UK a UNB, Nemocnica Ružinov, Bratislava, Slovenská republika 4; Klinická biochémia, s. r. o, Žilina, Slovenská republika 5
Vyšlo v časopise: Vnitř Lék 2017; 63(6): 403-408
Kategorie: Původní práce
Souhrn
Cieľ:
Cieľom štúdie bolo porovnať 3 rutinné imunochemické metódy stanovenia celkového 25-hydroxy-vitamínu D [25-(OH) D] s vysokoúčinnou kvapalinovou chromatografiou s UV detekciou.Materiál a metódy:
Sérové hladiny 25-(OH) D boli stanovované u 109 pacientov rôznymi imunochemickými metódami (ABBOTT, ROCHE, SIEMENS) a metódou HPLC, ktorá bola v predkladanej práci považovaná za referenčnú. V prvom kroku boli vybrané imunochemické metódy porovnané s ohľadom na metódu HPLC. V druhom kroku boli tieto metódy porovnané navzájom medzi sebou. Na porovnanie metód bola použitá regresná analýza (Passing-Bablok) a Bland-Altmanova analýza diferencií. Za maximálne akceptovateľné diferencie v jednotlivých výsledkoch boli považované hodnoty v rozmedzí ± 21,5 %. Toto kritérium bolo zvolené na základe CDC Vitamin D Standardization-Certification Program (VDSCP). V poslednom kroku bola vyhodnotená miera zhody v interpretácii nameraných výsledkov 25-(OH) D.Výsledky:
Žiadna zo skúmaných imunochemických metód stanovenia 25-(OH) D nebola porovnateľná s metódou HPLC a takisto neboli porovnateľné navzájom medzi sebou. Bland-Atlmanova analýza odhalila, v porovnaní s HPLC, že metóda ROCHE vykazuje bias +28,0 %, metóda ABBOTT +0,2 % a metóda Siemens -23,4 %. Priemerný bias u metódy ABBOTT je síce nevýznamný, avšak jednotlivé výsledky vykazovali bias v rozmedzí -89,4 % až 89,0 %. V porovnaní s metódou HPLC bola miera zhody v klinickej interpretácii výsledkov u metódy ABBOTT 65,21 %, ROCHE 59,63 % a SIEMENS 47,79 %.Záver:
Výsledky predkladanej práce poukazujú na slabú úroveň štandardizácie metód stanovenia 25-(OH) D, ako aj na možnosť zvážiť používanie na metóde závislých rozhodovacích limitov.Kľúčové slová:
25-hydroxy-vitamín D – interpretácia – porovnanie metód – štandardizáciaÚvod
Celosvetový nárast hypovitaminózy D má za následok prudký vzostup záujmu o jeho laboratórne stanovenie [1,2]. Deficit vitamínu D je spájaný s incidenciou mnohých ochorení. Známy je vzájomný vzťah hypovitaminózy D so vznikom osteoporózy a osteomalácie [3–5]. V súčasnosti sa pozornosť sústreďuje na koincidenciu hypovitaminózy D s ochoreniami ako diabetes mellitus [6], kardiovaskulárne ochorenia [7], imunologické a onkologické ochorenia [8,9]. Receptory pre vitamín D boli zistené na niekoľkých tkanivách vrátane čreva, žalúdka, pečene, tukového tkaniva, srdcového a kostrového svalstva, obličiek, imunitného systému, centrálneho nervového systému, štítnej žľazy, prištítnych teliesok, nadobličiek a B buniek pankreasu. Vitamín D sa stáva potenciálnym kľúčovým hráčom v rozvoji týchto ochorení. Pod označením vitamín D sa skrýva niekoľko v tukoch rozpustných kalciferolov, pričom 2 hlavné formy – cholekalciferol (vitamín D3) a ergokalciferol (vitamín D2) sú vlastne prohormóny, z ktorých v pečeni vzniká hydroxyláciou 25-hydroxycholekalciferol (kalcidiol), resp. 25-hydroxyergokalciferol, a následne v obličkách definitívna biologicky aktívna forma 1,25-dihydroxycholekalciferol (kalcitriol), resp. 1,25-dihydroxyergkokalciferol [11].
Ukázalo sa, že meranie 25-hydroxy-vitamínu D [25-(OH) D] je optimálny ukazovateľ stavu saturácie vitamínu D v organizme [12,13]. Na stanovenie 25-(OH) D sa v súčasnosti využívajú najmä 2 typy metód: imunochemické (rádioimunoanalýza, chemiluminiscenčná imunoanalýza, elektro-chemiluminiscenčná imunoanalýza, enzýmová imunoanalýza) a separačné (vysokoúčinná kvapalinová chromatografia, kvapalinová chromatografia – tandemová hmotnostná spektrometria) [14,15]. Široké spektrum dodávateľov ponúka automatizované imunochemické stanovenie, ktoré jednoznačne urýchlilo stanovenie 25-(OH) D [16,17]. Rozdiely medzi imunochemickými stanoveniami môžu byť markantné, čo môže viesť k sťaženej interpretácii výsledkov [18–20]. Naša práca informuje o výsledkoch porovnania troch automatizovaných imunochemických metód stanovenia 25-(OH) D s metódou HPLC.
Súbor pacientov a metodika
Vzorky
Pre účel tejto štúdie bolo vybratých celkovo 109 probandov s vekom 17–86 rokov (priemer 56,89). Z toho bolo 13 mužov s vekom 31–77 rokov (priemer 56,3) a 96 žien s vekom 17–86 rokov (priemer 56,9). Žiadne bližšie kritériá okrem rutinne stanovenej hladiny 25-(OH) D neboli pri výbere aplikované. Na analýzu boli použité pacientske vzorky venóznej krvi, ktoré boli odobraté za štandardných podmienok a u ktorých bolo indikované vyšetrenie 25-(OH) D lekármi Národného endokrinologického a diabetologického ústavu v Ľubochni. Vzorky boli po doručení do laboratória štandardne odstredené a po vykonaní analýz indikovaných lekármi boli zvyšné séra odpipetované do alikvotačných skúmaviek (pre každú metódu osobitne), označené a uskladnené pri -30 °C v laboratóriu klinickej biochémie a hematológie v Ľubochni (Alphamedical, s.r.o.). Po nazbieraní dostatočného počtu vzoriek boli, v zamrazenom stave, transportované do cieľových pracovísk: oddelenie klinickej biochémie firmy Klinická biochémia, s.r.o. v Žiline, laboratórium špeciálnych metód v Bratislave firmy Alphamedical, s.r.o. Každá analýza bola vykonaná z čerstvo rozmrazenej alikvotnej časti.
Metódy stanovenia 25-(OH) D
Na stanovenie celkového 25-(OH) D vo vzorkách boli použité komerčné chemiluminiscenčné imunochemické metódy od firmy Diagnostic/Architect, Siemens/Centaur a Roche Diagnostic/Cobas. Zo separačných metód bola použitá HPLC s UV detekciou od firmy Immundiagnostik AG (Bensheim, Germany) – set na stanovenie 25-(OH) D3/D2 RP – HPLC Kit (Article Nr. KC3000). Metóda HPLC-UV bola považovaná v našej práci za referenčnú. Meranie bolo vykonané na niekoľkých pracoviskách. Pracovisko Alphamedical, s.r.o. v Ľubochni analyzovalo vzorky na analyzátoroch Centaur XP (Siemens) a Cobas e411 (Roche). Na oddelení klinickej biochémie v Žiline firmy Klinická biochémia, s.r.o. boli vzorky vyšetrené na analyzátore Architect i2000 (Abbott) a laboratórium špeciálnych metód v Bratislave firmy Alphamedical, s.r.o. zabezpečilo analýzu separačnou metódou HPLC.
AdviaCentaur celkový vitamín D
Jedná sa o 18-minútovú protilátkovú kompetitívnu imunoanalýzu, ktorá využíva monoklonálnu myšiu protilátku proti fluoresceínu kovalentne spojenú s paramagnetickými časticami, monoklonálnu myšiu protilátku proti 25-(OH) D označenú esterom akridínu a analóg vitamínu D označený fluoresceínom. Existuje recipročný vzťah medzi množstvom vitamínu D prítomným vo vzorke pacienta a množstvom relatívnych svetelných jednotiek (RLU) zistených systémom [21]. Výrobca udáva skríženú reaktivitu s inými metabolitmi (3-epi-25(OH) vitamínu D3, parikalcitol, vitamín D2, vitamín D3, 1,25(OH)2 D2, 1,25(OH)2 D3, ktorá však podľa jeho vyhlásenia je minimálna.
Architect 25-OH Vitamín D
Metóda je oneskorená jednokroková chemiluminiscenčná imunoanalýza na mikročasticiach (CMIA – Chemiluminscent Microparticle Immunoassay) k kvantitatívnemu stanoveniu 25-(OH) D v ľudskom sére a plazme. Táto metóda využíva ovčiu polyklonálnu protilátku proti ľudskému vitamínu D triedy IgG v TRIS pufry. Množstvo vitamínu D vo vzorke je nepriamo úmerné signálu v jednotkách RLU detegovaného optikou systému ARCHITECT iSystem [22]. Aj tu výrobca deklaruje krížovú reaktivitu už spomínaných metabolitov, ktorá je podľa jeho vyhlásenia minimálna.
Elecsys Vitamin D total
Jedná sa o kompetitívny elektrochemiluminiscenčný väzobný test. Súprava Elecsys vitamin D total využíva proteín viažuci vitamín D (VDBP) ako vychytávajúci proteín, na ktorý sa viaže 25-(OH) D3 a 25-(OH) D2. Stanoveniu predchádza denaturácia a uvoľnenie 25-(OH) D z väzby na VDBP. Metóda je založená na väzbe 25-(OH) D s rutheniom značeným VDBP. Následne je pridaný biotínom značený 25-(OH) D, dôjde ku kompetícii o väzobné miesta na rutheinilovanom VDBP. Po pridaní streptavidínom potiahnutých mikročastíc prebehne interakcia biotín-streptavidín. Nenaviazané zložky sú odstránené. Privedené napätie na elektróde vyvolá chemiluminscenčnú emisiu fotónov. Emitované fotóny sú zmerané fotonásobičom a množstvo 25-(OH) D vo vzorke je nepriamo úmerné s množstvom emitovaných fotónov [23]. Výrobca udáva značnú skríženú reaktivitu s C3-epimérom-25 hydroxivitamínu D3 a 24,25-dihydroxy vitamínom D3. Ostatné metabolity vykazujú minimálnu skríženú reaktivitu.
25-OH Vitamin D3/D2 RP – HPLC
Separačná metóda HPLC s obrátenou fázou je určená pre kvantitatívne stanovenie 25-(OH) D3 a 25-(OH) D2 v sére a plazme. Ide o test, v ktorom vlastnú analýzu vzorky predchádza jednoduchá príprava vzorky pozostávajúca z kombinácie precipitácie a extrakcie. Separácia HPLC prebieha v izokratickom režime pri 30 °C na kolóne s „reverznou fázou“. Rozmer kolóny je 125 × 4 mm, prietoková rýchlosť 1 ml/min. Formy 25-(OH) D sú detegované pomocou UV detektora pri 264 nm. Limit detekcie pre 25-(OH) D3 je 7 nmol/l a pre 25-(OH) D2 9,4 nmol/l. Linearita 25-(OH) D3/D2 je do 1 250 nmol/l. Výťažnosť pre 25-(OH) D3 je 109,8 % a pre 25-(OH) D2 102,8 %. Špecificita metódy bola testovaná porovnaním retenčných časov zmesí štandardných roztokov 25-(OH) D3/D2 s kalibrátorom. Minimálne rozdiely medzi retenčnými časmi (< 3 %) umožňujú spoľahlivú identifikáciu píkov. Pridaním metabolitov [1,25-(OH)2 D3/D2, 24,25-(OH)2 D3] nebola pozorovaná interferencia. Separácia trvá 15 minút pre každý beh. Výsledky sa kvantifikujú podľa kalibrátora a vypočítavajú sa externým štandardným spôsobom stanovením výšky píku. Systém využíva jednobodovú kalibráciu a má 2 hladiny kontrol [24]. Pri analýze pacientskych vzoriek, pre účely predkladanej práce, boli použité kalibrátory výrobcu s cieľovými koncentráciami pre 25-(OH) D3 =142 nmol/l a pre 25-(OH) D2 =185 nmol/l. Pre kontrolu kvality boli použité lyofilizované kontrolné materiály výrobcu s cieľovými hodnotami pre 25-(OH) D3, L1 = 51,8, resp. L2 = 89,9 nmol/l, a pre 25-(OH) D2, L1 = 116,7, reps. L2 = 209,1 nmol/l. Celkovo bolo vykonaných 24 kontrolných meraní, 6 kontrolných meraní pre každý analyt a kontrolnú hladinu. Priemerná nameraná koncentrácia pre 25-(OH) D3 bola L1 = 47,1 nmol/l (bias = -9,14 %) a L2 = 87,5 nmol/l (bias = -2,69 %). Priemerná nameraná koncentrácia pre 25-(OH) D2 bola: L1 = 119,7 nmol/l (bias = -1,30 %) a L2 = 209,1 nmol/l (bias = -3.83 %). Žiadne z kontrolných meraní neprekročilo definovaný limit ± 21,5 %.
Štatistická analýza
Na porovnanie metód bola použitá regresná analýza podľa Passing-Babloka a Bland-Altmanova analýza diferencií. Za maximálne akceptovateľné diferencie v jednotlivých výsledkoch boli považované hodnoty v rozmedzí ± 21,5 %. Toto kritérium bolo zvolené na základe CDC Vitamin D Standardization-Certification Program (VDSCP). Kritérium tak bolo vypočítané, z podmienok pre bias = 5 % a pre precíznosť = 10 %, podľa vzťahu TEA = 1,65 * CV + bias. Pre účely korelačnej analýzy boli, vzhľadom na negaussovské rozdelenie dát, použité Spearmanove korelačné koeficienty. Za štatisticky významné boli považované hodnoty P ≤ 0,05. Hodnoty 25-(OH) D2 a 25-(OH) D3 namerané pomocou HPLC boli sčítané a uvedené ako 25-(OH) D. Stredné koncentrácie 25-(OH) D, D2 a D3 boli vyjadrené formou mediánu spolu s interkvartilovým rozsahom (IQR). Miera zhody v interpretácii nameraných výsledkov celkového vitamínu D bola vyhodnotená jednak na základe odporúčaných kritérií pre centrálnu Európu [26] a následne na základe metódo-špecifických rozhodovacích limitov, ktoré boli získané prepočtom odporúčaných kritérií pomocou regresných rovníc. Na vyhodnotenie dát bol použitý MedCalcStatistical Software version 13.1.2 (MedCalc Software bvba, Ostend, Belgium; http://www.medcalc.org; 2014) a Microsoft Excel (2013).
Výsledky
Najväčšia stredná koncentrácia 25-(OH) D bola zaznamenaná u metódy ROCHE (medián = 91,02 nmol/l, IQR = 42,58–123,1 nmol/l), potom u metódy HPLC (medián = 71,8 nmol/l, IQR = 38,55–100,4 nmol/l), následne u metódy ABBOTT (medián = 67,93 nmol/l, IQR = 32,28–91,35 nmol/l) a nakoniec u metódy SIEMENS (medián = 51,73 nmol/l, IQR = 18,01–70,12 nmol/l). Koncentrácia 25-(OH) D bola determinovaná takmer výlučne 25-(OH) D3. Metóda HPLC poukázala na strednú koncentráciu 25-(OH) D3 = 71,9 nmol/l (IQR = 44,08–100,0 nmol/l). Medián 25-(OH) D2 z celého súboru výsledkov nebol kvantifikovateľný. Merateľná koncentrácia 25-(OH) D2 bola zaznamenaná iba v 7 prípadoch. Medián 25-(OH) D2 z tohto súboru výsledkov bol 30,4 nmol/l (IQR = 23,45–115,8 nmol/).
Namerané výsledky 25-(OH) D pomocou 3 imunochemických metód boli porovnané s metódou HPLC ako aj navzájom medzi sebou pomocou regresnej analýzy podľa Passing-Babloka. Výsledky tejto analýzy sú zhrnuté v tab. 1 a graficky je znázorňuje graf 1. Spomedzi porovnávaných metód bola korelácia medzi HPLC a ABBOTT najlepšia (R = 0,873, P < 0,0001), potom medzi HPLC a ROCHE (R = 0,849, P < 0,0001) a nakoniec medzi HPLC a SIEMENS (R = 0,842, P < 0,0001). Pri porovnaní imunochemických metód navzájom bola zistená najlepšia korelácia medzi SIEMENS a ABBOTT (R = 0,972, P < 0,0001), potom medzi ROCHE a ABBOTT (R = 0,923, P < 0,0001) a nakoniec medzi SIEMENS a ROCHE (R = 0,904, P < 0,0001).
Tab. 1. Porovnanie metód stanovenia 25-(OH) D pomocou regresnej analýzy podľa Passing-Babloka 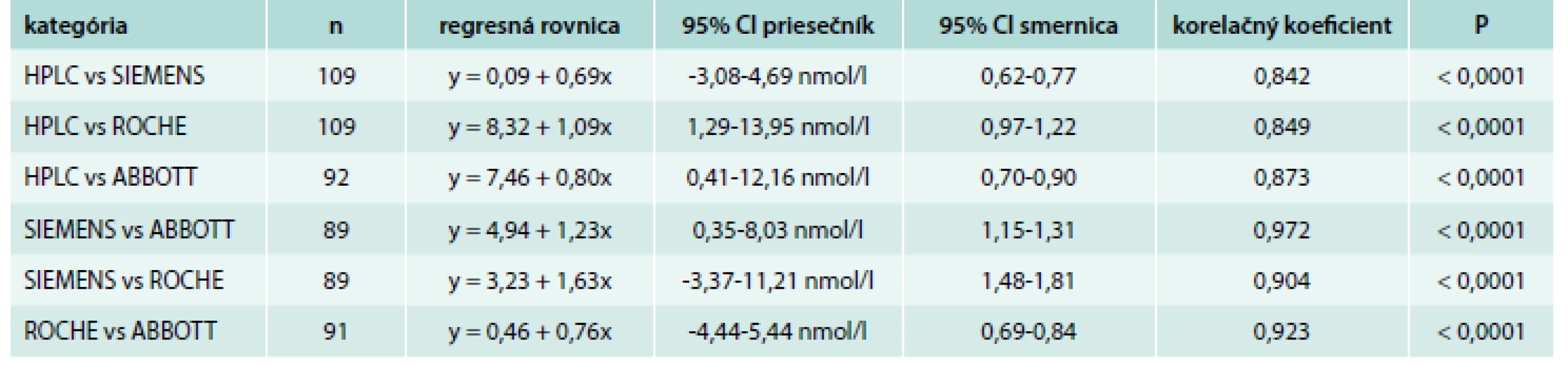
Hodnota P predstavuje štatistickú významnosť korelácie. 95% CI znamená 95% interval spoľahlivosti. Graf 1. Sumárny regresný graf z porovnania vybraných imunochemických metód s HPLC 
Bias medzi imunochemickými metódami a metódou HPLC bol vyhodnotený pomocou Bland-Altmanovej analýzy. Výsledky tejto analýzy graficky znázorňuje graf 2. Spomedzi porovnávaných metód bol zaznamenaný najmenší priemerný bias medzi metódou HPLC a ABBOTT (-0,2 %), potom medzi HPLC a SIEMENS (23,4 %) a nakoniec medzi HPLC a ROCHE (-28,0 %).
Graf 2. Bland-Altmanove grafy porovnania rutinných imunochemických metód stanovenia 25-(OH) D vyjadrujúce priemerný relatívny bias. 
(A) HPLC-UV vs SIEMENS, (B) HPLC-UV vs ABBOTT, (C) HPLC-UV vs ROCHE. Neprerušovaná línia reprezentuje priemerný relatívny bias, prerušovaná línia s bodkou regresnú priamku diferencií a prerušované línie limity zhody (bias ± 1,96 SD) Pri vzájomnom porovnaní imunochemických metód bol zaznamenaný najmenší priemerný bias medzi metódou ROCHE a ABBOTT (22,8 %), potom medzi SIEMENS a ABBOTT (-32,1 %) a nakoniec medzi SIEMENS a ROCHE (-53,6 %).
V tab. 2 je znázornená miera zhody v klasifikácii výsledkov 25-(OH) D s ohľadom na odporúčané ako aj metódo-špecifické rozhodovacie limity. Na základe odporúčaných kritérií bola medzi metódou HPLC a ABBOTT zhoda v 65,22 %, medzi metódami HPLC a ROCHE v 59,63 % a medzi metódou HPLC a SIEMENS 46,79 % prípadov. Miera falošnej negativity výsledkov bola najväčšia u metódy SIEMENS (50,46 %), potom u metódy ABBOTT (30,43 %) a nakoniec u metódy ROCHE (11,93 %). Miera falošnej pozitivity bola naopak najvyššia u metódy ROCHE (28,44 %), potom u metódy ABBOTT (4,35 %) a nakoniec u metódy SIEMENS (2,75 %). Pri interpretácii výsledkov na základe metódo-špecifických rozhodovacích limitov bola medzi metódou HPLC a ABBOTT zhoda v 67,39 %, medzi metódami HPLC a ROCHE v 66,06 % a medzi metódou HPLC a SIEMENS v 65,14 % prípadov. Z tohto jednoduchého experimentu je zrejmé, že miera zhody sa vylepšila u všetkých troch imunochemických metód s najvýraznejším zlepšením u metódy SIEMENS (46,79 % vs 65,14 %) a je porovnateľná u všetkých 3 metód. Podobne došlo aj k rovnomernejšiemu rozloženiu falošne negatívnych a pozitívnych výsledkov.
Tab. 2. Zhoda v klasifikácii nameraných výsledkov 25-(OH) D s ohľadom na odporúčania pre centrálnu Európu, resp. na metódo-špecifické rozhodovacie limity 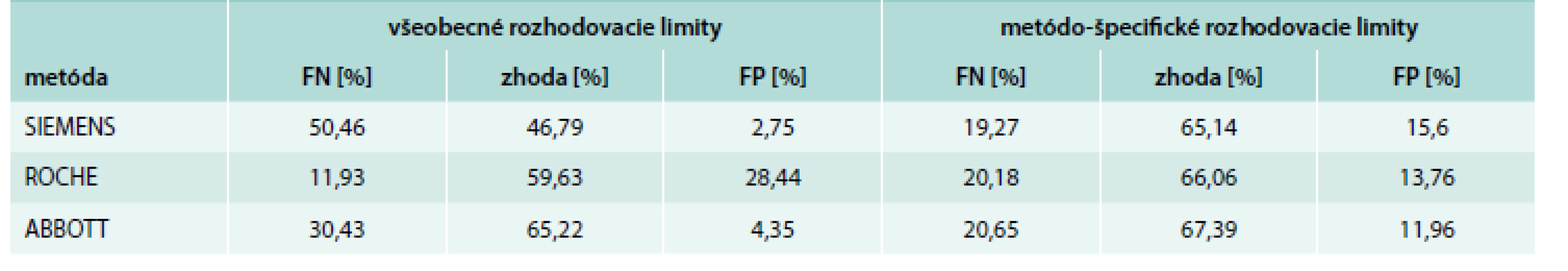
FN – falošná negativita FP – falošná pozitivita Diskusia
Stanovenie hladiny 25-(OH) D sa stáva predmetom záujmu mnohých medicínskych špecializácií. Klinické laboratóriá sa musia vysporiadať s narastajúcim počtom indikácií stanovenia hladiny 25-(OH) D. I keď sa za referenčnú metódu považuje metóda LC-MS/MS, tá je pre svoju prístrojovú, ekonomickú náročnosť a náročnosť na obsluhu v rutinných podmienkach laboratórií nahradzovaná imunochemickými metódami, ktoré v súčasnosti poskytujú viacerí výrobcovia IVD prostriedkov [26]. Výber metódy je na rozhodnutí laboratórií, pričom neexistuje jednoznačný návod, ktorý by pomohol pri výbere najvhodnejšej metódy. Situáciu výrazne komplikuje nízka úroveň štandardizácie metód, ktorá spolu so všeobecnými cut-off hodnotami pre hodnotenie statusu 25-(OH) D môže v konečnom dôsledku skomplikovať klinické rozhodovanie. Už niekoľko autorov zaoberajúcich sa touto problematikou poukazuje na riešenie situácie, pričom poukazujú na nutnosť štandardizácie metód s vhodným referenčným materiálom [15], prípadne vytvorením metódo-špecifických referenčných intervalov[16,26,27]. V tejto štúdii sme sa zamerali na porovnanie 3 imunochemických metód stanovenia 25-(OH) D s HPLC, ktoré sa podľa nášho názoru a skúseností, využívajú v rutinnej praxi najčastejšie. Počas trvania tejto štúdie mali všetky použité imunochemické metódy vydaný certifikát VDSCP (Vitamin D Standardization-Certification Program). Tento certifikát sa vydáva pre metódy, ktoré splnia certifikačné podmienky, bias ≤ 5 % a precíznosť ≤ 10 %, od CDC a University of Ghent Vitamin D2 and D3 referenčných metód v rozsahu 22,5–275 nmol/l. Výsledky regresnej analýzy ako aj analýzy diferencií v tejto práci poukázali na významné rozdiely medzi skúmanými metódami. K podobným záverom sa dopracovali viaceré publikované štúdie [28–34].
Namerané výsledky 25-(OH) D sme podrobili aj interpretácii s ohľadom na všeobecné rozhodovacie limity platné pre centrálnu Európu [26]. Tieto odporúčania rozoznávajú 6 pásiem koncentrácie 25-(OH) D: < 50 nmol/l (deficit), 50–75 nmol/l (suboptimum), 75–125 nmol/l (adekvátny status), 125–250 nmol/l (nadmerná zásoba), 250–500 nmol/l (riziková koncentrácia), > 500 nmol/l (toxicita). Na základe týchto kritérií bola medzi metódami značná diverzita v miere zhody ako aj v miere falošne negatívnych a pozitívnych výsledkov. Po prepočte rozhodovacích limitov pomocou regresných rovníc pre každú metódu sa miera zhody ako aj miera falošne negatívnych a pozitívnych výsledkov ustálila na približne rovnakej úrovni naprieč všetkými metódami, pričom vo všetkých prípadoch došlo k zlepšeniu týchto ukazovateľov.
I keď štandardizácia je najčastejšie skloňovaným problémom, je nutné zmieniť aj iné potencionálne zdroje príčin diskrepancií medzi výsledkami 25-(OH) D. Viacerí autori v literatúre poukazujú na ďalšie príčiny, ktoré môžu spôsobiť značné rozdiely medzi metódami stanovenia 25-(OH) D. Podľa nich sa javia ako problematické metabolity vitamínu D, napr. 3-epi-25 hydroxivitamín D, 24,25-dihydroxyvitamin D, rozdielna imunoreaktivita 25-(OH) D2 a 25-(OH) D3, heterofilné protilátky, VDBP (Vitamin D Binding Protein) [35–37].
Záver
Úroveň štandardizácie metód stanovenia 25-(OH) D je i doposiaľ nedostatočná a spolu s ďalšími faktormi môže skresľovať klinické rozhodovanie, čo môže viesť k neadekvátnym terapeutickým postupom. Nedá sa očakávať, že sa situácia v blízkej budúcnosti významne zmení, a preto je vhodné uvažovať aspoň o používaní na metóde závislých rozhodovacích limitov, ktoré môžu pri najmenšom zlepšiť interpretáciu výsledkov 25-(OH) D naprieč rôznymi rutinne používanými metódami.
Mgr. Anton Vaňuga
vvanuga@nedu.sk
Národný endokrinologický a diabetologický ústav, n.o.,
Ľubochňa,
Slovenská republika
www.nedu.sk
Doručeno do redakce 9. 3. 2017
Přijato po recenzi 27. 6. 2017
Zdroje
1. Cannell JJ, Hollis BW, Zasloff M et al. Diagnosis and treatment of vitamin D deficiency. Expert Opin Pharmacother 2008; 9(1): 107–118.
2. Huibers MH, Visser DH, Deckers MM et al. Vitamin D deficiency among native Dutch and first – and second generationnon – Westernimmigrants. Eur J Pediatr 2014; 173(5): 583–588. Dostupné z DOI: <http://dx.doi.org/10.1007/s00431–013–2198-x>.
3. Bischoff-Ferrari HA, Dietrich T, Orav EJ et al.l Positive association between 25-hydroxy vitamin D levels and bone mineral density: a population-based study of younger and older adults. Am J Med 2004; 116(9): 634–639.
4. Murad MH, Elamin KB, Abu Elnour NO et al. Clinical review: The effect of vitamin D on falls: a systematic review and meta-analysis. J Clin Endocrinol Metab 2011; 96 : 2997–3006. Dostupné z DOI: <http://dx.doi.org/10.1210/jc.2011–1193>.
5. Bentley J. The role of vitamin D in infants, children and young people. Nurs Child Young People 2015; 27(1): 28–35; quiz 36. Dostupné z DOI: <http://dx.doi.org/10.7748/ncyp.27.1.28.e508>.
6. Pittas AG, Lau J, Hu FB et al. The role of vitamin D and calcium in type 2 diabetes. A systematic review and meta-analysis. J Clin Endocrinol Metab 2007; 92(6): 2017–2029.
7. Forman JP, Bischoff-Ferrari HA, Willett WC et al. Vitamin D intake and risk of incident hypertension: results from three large prospective cohort studies. Hypertension 2005; 46 : 676–682.
8. Grant WB. How strong is the evidence that solar ultraviolet B and vitamin D reduce the risk of cancer? An examination using Hill’s criteria for causality. Dermatoendocrinol 2009; 1(1): 17–24.
9. Melamed ML, Michos ED, Post W et al. 25-hydroxyvitamin D levels and the risk of mortality in the general population. Arch Intern Med 2008; 168(15): 1629–1637. Dostupné z DOI: <http://dx.doi.org/10.1001/archinte.168.15.1629>.
10. Garland CF, Gorham ED, Mohr SB et al. Vitamin D for cancer prevention: global perspective. Ann Epidemiol 2009; 19(7): 468–483. Dostupné z DOI: <http://dx.doi.org/10.1016/j.annepidem.2009.03.021>.
11. Saenger AK, Laha TJ, Bremner DE et al. Quantification of serum 25-hydroxyvitamin D(2) and D(3) using HPLC-tandem mass spectrometry and examination of reference intervals of or diagnosis of vitamin D deficiency. Am J Clin Pathol 2006; 125(6): 914–920.
12. Ross AC, Taylor CL, Yaktine AL et al (eds). [Institute of Medicine (IOM)]. Dietary Reference Intakes for Calcium and Vitamin D. The National Academic Press: Washington (DC) 2011. ISBN 978–0-309–16394–1.
13. Seamans KM, Cashman KD. Existing and potentially novel functional Markers of vitamin D status: a systematic review. Am J Clin Nutr 2009; 89(6): 1997S-2008S. Dostupné z DOI: <http://dx.doi.org/10.3945/ajcn.2009.27230D>.
14. Kwak HS, Chung HJ, Cho DH et al. Efficacy of the measurement of 25-hydroxyvitamin D2 and D3 levels by using Perkin Elmer liquid chromatography-tandem mass spectrometry vitamin D kit compared with Dia Sorinradio immunoassay kit and Elecsys vitamin D total assay. Ann Lab Med 2015; 35(2): 263–265. Dostupné z DOI: <http://dx.doi.org/10.3343/alm.2015.35.2.263>.
15. Tsugawa N, Suhara Y, Kamao M et al. Determination of 25-hydroxyvitamin D in human plasma using high-performance liquid chromatography – tandem mass spectrometry. Anal Chem 2005; 77(9): 3001–3007.
16. Wallace AM, Gibson S, de la Hunty A et al. Measurement of 25-hydroxyvitamin D in the clinical laboratory: current procedures, performance characteristics and limitations. Steroids 2010; 75(7): 477–488. Dostupné z DOI: <http://dx.doi.org/10.1016/j.steroids.2010.02.012>.
17. Janssen MJ, Wielders JP, Bekker CC et al. Multicenter comparison study of current methods to measure 25-hydroxyvitamin D in serum. Steroids 2012; 77(13): 1366–1372. Dostupné z DOI: <http://dx.doi.org/10.1016/j.steroids.2012.07.013>.
18. Carter GD. 25-Hydroxyvitamin D assays: the quest for accuracy. Clin Chem 2009; 55(7): 1300–1302. Dostupné z DOI: <http://dx.doi.org/10.1373/clinchem.2009.125906>.
19. Binkley N, Krueger D, Cowgill CS et al. Assay variation confounds the diagnosis of hypovitaminosis D: a call for standardization. J Clin Endocrinol Metab 2005; 89(7): 3152–3157.
20. Binkley N, Krueger D, Gemar D et al. Correlation among 25-hydroxy-vitamin D assays. J Clin Endocrinol Metab 2008; 93(5): 1804–1808. Dostupné z DOI: <http://dx.doi.org/10.1210/jc.2007–2340>.
21. Siemens Advia Centaur® XP. Celkový vitamín (Vit D) [direction. insert 0699279_SK Rev D]. Siemens Healthcare Diagnostics: Tarrytown (NY) 2016–04.
22. Architect® 25-OH Vitamin D [directional insert 3L52, G2–4021/R03]. Abbott Laboratories. Wiesbaden 2012. Dostupné z WWW: <http://www.ilexmedical.com/files/download/1306390706e06Sh.pdf>.
23. Roche ELECSYS®. Vitamin D total [directional insert 05894913 190, V 7.0 Slovenskz]. Roche Diagnostics GmbH: Mannheim 2016–08.
24. Immunodiagnostik 25-OH-Vitamin D3/D2 RP-HPLC Kit [directional insert KC3000], Immundiagnostik AG: Bensheim 2015–06. Dostupné z WWW: http://www.immundiagnostik.com/fileadmin/pdf/KC3000%20Vitamin%20D3%20D2_RP.pdf
25. Pludowski P, Karczmarewicz E, Bayer M et al. Practical guidelines for the supplementation of vitamin D and the treatment of deficits in Central Europe – recommended vitamin D intakes in the general population and group sat risk of vitamin D deficiency. Endokrynol Pol 2013; 64(4): 319–327.
26. Holick MF, Binkley NC, Bischoff-Ferrari HA et al. Endocrine Society. Evaluation, treatment, and prevention of vitamin D deficiency: an Endocrine Society clinical practice guideline. J Clin Endocrinol Metab 2011; 96(7): 1911–1930. Dostupné z DOI: <http://dx.doi.org/10.1210/jc.2011–0385>. Erratum in J Clin Endocrinol Metab 2011; 96(12): 3908.
27. Ross AC, Taylor CL, Yaktine AL et al. (eds). [Institute of Medicine (US) Committee to Review Dietary Reference Intakes for Vitamin D and Calcium]. Dietary Reference Intakes for Calcium and Vitamin D. National Academies Press: Washington (DC): 2011. ISBN 978–0-309–16394–1.
28. Cavalier E, Dozet E, Gadisseur R et al. Measurement uncertainty of 25-OH vitamin D determination with different commercially available kits: impact on the clinical cutoffs. Osteoporosis Int 2010; 21(6): 1047–1051. Dostupné z DOI: <http://dx.doi.org/10.1007/s00198–009–1052–5>.
29. Cavalier E, Carlisi A, Beckert A et al. Analytical evaluation of the new Abbott Architect 25-OH vitamin D assay. Clin Biochem 2012; 45(6): 505–508. Dostupné z DOI: <http://dx.doi.org/10.1016/j.clinbiochem.2012.01.021>.
30. Lei JK, Lucas RM, Clements MS et al. Assessing vitamin D status: pit falls for the un way. Mol Nutr Food Res 2010; 54(8): 1062–1071. Dostupné z DOI: <http://dx.doi.org/10.1002/mnfr.200900468>.
31. Roth HJ, Schmidt-Gayk H, Weber H et al. Accuracy and clinical implications of seven 25-hydroxyvitamin D compared with liquid chromatography – tandem mass spectrometry as reference. Ann Clin Biochem 2008; 45(Pt 2): 153–159. Dostupné z DOI: <http://dx.doi.org/10.1258/acb.2007.007091>.
32. Farrell CJ L, Martin S, Mc Whinney B et al. State of Art vitamin D assays: A comparison of Automated Immunoassays with Liquid chromatography-Tandem Mass Spectrometry Methods. Clin Chem 2012; 58(3): 531–542. Dostupné z DOI: <http://dx.doi.org/10.1373/clinchem.2011.172155>.
33. Ong L, Saw S, Schabdeen NB et al. Current 25-hydroxyvitamin D assays: Do the ypass the test? Clin Chim Acta 2012; 413(13–14): 1127–1134. Dostupné z DOI: <http://dx.doi.org/10.1016/j.cca.2012.03.009>.
34. Snellman G, Melkus H, Godeborg R et al. Determining vitamin D status, a comparison between commercially available assays. Plos One 2010; 5(7): e11555. Dostupné z DOI: <http://dx.doi.org/10.1371/journal.pone.0011555>.
35. Friedecký B, Vávrová J. Současný stav stanovení vitaminu D v séru. Klin Biochem Metab 2012; 20[41](3): 174–178 .Dostupné z WWW: <http://www.cskb.cz/res/file/KBM-pdf/2012/2012–3/KBM12–3-Fr-vitD-174.pdf>.
36. Carter GD. 25-hydroxyvitamin D: A difficult analyte. Clin Chem 2012; 58(3): 486–488. Dostupné z DOI: <http://dx.doi.org/10.1373/clinchem.2011.180562>.
37. Kricka LJ. Human anti-animal antibody interferences in immunological assays. Clin Chem 1999; 45(7): 942–956.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2017 Číslo 6- Statinová intolerance
- Efekt itopridu na motilitu jícnu a funkci dolního jícnového svěrače
- Vliv doporučené léčby srdečního selhání na riziko vzniku FiS a její účinnost u pacientů s již rozvinutou FiS
- Přínos empagliflozinu v léčbě HFpEF nezávisle na přítomnosti fibrilace síní
- Nattokináza snižuje krevní tlak u experimentálního modelu
-
Všechny články tohoto čísla
- Screening potomků osob s časnou manifestací ICHS – editorial
- Je konečně na řadě primární prevence kardiovaskulárních onemocnění? – editorial
- Význam metabolitů vitaminu D a správnost jejich stanovení – editorial
- Testikulární lymfomy – editorial
- Trombóza a malignita – editorial
- Prediktory kvality života u českých pacientek po léčbě karcinomu prsu se zaměřením na dovednosti zvládání zátěže
- Rizikové faktory kardiovaskulárních onemocnění u potomků nemocných po časném infarktu myokardu
- Úskalia stanovenia vitamínu D
- Klinická štúdia FOURIER
- Primární testikulární lymfomy
- Rivaroxaban u rizikových pacientů
- Dva pohľady na venózny tromboembolizmus u onkologických pacientov
- Inzulinová pumpa u diabetu 2. typu: léčba zaměřená na B-buňku
- Kardiovaskulární mortalita u diabetu
-
Účinnost a bezpečnost dabigatranu při podávání dle SPC a evropských doporučení
Komentář k článku Patient outcomes using the European label for dabigatran - Z odborné literatury
- Z odborné literatury
- Z odborné literatury
- Z odborné literatury
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Primární testikulární lymfomy
- Inzulinová pumpa u diabetu 2. typu: léčba zaměřená na B-buňku
- Úskalia stanovenia vitamínu D
- Dva pohľady na venózny tromboembolizmus u onkologických pacientov
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



