-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Dosavadní zkušenosti s léčbou ropeginterferonem alfa-2b u pacientů s Ph negativními myeloproliferacemi na Interní hematologické a onkologické klinice LF MU a FN Brno
Current experience with ropeginterferon Alfa-2b in Ph negative myeloproliferative neoplasm at the Department of Internal Medicine – Haematology and Oncology in Brno
Background: Ropeginterferon alfa-2b demonstrated efficacy and safety in patients with polycythaemia vera in the PROUD-PV and CONTINUATION-PV multicentric randomised studies. These studies reported the superior effect of ropeginterferon alfa-2b in attaining haematological and molecular remission during the fourth and fifth year of therapy. Patients and Methods: A total of 14 Ph-MPN patients treated with ropeginterferon alfa-2b at our Dept. of Internal Medicine – Haematology and Oncology were analysed from May 2020 to July 2022. Therapy duration, dosing, effect, and tolerance were evaluated. Results: Therapy median duration was 266 days. 14 patients in total were treated; 11 had polycythaemia vera (79%), 2 had essential thrombocythemia (14%), and one patient had secondary myelofibrosis post polycythaemia vera (7%). The median ropeginterferon alfa 2-b dose was 150 μg. Complete haematological remission was attained in 11 (79%) patients. Two patients (14%) had to discontinue treatment. During therapy, six patients (43%) suffered adverse events; only one patient (7%) developed a thromboembolic event. Conclusion: Our initial experience has confirmed the promising effect of ropeginterferon alfa 2-b on haematocrit control and its excellent tolerance among patients.
Keywords:
polycythemia vera – Ph negative myeloproliferative neoplasms – ropeginteferon alpha-2b
Autoři: N. Podstavková 1; B. Weinbergerová 1; J. Procházková 1; M. Bohúnová 2; A. Marečková 2; J. Kotašková 2; I. Ježíšková 2; M. Doubek 1; J. Mayer 1,2
Působiště autorů: Interní hematologická a onkologická klinika, LF MU a FN Brno 1; Centrum molekulární bio logie a genetiky, Interní hematologická a onkologická klinika LF MU a FN Brno 2
Vyšlo v časopise: Transfuze Hematol. dnes,28, 2022, No. 4, p. 213-218.
Kategorie: Původní práce
doi: https://doi.org/10.48095/cctahd2022prolekare.cz15Souhrn
Úvod: Ropeginterferon alfa-2b (RopegIFN) prokázal účinnost a bezpečnost u pacientů s pravou polycytémií v multicentrických randomizovaných studiích PROUD-PV a CONTINUATION-PV. Během 4.–5. roku terapie byl prokázán jednoznačný benefit terapie RopegIFN ve srovnání s nejlepší dostupnou terapií, a to jak ve smyslu dosažení kompletní hematologické remise onemocnění, tak i výrazného snížení mutační alelické zátěže JAK2V617F. Materiál a metodika: Retrospektivní neintervenční analýza byla provedena u celkem 14 pacientů s Ph negativními myeloproliferacemi (Ph-MPN) léčených RopegIFN na Interní hematologické a onkologické klinice (IHOK) v období od května 2020 do července 2022. Hodnocena byla data týkající se délky terapie, dávkování, efektu a tolerance terapie. Výsledky: Medián délky terapie v souboru byl 266 dní. Léčeno bylo celkem 14 pacientů, z toho 11 s pravou polycytémií (79 %), 2 s esenciální trombocytémií (14 %) a 1 se sekundární myelofibrózou po pravé polycytémii (7 %). Medián dávky RopegIFN byl 150 μg. Dosažení kompletní hematologické remise bylo u 11 pacientů (79 %). Terapie byla během doby sledování ukončena u 2 pacientů (14 %). Nežádoucí účinky byly zaznamenány u 6 pacientů (43 %), tromboembolická příhoda byla dokumentována u jednoho pacienta (7 %). Závěr: Naše analýza prvotních zkušeností s terapií RopegIFN potvrdila jeho velmi dobrý efekt na kontrolu hematokritu a zároveň výbornou toleranci u pacientů s Ph-MPN.
Klíčová slova:
pravá polycytemie – Ph negativní myeloproliferativní neoplázie – ropeginterferon alfa-2b
ÚVOD
Ph negativní myeloproliferativní neoplázie představují heterogenní skupinu onemocnění postihujících hematopoetickou kmenovou buňku s následnou aberantní proliferací buněk myeloidní krevní řady, která vede k zvýšené tvorbě erytrocytů, trombocytů a/nebo granulocytů. Mezi nejčastěji se vyskytující podjednotky této skupiny se řadí pravá polycytémie (polycythemia vera – PV), esenciální trombocytémie (ET) a primární myelofibróza (PMF). Mají několik společných znaků; kromě společné patogeneze je pojí obdobný klinický obraz, zvýšený výskyt trombotických a krvácivých komplikací a riziko fibrotické a leukemické transformace. Jednotlivé nozologické jednotky se od sebe navzájem odlišují především dlouhodobou prognózou [1].
Pravá polycytémie, nejčastěji se vyskytující jednotka ze skupiny Ph negativních myeloproliferativních onemocnění, je charakterizována především zmnožením červené krevní řady, často provázené i zvýšením počtu leukocytů a trombocytů [2]. V patogenezi onemocnění hraje klíčovou roli mutace JAK2V617F, přítomná u více než 95 % pacientů s PV. To vede k poruše regulace dráhy JAK/STAT (Janus kinase/signal transducers and activators of transcription), a tím k podpoře nekontrolované proliferace hematopoetických kmenových buněk a zároveň prozánětlivého prostředí v organizmu [2,3]. Kvalitu života pacientů s PV výrazně zhoršují příznaky, jako jsou svědění kůže, únava a poruchy mikrocirkulace. Největším problémem vedoucím ke zvýšené mortalitě a zkrácení délky života této skupiny nemocných oproti zdravé populaci zůstává vysoká četnost trombotických a krvácivých příhod [4].
Možnosti terapie pacientů s PV i přes významný pokrok v terapii hematologických malignit zůstávají limitované. Hlavním cílem terapie u této skupiny onemocnění je snížení rizika vzniku trombotických příhod a oddálení leukemické transformace [4]. Interferon, jako dosud jediný ze skupiny cytoredukční terapie, prokázal u vysokého procenta pacientů navození nejen hematologické, ale i molekulární remise trvající i několik let po ukončení léčby [5]. Vzhledem k absenci teratogenity a leukemogenního transformačního potenciálu je nyní považován za jeden z nejlepších léčivých přípravků na dlouhodobou terapii pacientů nejen s PV, ale i s esenciální trombocytémií a primární myelofibrózou [6]. Interferony-alfa jsou součástí léčebného přístupu u Ph-MPN již více než 40 let, běžnému použití v klinické praxi ale bránila především vyšší četnost jejich nežádoucích účinků ve srovnání s konvenční terapií a jejich off-label použití [7]. Během posledních let vývoj nových pegylovaných forem interferonu-alfa s lepšími farmakokinetickými vlastnostmi a profilem nežádoucích účinků výrazně zvýšil zájem o tuto léčbu u pacientů s Ph-MPN [4]. Díky tomu se terapie pegylovanými formami interferonu rozšířila a stala se součástí oficiálních ELN (European LeukemiaNet) doporučení z roku 2021 do 1. linie terapie pacientů s PV s nízkým rizikem [8].
Ropeginterferon alfa-2b (Besremi®) je v současnosti jako jediný z pegylovaných interferonů schválen a registrován v ČR pro terapii pacientů s PV bez symptomatické splenomegalie. Efektivita a bezpečnost tohoto preparátu byla ověřena v multicentrických randomizovaných studiích PROUD-PV a CONTINUATION-PV, kde byl srovnáván s nejlepší dostupnou terapií, hydroxyureou [9]. Výsledky této studie prokázali v 36. měsíci terapie signifikantně vyšší podíl dosažení celkové hematologické odpovědi a zároveň snížení alelické nálože mutace JAK2V617F ve skupině léčené RopegIFN oproti skupině léčené hydroxyureou [9]. Vysoká alelická nálož mutace JAK2V617F byla identifikována jako rizikový faktor pro vznik trombotických komplikací a taktéž fibrotické transformace u pacientů s PV a ET [10].
Účinnost terapie RopegIFN je dále ověřována i u jiných podtypů Ph-MPN, aktuálně probíhá otevřená multicentrická randomizovaná studie fáze III, SURPASS-ET, hodnotící bezpečnost a efektivitu RopegIFN v srovnání s anagrelidem v rámci druhé linie terapie u pacientů s ET vysokého rizika [11].
Tato práce představuje dosavadní výsledky léčby RopegIFN u pacientů s Ph-MPN v běžné klinické praxi a srovnává je s výsledky léčby v kontrolovaných klinických studiích.
MATERIÁL A METODIKA
Provedli jsme retrospektivní neintervenční analýzu dat týkající se dávkování, efektu a bezpečnosti terapie RopegIFN u pacientů s Ph-MPN sledovaných na IHOK od května 2020 do července 2022.
Zdrojová data byla čerpána z dokumentace pacientů a taktéž z databáze České leukemické skupiny pro život (the Czech Leukemia Study Group – for Life – CELL) pro Ph-MPN (Myeloproliferative Neoplasia Database – MIND).
Parametry krevního obrazu byly sledovány v pravidelných intervalech, kvantita alelické nálože mutace JAK2V617F z periferní krve byla vyšetřována každé 3 měsíce terapie. Analýza přídatných genetických změn byla provedena pomocí NGS (next-generation sequencing) periferní krve před zahájením terapie a následně v pravidelných ročních intervalech. V rámci myeloidního panelu bylo analyzováno celkem 37 genů. Toxicita terapie byla hodnocena podle Společných terminologických kritérií pro nežádoucí účinky – CTCAE (Common Terminology Criteria for Adverse Events) verze 5.0. z roku 2017 [12]. Léčebný efekt byl hodnocen podle společných kritérií ELN a IWG-MRT (International Working Group-Myeloproliferative Neoplasms Research and Treatment) [13]. Trombotické riziko u PV bylo posouzeno na základě věku pacienta a trombotické události v anamnéze, u ET podle tzv. „IPSET skóre“ (International Prognostic Score of Thrombosis in Essential Thrombocytemia) [14,15].
VÝSLEDKY
Ve sledovaném období bylo na IHOK léčeno RopegIFN celkem 14 pacientů. Kompletní charakteristiku sledovaného souboru ukazuje tab. 1. Medián věku pacientů byl 51 let. Dominantně byli zastoupeni pacienti s PV (79 %, n = 11), 2 s ET (14 %) a 1 pacient se sekundární myelofibrózou po PV (7 %), u kterého nebyly přítomné splenomegalie ani konstituční symptomy. V hodnoceném souboru převažovali pacienti, kteří byli v čase diagnózy v nízkém trombotickém riziku (71 %, n = 10) (tab. 1).
Tab. 1. Základní charakteristika souboru pacientů (n = 14). 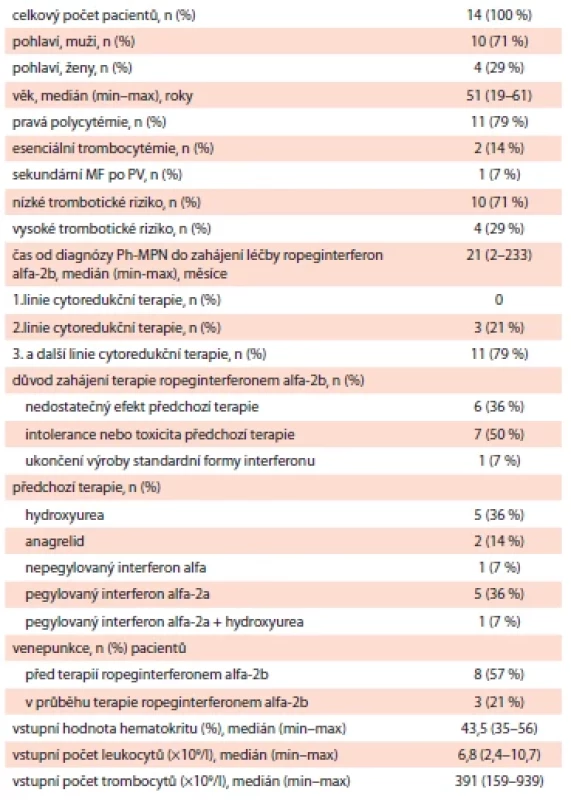
MF po PV – myelofi bróza po pravé polycytémii; Ph-MPN – Ph negativní myeloproliferativní neoplázie Medián času od stanovení diagnózy Ph-MPN do zahájení terapie RopegIFN byl 21 měsíců (min. – 2 měsíce; max. – 233 měsíců). U žádného pacienta nebyl RopegIFN podáván v rámci první léčebné linie, u většiny nemocných se jednalo o třetí nebo vyšší linii terapie. Co se týče důvodů nasazení této terapie, až u poloviny sledovaných se jednalo o toxicitu nebo intoleranci předchozí léčby (50 %, n = 7), u 6 pacientů byl důvodem nedostatečný efekt dosavadní léčby (43 %) a u jednoho pacienta byla terapie nasazena po ukončení výroby standardní formy interferonu (7 %, n = 1). Před nasazením terapie RopegIFN bylo 5 pacientů (36 %) léčeno pegylovaným interferonem alfa-2a, 5 pacientů (36 %) hydroxyureou, 2 pacienti (14 %) užívali anagrelid, 1 pacient (7 %) byl na terapii nepegylovaným interferonem-alfa a rovněž 1 pacient (7 %) byl na kombinované terapii pegylovaným interferonem alfa-2a a hydroxyureou. Před zahájením terapie RopegINF byly venepunkce součásti terapeutického postupu u 8 pacientů (57 %), v průběhu léčby RopegINF byly venepunkce nutné pouze u 3 pacientů (21 %).
Medián délky terapie v souboru byl 266 dní. Přehled nejdůležitějších informací o průběhu terapie RopegIFN zobrazuje tab. 2. U všech pacientů byla účinná dávka podávána každých 14 dnů, u jednoho pacienta došlo za dobu sledování k přechodu do udržovací terapie, a tedy prodloužení aplikace na jednou za 4 týdny. Iniciální dávka byla u 11 pacientů (79 %) 50 µg, u zbylých 3 pacientů (21 %) byla úvodní dávka 100 µg. Dávka byla postupně navyšována dle efektu a tolerance (medián – 150 μg, min. – 50 μg, max. – 250 μg).
Tab. 2. Základní charakteristika průběhu terapie ropeginterferonem alfa-2b (n = 14). 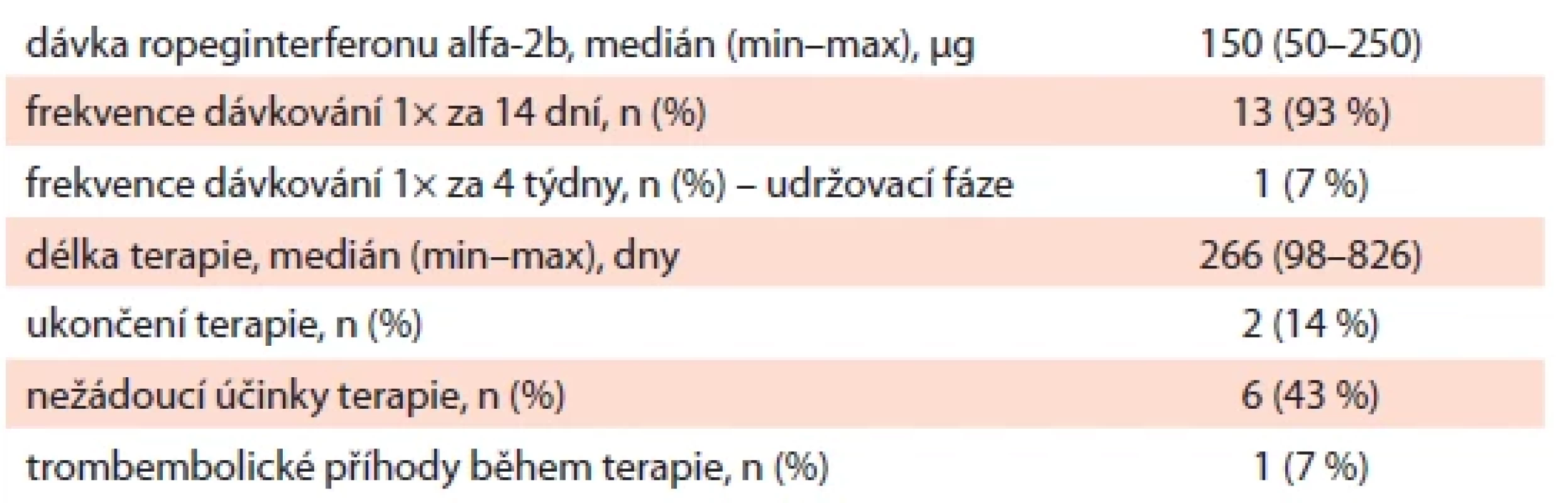
Během sledovaného období došlo u všech pacientů v souboru ke stabilizaci a postupnému poklesu hodnoty hematokritu (graf 1). U pacientů s ET během sledovaného období byl zaznamenán pozvolný pokles trombocytémie. Kompletní hematologické remise bylo dosaženo u 11 pacientů (79 %), medián doby do dosažení této odpovědi byl 5 měsíců.
Graf 1. Vývoj mediánu hladiny hematokritu od zahájení léčby ropeginterferonem alfa-2b ve sledovaném souboru. 
Vývoj mutační alelické nálože JAK2V617F v průběhu léčby RopegIFN ukazuje podrobně tab. 3. Během sledovaného období došlo u všech sledovaných k postupnému poklesu alelické nálože JAK2V617F (graf 2). Při zahájení terapie bylo provedeno vyšetření NGS periferní krve u celkem 12 pacientů, u 7 (58 %) z nich byla přítomna pouze mutace JAK2V617F, u 4 pacientů (33 %) byly zachyceny i další přídatné mutace, konkrétně ASXL1, DNMT3A a DDX41, u jednoho pacienta (9 %) nebyla prokázaná přítomnost žádné mutace z vyšetřovaného myeloidního panelu. V druhém roku terapie byla NGS analýza provedena u 7 pacientů, u naprosté většiny vyšetřených (n = 6; 86 %) byly výsledky shodné s vyšetřením v době zahájení terapie, pouze u jednoho pacienta (14 %) došlo k vymizení mutace JAK2V617F pod detekční hladinu.
Tab. 3. Vývoj mutační alelické zátěže JAK2V617F od zahájení léčby ropeginterferonem alfa-2b ve sledovaném souboru. 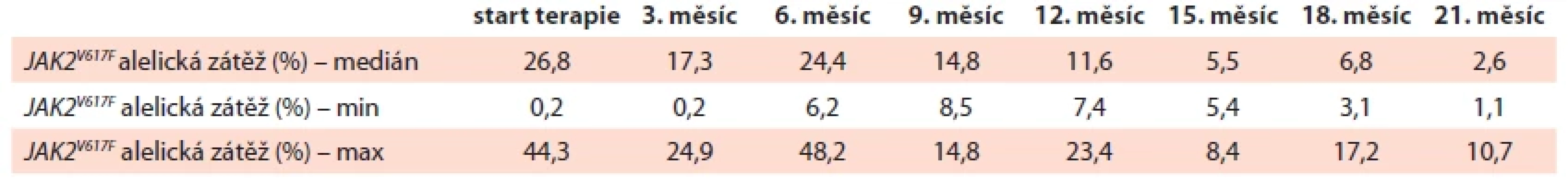
Graf 2. Vývoj mediánu mutační alelické zátěže JAK2V617F od zahájení léčby ropeginterferonem alfa-2b ve sledovaném souboru. 
Terapie byla během doby sledování ukončena u dvou pacientů (14 %), u jednoho pacienta s PV z důvodu progrese onemocnění – přechodu do sekundární myelofibrózy. Následně byla u tohoto pacienta zahájena terapie ruxolitinbem. U druhého pacienta byla terapie RopegIFN předčasně ukončena z důvodu neschválení pokračování terapie zdravotní pojišťovnou, dále byl pacient převeden na léčbu pegylovaným interferonem alfa-2a.
Nežádoucí účinky léčby byly zaznamenány u celkem šesti pacientů (43 %), přičemž u jednoho pacienta se mohlo vyskytovat i více různých nežádoucích účinků. Dominantně se jednalo o hepatopatii (n = 5, 46 %) a neutropenii (n = 4, 36 %), v jednom případě se jednalo o svědění kůže a v jednom případě byly taktéž zaznamenány změny a poruchy nálady. Všechny nežádoucí příhody byly nižších stupňů závažnosti dle CTCAE, max. 2. stupně, podrobně (graf 3). U žádného pacienta nebyl pozorován flu-like syndrom. Terapie nebyla ukončena ani přerušena u žádného pacienta z důvodu nežádoucích účinků nebo intolerance preparátu pacientem.
Graf 3. Vývoj mutační alelické zátěže JAK2V617F od zahájení léčby ropeginterferonem alfa-2b ve sledovaném souboru. 
Během sledovaného období byla zaznamenána pouze 1 trombembolická komplikace (7 %), která se však rozvinula u pacienta během pneumonie způsobené virem SARS-CoV-2 (severe acute respiratory syndrome coronavirus 2).
DISKUZE
Naše práce ukazuje první výsledky a dosavadní zkušenosti s terapií RopegIFN na jednom centru. Medián délky terapie byl pouze 266 dní, nicméně již během této krátké doby bylo možno pozorovat efekt poklesu a stabilizace hodnoty hematokritu a taktéž postupné snížení alelické zátěže mutovaného JAK2V617F. Také je však nutné uvést, že u podstatné části pacientů byla terapie RopegIFN zahájena až v rámci 3. nebo další linie, což mohlo přispět k rychlému dosažení hematologické remise i v krátkém časovém horizontu při nižších dávkách RopegIFN.
Oproti datům ze studií, v našem souboru byly k dosažení hematologické odpovědi postačující výrazně nižší celkové dávky RopegIFN. Medián dávky u sledovaných pacientů byl 150 μg aplikovaný podkožně každých 14 dnů a nejvyšší podaná dávka byla 250 μg každých 14 dnů. Ve studii PROUD-PV a CONTINUATION-PV byl výrazně vyšší medián využívané dávky v 36. měsíci terapie (425 μg) a nejvyšší podávaná dávka (500 μg) [9]. Léčebný efekt ve smyslu dosažení kompletní hematologické remise ve vysokém procentu pacientů (79 %) byl srovnatelný s daty ve studiích PROUD-PV (43 %) a CONTINUATION-PV (71 %) [9].
V souladu s výsledky randomizovaných studií jsme i v souboru našich pacientů prokázali nízkou frekvenci nežádoucích účinků terapie, přičemž nejčastěji se vyskytovala elevace jaterních testů.
Předností naší práce jsou výsledky použití RopegIFNu Ph-MPN v reálné klinické praxi se současným zohledněním velikosti souboru při hodnocení výstupů.
ZÁVĚR
Ropeginterferon alfa-2b představuje účinnou a bezpečnou terapii pacientů s pravou polycytémií, jak bylo prokázáno v klinických studiích s následným schválením EMA (European Medicines Agency) v roce 2018. Léčebný přípravek má potenciál – jako jediný z dosud dostupných cytoredukčních léků pro Ph-MPN dosáhl kromě dosažení hematologické odpovědi taktéž snížení alelické zátěže JAK2V617F, a tím zpomalení přirozené progrese onemocnění. Tento fakt je důležitý především u mladší skupiny pacientů. Jedna z jeho největších předností vzhledem k odlišné pegylaci molekuly a prodlouženému poločasu je reprezentována výrazně lepší snášenlivostí, a tak vynikající compliance pacientů k léčbě.
PODÍL AUTORŮ NA RUKOPISU
NP – napsání rukopisu
NP, JP – příprava analýzy
NP, BW, MD, JM – diagnostika a léčba nemocných
AM, MB, JK, IJ – diagnostika nemocných, molekulární analýzy
NP, BW, MD, JM, AM, MB, JK, IJ – revize a připomínkování rukopisu
PODĚKOVÁNÍ
Práce byla podpořena grantem MZ ČR – RVO (FNBr 65269705), MUNI/A/1330/2021 a projektem Národního ústavu pro výzkum rakoviny (Program EXCELES, ID: LX22NPO5102) – financováno Evropskou unií – Next Generation EU. Molekulární analýzy byly finančně podpořeny firmou AOP Orphan.
PROHLÁŠENÍ AUTORŮ O KONFLIKTU ZÁJMŮ
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Doručeno do redakce dne: 6. 10. 2022.
Přijato po recenzi dne: 27. 10. 2022.
MUDr. Natália Podstavková
Interní hematologická a onkologická
klinika
LF MU a FN Brno
Jihlavská 20
625 00 Brno
e-mail: podstavkova.natalia@fnbrno.cz
Zdroje
1. Dunbar AJ, Rampal RK, Levine R. Leukemia secondary to myeloproliferative neoplasms. Blood. 2020; 136 (1): 61–70.
2. Spivak JL. Polycythemia vera. Curr Treat Options Oncol. 2018; 19 (2): 12.
3. Hasselbalch HC, Holmstrom MO. Perspectives on interferon-alpha in the treatment of polycythemia vera and related myeloproliferative neoplasms: minimal residual disease and cure? Semin Immunopathol. 2019; 41 : 5–19.
4. Griesshammer M, Gisslinger H, Mesa R. Current and future treatment options for polycythemia vera. Ann Hematol. 2015; 94 : 901–910.
5. Gisslinger H, Zagrijtschuk O, Buxhofer-Ausch V, et al. Ropeginterferon alfa-2b, a novel IFNa-2b, induces high response rates with low toxicity in patients with polycythemia vera. Blood. 2015; 126 (15): 1762–1769.
6. Hasselbalch HC. A new era for IFN-a in the treatment of Philadelphia-negative chronic myeloproliferative neoplasms. Expert Rev Hematol. 2011; 4 (6): 637–655.
7. Kiladjian JJ, Cassinat B, Turlure P, et al. High molecular response rate of polycythemia vera patients treated with pegylated interferon alpha-2a. Blood. 2006; 108 (6): 2037–2040.
8. Marchetti M, Vannucchi AM, Griesshammer M, et al. Appropriate management of polycythaemia vera with cytoreductive drug therapy: European LeukemiaNet 2021 recommendations. Lancet Haematol. 2022; 9 (4): e301–e311.
9. Gisslinger H, Klade C, Georgiev P, et al. PROUD-PV Study Group. Ropeginterferon alfa-2b versus standard therapy for polycythaemia vera (PROUD-PV and CONTINUATION-PV): a randomised, non-inferiority, phase 3 trial and its extension study. Lancet Haematol. 2020; 7 (3): e196–e208.
10. Alvarez-Larrán A, Bellosillo B, Pereira A, et al. JAK2V617F monitoring in polycythemia vera and essential thrombocythemia: clinical usefulness for predicting myelofibrotic transformation and thrombotic events. Am J Hematol. 2014; 89 : 517–523.
11. Verstovsek S, Komatsu N, Gill H, et al. SURPASS-ET: phase III study of ropeginterferon alfa-2b versus anagrelide as second-line therapy in essential thrombocythemia. Future Oncol. 2022; 18 (27): 2999–3009.
12. https: //ctep.cancer.gov/protocoldevelopment/electronic_applications/docs/ctcae_v5_quick_reference_8.5x11.pdf
13. Barosi G, Mesa R, Finazzi G, et al. Revised response criteria for polycythemia vera and essential thrombocythemia: an ELN and IWG-MRT consensus project. Blood. 2013; 121 (23): 4778–4781.
14. Barbui T, Barosi G, Birgegard G, et al. European LeukemiaNet. Philadelphia-negative classical myeloproliferative neoplasms: critical concepts and management recommendations from European LeukemiaNet. J Clin Oncol. 2011; 29 (6): 761–770.
15. Barbui T, Finazzi G, Carobbio A, et al. Development and validation of an International Prognostic Score of thrombosis in World Health Organization-essential thrombocythemia (IPSET-thrombosis). Blood. 2012; 120 (26): 5128–5133. AE verze 5.0. z roku 2017
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2022 Číslo 4- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Ibrance® – nová šance pro pacientky s HR+/HER2– karcinomem prsu
-
Všechny články tohoto čísla
- Efektivita kombinace monoklonálních protilátek tixagevimab-cilgavimab v prevenci a léčbě pacientů s vysokým rizikem rozvoje COVID-19
- Jak anti-SARS-CoV-2 IgG a IgM predikují titr virus neutralizačních protilátek u dárců rekonvalescentní plazmy proti onemocnění COVID-19?
- Dosavadní zkušenosti s léčbou ropeginterferonem alfa-2b u pacientů s Ph negativními myeloproliferacemi na Interní hematologické a onkologické klinice LF MU a FN Brno
- Hemolytická nemoc plodu a novorozence
- Beta-thalassemia minor a maior v těhotenství
- 30 let Českého národního registru dárců dřeně (ČNRDD) a Nadace pro transplantace kostní dřeně
- Prof. MUDr. Karel Indrák, DrSc. se dožívá 75 let
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Hemolytická nemoc plodu a novorozence
- Beta-thalassemia minor a maior v těhotenství
- Dosavadní zkušenosti s léčbou ropeginterferonem alfa-2b u pacientů s Ph negativními myeloproliferacemi na Interní hematologické a onkologické klinice LF MU a FN Brno
- Jak anti-SARS-CoV-2 IgG a IgM predikují titr virus neutralizačních protilátek u dárců rekonvalescentní plazmy proti onemocnění COVID-19?
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



