-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Odběry kostní dřeně pro alogenní transplantaci – zhodnocení desetileté zkušenosti se zaměřením na využití autotransfuzí u dárců
Bone marrow harvesting for allogeneic transplantation – evaluation of ten years’ experience focusing on donor auto-transfusion utilisation
Bone marrow (BM) is one of the sources of hematopoietic stem cells used for allogeneic transplantation. In this retrospective study, we analysed bone marrow harvests in 216 healthy donors over a ten-year period (2007–2017). Larger volumes of bone marrow were obtained from male compared to female donors (1300 ml vs. 1100 ml) due to their higher body weight, resulting in a higher number of nucleated cells (156 vs. 124 x 106 TNC, ns). The total yield was dependent on the volume of marrow (p < 0.0001) and donor weight (p = 0.01). Suboptimal grafts containing ≤ 2.0 x 108 TNC/kg (recipient) were collected in 6 % of cases, always with significant differences of weight between donor and recipient (median 20 kg). All donors underwent preoperative autologous blood donation (PAD). The initial haemoglobin level of 153 g/L (male donors) and 135 g/L (female donors) decreased by about 8 g/L after preoperative blood donation and by 23 g/L after bone marrow harvest. Auto-transfusion was administered to 70 % of donors, 30 % of the units remained unused. Evaluation of the risk of reaching transfusion threshold (<115 g/L males, < 105 g/L females) revealed that donors with initial haemoglobin level above 145 g/L and those weighing more than 75 kg have a minimal risk of requiring blood substitution (about 10 %). The incidence of adverse events associated with bone marrow harvests was low (5 %) and none of these were classified as serious. The analysis proved that the amount of nucleated cells harvested and substitution requirements are determined by donor parameters (weight, haemoglobin level) and recipient parameters (weight). Given the changing policy to auto-transfusion during bone marrow collection, the issue of balancing the benefits and risks of administering preoperative autologous transfusion should be addressed.
Keywords:
CD34+ – bone marrow – harvest – allogeneic – preoperative autologous blood donation – donor
Autoři: L. Hejretová 1; D. Lysák 1; M. Hrabětová 1; P. Jindra 1,2
Působiště autorů: Hematologicko-onkologické oddělení, Fakultní nemocnice Plzeň 1; Český národní registr dárců dřeně 2
Vyšlo v časopise: Transfuze Hematol. dnes,25, 2019, No. 4, p. 350-360.
Kategorie: Původní práce
Souhrn
Kostní dřeň (BM) je jedním ze zdrojů hematopoetických kmenových buněk pro účely jejich alogenní transplantace. V retrospektivní studii jsme analyzovali odběry kostní dřeně 216 zdravých dárců za desetileté období 2007–2017. Dárcům byl vzhledem k jejich vyšší tělesné hmotnosti odebírán větší objem dřeně oproti dárkyním (1300 ml vs. 1100 ml), což vedlo k zisku většího množství jaderných buněk (156 vs. 124 x 106 TNC, p = ns). Získaný výtěžek závisel na objemu dřeně (p < 0,0001) a hmotnosti dárce (p = 0,01). Suboptimální transplantát s obsahem ≤ 2,0 x 108 TNC/kg příjemce byl odebrán v 6 % případů, vždy byl přítomen velký hmotnostní rozdíl mezi dárcem a příjemcem (medián 20 kg). Všem dárcům byla připravena k odběru BM jedna jednotka autologní krve. Vstupní hladina hemoglobinu dárců (Hb; 153 g/l u mužů, 135 g/l u žen) se snížila odběrem autotransfuze (AT) o cca 8 g/l a odběrem kostní dřeně o dalších cca 23 g/l. AT byla podána celkem u 70 % dárců, 30 % přípravků zůstalo nevyužito. Vyhodnocení rizika dosažení substitučních hodnot hemoglobinu (< 115 g/l u mužů, < 105 g/l u žen) ukázalo, že dárci s hladinou nad 145 g/l před odběrem a hmotností nad 75 kg mají minimální riziko potřeby substituce (cca 10 %). Výskyt komplikací v souvislosti s odběrem byl nízký (5 %) a žádná z nich nebyla klasifikována jako závažná. Analýza ukázala, že parametry dárce (hmotnost, hladina Hb) a příjemce (hmotnost) určují množství odebraných nukleárních buněk a také potřebu zajištění odběru AT. Vzhledem k tomu, že se mění postoj k využití AT při odběrech kostní dřeně, je na místě diskuze o benefitu a rizicích vyplývajících z odběrů autologní krve u dárců kostní dřeně.
Klíčová slova:
kostní dřeň – odběr – alogenní – autotransfuze – dárce – CD34+
ÚVOD
Alogenní transplantace hematopoetických kmenových buněk je standardní léčebnou procedurou u řady hematologických nádorových i nenádorových onemocnění. Jako transplantát lze využít kostní dřeň (BM) nebo periferní krvetvorné kmenové buňky (PBSC) mobilizované růstovým faktorem granulopoezy. Při odběrech alogenních krvetvorných buněk jsou v posledních dvou dekádách preferovány PBSC oproti BM, která byla v roce 2017 v Evropě využita pouze u cca 20 % transplantací [1]. Tento trend je patrný také v rámci České republiky, kdy transplantační centra v posledních letech volí kostní dřeň jako zdroj krvetvorných buněk pouze v cca 10 % případů (graf 1).
Graf 1. Využití BM a PBSC jako zdroje kmenových buněk pro alogenní transplantaci v ČR v letech 2007–2018
Data ze statistiky EBMT survey.
Transplantace PBSC vedou oproti BM k rychlejšímu přihojení štěpu a k časnějšímu obnovení krvetvorby. Zároveň se méně často komplikují selháním štěpu [2, 3]. Naopak příjemci kostní dřeně mají menší riziko vzniku akutní a zejména chronické reakce štěpu proti hostiteli (GVHD). Transplantace PBSC je podle některých prací spojena s méně častými relapsy základního onemocnění právě díky akcentaci GVHD [4–6]. Ve výsledku však nebývá prokazován statisticky významný rozdíl v přežití pacientů při porovnání obou typů transplantátů, a to jak u transplantací s redukovanou, tak myeloablativní přípravou [4, 5, 7, 8]. Pouze některé studie uvádějí lepší přežití jak celkové (OS), tak bez leukemie (LFS) po transplantaci PBSC. Nicméně i zde zůstává otevřena otázka dopadu GVHD na dlouhodobou morbiditu a mortalitu [6, 9]. Ukazuje se, že při delším sledování mají pacienti po transplantaci kostní dřeně méně komplikací plynoucích z chronické GVHD, a díky tomu si udržují lepší kvalitu života, psychický stav a mají také větší šanci na návrat do zaměstnání [7]. Transplantační centra začínají častěji zvažovat kostní dřeň jako preferovaný typ štěpu (informace z koordinačního centra ČNRDD).
Cílem alogenního odběru je zisk dostatečného množství hematopoetických kmenových buněk se snahou o minimalizaci případných zdravotních dopadů na dárce. Darování kostní dřeně je bezpečnou procedurou, která se provádí více než čtyři desetiletí. Hlavním vedlejším účinkem odběru je bolest, kterou shodně uvádějí dárci BM i PBSC. Při odběru PBSC jsou to zejména bolesti skeletu při mobilizaci G-CSF, u odběru kostní dřeně dominují bolesti v místě odběru (82 % dárců) a bolesti související s anestezií (bolesti v krku, bolesti hlavy). Oproti darování PBSC je odběr BM spojen s delší dobou do plného zotavení dárce po odběru (3 týdny vs. 1 týden) [10]. Přestože dárci BM vnímají proceduru bezprostředně po odběru jako fyzicky více stresující, nejsou mezi oběma způsoby odběru dlouhodobé rozdíly ve vnímání kvality života spojené se zdravím [11].
Optimální transplantát obsahuje mezi 3–5 x 108 TNC na kilogram hmotnosti příjemce. Získání dostatečně bohatého štěpu je dáno jak parametry dárce, tak způsobem vedení odběru [12]. Odběr kostní dřeně je vždy spojen s poklesem hladiny hemoglobinu. Ke snížení rizika rozvoje závažné anémie se dárcům odebírá preoperačně autologní transfuze, která jim může být podána po odběru BM při významném poklesu v červeném krevním obraze. Tento přístup byl historicky přijímán jako součást standardní péče o dárce a vychází ze situace v 80. a 90. letech minulého století, kdy autotransfuze nabyly na významu v souvislosti se zvýšenými infekčními riziky podání alogenní krve (HIV, hepatitidy). Z těchto důvodů bylo doporučováno připravovat dárcům BM rutinně autotransfuze, aby se pravděpodobnost substituce alogenní krví minimalizovala. Toto doporučení platilo více než 30 let, nicméně v současné době se v souvislosti s nárůstem bezpečnosti alogenní krve diskutuje otázka účelnosti odběrů autotransfuzí u dárců kostní dřeně [13–15]. Příprava autotransfuze znamená snížení hladiny hemoglobinu před vlastním odběrem dřeně a nakonec je využita jen u části dárců. Světová asociace dárců kostní dřeně (World Marrow Donor Association;WMDA) aktuálně ve svých standardech využívání AT vůbec nespecifikuje (WMDA standardy 2017). JACIE standardy požadují dostupnost autologní nebo ozářené alogenní krve (FACT-JACIE standardy edice 7.). Praxe řady transplantačních center tomuto trendu odpovídá a autotransfuze nejsou odebírány vůbec nebo se rozhodnutí o odběru řídí předpokládanou krevní ztrátou a požadovaným množstvím odebraných buněk [16].
Vyhodnotili jsme soubor dárců kostní dřeně odebraných v desetiletém období. Cílem bylo definovat parametry odběru, případně charakteristiky dárců a příjemců, které ovlivňují výtěžek odběru, tedy množství odebraných jaderných buněk. Zároveň jsme se zaměřili na dynamiku poklesu hemoglobinu po odběru BM a pokusili jsme se identifikovat dárce, kteří z předoperačního odběru autotransfuze profitují a ty, u nichž je naopak její následná potřeba nepravděpodobná a příprava zbytečná.
SOUBOR DÁRCŮ A METODIKA ODBĚRU KOSTNÍ DŘENĚ
V retrospektivní studii byly analyzovány charakteristiky 216 zdravých dobrovolných příbuzných i nepříbuzných dárců (160 mužů a 56 žen), kterým byla odebrána kostní dřeň v letech 2007–2017 na Hematologicko-onkologickém oddělení Fakultní nemocnice v Plzni. Všichni dárci podepsali informovaný souhlas s odběrem a anonymním zpracováním dat. Byli poučeni o možných způsobech odběru hematopoetických kmenových buněk a po důkladném zhodnocení individuálních rizik zvolili jeden z nich. Dva až čtyři týdny před odběrem bylo u všech dárců provedeno vyšetření před odběrem („work-up“), v rámci kterého byla posouzena jejich zdravotní způsobilost. Zároveň byla všem dárcům odebrána jedna autotransfuze (350–450 ml), která byla zpracována na Transfuzním oddělení FN Plzeň. Pouze u 4 dárců nebyly autologní erytrocyty připraveny (3krát odběr pro pediatrického příjemce, 1krát neplánovaný odběr při selhání mobilizace periferních kmenových buněk). Medián věku dárců byl 32 let (19–63), hmotnost 82 kg (50–131). Charakteristiky dárců jsou uvedeny v tabulce 1.
Tab. 1. Charakteristika dárců a odběrů 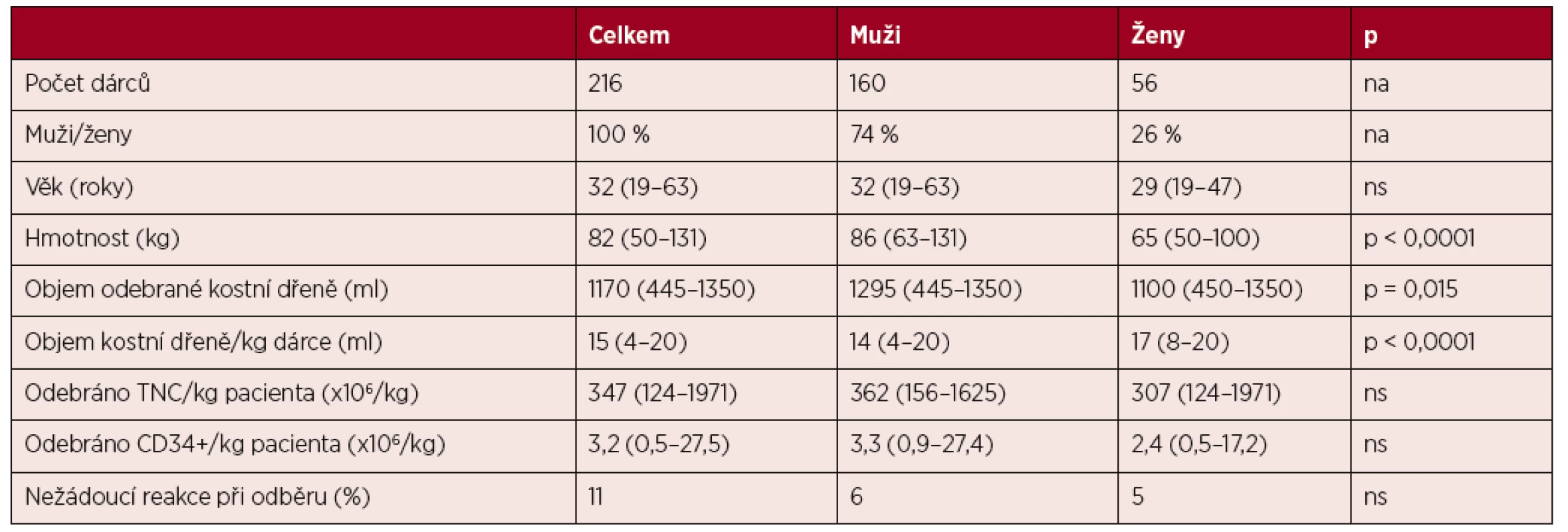
Hodnoty uvedeny jako mediány.
TNC – nukleární buňkyOdběry prováděl dvoučlenný odběrový tým v aseptickém prostředí operačního sálu v celkové anestezii. Technika spočívala v opakovaných aspiracích trepanobioptickými odběrovými jehlami ze spina iliaca posterior superior kosti kyčelní. Při každé aspiraci bylo nasáváno malé množství kostní dřeně s krví (kolem 5 ml), poté se měnila pozice aspirační jehly. Jako antikoagulant byl využíván roztok ACD-A v poměru 1 : 10 ke kostní dřeni. Maximální odebrané množství nepřesahovalo 20 ml/kg hmotnosti dárce nebo 1500 ml včetně antikoagulantu (tedy 1350 ml kostní dřeně). Metodika odběrů odpovídala platné národní legislativě, standardům Českého národního registru dárců dřeně i WMDA. Podání autotransfuze přímo na operačním sále bylo dáno rozhodnutím anesteziologa a odběrového týmu na základě vstupní hladiny hemoglobinu, krevní ztráty a vitálních funkcí. Pokud nebyla AT podána během odběru, bylo další rozhodnutí o substituci řízeno hladinou hemoglobinu z kontrolního krevního obrazu vyšetřeného 8–10 hodin po odběru.
Statistika
Pro měřené parametry v celém souboru, v jednotlivých skupinách a podskupinách byly počítány základní statistické parametry (průměr, směrodatná odchylka, rozptyl, medián, minimum, maximum). Pro zjištění závislostí zkoumaných parametrů byl použit Spearmanův koeficient korelace a také lineární regrese. Pomocí mnoharozměrné regrese jsme se snažili nalézt ty faktory, které vzhledem ke sledovaným výstupům vykazovaly statistickou významnost, a následně jsme je pomocí logistické regrese („score selection“ a „stepwise“ regrese) zpracovali do podoby Klasifikačních a regresních stromů (CART). Statistická významnost byla stanovena na hranici alpha = 5 %. Statistická analýza byla provedena s užitím software SAS (SAS Institute Inc., Cary, NC, USA).
VÝSLEDKY
Celkový čas odběru se pohyboval od 15 do 95 minut (medián 35 minut). Medián odebraného množství kostní dřeně byl 1170 ml (445–1350 ml) bez antikoagulantu, což odpovídalo 15 ml/kg hmotnosti dárce (4–20 ml/kg). Požadavek transplantačních center na množství odebraných TNC se pohyboval v rozmezí 2–8 x 108/kg hmotnosti příjemce (medián 3 x 108/kg). Splnit se jej podařilo u 69 % odběrů (u 73 % mužů a 59 % žen).
Při porovnání odběrů s ohledem na pohlaví, byl u mužů odebírán o cca 200 ml větší objem dřeně (medián 1295 ml vs. 1100 ml, p = 0,015), což souviselo s větší hmotností dárců (86 vs. 65 kg, p < 0,0001). Celkové množství získaných TNC, resp. CD34+ buněk na kilogram hmotnosti příjemce bylo u mužů o něco vyšší, ovšem bez dosažení statistické významnosti (viz tab. 1).
Dále jsme se zaměřili na analýzu parametrů, které mají vliv na výtěžek TNC (parametry dárce, příjemce a odběru). Pomocí mnoharozměrné regrese byly otestovány různé modely a nakonec byl vypracován model se dvěma nezávislými proměnnými, které nejlépe určovaly výtěžnost odběru: objem odebrané dřeně (p < 0,0001) a hmotnost dárce (p = 0,01). Množství TNC se zvyšovalo s rostoucí hmotností dárce a objemem odebrané dřeně. Porovnání výtěžků vypočítaných podle modelu (TNC = 75,88 + 0,09 . objem BM + 0,81 . hmotnost dárce) korelovalo se skutečnými hodnotami (p < 0,0001; r = 0,34) – graf 2.
Graf 2. Porovnání vypočtených a skutečných výtěžků (TNC x 108), lineární regrese 
Množství TNC požadované transplantačními centry bylo 3 x 108/kg hmotnosti příjemce (medián). Pomocí CART modelů jsme proto hledali faktory, které predikují odběr nedosahující této cílové hodnoty. Jako jediný statisticky významný faktor se ukázal hmotnostní rozdíl mezi dárcem a příjemcem. Dárci s hmotností o 20 a více kg vyšší oproti příjemcům měli pouze 1,5 % pravděpodobnost nedosažení cílové dávky 3 x 108/kg. S klesajícím hmotnostním rozdílem se riziko zvyšovalo až na 67 % u dárců, kteří vážili o ≥ 15 kg méně než příjemci (graf 3).
Graf 3. CART model pro pravděpodobnost odběru štěpu s obsahem TNC ≤ 3 x 108/kg příjemce v závislosti na rozdílu hmotnosti dárce a příjemce 
Za minimální dávku nukleár-ních buněk, která umožňuje dlouhodobé přihojení, je považováno ≥ 2 x 108/kg, transplantáty s nižším obsahem jsou suboptimální a roste u nich riziko selhání štěpu a případné potřeby druhého darování. Suboptimální produkt s obsahem méně než 2 x 108/kg byl odebrán v 6 % případů (3,8 % odběrů u mužů a 12,5 % odběrů u žen, p = 0,043). Ve všech případech byl přítomen významný hmotnostní nepoměr v neprospěch dárce (medián 20 kg) a i přes odběr maximálního množství dřeně se nepodařilo získat dostatečný transplantát.
Koncentrace TNC v produktu klesala s jeho rostoucím objemem. Odběry o větších objemech měly nižší koncentrace buněk pravděpodobně danou „vyčerpáním“ aspiračních míst a/nebo méně precizní technikou odběru s většími aspiračními objemy. Závislost koncentrace TNC na objemu ukazuje graf 4.
Graf 4. Závislost koncentrace TNC (x 109/l) na objemu odebrané kostní dřeně (ml) 
Dále byly analyzovány hladiny hemoglobinu (Hb) dárců, jejich vývoj po odběru autotransfuze a odběru kostní dřeně, s cílem ověřit pravděpodobnost potřeby substituce a eventuálně modifikovat transfuzní politiku. Hladina Hb při vyšetření před odběrem byla v mediánech 153 g/l u mužů a 135 g/l u žen (p < 0,0001). Odběrem autotransfuze došlo k jejímu snížení o cca 8 g/l. Celkové snížení hemoglobinu při porovnání krevního obrazu před odběrem kostní dřeně a po odběru bylo podobné u obou pohlaví, v mediánech 23 g/l u mužů a 25 g/l u žen (p = ns). Pouze u 13 % dárců došlo k poklesu hemoglobinu do rozmezí 90–100 g/l a pouze u jediného dárce (0,6 %) pod 90 g/l. Jednalo se častěji o ženy (91 %) a o dárce s nižší hmotností oproti příjemci (61 %). Pokud by teoreticky nebyly odebrány žádné autotransfuze a hladina Hb by se snížila jen odběrem BM, byl by pouze u 3 % dárců hemoglobin po odběru nižší než 100 g/l. Autotransfuze byla podána celkem 149 dárcům (70 %), z toho 25 % dárců bylo substituováno ještě na operačním sále a 75 % ve večerních hodinách po kontrole krevního obrazu. Celkem 30 % autotransfuzí se nepodalo. Hladiny hemoglobinu po odběru kostní dřeně jsou uvedeny v tabulce 2.
Tab. 2. Změny hladiny hemoglobinu při odběru autotransfuze a kostní dřeně 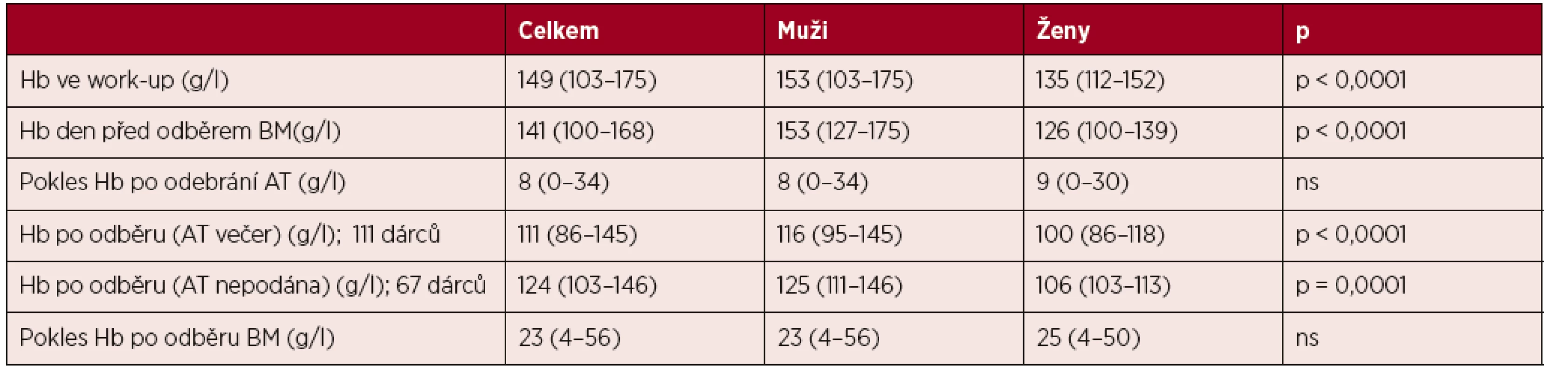
Hodnoty uvedeny jako mediány.
AT – autotransfuze, BM – kostní dřeňPokusili jsme se blíže charakterizovat skupinu dárců, kteří mají riziko poklesu hemoglobinu po odběru pod 115 g/l (muži), resp. 105 g/l (ženy), což odpovídá naší aktuální substituční hladině. Potvrdil se logický předpoklad, že vyšší riziko závažnějšího poklesu v průběhu odběru s následnou potřebou substituce krevní transfuzí mají dárci, kteří vstupují do odběru s nižší hodnotou hemoglobinu. Při vstupním Hb ≤ 131 g/l je tato pravděpodobnost téměř 90%. Pro dárce s Hb nad 131 g/l existuje další upřesňující faktor, kterým je hmotnost dárce. Při hmotnosti nad 76 kg je pravděpodobnost substituce cca 20 %, pokud má dárce Hb nad 145 g/l a hmotnost nad 76 kg je pravděpodobnost podání AT pouze 10 %. To vše při výše uvedených substitučních hodnotách (graf 5). Všechna tato hodnocení byla provedena pouze u dárců, kteří nedostali AT na operačním sále (176 dárců).
Graf 5. CART model pro riziko poklesu Hb po odběru pod 115 g/l (muži), resp. 105 g/l (ženy) 
Výskyt komplikací spojených s odběrem byl nízký. Objevily se pouze v 11 případech, což odpovídá 5 % z celkového počtu odběrů. Vždy se jednalo o mírné komplikace (hypotenze, podráždění kůže dezinfekcí, teploty), nedošlo k výskytu žádné závažné nežádoucí reakce. Nezávažné komplikace, jako nauzea a zvracení v souvislosti s ane-stezií či bolestivost v místě vpichu nebyly hodnoceny. U jednoho dárce bylo nutné pro selhání odběru indikovat mobilizaci a odběr PBSC. Nebylo nutné podávat alogenní krev, ani nedošlo ke vzniku potransfuzní reakce. Při hodnocení sterility odebrané BM byla bakteriální kontaminace prokázána pouze ve 3 případech (1,4 %), jednalo se o běžné kožní patogeny a žádná z těchto události neměla nepříznivý dopad na příjemce.
DISKUSE
Hlavním zdrojem hematopoetických kmenových buněk pro účely alogenní transplantace jsou v současné době periferní kmenové buňky. Využívána je i kostní dřeň, která nabízí nižší riziko GVHD, a to jak u HLA kompatibilních, tak u haploidentických transplantací [4, 5, 17]. Počet pacientů, kteří dlouhodobě žijí po úspěšné alogenní transplantaci, se zvyšuje, a můžeme předpokládat, že v roce 2030 jich bude 5krát více než nyní. V souvislosti s tím roste význam prevence pozdních komplikací transplantace, zejména chronické GVHD, s cílem udržet dostatečnou kvalitu života. Pokud nedojde k relapsu, jsou transplantovaní pacienti oproti běžné populaci zatíženi vyšším rizikem úmrtí na infekce, respirační onemocnění, sekundární nádory aj. Rizikovým faktorem je zejména chronická GVHD [18]. Využití transplantátů odebraných z kostní dřeně bude při alogenní transplantaci pravděpodobně stále více zvažováno a kostní dřeň má potenciál stát se častěji využívaným typem štěpu, minimálně u některých skupin pacientů.
Dostatečný obsah hematopoetických kmenových buněk v transplantátu je jedním z nejvýznamnějších faktorů ovlivňujících jeho úspěšné přihojení. V naší studii se ukázalo, že množství odebraných TNC souvisí zejména s hmotností dárce a objemem odebrané kostní dřeně. Riziko nesplnění standardního požadavku 3 x 108/kg vyplývalo z rozdílu hmotnosti mezi dárcem a příjemcem a narůstalo z 1,5 % u dárců těžších o ≥ 20 kg až na 67 % u dárců s hmotností nižší o ≥ 15 kilogramů. Význam hmotnosti dárce demonstrují také odběry se suboptimálním ziskem TNC ≤ 2 x 108/kg, které byly pozorovány v 6 % případů, a to vždy u dárců s významným hmotnostním nepoměrem oproti příjemci. Poměr hmotnosti dárce/příjemce je tedy zásadním parametrem určujícím výtěžek TNC. Pokud je to možné, je vhodné volit dárce se stejnou nebo vyšší hmotností, případně u menších dárců preferovat odběr PBSC, u kterého je výtěžek (CD34+ buněk) na hmotnostním nepoměru méně závislý.
Pro efektivní odběr kostní dřeně je nezbytná také správná technika odběru. Studie ukazují, že aspirace malých objemů (do 3 ml) umožňuje získat více nukleárních buněk v porovnání s objemnými aspiracemi z jednoho místa [19]. Také v našem souboru jsme pozorovali nižší koncentrace jaderných buněk v závislosti na zvyšujícím se objemu dřeně, což implikuje větší naředění periferní krví.
Pro kvalitní a bezpečný odběr je velmi důležitá zkušenost odběrového týmu, která se s klesajícím počtem odběrů zhoršuje [20]. Zároveň roste riziko nežádoucích reakcí v souvislosti s odběrem [21]. Anketa mezi 120 americkými transplantačními centry ukázala, že 64 % center provádí méně než 10 odběrů kostní dřeně od nepříbuzných dárců za rok [16]. Řada center v rámci boomu PBSC ztratila odbornou erudici a musí jí znovu vybudovat. Za minimální počet nezbytný k udržení způsobilosti týmu lze považovat cca 10 odběrů BM ročně.
Odběr kostní dřeně vede k poklesu hladiny hemoglobinu, v naší studii o 23 g/l (medián). Pro doplnění krevní ztráty při/po odběru BM se dárcům připravují při vyšetření před odběrem autotransfuze. Tato praxe byla historicky motivována snahou vyhnout se případnému podání alogenních erytrocytů a tedy riziku infekcí přenosných krví. V současné době již není toto riziko v transfuzní službě tolik aktuální a přístup transplantačních center se individualizuje. Nabízí se otázka, zda a případně pro jaké dárce je příprava autotransfuze vhodná či nezbytná. Využití autotransfuzí se v posledních letech celosvětově snižuje, a to nejen díky malému riziku přenosu infekce alogenní krví, ale také zaváděním nových technik perioperačního managementu, který snižuje potřebu substitucí (normovolemická hemodiluce, perioperační sběr krve aj.). Počty autologních jednotek představují zlomky procenta ze všech odebraných erytrocytárních přípravků [22]. Autotranfuze je bezpečná z pohledu přenosu infekčních onemocnění, ale její podání není zcela bez rizika. Špatné načasování odběru může snížit předoperační hladinu hemoglobinu (v našem souboru v mediánu o 8 g/l) a zvyšovat riziko expozice dárce alogenní krví v pooperačním období. Nejsou vyloučeny ani imunologické komplikace, bakteriální kontaminace, záměny přípravků. Studie na zdravých dárcích prokázala, že obnovení hladiny hemoglobinu na 80 % vstupní hodnoty trvá po odběru 500 ml krve a při poskytnutí substituce železa cca 30 dní, bez substituce v závislosti na zásobách železa (nízká hladina feritinu) dokonce déle než 100 dní [23]. Pokud tedy není autotransfuze klinicky potřebná, neměly by být její odběr a použití indikovány.
Některá transplantační centra AT neodebírají pro jejich nízkou klinickou využitelnost [24, 25], pro jiná je její odběr naopak rutinní procedurou [13, 15]. Práce amerických autorů ukázala, že pouze 23 % center autotransfuze neodebírá a 41 % je naopak podává rutinně bez ohledu na pooperační hladinu hemoglobinu [16]. Počet autotransfuzí, které se nepodají a likvidují se, může dosahovat 25 % nebo dokonce až 50 % [13–15, 26]. Sami jsme AT podali celkem 70 % dárcům, tzn. se 30 % jednotek vůbec nevyužilo.
Potřeba autotransfuze a riziko podání alogenní krve je dáno také hladinou hemoglobinu, která je stanovena jako hranice pro substituci. Někteří autoři poukazují na skutečnost, že pouze u malé skupiny dárců klesá Hb po odběru na nebezpečnou hodnotu, a to bez ohledu na to, zda byla autotransfuze odebrána a podána [13]. Pokud bychom akceptovali substituční hladinu hemoglobinu 70–80 g/l doporučenou pro pacienty bez kardiovaskulárních či respiračních onemocnění [27], bude počet dárců vyžadujících auto/transfuzi velmi nízký. Ve studii Bartnik et al. pouze 1,3 % dárců pokleslo po odběru s Hb pod 80 g/l, žádný z nich pod 70 g/l a příprava AT se tedy jevila jako neopodstatněná [25]. K podobným závěrům docházejí i jiní autoři, kteří uvádějí hladinu Hb po odběru pod 85 g/l u 2 % dárců [13]. V našem souboru poklesl hemoglobin na 90–100 g/l pouze u 13 % dárců a pouze jediný dárce měl hladinu Hb po odběru pod 90 g/l. Hodnoceno nebylo celkem 38 dárců, kteří byli substituováni přímo na operačním sále, přesto můžeme konstatovat, že jen u malého počtu dárců se hladina hemoglobinu po odběru snižuje na hodnoty, které mohou být klinicky významné či ohrožující.
Naše substituční hladina Hb je vyšší než 70–80 g/l doporučovaných pro nekomorbidní pacienty. V případě zdravých dárců nemůžeme hodnotit pooperační hladinu hemoglobinu pouze v kontextu ochrany zdraví dárce, ale musíme brát do úvahy také jeho komfort, osobní a pracovní aktivity. Hladina 70 g/l je určitě dostatečná pro hospitalizované hemodynamicky stabilní pacienty, nicméně u dárců bychom měli pravděpodobně uplatňovat liberálnější transfuzní politiku. Nízké hladiny hemoglobinu mohou vést k příznakům slabosti, diskomfortu, výraznější nauzee, zvracení, případně k prodloužení doby hospitalizace.
Přesto naše transfuzní politika prošla určitým vývojem a došlo ke zmírnění požadavků na využití autotransfuzí. Na začátku sledovaného období byly odebírány a podávány rutinně všem dárcům bez ohledu na pokles v krevním obraze. Řada dárců tak byla transfundována zbytečně. Od roku 2009 jsme upravili pravidla tak, aby lépe odpovídala aktuálním potřebám. AT se podává na operačním sále pouze při klinicky významné krevní ztrátě či nízké vstupní hodnotě hemoglobinu, jinak se podání AT zvažuje na základě kontrolního krevního obrazu za 8–10 hodin po odběru. Substituční politika zůstává přesto liberální a AT se indikuje při poklesu hemoglobinu pod 105 g/l u žen a pod 115 g/l u mužů nebo při poklesu o 30–35 g/l, případně při špatné toleranci krevní ztráty. Analýzou faktorů, které predikují pokles Hb po odběru pod tyto hodnoty, jsme identifikovali dárce, kteří mají nízké riziko potřeby AT, a není ji proto nutné odebírat. Jedná se o dárce s Hb nad 145 g/l a s hmotností nad 76 kg. Pokud bychom použili nižší než výše uvedené substituční hodnoty, počet dárců schopných podstoupit odběr kostní dřeně bez autotransfuze se bude zvyšovat.
Na druhou stranu z odběru kostní dřeně není nutné předem vylučovat ani dárce s mírnou anémií benigní etiologie, která je v akceptovatelných mezích daného transplantačního centra [28]. Mírná anémie nemá nepříznivý vliv na množství odebraných TNC a dárci nemají při dodržení limitu objemu odebrané dřeně na 1 kg hmotnosti zvýšené riziko významného poklesu Hb s potřebou podání transfuze [25]. Odběr kostní dřeně jsme provedli úspěšně u osmi dárkyň se vstupní hladinou Hb < 125 g/l. U všech dárců, a zejména těch s hodnotou hemoglobinu na dolní hranici normy a u žen, je vhodná suplementace železa se zahájením v době odběru AT minimálně do odběru BM, podle vývoje krevního obrazu případně i po vlastním odběru. Toto opatření spolu s dostatečně dlouhým intervalem mezi odběrem autotransfuze a kostní dřeně (3–4 týdny) by mělo dát prostor pro regeneraci červeného krevního obrazu.
V současné době tedy existuje konsenzus, že rutinní odběry autologní krve před odběrem kostní dřeně nejsou nezbytně nutné. Transplantační centrum by však mělo mít ve svých postupech pro posuzování zdravotní způsobilosti dárců definovanou politiku pro přípravu autotransfuzí, specifikovanou cílovou populaci, u které se odběr má a naopak nemusí provádět. Tato pravidla by měla vycházet z parametrů dárce a příjemce, předpokládaného objemu odebrané kostní dřeně i monitorování po odběru. Naše zkušenost ukazuje, že odběr AT není nutný u dárců s dostatečně vysokou hladinou Hb (~145 g/l) a dostatečnou hmotností (~76 kg) nebo při významném hmotnostním nepoměru ve prospěch dárce (~20 kg).
Odběr hematopoetických kmenových buněk od zdravých dárců je v současnosti bezpečnou metodou zatíženou nízkým procentem závažných komplikací [29], je-li prováděn za dodržení všech pravidel a na specializovaných pracovištích. Zdravotní rizika pro dárce nejsou vysoká, přesto je vhodné postup stále optimalizovat, abychom veškeré zdravotní dopady na dobrovolné dárce kostní dřeně minimalizovali a metodika odpovídala mezinárodním doporučením [24].
Výskyt závažných nežádoucích reakcí u dárců kostní dřeně se podle studií pohybuje od 0,04 % do 1,34 %. Nejčastěji se jedná o lokální reakci nebo komplikace související s celkovou anestezií [30, 31]. V našem souboru nedošlo během sledovaného období k rozvoji žádných závažných komplikací po odběru a počty nežádoucích reakcí se nevymykaly celosvětovým průměrům. Počet odběrů s pozitivní zkouškou na sterilitu byl velmi nízký (1,4 %) a odpovídá zkušenosti jiných pracovišť (1,6 %) [24].
Pro zajištění ochrany zdraví dárců je nezbytné mít definované postupy pro všechny aspekty péče o dárce, od posuzování zdravotní způsobilosti, odběry a využití autotransfuzí, až po metodiku odběru a dispenzarizaci dárce po odběru.
ZÁVĚR
Odběr kostní dřeně pro alogenní transplantaci musí být bezpečný pro dárce i pro pacienta. Zejména z pohledu dárce je uplatňována tzv. „zero risk“ politika, která má minimalizovat riziko poškození zdraví dárce při odběru. Při výběru dárce je třeba respektovat nejen HLA shodu, ale také non-HLA aspekty, které určují mimo jiné kvalitu odebraného transplantátu a nutnost využití autotransfuze při odběru. Aktuálně nejsou autotransfuze při odběrech kostní dřeně rutinně doporučovány a jejich využití závisí na politice konkrétního transplantačního centra. Proti jejich odběrům hovoří relativní bezpečnost podání alogenní krve, nevyužití validního množství jednotek a riziko prohloubení předoperační anémie. Na druhou stranu udržení dostatečné hladiny hemoglobinu u dárce by mělo minimalizovat snížení kvality života dárce v období po odběru. Na otázku, zda preferovat restriktivní nebo liberální transfuzní politiku, nelze nyní jednoznačně odpovědět, protože nejsou k dispozici dlouhodobá data o vlivu různých odlišných substitučních přístupů na kvalitu života dárců, jejich výkonnost při každodenních aktivitách nebo morbiditu, a je nezbytný další výzkum v této oblasti.
Podíl autorů na přípravě rukopisu
LH – sběr dat a příprava rukopisu
DL – analýza dat a finalizace rukopisu
MH – korekce rukopisu
PJ – revize rukopisu
Poděkování
Podpořeno projektem institucionálního výzkumu MZČR –FNPI, 00669806.Čestné prohlášení
Autoři práce prohlašují, že v souvislosti s tématem, vznikem a publikací tohoto článku nejsou ve střetu zájmů a vznik ani publikace článku nebyly podpořeny žádnou farmaceutickou firmou.
Doručeno do redakce dne 18. 3. 2019
Přijato po recenzi dne 18. 4. 2019.
doc. MUDr. Daniel Lysák, PhD.
Hematologicko-onkologické oddělení
Fakultní nemocnice Plzeň
Alej Svobody 80
304 60 Plzeň
e-mail: lysak@fnplzen.cz
Zdroje
1. Passweg JR, Baldomero H, Basak GW, et al. The EBMT activity survey report 2017: a focus on allogeneic HCT for nonmalignant indications and on the use of non-HCT cell therapies. Bone Marrow Transplant 2019; doi:10.1038/s41409-019-0465-9.
2. Blaise D, Kuentz M, Fortanier C, et al. Randomized trial of bone marrow versus lenograstim-primed blood cell allogeneic transplantation in patients with early-stage leukemia: a report from the Societe Francaise de Greffe de Moelle. J Clin Oncol 2000;18 : 537–546.
3. Anasetti C, Logan BR, Lee SJ, et al. Peripheral-blood stem cells versus bone marrow from unrelated donors. N Engl J Med 2012;367 : 1487–1496.
4. Nagler A, Labopin M, Shimoni A, et al. Mobilized peripheral blood stem cells compared with bone marrow as the stem cell source for unrelated donor allogeneic transplantation with reduced-intensity conditioning in patients with acute myeloid leukemia in complete remission: an analysis from the Acute Leukemia Working Party of the European Group for Blood and Marrow Transplantation. Biol Blood Marrow Transplant 2012;18 : 1422–1429.
5. Holtick U, Albrecht M, Chemnitz JM, et al. Comparison of bone marrow versus peripheral blood allogeneic hematopoietic stem cell transplantation for hematological malignancies in adults – a systematic review and meta-analysis. Crit Rev Oncol Hematol 2015;94 : 179–188.
6. Savani BN, Labopin M, Blaise D, et al. Peripheral blood stem cell graft compared to bone marrow after reduced intensity conditioning regimens for acute leukemia: a report from the ALWP of the EBMT. Haematologica 2016;101 : 256–262.
7. Lee SJ, Logan B, Westervelt P, et al. Comparison of patient-reported outcomes in 5-year survivors who received bone marrow vs peripheral blood unrelated donor transplantation: long-term follow-up of a randomized clinical trial. JAMA Oncol 2016;2 : 1583–1589.
8. Eapen M, Logan BR, Horowitz MM, et al. Bone marrow or peripheral blood for reduced-intensity conditioning unrelated donor transplantation. J Clin Oncol 2015;33 : 364–369.
9. Byrne M, Savani BN, Mohty M, Nagler A. Peripheral blood stem cell versus bone marrow transplantation: A perspective from the Acute Leukemia Working Party of the European Society for Blood and Marrow Transplantation. Exp Hematol 2016;44 : 567–573.
10. Miller JP, Perry EH, Price TH, et al. Recovery and safety profiles of marrow and PBSC donors: experience of the National Marrow Donor Program. Biol Blood Marrow Transplant 2008;14 : 29–36.
11. Switzer GE, Bruce JG, Harrington D, et al. Health–related quality of life of bone marrow versus peripheral blood stem cell donors: a prespecified subgroup analysis from a phase III RCT – BMTCTN Protocol 0201. Biol Blood Marrow Transplant 2013;20 : 118–127.
12. Spitzer TR, Areman EM, Cirenza E, et al. The impact of harvest center on quality of marrows collected from unrelated donors. J Hematother 1994;3 : 65–70.
13. Parkkali T, Juvonen E, Volin L, et al. Collection of autologous blood for bone marrow donation: how useful is it? Bone Marrow Transplant 2005;35 : 1035–1039.
14. Mijovic A, Britten C, Regan F, et al. Preoperative autologous blood donation for bone marrow harvests: Are we wasting donors time and blood? Transfusion Med 2006;16 : 57–62.
15. Arora K, Kelley J, Martinez F, et al. Preoperative autologous collec-tion before bone marrow harvests in haploidentical related donors: is it justified? Transfusion 2018;58 : 1618–1625.
16. Spitzer TR, Sugrue MW, Gonzalez C, et al. Transfusion practices for bone marrow harvests: a survey analysis from the AABB Bone Marrow Quality Improvement Initiative Working Group. Bone Marrow Transplant 2017;52 : 1199–1200.
17. Bashey A, Zhang MJ, McCurdy SR, et al. Mobilized peripheral blood stem cells versus unstimulated bone marrow as a graft source for T-cell-replete haploidentical donor transplantation using post-transplant cyclophosphamide. J Clin Oncol 2017;10;3002–3009.
18. Battiwalla M, Tichelli A, Majhail NS. Long-term survivorship after hematopoietic cell transplantation: roadmap for research and care. Biol Blood Marrow Transplant 2017;2 : 184–192.
19. Bacigalupo A, Tong J, Podesta M, et al. Bone marrow harvest for marrow transplantation: effect of multiple small (2 ml) or large (20 ml) aspirates. Bone Marrow Transplant 1992;9 : 467–470.
20. Remberger M, Ringden O, Mattsson J. Bone marrow aspiration technique has deteriorated in recent years. Bone Marrow Transplant 2015;50 : 1007–1009.
21. Pulsipher MA, Logan BR, Kiefer DM, et al. The effect of race, socioeconomic status, and collection center size on bone marrow (BM) and peripheral blood stem cell (PBSC) donor experiences at National Marrow Donor Program (NMDP) collection centers. Biol Blood Marrow Transplant 2015;21 : 40–41.
22. Vassallo R, Goldman M, Germain M, Lozano M, BEST Collaborative. Preoperative autologous blood donation: waning indications in an era of improved blood safety. Transfus Med Rev 2015;29 : 268–275.
23. Kiss JE, Brambilla D, Glynn SA, et al. National Heart, Lung, and Blood Institute (NHLBI) Recipient Epidemiology and Donor Evaluation Study–III (REDS-III). Oral iron supplementation after blood donation: a randomized clinical trial. JAMA 2015;10 : 575–583.
24. Pruszczyk K, Skwierawka K, Malgorzata K, et al. Bone marrow harvest from unrelated donors-up-to-date methodology. Eur J Haematol 2017;99 : 357–365.
25. Bartnik K, Pruszczyk K, Skwierawska K, et al. Bone marrow harvest in donors with anaemia. Vox Sang 2018;113 : 795–802.
26. Gouëzec H, Ferré N, Hervé F, et al. Suitability of autologous blood donation before bone marrow donation. Transfus Clin Biol 2015;22 : 71–75.
27. Carson JL, Grossman BJ, Kleinman S, et al. Red blood cell transfusion: a clinical practice guideline from the AABB*. Ann Intern Med 2012;157 : 49–58.
28. Lown RN, Philippe J, Navarro W, et al. Unrelated adult stem cell donor medical suitability: recommendations from the World Marrow Donor Association Clinical Working Group Committee. Bone Marrow Transplant 2014;49 : 880–888.
29. Lysák D, Hrabětová M, Jungová A, Svoboda T, Navrátilová J, Koza V. Nežádoucí reakce při odběru hemopoetických kmenových buněk u nepříbuzných dárců – desetiletá zkušenost Českého národního registru dárců dřeně (ČNRDD). Transfuze Hematol dnes 2011;3 : 130–137.
30. Miller JP, Perry EH, Price TH, et al. Recovery and safety profiles of marrow and PBSC donors: experience of the national marrow donor program. Biol Blood Marrow Transplant 2008;14 : 29–36.
31. Halter J, Kodera Y, Ispizua AU, et al. Severe events in donors after allogeneic hematopoietic stem cell donation. Haematologica 2009; 94 : 94–101.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2019 Číslo 4- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Steroidní a nesteroidní inhibitory aromatázy v léčbě rakoviny prsu u postmenopauzálních žen
- Ibrance® – nová šance pro pacientky s HR+/HER2– karcinomem prsu
-
Všechny články tohoto čísla
- Genová editace systémem CRISPR/Cas9 a její využití v hematologii
- Komplexní mechanismy účinku inhibitorů „BCR signalizace“ a vzniku rezistence na tuto cílenou léčbu u chronické lymfocytární leukemie
- Úloha signální dráhy transformačního růstového faktoru β v hemopoéze a studie nových inhibitorů této dráhy pro léčbu nízkorizikového myelodysplastického syndromu
- Denosumab a bisfosfonáty u mnohočetného myelomu v roce 2019
- Mutace genů rodiny RAS u pacientů s akutní myeloidní leukemií
- Charakteristika a výsledky léčby pacientů s akutní myeloidní leukemií ≥ 60 let – data z databáze CELL DATOOL AML
- Odběry kostní dřeně pro alogenní transplantaci – zhodnocení desetileté zkušenosti se zaměřením na využití autotransfuzí u dárců
- Transfuze a hematologie dnes
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Genová editace systémem CRISPR/Cas9 a její využití v hematologii
- Charakteristika a výsledky léčby pacientů s akutní myeloidní leukemií ≥ 60 let – data z databáze CELL DATOOL AML
- Komplexní mechanismy účinku inhibitorů „BCR signalizace“ a vzniku rezistence na tuto cílenou léčbu u chronické lymfocytární leukemie
- Mutace genů rodiny RAS u pacientů s akutní myeloidní leukemií
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



