-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Lymfatický systém: novinky v morfologii a patologii
Lymphatic System: Morphology and Pathology Update
The lymphatic system is crucial for the maintenance of tissue fluid balance, immune surveillance, and fatty acids absorption in the intestine. The lymphatic vessels are also involved in the pathogenesis of tumor metastasis, lymphedema, and various inflammatory processes. Recently, several markers specific for lymphatic endothelium were found. Progress in the field of lymphatic growth factors and their receptors, and molecular lymphatic biology has helped to understand better the lymphatic vasculature. This review summarizes the updates on lymphatic system research and possible applications in routine pathological diagnostics.
Key words:
lymphangiogenesis – lymphatic system
Autoři: I. Kholová
Působiště autorů: Pathology, Laboratory Centre, Tampere University Hospital, Tampere, Finland
Vyšlo v časopise: Čes.-slov. Patol., 46, 2010, No. 4, p. 98-103
Kategorie: Přehledový článek
Souhrn
Lymfatický systém hraje nezastupitelnou roli v tkáňové homeostáze tekutin, imunitních mechanismech organismu a absorpci mastných kyselin ve střevě. Lymfatické cévy jsou zapojeny do procesu nádorového šíření, lymfedému a řady zánětlivých onemocnění. V nedávné době byly objeveny a popsány specifické protilátky, schopné detekovat endotel lymfatických cév. Zároveň došlo k pokroku ve výzkumu vaskulárních růstových faktorů, jejich receptorů a molekul zapojených do vývoje lymfatického systému. Předkládaný článek shrnuje nejnovější poznatky z oblasti výzkumu lymfatického systému a jejich možné aplikace do rutinní patologické diagnostiky.
Klíčová slova:
lymfangiogeneze – lymfatický systémHistorická perspektiva
První popis lymfatického systému se datuje do 17. století, kdy Gasparo Aselli popsal lymfatické cévy mesenteria u psa jakožto mléčné žíly (2). Jejich embryogeneze zůstávala neznámou do začátku 20. století, kdy Sabin a Lewis navrhli jejich původ z žilního endotelu (49). Tzv. centrifugální teorie navrhuje původ lymfatik pučením z žilních cév a tvorbu primitivního lymfatického vaku v jugulární oblasti. Vytvořené lymfatické endotelie pak putují do periferie, kde vytvářejí kapiláry obkružující orgány. Tato teorie byla podpořena nedávnými genetickými studiemi (62). Alternativní teorie (centripetální) navrhla původ lymfatických endotelií z mesenchymu (19). Mesenchymální progenitorové buňky nazýváme lymfangioblasty. Podle duální teorie, část lymfatik, především v povrchových orgánech a kůži, vzniká z lymfangioblastů (63).
Lymfatický vaskulární systém
Struktura a funkce
Lymfatický systém funguje jako otevřený jednocestný systém začínající slepě ve tkáních. Síť lymfatických kapilár se specializuje na drenáž intersticiální tekutiny (tkáňového moku) a návrat makromolekul a leukocytů z tkáňového intersticia do oběhu. Histologicky je stěna lymfatických kapilár tvořena endoteliemi obklopenými nesouvislou bazální membránou. Lymfatické kapiláry bývají často kolabované. Větší lymfatické cévy tkáňový mok transportují do lymfatických uzlin, které jsou v jejich průběhu. Lymfatické cévy mají stěnu tvořenou lymfatickým endotelem, hladkou svalovinou a bazální membránou. V jejich průběhu se nacházejí chlopně regulující tok tkáňového moku. Tkáňový mok je z lymfatického systému vyprazdňován do žilního oběhu. Lymfatické cévy se vyskytují ve všech tkáních s výjimkou nevaskularizovaných jako je epidermis, chrupavka a rohovka a z vaskularizovaných tkání pak nejsou v mozku, kostní dřeni a sítnici (26).
Vývoj lymfatického systému a jeho molekulární regulace
Lymfatický systém se vyvíjí v průběhu midgestace. Identifikace klíčových molekul zapojených do vývoje lymfatického systému umožnila hlouběji pochopit celý proces. Výzkum probíhal pomocí knock-out myší. Nicméně část mechanismů včetně tzv. fine-tuning zůstává neobjasněna. LYVE-1, hyaluronový receptor-1 lymfatického endotelu, je prvním indikátorem polarizace žilního endotelu lymfatickým směrem (41). Prox-1 je klíčová molekula ve vývoji; záhy po začátku exprese v endotelu přední kardinální žíly dochází k pučení, migraci a vytvoření lymfatického vaku (42, 61). VEGF-C/VEGFR-3 se podílí na počátečním větvení a migraci a později během embryonálního vývoje a krátce po narození hraje roli v udržení soudržnosti a charakteristik lymfatického endotelu (25). Na rozdíl od VEGF-C, VEGF-D vázající se též na VEGFR-3 nehraje žádnou zásadní roli ve vývoji lymfatického systému (3). Role VEGFR-2 je především ve formě VEGFR-2/VEGFR-3 heterodimeru v migraci a proliferaci lymfatických endotelií (12, 39). Podoplanin je membránový glykoprotein a klíčová molekula ve vývoji lymfatických cév (50). FOXC2 je transkripční faktor, který hraje roli v pozdní embryonální morfogenezi lymfatického systému, kdy kontroluje vztah lymfatického endotelu s neendotelovými buňkami cévní stěny (26).
Další molekuly podílející se na vývoji lymfatického systému jsou neuropilin-2, angiopoietiny, ephrinB2, Syk a Slp76 (26, 27). Heterogenita lymfatického systému na molekulární úrovni nebyla doposud podrobně studována.
Imunohistochemická detekce
Před objevem protilátek specifických pro endotel lymfatických cév, byly nejrůznější morfologické studie prováděny pomocí nástřiku lymfatických cév (13). Ultrastruktura byla studována pomocí elektronového mikroskopu. Z histochemických technik, enzym 5’nukleotidáza je exprimován endotelem lymfatik a jeho detekce je možná na zmrazených řezech azokopulační či ceriovou reakcí (28, 46) (obr. 1a).
Obr. 1. Lymfatické cévy v různých normálních a patologicky změněných tkáních. a. Lymfatická kapilára v myším jazyku detekovaná histochemicky ceriovou reakcí na 5’nukleotidázu (400krát); b. Lymfatické cévy v normálním myokardu lidského srdce; imunohistochemická reakce s protilátkou D2-40 (100krát); c. Jejunální lymfangiom vykazuje podoplanin imunopozitivitu v lymfatických cévách (200krát); d. Zvýšené množství lymfatik v perikardu postiženém perikarditidou; imunohistochemická reakce s protilátkou D2-40 (100krát); e. Šíření nádorových buněk adenokarcinomu žaludku lymfatickými cévami (HE, 200krát); f. Intratumorální lymfatické cévy v adenokarcinomu tlustého střeva; imunohistochemická reakce s protilátkou proti podoplaninu (100krát) 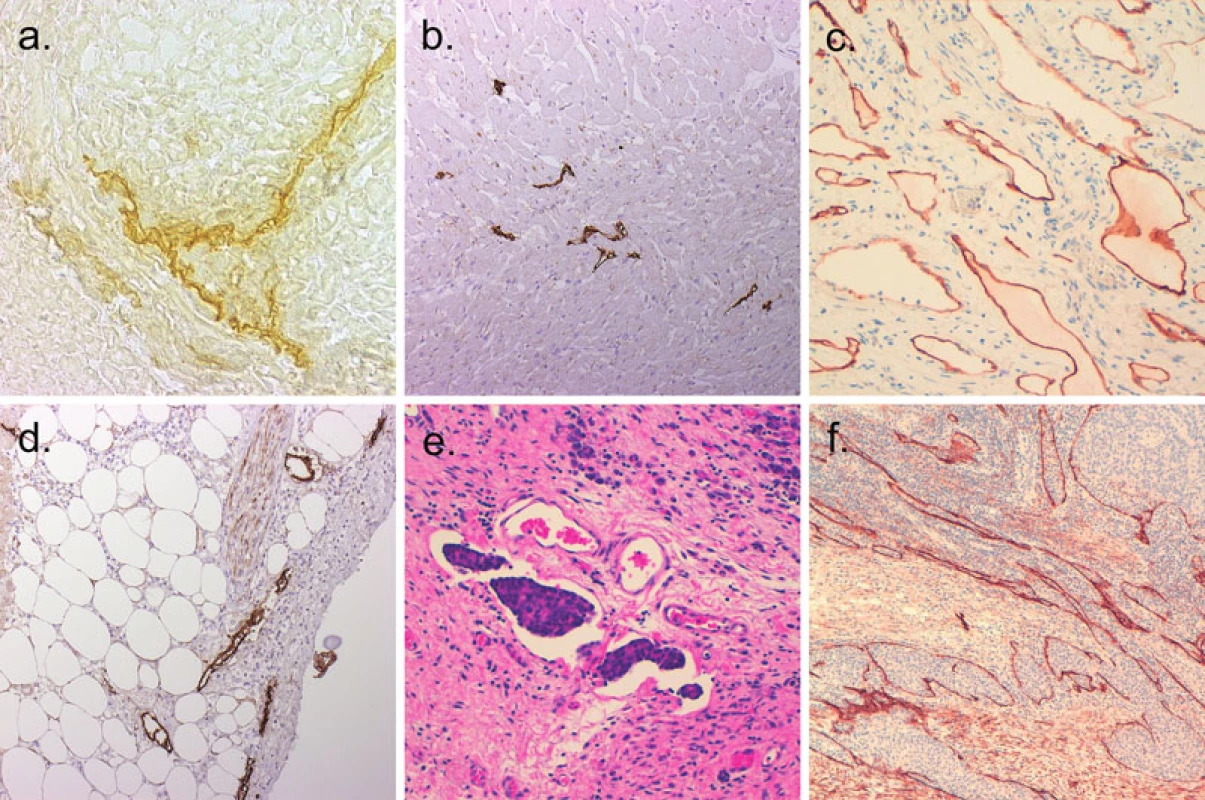
Protilátek pro imunohistochemickou reakci bylo popsáno hned několik. LYVE-1 vykazuje vysokou pozitivitu v endotelu kapilár, ale ke snížení exprese dochází v endotelu sběrných lymfatických žil u dospělých (6, 36). V určitých tkáních však může být problematický fakt, že LYVE-1 exprimují také makrofágy (20). Prox-1 je specifický pro endotelie, ale jeho exprese v jejich jádře jej činí méně vhodný pro morfologické studie. VEGFR-3 je exprimován v období vývoje lymfatických endotelií, ale není vhodný pro dospělé organismy, u kterých je též pozitivní na fenestrovaných kapilárách (36). Podoplanin je pozitivní jak v endotelu kapilár, tak sběrných lymfatických žil u dospělých (10) (obr. 1b). D2-40 byl popsán poprvé u lymfangiosarkomu a podskupiny angiosarkomů, včetně Kaposiho sarkomu. Jedná se o protilátku detekující M2A antigen, který je fixaci odolný epitop podoplaninu. M2A antigen detekovaný D2-40 protilátkou byl však popsán i v řadě normálních a nádorových neendoteliálních buněk včetně myoepitelií mléčné žlázy, Cajalových buněk, folikulárních dendritických buněk, mesotelií a seminálních buněk (5, 23). Protilátky detekující lymfatické cévy v parafinových řezech jsou shrnuty v tabulce 1.
Tab. 1. Protilátky pro imunohistochemickou detekci lymfatického endotelu v parafinových řezech 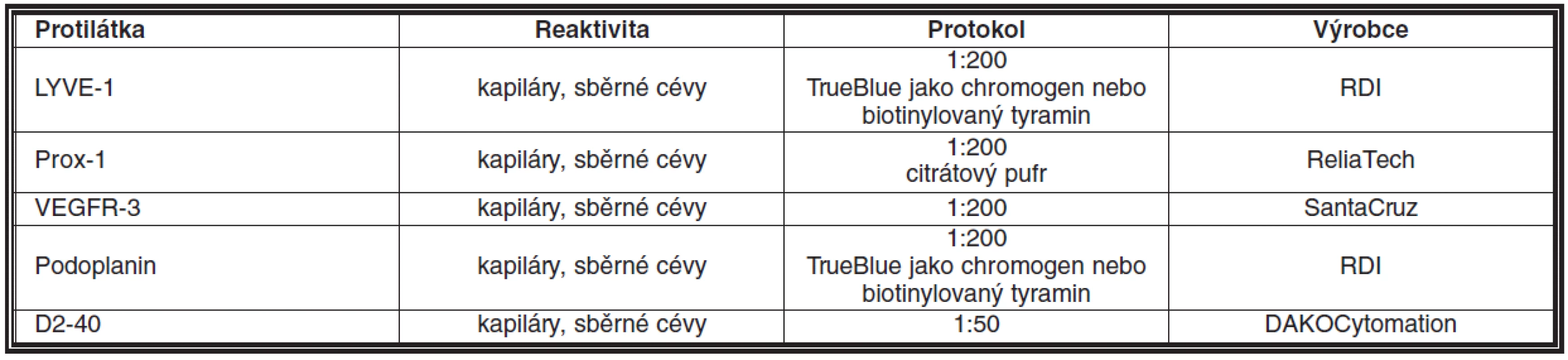
Lymfangiogeneze a růstové faktory
V dospělosti, podobně jako u angiogeneze, jsou lymfatické cévy v tzv. klidovém stadiu. Výjimkou je tkáňová a orgánová regenerace, hojení ran, zánět a nádorový růst, včetně šíření nádorových buněk. Novotvorba v dospělosti probíhá hlavně z již existujících lymfatik tzv. sprouting („pučení“) mechanismem. Endoteliální progenitorové buňky se podílí spíše na tvorbě podpůrných buněk cévní stěny. Role diferencovaných makrofágů byla navržena především v patologické lymfangiogenezi (26, 45).
VEGFR-3 je hlavním regulačním faktorem lymfangiogeneze. Podílí se na růstu lymfatických endotelií pre - a postnatálně a na přežívání lymfatických endotelií v embryogenezi a krátce po narození. Jeho dvě ligandy: VEGF-C a VEGF-D jsou schopné indukovat lymfangiogenezi jak in vivo, tak in vitro (26). Biologické vlastnosti VEGF-C a VEGF-D však odvisí od jejich formy a tzv. krátké molekuly jsou především angiogenní (9, 31, 46). Překvapivě také VEGF-A je za určitých podmínek lymfangiogenní, a to v průběhu hojení a nádorového bujení (16, 38).
Patologie lymfatických cév
Nádorová lymfangiogeneze a metastazování
U většiny nádorů je rozšíření do regionálních lymfatických uzlin první známkou rozsevu nádoru. Rozsah metastazování do lymfatických uzlin je součástí TNM klasifikace a stagingu a má vliv na prognózu nádorového onemocnění. Přítomnost a hustota lymfatických cév byla studována v celé řadě nádorů. Mechanismus, jakým nádorové buňky vstupují do lymfatického systému není ještě zcela pochopen. Nádorové buňky jednak využívají již existující cévy na svém okraji či cévy novotvořené. Mechanismus vzniku lymfatických cév v oblasti nádoru je obdobou nenádorové lymfangiogeneze. Lymfatické cévy uvnitř nádoru bývají však často nefunkční a na metastazování se podílejí především cévy na periferii nádoru (1, 52) (obr. 1e, f).
VEGF-A je považován za hlavní molekulu nádorové angiogeneze, avšak skrze VEGFR-1 pozitivní makrofágy je schopen navýšit také hladinu lymfangiogeních faktorů VEGF-C a VEGF-D v oblasti nádoru (16). V experimentálních podmínkách, při zvýšení hladiny VEGF-C a VEGF-D v oblasti nádoru, metastazovaly do lymfatických uzlin dokonce i nádory běžně nemetastazující. Naopak blokováním VEGF-D kaskády se v experimentu podařilo snížit metastazování do lymfatických uzlin o 60–70 % (1). U lidských nádorů byla prokázána korelace mezi hladinami VEGF-C a VEGF-D a invazí lymfatického systému, včetně uzlin a orgánových metastáz. Hladina VEGF-C a VEGF-D však nekorelovala s hustotou lymfatických cév v oblasti nádoru (55). VEGF-C má vliv na rozšíření lumina sběrných lymfatických cév (52). V sentinelových lymfatických uzlinách byla prokázána hyperplazie sinusů ještě před přítomností prvních nádorových buněk a tato reakce je považována za přípravu uzliny k přijetí buněk (55).
Lymfedém: primární a sekundární
Nedostatečnost lymfatických cév se projevuje nahromaděním bílkovin a následně tekutiny v mezibuněčném prostoru. Přítomnost tekutiny bohaté na bílkoviny v intersticiu vede k zánětlivé reakci, nahromadění vaziva a tuku a narušení místního imunitního systému.
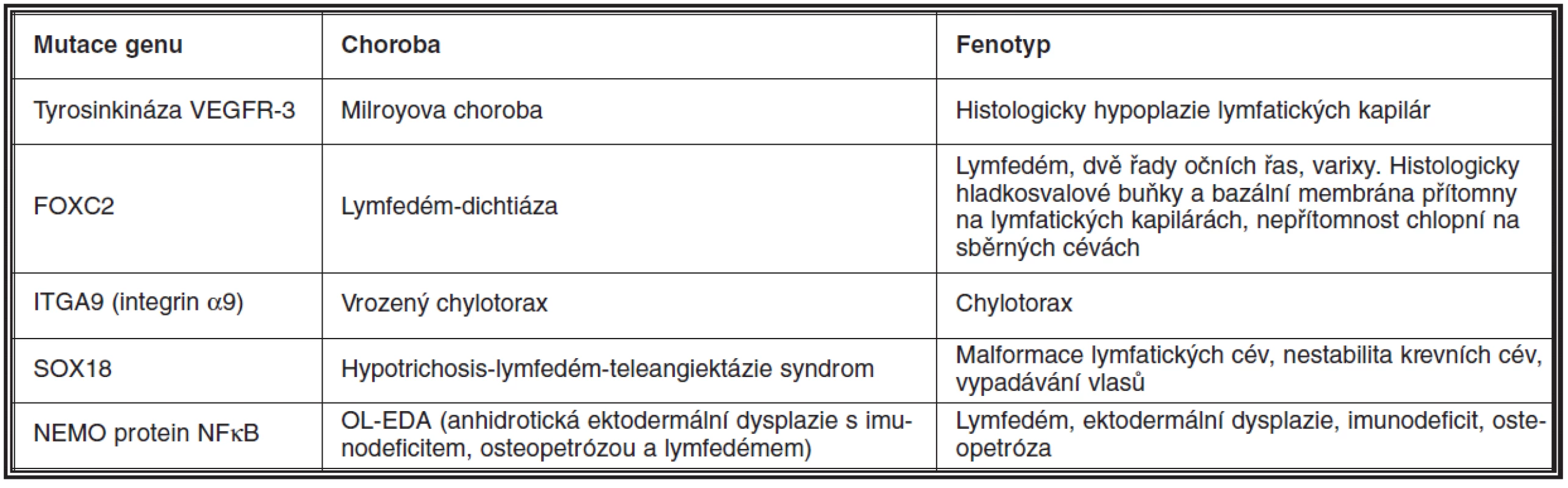
Lymfedém je podle mechanismu vzniku dělen na primární – geneticky podmíněný, a sekundární. Primární lymfedém je vzácný. Doposud byla popsána celá řada mutací a s nimi spojených syndromů, které doprovází porucha lymfatických cév a následný lymfedém (52). Nejčastěji se vyskytující jsou shrnuty v tabulce 2.
Sekundární lymfedém tvoří 99 % všech postižení. Jeho nejčastější příčinou je filariáza, nazývaná též elefantiáza. Postihuje celosvětově 100 milionů lidí. Infekce lymfatických cév parazity Wuchereria bancrofti, Brugia malayi či Brugia timori vede k jizvení a obstrukci cév a následnému edému dolních končetin a genitálií. Patogeneticky zánětlivá reakce na počátku onemocnění vede ke zvýšené produkci VEGF-A, VEGF-C a VEGF-D a hyperplazii lymfatických cév (43). Nejčastější příčinou lymfedému v rozvinutém světě je operace karcinomu prsu a následná radioterapie. Lymfedém horní končetiny vzniká u 20–30 % pacientek, které podstoupily axilární lymfadenektomii. Dalšími příčinami sekundárního lymfedému jsou bakteriální infekce kůže (např. erysipel) či lymfatických cév (60).
Sekundární lymfedém vzniká poškozením sběrných lymfatických cév. Experimentálně, VEGF-C stimuloval novotvorbu lymfatik u myšího modelu lymfedému a následné zmenšení edému. V jiném myším modelu VEGF-C a VEGF-D genový transfer vedl k novotvorbě lymfatik v oblasti axilární lymfadenektomie. VEGF-C navíc zvýšil úspěšnost transplantace lymfatických uzlin (53).
Zánět
Lymfatický systém hraje významnou roli v regulaci zánětu. Podílí se na přenosu antigenu a leukocytů z místa zánětu do lymfatických uzlin a sekundárních lymfatických orgánů. Novotvořené lymfatické cévy se vyskytují v místech zánětlivé reakce (4, 52) (obr. 1d). Prozánětlivé cytokiny zvyšují hladinu VEGF-C a VEGF-D (4, 47). NFκB je pozitivní v některých lymfatických cévách (48). Makrofágy exprimují VEGFR-1 a VEGFR-3 a jsou tak zapojeny do procesu novotvorby jak krevních, tak lymfatických cév (11). Novotvorba lymfatik doprovází i chronické zánětlivé procesy, např. psoriázu a revmatoidní artritidu (24, 32). V aterosklerotických lézích byly rovněž popsány novotvořené lymfatické cévy. Lymfatika přítomná v adventicii velkých cév se pravděpodobně podílejí na drenáži zánětlivých buněk z aterosklerotických lézí (64). V polovině z vyšetřovaných kalcifikovaných aortálních stenóz, které jsou považovány za formu aterosklerózy, byly prokázány lymfatické cévy (51).
Transplantace
Rejekce ledvinového štěpu je spojena s lymfangiogenezí. Lymfatické cévy hostitele produkují CCL21, který aktivuje dendritické buňky a celou kaskádu reakcí (29, 30). Blokáda VEGFR-3 v experimentu v srdečních štěpech vedla ke snížení CCL21 a ovlivnění imunitní reakce a rejekce (40).
Lymfangiektázie a nádory lymfatického systému
Lymfangiektázie je definována jako místní vakovité rozšíření lymfatických cév. V literatuře bývá nesprávně používán i termín získaný či sekundární lymfangiom. Vyskytuje se jednak vrozeně jako součást geneticky podmíněných vrozených vad a také postoperačně a po ozáření, spolu s lymfedémem a v souvislosti s místním postižením lymfatických cév. V oblasti kůže byly lymfangiektázie popsány i jako komplikace infekcí např. skrofulodermy a erysipelu (58).
Plicní lymfangiektázie je vzácná vrozená abnormalita charakterizovaná rozšířenými lymfatiky v oblasti pleury, interlobárně, perivaskulárně a peribronchiálně. V etiopatogenezi se spekuluje o poruše regrese lymfatických kanálů plic v období 20. týdne gestace. Sekundárně se vyvíjí u vrozených srdečních vad. Plicní lymfangiektázie bývají jak sporadické, tak součástí jiných vrozených syndromů, např. Downova a Turnerova (8).
Ve střevech se lymfangiektázie vyskytuje primárně jako tzv. Waldmannova choroba, u které dilatovaná střevní lymfatika vedou ke ztrátě bílkovin do střevního lumena a sekundárně k lymfopénii, hypoalbuminémii a hypogamaglobulinémii. Klinicky se choroba projevuje oboustranným edémem dolních končetin; edém postihuje i tělesné dutiny. Střevní biopsie je diagnostická a diferenciální diagnostika zahrnuje střevní lymfomy, Whippleovu chorobu, Crohnovu chorobu a střevní granulomatózní záněty (59). Sekundární střevní lymfangiektázie byla popsána u Waldenströmovy makroglobulinémie (44).
Renální lymfangiektázie je vzácná vývojová malformace, kdy ledvinná lymfatika v průběhu vývoje nejsou spojena s lymfatickým systémem. Nekomunikující lymfatika tak cysticky dilatují. Postižena bývá oblast pánvičky, parenchym či fascie, někdy je postižena i oblast retroperitonea. Zároveň byly popsány případy, kdy jsou v retroperitoneu perivaskulární lymfatické cysty. Klinicky může být malformace asymptomatická, pouze u jediného dětského pacienta byla popsána ledvinová nedostatečnost (56).
Hennekamův syndrom je kombinace lymfedému, lymfangiektázií a mentální retardace. Lymfangiektázie postihují nejčastěji střeva, ale byly popsány i v oblasti pleury, perikardu, štítné žlázy a ledvin (57).
Lymfangiom je benigní nádor z lymfatických cév, který se vyskytuje často u dětí a řada forem je vrozená (obr. 1c). Cystická forma je nejčastěji lokalizována v oblasti krku, podpaží či třísel. Kavernózní forma bývá popisována navíc v oblasti úst, trupu a končetin. Tenkostěnné dilatované cévy mohou obsahovat bílkovinnou tekutinu, lymfocyty a nezřídka erytrocyty. Častá je lymfocytární infiltrace nádorového stromatu (7).
Lymfangiosarkom je nejčastěji popisován jako komplikace dlouhotrvajícího lymfedému a v souvislosti s mastektomií a ozařováním pro karcinom prsu (21, 37).
Kaposiho sarkom se vyskytuje v klasické, endemické, iatrogenní a HIV/AIDS asociované formě. Typicky postihuje kůži, ale v průběhu choroby se léze šíří do sliznic, lymfatických uzlin a vnitřních orgánů. Etiopatogeneze je dávána do souvislosti s lidským herpesvirem 8 (33). V nádorových vřetenitých buňkách jsou pozitivní markery jak krevních, tak lymfatických endotelií (22).
Lymfangioleiomyomatóza
Lymfangioleiomyomatóza je vzácná choroba postihující ženy ve středním věku, s fatální prognózou. Histologicky je charakterizována proliferací abnormálních hladkosvalových buněk, které vytvářejí plicní cysty, cystické útvary v uzlinách podpaží a nádory v břišní dutině, nejčastěji v oblasti ledvin. Choroba se vyskytuje ve sporadické formě a jako součást tuberózní sklerózy (17, 54).
Obezita a metabolismus tuků
Lymfatické cévy slouží k absorbci triglyceridů, cholesterolu a dalších tuků ve střevě. Prox-1 heterozygotním myším se v dospělosti vyvine chylózní výpotek a obezita (15). Rovněž lymfedém je doprovázen nahromaděním tuku (60).
Hypertenze
Lymfatické cévy hrají významnou roli v tkáňové homeostáze tekutin. Nedávné studie ukázaly vliv VEGF-C modulovaného monocyto-makrofágového systému na hyperplazii lymfatických cév v kůži experimentálních krys při dietě se zvýšeným obsahem sodíku. Na druhou stranu, VEGF-C/eNOS má vliv na snížení krevního tlaku (35).
Shrnutí
Patologové mají v současnosti možnost využívat v rutinní diagnostice hned několik markerů specifických pro lymfatické endotelie. Stanovení lymfatických cév a prolymfangiogenních růstových faktorů má význam také v prognóze nádorových onemocnění.
Autorka pracovala řadu let a nadále spolupracuje s Center of Excellence for Research in Cardiovascular Diseases and Type 2 Diabetes of the Academy of Finland v A. I. Virtanen institutu molekulárních věd v Kuopiu, které patří ke špičkovým pracovištím zabývajícím se lymfangiogenezí.
Doc. MUDr. Ivana Kholová, Ph.D., Pathology, Laboratory Centre,
P.O.Box 2000, FIN-33521 Tampere, Finland
telefon +358 3 311 717, e-mail ivana.kholova@sll.fimnet.fi
Zdroje
1. Achen, M.G., McColl, B.K., Stacker, S.A.: Focus on lymphangiogenesis in tumor metastasis. Cancer Cell, 7, 2005, s. 121–127.
2. Asellius, G.: De lactibus sive lacteis venis. Milan: Mediolani, 1627.
3. Baldwin, M.E., Halford, M.M., Roufail, S. et al.: Vascular endothelial growth factor D is dispensable for development of the lymphatic system. Mol. Cell. Biol., 25, 2005, s. 2441–2449.
4. Baluk, P., Tammela, T., Ator, E. et al.: Pathogenesis of persistent lymphatic vessel hyperplasia in chronic airway inflammation. J. Clin. Invest., 115, 2005, s. 247–257.
5. Bandarchi, B., Ma, L., Marginean, C., Hafezi, S., Zubovits, J., Rasty, G: D2-40, a novel immunohistochemical marker in differentiating dermatofibroma from dermatofibrosarcoma protuberans. Mod. Pathol., 23, 2010, s. 434–438.
6. Banerji, S., Ni, J., Wang S.X. et al.: LYVE-1, a new homologue of the CD44 glycoprotein, is a lymph-specific receptor for hyaluronan. J. Cell. Biol, 144, 1999, s. 789–801.
7. Beham, A.: Lymphangioma. In: Tumours of soft tissue and bone. Ed. Fletcher, Ch.D.M., Unni, K.K., Mertens, F. IARCPress, Lyon, 2002, s. 162–163.
8. Bellini, C., Boccardo, F., Campisi, C., Bonioli, E.: Congenital pulmonary lymphangiectasia. Orp. J. Rare Dis., 43, 2006, s. 43.
9. Bhardwaj, S., Roy, H., Gruchala, M. et al.: Angiogenic responses of vascular endothelial growth factors in periadventitial tissue. Hum. Gene Ther., 14, 2003, s. 1451–1462.
10. Breiteneder-Geleff, S., Soleiman, A., Kowalski, H. et al.: Angiosarcomas express mixed endothelial phenotypes of blood and lymphatic capillaries: podoplanin as a specific marker for lymphatic endothelium. Am. J. Pathol., 154, 1999, s. 385–394.
11. Cursiefen, C., Chen, L., Borges, L.P. et al.: VEGF-A stimulates lymphangiogenesis and hemangiogenesis in inflammatory neovascularization via macrophage recruitment. J. Clin. Invest., 113, 2004, s. 1040–1050.
12. Dixelius, J., Makinen, T., Wirzenius, M. et al.: Ligand-induced vascular endothelial growth factor receptor-3 (VEGFR-3) heterodimerization with VEGFR-2 in primary lymphatic endothelial cells regulates tyrosine phosphorylation sites. J. Biol. Chem., 278, 2003, s. 40973–40979.
13. Eliskova, M., Eliska, O.: Light microscopy of the lymphatics of the human atrial wall and lymphatic drainage of supraventricular pacemakers. Int. Angiol., 8, 1989, s. 1–6.
14. Gale, N.W., Thurston, G., Hackett, S.F. et al.: Angiopoietin-2 is required for postnatal angiogenesis and lymphatic patterning, and only the latter role is rescued by Angiopoietin-1. Dev. Cell, 3, 2002, s. 411–423.
15. Harvey, N.L.: The link between lymphatic function and adipose biology. Ann. N. Y. Acad., 1131, 2008, s. 82–88.
16. Hirakawa, S., Kodama, S., Kunstfeld, R., Kajiya, K., Brown, L.F., Detmar, M.: VEGF-A induces tumor and sentinel lymph node lymphangiogenesis and promotes lymphatic metastases. J. Exp. Med., 201, 2005, s. 1089–1099.
17. Hohman, D.W., Noghrehkar, D., Ratnayake, S.: Lymphangioleiomyomatosis: a review. Eur. J. Intern. Med., 19, 2008, s. 319-324.
18. Huang, X.Z., Wu, J.F., Ferrando, R. et al.: Fatal bilateral chylothorax in mice lacking integrin α91. Mol. Cell. Biol., 20, 2000, s. 5208–5215.
19. Huntington, G.C., McClure, C.F.W.: The anatomy and development of the jugular lymph sacs in the domestic cat (Felis domestica). Am. J. Anat., 10, 1910, s. 177–311.
20. Cho, C.-H., Koh, Y.J., Han, J. et al.: Angiogenic role of LYVE-1-positive macrophages in adipose tissue. Circ. Res., 100, 2007, s. 47–57.
21. Chung, K.C., Kim, H.J., Jeffers, L.L.: Lymphangiosarcoma (Stewart-Treves syndrome) in postmastectomy patients. J. Hand Surg. Am., 25, 2000, s. 1163–1168.
22. Jussila, L., Valtola, R., Partanen, T.A. et al.: Lymphatic endothelium and Kaposi’s sarcoma spindle cells detected by antibodies against the vascular endothelial growth factor receptor-3. Cancer Res., 58, 1998, s. 1599–1604.
23. Kahn, H.J., Bailey, D., Marks, A.: Monoclonal antibody D2-40, a new marker of lymphatic endothelium, reacts with Kaposi’s sarcoma and subset of angiosarcomas. Mod. Pathol, 15, 2002, s. 434–440.
24. Kajiya, K., Detmar, M.: An important role of lymphatic vessels in the control of UVB-induced edema formation and inflammation. J. Invest. Dermatol., 126, 2006, 919–921.
25. Karkkainen, M.J., Haiko, P., Sainio K. et al.: Vascular endothelial growth factor C is required for sprouting of the first lymphatic vessels from embryonic veins. Nat. Immunol., 5, 2004, s. 74–80.
26. Karpanen, T., Alitalo K.: Molecular biology and pathology of lymphangiogenesis. Annu. Rev. Pathol. Mech. Dis., 3, 2008, s. 367–397.
27. Karpanen, T., Heckman, C.A., Keskitalo, S., et al.: Functional interaction of VEGF-C and VEGF-D with neuropilin receptors. FASEB J., 20, 2006, s. 1462–1472.
28. Kato S., Yasunaga, A., Uchida U.: Enzyme-histochemical method for identification of lymphatic capillaries. Lymphology, 24, 1991, s. 125–129.
29. Kerjaschki, D., Huttary, N., Raab, I. et al.: Lymphatic endothelial progenitor cells contribute to de novo lymphangiogenesis in human renal transplants. Nat. Med. 12, 2004, 230–234.
30. Kerjaschki, D., Regele, H.M., Moosberger, I. et al.: Lymphatic neoangiogenesis in human kidney transplants is associated with immunologically active lymphocytic infiltrates. J. Am. Soc. Nephrol., 15, 2004, 603–612.
31. Kholová, I., Koota, S., Kaskenpaa, N. et al.: Adenovirus-mediated gene transfer of human vascular endothelial growth factor-d induces transient angiogenic effects in mouse hind limb muscle. Hum. Gene Ther., 2007, 18, s. 232–244.
32. Kunstfeld, R., Hirakawa, S., Hong, Y.K.: Induction of cutaneous delayed-type hypersensitivity reactions in VEGF-A transgenic mice results in chronic skin inflammation associated with persistent lymphatic hyperplasia. Blood, 104, 2004, s. 1048–1057.
33. Lakomec, J., Knuutila, S.: Kaposi sarcoma. In: Tumours of soft tissue and bone. Ed. Fletcher, Ch.D.M., Unni, K.K., Mertens, F. IARCPress, Lyon, 2002, s. 170–172.
34. Lewis, F.: The development of the lymphatic system in rabbits. Am. J. Anat., 5, 1905, s. 95–111.
35. Machnik, A., Neuhofer, W., Jantsch, J. et al.: Macrophages regulate salt-dependent volume and blood pressure by a vascular endothelial growth factor-C-dependent buffering mechanism. Nat. Med., 15, 2009, s. 545–552.
36. Makinen, T., Adams, R.H., Bailey, J. et al.: PDZ interaction site in ephrinB2 is required for the remodeling of lymphatic vasculature. Genes Dev., 19, 2005, s. 397–410.
37. Mulvenna, P.M., Gillham, L., Regnard, C.F.: Lymphangiosarcomata - experience in a lymphoedema clinic. Palliat. Med., 9, 1995, s. 55–59.
38. Nagy, J.A., Vasile, E., Feng, D. et al.: Vascular permeability factor/vascular endothelial growth factor induces lymphangiogenesis as well as angiogenesis. J. Exp. Med., 196, 2002, s. 1497–1506.
39. Nilsson, I., Bahram, F., Li, X. et al.: VEGF receptor 2/-3 heterodimers detected in situ by proximity ligation on angiogenic sprouts. EMBO J., 29, 2010, s. 1377–1388.
40. Nykänen, A.I., Sandelin, H., Krebs, R. et al.: Targeting lymphatic vessel activation and CCL21 production by vascular endothelial growth factor receptor-3 inhibition has novel immunomodulatory and antiatherosclerotic effects in cardiac allografts. Circulation, 121, 2010, s. 1413–1422.
41. Oliver G.: Lymphatic vasculature development. Nat. Rev. Immunol., 4, 2004, s. 35–45.
42. Petrova, T.V., Makinen, T., Makela, T.P. et al.: Lymphatic endothelial reprogramming of vascular endothelial cells by the Prox-1 homeobox transcription factor. EMBO J., 21, 2002, s. 4593–4599.
43. Pharr, K.M., Debrah, A.Y., Specht, S., Hoerauf, A.: Filariasis and lymphoedema. Parasite Immunol., 31, 2009, s. 664–672.
44. Pratz, K.W., Dingli, D., Smyrk, T.C., Lust, J.A.: Intestinal lymphangiectasia with protein-losing enteropathy in Waldenström macroglobulinemia. Medicine (Baltimore), 86, 2007, s. 210–214.
45. Purhonen, S., Palm, J., Rossi D. et al.: Bone-marrow-derived circulating endothelial precursors do not contribute to vascular endothelium and are not needed for tumor growth. Proc. Natl. Acad. Sci. USA., 312, 2008, s. 6620–6625.
46. Rissanen, T.T., Markkanen, J.E., Gruchala, M. et al.: VEGF-D is the strongest angiogenic and lymphangiogenic effector among VEGFs delivered into skeletal muscle via adenoviruses. Circ. Res., 92, 2003, s. 1098–1106.
47. Ristimäki, A., Narko, K., Enholm, B., Joukov, V., Alitalo, K.: Proinflammatory cytokines regulate expression of the lymphatic endothelial mitogen vascular endothelial growth factor-C. J. Biol. Chem., 273, 1998, s. 8413-8418.
48. Saban, M.R., Memet, S., Jackson, D.G. et al.: Visualization of lymphatic vessels through NF-κB activity. Blood, 104, 2004, s. 3228–3230.
49. Sabin, F.R.: On the origin of lymphatic system from the veins and the development of the lymph hearts and thoracic ducts in the pig. Am. J. Anat., 1, 1902, s. 367–389.
50. Schacht, V., Ramirex, M.I., Hong, Y.K. et al.: T1α/podoplanin deficiency disrupts normal lymphatic vasculature formation and causes lymphedema. EMBO J., 22, 2003, s. 3546–3456.
51. Šteiner, I., Krbal, L., Dominik, J.: Blood vessels and lymphatics in calcific aortic stenosis – in support of its inflammatory pathogenesis. Ces.-slov. Patol., 46, 2010, s. 33–36.
52. Tammela, T., Alitalo, K.: Lymphangiogenesis: molecular mechanisms and future promise. Cell, 140, 2010, s. 460–476.
53. Tammela, T., Saaristo, A., Holopainen, T. et al.: Therapeutic differentiation and maturation of lymphatic vessels after lymph node dissection and transplantation. Nat. Med., 13, 2007, s. 1458-1466.
54. Taveira-DaSilva, A.M., Steagall, W.K., Moss, J.: Lymphangioleiomyomatosis. Cancer Control., 13, 2006, s. 276-285.
55. Tobler, N.E., Detmar, M.: Tumor and lymph node lymphangiogenesis – impact on cancer metastais. J. Leukoc. Biol., 80, 2006, s. 691–696.
56. Upreti, L., Dev, A., Puri, S.K.: Imaging in renal lymphangiectasia: report of two cases and review of literature. Clin. Radiol., 2008, 63, s. 1057–1062.
57. Van Balkom, I.D., Alders, M., Allanson, J. et al.: Lymphedema-lymphangiectasia-mental retardation (Hennekam) syndrome: a review. Am. J. Med. Genet., 112, 2002, s. 412–421.
58. Verma, S.B.: Lymphangiectasias of the skin: victims of confusing nomenclature. Clin. Exp. Dermatol., 34, 2009, s. 566–569.
59. Vignes, S., Bellanger, J.: Primary intestinal lymphangiectasia (Waldmann’s disease). Orphanet J. Rare Dis., 3, 2008, s. 5.
60. Warren, A.G., Brorson, H., Borud, L.J., Slavin, S.A.: Lymphedema: a comprehensive review. Ann. Plast. Surg., 56, 2007, s. 464–472.
61. Wigle, J.T., Oliver, G.: Prox1 function is required for the development of the murine lymphatic system. Cell, 98, 1999, s. 769–778.
62. Wigle, J.T., Harvey, N., Detmar, M. et al.: An essential role for Prox1 in the induction of the lymphatic endothelial cell phenotype. EMBO J., 21, 2002, s. 1505–1513.
63. Wilting, J., Aref, Y., Huang, R. et al.: Dual origin of avian lymphatics. Dev. Biol., 292, 2006, s. 165–173.
64. Xu, X., Lin, H., LV, H., Zhang, M., Zhang, Y.: Adventitial lymphatic vessels – an important role in atherosclerosis. Med. Hypotheses, 69, 2007, s. 1238–1241.
65. Yuan L., Moyon, D., Pardanaud, L. et al.: Abnormal lymphatic development in neuropilin 2 mutant mice. Development, 129, 2002, s. 4797–4806.
Štítky
Patologie Soudní lékařství Toxikologie
Článek ÚvodníkČlánek Primár Cibiček šesťdesiatnikČlánek JAKÁ JE VAŠE DIAGNÓZA?Článek PoděkováníČlánek JAKÁ JE VAŠE DIAGNÓZA?Článek Jak se vám líbí?
Článek vyšel v časopiseČesko-slovenská patologie

2010 Číslo 4-
Všechny články tohoto čísla
- Primár Cibiček šesťdesiatnik
- JAKÁ JE VAŠE DIAGNÓZA?
- Dlhodobá dialyzačná liečba chronickej obličkovej nedostatočnosti sprevádzaná získanou cystickou chorobou obličiek a súčasnými prednádorovými zmenami a mnohopočetnými nádormi ľavej obličky
- Poděkování
- Patolog by se neměl (nechat) tlačit do práce soudního lékaře
- JAKÁ JE VAŠE DIAGNÓZA?
- Jak se vám líbí?
- ČESKO-SLOVENSKÁ PATOLOGIE ROČNÍK 46
- Úvodník
- Systémová sklerozující choroba spojená s imunoglobuliny IgG4 – současné poznatky
- Muir-Torre syndrom – fenotypická varianta Lynchova syndromu
- Úloha molekulárnej biológie pri diagnostike a monitoringu karcinómu prostaty
- Lymfatický systém: novinky v morfologii a patologii
- Česko-slovenská patologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Muir-Torre syndrom – fenotypická varianta Lynchova syndromu
- Lymfatický systém: novinky v morfologii a patologii
- Patolog by se neměl (nechat) tlačit do práce soudního lékaře
- Systémová sklerozující choroba spojená s imunoglobuliny IgG4 – současné poznatky
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: MUDr. Petr Výborný, CSc., FEBO
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání