-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaVliv albuminemie na farmakokinetiku infliximabu u nemocných s idiopatickými střevními záněty
Influence of albuminemia on the pharmacokinetics of infliximab in patients with inflammatory bowel diseases
Purpose of the study:
To analyse infliximab and albumin serum levels in different stages of the biological treatment of patients with inflammatory bowel diseases (IBD).Methods:
We examined the serum trough levels of infliximab and albuminemia in 85 patients with IBD in weeks 2 and 14 of biological treatment with infliximab.Results:
In week 2, infliximab was detected in the sera of 34 patients (40%) and in week 14 in 44 patients (52%). Serum infliximab trough levels were significantly lower in week 2 than in week 14 (p = 0.0138). Likewise, levels of albumin in week 2 were significantly lower than in week 14 (p = 0.0002). In patients with detectable serum infliximab trough levels (concentration ≥ 3 mg/mL), albuminemia was significantly higher than in patients with undetectable serum infliximab levels, regardless of the biological treatment stage. The correlation between serum infliximab levels and albuminemia was significantly positive (r = 0.39, pConclusions:
Levels of both infliximab and albumin rise during biological treatment of IBD. We confirmed a significant positive correlation between albumin and infliximab serum levels, suggesting the theoretical possibility of using serum albumin to predict infliximab pharmacokinetics.Key words:
inflammatory bowel diseases – biological therapy – infliximab – albumin
Autoři: K. Malíčková 1; M. Bortlík 2,3; D. Ďuricová 2
; H. Brodská 1; N. Machková 2; I. Janatková 1; T. Zima 1; M. Lukáš 1,2
Působiště autorů: Ústav klinické biochemie a laboratorní diagnostiky 1. LF UK a VFN Praha 1; Klinické a výzkumné centrum pro střevní záněty, ISCARE Lighthouse a 1. LF UK Praha3Interní klinika 1. LF UK a ÚVN Praha 2
Vyšlo v časopise: Gastroent Hepatol 2011; 65(2): 70-74
Kategorie: IBD: původní práce
Souhrn
Účel studie:
Analýza sérových hladin infliximabu a albuminu v různých fázích léčby pacientů s idiopatickými střevními záněty (IBD).Metody:
Vyšetřili jsme sérové hladiny infliximabu a albuminemii u 85 nemocných s IBD v průběhu biologické léčby infliximabem. Odběry byly provedeny v týdnech 2 a 14 těsně před podáním infuze infliximabu (tzv. trough levels).Výsledky:
V týdnu 2 byl infliximab v séru detekován u 34 (40 %) pacientů, v týdnu 14 u 44 (52 %) pacientů. Hladiny infliximabu v séru byly v týdnu 2 signifikantně nižší než v týdnu 14 (p = 0,0138). Rovněž sérové hladiny albuminu byly na počátku terapie v týdnu 2 signifikantně nižší než v průběhu udržovací léčby v týdnu 14 (p = 0,0002). U nemocných s detekovatelným infliximabem v séru (koncentrace ≥ 3 μg/ml) byla albuminemie signifikantně vyšší než u pacientů s nedetekovatelným sérovým infliximabem, a to bez ohledu na týden biologické léčby. Hladiny sérového infliximabu signifikantně korelovaly s albuminemií (r = 0,39, pZávěry:
V průběhu biologické terapie IBD stoupají hladiny infliximabu a rovněž dochází k nárůstu hodnot albuminemie. Potvrdili jsme významnou pozitivní korelaci sérových hladin infliximabu a albuminu, z čehož vyplývá teoretická možnost využít stanovení sérového albuminu k predikci vývoje farmakokinetiky infliximabu.Klíčová slova:
idiopatické střevní záněty – biologická terapie – infliximab – albuminÚvod
Biologická terapie představuje významný pokrok v léčbě idiopatických střevních zánětů (Inflammatory Bowel Diseases, IBD). Největší a nejdelší zkušenosti jsou s podáváním infliximabu (Remicade®, Schering-Plough & Merck Inc., USA) který byl do klinické praxe zaveden v roce 1998 v USA a v roce 1999 v Evropě [1].
Infliximab je rekombinantní chimérická monoklonální protilátka izotypu IgG1 kappa proti lidskému cytokinu TNF-alfa. Její molekula je tvořena myšími variabilními regiony (25 %) a lidskými konstantními regiony (75 %), které jsou navzájem spojeny disulfidovými můstky [2]. Infliximab se váže na solubilní i transmembránovou formu TNF-alfa. Po této vazbě jsou spouštěné četné protizánětlivé reakce a kaskády, nicméně přesné mechanizmy protizánětlivého účinku infliximabu nejsou dosud zcela známy [3].
Farmakokinetika infliximabu je předmětem zájmu řady recentních studií [4–11]. Je známo, že mezi intravenózně podanou dávkou infliximabu a sérovou koncentrací léčiva existuje lineární závislost [4].
Sérová hladina infliximabu se zdá být významným faktorem ovlivňujícím úspěšnost biologické léčby [5,6]. Interindividuální variabilita sérových koncentrací infliximabu je však vysoká [7,8]. Vedle tvorby protilátek proti infliximabu může být jedním z důvodů fakt, že infliximab jako protein (imunoglobulin G1) podléhá změnám souvisejícím s chronicky aktivním střevním zánětem, při kterém dochází ke zvýšenému katabolizmu bílkovin, k tvorbě proteinů akutní fáze na úkor jiných bílkovin, či ke ztrátám proteinů poškozenou střevní sliznicí nebo při krvácení. Protože největší podíl na všech plazmatických bílkovinách má albumin, lze jej v těchto klinických situacích označit za vhodný ukazatel dysproteinemie.
Vztah mezi hladinou infliximabu a albuminu prokázali v nedávné publikaci Fasanmade et al u nemocných s ulcerózní kolitidou [12]. Podle této práce lze za určitých okolností považovat albuminemii za prediktivní faktor pro vývoj hladin infliximabu.
Cílem předkládané studie byla analýza sérových hladin infliximabu a albuminu v různých fázích léčby pacientů s IBD.
Metody
Provedli jsme observační deskriptivní studii rozložení sérových hladin infliximabu a albuminu u nemocných s IBD léčených biologickou terapií. Metodou prostého náhodného výběru byly do souboru zařazeny vzorky sér 85 pacientů, kteří odpověděli na indukční léčbu infliximabem a jejichž séra byla součástí IBD sérové banky ÚKBLD VFN a 1. LF UK v Praze. Na základě srovnání s podobnými studiemi [13,14] a podle analýzy síly testů provedené pomocí softwaru STATISTICA Power Analysis CZ (Statsoft, USA) lze označit velikost zkoumaného výběru jako přiměřenou záměrům studie.
Léčba pacientů probíhala v letech 2009–2010 v Klinickém a výzkumném centru pro idiopatické střevní záněty ISCARE a 1. LF UK v Praze. Biologická terapie se řídila doporučenými postupy Pracovní skupiny pro idiopatické střevní záněty ČGS JEP [15]. Indukční terapii představovaly 3 infuze infliximabu v dávce 5 mg/kg podané v 0., 2. a 6. týdnu léčby. Po ukončení indukční léčby následovala v případě pozitivní terapeutické odpovědi udržovací léčba s podáváním infuzí léčiva v osmitýdenních intervalech.
Základní demografická data vyšetřených pacientů uvádí tab. 1.
Tab. 1. Charakteristika vyšetřeného souboru. Tab. 1. Characteristics of examined cohort. 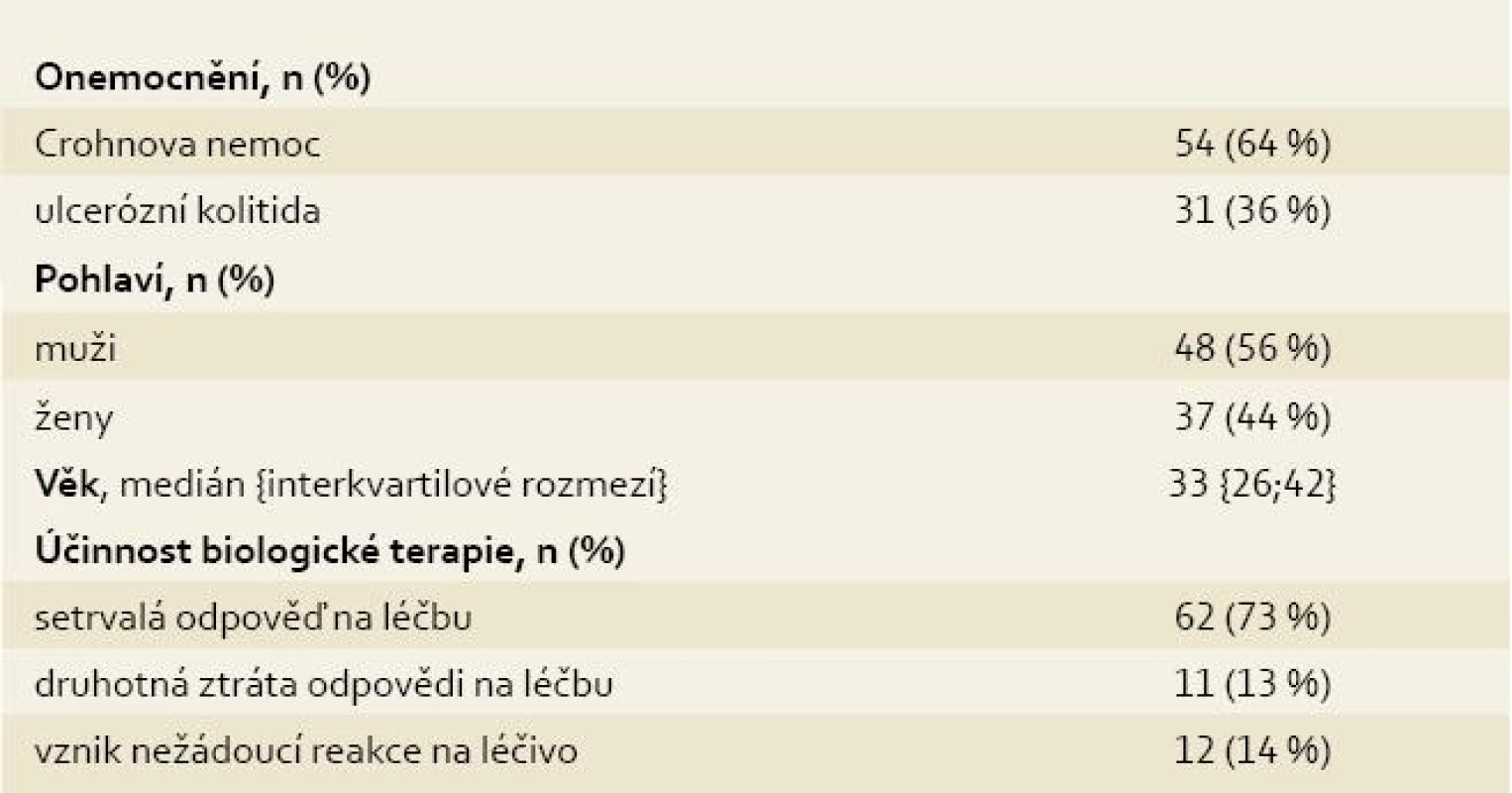
Provedení studie bylo schváleno Etickou komisí 1. LF UK a VFN v Praze dne 5. 11. 2009 (čj. 44/09).
K laboratornímu vyšetření byla použita séra z druhého (W2) a čtrnáctého (W14) týdne biologické léčby. Krevní vzorky byly odebrány těsně před podáním infuze infliximabu (tzv. trough levels). Srážlivá krev byla centrifugována rychlostí 1 000 g po dobu 10 minut, sérum rozpipetováno do alikvot po 100 µl a zamraženo na -80 °C. Před provedením vyšetření byly vzorky séra rozmraženy na ledu a následně vytemperovány na pokojovou teplotu.
Hladina infliximabu v séru byla detekována metodou enzymové imunoanalýzy pomocí validované standardizované soupravy Q-INFLIXI Matriks Biotek ELISA (Exbio, ČR). Koncentrace infliximabu je udávána v μg/ml. Výrobcem je doporučena terapeutická hladina infliximabu ≥ 3 μg/ml.
Koncentrace sérového albuminu byly vyšetřeny fotometricky s bromkrezolovou zelení (Roche Modular, Roche Diagnostics GmbH, Německo). Koncentrace albuminu je vyjádřena v g/l, referenční rozmezí koncentrací je 35–53 g/l.
Statistická analýza dat byla provedena pomocí softwaru STATISTICA CZ 8.0 (Statsoft, USA). Pro popis dat byla použita deskriptivní statistika, přičemž jako míry polohy spojitých proměnných jsou uváděny medián a interkvartilové rozmezí ({IQR}). S ohledem na charakter a rozsah souboru byly k analýzám použity neparametrické testy. Ke zhodnocení rozdílů hodnot mezi soubory byl použit Kruskal-Wallisův test a hladina významnosti p < 0,05. Ke zjištění korelace mezi koncentracemi měřených analytů byl použit Spearmanův korelační koeficient na hladině významnosti p < 0,05.
Výsledky
V týdnu 2 (W2) byl infliximab v séru detekován u 34 (40 %) pacientů, v týdnu 14 (W14) u 44 (52 %) pacientů. Hladiny infliximabu v séru byly u nemocných v týdnu 2 (0 {0; 6,57}) signifikantně nižší než v týdnu 14 (1,9 {0,53; 7,85} (obr. 1). Neprokázali jsme závislost hladin infliximabu na věku, pohlaví ani diagnóze pacientů.
Obr. 1. Sérové hladiny infliximabu ve druhém (W2) a čtrnáctém (W14) týdnu léčby. Fig. 1. Serum trough infliximab levels at weeks 2 and 14 (W2 and W14). 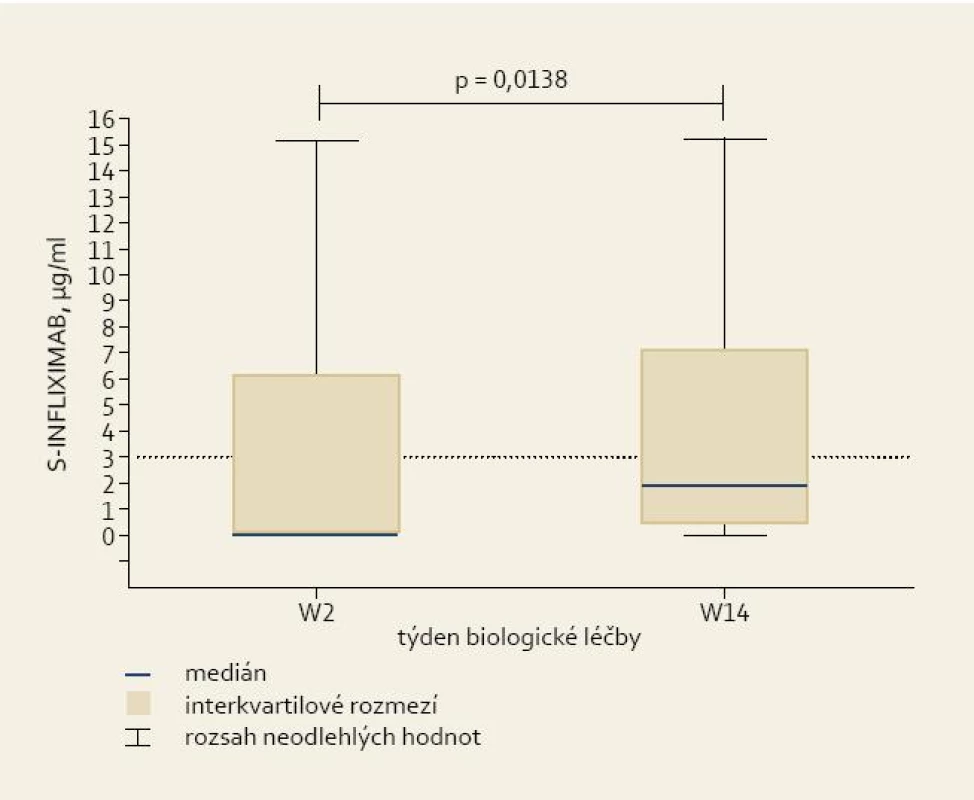
Rovněž sérové hladiny albuminu byly u nemocných na počátku terapie v týdnu 2 (43,7 {39,5; 48,4}) signifikantně nižší než v průběhu udržovací léčby v týdnu 14 (47,5 {43,5; 52,4}) (obr. 2). Po rozdělení dle věku, pohlaví a diagnózy se nemocní v albuminemii signifikantně nelišili.
Obr. 2. Sérové hladiny albuminu ve druhém (W2) a čtrnáctém (W14) týdnu léčby. Fig. 2. Serum albumin levels in weeks 2 and 14 (W2 and W14). 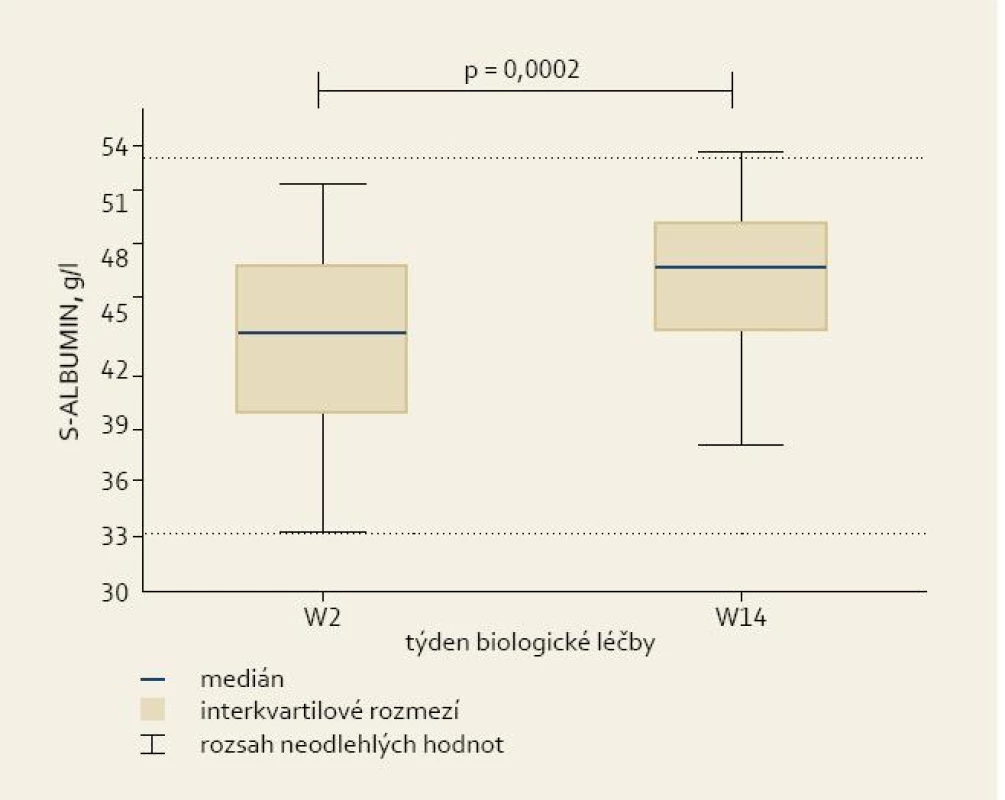
U nemocných s detekovatelným infliximabem v séru (koncentrace ≥ 3 μg/ml) byla albuminemie signifikantně vyšší než u pacientů s nedetekovatelným sérovým infliximabem, a to bez ohledu na týden biologické léčby. Signifikantní pozitivní korelaci sérového infliximabu a albuminu (r = 0,39, p < 0,0001) ukazuje obr. 3.
Obr. 3. Vztah mezi albuminemií a sérovou hladinou infliximabu. Fig. 3. Relationship of albuminemia and infliximab trough levels. 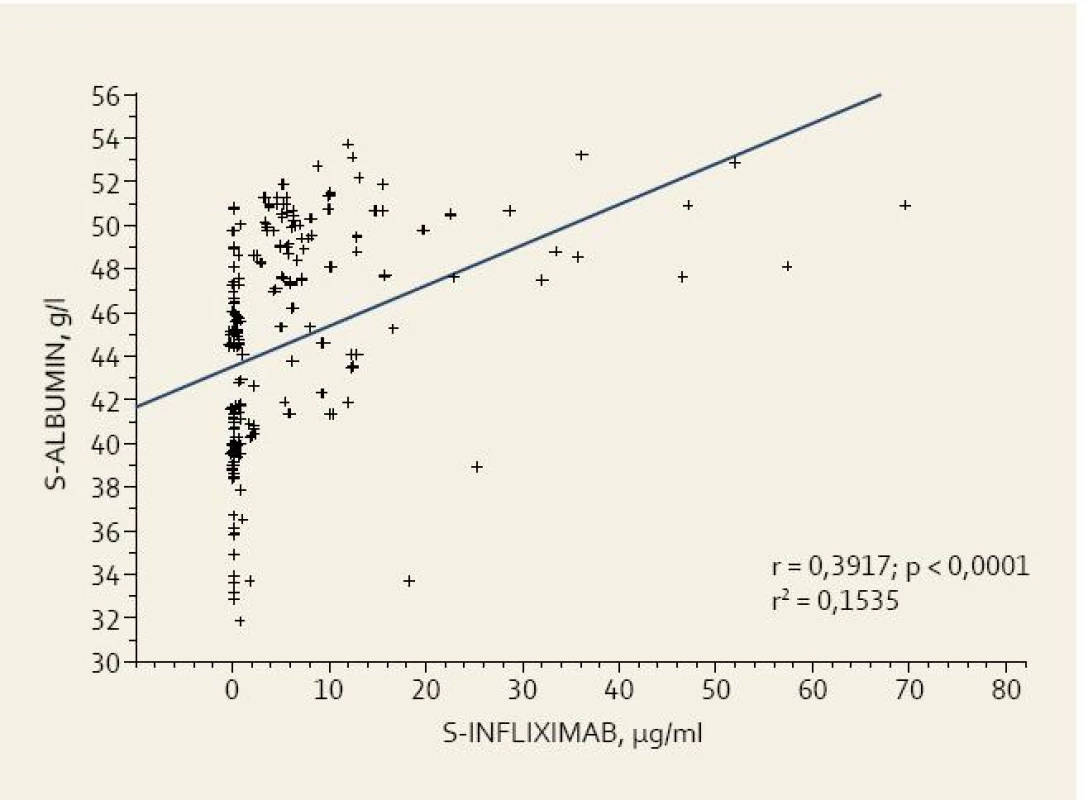
Diskuze a závěry
Naše studie prokázala, že v průběhu biologické terapie IBD stoupají hladiny infliximabu a rovněž dochází k nárůstu hodnot albuminemie. Potvrdili jsme významnou pozitivní korelaci sérových hladin infliximabu a albuminu.
Podle recentních prací se ukazuje, že hladina infliximabu přímo souvisí s efektivitou biologické terapie [16]. U nemocných s detekovatelnou sérovou hladinou infliximabu byly pozorovány častější remise základního onemocnění, dostatečné hladiny léčiva byly spjaty s častějším průkazem endoskopicky ověřeného slizničního zhojení a s významně nižšími hladinami sérového CRP [17]. Dosažení a udržení požadované hladiny infliximabu v séru se proto zdá být důležitým aspektem terapie tímto léčivem.
Biologická léčba IBD je indikována u nemocných s vysokou zánětlivou aktivitou, kteří nereagovali na předchozí terapii, u pacientů s perianálními píštělemi, u kortikodependentních nemocných nebo u pacientů s extraintestinálními projevy IBD [18]. Není proto překvapením, že na počátku indukční fáze léčby (týden 2) byly koncentrace sérového albuminu u nemocných v našem souboru významně nižší než o 12 týdnů později, kdy byla u všech pacientů konstatována primární odpovídavost na indukční léčbu a probíhala udržovací fáze terapie. Nižší albuminemie v aktivní fázi střevního zánětu je dána jak poklesem jeho syntézy při proteinové malnutrici, tak zvýšeným katabolizmem v průběhu zánětu a zvýšenými ztrátami střevem.
Zjistili jsme, že u pacientů s nižší albuminemií jsou i sérové koncentrace infliximabu obvykle nízké. Tuto skutečnost lze vysvětlit jednak rychlejší degradací infliximabu ve fázi aktivního zánětu, jeho distribucí v kompartmentech, anebo ztrátami do třetích prostorů či mimo organizmus. Významnou úlohu by mohla rovněž hrát vysoká exprese scavenger receptorů, které vychytávají proteiny určené k degradaci v buňkách retikuloendotelového systému. Fasanmade et al [12] předpokládají, že ústřední úlohu hrají homeostatické mechanizmy Brambellova neboli neonatálního Fc receptoru (FcRn).
Albumin a imunoglobulin G (IgG) tvoří společně až 90 % plazmatických proteinů. Jejich biologické funkce jsou odlišné, od ostatních krevních bílkovin se však oba tyto proteiny liší svým poměrně dlouhým biologickým poločasem. Teprve od roku 2003 je známo, že společným regulátorem homeostázy albuminu a IgG je FcRn [19]. Tento protein, strukturou podobný MHC molekulám I. třídy, je znám již dlouho jako receptor umožňující transplacentární transport maternálního IgG do cirkulace plodu [20], odtud také pochází jeho pojmenování. Je hojně exprimován na endoteliálních buňkách cév, v dendritických buňkách, hepatocytech a Kupferových buňkách a nachází se především intracelulárně. Při kyselém pH jsou albumin a IgG vázány na histidinové domény FcRn, při normálním a zásaditém pH jsou z této vazby promptně uvolňovány. Anderson et al [21] prokázali, že cirkulující molekuly albuminu a IgG jsou kontinuálně vychytávány a endocytózou transportovány k intracelulárním endozomům s kyselým pH, kde dochází k vazbě na FcRn. Komplex IgG-FcRn-albumin je pak zpracován v lyzozomech a exocytózou projde zpět do cirkulace. Za fyziologického pH jsou IgG i albumin z vazby uvolněny a plní dál své fyziologické funkce v organizmu. V podmínkách katabolizmu zůstává vazba IgG-FcRn-albumin pevná a hladiny cirkulujícího albuminu a IgG jsou nízké [21].
Vliv FcRn na kinetiku infliximabu (a albuminu) v organizmu by se teoreticky mohl uplatňovat např. i při kombinované terapii infliximab + azathioprin. Studie SONIC [22], která zkoumala současné podávání azathioprinu a infliximabu u dosud takto neléčených nemocných s Crohnovou chorobou, ukázala, že nemocní užívající současně azathioprin mají vyšší sérové hladiny infliximabu [23]. Na počátku této kombinované terapie může být stěží vysvětlením imunosupresivní působení azathioprinu, terapeutický efekt tohoto antimetabolitu je totiž patrný až po několika měsících užívání [24]. Metabolitem azathioprinu jsou však kromě 6-merkaptopurinu methylnitroimidazolové sloučeniny, které jsou inhibitory indukovatelné syntázy oxidu dusnatého (iNOS) [25], a ovlivňují tak redoxní (oxidačně-redukční) stav buněk. Ovlivněním intracelulárního pH by azathioprin teoreticky mohl snižovat sílu vazby IgG-FcRn-albumin, a nepřímo tak vést ke zvýšení hladin infliximabu v cirkulaci.
Jedním z praktických důsledků naší studie je teoretická možnost ovlivnit farmakokinetické parametry a potažmo i efektivitu léčby u nemocných s IBD úpravou dávky infliximabu na samém počátku léčby. Pacienti s nízkou vstupní hladinou albuminu by například mohli profitovat z vyšší dávky infliximabu, která by zvýšila pravděpodobnost pozitivní odpovědi a následně i urychlila korekci iniciální hypalbuminemie a acidózy. Je ovšem pochopitelné, že tento teoretický předpoklad bude nutno ověřit v patřičně designované studii, popř. v rutinní klinické praxi.
Závěrem konstatujeme, že monitorace sérových hladin infliximabu je užitečným pomocným laboratorním vyšetřením při biologické léčbě IBD, hodnoty koncentrací infliximabu je však třeba posuzovat individuálně a s ohledem na metabolické aspekty základního onemocnění.
Seznam zkratek
- CRP – C-reaktivní protein
- FcRn – neonatální Fc receptor
- IBD – idiopatický střevní zánět (Inflammatory Bowel Disease)
- iNOS – indukovatelná syntáza oxidu dusnatého
- IQR – interkvartilové rozmezí
- MHC – hlavní histokompatibilní komplex (Major Histocompatibility Complex)
- SONIC – A Randomized, Double-Blind Trial Comparing Infliximab and Infliximab plus Azathioprine to Azathioprine in Patients with Crohn‘s Disease Naive to Immunomodulators and Biologic Therapy
- TNF-alfa – Tumor Necrosis Factor alfa
- W2 – druhý týden biologické léčby
- W14 – čtrnáctý týden biologické léčby
Autoři deklarují, že v souvislosti s předmětem studie nemají žádné komerční zájmy.
The author declares he has no potential conflicts of interest concerning drugs, products, or services used in the study.Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.Práce byla podpořena grantem GAUK 69810/2010.
Děkujeme paní Marcele Jarolímové za pomoc při odběru biologického materiálu a panu Tomáši Vyhnalíkovi za spolupráci při laboratorních analýzách.
MUDr. Karin Malíčková
Klinická imunologie a alergologie – laboratoř, Ústav klinické biochemie a laboratorní diagnostiky VFN a 1. LF UK Praha
Karlovo nám. 32, 121 11 Praha 2
kmali@lf1.cuni.cz
Zdroje
1. Lukáš M. Biologická terapie a idiopatické střevní záněty. Současný stav a výhled do budoucnosti. Čes a Slov Gastroent a Hepatol 2005; 59(5): 217–226.
2. Licastro F, Chiappelli M, Ianni M et al. Tumor necrosis factor-alpha antagonists: differential clinical effects by different biotechnological molecules. Int J Immunopathol Pharmacol 2009; 22(3): 567–572.
3. Shah B, Mayer L. Current status of monoclonal antibody therapy for the treatment of inflammatory bowel disease. Expert Rev Clin Immunol 2010; 6(4): 607–620.
4. Klotz U, Teml A, Schwab M. Clinical pharmacokinetics and use of infliximab. Clin Pharmacokinet 2007; 46(8): 645–660.
5. Svenson M, Geborek P, Saxne T et al. Monitoring patients treated with anti-TNF-alpha biopharmaceuticals: assessing serum infliximab and anti-infliximab antibodies. Rheumatology (Oxford) 2007; 46(12): 1828–1834.
6. Fasanmade AA, Adedokun OJ, Ford J et al. Population pharmacokinetic analysis of infliximab in patients with ulcerative colitis. Eur J Clin Pharmacol 2009; 65(12): 1211–1228.
7. Bendtzen K, Ainsworth M, Steenholdt C et al. Individual medicine in inflammatory bowel disease: monitoring bioavailability, pharmacokinetics and immunogenicity of anti-tumour necrosis factor-alpha antibodies. Scand J Gastroenterol 2009; 44(7): 774–781.
8. Ternant D, Aubourg A, Magdelaine-Beuzelin C et al.Infliximab pharmacokinetics in inflammatory bowel disease patients. Ther Drug Monit 2008; 30(4): 523–529.
9. Lichtenstein GR, Diamond RH, Wagner CL et al. Clinical trial: benefits and risks of immunomodulators and maintenance infliximab for IBD-subgroup analyses across four randomized trials. Aliment Pharmacol Ther 2009; 30(3): 210–226.
10. Tracey D, Klareskog L, Sasso EH at al. Tumor necrosis factor antagonist mechanisms of action: a comprehensive review. Pharmacol Ther 2008; 117(2): 244–279.
11. Magro F, Bastos R, Marques M et al. Infliximab dose intensification by shortening infusion intervals. Inflamm Bowel Dis 2008; 14(3): 432–434.
12. Fasanmade AA, Adedokun OJ, Olson A et al. Serum albumin concentration: a predictive factor of infliximab pharmacokinetics and clinical response in patients with ulcerative colitis. Int J Clin Pharmacol Ther 2010; 48(5): 297–308.
13. Koelewijn CL, Schwartz MP, Samsom M et al. C-reactive protein levels during a relapse of Crohn‘s disease are associated with the clinical course of the disease. World J Gastroenterol 2008; 14(1): 85–89.
14. Sokol H, Seksik P, Carrat F et al. Usefulness of co-treatment with immunomodulators in patients with inflammatory bowel disease treated with scheduled infliximab maintenance therapy. Gut 2010; 59(10): 1363–1368.
15. Lukáš M, Ďuricová D, Bortlík M et al. Doporučení pro podávání biologické terapie u idiopatických střevních zánětů. Čes a Slov Gastroent a Hepatol 2008; 62(5): 285–291.
16. Maser EA, Villela R, Silverberg MS et al. Association of trough serum infliximab to clinical outcome after scheduleded maintenance treatment for Crohns disease. Clin Gastroenterol Hepatol 2006; 4(10): 1248–1254.
17. Schnitzler F, Fidder H, Ferrante M et al. Mucosal healing predicts long-term outcome of maintenance therapy with infliximab in Crohn‘s disease. Inflamm Bowel Dis 2009; 15(9): 1295–1301.
18. Lukáš M, Bortlík M. Je biologická léčba idiopatických střevních zánětů definitivním řešením? Aneb deset poznámek k biologické léčbě. Čes a Slov Gastroent a Hepatol 2007; 61(6): 293–296.
19. Chaudhury C, Mehnaz S, Robinson JM et al. The major histocompatibility complex-related Fc receptor for IgG (FcRn) binds albumin and prolongs its lifespan. J Exp Med 2003; 197(3): 315–322.
20. Kuo TT, Baker K, Yoshida M et al. Neonatal Fc receptor: from immunity to therapeutics. J Clin Immunol 2010; 30(6): 777–789.
21. Anderson CL, Chaudhury C, Kim J et al. Perspective- - FcRn transports albumin: relevance to immunology and medicine. Trends Immunol 2006; 27(7): 343–348.
22. Sandborn WJ, Rutgeerts P, Reinish W et al. One year data from the SONIC study: A Randomized, Double-Blind Trial Comparing Infliximab and Infliximab plus Azathioprine to Azathioprine in Patients with Crohn‘s Disease Naive to Immunomodulators and Biologic Therapy. Gastroenterology 2009; 136 (Suppl. 1): A116.
23. Lukáš M, Bortlík M. Infliximab a/nebo azathioprin u nemocných s Crohnovou chorobou Komentovaný referát ke studii SONIC. Remedia 2009; 19(5): 381–384.
24. Chalupná P, Lukáš M, Šroubková R et al. 6-thioguanine therapy in inflammatory bowel disease. Folia Gastroenterol Hepatol 2004; 2(3): 112–120.
25. Moeslinger T, Friedl R, Spieckermann PG. Inhibition of inducible nitric oxide synthesis by azathioprine in a macrophage cell line. Life Sci 2006; 79(4): 374–381.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek Jubilejní rok
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2011 Číslo 2- Efekt itopridu na motilitu jícnu a funkci dolního jícnového svěrače
- Itoprid v léčbě funkční dyspepsie
- Farmakokinetika a tolerance pantoprazolu v dětském věku
- Vliv podávání prokinetik na riziko syndromu bakteriálního přerůstání u pacientů užívajících inhibitory protonové pumpy
- Strava bohatá na arginin a prolin slibuje urychlení hojení ran u diabetických pacientů
-
Všechny články tohoto čísla
- Rozhovor s prof. dr. Petrem Dítě, DrSc., prezidentem EAGE (European Association for Gastroenterology and Endoscopy) a ředitelem 7. kurzu EAGE pro mladé gastroenterology
- Ostrava live endoscopy 18. 3. 2011
- O čem také psal profesor Mařatka
- Jubilejní rok
- Etiologie a patogeneze ulcerózní kolitidy. Stále více otazníků než jasných odpovědí
- Doporučený postup pro vyšetření tenkého střeva u pacientů s Crohnovou chorobou
- Vliv albuminemie na farmakokinetiku infliximabu u nemocných s idiopatickými střevními záněty
- Biologická léčba nemocné s ulcerózní kolitidou v průběhu gravidity
- 10. výročí založení organizace ECCO a 6. ECCO kongres v Dublinu
- Endoskopická submukózní disekce v léčbě recidivující high-grade neoplazie v rektu
- Odběr bioptického materiálu při endoskopickém vyšetření gastrointestinálního traktu pro vybraná zánětlivá onemocnění
- Kvantitativní test ve screeningu kolorektálního karcinomu – pohled do blízké budoucnosti
- Gastrointestinální manifestace Henoch-Schönleinovy purpury napodobující akutní pankreatitidu
- Ohlédnutí za 15. hradeckými gastroenterologickými a hepatologickými dny
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Odběr bioptického materiálu při endoskopickém vyšetření gastrointestinálního traktu pro vybraná zánětlivá onemocnění
- Doporučený postup pro vyšetření tenkého střeva u pacientů s Crohnovou chorobou
- Kvantitativní test ve screeningu kolorektálního karcinomu – pohled do blízké budoucnosti
- Etiologie a patogeneze ulcerózní kolitidy. Stále více otazníků než jasných odpovědí
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



