-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaKvantitativní test ve screeningu kolorektálního karcinomu – pohled do blízké budoucnosti
Quantitative testing in colorectal cancer screening – a view of the near future
The author offers a systematic account of the new generation of quantitative immunochemical fecal occult blood tests, and outlines a scheme for their integration into the existing Czech program that screens for colorectal cancer. The characteristics of the quantitative immunochemical test (q-FIT) are described, as well as the types of the fecal occult test (FOBT), and their advantages and disadvantages, together with possible ways of the incorporating q-FIT into the colorectal cancer screening program in the Czech Republic. The inclusion of q-FIT in the Czech colorectal cancer screening program, combined with the existing primary screening colonoscopy, could make a contribution to effectiveness.
Key words:
cut off – quantitative immunochemical test – colorectal cancer – screening – fecal occult blood test
Autoři: J. T. Kovářová
Působiště autorů: IV. interní klinika VFN a 1. LF UK Praha
Vyšlo v časopise: Gastroent Hepatol 2011; 65(2): 90-93
Kategorie: Klinická a experimentální gastroenterologie: přehledová práce
Souhrn
Autorka podává přehledné informace o nové generaci kvantitativních testů na okultní krvácení do stolice a naznačuje další postup v jejich začlenění do screeningového programu v ČR. Jsou zmíněny charakteristiky kvantitativního imunochemického testu (q-FIT); jednotlivé skupiny testů na skryté krvácení do stolice (TOKS), jejich výhody a nevýhody; možnosti začlenění q-FIT do screeningu kolorektálního karcinomu v ČR. Začleněním kvantitativního testu na skryté krvácení do stolice do českého screeningového programu kolorektálního karcinomu se náš screeningový program může stát efektivnější spolu s již existující možností primární screeningové koloskopie.
Klíčová slova:
hraniční hodnota – kvantitativní imunochemický test – kolorektální karcinom – screening – test na okultní krvácení do stoliceKolorektální karcinom (KRK) je nejčastější nádor trávicího traktu. V roce 2007 bylo v ČR nově diagnostikováno 7 826 pacientů s tímto karcinomem, z toho 4 638 mužů a 3 188 žen [1]. I když díky deset let probíhajícímu screeningovému programu incidence stagnuje a mortalita mírně klesá, ČR stále zaujímá přední místa světových statistik. U mužů jsme na druhém místě po Maďarsku, u žen na třetím místě po Maďarsku a Slovenské republice [2]. Stále neuspokojivé jsou především výsledky s ohledem na mortalitu a diagnostiku časných stadií tohoto onemocnění. V roce 2007 zemřelo na KRK 4 154 pacientů, z toho 2 418 mužů a 1 736 žen. Tato více než 50% mortalita je způsobena vysokým podílem pacientů diagnostikovaných v pokročilých stadiích III a IV (3 605 pacientů). Tato fakta jsou imperativem pro to, abychom v úsilí o zdokonalování screeningového programu nepolevili a snažili se zachytit ve světě nejnovější trendy a co nejrychleji je zařadili do našeho screeningového programu.
V předchozích letech byla v průběhu národních kongresů ČGS zmíněna příprava nové generace imunochemických testů na skryté krvácení do stolice – testů kvantitativních – pro český screeningový program. V listopadu 2010 byla tato informace završena i časovým nastíněním začlenění tohoto testu do praxe (leden 2012). Jde o velmi důležitý krok na cestě k tomu, aby byl náš screeningový program ještě efektivnější a vedl k významnému poklesu epidemiologických ukazatelů incidence a mortality a také k úspoře ekonomických zdrojů. Na druhu testu na okultní krvácení (TOKS), který se ve screenigu KRK použije, záleží nejen to, zda neoplazii zachytíme včas, ale použitý druh testu ovlivňuje i compliance vyšetřované populace [3]. Roli v tom hraje také alternativní možnost distribuce testu k pacientům.
Vývoj testů na okultní krvácení ve stolici je kontinuální proces a je možné konstatovat, že stoupá citlivost testu, a v důsledku toho je moderními testy zachycen mnohem větší počet prekancerózních lézí a časných stadií KRK. Stejně kontinuální by měl být také proces začleňování nových testů do probíhajícího screeningového programu. Od roku 2009 je možné vykazovat ve screeningu KRK imunochemické testy. V ČR je provádění screeningu KRK upraveno Věstníkem Ministerstva zdravotnictví ČR 02/2009, který uvádí, že je možno využívat guajakové (gTOKS), ale také imunochemické (FIT) testy na okultní krvácení. Od začátku roku 2009 lze tedy využívat jak imunochemické testy kvalitativní, tak i testy kvantitativní.
Kvantitativní testy stanoví číselnou hodnotu množství lidského hemoglobinu ve stolici, což je vlastnost obohacující screeningový program o nový rozměr, a také zvětšující jeho flexibilitu. Tyto testy rovněž přináší možnost přizpůsobení se epidemiologickým výstupům a ekonomické situaci země či kapacitě sítě koloskopických screeningových center. Navíc tyto testy přináší možnost distribuce testu přímo k pacientovi, což by mohlo znamenat významný pokrok a zlepšení compliance screenované populace.
Jednotlivé skupiny TOKS
Guajakové testy (g-TOKS) jsou založeny na pseudoperoxidázové reakci hemoglobinu nejen lidského s guajakovou pryskyřicí. Působením hemu dochází k přenosu kyslíku ze zdroje (peroxid vodíku) na guajakovou pryskyřici. Ta se tímto mění z bezbarvé redukované formy na modrou oxidovanou. Odečtení modrého zbarvení se provádí pouhým okem. Testy zachycují i krev z vyšších oddílů gastrointestinálního traktu (hem je stabilní), naopak hůře zachycují krev z nejaborálnějších úseků (hem uzavřen v erytrocytech). Tuto peroxidázovou reakci mohou kromě hemu způsobit i např. rostlinné peroxidázy nebo větší množství červeného masa. Naopak falešnou negativitu testu způsobí např. větší přísun kyseliny askorbové (několik g/den). Test tedy vyžaduje dietu. Vyhodnocení testu vyškoleným středním zdravotnickým personálem v ambulanci praktických lékařů se provádí s odstupem 72 hodin (snížení vlivu rostlinných peroxidáz). Skladování testu vyžaduje vyloučení interakce se světlem. Senzitivita testu je nízká, proto je test třeba pravidelně opakovat. Výhodou je vysoká specificita. Ta však klesá při použití citlivějšího modifikovaného Heamoccult Sensa. Odběr vzorku dřevěnou špátlí není příliš komfortní. Především s ohledem na nízkou cenu a zaběhnuté užití jsou tyto testy stále v některých zemích pro screening užívány masově. Vliv screeningu pomocí g-TOKS na mortalitu je mírný, ale studiemi jasně dokumentovaný [6–8].
Imunochemické testy (i-TOKS) je velká nehomogenní skupina nekvantitativních testů, které detekují specifické protilátky k lidskému hemoglobinu. Dieta tedy není nutná. Vzhledem k menší stabilitě globinu tyto testy nezachycují krvácení z vyšších oddílů GIT (žaludek). Odběr stolice je většinou jednodušší, hygieničtější. Testy mají zhruba 2× vyšší citlivost oproti g-TOKS. Na trhu je velké množství různých imunochemických testů, jejich parametry se bohužel značně liší [9], mnohé používané testy mají naprostou absenci studií dokladujících jejich efektivitu. I přesto řada ambulantních lékařů přešla na jejich provádění z důvodu jasně vyšší citlivosti a komfortnějšího provádění. Od roku 2009 byly testy imunochemické i oficiálně začleněny do screeningového programu. Pozitivita testu při neznalosti číselné hodnoty nenapovídá nic o možné míře rizika plynoucí z následného nedovyšetření pacienta. Přitom stále existuje nezanedbatelné procento pacientů s pozitivním TOKS, kteří odmítají kolonoskopické vyšetření. Znalost číselné hodnoty testu při vyšších hodnotách může být dalším pádným argumentem v rukou lékaře v přesvědčovacím procesu váhavého pacienta.
Kvantitativní imunochemické testy (q-FIT) vznikly zdokonalením a vývojem z testů nekvantitativních. Jejich výhody jsou doplněny o parametr kvantity. Tyto testy umožňují ve screeningu nastavením hraniční hodnoty získat optimální citlivost a specificitu [10,11]. Z důvodu menší stability globinu oproti hemu je nutno testy uchovávat v chladničce a zpracovat do 7 dnů [12,13]. q-FIT testy zachytí více pokročilých polypů a časných stadií I a II kolorektálního karcinomu [14]. Sofistikovanost testu zvyšuje účast populace ve screeningu oproti g-TOKS o 13 % [3].
Charakteristika kvantitativního imunochemického testu na skryté krvácení do stolice (q-FIT)
Práce izraelských autorů [4] představila q-FIT OC-Sensor® (Eiken, Japonsko) ve studii na symptomatické (nescreeningové) populaci 1 000 kolonoskopovaných pacientů. Při počtu 3 kvantitativních testů a hraniční hodnotě 100 ng/ml byla senzitivita pro záchyt KRK 94,1 % při specificitě 87,5 %. Záchyt klinicky signifikantní neoplazie (pokročilé adenomy + karcinomy) dosahoval senzitivity 67 % a specificity 91,4 % [4].
Informaci, jak nastavit q-FIT v české populaci, přinesla studie provedená v předchozích dvou letech ve spolupráci IV. interní kliniky VFN, II. interní kliniky FTN a Ústavu klinické biochemie a laboratorní diagnostiky VFN a 1. LF UK Praha.
Cílem studie bylo ukázat, že uspokojivé parametry senzitivity a specificity lze dosáhnout při použití pouze jednoho testu snížením hraniční hodnoty (cut off) detekovaného množství krve ve stolici. Na souboru 815 kolonoskopovaných pacientů byla prokázána senzitivita 73 % a specificita 90,1 % při provedení jednoho q-FIT a hraniční hodnotě 75 ng/ml pro skupinu pokročilých polypů a karcinomů, tedy výsledky přinejmenším srovnatelné s výsledky Leviho studie [4].
Testovací zkumavka q-FIT testu OC-Sensor sestává z víčka a tuby. Součástí víčka je odběrová tyčinka s drážkami na konci (obr. 1). Po odběru přiměřeného množství stolice je po zasunutí tyčinky s víčkem do tuby protlačeno při průchodu membránou mezi drážkami tyčinky přesně 10 mg stolice do 2 ml stabilizujícího pufrovacího roztoku. Po zaklapnutí víčka obsah zkumavky nevytéká ani nezapáchá. Zkumavka se uchovává v chladničce po odběru doma i následně v biochemické laboratoři. Analýza testu by měla proběhnout do 7 dnů.
Obr. 1. Odběrový systém OC -Sensor: A – zasunuté víčko s odběrovou tyčinkou, nad ní septum definující množství stolice, nad ním filtrační vložka a nahoře hliníkový uzávěr pro perforaci nástřikovou jehlou. B – tyčinka pro odběr stolice s drážkami. C – identifikační čárový kód vzorku. Fig. 1. Take-off system OC-Sensor: A – inserted cap of the test tube with the take-off stick, septum defining amount of the stool above it, filter plug and aluminium cover for the perforation by a needle. B – take-off stool stick. C – barcode of the sample. 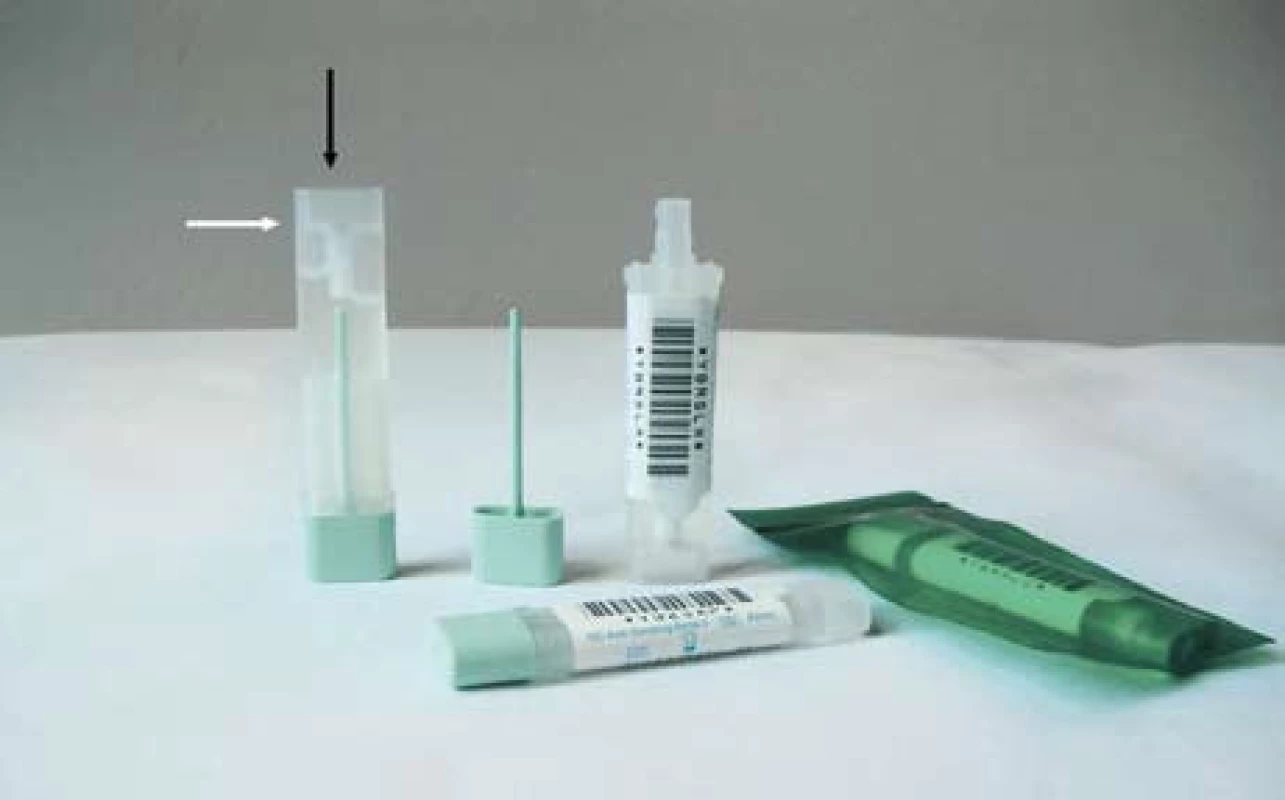
Zkumavky se vkládají do automatického analyzátoru (obr. 2). Jde o kombinaci kvantitativního odběru stolice s kvantitativní analýzou. Ta je prováděna latex aglutinační imunoturbidimetrickou reakcí s protilátkou k A0 lidskému hemoglobinu. Citlivost detekce je 20–2 000 ng/ml [5]. Kapacita analyzátorů u nás používaných je 80 vzorků za hodinu. Výsledek testu je číselná hodnota množství lidského hemoglobinu ve stolici. Při optimální hraniční hodnotě (75 ng/ml) test dává optimální proporci mezi senzitivitou (73 %) a specificitou (90 %). Při této a vyšší hodnotě je pacient odeslán ke kolonoskopickému vyšetření. Při normálním kolonoskopickém nálezu je 95% rozsah průměrných hodnot (95% CI) 24–45 ng/ml, u pokročilých adenomů 315–654 ng/ml, u karcinomů 697–1 477 ng/ml. S poklesem hraniční hodnoty stoupá citlivost a klesá specificita testu, je tedy zachyceno více lézí za cenu většího počtu kolonoskopií. V extrémním případě při hraničí hodnotě 0 ng/ml by byl každý pacient kolonoskopován, což je situace totožná s primárním kolonoskopickým screeningem. V současné době se cena tohoto testu u nás pohybuje kolem 35 korun.
Obr. 2. Analyzátor OC -Sensor. Fig. 2. OC-Sensor analyzer. 
Model začlenění q-FIT do screeningového programu v ČR
Při začlenění kvantitativního testu do screeningu kolorektálního karcinomu vyvstává nezbytnost začlenění klinických biochemiků do již fungující struktury screeningových center a koordinátorů, nezbytnost dobře fungující spolupráce praktických lékařů a gynekologů na straně jedné a biochemických laboratoří na straně druhé.
Prvním krokem je vytvoření proporcionální sítě analyzátorů na území ČR s využitím nezanedbatelného počtu již instalovaných analyzátorů (VFN Praha, ÚVN Praha, Masarykův onkologický ústav Brno, Fakultní Thomayerova nemocnice Praha, Nemocnice na Homolce, ADC Sanatorium Praha, FN Ostrava, FN Plzeň, nemocnice Karlovy Vary, nemocnice Písek, P+P klinika Kladno). Druhým krokem je rozšíření informací formou seminářů a publikací cílených na praktické lékaře a gynekology. Tento proces byl zhájen a probíhá kontinuálně. Probíhá jak formou prezentací na kongresech, tak formou seminářů v místech, kde jsou analyzátory umisťovány. Důraz je třeba klást na správné skladování testů v chladničce, na zajištění včasné dodávky testu do laboratoře a na včasné vyhodnocení testu laboratoří. Výsledek testu musí být lékařům primární péče poskytnut číselným vyjádřením hodnoty prokázaného lidského hemoglobinu ve stolici. Třetím neméně důležitým krokem je zakládání dat do onkologického registru kolorektálního karcinomu, kdy je třeba do systému poskytnout výslednou hodnotu testu. Domnívám se, že toto zadávání by optimálně mělo být povinností biochemické laboratoře a být definováno jako součást výkonu hrazeného pojišťovnou. To by v budoucnosti umožnilo přesné vyhodnocení a dle potřeby přenastavení hraniční hodnoty dle výsledků screeningového programu.
Kvantitativní test má však i další velkou výhodu – při nefunkčnosti distribuce testu lékaři primární péče lze rozeslat test poštou s patřičným poučením a pacient test dopraví buď osobně, nebo poštou do nejbližší biochemické laboratoře vybavené analyzátorem. K lékaři primární péče přijde až pacient s pozitivním výsledkem testu, nebo může zamířit rovnou do centra pro screening kolorektálního karcinomu. Tato možnost je velkou výzvou pro všechny zúčastněné strany: nováčky ve screeningovém programu – pro klinické biochemiky, pro onkology, s jejichž pomocí jsou v ČR dlouhodobě využívána data Národního onkologického registru. Je výzvou pro gynekology, kteří zvládají prevenci gynekologických nádorů s poměrně dobrou compliance populace kolem 50 % i pro praktické lékaře s compliance populace dosahující zatím zhruba 18 %. Nakonec je výzvou i pro gastroenterology, kteří mohou v tomto případě skutečně očekávat nápor práce.
Nikdo nepochybuje o nezbytnosti pečlivého provádění očkovacího kalendáře u dětí cestou pediatrických ambulancí. Laxnost v přístupu k prevenci kolorektálního karcinomu jak ze strany lékařů, tak ze strany pojišťoven je v tomto ohledu až zarážející. Přitom nečinnost v této oblasti znamená velké nejen zdravotní, ale i finanční ztráty. Stadia zachytitelná včasně a léčitelná prostou polypektomií se přesouvají do stadií vyžadujících operační výkony a nákladnou onkologickou léčbu a ztrátu ekonomické produktivity pacienta. Pozitivní motivace ze strany některých pojišťoven, které se v minulých letech snažily mírně finančně zvýhodnit lékaře provádějící v dostatečné míře screening, nebyla účinná. Což tedy zkusit motivaci negativní? Ani špičkový screeningový program, kterým se náš program může stát v okamžiku kombinace kvantitativního testu s primární screeningovou kolonoskopií, nemůže přinášet uspokojivý výsledek, pokud nebude prováděn masově.
Závěr
Český screeningový program kolorektálního karcinomu dostává v posledních letech začleněním velmi kvalitních vyšetřovacích modalit, tj. primární screeningové kolonoskopie a kvantitativního q-FIT, podobu vysoce efektivního screeningového programu. Velkou výhodou by mohla být dobře organizovaná síť primární péče, kvalitní osvěta a propagace spolu s onkologickými registry umožňujícími vyhodnocení dat. V této situaci úspěch celého projektu závisí na jediném faktoru – masové účasti populace.
Autorka deklaruje, že v souvislosti s předmětem studie nemá žádné komerční zájmy.
The author declares she has no potential conflicts of interest concerning drugs, products, or services used in the study.Redakční rada potvrzuje, že rukopis práce splnil ICMJE kritéria pro publikace zasílané do biomedicínských časopisů.
The Editorial Board declares that the manuscript met the ICMJE „uniform requirements“ for biomedical papers.Příprava článku byla podpořena VZ MSM 0021620820.
MUDr. Jaroslava Tereza Kovářová
IV. interní klinika VFN a 1. LF UK
U nemocnice 2, 128 02 Praha 2
jaroslava.kovarova@vfn.cz
Zdroje
1. Dušek L, Abrahámová J, Mužík J et al. Populační odhady počtu nemocných s kolorektálním karcinomem v ČR – jeden z nástrojů hodnocení včasné diagnostiky časných stadií a rekurence onemocnění. Farmakoterapie – speciální příloha Kolorektální karcinom 2009; 11–20.
2. Zavoral M, Suchanek S, Zavada F et al. Colorectal cancer screening in Europe. World J Gastroenterol 2009; 15(47): 5907–5915.
3. Rossum LG, Rijn AF, Laheij RJ et al. Random comparison of guaiac and immunochemical fecal occult blood tests for colorectal cancer in a screening population. Gastroenterology 2008; 135(1): 82–90.
4. Levi Z, Rozen P, Hazazi R et al. A Quantitative immunochemical fial occult blood test for colorectal neoplasia. Ann Intern Med 2007; 146(4): 244–255.
5. Dubská L, Nechvátal J. Kvantitativní stanovení hemoglobinu ve stolici, Laboratorní technologie. http://www.stapro.cz/bullfons/32009/labo1.pdf
6. Mandel JS, Bond JH, Church TR et al. Reducing mortality from colorectal cancer by screening for fecal occult blood. N Engl J Med 1993; 329(9): 672.
7. Mandel JS, Church TR, Bond JH et al. The effect of fecal occult-blood screening on the incidence of colorectal cancer. N Engl J Med 2000; 343(22): 1603–1607.
8. Hardcastle JD, Chamberlain JO, Robinson MH et al. Randomised controlled trial of faecal-occult-blood screening for colorectal cancer. Lancet 1996; 348(9040): 1472–1477.
9. Hundt S, Haug U, Brenner H. Comparative evaluation of immunochemical fecal occult blood tests for colorectal adenoma detection. Ann Intern Med 2009; 150(3): 162–169.
10. Vilkin A, Rozen P, Levi Z et al. Performance characteristic and evaluation of an automated-developed and quantitative, immunochemical, fecal occult blood screening test. Am J Gastroenterol 2005; 100(11): 2519–2525.
11. Grazzini G, Visioli CB, Zorzi M et al. Immunochemical faecal occult blood test: number of samples and positivity cutoff. What is the best strategy for colorectal cancer screening? Br J Cancer 2009; 100(2): 259–265.
12. Rossum LG, Rijn AF, Oijen MG et al. False negative fecal occult blood test due to delayed sample return in colorectal cancer screening. Int J Cancer 2009; 125(4): 746–750.
13. Grazzini G, Ventura L, Zappa MS et al. Influence of seasonal variations in ambient temperatures on performance of immunochemical faecal occult blood test for colorectal cancer screening: observational study from the Florence distrikt. Gut 2010; 59(11): 1511–1515.
14. Levi Z, Hazazi R, Rozen P et al. A quantitative immunochemical faecal occult blood test is more efficient for detecting significant colorectal neoplasia than a sensitive guaiac test. Aliment Pharmacol Ther 2006; 23(9): 1359–1364.
Štítky
Dětská gastroenterologie Gastroenterologie a hepatologie Chirurgie všeobecná
Článek Jubilejní rok
Článek vyšel v časopiseGastroenterologie a hepatologie
Nejčtenější tento týden
2011 Číslo 2- Efekt itopridu na motilitu jícnu a funkci dolního jícnového svěrače
- Itoprid v léčbě funkční dyspepsie
- Farmakokinetika a tolerance pantoprazolu v dětském věku
- Vliv podávání prokinetik na riziko syndromu bakteriálního přerůstání u pacientů užívajících inhibitory protonové pumpy
- Strava bohatá na arginin a prolin slibuje urychlení hojení ran u diabetických pacientů
-
Všechny články tohoto čísla
- Rozhovor s prof. dr. Petrem Dítě, DrSc., prezidentem EAGE (European Association for Gastroenterology and Endoscopy) a ředitelem 7. kurzu EAGE pro mladé gastroenterology
- Ostrava live endoscopy 18. 3. 2011
- O čem také psal profesor Mařatka
- Jubilejní rok
- Etiologie a patogeneze ulcerózní kolitidy. Stále více otazníků než jasných odpovědí
- Doporučený postup pro vyšetření tenkého střeva u pacientů s Crohnovou chorobou
- Vliv albuminemie na farmakokinetiku infliximabu u nemocných s idiopatickými střevními záněty
- Biologická léčba nemocné s ulcerózní kolitidou v průběhu gravidity
- 10. výročí založení organizace ECCO a 6. ECCO kongres v Dublinu
- Endoskopická submukózní disekce v léčbě recidivující high-grade neoplazie v rektu
- Odběr bioptického materiálu při endoskopickém vyšetření gastrointestinálního traktu pro vybraná zánětlivá onemocnění
- Kvantitativní test ve screeningu kolorektálního karcinomu – pohled do blízké budoucnosti
- Gastrointestinální manifestace Henoch-Schönleinovy purpury napodobující akutní pankreatitidu
- Ohlédnutí za 15. hradeckými gastroenterologickými a hepatologickými dny
- Gastroenterologie a hepatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Odběr bioptického materiálu při endoskopickém vyšetření gastrointestinálního traktu pro vybraná zánětlivá onemocnění
- Doporučený postup pro vyšetření tenkého střeva u pacientů s Crohnovou chorobou
- Kvantitativní test ve screeningu kolorektálního karcinomu – pohled do blízké budoucnosti
- Etiologie a patogeneze ulcerózní kolitidy. Stále více otazníků než jasných odpovědí
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



