-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaCo bychom měli vědět o diagnostických testech
What we should know about diagnostic tests
Diagnostic tests play a very important role in rheumatology. Despite the fact that we use them on daily basis, we often do not appreciate the influence of basic statistical principles on their interpretation. Rheumatic diseases are rare, therefore in order to avoid falsely positive results we have to order diagnostic tests only in patients with strong suspicion of a given disease. Understanding of diagnostic test characteristics and the basics of bayesian approach alows us to combine diagnostic tests in an effective manner in order to minimize costs and risks associated with ruling-in or ruling-out a disease.
Key words:
Diagnostic test, uncertainity, sensitivity, specificity, predictive value
Autoři: H. Mann
Působiště autorů: Revmatologický ústav, Praha
Vyšlo v časopise: Čes. Revmatol., 21, 2013, No. 2, p. 98-104.
Kategorie: Komentáře
Medicína je věda o nejistotě a umění pravděpodobnosti.
Sir William OslerSouhrn
Diagnostické testy hrají v revmatologii velmi důležitou roli. Přestože je denně používáme, často si neuvědomujeme vliv statistických principů na interpretaci jejich výsledků. Revmatická onemocnění jsou vzácná, proto abychom předešli falešně pozitivním výsledkům, musíme diagnostické testy ordinovat s rozmyslem pouze u pacientů se skutečně důvodným podezřením na danou chorobu. Pochopení významu pojmů charakterizujících diagnostické testy a základů bayesovského přístupu nám umožňuje poskládat diagnostické kroky účelně, aby náklady a rizika nutná k potvrzení nebo k vyloučení diagnózy byla co nejnižší.
Klíčová slova:
Diagnostický test, nejistota, senzitivita, specificita, prediktivní hodnotaÚvod
Určení správné diagnózy je základním předpokladem úspěšné léčby revmatických onemocnění. V praxi jsme si ale v okamžiku zahájení léčby diagnózou zcela jisti jen výjimečně. V drtivé většině případů se musíme smířit s větší nebo menší mírou nejistoty. Jak vysokou míru diagnostické nejistoty jsme ochotni tolerovat, závisí na řadě okolností – na charakteru a závažnosti zvažovaného onemocnění, na dostupnosti diagnostických metod a v neposlední řadě na účinnosti, bezpečnosti a ceně léčby. Svou roli hrají i osobní preference lékaře a pacienta.
Nasadit krátkodobou léčbu nesteroidními antirevmatiky, která pomáhají na bolesti způsobené řadou různých procesů a mají relativně příznivý bezpečnostní profil, se příliš nezdráháme, i když přesnou diagnózu ještě neznáme. Na druhou stranu indikace potenciálně nebezpečné léčby cyklofosfamidem musí být podložena skutečně dobrými důvody, a proto v takových případech obvykle před zahájením léčby vyžadujeme bioptický průkaz přítomnosti a aktivity onemocnění.
Vztah mezi mírou dosažené diagnostické jistoty a náklady, respektive riziky, spojenými s jejím dosažením ilustruje s jistou nadsázkou graf na obrázku 1. Obecně platí, že vyšší jistota je vykoupena vyšší cenou a rizikem. Navíc je třeba zvažovat nejen náklady a rizika, která jsou spojena s provedením daného testu, ale i nepřímé náklady a rizika, která mohou vzniknout v důsledku tohoto vyšetření. Například kontaminace vzorku odeslaného na kultivační vyšetření vede k prodloužení hospitalizace a k neindikované aplikaci antibiotik, která mohou způsobit další závažné komplikace. Čím více vyšetření provádíme, tím vyšší je riziko falešně pozitivních výsledků. Úkolem lékaře je proto v rámci diagnostické strategie vybrat taková vyšetření, která skutečně pomáhají při klinickém rozhodování a vyvarovat se testování pro "klid duše". Pokud je zvažované onemocnění na základě provedených vyšetření pravděpodobné natolik, že považujeme léčbu za indikovanou (poměr předpokládaného prospěchu léčby k možným rizikům a nákladům je jednoznačně na straně zahájení léčby), pak jsou další vyšetření již zbytečná.
Obr. 1. Vztah mezi dosaženou mírou jistoty a vynaloženými náklady (riziky). 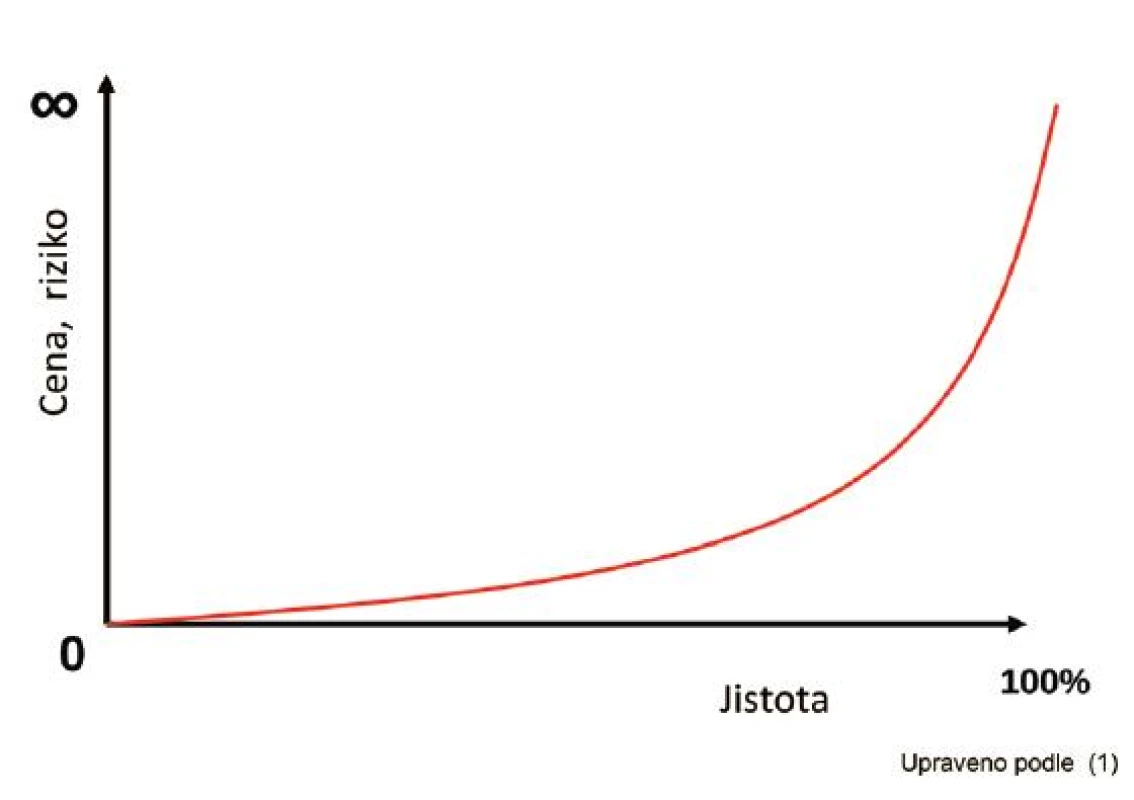
Diagnostické testy
Většina revmatologických onemocnění jsou klinické syndromy, pro které není k dispozici žádný specifický diagnostický test. Jak dále uvidíme, situaci komplikuje i skutečnost, že v řadě případů se jedná o vzácné choroby. Diagnostické testy samy o sobě neurčují, jakou léčebnou strategii máme u pacienta zvolit, jejich výsledky pouze zvyšují nebo snižují pravděpodobnost daného onemocnění u konkrétního pacienta. Žádný test není dokonalý a proto je třeba výsledky vždy interpretovat ve světle ostatních informací o nemocném. Indikujeme pouze taková vyšetření, u kterých můžeme předpokládat, že budou mít vliv na léčbu. Úzkostní nemocní nebo pacienti se somatizačními poruchami často nutí lékaře provádět další a další vyšetření, takové nemocné však negativní výsledek testu neuklidní a falešně pozitivní výsledek povede jen k dalšímu roztáčení bludného kruhu nikdy nekončícího vyšetřování. Pokud jsou k dispozici dva testy, které mají potenciál poskytnout stejnou informaci, pak neprovádíme oba, ale vybereme levnější, jednodušší nebo méně invazivní možnost. Když už určité vyšetření provedeme, pak bychom se neměli spokojit jen se závěrem pozitivní/negativní, ale měli bychom se snažit využít všechny výsledky, které nám poskytuje (význam může mít např. numerická hodnota titru autoprotilátek, zjištění přítomnosti cytoplazmatické imunofluorescence při vyšetření antinukleárních protilátek nebo popis vedlejších nálezů při CT vyšetření hrudníku indikovaného k vyloučení intersticiálního plicního procesu). V neposlední řadě nesmíme zapomínat, že i výsledky vysoce nákladných a sofistikovaných vyšetření podléhají stejným omezením a pravidlům jako informace získané při anamnéze a fyzikálním vyšetření.
V praxi nesmíme samozřejmě opomíjet ani riziko plynoucí z falešně negativních výsledků. Zdrojem omylů a nejistot v klinické praxi může být také chyba měření, špatně provedený odběr nebo záměna vzorků. Pokud se výsledek provedeného vyšetření zásadně rozchází s předchozími hodnotami, nebo když neodpovídá klinickému nálezu, měli bychom zvážit zopakování testu nebo doplnit vyšetření jinou metodou.
Referenční rozmezí
Klinické otázky mívají binární charakter, zajímá nás, zda pacient trpí danou nemocí nebo ne. Výsledky laboratorních testů jsou ovšem obvykle kontinuum, proto jsou doplněny referenčním rozmezím normálních hodnot, které jsou specifické pro danou metodu a konkrétní laboratoř. Referenční rozmezí je zpravidla rozsah změřených hodnot u 95 % osob z referenčního vzorku zdravé populace (obr. 2). Z této definice vyplývá, že při provedení jednoho vyšetření bude mít 5 % zdravých osob výsledek mimo referenční rozmezí. Při provedení 20 na sobě nezávislých testů je u zdravého člověka pravděpodobnost, že všechny výsledky budou v „normě“ pouze 36 % (0,9520 = 0,36). Referenční rozmezí nám navíc neříká nic o distribuci hodnot u nemocných pacientů. Hodnota mimo referenční rozmezí tedy automaticky neznamená, že se jedná o nemocného a, protože v praxi se distribuce hodnot mezi zdravou a nemocnou populací většinou částečně překrývá, někteří nemocní mohou mít výsledek v „normě“.
Obr. 2. Referenční rozmezí laboratorních hodnot. 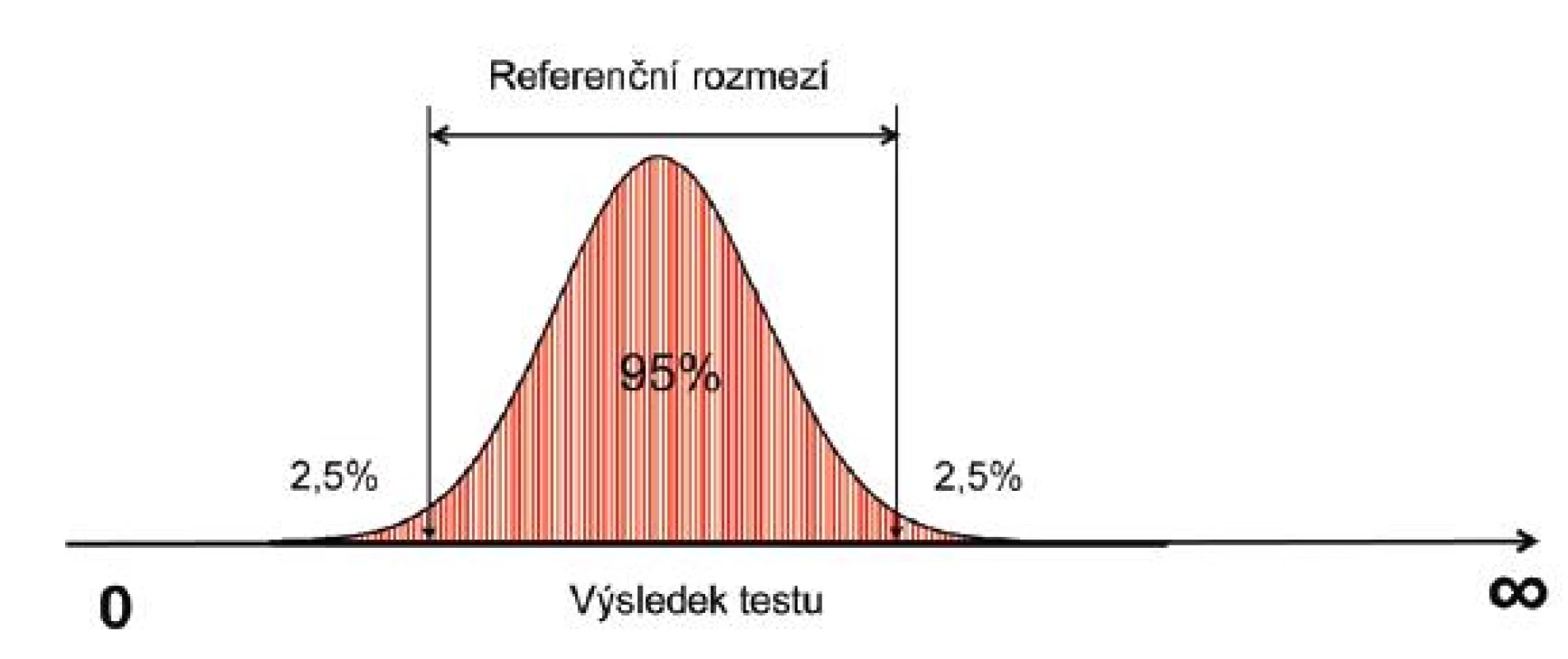
Pro diagnostické účely je nutné testy s kontinuálním rozsahem hodnot doplnit arbitrárně určenou prahovou hodnotou, nad kterou je test považován za pozitivní. Posunutím této hodnoty můžeme podle potřeby měnit parametry testu (obr. 3).
Obr. 3. Prahová hodnota diagnostického testu Hodnoty, které nabývají výsledky testu u zdravých a nemocných osob se u tohoto testu částečně překrývají. Pokud zvolíme jako prahovou hodnotu A, pak dosáhneme 100% senzitivity (všichni nemocní budou mít pozitivní výsledek) za cenu nižší specificity (část zdravých osob bude mít také pozitivní výsledek). Pokud zvolíme za prahovou hodnotu B, pak bude senzitivita nižší, ale specificita stoupne na 100%. 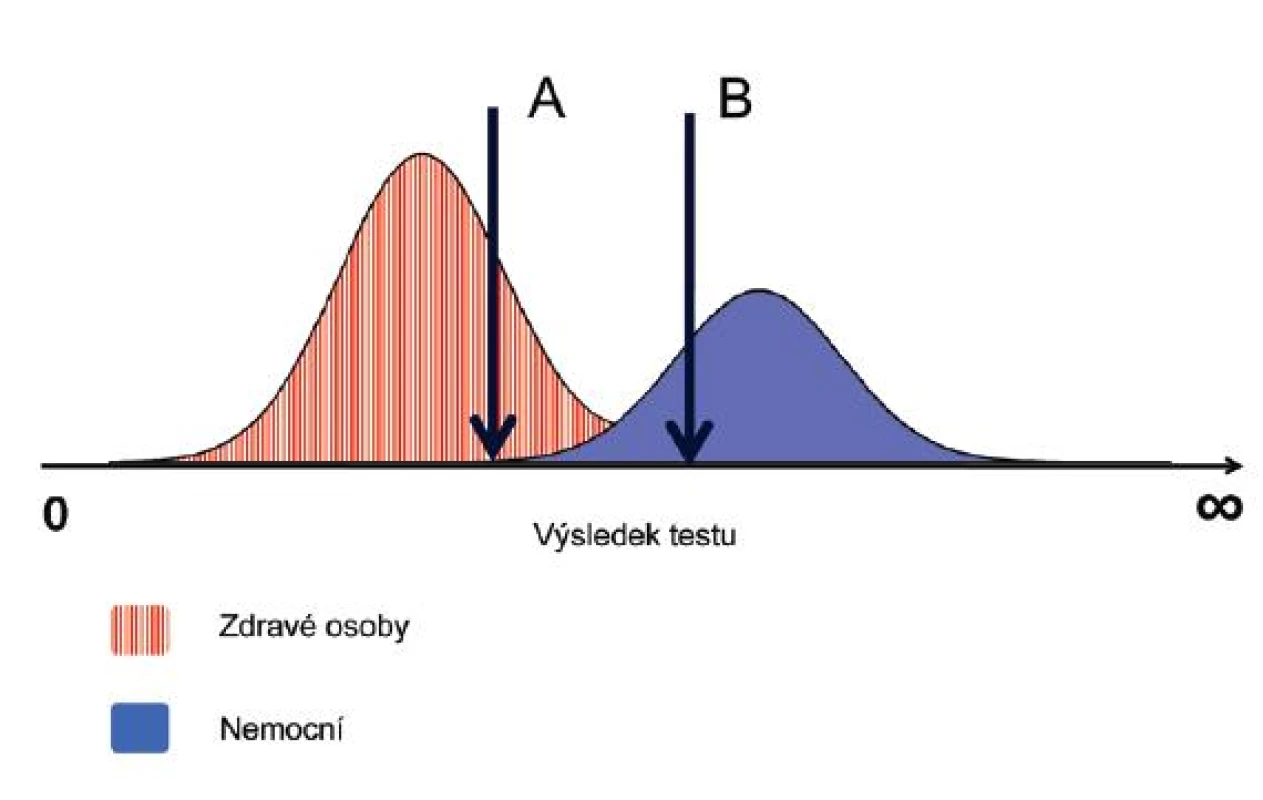
Senzitivita a specificita
Schopnost testu diagnostikovat určité onemocnění shrnují parametry nazývané jako senzitivita a specificita. Senzitivita označuje percentuální podíl nemocných, u nichž je výsledek testu pozitivní (správně pozitivní výsledek). Například 75 % nemocných s revmatoidní artritidou má pozitivní latex fixační test, senzitivita vyšetření pro revmatoidní artritidu je tedy 75 %. Specificita je podíl zdravých osob, které mají negativní výsledek testu (správně negativní výsledek). Latex fixační test je negativní u 91 % osob, které netrpí revmatoidní artritidou. Specificita tohoto vyšetření je 91 %. Pro výpočet senzitivity a specificity se užívá čtyřpolní kontingenční tabulka (tab. 1). O senzitivitě a specificitě testu má smysl uvažovat jen v souvislosti s určitou chorobou. Vyšetření C reaktivního proteinu (CRP) samo o sobě žádnou senzitivitu ani specificitu nemá. Můžeme se ale například pokusit na vybraném vzorku nemocných a zdravých kontrol zjistit senzitivitu a specificitu hodnoty CRP vyšší než 5 mg/l pro diagnostiku časté revmatoidní artritidy (v této indikaci se samozřejmě nejedná o příliš dobrý test).
Tab. 1. Základní charakteristiky diagnostických testů. 
LR - věrohodnostní poměr (angl. likelihood ratio) Informace o senzitivitě a specificitě jednotlivých testů lze poměrně snadno získat ať už z laboratoře, která test provádí, od výrobce testu nebo z literatury. Problémem je, že tyto údaje platí, jen pokud je test použit za obdobných podmínek a u populace srovnatelné s tou, v jaké byly parametry testu původně měřeny. Senzitivita a specificita diagnostického testu se může například lišit podle toho, zda vyšetřujeme nemocné s počátečním stadiem choroby v ambulanci obvodního lékaře nebo komplikované pacienty na terciárním revmatologickém pracovišti. V praxi proto údaje o senzitivitě a specificitě můžeme použít jen jako rámcový odhad, protože většinou nemáme k dispozici přesné charakteristiky testu při použití u konkrétní populace.
Již jsme si ukázali, že specificita a senzitivita vyšetření závisí na zvolené prahové hodnotě. Při zvýšení prahové hodnoty dosáhneme vyšší senzitivity za cenu ztráty specificity a naopak. K nalezení optimální prahové hodnoty (tj. nastavení takové hranice normy, abychom dosáhli nejlepšího poměru mezi senzitivitou a specificitou pro daný účel) slouží tzv. ROC (Receiver Operating Characteristic) křivka, která graficky znázorňuje vztah mezi správnou pozitivitou (osa y: senzitivita) a falešnou pozitivitou (osa x: 1 - specificita). U testu, který nemá diskriminační schopnost, probíhá křivka jako diagonála. Pokud test odliší stav nemoci od stavu bez nemoci, křivka se posouvá směrem k levému hornímu rohu (obr. 4). Plocha pod ROC křivkou slouží ke standardnímu vyjádření diagnostické efektivity testu. Čím lepší test, tím více je křivka blíže levému hornímu rohu a plocha pod křivkou se zvětšuje. Výpočet plochy pod křivkou při ROC analýze pomáhá při porovnání různých diagnostických testů mezi sebou.
Obr. 4. ROC křivka Čárkovaná úsečka představuje test bez diskriminační schopnosti, tedy diagnosticky bez užitku. Tečkovaná čára zachycuje výsledky nového testu, který má lepší parametry (větší plochu pod křivkou) ve srovnání se standardním diagnostickým testem znázorněným plnou čárou. 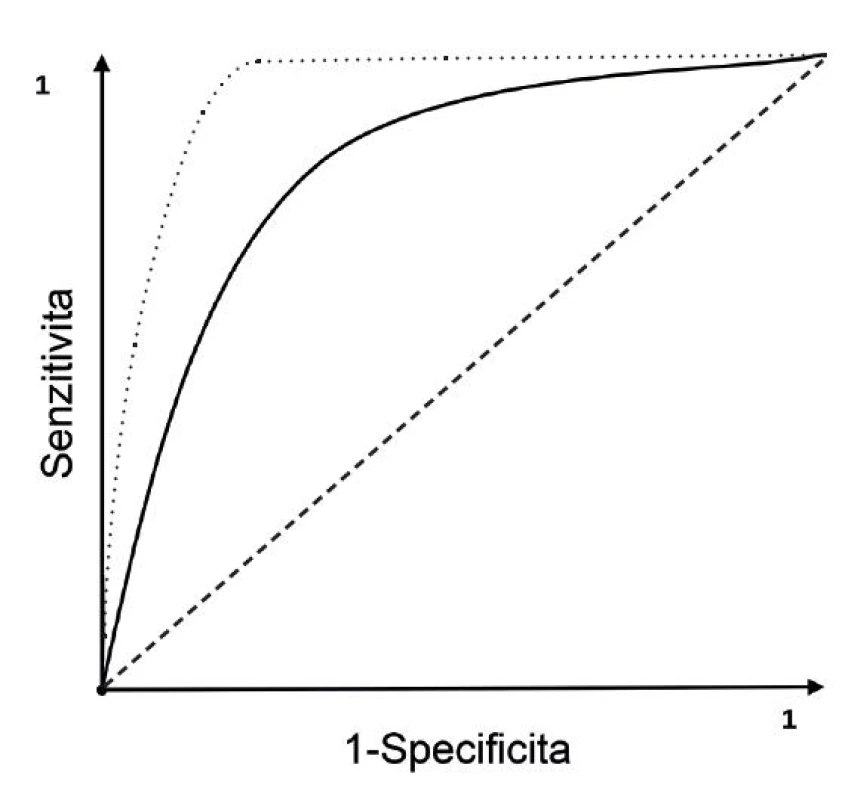
Prediktivní hodnoty
Viděli jsme, že senzitivita a specificita jsou odrazem schopnosti testu odlišit od sebe osoby s a bez dané nemoci. V klinické praxi nás ale nezajímá, jaká je pravděpodobnost abnormálního výsledku u nemocného s danou chorobou, chceme vědět, jaká je pravděpodobnost, že náš nemocný s určitým výsledkem testu trpí daným onemocněním. Odpověď nám poskytne prediktivní hodnota testu. Pozitivní prediktivní hodnota označuje podíl nemocných s pozitivním výsledkem testu, kteří skutečně mají danou nemoc. Negativní prediktivní hodnota je podíl zdravých osob ve skupině s negativním výsledkem testu. Prediktivní hodnoty na rozdíl od senzitivity a specificity zohledňují prevalenci daného onemocnění (tab. 1).
Už jsme si ukázali, že latex fixační test není příliš vhodný ke screeningu revmatoidní artritidy, protože 1/4 nemocných s revmatoidní artritidou bude mít negativní výsledek (senzitivita 75 %). Co když ale budeme hledat jen nemocné se séropozitivní revmatoidní artritidou? Pokud použijeme náš latex fixační test ke screeningu celé populace, kolik procent jedinců s pozitivním výsledkem bude mít séropozitivní revmatoidní artritidu? Předpokládáme-li prevalenci revmatoidní artritidy kolem 1 %, pak nám vyjde pozitivní prediktivní hodnota testu 8 %. Vzhledem k nízké prevalenci revmatoidní artritidy v populaci bude 92 % abnormálních výsledků falešně pozitivních! (obr. 5). Je důležité si uvědomit, že zvláště při diagnostice vzácných revmatických onemocnění jsou i testy s velmi dobrými parametry (tj. s vysokou senzitivitou a specificitou) zatížené vysokým rizikem falešně pozitivních výsledků. Proto má smysl diagnostické testy indikovat jen u nemocných, u nichž je na základě anamnézy, fyzikálního nálezu a předchozích výsledků pravděpodobnost daného onemocnění poměrně vysoká.
Obr. 5. Vliv prevalence onemocnění na výsledky testu. Pokud použijeme latex fixační test se senzitivitou 75% a specificitou 91% v neselektované populaci (prevalence revmatoidní artritidy 1%), pak bude drtivá většina pozitivních výsledků falešně pozitivních (a). Při použití stejného testu u nemocných s bolestmi drobných ručních kloubů, u nichž předpokládáme a priori pravděpodobnost výskytu revmatoidní artritidy 20% bude falešně pozitivních již jen 32 % výsledků (720/2220 = 0,32) viz také tabulka 1. 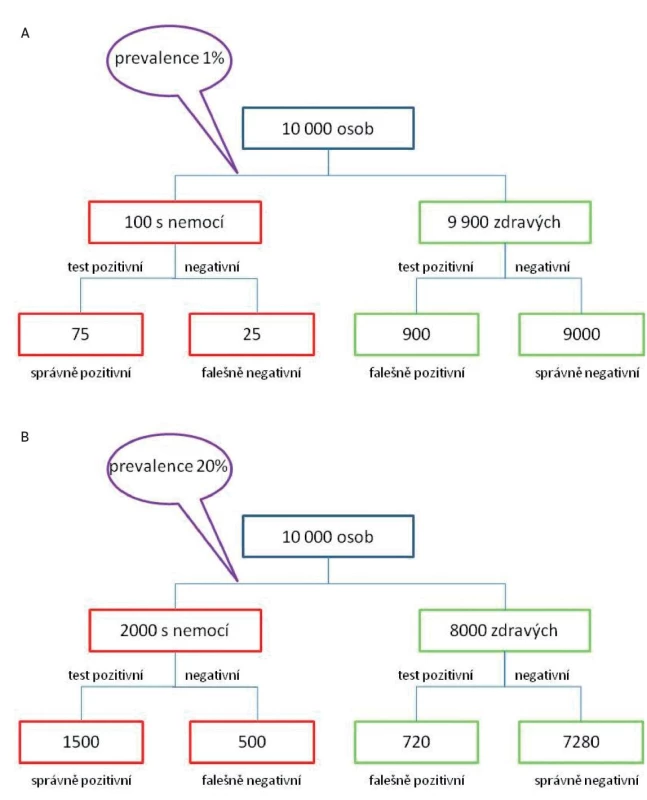
Šance a poměr pravděpodobnosti
Pravděpodobnost jsme většinou zvyklí vyjadřovat v procentech (0–100 %), ale pro účely klinického rozhodování je potřeba se seznámit i s pojmem šance (angl. odds). Šance vyjadřuje podíl pravděpodobnosti výskytu určitého jevu ku pravděpodobnosti jeho nevýskytu. Při hodu mincí je pravděpodobnost, že padne panna 50%. Šance, že padne panna, je tedy 1 : 1. Šance hodit jedním hodem kostkou šestku je 1 : 5. Jak ilustrují naše dva příklady, pojem šance se běžně užívá ve světě hazardních her. Vztah mezi pravděpodobností vyjádřenou v procentech a šancí znázorňuje graf na obrázku 6.
Obr. 6. Vztah mezi pravděpodobností a šancí. 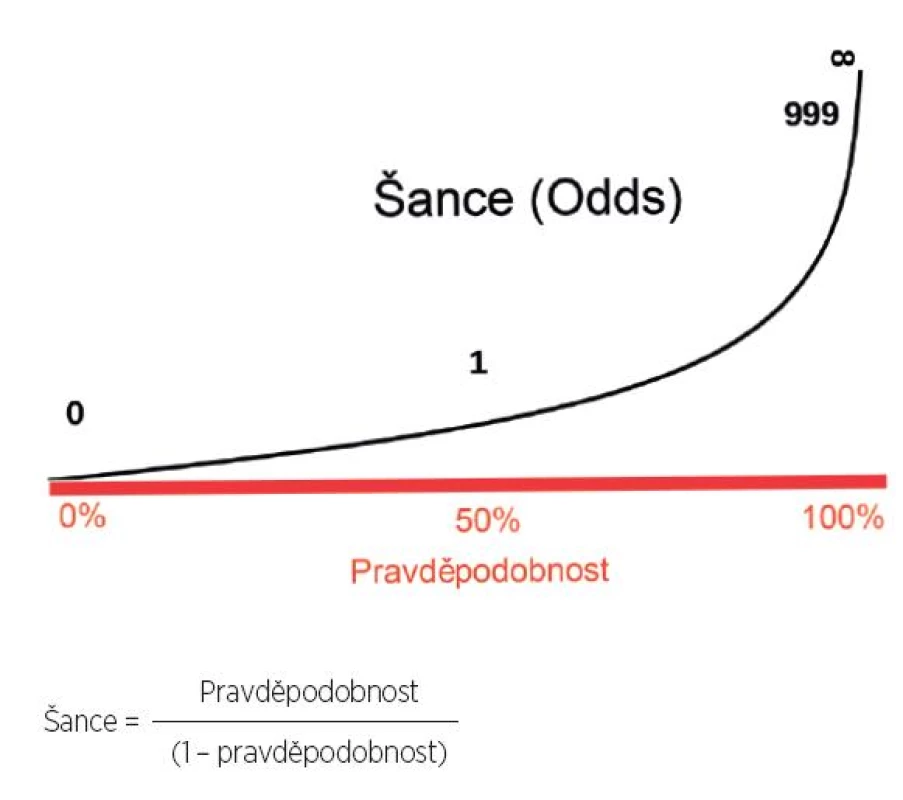
Pravděpodobnost 50% odpovídá šanci 1. Všiměte si, že hodnoty šancí jsou asymetrické a dosahují hodnot od 0 do nekonečna. Upraveno podle (1). Dalším důležitým pojmem je věrohodnostní poměr (LR, angl. likelihood ratio). LR pozitivního výsledku testu nám říká, o kolik je diagnóza pravděpodobnější při pozitivním výsledku testu ve srovnání s pravděpodobností před provedením testu. LR negativního výsledku testu naopak určuje, o kolik méně je pravděpodobné onemocnění při negativním výsledku testu (tab. 2). Uvažování ve formě šancí a LR výrazně usnadňuje použití Bayesovské analýzy.
Tab. 2. Orientační význam různě vysokých hodnot LR diagnostických testů. 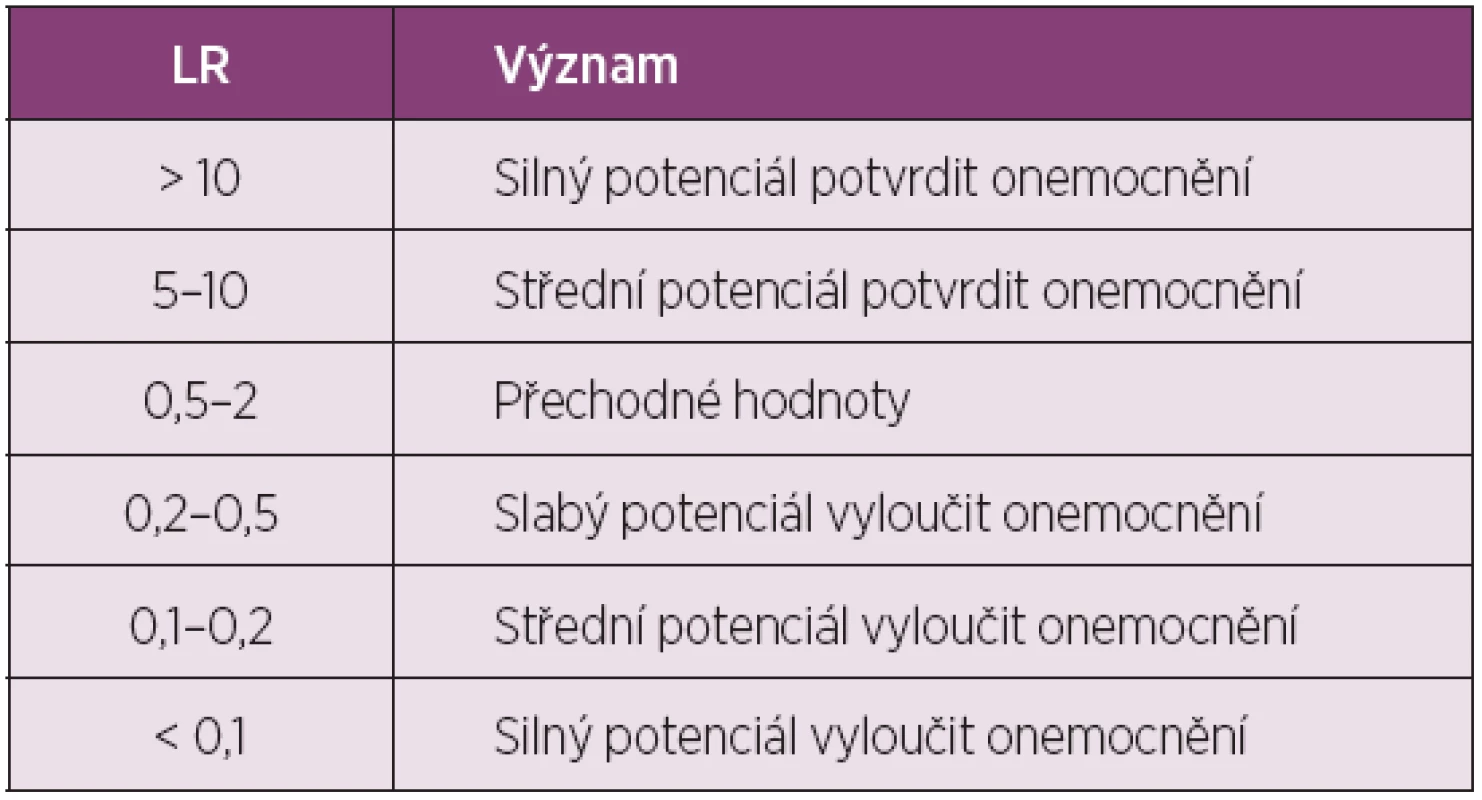
LR – věrohodnostní poměr (angl. likelihood ratio) Bayesova věta
Thomas Bayes byl anglický nonkonformistický duchovní a matematik, který se díky své posmrtně publikované práci s názvem Essay towards solving a problem in the doctrine of chances (Esej směrovaná k řešení problému ve vědě o náhodě) stal jedním ze zakladatelů induktivní statistiky (obr. 7). Bayesova věta nám umožňuje vypočítat, nakolik ovlivní výsledek testu pravděpodobnost výskytu onemocnění u daného pacienta. Pravděpodobnost výskytu onemocnění před provedením diagnostického testu nazýváme apriorní pravděpodobností (angl. pre-test probability). Pokud aplikujeme test na náhodně vybraného jedince, pak je apriorní pravděpodobnost shodná s prevalencí onemocnění v dané populaci. Pravděpodobnost výskytu onemocnění po provedení diagnostického testu se označuje jako aposteriorní pravděpodobnost (angl. post-test probability). Pro potřeby diagnostiky lze Bayesovu větu vyjádřit jednoduchou rovnicí: W1 = W0 x LR, kde W1 je pravděpodobnost daného onemocnění po provedení testu ve formě šance (aposteriorní pravděpodobnost), W0 je pravděpodobnost onemocnění před provedením testu ve formě šance (apriorní pravděpodobnost) a LR je věrohodnostní poměr daného testu. Pokud je apriorní pravděpodobnost daného onemocnění velmi nízká (např. prevalenci systémového lupusu erythematodes u asymptomatických žadatelů o zaměstnání pilota dopravních letadel můžeme odhadnout na méně než 1 : 2000), pak ani pozitivní výsledek specifického testu (např. anti-dsDNA s LR = 16) nezvýší pravděpodobnost onemocnění natolik, abychom na základě tohoto výsledku podnikali nějaké další kroky (aposteriorní pravděpodobnost bude méně než 16 : 2000, tedy pod 0,8 %). Jiná situace ovšem nastane, pokud bude apriorní pravděpodobnost významně vyšší (např. náš uchazeč o místo pilota bude mít charakteristickou vyrážku v obličeji, artritidu a hematurii, apriorní pravděpodobnost SLE u takového nemocného můžeme odhadnout na 1 : 4 a při průkazu anti-dsDNA stoupne na 4 : 1, tedy na 80 %). Rovnice pro výpočet aposteriorní pravděpodobnosti při použití procent místo šancí je složitější, můžeme ale použít nomogram (obr. 8).
Obr. 7. Thomas Bayes (1702–1761). 
Obr. 8. Nomogram k výpočtu aposteriorní pravděpodobnosti podle Bayesovy rovnice a jeho použití v praxi. A) Nomogram navržený Faganem (2) umožňuje vypočítat aposteriorní pravděpodobnost, aniž bychom museli převádět hodnoty z procent na šance. Při použití nomogramu graficky spojíme apriorní pravděpodobnost v levém sloupci s LR použitého testu ve sloupci prostředním. V pravém sloupci potom dostaneme výslednou hodnotu aposteriorní pravděpodobnosti. B) Pokud použijeme vysoce specifické vyšetření antiCCP protilátek, které má LR 12,5 (3) u asymptomatického jedince (přerušovaná čára), pak bude získaná aposteriorní pravděpodobnost při pozitivním výsledku pouze okolo 10%. Ovšem při vyšetření ženy s typickými příznaky (tečkovaná čára) stoupne aposteriorní pravděpodobnost z 30% na téměř 90%. 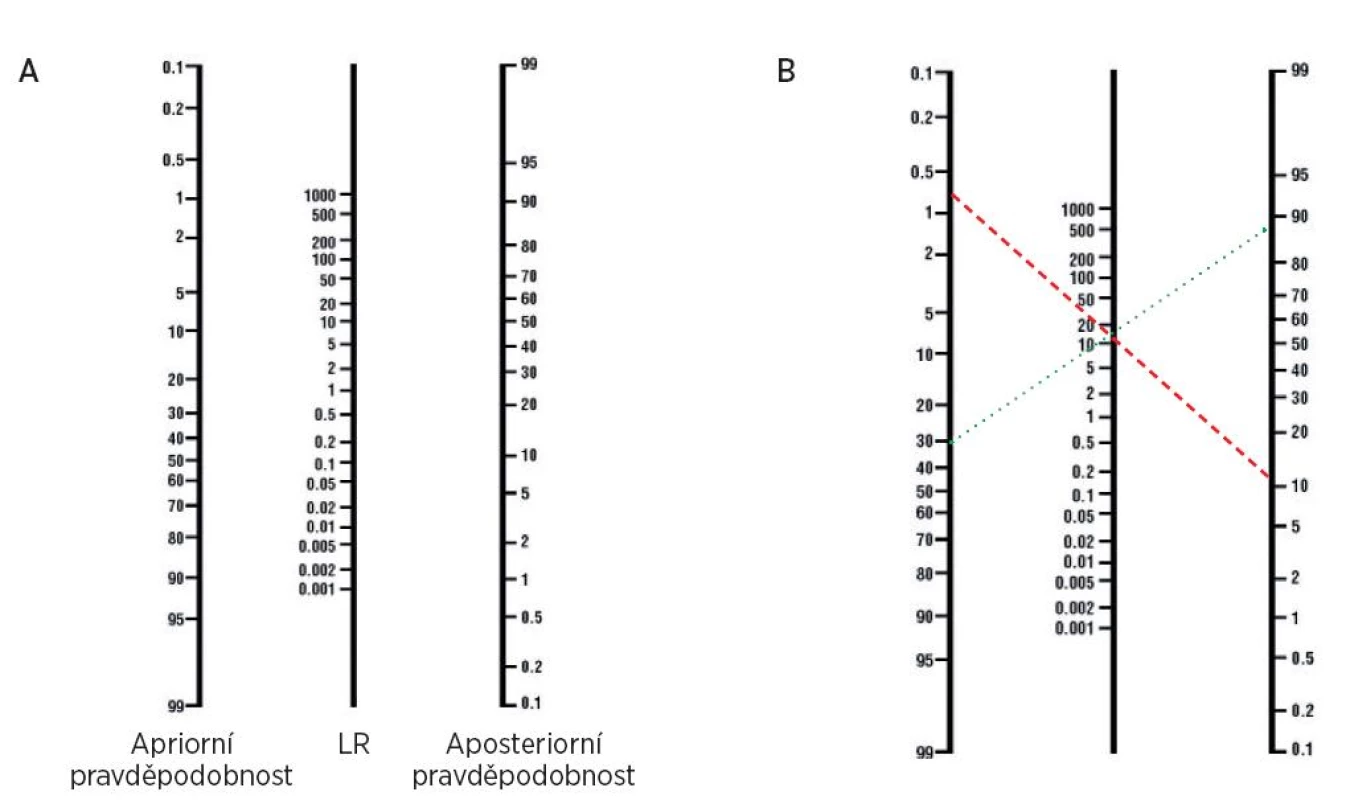
V praxi jen málokterý test významně zvýší pravděpodobnost daného onemocnění u pacienta s apriorní pravděpodobností nižší než 10 %, proto je třeba diagnostické testy indikovat jen na základě skutečně důvodného klinického podezření. Při použití několika navzájem nezávislých testů slouží aposteriorní pravděpodobnost jednoho jako apriorní pravděpodobnost pro následující test.
Závěr
Při péči o nemocné si většinou neuvědomujeme, že se vlastně zabýváme aplikovanou statistikou. Bayesovský přístup nám umožňuje poskládat diagnostické kroky co nejúčelněji tak, aby náklady a rizika nutná k potvrzení nebo k vyloučení diagnózy byla co nejnižší. Zkušení klinici užívají tohoto principu v praxi intuitivně, nám ostatním může pomoci pochopení základních principů popsaných v tomto článku.
Dedikace: Podpořeno projektem koncepčního rozvoje výzkumné organizace MZ ČR 023728 (Revmatologický ústav)
Adresa pro korespondenci:
MUDr. Heřman Mann
Revmatologický ústav
Na Slupi 4
128 50 Praha 2
Zdroje
1. Gross R. Making clinical decisions. ACP, Philadelphia 1999.
2. Fagan TJ. Letter: Nomogram for Bayes theorem. N Engl J Med 1975; 293 : 257.
3. Nishimura K, Sugiyama D, Kogata Y, et al. Meta-analysis: diagnostic accuracy of anti-cyclic citrullinated peptide antibody and rheumatoid factor for rheumatoid arthritis. Ann Intern Med 2007; 146 : 797-808.
Štítky
Dermatologie Dětská revmatologie Revmatologie
Článek OznámeníČlánek Eozinofilní fasciitida
Článek vyšel v časopiseČeská revmatologie
Nejčtenější tento týden
2013 Číslo 2- Takrolimus v terapii atopické dermatitidy a analýza jeho nákladové efektivity ve srovnání s kortikosteroidní léčbou
- Daivobet gel – lékový profil
- Fixní kombinace kalcipotriol/betamethason v topické léčbě psoriázy
- Psoriáza a kouření – vzájemně se potencující rizika?
- Selektivní inhibitor IL-23 risankizumab: nejnovější posila v biologické léčbě psoriázy
-
Všechny články tohoto čísla
- Doporučení České revmatologické společnosti pro diagnostiku a sledování nemocných se systémovým lupus erythematodes
- Oznámení
- Průběh těhotenství u žen se systémovým lupus erythematodes
- Ranní a večerní chronotypy u revmatoidní artritidy
- Eozinofilní fasciitida
- Je ultrazvuk spolehlivým pomocníkem revmatologa?
- Co bychom měli vědět o diagnostických testech
- Česká revmatologie
- Archiv čísel
- Aktuální číslo
- Informace o časopisu
Nejčtenější v tomto čísle- Průběh těhotenství u žen se systémovým lupus erythematodes
- Eozinofilní fasciitida
- Doporučení České revmatologické společnosti pro diagnostiku a sledování nemocných se systémovým lupus erythematodes
- Co bychom měli vědět o diagnostických testech
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



