-
Články
- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Výskyt agranulocytózy po tyreostaticích v kohortě pacientů s Gravesovou nemocí léčených radioaktivním jodem 131I v průběhu 14 let
The occurrence of agranulocytosis due to antithyroid drugs in a cohort of patients with Graves‘ disease treated with radioactive iodine 131I during 14 years
Introduction:
Agranulocytosis is a serious complication of antithyroid drugs (ATD) treatment of thyrotoxicosis. The aim of our work was to assess the occurrence of agranulocytosis in Graves’ disease (GD) patients admitted for radioactive iodine 131I (RAI) treatment to our thyroid unit.Patients and methods:
We analyzed retrospectively a cohort of 603 GD patients (500 women and 103 men; mean age 51.5 ± 12.7 years) who received RAI between 1999 and 2012. Of them, 327 (54 %) patients were originally treated with carbimazole (CBZ), 215 (36 %) with methimazole (MMI) and 61 (10 %) with propylthiouracil (PTU).Results:
Agranulocytosis due to ATD was the cause of RAI treatment in 7 patients of 603. All of them were women (mean age 48.7 years; range 23–78). In 4 patients, agranulocytosis occurred on MMI treatment, and in 3 patients on CBZ. After recalculation of CBZ to the equipotent dose of MMI, the mean ATD dose was 22.4 mg MMI/day (range 9–40). No agranulocytosis due to PTU was found in our cohort. The time from beginning ATD treatment to agranulocytosis was 20–41 days. In 5 patients there was a development of fever, while in 2 patients the complication was diagnosed from routine blood count. The mean duration of agranulocytosis was 5.9 days (range 4–8).Conclusion:
Agranulocytosis incidence in our cohort of patients was 1.2 %, while in most reports the prevalence ranged from 0.2 to 0.5 %. In all patients, agranulocytosis occurred early, and in one third it was asymptomatic when found. The aim of our report is to bring attention to a relatively rare, but potentially serious, complication of ATD treatment.Key words:
agranulocytosis – carbimazole – Graves’ disease – methimazol – propylthiouracil
Autoři: Jitka Čepková; Filip Gabalec; Ioannis Svilias; Jiří Horáček
Působiště autorů: IV. interní hematologická klinika LF UK a FN Hradec Králové, přednosta doc. MUDr. Pavel Žák, Ph. D.
Vyšlo v časopise: Vnitř Lék 2014; 60(10): 832-836
Kategorie: Původní práce
Souhrn
Úvod:
Agranulocytóza je závažná komplikace léčby tyreostatiky (ATD) u zvýšené funkce štítné žlázy. Cílem naší práce bylo zjistit výskyt agranulocytózy u pacientů s Gravesovou nemocí (GD) přijatých k léčbě radioaktivním jodem 131I (RAI) na tyreoidální jednotku naší kliniky.Pacienti a metody:
Retrospektivně jsme analyzovali 603 pacientů s GD (500 žen a 103 mužů; průměrný věk 51,5 ± 12,7 let), kterým byl v letech 1999–2012 aplikován RAI. Z nich 327 (54 %) předtím užívalo karbimazol (CBZ), 215 (36 %) methimazol (MMI) a 61 (10 %) propylthiouracil (PTU).Výsledky:
Agranulocytóza po ATD byla důvodem k léčbě RAI u 7 z 603 nemocných. Šlo vždy o ženy, s věkovým průměrem 48,7 let (rozpětí 23–78). U 4 pacientek agranulocytóza vznikla po MMI a 3 pacientky užívaly CBZ. Po přepočtu CBZ na odpovídající dávku MMI byla průměrná dávka ATD 22,4 mg MMI/den (rozpětí 9–40). Agranulocytózu po PTU jsme v našem souboru nezachytili. Interval od zahájení terapie ATD do vzniku agranulocytózy byl 20–41 dní. U 5 nemocných došlo k rozvoji teploty, ve 2 případech byla komplikace diagnostikována z rutinní kontroly krevního obrazu. Průměrná doba trvání agranulocytózy byla 5,9 dní (rozpětí 4–8).Závěr:
Výskyt agranulocytózy v našem souboru nemocných byl 1,2 %, zatímco literární data uvádějí výskyt 0,2–0,5 %. U všech nemocných došlo k rozvoji agranulocytózy časně, z toho asi 30 % bylo v době diagnózy asymptomatických. Práce má za cíl upozornit na poměrně vzácnou, ale potenciálně závažnou komplikaci léčby ATD.Klíčová slova:
agranulocytóza – Gravesova nemoc – karbimazol – methimazol – propylthiouracilÚvod
Gravesova nemoc (GD) je nejčastější příčinou hypertyreózy s prevalencí asi 0,5–1 % [1]. Po potvrzení diagnózy GD máme k dispozici 3 efektivní a relativně bezpečné možnosti léčby: navození farmakologické remise tyreostatiky (ATD), aplikaci radioaktivního jodu 131I (RAI) nebo chirurgické řešení [2]. Mezi jednotlivými zeměmi existují rozdílné přístupy v použití jednotlivých léčebných metod [3]. V USA je na prvním místě zvažována aplikace RAI, v Evropě (a stejně tak i v ČR) se na prvním místě zahajuje terapie ATD [3,4]. K radikální léčbě (aplikace RAI nebo chirurgické řešení) se přistupuje až při recidivě onemocnění nebo při nemožnosti vysadit ATD [5].
ATD se v léčbě GD používají již více než 60 let [6]. Hlavní efekt léčby je snížení tvorby tyreoidálních hormonů a udržení eutyreózy, dokud nedojde k remisi. Mezi ATD patří karbimazol (CBZ), který v současné době není na českém trhu dostupný, a methimazol (MMI) nebo chemicky odlišný propylthiouracil (PTU). Tato tyreostatika inhibují oxidaci jodu a jeho vazbu na tyrozolové zbytky. PTU navíc zčásti inhibuje periferní přeměnu tyroxinu (T4) na trijodtyronin (T3) [7]. CBZ je prekurzorem MMI; po vstřebání se rychle konvertuje na MMI (10 mg CBZ je metabolizováno přibližně na 6 mg MMI) [2].
Vstupní dávka ATD je vyšší než udržovací dávka (asi 30–60 mg MMI nebo 300–600 mg PTU) [8], přesto je vzhledem k dlouhému eliminačnímu poločasu T4 (asi 7 dní) nástup účinku ATD pomalý; plný efekt lze očekávat asi za 4–8 týdnů. Po této době by mělo dojít ke klinickému zlepšení s odpovídajícím laboratorním nálezem; normalizace nebo pokles volného tyroxinu (fT4), tyrotropin (TSH) může zůstat suprimován déle. Po dosažení eutyreózy je doporučováno pokračovat v udržovací terapii ATD v nízké dávce (asi 10 mg MMI nebo 100 mg PTU) po dobu 12–18 měsíců [9], pak ATD zpravidla zkoušíme vysadit. K navození dlouhodobé remise po monoterapii ATD však dochází pouze v 40–50 % [10,11]. Prodloužení podávání ATD po dobu delší než 18 měsíců po první atace choroby již nezvyšuje pravděpodobnost udržení dlouhodobé remise [12].
Vyšší riziko relapsu tyreotoxikózy mají muži, kuřáci, pacienti s objemnou strumou (> 80 ml) [13–15]. Přetrvávající vyšší hodnota protilátek proti TSH receptoru (TRAK) a vyšší vaskularizace žlázy dle dopplerovského vyšetření má rovněž souvislost s vyšší pravděpodobností reaktivace GD [15–18]. Po vysazení ATD by tito pacienti měli být kontrolováni častěji. Doporučeny jsou 1–3měsíční intervaly po dobu 6–12 měsíců [2]. Za remisi považujeme, pokud pacienti mají normální TSH, fT4 a fT3 rok po vysazení ATD [2]. Recidivy choroby se však mohou vyskytovat i déle než 1 rok po vysazení ATD.
Vedlejší účinky se mohou vyskytnout asi u 5 % pacientů užívajících ATD [19]. Mezi ty mírné řadíme vyrážku, bolesti kloubů, GIT obtíže, snížení chuti a čichu. Pravděpodobnost výskytu obtíží je adekvátní výši dávky ATD zejména u MMI, u PTU tato závislost není až tolik nápadná [6]. Menší kožní reakce se dají zvládnout současným podáním antihistaminik bez přerušení ATD. Při přetrvávání obtíží je možná výměna za jiné tyreostatikum. Při vážné alergické reakci předepsání alternativního tyreostatika není doporučováno [2].
Mezi závažné komplikace léčby ATD patří agranulocytóza. Predikce a prevence je velmi obtížná. Prevalence je naštěstí nízká, okolo 0,2–0,5 % nemocných s GD užívajících ATD [2,20–22]. Nejčastěji se obtíže (vysoké teploty, bolesti v krku, soor) objevují náhle v prvních 3 měsících po zahájení léčby tyreostatiky [23]. Obvykle bývají po MMI nebo CBZ a riziko vzniku obtíží se zvyšuje se stoupající dávkou ATD [24]. Ojediněle se obtíže mohou vyskytnout i později nebo se vyvíjet plynule [23]. PTU agranulocytózu způsobuje méně často [25,26]. Pacienti musí být upozorněni, aby při výskytu horečky, bolesti v krku nebo sooru v dutině ústní neprodleně navštívili lékaře. Při poklesu absolutního počtu neutrofilů (ANC) pod 1 000/µl je nutné ukončit podávání ATD a zahájit empirickou intravenózní ATB terapii [27]. Po zvládnutí akutních obtíží je na místě po domluvě s pacientem radikální řešení. Dlouhodobé podávání ATD je v tomto případě kontraindikováno pro existenci zkřížené reaktivity mezi MMI a PTU stran rozvoje agranulocytózy [28].
Z dalších vážných komplikací je možný hepatotoxický účinek PTU, v ojedinělých případech může dojít až k akutnímu jaternímu selhání. Hepatotoxický efekt přetrvává i po vysazení PTU a může mít fatální následky [29]. Dle doporučení ATA by PTU neměl být předepisován v první linii léčby, ale jeho použití by mělo být indikováno ve zvláštních případech, jako je první trimestr gravidity, tyreotoxická krize a u pacientů netolerujících MMI (s výjimkou agranulocytózy) [29]. Hepatotoxický efekt MMI je typicky cholestatický. Zřídka může dojít k hepatocelulárnímu postižení, které je obvykle mírné a spontánně odezní [30,31]. ANCA pozitivní vaskulitida je další vzácnou komplikací, u které je nutné přerušit podávání ATD [32].
Pacienti a metody
Retrospektivně jsme analyzovali 603 pacientů s GD, kterým byl v letech 1999–2012 aplikován RAI na tyreoidální jednotce IV. interní hematologické kliniky LF UK a FN Hradec Králové, provozované ve spolupráci s oddělením nukleární medicíny FN Hradec Králové. V souboru bylo 500 žen a 103 mužů. Průměrný věk v době aplikace RAI byl 51,5 ± 12,7 let. Dle doporučených postupů v České republice se obvykle jednalo o pacienty s delší než roční anamnézou nemoci, v prvním nebo dalším relapsu onemocnění. Výjimečně byl RAI podán již po zaléčení první ataky choroby. V tomto případě šlo především o mladé pacientky plánující do budoucna těhotenství, o pacienty s nežádoucími účinky ATD a o starší pacienty s vysokým rizikem převážně kardiálních a skeletálních komplikací při nedostatečně kompenzované tyreotoxikóze. Před aplikací RAI 327 (54 %) pacientů užívalo CBZ, 215 (36 %) MMI a 61 (10 %) PTU. Agranulocytóza byla definovaná jako počet granulocytů pod 500/µl. Kontroly krevního obrazu po zahájení terapie ATD nebyly rutinně prováděny.
Výsledky
Z celkového počtu 603 nemocných byla agranulocytóza zachycena u 7 případů (1,2 %), u kterých bylo nutno ATD léčbu ukončit a aplikovat RAI jako radikální řešení. Ve všech případech šlo o ženy s prvním záchytem GD s věkovým rozmezím 23–78 let, průměrný věk byl 48,7 ± 19,4 let (tab). Čtyři pacientky užívaly MMI a 3 pacientky užívaly CBZ. Po přepočtu CBZ na odpovídající dávku MMI byla průměrná dávka ATD 22,4 mg MMI/den (rozpětí 9–40). Interval od zahájení terapie ATD do rozvoje agranulocytózy (potvrzeno dle hodnot krevního obrazu) byl 20–41 dní. U 5 nemocných došlo ke vzniku obtíží (vysoké teploty), ve 2 případech byla agranulocytóza diagnostikována u asymptomatické pacientky z hodnot krevního obrazu při standardní endokrinologické kontrole. Průměrná doba trvání agranulocytózy byla 5,9 dní (rozpětí 4–8). V 5 případech došlo ke spontánní regeneraci krvetvorby po vysazení ATD. V tomto případě agranulocytóza průměrně trvala 5,6 dní (rozpětí 4–8). Ve 2 případech byl podáván růstový faktor (filgrastim, G-CSF) ke stimulaci tvorby granulocytů s trváním agranulocytózy průměrně 6,5 dní (rozpětí 6–7). Po regeneraci krvetvorby byl všem pacientkám přechodně podáván PTU a jako definitivní léčba GD byl aplikován RAI s úspěšnou odezvou. Rok po aplikaci RAI všech 7 nemocných užívalo hormonální substituci levotyroxinem a mělo normální hodnoty krevního obrazu. V naší kohortě 603 pacientů jsme nezaznamenali žádný výskyt závažných hepatotoxických účinků tyreostatik a žádný případ tyreostatiky navozené vaskulitidy.
Tab. 1. Pacienti s agranulocytózou po podání methimazolu (MMI) a karbimazolu (CBZ) 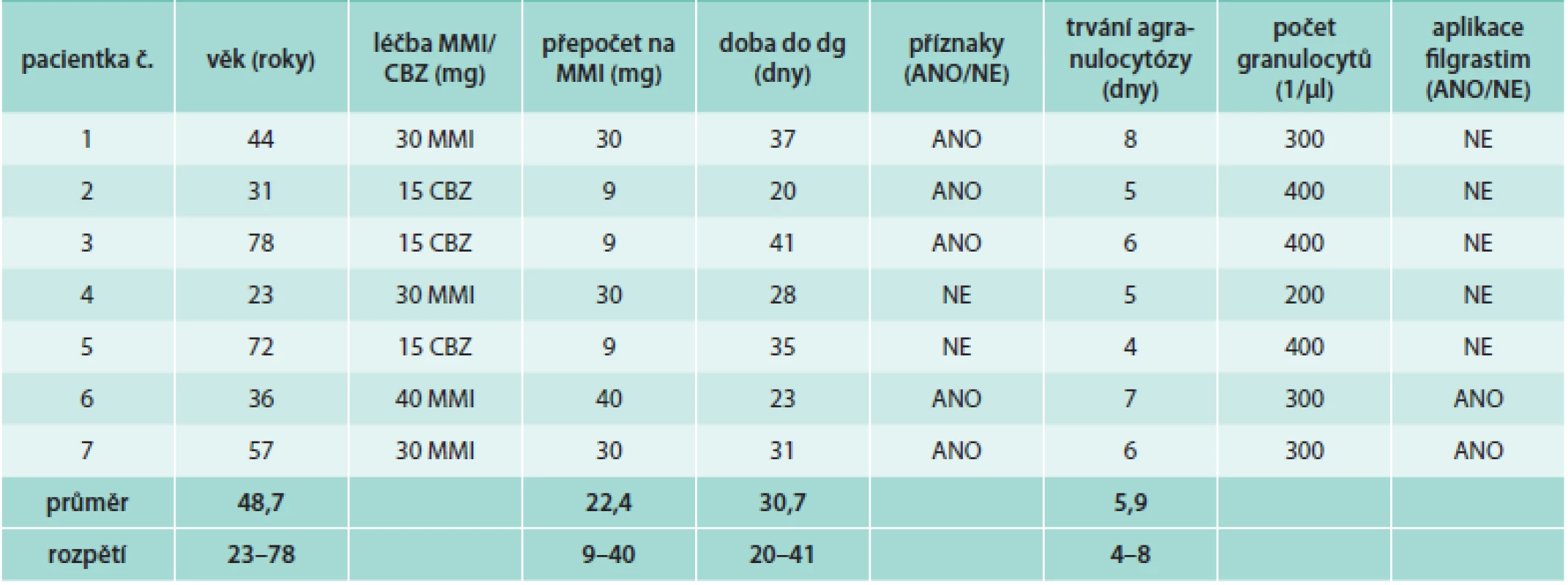
Diskuse
V této retrospektivní studii jsme analyzovali 7 případů agranulocytózy způsobené ATD z celkového počtu 603 pacientů s GD, kteří byli léčení aplikací RAI v průběhu 14 let. Výskyt této závažné až život ohrožující komplikace v našem souboru nemocných tak byl 1,2 % oproti očekávaným 0,2–0,5 % [2,20,21]. Dle nedávné práce japonských autorů, kteří zkoumali 754 případů ATD indukované agranulocytózy u GD v průběhu 30 let, je výskyt této vážné komplikace dokonce ještě nižší 0,1–0,15 % [23]. Zvýšený výskyt agranulocytózy v naší kohortě pacientů je pravděpodobně způsoben tím, že se jednalo o nemocné vyžadující radikální léčbu GD. Šlo nejčastěji o pacienty s relapsem choroby, ale také (vzácně) s nežádoucími účinky ATD. V našem souboru však nebyl zaznamenán žádný výskyt závažných hepatotoxických účinků ATD, pravděpodobně proto, že naši pacienti byli léčeni převážně MMI a CBZ, jejichž případný hepatotoxický účinek bývá mírný [30,31]. Pouze 10 % našich pacientů užívalo PTU, který může způsobit těžké jaterní poškození až akutní jaterní selhání [29].
Při bližší analýze jednotlivých případů agranulocytózy šlo ve všech případech o ženy s nově diagnostikovanou GD. Oproti původnímu očekávání věkový medián ve skupině s výskytem agranulocytózy (44 let) byl nižší než v celém souboru (51 let). V dříve publikovaných pracích je výskyt agranulocytózy spojován s vyšším věkem [23,33].
Ke vzniku agranulocytózy v našem souboru nemocných došlo ve všech případech během prvních 2 měsíců terapie ATD, medián byl 31 dní od zahájení léčby. Tyto výsledky jsou v dobré shodě s dříve publikovanými pracemi [33–35]. Dle rozsáhlé studie japonských autorů (Nakamura et al) [23] se více než 70 % případů agranulocytózy objevilo během prvních 60 dní terapie ATD a téměř 85 % během prvních 90 dní podávání tyreostatik. Pouze u 55 pacientů (7 %) z celkových 754 se rozvinula agranulocytóza později než 4 měsíce od zahájení terapie ATD. Ke vzniku agranulocytózy rovněž může dojít po znovuzahájení léčby ATD při relapsu onemocnění.
K rozvoji obtíží (vysoké teploty, bolesti v krku, soor) obvykle dochází náhle. U 5 našich pacientek s diagnózou agranulocytózy došlo náhle ke vzniku vysokých teplot bez předchozích příznaků. Naopak u 2 nemocných byla diagnóza učiněna náhodně z rutinního odběru krevního obrazu v rámci standardní endokrinologické kontroly. Pravidelné monitorování krevních testů není mnohými autory doporučováno pro malou výpovědní hodnotu v predikci agranulocytózy [2,20,21]. Naopak v Japonsku je doporučováno pravidelné monitorování krevního obrazu v intervalu 2 týdnů během prvních 2 měsíců terapie ATD [23]. Tajiri et al [33] publikovali, že pouze 12 z 55 nemocných s ATD indukovanou agranulocytózou mělo klinicky manifestní příznaky v době diagnózy. Více než 70 % případů bylo diagnostikováno náhodně z rutinního odběru krevních testů. Naopak Nakamura et al [23] varují před přílišným spoléháním na rutinní monitorování krevního obrazu. Více než polovina nemocných v jejich souboru (n = 754) měla normální krevní testy 2 týdny před klinickou manifestací agranulocytózy.
V našem souboru nebyl zaznamenán žádný případ vzniku agranulocytózy po užívání PTU. CBZ byl podáván ve 3 případech a MMI ve 4 případech. Po přepočtu dávky CBZ na adekvátní dávku MMI byla průměrná dávka MMI 22,4 ± 12,1 mg/den v době diagnózy agranulocytózy. Podobnou průměrnou dávku (25,2 ± 12,8 mg/den) vypočítali i Nakamura et al v jejich souboru pacientů [23]. Vyšší dávka ATD je spojena se zvýšeným rizikem. Dle jiné rozsáhlé studie byl výskyt agranulocytózy 0,8 % z 2 087 pacientů léčených počáteční dávkou MMI 30 mg/den, ale jen 0,2 % z 2 739 pacientů léčených počáteční dávkou MMI 15 mg/den [24].
Při diagnóze agranulocytózy je na zvážení přechodné podávání G-CSF ke stimulaci tvorby granulocytů k celkovému zkrácení regenerace krvetvorby, a tím i doby hospitalizace, ačkoliv prospektivní randomizovaná studie tento fakt nepotvrdila [36]. Jiní autoři naopak prokázali zkrácení doby regenerace podáním G-CSF [37]. Při rozdělení našeho souboru na 2 skupiny podle aplikace G-CSF nebyl zřetelný rozdíl v délce regenerace krvetvorby. Soubor však byl příliš malý a sledování nikoli prospektivní, takže toto zjištění má jen orientační výpovědní hodnotu.
Závěr
Práce má za cíl upozornit na poměrně vzácnou, ale potenciálně závažnou komplikaci léčby ATD. Prevalence agranulocytózy v naší kohortě 603 pacientů byla 1,2 % proti v literatuře uváděným 0,2–0,5 %. Tento zvýšený výskyt byl pravděpodobně způsoben povahou našeho souboru, jednalo se o pacienty vyžadující radikální léčbu GD.
Retrospektivní design naší studie neumožňuje posoudit, zda rutinní monitorování krevního obrazu při léčbě ATD má v časném odhalení vzniku agranulocytózy klinický význam. Pozorovali jsme však, že skoro ve 30 % případů v našem souboru byla agranulocytóza zachycena právě při rutinním vyšetření, tedy ještě bez příznaků. Vzhledem k běžné dostupnosti a nízké ceně se nám rutinní vyšetřování krevního obrazu při standardních kontrolách jeví spíše vhodné, přinejmenším během prvních 3 měsíců terapie ATD, kdy je vznik této komplikace nejpravděpodobnější. V každém případě musí být pacienti poučeni, aby při výskytu obtíží (vysoké teploty, bolesti v krku, soor) přestali užívat ATD a neprodleně navštívili lékaře.
Aplikace G-CSF v našem (pro spolehlivé hodnocení příliš malém) souboru léčených nevedla ke zkrácení doby regenerace krvetvorby.
Podpořeno projektem IGA MZ ČR NT 13535–3/2012.
MUDr. Jitka Čepková
jitka.cepkova@fnhk.cz
IV. interní hematologická klinika LF UK a FN Hradec Králové
www.fnhk.cz
Doručeno do redakce 11. 6. 2014
Přijato po recenzi 14. 7. 2014
Zdroje
1. Zamrazil V. Nemoci štítné žlázy v klinické praxi. Postgrad Med J 2013; 15(7): 720–729.
2. Bahn Chair RS, Burch HB, Cooper DS et al. Hyperthyroidism and other causes of thyrotoxicosis: management guidelines of the American Thyroid Association and American Association of Clinical Endocrinologists. Thyroid 2011; 21(6): 593–646.
3. Burch HB, Burman KD, Cooper DS. A 2011 survey of clinical practice patterns in the management of Graves' disease. J Clin Endocrinol Metab 2012; 97(12): 4549–4558.
4. Wartofsky L, Glinoer D, Solomon B et al. Differences and similarities in the diagnosis and treatment of Graves' disease in Europe, Japan, and the United States. Thyroid 1991; 1(2): 129–135.
5. Vaidya B, Williams GR, Abraham P et al. Radioiodine treatment for benign thyroid disorders: results of a nationwide survey of UK endocrinologists. Clin Endocrinol (Oxf) 2008; 68(5): 814–820.
6. Cooper DS. Antithyroid drugs. N Engl J Med 2005; 352(9): 905–917.
7. Dokupilova A, Payer J. Thyrostatic treatment and its adverse effects. Vnitř Lék 2013; 59(11): 989–995.
8. Brunová J Diagnostika a terapie poruch funkce štítné žlázy. Med pro praxi 2008; 5(9): 315–321.
9. Rajput R, Goel V. Indefinite antithyroid drug therapy in toxic Graves' disease: What are the cons. Indian J Endocrinol Metab 2013; 17(Suppl 1): S88-S92.
10. Allannic H, Fauchet R, Orgiazzi J et al. Antithyroid drugs and Graves' disease: a prospective randomized evaluation of the efficacy of treatment duration. J Clin Endocrinol Metab 1990; 70(3): 675–679.
11. Maugendre D, Gatel A, Campion L et al. Antithyroid drugs and Graves' disease – prospective randomized assessment of long-term treatment. Clin Endocrinol (Oxf) 1999; 50(1): 127–132.
12. Weetman AP. Graves' hyperthyroidism: how long should antithyroid drug therapy be continued to achieve remission? Nat Clin Pract Endocrinol Metab 2006; 2(1): 2–3.
13. Allahabadia A, Daykin J, Holder RL et al. Age and gender predict the outcome of treatment for Graves' hyperthyroidism. J Clin Endocrinol Metab 2000; 85(3): 1038–1042.
14. Nedrebo BG, Holm PI, Uhlving S et al. Predictors of outcome and comparison of different drug regimens for the prevention of relapse in patients with Graves' disease. Eur J Endocrinol 2002; 147(5): 583–589.
15. Orunesu E, Bagnasco M, Salmaso C et al. Use of an artificial neural network to predict Graves' disease outcome within 2 years of drug withdrawal. Eur J Clin Invest 2004; 34(3): 210–217.
16. Glinoer D, de Nayer P, Bex M et al. Effects of l-thyroxine administration, TSH-receptor antibodies and smoking on the risk of recurrence in Graves' hyperthyroidism treated with antithyroid drugs: a double-blind prospective randomized study. Eur J Endocrinol 2001; 144(5): 475–483.
17. Orgiazzi J, Madec AM. Reduction of the risk of relapse after withdrawal of medical therapy for Graves' disease. Thyroid 2002; 12(10): 849–853.
18. Takasu N, Yamashiro K, Komiya I et al. Remission of Graves' hyperthyroidism predicted by smooth decreases of thyroid-stimulating antibody and thyrotropin-binding inhibitor immunoglobulin during antithyroid drug treatment. Thyroid 2000; 10(10): 891–896.
19. Abraham P, Avenell A, Park CM et al. A systematic review of drug therapy for Graves' hyperthyroidism. Eur J Endocrinol 2005; 153(4): 489–498.
20. Brent GA. Clinical practice. Graves' disease. N Engl J Med 2008; 358(24): 2594–2605.
21. Franklyn JA, Boelaert K. Thyrotoxicosis. Lancet 2012; 379(9821): 1155–1166.
22. Watanabe N, Narimatsu H, Noh JY et al. Antithyroid drug-induced hematopoietic damage: a retrospective cohort study of agranulocytosis and pancytopenia involving 50,385 patients with Graves' disease. J Clin Endocrinol Metab 2012; 97(1): E49-E53.
23. Nakamura H, Miyauchi A, Miyawaki N et al. Analysis of 754 cases of antithyroid drug-induced agranulocytosis over 30 years in Japan. J Clin Endocrinol Metab 2013; 98(12): 4776–4783.
24. Takata K, Kubota S, Fukata S et al. Methimazole-induced agranulocytosis in patients with Graves' disease is more frequent with an initial dose of 30 mg daily than with 15 mg daily. Thyroid 2009; 19(6): 559–563.
25. Andersohn F, Konzen C, Garbe E. Systematic review: agranulocytosis induced by nonchemotherapy drugs. Ann Intern Med 2007; 146(9): 657–665.
26. Meyer-Gessner M, Benker G, Lederbogen S et al. Antithyroid drug-induced agranulocytosis: clinical experience with ten patients treated at one institution and review of the literature. J Endocrinol Invest 1994; 17(1): 29–36.
27. Abraham P, Acharya S. Current and emerging treatment options for Graves' hyperthyroidism. Ther Clin Risk Manag 2010; 6 : 29–40.
28. Ahmed K, Rao S, Simha V. Antineutrophil cytoplasmic antibody-positive vasculitis in a patient with graves disease: cross-reaction between propylthiouracil and methimazole. Endocr Pract 2010; 16(3): 449–451.
29. Bahn RS, Burch HS, Cooper DS et al. The Role of Propylthiouracil in the Management of Graves' Disease in Adults: report of a meeting jointly sponsored by the American Thyroid Association and the Food and Drug Administration. Thyroid 2009; 19(7): 673–674.
30. Vilchez FJ, Torres I, Garcia-Valero A et al. Concomitant agranulocytosis and hepatotoxicity after treatment with carbimazole. Ann Pharmacother 2006; 40(11): 2059–2063.
31. Woeber KA. Methimazole-induced hepatotoxicity. Endocr Pract 2002; 8(3): 222–224.
32. Kaňová N. Tyreostatika stále aktuální. DMEV 2007; 10(1): 37–42.
33. Tajiri J, Noguchi S, Murakami T et al. Antithyroid drug-induced agranulocytosis. The usefulness of routine white blood cell count monitoring. Arch Intern Med 1990; 150(3): 621–624.
34. Dai WX, Zhang JD, Zhan SW et al. Retrospective analysis of 18 cases of antithyroid drug (ATD)-induced agranulocytosis. Endocr J 2002; 49(1): 29–33.
35. Pearce SH. Spontaneous reporting of adverse reactions to carbimazole and propylthiouracil in the UK. Clin Endocrinol (Oxf) 2004; 61(5): 589–594.
36. Fukata S, Kuma K, Sugawara M. Granulocyte colony-stimulating factor (G-CSF) does not improve recovery from antithyroid drug-induced agranulocytosis: a prospective study. Thyroid 1999; 9(1): 29–31.
37. Andres E, Kurtz JE, Perrin AE et al. Haematopoietic growth factor in antithyroid-drug-induced agranulocytosis. QJM 2001; 94(8): 423–428.
Štítky
Diabetologie Endokrinologie Interní lékařství
Článek vyšel v časopiseVnitřní lékařství
Nejčtenější tento týden
2014 Číslo 10- Trombóza portální žíly jako komplikace infekce COVID-19 – kazuistika
- Přínos perorálního semaglutidu pro pacienty s DM 2. typu v ordinaci praktického lékaře
- Neuropatie u diabetu: Proč ji nepřehlédnout a kdy myslet i na deficit vitaminů B?
- Úloha růstového faktoru TGF-β v procesu hojení ran
- Topicky aplikovaný propolis může urychlovat hojení diabetických bércových vředů
-
Všechny články tohoto čísla
- Výskyt agranulocytózy po tyreostaticích v kohortě pacientů s Gravesovou nemocí léčených radioaktivním jodem 131I v průběhu 14 let – editorial
- Czech TAVI Registry. Potrebujeme registre? – editorial
- Léčba obezity u osob s diabetem 2. typu – editorial
- Léčba bortezomibem u pacientů s onemocněním z depozice lehkých řetězců imunoglobulinu
- Infekční endokarditidy v okrese Tábor v letech 2009–2013
- Výskyt agranulocytózy po tyreostaticích v kohortě pacientů s Gravesovou nemocí léčených radioaktivním jodem 131I v průběhu 14 let
- Uživatelské výstupy z národního registru katetrových implantací aortální chlopně (Czech TAVI Registry): možnosti analytických výstupů založených na databázovém systému TrialDB2
- Terapeutické monitorování vankomycinu v rutinní klinické praxi
- Plicní hypertenze – patofyziologické mechanizmy
- Monoklonální gamapatie nejistého významu a asymptomatický mnohočetný myelom z pohledu roku 2014
- Asociace aterotrombózy a trombofilie – genetické aspekty
- Optimální způsob podání vysokodávkového i.v. furosemidu – kontinuálně nebo bolusově?
- Dna a kardiovaskulární riziko
- Jak se mění možnosti léčby obézních diabetiků 2. typu
- Aktualizované stanovisko České společnosti pro hypertenzi k provádění renálních denervací u rezistentní hypertenze
- Jiří Gallo. Osteoartróza. Průvodce pro každodenní praxi.
- Vnitřní lékařství
- Archiv čísel
- Aktuální číslo
- Pouze online
- Informace o časopisu
Nejčtenější v tomto čísle- Terapeutické monitorování vankomycinu v rutinní klinické praxi
- Optimální způsob podání vysokodávkového i.v. furosemidu – kontinuálně nebo bolusově?
- Monoklonální gamapatie nejistého významu a asymptomatický mnohočetný myelom z pohledu roku 2014
- Dna a kardiovaskulární riziko
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



