-
Články
Top novinky
Reklama- Vzdělávání
- Časopisy
Top články
Nové číslo
- Témata
Top novinky
Reklama- Kongresy
- Videa
- Podcasty
Nové podcasty
Reklama- Práce v oboru
Doporučené pozice
Reklama- Praktické
Top novinky
ReklamaDiagnostika a léčba systémové AL amyloidózy
Vyšlo v časopise: Transfuze Hematol. dnes,28, 2022, No. Supplementum 1, p. 6-40.
Kategorie: Doporučené postupy
Doporučení vypracovaná Českou myelomovou skupinou (CMG), Myelomovou sekcí České hematologické společnosti ČLS JEP.
Na vytvoření tohoto doporučení se podíleli členové České myelomové skupiny, Myelomové sekce ČHS v uvedeném pořadí:
Hlavní autoři
MUDr. Tomáš Pika, Ph.D.
Hemato-onkologická klinika, LF UP a FN Olomouc
prof. MUDr. Roman Hájek, CSc.
Klinika hematoonkologie, LF OU a FN Ostrava
Spoluautoři
Na vytvoření tohoto doporučení se podíleli spoluautoři uvedení v abecedním pořadí:
MUDr. Patrik Flodr, Ph.D.
Ústav klinické a molekulární patologie, LF UP a FN Olomouc
MUDr. Pavla Flodrová, Ph.D.
Ústav klinické a molekulární patologie, LF UP Olomouc
Mgr. Dušan Holub, Ph.D.
Ústav molekulární a translační medicíny, LF UP Olomouc
MUDr. Tomáš Jelínek, Ph.D.
Klinika hematoonkologie, LF OU a FN Ostrava
Mgr. Zuzana Chyra, Ph.D.
Klinika hematoonkologie, LF OU a FN Ostrava
prof. MUDr. Vladimír Maisnar, Ph.D., MBA
4. Interní hematologická klinika LF UK a FN Hradec Králové
prof. MUDr. Luděk Pour, Ph.D.
Interní hematologická a onkologická klinika, LF MU a FN Brno
prof. MUDr. Romana Ryšavá, CSc.
Klinika nefrologie 1. LF UK a VFN v Praze
prof. MUDr. Ivan Špička, CSc.
1. Interní klinika – klinika hematologie, 1. LF UK a VFN v Praze
Recenzenti
prof. MUDr. Romana Ryšavá, CSc.
Klinika nefrologie 1. LF UK a VFN v Praze
prof. MUDr. Zdeněk Adam, CSc.
Interní hematologická a onkologická klinika LF MU a FN Brno
Obsah
Souhrn doporučení
1. Metodické postupy tvorby doporučení
1. 1. Úvod k amyloidózám
2. Charakteristika, výskyt a epidemiologie systémové AL amyloidózy
2.1. Charakteristika AL amyloidózy
2.2. Výskyt a epidemiologie
2.3. Patogeneze systémové AL amyloidózy
3. Klinický obraz systémové AL amyloidózy
3.1. Nejčastější projevy, které jsou indikací k dalšímu vyšetření
3.2. Nejvýznamnější klinické projevy amyloidózy
4. Vyšetřovací techniky u systémové AL amyloidózy
4.1. Přehled vyšetřovacích metod
4.2. Standardní techniky v diagnostice systémové AL amyloidózy
4.3. Speciální diagnostické techniky u systémové AL amyloidózy
5. Diagnostická kritéria a postupy u systémové AL amyloidózy
5.1. Diagnostická kritéria
5.2. Diagnostická kritéria postižení jednotlivých orgánových systémů u systémové AL amyloidózy
5.3. Diagnostický algoritmus systémové AL amyloidózy
6. Diferenciální diagnostika systémové AL amyloidózy
7. Prognostické faktory a klinická stratifikace systémové AL amyloidózy
7.1. Prognostické faktory
7.2. Klinická stratifikace
8. Systémová AL amyloidóza a mnohočetný myelom
9. Doporučení pro diagnostiku AL amyloidózy
10. Ložisková AL amyloidóza
10.1. Etiopatogeneze, diagnostika a klinický obraz
10.2. Léčba ložiskové AL amyloidózy
11. Cíle léčby a hodnocení léčebné odpovědi u AL amyloidózy
12. Léčebné strategie u AL amyloidózy v roce 2018
13. Autologní transplantace krvetvorných buněk (ASCT)
13.1 Léčebná účinnost vysokodávkované chemoterapie s následnou ASCT
14. Konvenční léčba založená na kombinaci vysokých dávek dexametazonu a alkylačních cytostatik
14.1. Kombinace alkylačního cytostatika a kortikoidu
14.2. Nežádoucí účinky léčby a selekce nemocných
15. Imunomodulační léky v terapii AL amyloidózy
15.1. Thalidomid v léčbě AL amyloidózy
15.2. Lenalidomid v léčbě AL amyloidózy
15.3. Pomalidomid v léčbě AL amyloidózy
16. Inhibitory proteasomu v léčbě AL amyloidózy
16.1. Bortezomib v léčbě AL amyloidózy
16.2. Ixazomib a carfilzomib v léčbě AL amyloidózy
17. Daratumumab v léčbě AL amyloidózy
18. Venetoclax v léčbě AL amyloidózy
19. Doxycyklin v léčbě AL amyloidózy
20. Léčba relabujících a refrakterních pacientů
21. Perspektivy v léčbě AL amyloidózy
22. Transplantace srdce, případně jiných orgánů, následovaná vysokodávkovanou chemoterapií s autologní transplantací krvetvorných buněk
23. Podpůrná péče při léčbě AL amyloidózy
24. Doporučení pro léčbu AL amyloidózy
Souhrn doporučení 2022
A. Doporučení pro diagnostiku AL amyloidózy
- Systémová AL amyloidóza (ALA) je vzácné hematologické onemocnění patřící mezi monoklonální gamapatie.
- Optimální péče o nemocné s ALA je založena na časné diagnóze s vyhodnocením závažnosti orgánového postižení, účinné terapii zaměřené zejména na snížení produkce amyloidogenních lehkých řetězců a léčbě podpůrné.
- V 12–20 % je asociována s jinou formou monoklonální gamapatie či B-lymfoproliferativního onemocnění.
- Amyloidóza musí být vždy histologicky verifikována spolu s potvrzením AL typu amyloidu.
- Podkladem onemocnění je depozice amyloidu v orgánech a tkáních, což vede k jejich funkčnímu postižení nebo i selhání. Pečlivé posouzení orgánového postižení je základním pilířem diagnostiky a stratifikce nemocných.
- Detekce a kvantifikace monoklonálního imunoglobulinu a zejména hladin volných lehkých řetězců patří mezi stěžejní aspekty diagnostiky a sledování nemocných se systémovou ALA.
B. Doporučení pro léčbu AL amyloidózy
- Principem léčby je eliminace patologického klonu se zastavením produkce amyloidogenních lehkých řetězců, redukcí jejich sérových hladin s cílem dosažení alespoň velmi dobré parciální hematologické remise (úroveň důkazu IIa, stupeň doporučení B).
- Dosažení hematologické léčebné odpovědi je podmínkou pro zlepšení funkce postižených orgánů a dosažení tzv. orgánové léčebné odpovědi (úroveň důkazu IIa, stupeň doporučení B).
- Léčba je volena individuálně s využitím „risk-adapted“ strategie (úroveň důkazu IV, stupeň doporučení C).
- Pouze část nemocných s ALA splňující výběrová kritéria je možno bezpečně léčit vysokodávkovanou terapií s podporou autologního štěpu, tito nemocní s nízkou mírou orgánového postižení z této terapie profitují (úroveň důkazu IIa, stupeň doporučení B).
- Režim daratumumab-CyBorD je indikován jako terapie první linie pro nemocné s nově diagnostikovanou ALA (úroveň důkazu Ib, stupeň doporučení A).
- Režim BMDex je považován za standard pro nově diagnostikované pacienty s ALA, kteří nejsou referováni k ASCT a u kterých není možné užít režim s daratumumabem (úroveň důkazu Ib, stupeň doporučení A).
- Kombinovaná schémata s bortezomibem jsou vhodnými léčebnými režimy pro všechny nově diagnostikované nemocné, bez ohledu na to, zda jsou či nejsou vhodnými kandidáty vysokodávkované terapie (úroveň důkazu IIa, stupeň doporučení B). Kombinovaná schémata s bortezomibem jsou vhodnými léčebnými režimy pro relabující nemocné (úroveň důkazu IIa, stupeň doporučení B).
- Ixazomib s dexametazonem a ev. cyklofosfamidem je indikován v léčbě nemocných s relabující/refrakterní amyloidózou a u nemocných v 1. linii terapie s preexistující neuropatií, kteří nejsou vhodní k terapii bortezomibem (úroveň důkazu IIa, stupeň doporučení B).
- Daratumumab v monoterapii či kombinovaných schématech je indikován u nemocných s refrakterní/relabující ALA (úroveň důkazu IIa, stupeň doporučení B).
- Schémata s imunomodulačními látkami jsou indikována u relabujících/refrakterních nemocných (úroveň důkazu IIa, stupeň doporučení B).
- Venetoclax je možno užít v terapii relabujících/refrakterních ALA nemocných s prokázanou t (11; 14) (úroveň důkazu IIa, stupeň doporučení B).
- Multioborová spolupráce při péči o nemocné s ALA je naprosto nezbytná.
1. METODICKÉ POSTUPY TVORBY DOPORUČENÍ
Předložené doporučení bylo vypracováno na základě medicíny založené na důkazech s cílem popsat všechny důležité oblasti diagnostiky a léčby ALA. Úrovně důkazů a stupně doporučení standardně používané v guidelines jsou uvedeny v tab. 1.
Tab. 1. Úrovně důkazu a stupně doporučení používané ve směrnicích (guidelines) a principech medicíny založené na důkazech (evidence based medicine). 
1.1. Úvod k amyloidózám
Amyloidózy představují heterogenní skupinu onemocnění charakterizovanou přítomností depozit amyloidu, amorfního bílkovinného materiálu uloženého extracelulárně v tkáních. Každý typ amyloidu má svůj specifický fibrilární prekurzorový protein, od něhož se odvíjí i jeho název, např. u familiární transthyretinové amyloidózy jde o molekuly mutovaného transthyretinu (mTTR), u AL amyloidózy jde o strukturálně aberantní molekuly lehkého řetězce imunoglobulinu (AL) [Kyle, 1995a; Dispenzieri, 2012]. Podle příčiny produkce amyloidogenního prekurzoru se rozlišují formy získané a hereditární, jež jsou spojeny s mutací genu zodpovědného za syntézu daného prekurzoru. Amyloidóza se vyskytuje ve formě lokalizované s pouze ložiskovou depozicí amyloidu, mnohem častější je ale forma systémová, vyznačující se postižením více orgánů a tkání. V současnosti zahrnuje členění založené na typu amyloidových prekurzorů 36 typů, v případě mTTR amyloidózy dalších > 100 variant [Sipe, 2016; Ryšavá, 2013; Benson, 2020]. Pro potřeby běžné medicínské praxe postačuje jednoduché, klinicky orientované, dělení (tab. 2) [Kyle, 1995a; Falk, 1997; Hassan, 2005].
Tab. 2. Zjednodušená klasifikace nejčastějších typů amyloidóz [Kyle, 1995a; Sipe, 2016, Benson, 2020]. ![Zjednodušená klasifikace nejčastějších typů amyloidóz [Kyle, 1995a; Sipe, 2016, Benson, 2020].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/9e0576f8f710bd0d8cf12a63da0f5614.jpg)
Z hlediska výskytu je nejčastější systémová AL amyloidóza (70 %), méně častá je její ložisková forma (19 %), zatímco ostatní typy amyloidóz se vyskytují mnohem vzácněji, např. senilní a familiární ve 4 % a AA amyloidóza jen ve 3 % [Kyle, 1992, 1995a]. Historické názvosloví, rozpoznávající pouze amyloidózu primární (AL typ) a amyloidózu sekundární (AA typ), se v současnosti již prakticky nepoužívá. Vzhledem k občasnému výskytu a zejména nízké informovanosti lékařů uniká i v současnosti amyloidóza časnému rozpoznání a většinou jsou podchyceny až pokročilé fáze nemoci se závažným, často i nevratným, poškozením životně důležitých orgánů. Amyloidóza se vyznačuje sklonem k trvalé progresi a nepříznivé prognóze, neboť všechny typy amyloidózy jsou doposud léčebně jen omezeně ovlivnitelné [Gertz, 2009; Ryšavá, 2013].
2. CHARAKTERISTIKA, VÝSKYT A EPIDEMIOLOGIE SYSTÉMOVÉ AL AMYLOIDÓZY
2.1. Charakteristika
Systémová AL amyloidóza (ALA) je onemocnění vyznačující se pozvolnou monoklonální proliferací plazmocytů v kostní dřeni („plazmocelulární dyskrazie“) provázenou lineární tkáňovou depozicí bílkovinného nerozpustného fibrilárního materiálu, tj. amyloidu, jehož prekurzorem jsou lehké řetězce (LŘ) monoklonálního imunoglobulinu (MIg) l (3× častěji) nežli k, nebo jejich fragmenty, jež jsou prokazatelné v séru a/nebo v moči. Název AL amyloidóza odpovídá charakteru prekurzorového proteinu, tj. A – amyloid, L – lehké řetězce MIg [Bird, 2004; Ščudla, 2009; Gertz, 2009]. Progresivní extracelulární akumulace AL amyloidu v cévní a parenchymové složce životně důležitých orgánů vede k tkáňové dezorganizaci s úbytkem normálních elementů a k progresivní poruše funkce zejména srdce, ledvin, jater, zažívacího traktu, periferního i autonomního nervového systému aj., avšak s výjimkou CNS. Depozita AL amyloidu vyvolávají pouze malou, případně žádnou, místní tkáňovou reakci, takže neexistuje přímá souvislost mezi tíží amyloidových depozit a závažností orgánové dysfunkce. Za narušení, případně selhání, funkce orgánů, v případě závažného postižení srdce i smrt, je odpovědná i vysoká tkáňová toxicita amyloidogenních lehkých řetězců [Rajkumar, 2007]. Optimální péče o nemocné s ALA je založena na časné diagnóze s vyhodnocením závažnosti orgánového postižení, účinné terapii zaměřené zejména na snížení produkce amyloidogenních LŘ a léčbě podpůrné. Díky prohloubení znalostí charakteristiky ALA dochází v posledních letech i ke zlepšení léčebných výsledků vyznačujících se zlepšením funkce postižených orgánů a prodloužením délky i kvality života nemocných s touto závažnou, život ohrožující, chorobou.
2.2. Výskyt a epidemiologie
AL amyloidóza je nejčastějším typem systémové amyloidózy. Její incidence je v USA odhadována na 5,1–12,8 nemocných na 1 milion obyvatel/rok [Kyle, 1992], v Evropě na 0,8–1,0/100 000 obyvatel/rok [Merlini, 2007]. Systémová ALA postihuje především jedince vyššího věku, v 66 % jde o nemocné mezi 50–70 lety, 17 % je mladší než 50 let a pouze 4 % je mladších 40 let, přičemž poněkud častěji jsou postiženi muži [Kyle,1995b; Bird, 2004].
U systémové ALA se setkáváme s přibližně následujícím zastoupením jednotlivých imunochemických typů MIg: IgG 35 %, IgA 10 %, IgM 5 %, IgD 1 %, ve zbývajících případech jde o přítomnost LŘ l nebo k. Ve 12–20 % provází systémová ALA mnohočetný myelom (MM), méně často Waldenströmovu makroglobulinémii (MW) a jen vzácně ostatní lymfoproliferativní stavy.
2.3. Patogeneze
Patogeneze ALA je složitá a doposud nebyla zcela objasněna. Základní příčinou je porucha funkce zvolna proliferujících monoklonálních plasmocytů produkujících klonální lehký řetězec s patologickou konformací (misfolded) mající amyloidogenní potenciál. K tvorbě AL amyloidu dochází v důsledku tvorby makromolekulárních agregátů bílkovinného fibrilárního materiálu za spoluúčasti kodepozice kofaktorů nefibrilárního charakteru. Všechny typy amyloidových depozit obsahují glykoprotein SAP (serum amyloid P komponenta), který je vysoce odolný proti proteolýze podílející se na rezistenci fibril amyloidu vůči degradaci. Nelze rovněž pominout vliv tkáňového mikroprostředí ovlivňujícího biochemické charakteristiky amyloidogenních LŘ i cytotoxický potenciál solubilních oligomerů [Merlini, 2007]. Dokladem toxicity amyloidových prekurzorů (např. LŘ) je klinické pozorování, že ke zlepšení orgánové funkce (např. poklesu NT-proBNP) dochází již záhy po nasazení terapie, tedy v příliš krátkém intervalu pro uplatnění resorpce fibrilárních depozit [Palladini, 2006].
3. KLINICKÝ OBRAZ SYSTÉMOVÉ AL AMYLOIDÓZY
3.1. Nejčastější projevy nemoci, které jsou indikací k dalšímu vyšetření
Vlastní projevy nemoci jsou velmi pestré a individuálně značně rozdílné, v závislosti na typu a závažnosti postižení orgánů. Pravidelnou součástí klinického obrazu jsou jednak celkové nespecifické projevy, tj. slabost, malátnost, únavnost, snížení chuti k jídlu a úbytek hmotnosti, jednak pestré projevy vyplývající z postižení jednotlivých orgánů a tkání [Bird, 2004; Ščudla, 2009]. Lze je rozdělit na příznaky subjektivní a objektivní, ovšem velmi důležitou manifestací jsou projevy charakteru různých klinických syndromů, jejichž diagnostické řešení může přivést lékaře ke kauzální diagnóze (tab. 3) [Bird, 2004; Gertz, 2005 a 2009; Ščudla, 2009; Ryšavá, 2013].
Tab. 3. Klinické projevy systémové AL amyloidózy [Bird, 2004; Gertz, 2009; Ryšavá, 2013]. ![Klinické projevy systémové AL amyloidózy [Bird, 2004; Gertz, 2009; Ryšavá, 2013].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/f5224832615beda655358a817725fb05.jpg)
DKK – dolní končetiny, GIT – gastrointestinální trakt, sy. – syndrom V souboru 868 nemocných se systémovou ALA byl zaznamenán výskyt slabosti v 68 %, edémy v 62 %, pokles hmotnosti v 43 %, dušnost v 40 %, ortostatická hypotenze v 27 %, dysestezie a parestezie v 23 %, dysgeusie v 18 %, makroglosie v 14 %, kožní purpura v 11 % a průjem v 9 % případů, zatímco projevy přímého postižení CNS jsou pro neprostupnost hematoencefalické bariéry vzácné [Merlini, 2007].
Postižení jednoho orgánu se vyskytuje v 25 %, dvou v 36 %, tři a více orgánů u 39 % nemocných, zatímco amyloidová nefropatie v 72 %, kardiomyopatie v 63 %, postižení jater v 27 %, periferní neuropatie v 19 %, postižení autonomního nervstva v 16 %, postižení měkkých tkání v 12 % a amyloidová kožní purpura v 11 % [Merlini, 2007]. Bylo zjištěno, že nemocní se systémovou ALA a přítomností MIg typu IgM mají oproti IgG typu poněkud odlišný klinický obraz: u poloviny nemocných jsou nejčastěji postiženy ledviny a měkké tkáně, častěji, a to v 21 %, jsou postiženy lymfatické uzliny a respirační aparát, naopak méně často, a to v 36 %, je postiženo srdce. U více než poloviny nemocných jsou při diagnóze známky postižení více než 2 orgánů a v 73 % infiltrace kostní dřeně lymfoplasmocytárními elementy [Wechalekar, 2008]. Nemocní s přítomností IgD typu M-proteinu se pak vyznačují nízkým výskytem postižení ledvin a srdce [Gertz, 2012].
3.2. Nejvýznamnější klinické projevy AL amyloidózy
3.2.1. Amyloidóza ledvin
Postižení funkce ledvin, zejména jejich glomerulárních funkcí, je nejčastějším ale málo specifickým projevem a nezávisí pouze na přítomnosti amyloidových depozit, ale i na stupni intersticiální fibrózy a tubulární atrofie [Bohle, 1993]. Klíčovým projevem vedoucím obvykle k odhalení ALA je výrazná proteinurie charakteru nefrotického syndromu (NS), vyznačujícího se navíc hypoalbuminémií, hyperhydratací, generalizovanými otoky vč. ascitu, pleurálního a perikardiálního výpotku, tj. případnou anasarkou s enormním nárůstem hmotnosti o 15–20 kg [Ryšavá, 2013]. Perzistentní NS se současným selháním ledvin a se zvětšením jejich velikosti je pro amyloidovou nefropatii velmi sugestivní. Dokud nedojde k infiltraci intrarenálních cévních struktur amyloidem, není přítomna arteriální hypertenze, která navíc nepatří do klinického obrazu amyloidové nefropatie [Dember, 2010]. Celkový katabolismus s negativní dusíkovou bilancí vede ke ztrátě svalové hmoty spojené s hypotonií a atrofií svalstva. NS se může v důsledku ztrát imunoglobulinů močí komplikovat zvýšeným výskytem infekcí, ale i tromboembolickou nemocí s trombózou renálních žil. Hyperlipoproteinémie provázená xantelasmaty víček a/nebo oblasti extenzorů vede k projevům akcelerované aterosklerózy, ztráta transferinu močí bývá jednou z příčin refrakterní anémie. Jen zřídka dochází k manifestaci Fanconiho syndromu (postižení proximálního tubulu), zatímco nefrogenní diabetes insipidus (postižení distálního tubulu) je spíše výrazem koincidence s MM [Ryšavá, 2013; Ryšavá 2019a].
3.2.2. Amyloidóza srdce
Postižení srdce u systémové ALA je velmi časté a při diagnóze bývá přítomno u více než 2/3 nemocných. Při autopsii se nacházejí myokardiální depozita AL amyloidu prakticky vždy, samotné izolované postižení myokardu je ale vzácné, pouze v 5 %. Depozita amyloidu vedou k progresivnímu zesílení stěn obou komor, což porušuje plnění srdce v průběhu diastoly, vzniká tedy obraz restriktivní, resp. hypertrofické kardiomyopatie. Infiltrace chlopenního a závěsného aparátu amyloidem může navodit chlopenní vady charakteru mitrální a trikuspidální insuficience, vzácně lze pozorovat perikarditidu, zcela raritně byla popsána ruptura stěny pravé komory. Manifestní srdeční selhání je vedoucím příznakem u 25 % nemocných, přičemž v popředí klinického obrazu jsou zejména projevy pravostranné srdeční slabosti nebo známky sníženého srdečního výdeje vedoucího k poklesu krevního tlaku, což spolu s projevy autonomní neuropatie vede k ortostatické a/nebo chronické hypotenzi a k častým synkopálním stavům. Projevy iniciálně diastolické, posléze i systolické, dysfunkce vedou nakonec k rozvoji globálního srdečního selhání s nízkou tolerancí tělesné zátěže, dušností, výskytu periferních otoků a nakonec i ascitu, pleurálnímu výpotku a anasarky. Častým projevem jsou i palpitace, synkopy v rámci rytmických poruch, např. supraventrikulární arytmie, syndrom chorého sinu a A-V blokády. Nepříliš časté jsou anginózní bolesti při postižení drobných koronárních tepen depozity amyloidu a aterosklerózou. I v současnosti platí, že postižení srdce amyloidem je nejvýznamnější prognostický faktor, jenž má vliv na volbu léčebné strategie a na délku celkového přežití [Kyle, 1986]. Nejčastější příčinou smrti u systémové AL amyloidózy je pokročilé, léčebně refrakterní, srdeční selhání, náhlá smrt v důsledku elektromechanické disociace nebo maligní komorová arytmie [Pika, 2008; Fikrle, 2013; Paleček, 2015, Quarta 2012; Rajkumar, 2013].
3.2.3. Periferní a autonomní neuropatie
Periferní neuropatie se projevuje širokou škálou příznaků, přičemž postižení hlavových nervů je vzácné. Dostavuje se obvykle záhy v oblasti DKK a se značným předstihem před vlastním rozpoznáním ALA. Je zpravidla axonální, charakteru distální smíšené, symetrické, periferní neuropatie projevující se přítomností dysestezie, parestézií s progresivní ztrátou citlivosti, trnutím a svalovou slabostí [Gertz, 2009]. Senzitivní neuropatie je obvykle symetrická, někdy značně bolestivá, zatímco motorická neuropatie je podstatně vzácnější. Do klinického obrazu patří i „syndrom neklidných nohou“. Častým projevem je syndrom karpálního tunelu, nezřídka předcházející ostatní projevy AL amyloidózy o několik let, vznikající v důsledku depozit amyloidu v oblasti vazů karpálního tunelu. Přítomný edém a útlak n. medianus se projevuje především nočními parestéziemi v oblasti dlaní, palce, ukazováku a prostředníčku s atrofií svalů v oblasti tenaru a hypotenaru [Kyle, 1995a].
Autonomní neuropatie je často v popředí klinického obrazu, neboť se vedle postižení srdce a hypokortikalismu podílí na rozvoji posturální hypotenze, kdy systolická hodnota TK se snižuje v ortostáze v odstupu 3–5 minut polohy ve stoje o > 20 mm Hg, obvykle na < 90 mm Hg. Projevuje se rovněž poruchou motility GIT s časným falešným pocitem sytosti a dysgeuzií, u mužů erektilní i ejakulační dysfunkcí, dysfunkcí močového měchýře s obtížným vyprazdňováním, ale i anhidrózou.
3.2.4. Amyloidóza GIT a jater
Gastrointestinální projevy vznikají v důsledku depozice amyloidu ve stěně GIT a v důsledku poruchy vegetativního systému. Nápadným, do jisté míry i příznačným, projevem AL amyloidózy je makroglosie způsobená imbibicí jazyka amyloidem. Vzhledem k dominantnímu postižení kořene jazyka může vést nejen k poruše polykání, ale i k výraznému zúžení dýchacích cest. Dyspeptický syndrom, dostavující se v důsledku gastroparézy, bývá spojen s pocity předčasné sytosti, nauseou a zvracením, postižení nižších etáží se vyznačuje bolestí břicha, obstipací (pseudoobstrukce), ale i obrazem explozivního postprandiálního průjmu s malabsorpcí a s úbytkem hmotnosti. V rámci amyloidózy GIT byla popsána i perforace střeva, střevní infarzace a výrazné krvácení z distálních oblastí zažívací trubice jako důsledek zvýšené fragility cév. Zvětšení jater s pozitivitou jaterních testů, zejména jaterní frakce alkalické fosfatázy, a portální hypertenze s ascitem a splenomegalií se vyskytují asi u čtvrtiny nemocných [Bird, 2004; Ryšavá, 2019b].
3.2.5. Postižení ostatních orgánů a tkání
Postižení dýchacích cest a plic se projevuje kašlem, dušností a hemoptýzou. Infiltrace stěny laryngu vede k obstrukci horních dýchacích cest, inspirační dušnosti a postižení hlasivek s dysfonií. Vzácně lze zachytit ložiskové nodulární postižení plic („coin lession“ resp. amyloidom) a/nebo amyloidovou infiltraci tracheobronchiálního stromu, vedoucí ke známkám obstrukce, zatímco postižení pleury se vyznačuje přítomností torpidního pleurálního výpotku.
Poměrně časté jsou i poruchy hemostázy, asi u čtvrtiny nemocných. Nejčastěji je přítomna vaskulární kožní purpura, např. periorbitální nebo v oblasti hřbetu rukou a předloktí, tzv. „syndrom červených očí“ v důsledku postižení cév spojivkového vaku s vývinem subkonjunktivální sufuze nebo slizniční krvácení v různých oblastech jako důsledek zvýšené fragility cév při subendoteliální depozici amyloidu. Na projevech hemoragické diatézy se může podílet i snížení počtu krevních destiček při splenomegalii a významné snížení hladiny faktoru X vedoucí k život ohrožujícímu krvácení po jaterní nebo renální biopsii [Bird, 2004; Mumford, 2000]. Makroskopická hematurie může být výsledkem výše uvedených poruch hemostázy, ale i důsledkem infiltrace vývodných močových cest amyloidem.
Postižení různých orgánů a tkání. Infiltrace nadledvin amyloidem se projevuje adrenální insuficiencí s obrazem Addisonovy choroby, inbibice štítné žlázy hypotyreózou. K vzácným projevům ALA patří umístění amyloidových depozit v oblasti očních spojivek, sklér, víček a orbity. Infiltrace lymfatických uzlin se manifestuje zvětšením uzlin, amyloidová myopatie svalovou slabostí v důsledku poškození a imbibice příčně pruhovaného svalstva amyloidem, depozita amyloidu v synovii a přilehlých kloubních strukturách obrazem neerozivní symetrické artropatie s predilekčním postižením ramenních, zápěstních, drobných ručních a kolenních kloubů. Postižení kůže se manifestuje jejím ztluštěním, případně přítomností papul a plaků, vzácně obrazem napodobujícím sklerodermii, postižení nehtů se ohlašuje onychodystrofií [Kyriakides, 2002].
4. VYŠETŘOVACÍ TECHNIKY U SYSTÉMOVÉ AL AMYLOIDÓZY
4.1. Přehled vyšetřovacích metod
Vzhledem k neuspokojivým výsledkům léčby pokročilé fáze systémové ALA je naléhavým požadavkem rozpoznat onemocnění již v jeho počáteční fázi. Klíčovým předpokladem správné diagnózy je požadavek, aby lékaři v klinické praxi na toto onemocnění mysleli. K podezření na diagnózu ALA by měla vést zejména přítomnost nefrotického syndromu s případnou renální insuficiencí, nedilatační kardiomyopatie, nejasné periferní a/nebo autonomní neuropatie a ostatních klinických syndromů, resp. mnohotvárných subjektivních příznaků a objektivních příznaků (tab. 3, kap. 3. Klinický obraz systémové AL amyloidózy). Za těchto okolností je povinností lékaře pátrat po přítomnosti MIg standardní a imunofixační elektroforézou séra, resp. zvýšených hladinách volných lehkých řetězců (FLC) vč. patologie poměru k/l a v případě jejich přítomnosti odeslat nemocného k dovyšetření na nejbližší hematologické oddělení [Bird, 2004; Ščudla, 2009; Gertz, 2009, 2010, 2016]. Včasné rozpoznání systémové ALA vyžaduje vedle dobré znalosti nemoci i notnou dávku diagnostické invence. Přehled základních i výběrově indikovaných vyšetření při podezření na systémovou ALA je uveden v tab. 4 [Dispenzieri, 2012, Gillmore, 2014], vlastní diagnostický algoritmus je shrnut v tab. 5 (kap. 5 Diagnostická kritéria a postupy u systémové AL amyloidózy).
Tab. 4. Přehled vyšetření nezbytných pro diagnózu a určení stadia AL amyloidózy [volně dle Dispenzieri, 2012; Gillmore, 2014]. ![Přehled vyšetření nezbytných pro diagnózu a určení stadia AL
amyloidózy [volně dle Dispenzieri, 2012; Gillmore, 2014].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/21ae7333de1c9f558521eb32cd710777.jpg)
CT – počítačová tomografie, DPD scan – scintigrafie s užítím kyseliny 3,3-difosfo- -no-1,2-propanodikarboxylové, EKG – elektrokardiografie, EMG – elektromyografie, FLC – volné lehké řetězce imunoglobulinu, GIT – gastrointestinální trakt, HRCT – „high resolution“ počítačová tomografie, M-FC – multiparametrická průtoková cytometrie, MRI – magnetická rezonance, NT-proBNP – propeptid mozkového natriuretického peptidu, PET/CT – pozitronová emisní tomografie/počítačová tomografie, RTG – standardní radiografie Tab. 5. Diagnostická kritéria systémové AL amyloidózy dle IMWG [upraveno dle Rajkumar, 2011; Gertz, 2016]. ![Diagnostická kritéria systémové AL amyloidózy dle IMWG
[upraveno dle Rajkumar, 2011; Gertz, 2016].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/a46b9a25d4a831cc54c895159b9824b5.jpg)
FLC – volné lehké řetězce, GIT – gastrointestinální trakt, IMWG – International Myeloma Working Group, M-FC – multiparametrická průtoková cytometrie 4.2. Standardní techniky v diagnostice systémové AL amyloidózy
4.2.1. Diagnostika amyloidu z pohledu patologa
Amyloidem nazýváme substanci tvořenou amyloidotvorným fibriláním proteinem a dalšími přídatnými složkami (serový amyloidový protein P, lipoproteiny, glykosaminoglykany, proteoglykany) [Pepys, 2006; Vrana, 2009; Vrana, 2014; D’Souza, 2013]. Amyloidotvorný fibrilární protein nabývá vzhledu rigidních nevětvících se fibril průměru přibližně 10 nm, které jsou nerozpustné a jsou výsledkem změn v uspořádání proteinových molekul.
V běžné morfologické praxi se s amyloidem setkáváme v základním a speciálním histologickém barvení, v imunohistochemii, imunofluorescenci, méně často se využívá elektronové mikroskopie. Mezi další užitečné metody sloužící k identifikaci amyloidových fibril patří Western blotting, sekvenování aminových kyselin a imunoelektronová mikroskopie [Sipe, 2016].
Metody rozdělujeme na detekční – pro zjištění přítomnosti amyloidu (speciální histologické barvení, elektronová mikroskopie), a typizační – pro určení konkrétního typu amyloidotvorného proteinu (imunohistochemie, imunofluorescence, imunoelektronová mikroskopie, proteomická analýza, …). Zájemce o tuto problematiku odkazujeme na uvedenou literaturu a také na text schválený Společností českých patologů ČLS JEP (Minimální požadavky na diagnostický postup pro detekci amyloidu v rámci systémových amyloidóz).
Histologické vyšetření v základním a speciálním barvení – Depozita amyloidu se v základním barvení histologických preparátů (hematoxylin-eozin) znázorní nespecificky, jako amorfní eozinofilní, tj. světle červený materiál. Pro specifické znázornění amyloidu existují speciální barvicí metody, přičemž pro diagnózu nepodkročitelným standardem je celosvětově používané barvení Kongo červení. V jeho výsledku poskytují depozita amyloidu oranžové až červené zbarvení, a to bez závislosti na typu amyloidu [Vacek, 1988]. Při vyšetření polarizačním mikroskopem pozorujeme charakteristické jevy, které dává konžská červeň ve vazbě na amyloid. Tradičně se označují jako dvojlom („birefringence“) a dichroismus „apple-green“ barevného charakteru, avšak jedná se o složité optické jevy komplexního charakteru a výsledné zbarvení může nabývat i jiných odstínů, např. žluté, oranžové či modré [Gertz, 2010; Howie, 2008; Sipe 2016].
Z ostatních speciálních histologických barvicích metod lze použít saturnovou červeň, thioflavin, metylvioleť apod. Lze jen doporučit provádět pro detekci amyloidu spolu s Kongo červení ještě alespoň jednu další speciální barvicí metodu. Speciální barvicí metody dávají dobrý výsledek při klasickém zpracování histologického materiálu – fixace formalinem a zalití do parafinu. Obdobně jako u ostatních barvicích metod dosáhneme kvalitnějšího výsledku barvením zmrazených řezů nefixované tkáně.
Imunohistochemické vyšetření – V současné diagnostice amyloidu zůstává imunohistochemie (IHC) nejvíce dostupnou rutinně používanou metodou, která umožňuje provést vyšetření z materiálu fixovaného formalinem a zalitého do parafinu (FFPE) s příznivými náklady a bez nutnosti pořízení specializovaného přístrojového vybavení.
Do běžné praxe patří vyšetření protilátkami proti k a l lehkých řetězců imunoglobulinů, transthyretinu a amyloidu A, přičemž spektrum komerčně dostupných primárních protilátek i proti vzácným a hereditárním formám amyloidózy se stále rozšiřuje. Depozita všech typů amyloidu obsahují konstantně příměs i jiných molekul, než je samotný amyloidogenní protein, což lze imunohistochemickým průkazem využít v diagnostice (zejm. protilátka proti sérovému amyloidovému proteinu P).
Senzitivita IHC vyšetření amyloidu (zejména AL typu) je ztížena několika okolnostmi. Kromě faktorů preanalytické fáze vyšetření (odběr materiálu, způsob a délka fixace apod.) hraje významnou roli samotný proces tvorby amyloidu (konformační změny s fragmentací lehkých řetězců a maskování antigenu při formování amyloidových fibril), dále přirozená heterogenita lehkých řetězců plynoucí z jejich variabilních domén, mutace amyloidotvorného proteinu a v neposlední řadě příměs séra. Také rozpoznávání epitopů jednotlivými protilátkami může být odlišné. Výše uvedené vede ke skutečnosti, že se závěry studií, které zkoumají spolehlivost IHC vyšetření v určování subtypů amyloidózy, často značně liší. V současné době je možné využít více polyklonálních i monoklonálních protilátek proti epitopům k i l lehkých řetězců. Aplikace více různých protilátek proti lehkým řetězcům imunoglobulinů zvyšuje validitu vyšetření AL amyloidu. Dle jedné ze studií, použití 4 protilátek anti - l v kombinaci se souvisejícími klinickými a laboratorními vyšetřeními přináší senzitivitu 94 % a specificitu 100 % [Schönland, 2012].
Fluorescenční vyšetření – Vyšetření amyloidu pomocí fluorescenčního mikroskopu lze provést pomocí přímé vazby fluorochromu na amyloidová depozita, což nastává v případě barvení parafinového řezu konžskou červení, která sama o sobě je fluorochromem. Ve srovnání s vyšetřením pouze polarizačním mikroskopem vykazuje fluorescenční vyšetření vyšší senzitivitu, zejména v případech málo objemných depozit amyloidu [Marcus, 2012]. Metodou volby je však vyšetření s využitím komerčně dostupných protilátek, které jsou značeny fluorochromem. Pro imunofluorescenci je nutné použít řezy připravené ze zmrazené nefixované tkáně, což vyžaduje přizpůsobit průběh odběrové fáze, neboť transport do laboratoře musí proběhnout bezprostředně po odběru a za odlišných podmínek oproti tkáním standardně zpracovávaným metodou FFPE. V tomto režimu jsou rutinně vyšetřovány vzorky z biopsie ledvin, na některých pracovištích také endomyokardiální biopsie. Imunofluorescenční vyšetření vykazuje vyšší diagnostickou úspěšnost (v různých studiích 67–88 %) [Collins, 2009] ve srovnání s imunohistochemií, nevýhodou a určitou limitací však stále zůstává nutnost použít nefixovaný mražený materiál, neboť amyloid je velmi často náhodným nálezem. V případě vysoké klinické suspekce na amyloid je již při prvním odběru necílené biopsie vhodné poslat do laboratoře část odebraného materiálu také na imunofluorescenční vyšetření. Novou možností vyšetření je metoda, která využívá natrávení parafinových fixovaných vzorků proteázami (protease digested), které lze následně vyšetřit imunofluorescenčně na průkaz depozice lehkých řětezců. Lze tak dodatečně provést imunofluorescenční vyšetření z fixovaných vzorků [Nasr 2006].
Elektronová mikroskopie – Charakteristickou fibrilární strukturu amyloidu lze prokázat vyšetřením elektronovým mikroskopem, který znázorní nevětvené splétající se mikrofibrily šíře 7,5–10 nm tvořící nepravidelnou síť. Stavba jednotlivých fibril se liší v závislosti na amyloidogenním proteinu. Vysoce specializovaná pracoviště mají k dispozici imunoelektronovou mikroskopii, která spojuje výhody vysokého rozlišení elektronového mikroskopu se specificitou reakce antigen-protilátka a umožňuje ověřit kolokalizaci imunohistochemické reakce a amyloidové fibrily [Steusloff, 2000; Arbustini, 2002].
4.2.2. Průkaz MIg a VLŘ v séru a/nebo moči
Detekce a kvantifikace MIg a hladin volných lehkých řetězců (FLC) vč. abnormálního poměru κ/λ patří mezi stěžejní aspekty diagnostiky a sledování nemocných se systémovou ALA. Standardní elektroforéza bílkovin séra (SPE) je stále základní, ovšem málo citlivou, metodou odhalující přítomnost MIg pouze u ~ 50 % AL amyloidóz, přičemž hodnota M-proteinu nebývá vysoká (u ~ 70 % jedinců je < 20 g/l) [Gertz, 2009; Bradwell, 2015]. Proto základním vyšetřením je imunofixační elektroforéza (IFIX) odhalující přítomnost MIg nebo LŘ v 71, resp. 84 %, nikoliv tedy u všech nemocných. Předností IFIX je schopnost detekce kteréhokoliv imunochemického typu MIg, a to i v případě, že se vyskytuje v séru a/nebo v moči v malém množství. Nevýhodou IFE je nemožnost monitorace průběhu léčby, neboť neposkytuje kvantitativní výsledky [Gertz, 2009; Bradwell, 2010; Maisnar, 2012]. Většina nemocných se systémovou ALA se vyznačuje nízkou hladinou nebo absencí intaktního MIg, charakteristické je zvýšení hladiny FLC l nebo k [Bradwell, 2015]. V současnosti je proto již naprosto standardním a neopominutelným postupem kvantitativní stanovení sérové hladiny VLŘ vč. indexu k/l s pomocí nefelometrické nebo turbidimetrické techniky (FreeliteTM), dosahující při kombinaci se SPE a IFIX 98–99 % senzitivity [Gertz, 2009; Bradwell, 2010; Katzmann, 2005; Vávrová, 2012]. Zvýšená hladina FLC v séru spolu s patologií indexu k/l se vyskytuje u ALA v 86–98 % a koreluje s náloží amyloidu [Lachmann, 2003; Comenzo, 2012]. Sledování pohybu sérových hladin FLC u ALA je metodou volby při monitorování a hodnocení hloubky léčebné odezvy, současně hodnota při diagnóze je velmi důležitým prognostickým faktorem s úzkým vztahem k celkovému přežití [Palladini, 2010b]. Rozdíl mezi hladinami postiženého a alternativního řetězce (dFLC – diference) v době diagnózy ≥ 50 mg/l definuje měřitelné onemocnění pomocí hladin FLC. Avšak přibližně u 10–15 % nemocných nacházíme pouze minimálně abnormální hladiny FLC, pro část nemocných lze užít modifikovaná kritéria léčebné odpovědi, nicméně u dalších nelze stanovení FLC pro monitorování užít [Palladini, 2010b]. U malé části nemocných, zejména s těžkým nefrotickým syndromem, bývají často nacházeny nízké hladiny obou typů lehkých řetězců z důvodu úniku do moči, u části těchto nemocných je možné detekovat a kvantifikovat MIg či Bence-Jonesovu bílkovinu analýzou moči. Koncentrace FLC v séru je jedním z 3 základních kritérií recentního revidovaného stratifikačního systému AL amyloidózy (kap. 7.2. Klinická stratifikace).
4.2.3. Zobrazovací techniky u systémové AL amyloidózy
Využití zobrazovacích metod u ALA sleduje 2 hlavní aspekty, tj. morfologické a funkční posouzení orgánového postižení amyloidem (zejména myokardu). K detekci amyloidových depozit v organizmu lze využít i scintigrafické vyšetření.
Radiografické vyšetření (RTG) – RTG vyšetření v diagnostickém algoritmu samotné amyloidózy nemá větší diagnostický přínos a dominantně je využíváno k vyloučení osteolytického postižení a tím i asociace systémové ALA s MM (kap. 8. Systémová AL amyloidóza a MM). Pomocí RTG hrudníku lze prokázat rozšíření srdečního stínu s městnáním v malém oběhu, pleurální výpotek a vzácně postižení plic v rámci ALA [Georgiades, 2004].
Počítačová tomografie (CT) – CT vyšetření má u systémové amyloidózy limitovaný význam zejména z důvodu nízké specificity a hlavní využití představují ložiskové formy onemocnění zejména v oblasti orbity, nasofaryngu či laryngu. Dominantně je však CT vyšetření využíváno k detekci amyloidózy v oblasti tracheobronchiálního stromu (fokální nebo difuzní submukózní depozita zobrazující se jako noduly, plaky či cirkulární ztluštění stěny) a k posouzení postižení plicního parenchymu (nodulární parenchymatózní amyloidóza nebo difúzní alveolární septální amyloidóza). CT vyšetření břicha je přínosné v diagnostice a diferenciální diagnostice jaterního postižení, přičemž diagnostická kritéria vyžadují hepatomegalii > 15 cm.
Ultrazvukové vyšetření (UZ) – Doménou UZ diagnostiky u ALA je echokardiografické (ECHO) posouzení srdečního postižení. ECHO je v současnosti stěžejní metodou pro diagnostiku a sledování srdečního postižení při amyloidóze. Kritériem postižení je koncentrická hypertrofie myokardu levé komory s diastolickou šíří interventrikulárního septa > 12 mm při absenci hypertenze nebo jiné příčiny hypertrofie myokardu [Gertz, 2005]. Dalšími ECHO nálezy jsou diastolická dysfunkce s restriktivním plněním levé komory, snížená ejekční frakce, ztráta longitudinální kontrakční schopnosti levé komory, dilatace levé síně a přítomnost chlopenních vad. Typickým nálezem je sonografický obraz jemně granulovaného myokardu („granular sparkling“) [Fikrle, 2013; Esplin, 2013]. ECHO je spolu se stanovením kardiálních biomarkerů stěžejní metodou v hodnocení orgánové léčebné odpovědi, resp. progrese onemocnění. Vybraná pracoviště dnes využívají nových echokardiografických modalit k detailnímu posouzení srdečního postižení, tj. tkáňový doppler, „strain, speckle cracking“ [Piper, 2010; Koyama, 2010].
Magnetická rezonance (MRI) – Stejně jako v případě UZ vyšetření je MRI využíváno zejména v hodnocení srdečního postižení. Vyšetření srdce MRI umožňuje morfologické a funkční zobrazení, navíc při užití kontrastního vyšetření gadoliniem dovoluje posouzení rozsahu imbibice myokardu amyloidovými masami. Fenomén pozdního sycení („delayed enhancement“) ve své difuzní subendokardiální či méně časté transmurální formě zobrazení je nález charakteristický pro postižení myokardu amyloidem [Maceira, 2005; Hosch, 2008; Ruberg, 2009; Fikrle, 2016]. Vyšetření je vysoce senzitivní a specifické, nicméně pro využití ke sledování nemocných a posuzování léčebné odpovědi nejsou zatím k dispozici dostatečná data. Dalšími modalitami MRI je mapování expanze extracelulárního objemu (ECV) myokardu a nativní T1 mapování. T1 mapování nevyžaduje užití gadolinia jako kontrastu a je tedy proveditelné i u pacientů s renální nedostatečností [Pan, 2020]. MRI je užitečná i v posuzování ložiskové amyloidózy v oblasti laryngu, nasofaryngu, míchy či urogenitálního traktu [Georgiades, 2004].
Radioscintigrafie – Radioscintigrafie s využitím značeného 123I-SAP je neinvazivní, kvantitativní a velmi citlivou metodou (u AL a AA amyloidózy 90% senzitivita) pro celotělovou detekci orgánové distribuce amyloidu s dobrou vizualizací depozit v ledvinách, játrech, kostech, slezině a nadledvinkách, a tím i vhodnou technikou k monitorování výsledků léčby. 123I-SAP scintigrafie umožňuje vizualizaci amyloidových depozit i v orgánech bez známek klinického postižení a v případě nemožnosti biopsie [Hawkins, 2002; Palladini, 2010a]. Celosvětově nízká dostupnost 123I-SAP je podmíněna potenciálním rizikem přenosu infekce, neboť SAP se připravuje z krve dárců. V ČR není tato metoda zavedena.
V současnosti je na řadě pracovišť využíváno 99mTc-3,3-diphosphono-1-2-propanodicarboxylic acid (DPD) scintigrafie. 99mTc-DPD je selektivně vychytáván v myokardu s depozitity TTR amyloidu, což je výhodné nejen pro diagnostiku a posuzování postižení srdce u hereditární a senilní ATTR amyloidózy, ale i pro diferenciální diagnostiku vůči ALA, u které akumulace radiofarmaka chybí či je velmi nízká [Rapezzi, 2011; Perugini, 2005; Weijia, 2021].
4.3. Speciální diagnostické techniky u systémové AL amyloidózy
4.3.1. DNA analýza
Analýza DNA je důležitým diagnostickým krokem zvláště pro stanovení hereditárních amyloidóz, což jsou onemocnění s geneticky podmíněnou změnou struktury proteinu. Pro genomické vyšetření pacientů s podezřením na hereditární formu amyloidózy je užívána detekce nukleových kyselin pomocí metody PCR (polymerázová řetězová reakce) s následným zjišťováním pořadí nukleových kyselin v polynukleotidovém řetězci (tzv. Sangerovo sekvenování). Cílem je zjistit možnou záměnu nukleotidu ve sledovaném genu, která následně může způsobit záměnu aminokyseliny v polypeptidovém řetězci, patologickou konformaci proteinu a tím i jeho dysfunkci [Sipe, 2016]. Jde o relativně jednoduchou metodiku zavedenou do praxe nejméně na dvou pracovištích v České republice (Praha, Ostrava). V současné době již existuje zavedený a validovaný panel pro diagnostiku hereditárních amyloidóz pomocí sekvenování nové generace (NGS). Tento panel by měl v blízké budoucnosti nahradit vyšetřování pomocí Sangerova sekvenování a snížit finanční i časovou náročnost vyšetření [Chyra, 2018].
4.3.2. Hmotnostní spektrometrie
Analýza amyloidních depozit pomocí hmotnostní spektrometrie
Cílem analýzy amyloidních depozit je najít nejvíce zastoupený amyloidní fibrilární protein, který určuje typ amyloidu [Holub 2019; Benson, 2020]. Před samotnou analýzou jsou proteiny extrahovány ze vzorků (FFPE vzorky nebo tuková tkáň) a následně jsou proteiny enzymaticky štěpeny na peptidy. Vzniklá peptidová směs je separována pomocí kapalinové chromatografie, kdy se využívá rozdílné hydrofobicity jednotlivých peptidů. Během analýzy jsou jednotlivé peptidy eluovány z kolony, ionizovány a analyzovány na hmotnostním spektrometru. Při analýze na hmotnostním spektrometru je změřena přesná hmota peptidu a také je u něj změřeno fragmentační spektrum. Z těchto informací je možné vyčíst sekvenční informaci o peptidu, tj. z jakých aminokyselin je peptid složen. Pokud je sekvenční informace peptidu unikátní, je identifikován unikátní protein. Z naměřených intensit peptidů je možné získat kvantitativní informaci o jednotlivých proteinech ve vzorku. Výsledkem proteomické analýzy je seznam identifikovaných proteinů s jejich kvantitativní informací [Mann, 2001]. Při analýze amyloidních depozit je hledán v seznamu identifikovaných proteinů nejvíce zastoupený amyloidní fibrilární protein, který určuje typ amyloidu [Dogan, 2017]. V amyloidních depozitech jsou také pozorovány proteiny podílející se na tvorbě amyloidu (Serum amyloid P, Apolipoprotein E, Apolipoprotein IV).
4.3.3. Vyšetření klonality plazmocytů pomocí multiparametrické průtokové cytometrie
Vzhledem k tomu, že pro ALA je typické nízké zastoupení PC, teprve detekce a identifikace dostatečného počtu PC na základě exprese povrchových znaků CD38 a CD138 umožňuje jejich detailní analýzu. Na rozdíl od MM, kde již kostní dřeň (KD) bývá infiltrována vesměs klonálními PC, u ALA, podobně jako u monoklonální gamapatie nejasného významu (MGUS), se v KD vyskytují v různých poměrech patologické i fyziologické PC. V takovýchto případech je identifikace a enumerace patologických PC pouze na základě stanovení „normality“ dle povrchového fenotypu s využitím znaků CD19 a CD56 (normální N-PC: CD19+CD56 - vs. abnormální A-PC: CD19-CD56+/–) často nepřesná [Kovářová, 2011]. Přesto však bylo zjištěno, že stanovení infiltrace kostní dřeně PC průtokovou cytometrii a procentuální zastoupení počtu normálních a abnormálních PC mohou sloužit jako prognostické parametry ovlivňující celkové přežití pacientů s ALA [Paiva, 2011; Jelínek, 2017]. Pro spolehlivé stanovení přítomnosti a počtu klonálních PC je však nezbytné stanovení intracelulární „klonality“ s využitím kombinace minimálně 6 znaků (CD38, CD138, CD19, CD56, ckappa a clambda), ještě lépe však v 8barevné kombinaci (CD38, CD138, CD19, CD56, CD45, CD27, ckappa a clambda) umožňující přesnější odlišení polyklonáních (N-PC) od klonálních (A-PC) plazmocytů. Analýza klonality PC u ALA je pak nezbytným nástrojem pro zhodnocení léčebné odpovědi, kdy dosažení hematologické kompletní remise je nutným předpokladem dosažení orgánové léčebné odpovědi [Adam, 2012b]. Palladini at al. uvádí, že dosažení negativity minimální reziduální choroby stanovené pomocí průtokové cytometrie nové generace (next-generation flowcytometry), je spojeno s vyšší mírou orgánových léčebných odpovědí. Naopak u nemocných s minimální reziduální chorobou by měla být zvážena další léčba [Palladini, 2021].
5. DIAGNOSTICKÁ KRITÉRIA A POSTUPY U SYSTÉMOVÉ AL AMYLOIDÓZY
5. 1. Diagnostická kritéria
Časná diagnóza systémové ALA je obtížná, poněvadž neexistuje žádný samostatný laboratorní ukazatel ani zobrazovací technika, které by diagnózu nemoci samy o sobě umožnily [Gertz, 2011]. Správná diagnóza systémové ALA se proto opírá o splnění souboru diagnostických kritérií sestavených v roce 2011 IMWG (International Myeloma Working Group) v tabelární formě (tab. 5).
Z předložených kritérií je zřejmé, že diagnóza systémové ALA vyžaduje splnění všech 4 základních kritérií nemoci:
1. Jednoznačný průkaz, že k postižení některého z orgánů, tj. ledvin, srdce, GIT vč. jater, nervové tkáně a vzácněji svalů, kůže aj., došlo v důsledku amyloidózy, nikoliv v rámci jiného onemocnění (např. diabetes mellitus, ateroskleróza aj).
2. V klinické praxi se k detekci amyloidu používá standardně současná aspirační biopsie podkožního tuku (pozitivita 60–80 %) a biopsie kostní dřeně (50–65 %), při jejich negativitě i slinné žlázy (asi 15% pozitivita při negativitě amyloidu v podkožním tuku), případně, a to i v souladu s klinickým obrazem (např. makroglosie) jazyka, rekta a gingivy. Při diagnostickém neúspěchu necíleného odběru se přistupuje k cílené biopsii dominantně postiženého orgánu, tj. ledviny, myokardu (endomyokardiální biopsie), jater, zažívací trubice, ojediněle i n. suralis, kosterního svalstva, uzliny aj., vyznačující se 80–100% výtěžností s následující hierarchií pozitivity: endomyokardiální biopsie (100 %), biopsie jater (97 %), ledvin (94 %), kůže (90 %), n. suralis (86 %), tenkého střeva (83 %), tkáně z oblasti karpálního tunelu (82 %), biopsie podkožního tuku s hodnocením 3 vzorků (80 %), biopsie rekta (75 %) a trepanobiopsie kostní dřeně (56 %) (kap. 4.2.1. Diagnostika amyloidu z pohledu patologa) [Gertz, 1991, 2009, 2016].
3. Vzhledem k jisté nespolehlivosti imunohistochemické identifikace AL typu amyloidu, používaného ve standardní klinické praxi (v 50 % ztráta antigenních epitopů v průběhu fibrilogenezy), se v současnosti mnohdy užívá kombinace technik, preferována je hmotnostní spektrometrie, na řadě pracovišť považovaná za „zlatý standard“, na vysoce specializovaných pracovištích navíc i imunoelektronová mikroskopie [Seldin, 2006; Lachmann, 2002; Dispenzieri, 2012] (kap. 4.2.1. Diagnostika amyloidu z pohledu patologa, kap; 4.3. Speciální diagnostické techniky u systémové AL amyloidózy).
Monoklonální charakter plazmocelulárních elementů u ALA lze prokázat detekcí intaktní molekuly MIg a/nebo zvýšené produkce FLC MIg s patologickým indexem k/l (kap. 4.2.2. Průkaz MIg a FLC v séru a/nebo moči). Klíčovým znakem systémové ALA je nejčastěji zvýšená hladina FLC typu l [Gertz, 2011]. Samotný průkaz MIg ovšem nepotvrdí s jistotou, že jde o AL typ amyloidu. Přímým průkazem monoklonality plazmocytů je stanovení poměru plazmocytů s expresí LŘ k/l pomocí imunohistochemického vyšetření trepanobioptického vzorku kostní dřeně nebo analýzou aspirátu KD pomocí M-FC (multiparametrické průtokové cytometrie) (kap. 4.2.1. Diagnostika amyloidu z pohledu patologa; 4.3.3. Vyšetření klonality plazmocytů pomocí multiparametrické průtokové cytometrie).
Vzhledem ke složitosti časné diagnostiky tak proměnlivého onemocnění, jakým je systémová ALA, byla pro potřeby klinické praxe dohodnuta v rámci „10th International symposium on amyloid and amyloidosis, Tours 2004“ kritéria přesně definující klinicko-laboratorní známky orgánového postižení. Tato kritéria byla v roce 2010 částečně revidována (tab. 6).
Tab. 6. Průkaz postižení orgánů při systémové AL amyloidóze [Gertz, 2005; Gertz et. Merlini, 2010]. („Consensus opinion from the 10th International symposium on amyloid and amyloidosis, Tours, 2004“) ![Průkaz postižení orgánů při systémové AL amyloidóze [Gertz, 2005; Gertz et. Merlini, 2010]. („Consensus
opinion from the 10th International symposium on amyloid and amyloidosis, Tours, 2004“)](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/574a214eb4b683d604d0b86c69d50bd8.jpg)
K histologickému potvrzení diagnózy AL amyloidózy lze použít i odběr z alternativních míst:
biopsie podkožního tuku v oblasti břicha tenkou jehlou a/nebo biopsie slinné žlázy, rekta nebo gingivy, při negativitě cílená biopsie postižených orgánů.
AF – alkalická fosfatáza, DKK – dolní končetiny, ECHO – echokardiografie, GIT – gastrointestinální trakt5.2. Diagnostická kritéria postižení jednotlivých orgánových systémů u systémové AL amyloidózy
5.2.1. Diagnostika amyloidové kardiomyopatie
Laboratorní vyšetření – Stanovení kardiálních biomarkerů je nedílnou součástí diagnostického algoritmu u nemocných s ALA. Obvykle jsou vyšetřovány hladiny troponinu T (TnT) a NT-pro „brain“ natriuretického peptidu (NT-proBNP), ojediněle i troponinu I (TnI), laboratorně standardizovanými metodami [Pika, 2008]. Hladina TnT je citlivým ukazatelem myokardiálního postižení a její hodnota stanovená v době diagnózy (> 0,035 µg/l) má úzký vztah k prognóze, proto se stala jedním z kritérií stratifikačního systému systémové ALA vypracovaného na Mayo klinice [Kristen, 2010; Dispenzieri, 2003; Dispenzieri, 2004b]. Přetrvávání zvýšené hladiny TnT signalizuje pokračující ztrátu kardiomyocytů, zato účinná terapie je spojena s různě významným poklesem. Rovněž hladina NT-proBNP má prognostický a stratifikační potenciál (> 332 ng/l) a při jeho normální hladině je amyloidová kardiomyopatie prakticky vyloučena [Dispenzieri, 2004b; Palladini, 2003]. Vzhledem k tomu, že při účinné léčbě dochází k poklesu hladin obou srdečních biomarkerů, jsou používána jako kritéria pro hodnocení orgánové kardiologické remise [Comenzo, 2012]. Limitací stanovení NT-proBNP je přetrvávání zvýšených hladin při terapii IMIDy a stejně jako v případě TnT jsou i hladiny NT-proBNP ovlivněny případnou renální nedostatečností [Dispenzieri, 2010b]. Proto v této situaci se jeví jako výhodnější stanovení samotného BNP („brain natriuretic peptide“), který není renální nedostatečností ovlivněn. Vzhledem k tomu, že metoda stanovení není standardizovaná, je nutné použít pro monitoraci stavu vždy stejnou laboratoř [Palladini, 2012].
Paraklinická vyšetření – Mezi základní a neopomenutelná vyšetření u ALA patří elektrokardiografické vyšetření (EKG). V případě pokročilé amyloidové kardiomyopatie je typickým nálezem snížená voltáž v končetinových svodech < 5 mm a obraz QS ve svodech V1-3 (tzv. obraz pseudoinfarktu), poměrně častým nálezem je záchyt arytmií či A-V blokád [Fikrle, 2013; Murtagh, 2005]. Stěžejním vyšetřením v diagnostice a sledování srdečního postižení při amyloidóze je echokardiografie a MRI (kap. 4.2.3. Zobrazovací techniky u systémové AL amyloidózy). Endomyokardiální biopsie (EMB) je indikována v případě podezření na srdeční amyloidózu při negativitě necílené biopsie. Stejně tak lze zvážit provedení EMB při přítomnosti atypických faktorů, např. arteriální hypertenzi či šíři interventrikulárního septa > 12 mm. O závažnosti postižení vegetativního nervového systému může do jisté míry informovat test variability srdeční frekvence (Ewingův test) [Reyners, 2002].
5.2.2. Diagnostika amyloidové nefropatie
Ledviny jsou v případě systémové ALA nej - častěji postiženým orgánem (50–80 %), projevujícím se v úvodu nápadnou proteinurií, případně i vzestupem sérového kreatininu. Neselektivní proteinurie dosahuje většinou intenzity nefrotického syndromu (NS) (2,5–30 g/24 hod.), kdy většinu tvoří albumin. Nezbytnou součástí vyšetření je nejen standardní, ale i IFE moče zaměřená na detekci MIg a FLC, tj. Bence-Jonesovu bílkovinu. Laboratorní vyšetření musí obsáhnout i ostatní atributy NS, vč. detekce hyperlipoproteinémie a dalších obvyklých komplikací. Minimální proteinurie se vyskytuje pouze v případech, kdy depozita amyloidu jsou omezena na tubuly, intersticium a cévní složku ledvinové tkáně.
Glomerulární filtrace – Vyšetření GF je standardním vyšetřením, neboť u amyloidové nefropatie dochází k jejímu rychlému poklesu s častým vývinem ESRD („end-stage renal disease“) [Dember, 2010]. I když rychlost poklesu GF je u ALA individuálně značně odlišná, u většiny nemocných postupně stále klesá zejména v případě prevalence glomerulárních amyloidových depozit nad depozity v tubulo-intersticiální oblasti. V pozdní fázi nemoci lze zaznamenat v důsledku poškození cévní stěny a zvýšené propustnosti bazální membrány glomerulu mikroskopickou hematurii. I v případě ledvin platí, že porucha orgánové funkce závisí především na toxicitě fibrilárních prekurzorů, tj. prekurzorových proteinů (amyloidogenních LŘ) a jejich oligomerů, nežli na rozsahu amyloidových depozit [Snanoudj, 2004; Dember, 2010]. Při hodnocení poklesu GF je nutno zohlednit i pokles prokrvení ledvin způsobený snížením srdečního výkonu, poklesem krevního tlaku a intravaskulárního objemu krve, závažností autonomní dysfunkce či předchozí aplikací kontrastní látky. K akutnímu, obvykle jen přechodnému, snížení GF s prohloubením retence dusíkatých katabolitů vyžadujícím dialyzační léčbu dochází asi u 20 % nemocných po vysokodávkové léčbě následované autologní transplantací, ale třeba i po léčbě lenalidomidem. Při hodnocení výsledku vyšetření GF nutno počítat s okolností, že dosažení hematologické remise s potlačením produkce amyloidogenních LŘ vede obvykle pouze ke stabilizaci než ke zlepšení renální funkce. Vyšetření GF v klinické praxi má v případě systémové ALA určité úskalí, neboť hladina kreatininu v séru může v případě ztráty svalové tkáně převyšovat stupeň snížení GF. Nutno počítat s jistou nepřesností výpočtu GF s pomocí clearence kreatininu i Cockroftovy-Gaultovy rovnice, neboť v případě NS je hodnocení objemu svalové hmoty nepřesné. V hraničních situacích lze využít vyšetření GF s pomocí cystatinu a radionuklidových metod.
Tubulární funkce, sonografie a biopsie ledviny – Vyšetření tubulárních funkcí je plně indikováno vzledem k relativně častému výskytu funkčních tubulárních poruch, avšak úplný obraz Fanconiho syndromu (postižení proximálního tubulu) nebo nefrogenního typu diabetes insipidus (postižení distálního tubulu) je spíše výrazem současné koincidence s MM [Ryšavá, 2013]. Součástí základního diagnostického algoritmu je i sonografie ledvin, neboť u většiny nemocných se setkáváme v důsledku renální depozice amyloidu se symetrickým zvětšením a změnou echogenity [Krejčí, 2011]. V případě absence pozitivity necílené biopsie je rozhodnutím volby cílená biopsie ledviny, nejčastěji dominantně postiženého parenchymatózního orgánu, vyznačující se 90–95% záchytem amyloidu a umožňující přesné rozpoznání umístění depozit a charakteru disrupce architektury ledvinové tkáně [Ryšavá, 2013].
5.2.3. Kritéria postižení ostatních orgánů u AL amyloidózy
V rámci systémové AL amyloidózy lze vedle dominantně postižených ledvin a srdce odhalit i postižení dalších orgánů a orgánových systémů:
Nervový systém – Zde se postižení projevuje přítomností distální symetrické, senzomotorické periferní neuropatie DKK a postižením autonomního nervového systému. Rozpoznání distální smíšené periferní neuropatie DKK je založeno na rozboru klinického obrazu (kap. 3.2.3. Periferní a autonomní neuropatie) a pečlivém neurologickém vyšetření doplněném o EMG, i když jeho nedostatkem je poměrně nízká citlivost. Individuálně lze použít histologické vyšetření surálního nervu. Rozpoznání autonomní neuropatie je založeno především na rozboru klinického obrazu (kap. 3.2.3. Periferní a autonomní neuropatie), případně doplněném o testy používané ke zhodnocení vegetativní dysfunkce.
Gastrointestinální trakt – Klinické projevy přímé infiltrace stěny zažívací trubice amyloidem vedoucí k poruše motility, erozivní amyloidové enteropatii či malabsorpci jsou indikací k endoskopickému vyšetření GIT s odběrem materiálu na histologické vyšetření. Podezření na postižení jater, vyznačující se vedle hepatomegalie ověřené sonograficky nebo pomocí CT (šíře >15 cm) přítomností portální hypertenze se splenomegalií a více nežli 1,5násobkem zvýšené jaterní frakce alkalické fosfatázy (AF), je indikací k provedení biopsie jater.
Postižení plic – Jeho průkaz je založen na provedení konvenčního radiografického vyšetření plic, případně i vysoce citlivého HRCT („high-resolution CT“) odhalujícího i jinak nerozpoznatelné postižení plic a pleury depozity amyloidu. V případě zmnožené retikulonodulární kresby (difuzní intersticiální amyloidóza), ložiskové léze („coin lesion“ resp. amyloidom), pleurálního výpotku při postižení pleury může správné diagnóze napomoci transbronchiální nebo video-asistovaná thorakoskopická biopsie. V odhalení depozit v bronchiálním stromu (tracheobronchiální amyloidóza) se uplatňuje bronchoskopie s odběrem materiálu na histologii a spirometrické vyšetření vč. vyšetření difuzní plicní kapacity.
Postižení pohybového aparátu – V případě postižení svalstva a kloubního systému (kap. 3.2.5. Postižení ostatních orgánů a tkání) lze využít vedle vyšetření svalových enzymů (kreatinkináza, myoglobin v séru) i MRI a biopsii svalu, v případě amyloidové artropatie biopsii synovie, či histologické vyšetření tkáně získané při operaci karpálního tunelu.
Postižení krvetvorného a koagulačního systému – Vyšetření krevního obrazu může odhalit anémii chronických chorob a zvýšení počtu krevních destiček. Koagulační vyšetření může zaznamenat zvýšení fragility kožních cév, prodlouženou krvácivost a aPTT spolu se sníženou hladinou faktoru X, ke které dochází v důsledku vazby tohoto koagulačního faktoru na amyloid [Mumford, 2000].
Postižení ostatních orgánů a tkání – Pro jeho potvrzení je vedle zhodnocení klinického obrazu (kap. 4.2.5. Postižení ostatních orgánů a tkání) vždy nutný odběr tkáně k histologickému vyšetření, např. excize svaloviny jazyka při makroglosii, biopsie kůže v případě kožních depozit amyloidu, histologie lymfatické uzliny při lymfadenomegalii.
5.3. Diagnostický algoritmus systémové AL amyloidózy
V klinické praxi lze přistupovat k nemocnému s podezřením na systémovou amyloidózu podle „diagnostického algoritmu“, zohledňujícího i další typy amyloidóz, nežli je ALA (tab. 7). Vždy je ale nutné splnit 4 základní diagnostické kroky, tj.: 1) na možnost ALA pomyslet; 2) potvrdit přítomnost amyloidózy s pomocí tkáňové biopsie; 3) určit prekurzorový protein; 4) posoudit rozsah orgánového postižení [Dispenzieri, 2012].
Tab. 7. Diagnostický algoritmus systémové amyloidózy. 
ALP – alkalická fosfatáza, CB-U – proteinurie, CT – vyšetření počítačovou tomografií, Echo – echokardiografie, EKG – elektrokardiografie, FLC – stanovení sérových hladin volných lehkých řetězců imunoglobulinu, IFE – imunofixace, MM – mnohočetný myelom, MR – magnetická rezonance, NHL – non-Hodgkinův lymfom, SPE – elektroforéza sérových proteinů, UPE – elektroforéza proteinů moči, UZ – ultrazvukové vyšetření, WM – Waldenströmova makroglobulinemie 6. DIFERENCIÁLNÍ DIAGNÓZA SYSTÉMOVÉ AL AMYLOIDÓZY
V případě histologického průkazu amyloidózy je nutné odlišení systémové ALA od formy ložiskové a AL amyloidózy provázející MM nebo jiný B-lymfoproliferativní stav (kap. 8. Systémová AL amyloidóza a mnohočetný myelom). Ložiskový typ AL amyloidózy se vyznačuje jistou predilekční lokalizací, nepřítomností MIg, normální hodnotou FLC v séru a nepřítomností monoklonální populace plazmocytů v kostní dřeni (kap. 10. Ložisková AL amyloidóza). Reaktivní AA amyloidóza navazuje na předchozí dlouhodobou přítomnost základního vyvolávajícího onemocnění (např. revmatoidní artritida), jsou zvýšeny hodnoty reaktantů akutní fáze a SAA, pozitivita imunohistologického vyšetření s použitím specifické monoklonální protilátky. Vzácný hereditární mTTR typ amyloidózy lze rozpoznat s pomocí vysoce specializovaných metod (DNA analýza, hmotnostní spektrometrie, imuno-elektronová mikroskopie) a nutno mít na paměti i možnou přítomnost MIg (v 5–10 %) [Bird, 2004]. U nemocných v dlouhodobé dialyzační léčbě se ojediněle vyskytuje hemodialyzační (Ab2M) amyloidóza. U starších mužů s dominantním postižením srdce a s projevy městnavé srdeční slabosti a/nebo poruchami rytmu je nutno pátrat po amyloidóze senilní (wtTTR). Musíme mít na paměti, že na možnost systémové ALA je nutno pomýšlet u všech jedinců s MGUS, a před stanovením definitivní diagnózy provést pečlivé vyšetření podle diagnostického algoritmu ALA, případně i opakovaně. Nutno odlišit rovněž „monoclonal gammopathy of renal significance“ (MGRS), provázející ojediněle MGUS s přítomností LŘ s vysokým nefrotoxickým potenciálem [Leung, 2012], ale i onemocnění s depozity lehkých řetězců (light chain deposition disease – LCDD) [Ščudla, 2012] nebo z depozice těžkých řetězců imunoglobulinu (heavy chain deposition disease – HCDD), pří - padně i periferní neuropatii s přítomností MIg [Bird, 2004]. Stejně jako u ALA jsou v případě LCDD postiženy nejčastěji ledviny (renální insuficience), méně časté je zvětšení jater s poruchou jaterní funkce a/nebo postižení srdce s projevy městnavé srdeční slabosti. Precizní zařazení zjištěné amyloidózy je nezbytné nejen z hlediska odlišné klinické manifestace, průběhu a prognózy jednotlivých typů, ale především z hlediska poskytnutí účelné, pro jednotlivé typy amyloidóz specifické, terapie [Falk, 1997; Ščudla, 2009].
7. PROGNOSTICKÉ FAKTORY A KLINICKÁ STRATIFIKACE SYSTÉMOVÉ AL AMYLOIDÓZY
7.1. Prognostické faktory
Prognóza nemocných se systémovou ALA je variabilní, stále ale nepříznivá, a to zejména pokud nebyla včas zahájena adekvátní terapie [Kyle, 1997]. V historických studiích byl medián celkového přežití 15–18 měsíců, ale v případě nemocných se závažným postižením srdce, manifestujícím se městnavou srdeční slabostí a/nebo synkopálními stavy, pouze 4–6 měsíců [Kyle 1995a; Dispenzieri, 2010a]. Nemocní s projevy závažné amyloidové kardiomyopatie se vyznačují vysokým rizikem náhlé smrti [Gertz, 1999, 2011]. V současnosti, díky časnější diagnóze a nesporným pokrokům v léčbě, se délka celkového přežití nemocných s ALA podstatně zlepšila, a v posledním desetiletí přesáhl medián přežití 5 let [Kumar, 2010; Ravichandran, 2020]. Prognóza nemocných se systémovou ALA závisí zejména na dosažení rychlé suprese syntézy monoklonálních LŘ a na stabilizaci, případně zlepšení, srdeční funkce [Wechalekar, 2009].
Excelentními prediktory prognózy ALA jsou sérové hladiny solubilních srdečních biomarkerů (troponin T, troponin I, NT-proBNP a BNP) [Palladini, 2003; Dispenzieri, 2003, 2004b], které se staly východiskem prognostického stratifikačního systému systémové ALA (kap. 7.2. Klinická stratifikace). Hladiny NT-proBNP > 8 500 ng/l spolu s nálezem hodnot systolického tlaku < 100 mm Hg identifikují nemocné s vysokým rizikem časného úmrtí [Wechalekar, 2013; Dittrich, 2020].
Významnými prognostickými ukazateli ALA jsou i charakteristiky plazmocelulárního klonu, jmenovitě stupeň plazmocytózy KD (> 10 %) či procento aberantních plazmocytů při použití multiparametrické průtokové cytometrie [Gertz, 1989; Dispenzieri, 2010a; Paiva, 2011]. Nemocní s přítomností t (11; 14) mají horší prognózu, pokud jsou léčeni režimy na bázi bortezomibu, naopak profitují z léčby vysokodávkovaným melfalanem [Bochtler, 2015, 2016]. Nemocní se ziskem v oblasti 1q21 neprofitují z léčby kombinací melfalanu a dexametasonu [Bochtler, 2014].
Vysoká hodnota dominantního FLC v séru a patologie kappa/lambda indexu vyšetřené v době stanovení diagnózy mají úzký vztah k prognóze [Dispenzieri, 2006]. Prognosticky příznivou skupinu tvoří nemocní s nízkou náloží FLC (dFLC < 50 mg/l) v době diagnózy. U těchto nemocných bývá menší procento a závažnost kardiálního postižení, naopak bývá častější renální postižení s vyšším stupněm proteinurie. Nemocní se vyznačují delším celkovým přežitím (Dittrich, 2017; Milani, 2017).
Z ukazatelů vyšetřených po ukončení terapie je nejvýznamnější hloubka orgánové léčebné odezvy a hloubka hematologické odezvy, zejména dosažení kompletní remise (CR) založené na vymizení M-proteinu v séru a/nebo v moči vyšetřeného IFE, normalizaci FLC v séru vč. indexu k/l a vymizení plazmocelulárního klonu v KD (viz. kapitola 10. Kritéria hematologické léčebné odpovědi) [Gertz, 2007].
7.2. Klinická stratifikace
V roce 2004 byl navržen stážovací systém rozdělující nemocné se systémovou AL amyloidózou na podkladě hodnot srdečních biomarkerů do 3 stádií [Dispenzieri, 2004b], neboť závažnost postižení srdce je i u asymptomatických jedinců stěžejním prognostickým faktorem [Palladini, 2010b; Comenzo, 2012] (tab. 8).
Tab. 8. „Mayo Clinic“ stážovací systém systémové AL amyloidózy [Dispenzieri, 2004b]. ![„Mayo Clinic“ stážovací
systém systémové AL amyloidózy
[Dispenzieri, 2004b].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/f84abf9456ddac936926f329c92c9d9a.jpg)
cTnI – i-troponin, cTnT – c-troponin, NT-proBNP – N-terminální pro-brain natriuretický peptid („N-terminal pro-brain natriuretic peptide“), OS – celkové přežití („overall survival“) V roce 2012 byl na Mayo klinice vypracován tzv. „revidovaný prognostický stážovací systém“, založený na hladinách cTnT, NT-proBNP a FLC v séru (tab. 9). To vedlo ve srovnání s původním stratifikačním systémem ke zlepšení hodnocení dlouhodobého prognostického výhledu u nemocných léčených standardní chemoterapií i ASCT [Gertz, 2011; Kumar, 2012].
Tab. 9. Revidovaný „Mayo Clinic“ stážovací systém systémové AL amyloidózy [Kumar, 2012]. ![Revidovaný „Mayo Clinic“ stážovací systém systémové
AL amyloidózy [Kumar, 2012].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/4ea009e3e0e27bd5b585afdc5b0d27de.jpg)
Použití BNP (≥ 400 ng/ml) namísto NT-proBNP: velmi podobný význam pro stratifikaci a prognózu, vč. hodnocení celkového přežití (p < 0,001).
cTnT – c-troponin, FLC – volné lehké řetězce imunoglobulinu („free light chain“), NT-proBNP – N-terminální pro-brain natriuretický peptid („N-terminal pro-brain natriuretic peptide“), OS – celkové přežití („overall survival“)Míra poškození srdce je prognosticky nejzávažnějším faktorem, který je nutné zohlednit i při stanovení intenzity léčby. U nemocných s vysokým kardiálním rizikem (troponin T > 0,06 ng/ml nebo NT-proBNP > 5 000 pg/ml u nemocných s normální funkcí ledvin) není doporučeno provedení autologní transplantace z důvodu vysoké časné peritransplantační mortality [Gertz, 2016]. Proto byl navržen a validován Evropský stážovací systém pokročilého srdečního postižení [Wechalekar, 2013] (tab. 10).
Tab. 10. Evropský stážovací systém pokročilého srdečního postižení při systémové AL amyloidóze [Wechalekar, 2013]. ![Evropský stážovací
systém pokročilého srdečního
postižení při systémové AL
amyloidóze [Wechalekar, 2013].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/1882e80e416b2574ea7b974ad1c964f5.jpg)
NT-proBNP – N-terminální pro-brain natriuretický peptid („N-terminal pro-brain natriuretic peptide“), OS – celkové přežití („overall survival“) 8. SYSTÉMOVÁ AL AMYLOIDÓZA A MNOHOČETNÝ MYELOM
Dle míry infiltrace kostní dřeně klonálními plazmocyty rozlišujeme nemocné s AL amyloidózou (< 10 % plazmocytů) a nemocné s mnohočetným myelomem a asociovanou AL amyloidózou (≥ 10 % plazmocytů). Někteří jedinci, u nichž se v průběhu sledování rozvinou příznaky systémové ALA, jsou dlouhodobě vedeni jako MGUS. U malé části nemocných s MGUS (~ 1–1,5 %/rok) dochází k vývinu systémové ALA, případně MM nebo MW, neboť jde ve všech případech o klonální proliferaci elementů plazmocelulární, případně lymfoplazmocytární, linie [Kyle, 2010]. Současný výskyt systémové ALA a MM se pozoruje u 10–15 % nemocných [Fielder, 1986; Kyle, 1995b], ovšem systémová ALA je asi 10× méně častá nežli MM. Asi u 1 % nemocných s nově diagnostikovaným symptomatickým i asymptomatickým MM lze cíleným vyšetřením rozpoznat asymptomatickou formu systémové ALA [Siragusa, 2011]. LŘ produkované maligními monoklonálními plazmocyty nabývají v důsledku polymerizace a částečné degradace v elementech monocytárně-makrofágového systému amyloidogenní potenciál. V klinické praxi diagnóza MM obvykle předchází nebo odpovídá době rozpoznání ALA. Z hlediska strategie léčby a hodnocení prognózy je vždy nutné v této situaci rozhodnout, který stav je „dominantní“. Naopak výjimečně, v 0,4 %, dochází k manifestaci MM ve více než 6měsíčním odstupu (odložená progrese) od diagnózy ALA, a to obvykle u relativně indolentních forem nemoci bez postižení srdce, ledvin a jater, vyznačujících se dlouhým průběhem [Rajkumar, 1998]. V této situaci je rozpoznání symptomatického MM založeno na přítomnosti anémie, > 30 % plazmocytů v KD, hyperkalcémii a bolestech skeletu s přítomností osteolytických lézí, ale i na odhalení dalších nálezů vč. cytogenetických změn, pozorovaných obvykle při maligní transformaci MGUS v MM [Alpers, 1986]. Na rozvoj ALA je nutno vždy pomýšlet především v případě výskytu projevů, které obvykle nepatří do klinického obrazu MM, např. závažné postižení srdce s projevy restriktivní kardiomyopatie, syndrom karpálního tunelu, makroglosie, nefrotický syndrom, projevy zejména autonomní neuropatie, nález kožních ložisek amyloidu aj. (kap. 3. Klinický obraz systémové AL amyloidózy). V případě přítomnosti plně vyjádřených projevů amyloidové kardiomyopatie je prognóza nemocných se současným MM značně nepříznivá, s celkovým přežitím ~ 9 měsíců [Madan, 2010]. Při nepřítomnosti závažného postižení srdce nebo jiného parenchymatózního orgánu je možná dobrá odezva k chemo-imunoterapii s dosažením délky přežití obdobné, jako je tomu u samotného MM [Fielder, 1986].
9. DOPORUČENÍ PRO DIAGNOSTIKU AL AMYLOIDÓZY
- Systémová AL amyloidóza je vzácné hematologické onemocnění patřící mezi monoklonální gamapatie.
- Optimální péče o nemocné s ALA je založena na časné diagnóze s vyhodnocením závažnosti orgánového postižení, účinné terapii zaměřené zejména na snížení produkce amyloidogenních lehkých řetězců a léčbě podpůrné.
- V 12–20 % je asociována s jinou formou monoklonální gamapatie či B-lymfoproliferativního onemocnění.
- Amyloidóza musí být vždy histologicky verifikována spolu s potvrzením AL typu amyloidu.
- Podkladem onemocnění je depozice amyloidu v orgánech a tkáních, což vede k jejich funkčnímu postižení ev. selhání. Pečlivé posouzení orgánového postižení je základním pilířem diagnostiky a stratifikce nemocných.
- Detekce a kvantifikace monoklonálního imunoglobulinu a zejména hladin volných lehkých řetězců patří mezi stěžejní aspekty diagnostiky a sledování nemocných se systémovou ALA.
10. LOŽISKOVÁ AL AMYLOIDÓZA
10.1. Etiopatogeneze, diagnostika a klinický obraz
Ložisková ALA se vyznačuje pouze lokální depozicí amyloidu bez známek systémového výskytu. Amyloid je deponován pouze v místě syntézy amyloidogenního proteinu, tj. v oblasti ložiskového nahromadění monoklonálních plazmocytů, přičemž prekurzorové amyloidogenní LŘ nejsou transportovány do krevního řečiště. Existují však i příklady terčové depozice cirkulujícího MIg u systémové ALA ve specifickém orgánu v důsledku „tkáňového tropizmu“ [Benson, 1995]. Incidence ložiskové AL amyloidózy odpovídá 10–20 % všech ALA a vyskytuje se především v 6. a 7. životní dekádě [Kyle, 1975]. I když byla odkryta již řada patofyziologických mechanizmů, její etiologie není doposud vyřešena. Amyloidogenní LŘ jsou vytvářeny populací klonálních plazmocelulárních nebo lymfoplazmocytárních elementů obklopujících formou nodulárních nebo difuzních infiltrátů ložiska amyloidu [Hamidi, 1999]. U většiny případů nelze zachytit MIg v séru a/nebo v moči, stejně tak ani zvýšení hladin FLC. Ložisková amyloidóza se v naprosté většině případů vyznačuje imunohistochemickou příslušností k AL typu. AA i transthyretinový typ amyloidu se objevují v ložiskové formě velmi vzácně, např. výjimečné ložiskové postižení hrtanu v případě hereditární systémové amyloidózy v rámci varianty apolipoproteinu AI. Lokalizovaná ALA se vyskytuje nejčastěji v oblasti horních dýchacích cest, zejména v nazofaryngu, v urogenitální oblasti a v kůži, je ale známo i postižení orbity, GIT, páteře, prsů a dalších měkkých tkání, zcela vzácně ve formě kostních lézí v oblasti páteře. Při objevení amyloidového ložiska je nutno nejprve vyloučit příslušnost k systémové formě ALA. Klinický průběh je většinou benigní a projevuje se lokálními příznaky, ojediněle však může vyústit v závažné narušení funkce postiženého orgánu. Postižení laryngu vč. hlasových vazů se projevuje vedle lokálního krvácení především dysfonií, ojediněle i obstrukcí s projevy inspirační dechové tísně vč. stridoru. K objasnění rozsahu procesu je nezbytná laryngoskopie s odběrem materiálu na histologické vyšetření, případně CT vyšetření [Ma, 2005; Harris, 2021]. Postižení hrtanu se projevuje přítomností difuzních subepiteliálních depozit (difuzní typ) nebo diskrétních či polypoidních nodulárních depozit (nodulární typ). Ložisková amyloidóza spojivek bývá zaměňována za maligní lymfom. V případě postižení uropoetického systému jde téměř výhradně o projev ložiskové, nikoliv systémové, ALA. Může být postižena ledvinová pánvička, močovod, močový měchýř, uretra a jde prakticky bezvýhradně o projev ložiskové, nikoliv systémové, AL amyloidózy. V klinickém obraze může dominovat vedle známek dysurie a recidivujících zánětů makroskopická hematurie. Diagnóza ložiskové ALA je založena na urologickém vyšetření vč. biopsie a CT-urografie. Kožní a podkožní depozita amyloidu se projevují ve formě makulárních pigmentových eflorescencí, papulárních a nodulárních útvarů v oblasti zad, hrudníku, šíje a rtů, a mohou perzistovat řadu let bez jakékoliv změny. Ložisková depozita amyloidu se mohou rovněž vyskytovat i v tkáni extramedulárního plazmocytomu, karcinomu nasopharyngu, prsu, močového měchýře a medulárního karcinomu štítné žlázy [Munichor, 2000; Chiang, 2013; Gupta, 2012].
Klinický obraz ložiskové AL amyloidózy, její průběh, prognóza a léčba se zcela zásadně liší od formy systémové, proto je před stanovením definitivní diagnózy nutné pečlivé rozlišení obou stavů. Přechod ložiskové ALA ve formu systémovou je velmi vzácný a byl popsán jen raritně [Paccalin, 2005].
10.2. Léčba ložiskové AL amyloidózy
V případě místních projevů ložiskové ALA se uplatňuje opakované chirurgické odstranění a mikroabraze místních ložiskových mas v rámci laryngoskopie a bronchoskopie s eventuální dilatací a případným zavedením silikonového stentu. Velmi příznivé zkušenosti jsou zejména v laryngeální oblasti s použitím Nd: YAG nebo CO2 laseru, vedoucí k dlouhodobé stabilizaci procesu [Motta, 2003; Kurrus, 1998; Harris, 2021]. V případě tracheobronchiální amyloidózy způsobující závažné zúžení dýchacích cest s výraznou inspirační dechovou tísní je nutná tracheotomie. Vzhledem k radiosenzitivitě plazmocelulárních elementů a tím i možnosti lokálního potlačení produkce amyloidogenních LŘ lze individuálně úspěšně využít zevní ložiskovou aktinoterapii formou 10–12 frakcí v celkové dávce 20–45 Gy. Té zpravidla předchází lokální odstranění amyloidových mas [Kalra, 2001; Kurrus, 1998; Neuner, 2012; Bertelsen, 2021]. Rovněž lze zvážit i použití endobronchiální brachyterapie [Moore, 2018]. V případě postižení močových cest lze vedle transuretrální resekce vyzkoušet i rozpuštění fibril amyloidu opakovanou instilací dimetylsulfoxidu do močového měchýře a u malých lézí ošetření laserem. U kožních forem se vedle chirurgické excize a ošetření laserem může uplatnit intralezionální aplikace kortikosteroidů a dermabraze. Systémová chemoterapie vč. léčby kortikosteroidy se pro svou neúčinnost u ložiskové ALA nedoporučuje [Bird, 2004; Dominguez, 1996]. Ložisková ALA je v podstatě nevyléčitelná a většinou proto vyžaduje opakovanou lokální léčbu. Přestože má ve srovnání se systémovou ALA mnohem příznivější prognózu, je i ložisková ALA provázena významnou morbiditou, která závisí na závažnosti postižení a orgánové lokalizaci [Buadi, 2010].
11. CÍLE LÉČBY A HODNOCENÍ LÉČEBNÉ ODPOVĚDI U AL AMYLOIDÓZY
Cílem léčby AL amyloidózy je eliminace produkce amyloidogenních lehkých řetězců klonálními plazmocyty. Redukce, resp. eliminace, nálože amyloidogenních lehkých řetězců a současně produkující klonální plazmocelulární populace je podmínkou dosažení hematologické remise onemocnění. Dosažení hematologické remise onemocnění je předpokladem pro dosažení orgánových léčebných odpovědí při postižení jednotlivých orgánových systémů, tedy zlepšení jejich funkce a prodloužení přežití nemocných [Merlini, 2006]. Palladini at al. definoval velmi dobrou parciální remisi (VGPR) onemocnění jako minimální míru hematologické léčebné odpovědi, která by měla být léčbou dosažena (úroveň důkazu IIa, stupeň doporučení B) [Palladini, 2012a].
Při hodnocení léčby AL amyloidózy se udává míra hematologické léčebné odpovědi, která je definována na základně stanovení hladin MIg v séru či moči a/nebo FLC a na základě vyšetření kostní dřeně [IMWG, 2003; Kyle, 2009]. Dále se stanovuje tzv. orgánová léčebná odpověď, jež je definována dalšími laboratorními a paraklinickými údaji vyjadřujícími funkční schopnost orgánů postižených depozity amyloidu [Gertz, 2005; Gertz, 2010b; Comenzo, 2012]. Definici hematologických léčebných odpovědí uvádí tab. 11, definice orgánových odpovědí jsou uvedeny v tab. 12.
Tab. 11. Definice hematologických léčebných odpovědí u pacientů s AL amyloidózou [Gertz, 2005; Gertz, 2010b; Comenzo, 2012]. ![Definice hematologických léčebných odpovědí u pacientů s AL amyloidózou [Gertz, 2005; Gertz, 2010b;
Comenzo, 2012].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/08ad42c627dc07b7a360fe92dd3a5113.jpg)
CR – kompletní remise, dFLC – rozdíl mezi koncentrací dominantního a alternativního lehkého řetězce v séru, NR – no response – stabilní onemocnění – nenaplněna kritéria PR ani progrese, PR – parciální remise, VGPR – velmi dobrá parciální remise Tab. 12. Definice orgánových léčebných odpovědí u pacientů s AL amyloidózou [Gertz, 2005; Gertz, 2010b; Comenzo, 2012]. ![Definice orgánových léčebných odpovědí u pacientů s AL amyloidózou [Gertz, 2005; Gertz, 2010b;
Comenzo, 2012].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/3629a531e622e5fbedf8641b0595f7e1.jpg)
12. LÉČEBNÉ STRATEGIE U AL AMYLOIDÓZY V ROCE 2022
AL amyloidóza je vzácné hematologické onemocnění a řada doporučení pro léčbu je vytvořena zpravidla na základě nekontrolovaných léčebných studií. U nemocných, u kterých je AL amyloidóza asociována s mnohočetným myelomem, se doporučovaná léčebná schémata neliší od terapeutických doporučení pro toto onemocnění s respektováním indikačních kritérií, kontraindikací a cíle dosažení alespoň velmi dobré parciální remise [Hájek 2018]. V současné době není zcela jasný mezinárodní konsensus stran optimální terapie pro nově diagnostikované pacienty s AL amyloidózou. Léčebná strategie je zaměřena na eliminaci fibrilárních prekurzorů, respektive volných lehkých řetězců, které jsou schopny infiltrovat extracelulární prostor cílových orgánů a po jistém čase způsobit jejich závažnou dysfunkci. Ta je především v případě poškození srdce velmi často fatální [Ryšavá 2018]. AL amyloidóza je zpravidla velmi senzitivní onemocnění, léčba nemusí být zpravidla tak intenzivní jako např. u mnohočetného myelomu. Tento názor podporuje i skutečnost, že nemocní s AL amyloidózou jsou častěji náchylní k závažným komplikacím, což souvisí s poškozením orgánů často vstupně skrytým. Mezi experty se stále více prosazuje názor, že by v případě nové diagnózy (ale i relapsů) měla být cílem hematologická kompletní remise, tedy eradikace klonu plazmocytů s produkcí volných lehkých řetězců [Gertz 2007]. Lze očekávat, že se zvyšujícím se počtem dostupných účinných léků bude tato léčebná strategie stále více preferovanou, třebaže stávajícím doporučením je dosažení nejméně velmi dobré parciální remise [Palladini, 2012a]. Nové léčebné možnosti umožňují nasazení jiné léčby v případě neúspěchu léčby první, což zcela jistě zvýší počet nemocných dosahujících kompletní hematologickou remisi. Je vhodné zdůraznit, že k průkazu léčebné odpovědi v případě orgánového postižení potřebujeme trpělivost, neboť někdy ji můžeme správně vyhodnotit až s odstupem 12–18 měsíců [Gavriatopoulou, 2018].
Existuje jen málo randomizovaných studií srovnávajících různé terapeutické přístupy a většina z nich nezahrnuje nejnovější léky nebo rizikovou stratifikaci. Nicméně v zahraničí je v řadě zemí péče o nemocné s AL amyloidózou směřována do velkých center a lze z části navázat na doporučení těchto pracovišť. Tato doporučení jsou běžně odbornou veřejností celosvětově akceptována a je nutné podotknout, že doporučení významných světových center se obsahově výrazně neliší [Wechalekar, 2015; Dispenzieri, 2015; Palladini, 2016]. V současnosti se v případě AL amyloidózy preferuje tzv. „risk-adapted“ přístup, tedy léčba pacientovi „šitá na míru“ dle stratifikačních kritérií uvedených v předchozích kapitolách. Efektivní využití srdečních biomarkerů a dalších parametrů usnadnilo selekci nemocných k vysokodávkované terapii a snížilo peritransplantační mortalitu, stejně tak napomohlo i ve výběru konvenční terapie. S ohledem na relativní vzácnost onemocnění by mělo být u všech nemocných zváženo zařazení do klinických studií.
Všeobecně se u nemocných do 70 let věku a schopných podstoupit intenzivní přístup preferuje léčba vysokodávkovaným alkeranem s podporou autologních kmenových buněk, tedy autologní transplantace (ASCT). S ohledem na míru nálože klonálních buněk a hladin lehkých řetězců je na individuálním zvážení podání 2–4 cyklů indukční terapie s následnou stimulací a sběrem periferních kmenových buněk [Dispenzieri, 2015; Palladini, 2016]. Nicméně pouze 14–24 % pacientů je schopno tento přístup podstoupit. U nemocných s počtem klonálních buněk v kostní dřeni nad 10 %, tedy v případě asociace s mnohočetným myelomem, je indukční léčba doporučována vždy. Konvenční terapie zahrnuje kombinované režimy s kortikoidy, alkylačními cytostatiky, bortezomibem a nejnověji daratumumabem, který představuje zásadní pokrok v prohloubení léčebné odpovědi. Výsledky publikovaných prací hovoří přibližně o 70% přežití v 5 letech u nemocných, kteří konvenční terapií dosáhnou kompletní remise; v případě ASCT a dosažené CR je udáváno 60% přežití v 10 letech, avšak jedná se vesměs o selektovanou skupinu nemocných [Sanchorawala, 2007a; Palladini, 2007; Gertz, 2007; Staron, 2021].
Schéma vhodné terapie pro pacienty s nově dg. AL amyloidózou je uvedeno v tab. 13.
Tab. 13. Schéma vhodné terapie pro pacienty s nově dg. AL amyloidózou [upraveno dle Mayo clinic; Dispenzieri, 2015; Muchtar, 2021; Sidiqi, 2021]. ![Schéma vhodné terapie pro pacienty s nově dg. AL amyloidózou
[upraveno dle Mayo clinic; Dispenzieri, 2015; Muchtar, 2021; Sidiqi, 2021].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/d1be20290c20a66c57a12497e3b12acd.jpg)
ASCT – autologní transplantace, BMDex – bortezomib, melfalan, dexametason, CyBorD – cyklofosfamid, bortezomib, dexametason, Dara – daratumumab, MDex – melfalan, dexametason, VGPR – velmi dobrá parciální remise 13. AUTOLOGNÍ TRANSPLANTACE KRVETVORNÝCH BUNĚK (ASCT)
Autologní transplantace krvetvorných buněk (ASCT) byla poprvé popsána jako efektivní terapie u AL amyloidózy v roce 1998 [Comenzo, 1998]. Při použití přípravného režimu melfalan 200 mg/m2 s následnou ASCT bylo dosaženo 76 % hematologických odpovědí, 33 % CR, peritransplantační mortalita byla 12–13 % [Gertz, 2004; Skinner, 2004]. Medián přežití transplantovaných pacienů byl 4,7 roku [Sanchorawala, 2007a].
Bylo ovšem také publikováno, že pacienti s pokročilým orgánovým postižením při AL amyloidóze mají vysoké riziko úmrtí v souvislosti s transplantací (TRM), až 40 % [Moreau, 1999]. Proto bylo vyvinuto úsilí pacienty stratifikovat podle rizika před případným provedením ASCT [Gatt, 2013]. V současnosti jsou definována indikační kritéria umožňující posoudit klinický stav nemocného a určit, zdali je vhodným kandidátem ASCT [Dispenzieri, 2015; Palladini, 2016]. Při výběru nemocných dle těchto indikačních kritérií se míra TRM pohybuje v centrech na úrovni 3 %. Míra léčebných odpovědí přesahuje 70 %, s 35–37 % kompletních remisí [Sanchorawala, 2015; D‘Souza, 2015, Cibeira, 2011, Ryšavá,2011, Sidiqi, 2018]. Lze konstatovat, že pro provedení ASCT je vhodná selektovaná skupina pacientů s AL amyloidózou, tito nemocní s nízkou mírou orgánového postižení však z této terapie profitují (úroveň důkazu IIa, stupeň doporučení B) [Gatt, 2013].
Indikační kritéria pro stratifikaci nemocných k vysokodávkované chemoterapii melfalanem s podporou autologního štěpu uvádí tab. 14.
Tab. 14. Indikační kritéria pro stratifikaci nemocných k vysokodávkované chemoterapii melfalanem s podporou autologního štěpu (úroveň důkazu IV, stupeň doporučení C) [Dispenzieri, 2015; Palladini, 2016; Sanchorawala, 2021]. ![Indikační kritéria
pro stratifikaci nemocných
k vysokodávkované
chemoterapii melfalanem s
podporou autologního štěpu
(úroveň důkazu IV, stupeň
doporučení C) [Dispenzieri, 2015;
Palladini, 2016; Sanchorawala,
2021].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/44deb336fac2426e0a5dea4eb2192f43.jpg)
13.1. Léčebná účinnost vysokodávkované chemoterapie s následnou ASCT
Pouze jediná prospektivní multicentrická randomizovaná studie, srovnávající klasickou chemoterapii melfalan a dexametazon s ASCT, byla studie francouzských autorů [Jaccard, 2007]. Do každé skupiny bylo zařazeno 50 pacientů. Medián přežití ve skupině léčené vysokodávkovanou chemoterapií byl 22,2 měsíce, medián přežití ve skupině léčené klasickou chemoterapií byl 56 měsíců. Z pacientů randomizovaných do skupiny vysokodávkované chemoterapie zemřelo ještě před podáním vysokodávkované chemoterapie celkem 10 osob, ASCT nakonec podstoupilo pouze 37 nemocných. Z nich dalších 9 zemřelo do dne 100 po transplantaci. Tato studie nepotvrdila lepší výsledky vysokodávkované chemoterapie oproti standardní chemoterapii melfalan a dexametazon. Řadou autorů je poukazováno na ne zcela optimální výběr pacientů pro ASCT v této klinické studii, a dále vysoký počet zařazujících center s malým počtem nemocných (a tedy s omezenou zkušeností s metodou), což vedlo ke značné mortalitě před i po provedení ASCT [Adam, 2013].
Nicméně řada prací referuje o účinnosti ASCT, udává 32–68 % hematologických odpovědí (16–50 % CR) a 31–64 % orgánových odpovědí. Respektive 35–37 % kompletních remisí při 3–3,4 % TRM [Sanchorawala, 2015; D‘Souza, 2015].
Redukce dávky melfalanu na 140 mg/m2 je doporučována u pacientů s clearancí kreatininu < 30 ml/min [Dispenzieri, 2015]. Redukce dávky melfalanu u rizikových nemocných však snížila počet hematologických odpovědí při stejné míře TRM [Gertz, 2004], a proto není běžně doporučována (úroveň důkazu IV, stupeň doporučení C). Efektivitu a mortalitu ASCT u AL amyloidózy shrnuje tab. 15.
Tab. 15. Výsledky multicentrických a velkých unicentrických studií popisujících výsledky vysokodávkované chemoterapie u pacientů s AL amyloidózou. 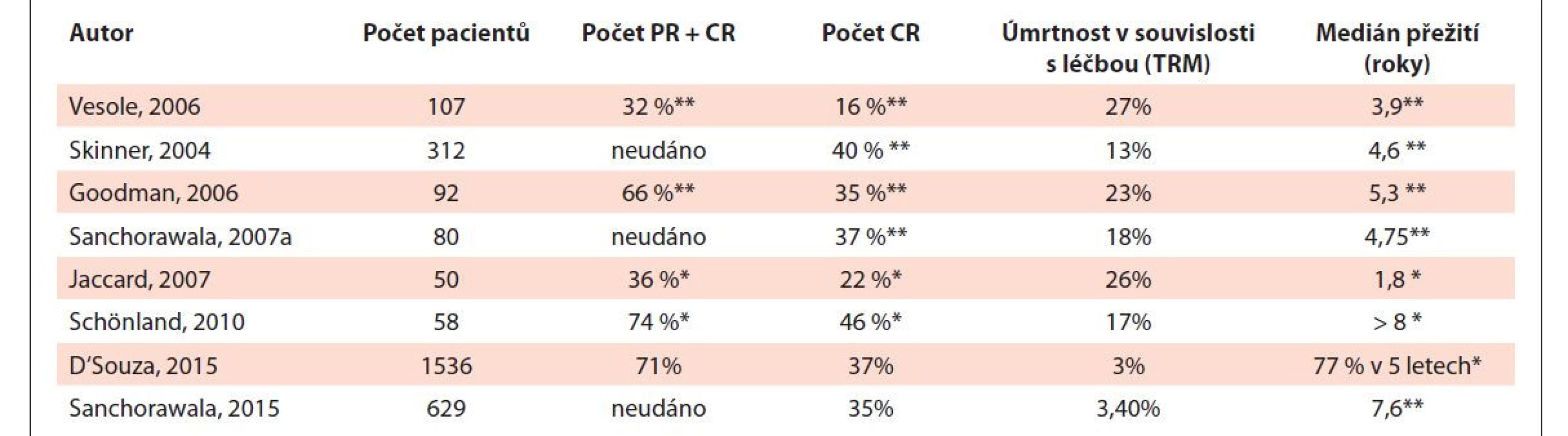
* jde o analýzu vycházející z počtu pacientů zařazených do studie (intent to treat analysis)
** jde o analýzu pouze těch pacientů, kteří dokončili léčbu14. KONVENČNÍ LÉČBA ZALOŽENÁ NA KOMBINACI VYSOKÝCH DÁVEK DEXAMETAZONU A ALKYLAČNÍCH CYTOSTATIK
14.1. Kombinace alkylačního cytostatika a kortikoidu
Alkylační látky jsou hlavními cytostatiky, která byla po desítky let používána u mnohočetného myelomu (MM) a byla následně terapeuticky využita i u AL amyloidózy [Kyle, 1997]. Ačkoli perorální terapie melfalanem a prednisonem je u AL amyloidózy dobře tolerovaná a prodlužuje přežití ve srovnání s neléčenými pacienty, léčebné odpovědi jsou nízké (30 %) a jsou dosahovány pomalu, obvykle více než po roce terapie [Skinner, 1996; Kyle, 1997].
Naopak oproti prednisonu byla pozorována u AL amyloidózy efektivita dexamethasonu ve vyšší dávce [Dhodapkar, 1997]. Klinické studie kombinující orální melfalan a pulsní dexametazon (MDex) referují o 26–72 % hematologických odpovědí s přibližně 8–33 % kompletních remisí. Míra orgánových léčebných odpovědí dosahuje až 48 %. V italské studii u pacientů s AL amyloidózou, kteří nebyli vhodní pro provedení ASCT, bylo dosaženo vysoké celkové léčebné odpovědi 67 %, z toho u 33 % pacientů kompletní remise, a také byla zaznamenána nízká úmrtnost v souvislosti s terapií (4 %) [Palladini, 2004; Palladini 2007]. Medián doby do progrese pacientů léčených kombinací MDex byl 3,8 roku a medián celkového přežití 5,1 roku. Terapie MDex byla v minulosti široce akceptovanou léčbou první linie pro pacienty s AL amyloidózou, kteří nejsou vhodnými kandidáty pro provedení ASCT (úroveň důkazu IIa, stupeň doporučení B). V současnosti lze režim MDex využít v první linii u nemocných s kontraindikací bortezomibu a daratumumabu [Al Hamed, 2021].
14.2. Nežádoucí účinky léčby a selekce nemocných
Terapeuticky problematičtí jsou pacienti s AL amyloidózou a pokročilým kardiálním postižením a obvykle špatně tolerující vyšší dávky dexametazonu. Ovšem snížení dávky ze 40 mg na 20 mg v dny 1–4 cyklu bylo spojeno se signifikantně nižším počtem CR (16 vs. 31 %) [Palladini, 2010]. Podání MDex u pacientů s pokročilým kardiálním postižením nevykazuje dobré výsledky, hematologická léčebná odpověď je udávána pouze 44 % a 26 % pacientů umírá v průběhu léčby [Dietrich, 2010]. Nicméně se zdá, že z léčebné kombinace profitují zejména nemocní ve středním riziku (stádia do IIIa). Palladini at al. uvádí 76 % hematologických odpovědí (31 %) s mediánem přežití 7,3 let pro tuto skupinu nemocných, což je srovnatelné s ASCT. Lze tedy konstatovat, že terapie MDex je bezpečná a efektivní především u pacientů se středním rizikem kardiálního postižení nebo bez kardiálního postižení, avšak není schopna překonat špatnou prognózu nemocných s pokročilým kardiálním postižením [Gatt, 2013; Palladini, 2004].
15. IMUNOMODULAČNÍ LÉKY V TERAPII AL AMYLOIDÓZY
15.1. Thalidomid v léčbě AL amyloidózy
Užití thalidomidu jako monoterapie či v kombinaci s kortikoidy a alkeranem bylo předmětem řady studií. Monoterapie thalidomidem se však neprojevila jako účinná, většinou nebylo dosaženo hematologické odpovědi (0–25 %), v kombinaci s kortikoidy pak s dosažením 48 % hematologické odpovědi. Nicméně terapie byla spojena s nezanedbatelnou nehematologickou toxicitou thalidomidu (až v 65 %), zejména časté byly projevy symptomatické bradykardie a symptomy spojené s neurotoxicitou [Palladini, 2005; Seldin, 2003; Dispenzieri, 2003]. Palladini at al. užil léčebnou kombinaci thalidomidu, alkeranu a dexametasonu ve skupině 22 nemocných s kardiálním postižením [Palladini, 2009]. Míra léčebné hematologické odpovědi dosáhla 36 %, nicméně toxicita nebyla zanedbatelná a pouze 20 % nemocných se dožilo 1 roku. Naopak britská studie referující o kombinaci thalidomidu, cyklofosfamidu a dexametasonu u nově diagnostikovaných pacientů vypovídá o efektivitě režimu s 74% hematologickou odpovědí (21 % CR) a 77% přežitím ve 2 letech [Wechalekar, 2007]. Nicméně i tato kombinace byla spojena s vyšší mírou zejména nehematologické toxicity. Kombinaci thalidomidu, dexametasonu a cyklofosfamidu lze ve vybraných případech zvážit jako iniciální léčebný režim, avšak s vyšším rizikem nežádoucích účinků léčby (úroveň důkazu IIa, stupeň doporučení B). V současné době jsou však režimy s thalidomidem považovány za obsolentní.
15.2. Lenalidomid v léčbě AL amyloidózy
Většina prací referujících o účinnosti lenalidomidu u nemocných s AL amyloidózou bohužel zahrnuje předléčené i nově diagnostikované pacienty, proto i interpretace dat je poměrně složitá. Kombinace lenalidomidu a dexametasonu bývá spojena s 38–47% hematologickou odpovědí (5–16 % CR) a mediánem přežití 1–2 roky u relabujících/refrakterních pacientů [Sanchorawala, 2007b; Palladini, 2012b]. Nicméně terapie u nemocných s AL amyloidózou je často spojena s významnou renální a kardiální toxicitou a celkovou alterací stavu, proto zejména u nemocných s renální nedostatečností či vysokou proteinurií by měla být léčba vedena velmi obezřetně [Specter, 2011]. Léčba bývá navíc spojena i s významným vzestupem v hodnotách kardiálních biomarkerů, zejména natriuretických peptidů, což mimo jiné činí posouzení srdeční orgánové odpovědi velmi problematické [Tapan, 2010]. Ve studii Moreau at al. bylo užito kombinace lenalidomidu, alkeranu a dexametasonu u 26 nemocných s nově diagnostikovanou AL amyloidózou. Celkem 58 % nemocných dosáhlo hematologické odpovědi, vč. 23 % kompletních remisí [Moreau, 2010]. Některé studie se stejným léčebným režimem však referují o nižším procentu léčebných odpovědí. Práce hodnotící kombinaci lenalidomidu, dexametasonu a cyklofosfamidu v souborech z části předléčených pacientů uvádějí přibližně 60 % hematologických odpovědí (5–11 % CR) [Palladini, 2013, Kumar, 2012].
Režimy s lenalidomidem nejsou v současnosti doporučovány v iniciální terapii nemocných s AL amyloidózou, nicméně jsou léčebnou možností pro nemocné refrakterní na režimy s bortezomibem či jiná chemoterapeutika, či pro nemocné s významnou polyneuropatií (úroveň důkazu IIa, stupeň doporučení B). Iniciální dávka je doporučována 15 mg/den. Lék není v ČR v roce 2021 pro léčbu AL amyloidózy registrován a je nutné žádat úhradu.
15.3. Pomalidomid v léčbě AL amyloidózy
Pomalidomid v kombinaci s dexametasonem byl iniciálně testován ve skupině předléčených nemocných v práci z Mayo clinic. Míra léčebných odpovědí dosáhla 41 %, v případě IMID-refrakterních nemocných 43 %. Jednoleté přežití dosahovalo 77 % [Dispenzieri, 2007]. Jiná studie hovoří o 50% léčebné odpovědi [Sanchorawala, 2016]. Palladini at al. ve studii s 28 pacienty s relabující/refrakterní AL amyloidózou uvádí 68 % léčebných odpovědí, vč. 29 % VGPR/CR [Palladini, 2012]. Pomalidomid v kombinaci s kortikoidy není doporučován pro iniciální terapii nemocných s AL amyloidózou (úroveň důkazu IIa, stupeň doporučení B). Lze jej však zvážit u relabujících/refrakterních pacientů v dobré klinické kondici. Lék není v ČR v roce 2021 pro léčbu AL amyloidózy registrován a je nutné žádat úhradu.
Přehled některých klinických zkušeností s léčbou AL amyloidózy imunomodulačními látkami uvádí tab. 16.
Tab. 16. Přehled některých klinických zkušeností s léčbou AL amyloidózy imunomodulačními látkami. 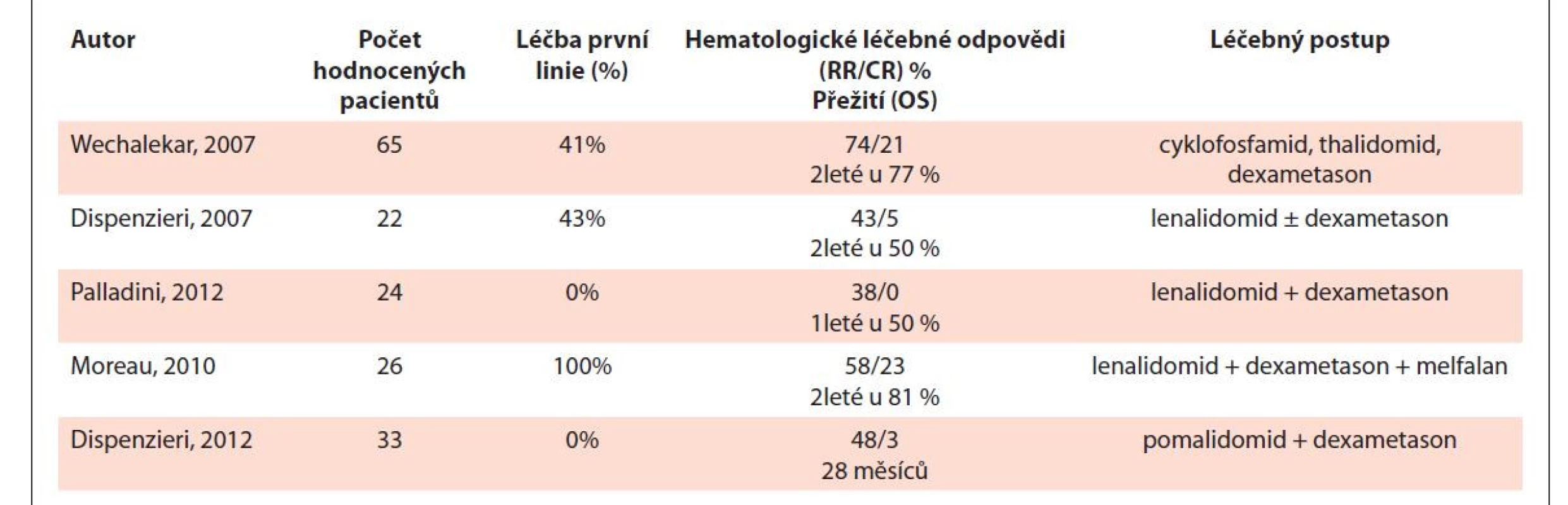
CR – kompletní remise, OS – celkové přežití, RR – response rate čili počet celkových hematologických léčebných odpovědí (CR + VGPR + PR) 16. INHIBITORY PROTEASOMU V LÉČBĚ AL AMYLOIDÓZY
16.1. Bortezomib v léčbě AL amyloidózy
16.1.1. Bortezomib v monoterapii a v kombinaci s dexametasonem
Bortezomib v monoterapii byl prospektivně hodnocen v klinické studii fáze I/II s eskalací dávek a dobrou tolerancí až do dávky 1,6 mg/m2 1× týdně nebo 1,3 mg/m2 2× týdně [Comenzo, 2010; Reece, 2011]. Hematologická odpověď byla 39 % (CR 11 %) při nižších dávkách, při dávce 1,6 mg/m2 1× týdně byla hematologická odpověď 69 % (z toho CR 38 %) a 67 % (z toho CR 24 %) při dávce 1,3 mg/m2 2× týdně [Comenzo, 2010]. Čas do dosažení léčebné odpovědi byl kratší při dávkovacím schématu 2× týdně, ovšem dávkovací schéma 1× týdně bylo lépe tolerováno. Kombinace bortezomibu a dexamethasonu (BDex) je spojena s vysokým procentem hematologických léčebných odpovědí (80–94 %) [Kastritis, 2007]. Retrospektivní studie 94 pacientů s AL amyloidózou udává hematologickou odpověď 71 %, z toho bylo dosaženo 25 % CR, dříve neléčení pacienti dosáhli CR v 47 % případů [Kastritis, 2010]. Medián doby do dosažení hematologické odpovědi byl 1,7 měsíce. Kombinace bortezomibu a dexametasonu je doporučována v iniciální terapii i léčbě relabujících nemocných s AL amyloidózou.
V případě nemocných s přítomností t (11; 14) léčených kombinací bortezomibu a dexametasonu či CyBorD byla zaznamenána nižší míra léčebných odpovědí i celkového přežití. Proto by u těchto nemocných měla být zvážena ASCT (neboť ASCT nepříznivý vliv t (11; 14) stírá) či kombinované schéma s alkeranem [Bochtler, 2015; Muchtar, 2017].
16.1.2. Kombinovaná schémata s bortezomibem
V současné době jsou ponejvíce v první linii terapie, ale i u relabujících nemocných doporučována kombinovaná schémata bortezomibu, dexametasonu a alkylačních cytostatik, neboť jsou spojena s nejvyšším procentem nejen hematologických, ale i orgánových odpovědí při akceptovatelné toxicitě (úroveň důkazu IIa, stupeň doporučení B).
Jedna z prvních prací Mikhaela et al. uvádí, že kombinace cyklofosfamidu, bortezomibu a dexamethasonu (CyBorD) vedla k dosažení VGPR/CR u 16 z 17 léčených pacientů [Mikhael, 2012] s minimální toxicitou. I řada dalších prací udává míru hematologické léčebné odpovědi v rozmezí 62–94 % při 17–61 % CR. V současné době největší publikovaný soubor zahrnoval 230 pacientů, kteří obdrželi kombinaci CyBorD, a ve kterém bylo dosaženo 62 % hematologických remisí, z čehož 21 % bylo kompletních [Palladini, 2015]. V této práci však byla identifikována skupina nemocných ve stádiu III Mayo klasifikace s hladinami NT-proBNP nad 8500 pg/ml (tedy stádium IIIb) s výrazně krátkým přežitím a ve které byla zaznamenána 66% míra úmrtí v prvních 12 měsících. Ačkoliv 39 % těchto nemocných vykazovalo hematologickou léčebnou odpověď, bohužel nadále byla u těchto pacientů sledována srdeční progrese onemocnění.
Venner at al. porovnával soubor 69 pacientů léčených režimem CyBorD a 69 nemocných léčených režimem CTD. Léčba režimem CyBorD byla spojena s vyšším procentem kompletních remisí (40 vs. 25 %) a delší dobou do progrese (28 vs 14 měsíců), jednoleté přežití bylo identické pro obě skupiny nemocných (65 vs. 67 %) [Venner, 2014]. Pokud nelze užít kombinovaný režim s daratumumabem, tak režim CyBorD představuje optimální režim pro indukční terapii před ASCT s ohledem na plánovaný bezpečný a dostatečný sběr periferních kmenových buněk.
V současnosti existuje jediná randomizovaná studie porovnávající kombinaci bortezomibu, alkeranu a dexametasonu (BMDex) s alkeranem a dexametasonem (MDex). Režim BMDex byl spojen s rychlejším efektem terapie, vyšším počtem hematologických odpovědí (81 vs. 57 %) i větší hloubkou odpovědi (CR/VGPR 64 vs. 39 %) a s prodloužením celkového přežití (medián nedosažen vs. 34 měsíců). Míra orgánové léčebné odpovědi byla u hodnocených nemocných stejná. Režim Mdex byl naopak spojen s nižší toxicitou [Kastritis, 2016; Kastritis, 2020]. Režim BMDex je považován za standard pro nově diagnostikované pacienty s AL amyloidózou, kteří nejsou referováni k ASCT a u kterých není možné užít režim s daratumumabem [Muchtar, 2021, Al Hamed, 2021] (úroveň důkazu Ib, stupeň doporučení A).
Přehled některých klinických studií s bortezomibem u pacientů s AL amyloidózou uvádí tab. 17.
Tab. 17. Přehled některých klinických zkušeností s léčbou AL-amyloidózy bortezomibem v monoterapii nebo v kombinaci s dalšími léky. 
CR – kompletní remise, PFR – progression free survival neboli délka přežití bez progrese, RR – response rate čili počet léčebných odpovědí
(CR + VGPR + PR), VGPR – velmi dobrá parciální remise16.1.3. Nežádoucí účinky léčby
Nežádoucí účinky terapie bortezomibem jsou popisovány u 30 % nemocných, nejčastěji se jedná o retenci tekutin, hypotenzi, projevy polyneuropatie periferní či viscerální a gastrointestinální obtíže [Kastritis, 2010]. V současnosti jsou jako u mnohočetného myelomu preferovány režimy s týdenním podáváním bortezomibu. Sidana at al. prokázal podobnou účinnost a nižší míru neuropatií u ALA při subkutánním podání bortezomibu jedenkrát týdně ve srovnání s jinými schématy režimů na bázi bortezomibu [Sidana, 2017]. U fragilních nemocných lze zvážit redukci dávky na 1 mg/m2. Stejně jako v případě mnohočetného myelomu je doporučována profylaxe antivirotiky proti infekci virem varicella zoster.
16.2. Ixazomib a carfilzomib v léčbě AL amyloidózy
Ixazomib představuje novou generaci proteasomového inhibitoru s plně perorálním podáním. Stejně jako v případě mnohočetného myelomu, kde prokázal účinnost zejména v kombinacích, byl testován i u AL amyloidózy. Výsledky studie fáze III hodnotící ixazomib s dexametazonem vs. volba lékaře (MDex, cyklofosfamid, thalidomid, lenalidomid) u relabující/refrakterní AL amyloidózy referují o 53 vs. 51 % hematologických odpovědí, přičemž míra CR byla 26, resp. 18 %. V rameni s ixazomibem byla rovněž zaznamenána delší doba do těžkého orgánového selhání či úmrtí (34,8 vs. 26,1 měsíců). Míra celkové léčebné odpovědi byla vyšší u nemocných, kteří nebyli předléčeni bortezomibem (63 vs. 41 %). Toxicita léčby byla akeptovatelná [Sanchorawala, 2017; Dispenzieri, 2021]. Studie fáze II hodnotila ixazomib v kombinaci s p. o. cyklofosfamidem a dexametasonem u 35 nemocných s nově diagnostikovanou ALA (studie nezahrnovala nemocné s těžkým orgánovým postižením). Celková hematologická odpověď dosáhla 57 %, přičemž CR bylo dosaženo u 14 %, VGPR u 26 % a PR u 17 % pacientů. Nežádoucí účinky léčby stupně 3 a vyšší byly zaznamenány u 41 % pacientů, přičemž nejčastěji se jednalo o průjem, slabost a hematologickou toxicitu [Muchtar, 2020]. Identicky, jako u mnohočetného myelomu, byla studována kombinace ixazomibu, lenalidomidu a dexametazonu ve skupině 40 nemocných s relabující ALA. Kompletní remise byla zaznamenána u 25,6 %, VGPR u 20,5 % a PR u 18 % nemocných. Kardiální a renální odpověď byla zaznamenána u 5,6 % resp. 13,3 % nemocných. Medián přežití byl 29,1 měsíců. Nejčastějšími nežádoucími účinky byly infekce, retence tekutin a srdeční arytmie [Cohen, 2020]. Ixazomib s dexametazonem a ev. cyklofosfamidem je indikován v léčbě nemocných s relabující/refrakterní amyloidózou a u nemocných v 1. linii terapie s preexistující neuropatií, kteří nejsou vhodní k terapii bortezomibem (úroveň důkazu IIa, stupeň doporučení B).
Carfilzomib, jako další z nových typů proteasomových inhibitorů, je rovněž testován i u AL amyloidózy. Cohen at al. hodnotili kombinaci carfilzomibu a dexametasonu ve skupině 28 nemocných s relabující/refrakterní AL amyloidózou. Hematologické odpovědi bylo dosaženo u 63 % nemocných s 21 % orgánových odpovědí. Nicméně léčba byla spojena s vysokým výskytem závažných komplikací, zejména kardiálních [Cohen, 2016]. Manwani at al. hodnotili carfilzomib v kombinaci s dexametazonem u 5 nemocných s nově diagnostikovanou ALA a přítomnou autonomní a periferní neuropatií. U 3/5 pacientů bylo dosaženo CR, u 2/5 nemocných VGPR. U žádného z nemocných nedošlo ke zhoršení srdečních funkcí [Manwani, 2019]. Další studie s carfilzomibem v současnosti probíhají.
17. DARATUMUMAB V LÉČBĚ AL AMYLOIDÓZY
Monoklonální antiCD38 protilátka daratumumab je v současnosti používána u relabujících/refrakterních pacientů s mnohočetným myelomem. Milníkem v terapii nemocných s nově zjištěnou ALA se staly výsledky randomizované studie fáze 3 Andromeda, porovnávající subkutánní podání daratumumabu CyBorD proti CyBorD. Do studie byli zařazeni pacienti s nově diagnostikovanou ALA, stádia I-IIIa, randomizováni 1 : 1. Nemocní ve zkušebním rameni byli indikováni k podání 6 cyklů daratumumab-CyBorD s následnou monoterapií daratumumabem do doby progrese, intolerance či celkové délky 24 měsíců. V současnosti jsou k dispozici výsledky od 388 zařazených pacientů s mediánem sledování 11,4 měsíců. Celková léčebná odpověď byla 91,8 % ve zkušebním rameni oproti 76,7 % v rameni kontrolním, přičemž míra VGPR/CR byla 78,5 vs. 49,2 % (četnost samotné CR byla 53,3 vs. 18,1 %). Srdeční a renální odpověď byla registrována u 41,5 vs. 22,2 %, resp. 53 vs. 23,9 %. Nemocní ve zkušebním rameni měli nižší riziko fatálního selhání orgánů, hematologické progrese či úmrtí (0,58; 95% CI, 0,36–0,93; p = 0,02). Nejčastějšími nežádoucími účinky stupně 3 a 4 ve zkušebním rameni byly lymfopenie (13 %), pneumonie (7,8 %), srdeční selhání (6,2 %) a průjem (5,7 %). Na podkladě výsledků studie Andromeda byla kombinace daratumumab-CyBorD schválena ve Spojených státech i v Evropské únii jako inciální léčba pro nemocné s nově diagnostikovanou ALA, stádia I-IIIA. Režim daratumumab-CyBorD je indikován jako terapie první linie pro nemocné s nově diagnostikovanou ALA (úroveň důkazu Ib, stupeň doporučení A) [Palladini, 2020; Kastritis, 2021b].
V případě konsolidační terapie, recentní práce Kastritis at al. referuje o užití měsíční (4 aplikace po týdnu) konsolidace daratumumabem u nemocných, kteří nedosáhli CR po konvenční léčbě CyBorD. Dodatečné dosažení CR bylo zaznamenáno u 32 % nemocných [Kastritis; 2021a].
V případě nemocných s relabovanou/refrakterní ALA byla rovněž publikována řada prací dokazující efekt daratumumabu v monoterapii či kombinační léčbě. Ve studii fáze II, Sanchorawala at al. léčili 22 nemocných daratumumabem v monoterapii. Celková hematologická léčebná odpověď byla 96 %, přičemž míra ≥ VGPR byla 86 %. Kardiální a renální orgánová odpověď byla zaznamenána u 50, resp. 67 % nemocných [Sanchorawala, 2020]. Roussel at al. hodnotili efekt monoterapie daratumumabem u 40 nemocných. Míra léčebné odpovědi ≥ VGPR byla u 48 % nemocných, kardiální a renální odpověď byla zaznamenána u 25, resp. 31 % nemocných [Roussel, 2020]. Kaufman at al. referuje o výborném efektu terapie ve skupině 25 nemocných s relabující/refrakterní AL amyloidózou, kdy hematologické odpovědi bylo dosaženo u 76 % nemocných, přičemž procento CR dosahovalo 36 %. Terapie byla dobře tolerována i u nemocných se srdečním postižením a medián dosažení léčebné odpovědi představoval jeden měsíc [Kaufman, 2017]. Kimmich at al. hodnotili 168 nemocných léčených kombinací daratumumabu a dexametazonu (106) a daratumumabu, bortezomibu a dexametazonu (62). Léčebná odpověď ≥ VGPR byla zaznamenána u 48 a 55 %, míra srdeční léčebné odpovědi byla 22 a 26 % [Kimmich, 2020]. Daratumumab v monoterapii či kombinovaných schématech je indikován u nemocných s refrakterní/relabující ALA (úroveň důkazu IIa, stupeň doporučení B).
18. VENETOCLAX V LÉČBĚ AL AMYLOIDÓZY
Venetoclax je perorální inhibitor BCL-2 indukující apoptózu nádorových buněk a je užíván v léčbě nemocných s chronickou lymfocytární leukémií a non-Hodgkinovými lymfomy. Je známo, že ~ 50 % nemocných s ALA je nositeli t (11; 14) a současně je známo, že tito nemocní hůře reagují na léčbu bortezomibem. Proto i venetoclax je využíván v léčbě nemocných s ALA s přítomnou t (11; 14). Sidiqi at al. hodnotili efekt venetoclaxu v monoterapii či kombinaci s dexametazonem a ev. bortezomibem u 11 nemocných s relabující/refrakterní amyloidózou. U 8 nemocných bylo možno hodnotit efekt terapie, přičemž 4 nemocní dosáhli CR, 3 nemocní VGPR a jeden nemocný na terapii neodpověděl. Míra léčebné dopovědi byla tedy 88 %. U žádného nemocného nebyl zaznamenán syndrom nádorového rozpadu, nejčastějším nežádoucím účinkem léčby byly dyspepsie [Sidiqi, 2020]. V další, větší retrospektivní studii bylo hodnoceno 43 nemocných s refrakterní/relabující ALA léčených režimy s venetoclaxem. V souboru bylo 31 nemocných nositeli t (11; 14), u 11 naopak translokace prokázána nebyla. Pacienti s t (11; 14) měli vyšší míru celkové léčebné odpovědi (81 vs. 40 %) i vyšší míru VGPR/CR odpovědí (78 vs. 30 %). Medián přežití nebyl u pacientů s t (11; 14) dosažen, oproti 6,7 měsíců ve druhé skupině. Orgánová léčebná odpověď byla zaznamenána v 38 %, zejména u nemocných s t (11; 14). Nežádoucí účinky léčby stupně 3 a vyšší byly zaznamenány u 19 % pacientů, přičemž v 7 % se jednalo o infekční komplikace [Premkumar, 2021]. Efekt venetoclaxu u relabovaných nemocných s ALA a t (11; 14) byl potvrzen i dalšími pracemi [Gounot, 2021; Nahi, 2021]. Venetoclax je možno užít v terapii relabujících/refrakterních ALA nemocných s t (11; 14) (úroveň důkazu IIa, stupeň doporučení B).
19. DOXYCYKLIN V LÉČBĚ AL AMYLOIDÓZY
Mezi léky interferujícími s formací amyloidových depozit patří antibiotikum doxycyklin. Preklinické studie prokázaly, že doxycyklin dokáže přerušit amyloidové fibrily u AL i transthyretinové amyloidózy. Wechalekar at al. v retrospektivní studii prokázal, že přidání doxycyklinu (100 mg 2× denně po jídle) k terapii u nemocných s kardiální amyloidózou vedlo k redukci časné mortality, k vyšší četnosti léčebných odpovědí (≥ PR 93 vs. 59 %) a delšímu přežití (medián nedosažen vs. 13 měsíců vůči kontrolní skupině). Nemocní léčení doxycyklinem měli rovněž lepší kardiální odpověď (60 vs. 18 %) [Wechalekar, 2015b, 2017]. Nicméně recentní prospektivní randomizovaná studie hodnotící kombinaci doxycyklinu a režimu CyBorD vůči CyBorD přínos doxycyklinu neprokázala [Shen, 2021]. Další prospektivní studie s doxycyklinem však probíhají. V současnosti by tedy doxycyklin měl být zvážen jako součást iniciální terapie a antimikrobní profylaxe.
20. LÉČBA RELABUJÍCÍCH A REFRAKTERNÍCH PACIENTŮ
Tabulka 18 shrnuje doporučení pro léčbu relabujících a refrakterních nemocných. U relabující/refrakterní AL amyloidózy může být léčba opakovaná (zvláště pokud byla dříve účinná, dobře tolerovaná a délka do další progrese je klinicky významná) nebo může být zvážena léčba i jinými preparáty. K dispozici jsou data ze studií fáze II. Mezi léky s efektem u relabujících nemocných patří např. bendamustin [Lagos, 2016, Milani, 2018; ]. V léčbě relapsu je opět preferována léčba v klinických studiích, pokud jsou dostupné [Dispenzieri, 2015; Palladini, 2016].
Tab. 18. Doporučené léčebné kombinace pro relabující/refrakterní nemocné [Sidiqi,2021; Al Hamed, 2021]. ![Doporučené léčebné kombinace pro relabující/refrakterní nemocné [Sidiqi,2021; Al Hamed, 2021].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/1d3944121d28c6a4598b9ddc742ad980.jpg)
ASCT – autologní transplantace, BMDex – bortezomib, melfalan, dexametason, CyBorD – cyklofosfamid, bortezomib, dexametason, MDex – melfalan, dexametason, VD – bortezomib, dexametazon 21. PERSPEKTIVY V LÉČBĚ AL AMYLOIDÓZY
Řada dalších molekul se v současnosti jeví jako perspektivní v terapii AL amyloidózy a jejich účinek je prověřován ve studiích fáze I/II. Řada monoklonálních protilátek je cílena na amyloidová depozita.
Mezi první patřila monoklonální protilátka NEOD001, která se cíleně vázala na protofilamenta a fibrily tvořené lehkými řetězci imunoglobulinu a které byly následně odstraňovány fagocytózou. Iniciální práce fáze I/II hovořila o 60 % orgánových odpovědí [Gertz, 2016]. Nicméně studie fáze III byla na jaře roku 2018 zastavena. Další a klinické zkoušení protilátky probíhá omezeně.
Jiný princip představuje léčba cílená proti SAP (sérová amyloidová P komponenta), proteinu, jenž je součástí všech typů amyloidových depozit a chrání amyloidová depozita proti degradaci. Pepys at al. prokázali, že molekula CPHPC dokáže redukovat cirkulující hladiny SAP a následná aplikace anti-SAP monoklonální protilátky (dezamizumab) vede k indukci makrofágové odpovědi a odstraňování tkáňových amyloidových depozit [Bodin, 2010]. Pilotní studie prokázala překvapivé výsledky a v současnosti probíhají klinická hodnocení u léčených nemocných i u nemocných po proběhlé terapii [Richards, 2015].
Poslední zkoušenou protilátkou je CAEL-101 – protilátka IgG1 reagující s fibrilami lehkých řetězců imunoglobulinu s následnou resorpcí amyloidových depozit. Iniciální studie fáze 1a/b zahrnovala 27 nemocných s perzistujícím orgánovým postižením a léčebné schéma obsahovalo 4 aplikace protilátky v týdenních intervalech. Orgánová léčebná odpověď byla zaznamenána u 63 % nemocných, zejména těch se srdečním postižením [Edwards, 2021]. Studie fáze II hodnotící bezpečnost a toleranci CAEL-101 byla v kombinaci s režimem CyBorD u 13 nemocných s postižením srdce a ledvin. Studie prokázala dobrou toleranci terapie, u hodnotitelné kohorty nemocných i orgánové léčebné odpovědi. Nábor do studie fáze III v současné době probíhá [Khouri, 2020].
22. TRANSPLANTACE SRDCE, PŘÍPADNĚ JINÝCH ORGÁNŮ, NÁSLEDOVANÁ VYSOKODÁVKOVANOU CHEMOTERAPIÍ S AUTOLOGNÍ TRANSPLANTACÍ KRVETVORNÝCH BUNĚK
Těžce poškozené srdce je kontraindikací vysokodávkované chemoterapie. Ale i konvenční léčba, obsahující vysoké dávky dexametazonu, která obvykle způsobuje retenci tekutin, nemusí být proveditelná při závažném poškození srdce. Pokud jde o mladšího nemocného a ostatní orgány nejsou kriticky poškozeny, tak je možné zvážit iniciální transplantaci srdce (úroveň důkazu IV, stupeň doporučení C). Tím se výrazně zlepší celková zdatnost, a pak je možno použít vysokodávkovanou chemoterapii s podporou ASCT s cílem eradikovat patologický klon plazmocytů. V literatuře lze nalézt četné popisy menších skupin nemocných, které dokládají přínos provedení orgánové transplantace nejvíce poškozeného orgánu (tedy nejen srdce) následované léčbou amyloidózy [Adam, 2013; Gatt, 2013]. Podstatné je, aby pacient byl v celkově dobrém stavu a měl amyloidózou závažně poškozen pouze jeden orgán, který je nahrazen orgánem transplantovaným.
U vybraných nemocných s izolovaným renálním postižením a celkově limitovaným onemocněním lze zvážit provedení transplantace ledviny (úroveň důkazu IV, stupeň doporučení C). Provedení transplantace ledviny, jako náhrady vlastního selhávajícího orgánu, je doporučováno po dosažení kompletní hematologické remise onemocnění, nejčastěji v návaznosti na proběhlou ASCT. Pětileté přežití nemocných je udáváno v rozmezí 67–78 % [Dispenzieri, 2015].
Transplantace jater v případě AL amyloidózy není doporučována, prognóza nemocných je krajně nepříznivá, 5leté přežití je udáváno ve 22 % (úroveň důkazu IV, stupeň doporučení C) [Dispenzieri, 2015].
23. PODPŮRNÁ PÉČE PŘI LÉČBĚ AL AMYLOIDÓZY
Systémová AL amyloidóza je nejen hematologické, ale zejména multiorgánové postižení a nemocní jsou zpravidla postiženi zhoršením či selháním funkcí jednoho a více tělesných orgánů. Nejen v diagnostice, ale i během vedení terapie je nutná spolupráce s odborníky z jiných oborů. Nejčastější spolupracující specialisté jsou z oboru kardiologie, nefrologie, neurologie, nutriční péče a mnoho dalších. Je více než vhodné, aby při specilizovaných centrech působil multidisciplinární tým lékařů se zaměřením na problematiku amyloidóz, neboť jak bylo výše řečeno, amyloidózy představují relativně vzácnou skupinu onemocnění a bylo by vhodné péči o pacienty svěřit do rukou odborníků.
Tabulka 19 částečně shrnuje specifickou farmakologickou a nefarmakologickou podpůrnou péči o nemocné s AL amyloidózou [Dispenzieri, 2015; Palladini, 2016].
Tab. 19. Podpůrná terapie u nemocných s AL amyloidózou [upraveno dle Dispenzieri, 2015; Palladini, 2016]. ![Podpůrná terapie u nemocných s AL amyloidózou
[upraveno dle Dispenzieri, 2015; Palladini, 2016].](https://pl-master.mdcdn.cz/media/cache/media_object_image_small/media/image_pdf/6accc90fc5bacc3338ec00360551308c.jpg)
24. DOPORUČENÍ PRO LÉČBU AL AMYLOIDÓZY
- Principem léčby je eliminace patologického klonu se zastavením produkce amyloidogenních lehkých řetězců, redukcí jejich sérových hladin s cílem dosažení alespoň velmi dobré parciální hematologické remise (úroveň důkazu IIa, stupeň doporučení B).
- Dosažení hematologické léčebné odpovědi je podmínkou pro zlepšení funkce postižených orgánů a dosažení tzv. orgánové léčebné odpovědi (úroveň důkazu IIa, stupeň doporučení B).
- Léčba je volena individuálně s využitím „risk-adapted“ strategie (úroveň důkazu IV, stupeň doporučení C).
- Pouze část nemocných s AL amyloidózou splňující výběrová kritéria je možno bezpečně léčit vysokodávkovanou terapií s podporou autologního štěpu, tito nemocní s nízkou mírou orgánového postižení z této terapie profitují (úroveň důkazu IIa, stupeň doporučení B).
- Režim daratumumab-CyBorD je indikován jako terapie první linie pro nemocné s nově diagnostikovanou ALA (úroveň důkazu Ib, stupeň doporučení A)
- Režim BMDex je považován za standard pro nově diagnostikované pacienty s AL amyloidózou, kteří nejsou referováni k ASCT a u kterých není možné užít režim s daratumumabem (úroveň důkazu Ib, stupeň doporučení A).
- Kombinovaná schémata s bortezomibem jsou vhodnými léčebnými režimy pro všechny nově diagnostikované nemocné, bez ohledu na to, zda jsou či nejsou vhodnými kandidáty vysokodávkované terapie (úroveň důkazu IIa, stupeň doporučení B). Kombinovaná schémata s bortezomibem jsou vhodnými léčebnými režimy pro relabující nemocné (úroveň důkazu IIa, stupeň doporučení B).
- Ixazomib s dexametazonem a ev. cyklofosfamidem je indikován v léčbě nemocných s relabující/refrakterní amyloidózou a u nemocných v 1. linii terapie s preexistující neuropatií, kteří nejsou vhodní k terapii bortezomibem (úroveň důkazu IIa, stupeň doporučení B).
- Daratumumab v monoterapii či kombinovaných schématech je indikován u nemocných s refrakterní/relabující ALA (úroveň důkazu IIa, stupeň doporučení B).
- Schémata s imunomodulačními látkami jsou indikována u relabujících/refrakterních nemocných (úroveň důkazu IIa, stupeň doporučení B).
- Venetoclax je možno užít v terapii relabujících/refrakterních ALA nemocných s prokázanou t (11; 14) (úroveň důkazu IIa, stupeň doporučení B).
- Multioborová spolupráce při péči o nemocné s AL amyloidózou je naprosto nezbytná
SEZNAM POUŽITÝCH ZKRATEK
A-PC – klonální plazmocyty
A-V – atrio-ventrikulární blokáda
Ab2M – hemodialyzační amyloidóza
AF – alkalická fosfatáza
AI – apolipoprotein
AL – amyloid tvořený lehkými řetězci imunoglobulinu
ALA – AL amyloidóza
ALP – alkalická fosfatáza
antiCD38 – monoklonální protilátka proti receptoru CD38
aPTT – aktivovaný parciální tromboplastinový čas
ASCT – autologní transplantace krvetvorných buněk
BDex – bortezomib, dexametason
BMDex – bortezomib, melfalan, dexametason
BNP – mozkový natriumuretický peptid
CB-U – proteinurie
CMG – Česká myelomová skupina
CNS – centrální nervová soustava
CR – kompletní remise
CT – počítačová tomografie
CyBorD – cyklofosfamid, bortezomib, dexametason
ČHS – Česká hematologická společnost
dFLC – diference hladin volných lehkých řetězců imunoglobulinu
DKK – dolní končetiny
DNA – deoxyribonukleová kyselina
DPD scan – scintigrafie s užitím kyseliny 3,3-difosfono-1,2-propanodikarboxylové
eGRF – clearance kreatininu
ECHO – echokardiografie
EKG – elektrokardiografie
EMB – endomyokardiální biopsie
EMG – elektromyografie
ESRD – „End-Stage Renal Disease“
FFPE vzorky – materiál fixovaný formalinem a zalitý do parafinu
FLC – volné lehké řetězce
GF – glomerulární filtrace
GIT – gastrointestinální trakt
HCDD – nemoc z ukládání těžkých řetězců
HRCT – počítačová tomografie s vysokým rozlišením
IFE – imunofixace
IFIX – imunofixační elektroforéza
IgA – typ monoklonálního imunoglobulinu A
IgD – typ monoklonálního imunoglobulinu D
IgG – typ monoklonálního imunoglobulinu G
IgM – typ monoklonálního imunoglobulinu M
IHC – imunohistochemie
IMIdy – imunomodulační léky
IMWG – International Myeloma Working Group
KD – kostní dřeň
LCDD – nemoc z ukládání lehkých řetězců
LŘ – lehké řetězce (v séru)
M-FC – multiparametrická průtoková cytometrie
MDex – melfalan, dexametason
MGRS – Monoclonal Gammopathy of Renal Significance
MGUS – monoklonální gamapatie nejistého významu
MIg – monoklonální imunoglobulin
MM – mnohočetný myelom
MRI – magnetická rezonance
mTTR – transthyretinová hereditární amyloidóza
MW – Waldenströmova makroglobulinémie
N-PC – polyklonální plazmocyty
NGS – sekvenování nové generace
NHL – non-Hodgkinův lymfom
NR – bez léčebné odpovědi
NS – nefrotický syndrom
NT-proBNP – propeptid mozkového natriuretického peptidu
OS – celkové přežití
PC – plazmocyty
PCR – polymerázová řetězová reakce
PET/CT – pozitronová emisní tomografie/počítačová tomografie
PR – parciální remise
RR – počet léčebných odpovědí
RTG – standardní radiografie
SAA – sérový amyloid A
SAP – glykoprotein (sérová amyloidní P komponenta)
SPE – elektroforéza sérových proteinů
sy – syndrom
TK – tlak krve
TnI – troponin I
TnT – troponin T
TRM – riziko úmrtí v souvislosti s transplantací
TTR – transthyretin
UPE – elektroforéza proteinů moči
UZ – ultrazvukové vyšetření
VGPR – velmi dobrá parciální remise
wtTTR – amyloidóza z depozice nativního transthyretinu (senilní)
PODĚKOVÁNÍ
Děkujeme recenzentům jednotlivých kapitol, členům předsednictva CMG a zástupcům KLS podílejícím se na přípravě doporučení. Vydání doporučení bylo podpořeno grantem firmy Janssen Cilag „Moderní diagnostické a léčebné přístupy u nemocných s amyloidózou“.
PODÍL AUTORŮ NA RUKOPISU
T.P. – vytvoření základní osnovy guidelines, napsání rukopisu, revize rukopisu
R.H. – vytvoření základní osnovy, napsání dílčí části rukopisu, revize rukopisu
P.F., P.F. – napsání dílčí části rukopisu, připomínky, revize rukopisu
Z.A., D.H., T.J., Z.Ch., V.M., R.R., V.Š., I.Š. – připomínky, revize rukopisu
KONFLIKT ZÁJMŮ
T.P., P.F., P.F., D.H., Z.Ch., L.P., V.Š., I.Š. – ne
R.H., V.M. – honoráře, přednášky, konzultace a nefinanční podpora od firmy Janssen
T.J. – honoráře, přednášky, výzkumné granty: Amgen, Takeda, Janssen, Bristol Meyers Squibb, Sanofi
Do redakce doručeno dne 17. 1. 2022.
MUDr. Tomáš Pika
Hemato-onkologická klinika
LF UP a FN Olomouc,
e-mail: tomas.pika@seznam.cz
Zdroje
LITERATURA PRO DIAGNOSTICKOU ČÁST
- • Adam Z, Ščudla V. Klinické projevy a diagnostika AL amyloidózy a některých dalších typů amyloidóz. Vnitř Lék. 2001; 47 : 36–45.
- • Adam Z, Elleder M, Moulis M, at al. Přínos PET-CT vyšetření pro rozhodování o léčbě lokalizované nodulární formy plicní AL-amyloidózy. Vnitř Lék. 2012; 58 : 241–252. (Adam, 2012a)
- • Adam Z, Stork M, Pour L, at al. Výsledky léčby AL-amyloidózy léčebnými režimy obsahujícími bortezomib, dexametazon a dále cyklofosfamid anebo doxorubicin. Vnitř Lék. 2012; 58 : 896–903. (Adam, 2012b)
- • Alpers CE, Cotran RS. Neoplasia and glomerular injury. Kidney Int. 1986; 30 : 465–470.
- • Arbustini E, Verga L, Concardi M, at al. Electron and immuno-electron microscopy of abdominal fat identifies and characterizes amyloid fibrils in suspected cardiac amyloidosis. Amyloid. 2002; 9 : 108–114.
- • Benson MD, Buxbaum JN, Eisenberg DS, at al. Amyloid nomenclature 2020: update and recommendations by the International Society of Amyloidosis (ISA) nomenclature committee. Amyloid. 2020; 27 (4): 217–222.
- • Bijzet J, Van Gameren II, Muller Kobold AC, at al. Heavy/light chain analysis can replace IFE in an algorithm utilizing Free light chain and urinary protein electrophoresis for identification of AL amyloidosis patients. Presented at XIII International Symposium on Amyloidosis 2012.
- • Bird J. Guidelines on the diagnosis and management of AL amyloidosis. Br J Haematol. 2004; 125 : 681–700.
- • Bohle A, Wehrmann R, Eissele R, at al. The long-term prognosis of AA and AL renal amyloidosis and the pathogenesis of chronic renal failure in renal amyloidosis. Path Res Pract. 1993; 189 : 316–321.
- • Bochtler T, Hegenbart U, Kunz C, at al. Gain of chromosome 1q21 is an independent adverse prognostic factor in light chain amyloidosis patients treated with melphalan/dexamethasone. Amyloid. 2014; 21 (1): 9–17.
- • Bochtler T, Hegenbart U, Kunz Ch, at al. Translocation t (11; 14) is associated with adverse outcome in patients with newly diagnosed AL amyloidosis when treated with bortezomib-based regimens. J Clin Oncol. 2015; 33 : 1371–1378.
- • Bochtler T, Hegenbart U, Kunz Ch, at al. Prognostic impact of cytogenetic aberrations in AL amyloidosis after high-dose melphalan: a long-term follow up. Blood. 2016; 128 (4): 594–602.
- • Bradwell AR. Serum free light chain analysis (plus Hevylite) 7th. ed., Birmingham: The Binding Site Ltd, 2015, p. 296–314.
- • Chyra Kufova Z, Sevcikova T, Januska J, at al. Newly designed 11-gene panel reveals first case of hereditary amyloidosis captured by massive parallel sequencing. J Clin Pathol. 2018; 71 (8): 687–694.
- • Collins A, Smith R, Stone J. Classification of amyloid deposits in diagnostic cardiac specimens by immunofluorescence. Cardiovasc Pathol. 2009; 18 : 205–216.
- • Comenzo RL, Reece D, Palladini G, at al. Consensus guidelines for the conduct and reporting of clinical trials in systemic light-chain amyloidosis. Leukemia. 2012; 26 : 2317–2325.
- • Comenzo RL, Wally J, Kica G, at al. Clonal immunoglobulin light chain variable region germline gene use in AL amyloidosis: association with dominant amyloid-related organ involvement and survival after stem cell transplantation. Br J Haematol. 1999; 106 : 744–751.
- • Dember LM. Renal amyloidosis. In: Gertz MA, Rajkumar SV. Amyloidosis: diagnosis and treatment, 1st.ed., Springer Science, New York 2010, 129–143.
- • Dinner S, Witteles W, Witteles R, at al. M. The prognostic value of diagnosing concurrent multiple myeloma in immunoglobulin light chain amyloidosis. Br J Haematol. 2013; 161 : 367–372.
- • Dittrich T at al. Prognosis and staging of AL amyloidosis. Acta Hematol. 2020; 143 : 388–399.
- • Dispenzieri A, Kyle RA, Gertz MA, at al. Survival in patients with primary systemic amyloidosis and raised serum cardiac troponins. Lancet. 2003; 361 : 1787–1789.
- • Dispenzieri A, Gertz MA, Kyle RA, at al. Prognostication of survival using cardiac troponins and N-terminal pro-brain natriuretic peptide in patiens with primary systemic amyloidosis undergoing peripheral blood stem cell transplantation. Blood. 2004; 104 : 1881–1887. (Dispenzieri 2004a)
- • Dispenzieri A, Gertz MA, Kyle RA, at al. Serum cardiac troponins and N-terminal pro-brain natriuretic peptide: A staging system for primary systemic amyloidosis. J Clin Oncol. 2004; 22 : 3751–3757. (Dispenzieri 2004b)
- • Dispenzieri A, Lacy MQ, Katzmann JA, at al. Absolute values of imunoglobulin free light chains are prognostic in patiens with primary systemic amyloidosis undergoing peripheral blood stem cell transplantation. Blood. 2006; 107 : 3378–3383.
- • Dispenzieri A. Assessing response and prognosis in AL amyloidosis. In. Gertz MA, Rajkumar SV. Amyloidosis: diagnosis and treatment, 1st. ed. Springer Science, New York 2010, 77–93. (Dispenzieri 2010a)
- • Dispenzieri A, Dingli D, Kumar SK, at al. Discordance between serum cardiac biomarker and immunoglobulin-free light-chain amyloidosis treated with immune modulatory drugs. Am J Hematol. 2010; 85 : 757–759. (Dispenzieri 2010b)
- • Dispenzieri A, Gertz MA, Buadi F. What do I need to know about immunoglobulin light chain (AL) amyloidosis? Blood Rev. 2012; 26 : 137–154.
- • Dittrich T, Bochtler T, Kimmich Ch, at al. AL amyloidosis patients with low amyloidogenic free light chain levels at first diagnosis have excellent prognosis. Blood. 2017; 130 (5): 632–642.
- • D’Souza A, Theis J, Quint P, at al. Exploring the amyloid proteome in immunoglobulin-derived lymph node amyloidosis using laser microdissection/tandem mass spectrometry. Am J Hematol. 2013; 88 : 577–580.
- • Dogan A. Amyloidosis: Insights from proteomics. Ann Rev Pathol Mechanisms Dis. 2017; 12 (1): 277–304.
- • Esplin BL, Gertz MA. Current trends in diagnosis and management of cardiac amyloidosis. Curr Probl Cardiol. 2013; 38 : 53–96.
- • Falk RH, Comenzo RL, Skinner M. The systemic amyloidosis. New Engl J Med. 1997; 337 : 898–909.
- • Fielder K, Durie BGM. Primary amyloidosis associated with multiple myeloma. Am J Med. 1986; 80 : 413–418.
- • Fikrle M, Paleček T, Kuchyňka P, at al. Cardiac amyloidosis: A comprehensive review. Cor et Vasa. 2013; 55 (1): e60–e75.
- • Fikrle M, Paleček T, Mašek M, at al. The diagnostic performance of cardiac magnetic resonance in detection of myocardial involvement in AL amyloidosis. Clin Physiol Funct Imaging. 2016; 36 : 218–224.
- • Georgiades CS, Neyman EG, Barish MA, at al. Amyloidosis: review and CT manifestation. Radiographics. 2004; 24 : 405–416.
- • Gertz MA, Kyle RA, Greipp PR. The plasma cell labeling index: a valuable tool in primary systemic amyloidosis. Blood. 1989; 74 : 1108–1111.
- • Gertz MA, Kyle RA, Greipp PR, at al. Beta2-microglobulin predicts survival in primary systemic amyloidosis. Am J Med. 1990; 89 : 609–614.
- • Gertz MA, Greipp PR, Kyle RA. Classification of amyloidosis by the detection of clonal exces of plasma cells in the bone marrow. J Lab Clin Med. 1991; 118 : 33–39.
- • Gertz MA, Kyle RA. Amyloidosis: prognosis and treatment. Semin Arthritis Rheum. 1994; 24 : 124–138.
- • Gertz MA, Lacy MQ, Dispenzieri A. Amyloidosis: recognition, confirmation, prognosis, and therapy. Mayo Clin Proc. 1999; 74 : 490–494.
- • Gertz MA, Comenzo R, Falk RH, at al. Definition of organ involvement and treatment response in immunoglobulin light chain amyloidosis (AL): A consensus opinion from the 10th International symposium on amyloid and amyloidosis. Am J Hematol. 2005; 79 : 319–328.
- • Gertz MA, Lacy MQ, Dispenzieri A, at al. Transplantation for amyloidosis. Curr Opin Oncol. 2007; 19 : 136–141.
- • Gertz MA, Hayman SR. Immunoglobulin light chain amyloidosis. In: Rajkumar SV, Kyle RA. Treatment of multiple myeloma and related disorders. Cambridge: Cambridge University Press 2009 : 112–128.
- • Gertz MA, Rajkumar SV. Amyloidosis, Contemporary Hematology. Springer Science+Business Media, LLC 2010, pp. 33–48.
- • Gertz MA, Merlini G. Definition of organ involvement and response to treatment in AL amyloidosis: an updated consensus opinion. Amyloid. 2010; 17 : 48–49.
- • Gertz MA, Buadi FK, Hayman SR, at al. Immunoglobulin D amyloidosis: a distinct entity. Blood. 2012; 119 (1): 44–48.
- • Gertz MA. Immunoglobulin light chain amyloidosis: 2011 update on diagnosis, risk-stratification, and management. Am J Hematol. 2011; 86 : 181–186.
- • Gertz MA. Immunoglobulin light chain amyloidosis: 2016 update on diagnosis, prognosis, and treatment. Am J Hematol. 2016; 91 : 948–956.
- • Gillmore JD, Wechalekar A, Bird J, at al. Guidelines on diagnosis and investigation of AL amyloidosis. Brit J Hematol. 2015; 168 : 207–218.
- • Hassan W, Al-Sergani H, Mourad W, at al. Amyloid heart dinase. Tex Heart Inst J. 2005; 32 : 178–184.
- • Hawkins PN. Serum amyloid P component scintigraphy for diagnosis and monitoring amyloidosis. Curr Opin Nephrol Hypertens. 2002; 11 : 649–655.
- • Holub D at al. Mass spectrometry amyloid typing is reproducible across multiple organ sites. Biomed Res Int. 2019; 31 : 3689091.
- • Hosch W, Kristen AV, Libicher M, at al. Late enhancement in cardiac amyloidosis: correlation of MRI enhancement pattern with histopatological findings. Amyloid. 2008; 15 : 196–204.
- • Howie AJ, Brewer DB, Howell D, at al. Physical basis of colors seen in Congo red-stained amyloid in polarized light. Lab Invest. 2008; 88 : 232–242.
- • Jelinek T, Bezdekova R, Zatopkova M, at al. Current applications of multiparameter flow cytometry in plasma cell disorders. Blood Cancer J. 2017; 7: e617.
- • Jelinek T, Kryukova E, Kufova Z, Kryukov F, Hajek R. Proteasome inhibitors in AL amyloidosis: focus on mechanism of action and clinical activity. Hematol Oncol. 2017; 35 (4): 408–419.
- • Jelinek T, Kufova Z, Hajek R. Immunomodulatory drugs in AL amyloidosis. Crit Rev Oncol Hematol. 2016; 99 : 249–60.
- • Kapoor P, Thenappan T, Singh E, at al. Cardiac amyloidosis: A practical approach to diagnosis and management. Am J Med. 2011; 124 : 1006–1015.
- • Katzmann JA, Abraham RS, Dispenzieri A, at al. Diagnostic performance of quantitative kappa and lambda free light chain assays in clinical practice. Clin Chem. 2005; 51 : 878–881.
- • Kovářová L, Varmužová T, Žarbochová P, at al. Průtoková cytometrie u monoklonálních gamapatií. Klin Onkol. 2011; 24 (Suppl): S24–S29.
- • Koyama J, Falk RH. Prognostic significance of strain doppler imaging in light-chain amyloidosis. J Am Coll Cardiol Img. 2010; 3 : 333–342.
- • Krejčí K, Zadražil J, Tichý T. Nefropatie v ultrazvukovém a histologickém obraze. 1. vyd., Praha 2011, Maxdorf. Jessenius, s. 186.
- • Kristen AV, Giannitsis E, Lehrke S, at al. Assessment of disease severity and outcome in patients with systemic light-chain amyloidosis by the high-sensitivity troponin T assay. Blood. 2010; 116 : 2455–2461.
- • Kumar S, Dispenzieri A, Lacy MQ, at al. Improved survival in light chain amyloidosis. Amyloid. 2010; 17 (Suppl 1): 89–95.
- • Kumar S, Dispenzieri A, Lacy MQ, at al. Revised prognostic staging system for light chain amyloidosis incorporating cardiac biomarkers and serum free light chain measurements. J Clin Oncol. 2012; 30 : 989–995.
- • Kyle RA, Greipp PR, O’Fallon WM. Primary systemic amyloidosis: multivariate analysis for prognostic factors in 168 cases. Blood. 1986; 68 : 220–224.
- • Kyle RA, Linos A, Beard CM, at al. Incidence and natural history of primary systemic amyloidosis in Olmsted county, Minessota,1950 through 1989. Blood. 1992; 79 : 1817–1822.
- • Kyle RA, Gertz MA. Primary systemic amyloidosis: clinical features in 474 and laboratory cases. Semin Hematol. 1995; 32 : 45–59. (Kyle, 1995a)
- • Kyle RA. Multiple myeloma and other plasma cell disorders. In: Hofman R, Bentz EJ Jr., Shattil SJ at al., Hematology: basic principles and practice, 2nd ed., New York: Churchill Livingstone, 1995 : 1354–1374. (Kyle, 1995b)
- • Kyle RA, Gertz MA, Greip PR, at al. A trial of three regimens for primary amyloidosis: colchicine alone, melphalan and prednisone, and melphalan, prednisone, and colchicine. New Engl J Med. 1997; 336 : 1202–1207.
- • Kyle RA, Durie BG, Rajkumar SV, at al. Monoclonal gammopathy of undetermined significance (MGUS) and smoldering (asymptomatic) multiple myeloma: IMWG consensus perspectives risk factors for progression and guidelines for monitoring and management. Leukemia. 2010; 24 (6): 1121–1127.
- • Kyriakides T, Marques B, Panousopoulos A, at al. Amyloid myopathy: evidence for mechanical injury to the sarcolemma. Clin Neuropathol. 2002; 21 : 145–148.
- • Lachmann HJ, Booth DR, Booth SE, at al. Misdiagnosis of hereditary amyloidosis as AL (primary) amyloidosis. New England J Med. 2002; 346 : 1786–1791.
- • Lachmann HJ, Gallimore R, Gillmore JD, at al. Outcome in systemic AL amyloidosis in relation to changes in concentration of circulating free immunoglobulin light chains following chemotherapy. Br J Haematol. 2003; 122 : 78–84.
- • Leung N, Bridoux F, Hutchison CA, at al. Monoclonal gammopathy of renal signifikance (MGRS): when MGUS is no longer undetermined or insignificant. Blood. 2012; 120 (22): 4292–4295.
- • Loo D, Mollee PN, Renaut P, Hill MM. Proteomics in molecular diagnosis: typing of amyloidosis. J Biomed Biotechnol. 2011; 754109.
- • Maceira AM, Joshi J, Prasad SK, at al. Cardiovascular magnetic resonance in cardiac amyloidosis. Circulation. 2005; 111 : 186–193.
- • Maceira AM, Prasad SK, Hawkins PN, at al. Cardiovascular magnetic resonance and prognosis in cardiac amyloidosis. J Cardiovasc Magn Reson. 2008; 10 : 54–59.
- • Madan S, Dispenzieri A, Lacy MQ, at al. Clinical features and treatment response of light chain (AL) amyloidosis diagnosed in patiens with previous diagnosis of multiple myeloma. Mayo Clin Proc. 2010; 85 : 232–236.
- • Mann M, Hendrickson RC, Pandey A. Analysis of proteins and proteomes by mass spectrometry. Ann Rev Biochem. 2001; 70 (1): 437–473.
- • Maisnar V, Tichý M, at al. Monoklonální imunoglobuliny – výskyt, význam a možnosti jejich průkazu. 1.vyd., Nucleus, Hradec Králové 2012, s. 125.
- • Marcus A, Sadimin E, Richardson M, at al. Fluorescence microscopy is superior to polarized microscopy for detecting amyloid deposits in Congo red-stained trephine bone marrow biopsy specimens. Am J Clin Pathol. 2012; 138 : 590–593.
- • Merlini G. AL amyloidosis: diagnosis and prognosis. Haematologica. 2007; 92 (Suppl 2): 58–59.
- • Milani P, Basset M, Russo, at al. Patients with light-chain amyloidosis and low free light-chain burden have distinct clinical features and outcome. Blood. 2017; 130 (5): 625–631.
- • Mumford AD, O’Donnell J, Gillmore JD. Bleeding symptoms and coagulation abnormalities in 337 patients with amyloidosis. Br J Haematol. 2000; 110 : 454–460.
- • Murtagh B, Hammill SC, Gertz MA, at al. Electrocardiographic findings in primary systemic amyloidosis and biopsy-proven cardiac involvement. Am J Cardiol. 2005; 95 : 535–537.
- • Nasr SH, Galgano SJ, Markowitz GS, at al. Immunofluorescence on pronase-digested paraffin sections: a valuable salvage technique for renal biopsies. Kidney Int. 2006; 70 : 2148–2151.
- • Paiva B, Vídriales MB, Pérez JJ, at al. The clinical utility and prognostic value of multiparameter flow cytometry immunophenotyping in light-chain amyloidosis. Blood. 2011; 117 : 3613–3616.
- • Palecek T, Fikrle M, Nemecek E, at al. Contemporary treatment of amyloid heart disease. Curr Pharm Des. 2015; 21 : 491–506.
- • Palladini G, Malamani G, Co F, at al. Holter monitoring in AL amyloidosis: prognostic implications. Pacing Clin Electrophysiol.2001; 24 : 1228–1233.
- • Palladini G, Campana C, Klersy C, at al. Serum N-terminal pro-brain natriuretic peptide is a sensitive marker of myocardial dysfunction in AL amyloidosis. Circulation. 2003; 107 : 2440–2445.
- • Palladini G, Lavatelli F, Russo P, at al. Circulating amyloidogenic free light chaos and serum N-terminal natriuretic peptide type B decrease simultaneously in association with improvement of survival in AL. Blood. 2006; 107 : 3854–3858.
- • Palladini G, Perlini S, Merlini G. Imaging of systemic amyloidosis. In: Gertz MA, Rajkumar SV: Amyloidosis: diagnosis and treatment. Springer Science and Business Media, LLC 2010; 15–32. (Palladini, 2010a)
- • Palladini G, Gertz MA, Kumar S, at al.Validation of the criteria of response to treatment in AL amyloidosis. Blood. 2010; 116 : 1364a. (Palladini, 2010b)
- • Palladini G, Foli A, Milani P, at al. Best use of cardiac biomarkers in patients with AL amyloidosis and renal failure. Am J Hematol. 2012; 87 : 465–471.
- • Palladini G, Barassi A, Klersy C, at al. The combination of high-sensitivity cardiac troponin T (hs-cTnT) at presentation and changes in N-terminal natriuretic peptide type B (NT-proBNP) after chemotherapy best predict survival in AL amyloidosis. Blood. 2010; 116 : 3426–3430. (Palladini 2010c)
- • Palladini G, Paiva B, Wechalekar A, at al. Minimal residual disease negativity by next-generation flow cytometry is associated with improved organ response in AL amyloidosis. Blood Cancer J. 2021; 11 : 34.
- • Pan JA, Kerwin MJ, Salerno M. Native T1 mapping, extracellular volume mappig, and late gadolinium enhancement in cardiac amyloidosis: a meta-analysis. JACC Cardiovasc Imaging. 2020; 13 (6): 1299–1310.
- • Perugini E, Guidalotti PL, Salvi F, at al. Noninvasive etiologic diagnosis of cardiac amyloidosis using 99mTc-3,3-diphosphono-1,2-propanodicarboxylic acid scintigraphy. J Am Coll Cardiol. 2005; 46 : 1076–1084.
- • Pepys M. Amyloidosis. Ann Rev Med. 2006; 57 : 223–241.
- • Pika T, Hegenbart U, Flodrova P, Maier B, Kimmich C, Schönland SO. First report of ibrutinib in IgM-related amyloidosis: few responses, poor tolerability, and short survival. Blood. 2018; 131 (3): 368–371.
- • Pika T, Vymětal J, Metelka R, at al. Postižení srdce při AL amyloidóze. Interní Med. 2008; 10 : 466–469.
- • Piper C, Butz T, Farr M, Faber L, at al. How to diagnose cardiac amyloidosis early: impact of ECG, tissue doppler echocardiography, and myocardial biopsy. Amyloid. 2010; 17 : 1–9.
- • Quarta CC, Kruger JL, Falk RH. Cardiac amyloidosis. Circulation. 2012; 126 : 178–182.
- • Rajkumar SV, Gertz MA, Kyle RA. Primary systemic amyloidosis with delayed progression to multiple myeloma. Cancer. 1998; 82 : 1501–1505.
- • Rajkumar SV, Gertz MA. Advances in the treatment of amyloidosis. New Engl J Med. 2007; 356 : 2413–15.
- • Rajkumar SV. Multiple myeloma: 2011 update to diagnosis, risk stratification, and management. Am J Hematol. 2011; 86 : 57–62.
- • Rapezzi C, Quarta CC, Guidalotti PL, at al. Role of (99m) Tc-DPD scintigraphy in diagnosis and prognosis of hereditary transthyretin-related cardiac amyloidosis. J Am Coll Cardiol Img. 2011; 4 : 659–670.
- • Ravichandran S, Lachmann HJ, Wechalekar AD. Epidemiologic and survival trends in amyloidosis, 1987-2019. N Engl J Med. 2020; 382 : 1567–1568.
- • Reyners AKL, Hazenberg BPC, Reitsma WD, at al. Heart rate variability as a predictor of mortality in patients with AA and AL amyloidosis. Eur Heart J. 2002; 23 : 157–161.
- • Ruberg FL, Appelbaum E, Davidoff R, at al. Diagnostic and prognostic utility of cardiovascular magnetic resonance imaging in light-chain cardiac amyloidosis. Am J Cardiol. 2009; 103 : 544–549.
- • Ryšavá R. Systémové amyloidózy a jejich léčba. Maxdorf Jessenius/Sv 61, Praha 2013, s. 124.
- • Ryšavá R. AL amyloidosis: advances in diagnostics and treatment. Nephrol Dial Transplant. 2019; 34 (9): 1460–1466. (Ryšavá, 2019a)
- • Ryšavá R. Postižení gastrointestinálního traktu amyloidózou – kdy na ni myslet a jak diagnostikovat. Gastroent Hepatol. 2019; 73 (2): 154–162. (Ryšavá, 2019b)
- • Sanchorawala V, Skinner M, Quillen K, at al. Long-term outcome of patiens with AL amyloidosis treated with high-dose melphalan and stem-cell transplantation. Blood. 2007; 110 : 3561–3563.
- • Seldin DC, Sanchorawala V. Adapting to AL amyloidosis. Haematologica. 2006; 91 : 1591–1595.
- • Schönland SO, Hegenbart U, Bochtler T, at al. Immunohistochemistry in the classification of systemic forms of amyloidosis: a systematic investigation of 117 patients. Blood. 2012; 119 : 488–493.
- • Sipe JD, Benson MD, Buxbaum JN, at al. Amyloid fibril proteins and amyloidosis: chemical identification and clinical classification International Society of Amyloidosis 2016 Nomenclature Guidelines. Amyloid. 2016; 23 (4): 209–213.
- • Siragusa S, Morice W, Gertz MA, at al. Asymptomatic immunoglobulin light chain amyloidosis (AL) at the time of diagnostic bone marrow biopsy in newly diagnosed patients with multiple myeloma and smoldering myeloma. A series of 144 cases and review of the literature. Ann Hematol. 2011; 90 : 101–106.
- • Snanoudj R, Durrbach A, Gauthier E, at al. Changes in renal function in patients with familial amyloid polyneuropathy treated with orthtopic liver transplantation. Nephrol Dial Transplant. 2004; 19 : 1779–1785.
- • Steusloff K, Röcken C, Saeger W. Basement membrane proteins and apolipoprotein E in growth hormone secreting adenomas and their correlation to amyloid: an immunoelectron microscopic study. Endocr Pathol. 2000; 11 : 49–56.
- • Ščudla V, Pika T. Současné možnosti diagnostiky a léčby systémové AL-amyloidózy. Vnitř Lék. 2009; 55 (Suppl 1): 77–87.
- • Ščudla V, Minařík J, Pika T. Nemoc z ukládání lehkých řetězců imunoglobulinu (light chain deposition disease). Vnitř Lék. 2012; 58 : 38–43.
- • Theis JD, Dasari S, Vrana JA, at al. Shotgun-proteomics-based clinical testing for diagnosis and classification of amyloidosis. J Mass Spectr. 2013; 48 (10): 1067–1077.
- • Vacek Z. Histologie a histologická technika. Avicenum, Praha 1988, p. 376–378.
- • Vávrová J, Tichý M, Maisnar V, at al. Stanovení volných lehkých řetězců a Hevylite u monoklonálních gamapatií. In: Maisnar V, Tichý M, a kol. Monoklonální imunoglobuliny – výskyt, význam a možnosti jejich průkazu. 1. vyd., Nucleus, Hradec Králové 2012, s. 55–60.
- • Vrana J, Gamez J, Madden B, at al. Classification of amyloidosis by laser microdissection and mass spectrometrybased proteomic analysis in clinical biopsy specimens. Blood. 2009; 114 : 4957–4959.
- • Vrana J, Theis J, Dasari S, at al. Clinical diagnosis and typing of systemic amyloidosis in subcutaneous fat aspirates by mass spectrometrybased proteomics. Haematologica. 2014; 99 : 1239–1247.
- • Warsame R, Kumar SK, Gertz MA, at al. Abnormal FISH in patients with immunoglobulin light chain amyloidosis is a risk factor for cardiac involvement and death. Blood Cancer J. 2015; 5: e310.
- • Wechalekar AD, Lachmann HL, Goodman JB, at al. AL amyloidosis associated with IgM paraproteinemia: clinical profile and treatment outcome. Blood. 2008; 112 : 40009–40016.
- • Wechalekar AD, Offer M, Gillmore JD, at al. Cardiac amyloidosis, a monoclonal gammopathy and a potentially misleading mutation. Nat Clin Pract Cardiovasc Med. 2009; 6 : 128–133.
- • Wechalekar A, Faint J, Bradwell S, at al. Significance of abnormal serum immunoglobulin heavy/light chain ratios (Hevylite) in 294 patients with systemic AL amyloidosis. Haematologica. 2011; 96 : 392–398.
- • Wechalekar AD; Schonland SO; Kastritis E, at al. A European collaborative study of treatment outcomes in 346 patients with cardiac stage III AL amyloidosis. Blood. 2013; 121 : 3420–3427.
- • Weijia L, Uppal D, Wang YC, at al. Nuclear imaging for the diagnosis of cardiac amyloidosis in 2021. Diagnostics. 2021; 11 (6): 996.
10.3. POUŽITÁ LITERATURA
- • Benson MD. Amyloidosis. In: Scriver CR, at al. 7th ed. The metabolic and molecular bases of inherited disease. New York 1995, McGraw Hill, 4159–4191.
- • Bertelsen C, Chadwick K, Holland J, Flint P, Schindler JS. Long-term follow-up after radiation therapy for laryngeal amyloidosis. Laryngoscope. 2021; 131 (8): 1810–1815.
- • Bird J. Guidelines on the diagnosis and management of AL amyloidosis. Br J Haematol. 2004; 125 (6): 581–700.
- • Buadi F. Localized amyloidosis. In: Gertz MA, Rajkumar SV. Amyloidosis: diagnosis and treatment, 1st ed., Springer Science, New York 2010, 95–106.
- • Dominguez W, Weinberg P, Claros P, at al. Primary localized nasopharyngeal amyloidosis. A case report. Int J Pediatr Otorhinolaryngol. 1996; 36 : 61–67.
- • Gupta P, Hanamshetti S, Kulkarni JN. Primary amyloidosis with high grade transitional cell carcinoma of bladder. J Cancer Res Ther. 2012; 8 (2): 297–299.
- • Hamidi AK. Organ-specific (localized) synthesis of Ig light chain amyloid. J Immunol. 1999; 162 : 556–560.
- • Harris G, Lachmann H, Hawkins P, Sandhu G. One hundred cases of localized laryngeal amyloidosis – evidence for future management. Laryngoscope. 2021; 131 (6): E1912–E1917.
- • Chiang D, Lee M, Germaine P, at al. Amyloidosis of the breast with multicentric DCIS and pleomorphic invasive lobular carcinoma in a patient with underlying extranodal Castleman‘s disease. Case Rep Radiol. 2013; 2013 : 190856.
- • Kalra S. External-beam radiation therapy in the treatment of difuse tracheobronchial amyloidosis. Mayo Clin Proc. 2001; 76 : 853–856.
- • Kurrus JA, Hayes JK, Hoidal JR. Radiation therapy for tracheobronchial amyloidosis. Chest. 1998; 114 : 1489–1492.
- • Kyle RA, Bayrd ED. Amyloidosis: review of 236 cases. Medicine (Baltimore). 1975; 54 : 271–299.
- • Ma L. Primary localized laryngeal amyloidosis: report of 3 cases with long-term follow-up and review of the literature. Arch Pathol Lab Med. 2005; 129 : 215–218.
- • Moore A, Kramer MR, Silvern D, Shtraichman O, Allen AM. Endobronchial brachytherapy–A novel approach for the management of airway amyloidosis. Brachytherapy. 2018; 17 (6): 966–972.
- • Motta G, Salzano FA, Motta S, Staibano S. CO (2) -laser treatment of laryngeal amyloidosis. J Laryngol Otol. 2003; 117 (8): 647–650.
- • Munichor M, Cohen H, Kerner H, Szvalb S, Iancu TC. Localized amyloidosis in nasopharyngeal carcinoma diagnosed by fine needle aspiration and electron microscopy. A case report. Acta Cytol. 2000; 44 : 637–638.
- • Neuner GA, Badros AA, Meyer TK, at al. Complete resolution of laryngeal amyloidosis with radiation treatment. Head Neck. 2012; 34 : 748–752.
- • Paccalin M. Localized amyloidosis: a survey of 35 French cases. Amyloid. 2005; 12 : 239–245.
LITERATURA PRO LÉČEBNOU ČÁST
- • Adam Z, Ščudla V, Krejčí M, at al. Léčba AL amyloidózy v roce 2012, přínos nových léků (bortezomibu, thalidomidu a lenalidomidu). Přehled publikovaných klinických studií. Vnitřní Lék. 2013; 59 : 37–58.
- • Al Hamed, Bazarbachi AH, Bazarbachi A, Malard F, Harousseau J-L, Mohty M. Comprehensive review of AL amyloidosis: some practical recommendations. Blood Cancer J. 2021; 11 : 97.
- • Bodin K, Ellmerich S, Kahan MC, at al. Antibodies to human serum amyloid P component eliminate visceral amyloid deposits. Nature. 2010; 468 (7320): 93–97.
- • Bochtler T, Hegenbart U, Kunz C, at al. Translocation t (11; 14) is associated with adverse outcome in patients with newly diagnosed AL amyloidosis when treated with bortezomib-based regimens. J Clin Oncol. 2015; 33 (12): 1371–1378.
- • Cibeira MT, Sanchorawala V, Seldin DC, at al. Outcome of AL amyloidosis after high-dose melphalan and autologous stem cell transplantation: long-term results in a series of 421 patients. Blood. 2011; 118: 4346–4352.
- • Cohen AD, Landau H, Scott EC, at al. Safety and efficacy of carfilzomib (CFZ) in previously-treated systemic light-chain (AL) amyloidosis. Blood. 2016; 128 : 645.
- • Cohen AD, Sharpley F, Gillmore JD, at al. Use of ixazomib, lenalidomide and dexamethasone in patients with relapsed amyloid light-chain amyloidosis. Br J Haematol. 2020; 189 (4): 643–649.
- • Comenzo RL, Vosburgh E, Falk RH, at al. Dose-intensive melphalan with blood stem-cell support for the treatment of AL (amyloid light-chain) amyloidosis: survival and responses in 25 patients. Blood. 1998; 91 : 3662–3670.
- • Comenzo RL, Hegenbart U, Sanchorawala W, at al. High rates of overall and complete haematologic response in a prospective phase ½ study of weeky and twice weekly bortezomib in relapsed AL amyloidosis. Amyloid. 2010; 17 : 83–84.
- • Comenzo RL, Reece D, Palladini G, at al. Consensus guidelins for the conduct and reporting of clinical trials in systemic light-chain amyloidosis. Leukemia. 2012; 26 : 2317–2325.
- • Dhopdapkar M, Jagannath S, Vesole D, at al. Treatment of AL-amyloidosis with dexamethasone plus alpha interferon. Leuk Lymphoma. 1997; 27 : 351–356.
- • Dietrich S, Schönland SO, Benner A, at al. Treatment with intravenous melphalan and dexamethasone is not able to overcome the poor prognosis of patients with newly diagnosed systemic light chain amyloidosis and severe cardiac involvement. Blood. 2010; 116 (4): 522–528.
- • Dispenzieri A, Lacy M, Rajkumar S, at al. Poor tolerance to high doses of thalidomide in patients with primary systemic amyloidosis. Amyloid. 2003; 10 : 257–261.
- • Dispenzieri A, Buadi F, Kumar SK, at al. Treatment of immunoglobulin light chain amyloidosis: Mayo stratification of myeloma and risk-adapted (mSMART) consensus statement. Mayo Clin Proc. 2015; 90 (8): 1054–1081.
- • Dispenzieri A, Lacy M, Zeldenrust S, at al. The activity of lenalidomide with or without dexamethasone in patiens with primary systemic amyloidosis. Blood. 2007; 109 : 465–470.
- • Dispenzieri A, Kastritis E, Wechalekar AD, at al. A randomized phase 3 study of ixazomib–dexamethasone versus physician’s choice in relapsed or refractory AL amyloidosis. Leukemia. 2021; 36 : 225–235.
- • D‘Souza A, Dispenzieri A, Wirk B, at al. Improved outcomes after autologous hematopoietic cell transplantation for light chain amyloidosis: A center for international blood and marrow transplant research study. J Clin Oncol. 2015; 33 (32): 3741–3749.
- • Edwards CV, Rao N, Bhutani D, at al. Phase 1a/b study of monoclonal antibody CAEL-101 (11-1F4) in patients with AL amyloidosis. Blood. 2021; 138 (25): 2632–2641.
- • Gavriatopoulou M, Musto P, Caers J, at al. European myeloma network recommendations on diagnosis and management of patients with rare plasma cell dyscrasias. Leukemia. 2018; 32 (9): 1883–1898.
- • Gertz M, Lacy M, Dispenzieri A, at al. Risk-adjusted manipulation of melphalan dose before stem cell transplantation in patients with amyloidosis is associated with a lower response rate. Bone Marrow Transplantation. 2004; 34 : 1025–1031.
- • Gertz MA, Comenzo R, Falk RH, at al. Definition of organ involvement and treatment response in immunoglobulin light chain amyloidosis. A consensus opinion from the 10th international symposium on amyloid and amyloidosis. Amer J Hematol. 2005; 79 : 319–328.
- • Gertz MA, Lacy MQ, Dispenzieri A, at al. Effect of hematologic response on outcome of patients undergoing transplantation for primary amyloidosis: importance of achieving a complete response. Haematologica. 2007; 92 (10): 1415–1418.
- • Gertz MA. I dont know how to treat amyloidosis. Blood. 2010; 116 : 507–508. (Gertz, 2010a)
- • Gertz MA, Merlini G. Definition of organ involvement and response to treatment in AL amyloidosis: an updated consensus opinion. Amyloid. 2010; 17 (Suppl 1): 48–49. (Gertz, 2010b)
- • Gertz MA, Landau H, Comenzo RL, at al. First-in-human phase I/II study of NEOD001 in patients with light chain amyloidosis and persistent organ dysfunction. J Clin Oncol. 2016; 34 (10): 1097–1103.
- • Hájek R, Maisnar V, Krejčí M, at al. Diagnostika a léčba mnohočetného myelomu. Transfuze Hematol Dnes. 2018; 24 (Suppl): 1–157.
- • International Myeloma Working Group: Criteria for the classification of monoclonal gammopathies, multiple myeloma and releated disorders: a report of the International Myeloma Working Group. Brit J Haematol. 2003; 121 : 749–757.
- • Jaccard A, Moreau P, Leblond V, at al. High-dose melphalan versus melphalan plus dexamethasone for AL amyloidosis. N Engl J Med. 2007; 357 : 83–93.
- • Kastritis E, Anagnostopoulos A, Roussou M, at al. Treatment of light chain (AL) amyloidosis with the combination of bortezomib and dexamethasone. Haematologica. 2007; 92 : 1351–1358.
- • Kastritis E, Wechalekar E, Dimopoulos M, at al. Bortezomib with or without dexamethasone in primary systemic (light chain) amyloidosis. J Clin Oncol. 2010; 28 : 1031–1037.
- • Kastritis E, Leleu X, Arnulf B, at al. A randomized phase III trial of melphalan and dexamethasone (MDex) versus bortezomib, melphalan and dexamethasone (BMDex) for untreated patients with AL amyloidosis. Blood. 2016; 128 : 646.
- • Kastritis E, Leleu X, Arnulf B, at al. Bortezomib, melphalan, and dexamethasone for light chain amyloidosis. J Clin Oncol. 2020; 38 : 3252–3260.
- • Kastritis E, Rousakis P, Kostopoulos IV, at al. Consolidation with a short course of daratumumab in patients with AL amyloidosis or light chain deposition disease. Amyloid. 2021; 1 : 1–8. (Kastritis, 2021a)
- • Kastritis E, Palladini G, Minnema MC, at al. Daratumumab-based treatment for immunoglobulin light-chain amyloidosis. N Engl J Med. 2021; 385 : 46–58. (Kastritis, 2021b)
- • Kaufman GP, Schrier SL, Lafayette LA, at al. Daratumumab yields rapid and deep hematologic responses in patients with heavily pretreated AL amyloidosis. Blood. 2017; 130 : 900–902.
- • Khouri J, Anwer F, Samaras CJ, at al. Safety, tolerability and efficacy of Cael-101 in AL amyloidosis patients treated on a phase 2, open-label, dose selection study to evaluate the safety and tolerability of Cael-101 in patients with AL amyloidosis. Blood. 2020; 136 : 21.
- • Kimmich CR, Terzer T, Benner A, at al. Daratumumab for systemic AL amyloidosis: prognostic factors and adverse outcome with nephrotic-range albuminuria. Blood. 2020; 135 (18): 1517–1530.
- • Kumar SK, Hayman SR, Buadi FK, at al. Lenalidomide, cyclophosphamide and dexamethasone (CRd) for light chain amyloidosis: long term results from a phase 2 trial. Blood. 2012; 112 : 4860–4867.
- • Kyle RA, Gertz MA, Greipp PR, at al. A trial of three regimens for primary amyloidosis: Colchicine alone, melphalan and prednisone, and melphalan, prednisone, and colchicine. N Engl J Med. 1997; 336 : 1202–1207.
- • Kyle RA, Rajkumar SV. Criteria for diagnosis, staging, risk stratification and response assessment of multiple myeloma. Leukemia. 2009; 23 : 3–9.
- • Lagos GG, Lentzsch S, Comenzo RL, at al. Final results of a phase 2 study of bendamustine in combination with dexamethasone in patients with previously treated systemic light-chain (AL) amyloidosis. Blood. 2016; 128 : 4523.
- • Landau H, Hassoun H, Rosenzweig MA, at al. Bortezomib and dexamethasone consolidation following risk-adapted melphalan and stem cell transplantation for patients with newly diagnosed light-chain amyloidosis. Leukemia. 2013; 27 (4): 823–828.
- • Manwani R, Mahmood S, Sachchithanantham S, at al. Carfilzomib is an effective upfront treatment in AL amyloidosis patients with peripheral and autonomic neuropathy. Br J Haematol. 2019; 187 (5): 638–641.
- • Merlini G, Stone MJ. Dangerous small B-cell clones. Blood. 2006; 108 : 2520–2530.
- • Mikhael JR, Schuster SR, Jimenez-Zepeda VH, at al. Cyclophosphamide-bortezomib-dexamethasone (CyBorD) produces rapid and complete hematologix response in patients with AL amyloidosis. Blood. 2012; 119 : 4391–4394.
- • Milani P, Schönland S, Merlini G, at al. Treatment of AL amyloidosis with bendamustine: a study of 122 patients. Blood. 2018; 132 : 1988–1991.
- • Moreau P. Autologous stem cell transplantation for AL amyloidosis: a standard therapy? Leukemia. 1999; 13 : 1929–1931.
- • Moreau P, Jaccard A, Benboubker L, at al. Lenalidomide in combination with melphalan and dexamethasone in patiens with newly-diagnosed AL amyloidosis: a multicenter phase ½ dose escalation study. Blood. 2010; 116 : 4777–4782.
- • Muchtar E, Dispenzieri A, Gertz MA, at al. Treatment of AL amyloidosis: Mayo stratification of myeloma and risk-adapted therapy (mSMART) consensus statement 2020 update. Mayo Clin Proc. 2021; 96 (6): 1546–1577.
- • Muchtar E, Gertz MA, Laplant B, at al. Phase 2 trial of ixazomib, cyclophosphamide and dexamethasone for treatment of previously untreated light chain amyloidosis. Blood. 2020; 136 : 52–53.
- • Muchtar E, Dispenzieri A, Kumar SK, at al. Interphase fluorescence in situ hybridization in untreated AL amyloidosis has an independent prognostic impact by abnormality type and treatment category. Leukemia. 2017; 31 (7): 1562–1569.
- • Nahi H, Kashif M, Klimkowska M, at al. Low dose venetoclax as a single agent treatment of plasma cell malignancies harboring t (11; 14). Am J Hematol. 2021; 96 (8): 925–933.
- • Palladini G, Perfetti V, Obici L, at al. Association of melphalan and high-dose dexamethasone is effective and well tolerated in patients with AL (primary) amyloidosis who are ineligible for stem cell transplantation. Blood. 2004; 103 : 2936–2938.
- • Palladini G, Perfetti V, Perlini S, at al. The combination of thalidomide and intermediate-dose dexamethasone is an effective but toxic treatment for patients with primary amyloidosis (AL). Blood. 2005; 105 : 2949–2951.
- • Palladini G, Russo P, Nuvolone M, at al. Treatment with oral melphalan plus dexamethasone produces long-term remissions in AL amyloidosis. Blood. 2007; 110 : 787–788.
- • Palladini G, Merlini G. What is new in diagnosis and management of light chain amyloidosis? Blood. 2016; 128 : 159–168.
- • Palladini G, Russo P, Lavatelli F, at al. Treatment of patients with advanced cardiac AL amyloidosis with oral melphalan, dexamethasone and thalidomide. Ann Hematol. 2009; 88 : 347–350.
- • Palladini G, Folli A, Milani P, at al. Oral melphalan and dexamethasone for AL amyloidosis: efficaccy, prognostic factors and response criteria. Amyloid. 2010; 17 : 81–82.
- • Palladini G, Dispenzieri A, Gertz MA, at al. New criteria for response to treatment in immunoglobulin light chain amyloidosis based on free light chain measurement and cardiac biomarkers: impact on survival outcomes. J Clin Oncol. 2012; 30 : 4514–4549. (Palladini, 2012a)
- • Palladini G, Russo P, Foli A, at al. Salvage therapy with lenalidomide and dexamethasone in patients with advanced AL amyloidosis refractory to melphalan, bortezomib, and thalidomide. Ann Hematol. 2012; 91 : 89–92. (Palladini, 2012b)
- • Palladini G, Russo P, Milani P, at al. A phase II trial of cyclophosphamide, lenalidomide and dexamethasone in previously treated patiens with AL amyloidosis. Haematologica. 2013; 98 : 433–436.
- • Palladini G, Sachchithanantham S, Milani P, at al. A European collaborative study of cyclophosphamide, bortezomib, and dexamethasone in upfront treatment of systemic AL amyloidosis. Blood. 2015; 126 (5): 612–615.
- • Palladini G, Kastritis E, Maurer MS, at al. Daratumumab plus CyBorD for patients with newly diagnosed AL amyloidosis: safety run-in results of Andromeda. Blood. 2020; 136: (1): 71–80.
- • Pasquer H, Belhadj K, Dupuis J, at al. Venetoclax induces profound and sustained responses in patients with relapsed/refractory light-chain amyloidosis. Brit J Haematol. 2021; 193 : 674–681.
- • Premkumar VJ, Lentzsch S, Pan S, at al. Venetoclax induces deep hematologic remissions in t (11; 14) relapsed/refractory AL amyloidosis. Blood Cancer J. 2021; 11 : 10.
- • Reece DE, Hegenbart U, Sanchorawala V, at al. Efficacy and safety of once-weekly and twice-weekly bortezomib in patients with relapsed systemic AL amyloidosis: results of a phase 1/2 study. Blood. 2011; 118 : 865–873.
- • Richards DB, Cookson LM, Berges AC, at al. Therapeutic clearance of amyloid by antibodies to serum amyloid P component. N Engl J Med. 2015; 373 (12): 1106–1114.
- • Roussel M, Merlini G, Chevret S, at al. A prospective phase 2 trial of daratumumab in patients with previously treated systemic light-chain amyloidosis. Blood. 2020; 135 (18): 1531–1540.
- • Ryšavá R, Straub J, Vacková B, at al. Results of autologous stem cell transplantation for AL amyloidosis in one Czech center. Amyloid. 2011; 18 Suppl 1 : 139–141.
- • Ryšavá R. AL amyloidosis: advances in diagnostics and treatment. Nephrol Dial Transplant. 2019; 34 (9): 1460–1466.
- • Sanchorawala V, Skinner M, Quillen K, at al. Long-term outcome of patients with AL amyloidosis treated with high-dose melphalan and stem cell transplantatrion. Blood 2007; 110 : 3561–3563. (Sanchorawala, 2007a)
- • Sanchorawala V, Wright D, Rosenzweig M, at al. Lenalidomide and dexamethasone in the treatment of AL amyloidosis: resutls of a phase 2 trial. Blood. 2007; 109 : 492–496. (Sanchorawala, 2007b)
- • Sanchorawala V, Wright DG, Quillen K, at al. Tandem cycles of high-dose melphalan and autologous stem cell transplantation increase the response rate in AL amyloidosis. Bone Marrow Transplant. 2007; 40 (6): 557–562. (Sanchorawala, 2007c)
- • Sanchorawala V, Sun F, Quillen K, at al. Long-term outcome of patients with amyloidosis treated with high-dose melphalan and stem cell transplantation: 20-year experience. Blood. 2015; 126 (20): 2354–2347.
- • Sanchorawala V, Shelton AC, Lo S, Varga C, Sloan JM, Seldin DC. Pomalidomide and dexamethasone in the treatment of AL amyloidosis: results of a phase 1 and 2 trial. Blood. 2016; 128 (8): 1059–1062.
- • Sanchorawala V, Palladini G, Kukreti V, at al. A phase 1/2 study of the oral proteasome inhibitor ixazomib in relapsed or refractory AL amyloidosis. Blood. 2017; 130 (5): 597–605.
- • Sanchorawala V, Sarosiek S, Schulman A, at al. Safety, tolerability, and response rates of daratumumab in relapsed AL amyloidosis: results of a phase 2 study. Blood. 2020; 135 (18): 1541–1547.
- • Sanchorawala V, Boccadoro M, Gertz M, at al. Guidelines for high dose chemotherapy and stem cell transplantation for systemic AL amyloidosis: EHA-ISA working group guidelines. Amyloid. Publikováno elektronicky 16. listopadu 2021, doi: 10.1080/ 13506129.2021.2002841.
- • Seldin D, Choufani E, Dember L, at al. Tolerability and efficacy of thalidomide for the treatment of patients with light chain-associated (AL) amyloidosis. Clinical Lymphoma. 2003; 3 : 241–246.
- • Shen K, Fu W, Wu Y, at al. Doxycycline combined with bortezomib-cyclophosphamide-dexamethasone chemotherapy for newly diagnosed cardiac light-chain amyloidosis: a multicenter randomized controlled trial. Circulation. 2022; 145 (1): 8–17.
- • Sidana S, Narkhede M, Elson P at al. Neuropathy and efficacy of once weekly subcutaneous bortezomib in multiple myeloma and light chain (AL) amyloidosis. PLoS One 2017; 9; 12 (3): e0172996.
- • Sidiqi MH, Aljama MA, Buadi FK, at al. Stem cell transplantation for light chain amyloidosis: decreased early mortality over time. J Clin Oncol. 2018; 36 : 1323–1329.
- • Sidiqi MH, Gertz MA. Immunoglobulin light chain amyloidosis diagnosis and treatment algorithm 2021. Blood Cancer J. 2021; 11 : 90.
- • Sidiqi MH, Al Saleh AS, Leung N, at al. Venetoclax for the treatment of translocation (11; 14) AL amyloidosis. Blood Cancer J. 2020; 10 (5): 55.
- • Skinner M, Anderson J, Simms R, at al. Treatment of 100 patients with primary amyloidosis: a randomized trial of melphalan, prednisone and colchicine versus colchicine only. A J Med. 1996; 100 : 290–298.
- • Skinner M, Sanchorawala V, Seldin D, at al. High-dise melphalan and autologous stem-cell transplantation in patients with AL amyloidosis: an 8-year study. Ann Int Med. 2004; 140 : 85–93.
- • Specter R, Sanchorawala V, Seldin DC, at al. Kidney dysfunction during lenalidomide treatment for AL amyloidosis. Nephrol Dial Transplant. 2011; 26 (3): 881–886.
- • Staron A, Zheng L, Doros G, at al. Marked progress in AL amyloidosis survival: a 40-year longitudinal natural history study. Blood Cancer J. 2021; 11 : 139.
- • Tapan U, Seldin DC, Finn KT, at al. Increases in B-type natriuretic peptide (BNP) during treatment with lenalidomide in AL amyloidosis. Blood. 2010; 116 (23): 5071–5072.
- • Venner CP, Lane T, Foard D, at al. Cyclophosphamide, bortezomib, and dexamethasone therapy in AL amyloidosis is associated with high clonal response rates and prolonged progression-free survival. Blood. 2012; 119 : 4387–4390.
- • Venner CP, Gillmore JD, Sachchithanantham S, at al. A matched comparison of cyclophosphamide, bortezomib and dexamethasone (CVD) versus risk-adapted cyclophosphamide, thalidomide and dexamethasone (CTD) in AL amyloidosis. Leukemia. 2014; 28 (12): 2304–2310.
- • Vesole DH, Perez WS, Akasheh M, at al. High-dose therapy and autologous hematopoietic stem cell transplantation for patients with primary systemic amyloidosis: A Center for International Blood and Marrow Transplant Research Study. Mayo Clin Proc. 2006; 81 : 880–888.
- • Wechalekar AD, Goodman HJ, Lachmann HJ, at al. Safety and efficacy of risk-adapted cyclophosphamide, thalidomide, and dexamethasone in systemic AL amyloidosis. Blood. 2007; 109 : 457–464.
- • Wechalekar AD, Schonland SO, Kastritis E, at al. A European collaborative study of treatment outcomes in 346 patients with cardiac stage III AL amyloidosis. Blood. 2013; 121 : 3420–3427.
- • Wechalekar AD, Gillmore JD, Bird J, at al. Guidelines on the management of AL amyloidosis. Brit J Hematol. 2015; 168 : 186–206. (Wechalekar, 2015a)
- • Wechalekar AD, Whelan C, Lachmann H, at al. Oral doxycycline improves outcomes of stage III AL amyloidosis – a matched case control study. Blood. 2015; 126 : 732. (Wechalekar, 2015b)
- • Wechalekar AD, Whelan C. Encouraging impact of doxycycline on early mortality in cardiac light chain (AL) amyloidosis. Blood Cancer J. 2017; 7 (3): e546.
Štítky
Hematologie a transfuzní lékařství Interní lékařství Onkologie
Článek vyšel v časopiseTransfuze a hematologie dnes
Nejčtenější tento týden
2022 Číslo Supplementum 1- Aktuální doporučení pro diagnostiku von Willebrandovy choroby
- Efekt itopridu na motilitu jícnu a funkci dolního jícnového svěrače
- Ibrance® – nová šance pro pacientky s HR+/HER2– karcinomem prsu
- Strava bohatá na arginin a prolin slibuje urychlení hojení ran u diabetických pacientů
- Úloha růstového faktoru TGF-β v procesu hojení ran
Nejčtenější v tomto čísle- Diagnostika a léčba Waldenströmovy makroglobulinémie
- Diagnostika a léčba systémové AL amyloidózy
- Editorial
- Editorial
Kurzy
Zvyšte si kvalifikaci online z pohodlí domova
Revma Focus: Spondyloartritidy
nový kurz
Autoři: prof. MUDr. Vladimír Palička, CSc., Dr.h.c., doc. MUDr. Václav Vyskočil, Ph.D., MUDr. Petr Kasalický, CSc., MUDr. Jan Rosa, Ing. Pavel Havlík, Ing. Jan Adam, Hana Hejnová, DiS., Jana Křenková
Autoři: MDDr. Eleonóra Ivančová, PhD., MHA
Autoři: prof. MUDr. Eva Kubala Havrdová, DrSc.
Autoři: prof. MUDr. Pavel Horák, CSc., doc. MUDr. Ludmila Brunerová, Ph.D., doc. MUDr. Václav Vyskočil, Ph.D., prim. MUDr. Richard Pikner, Ph.D., MUDr. Olga Růžičková, MUDr. Jan Rosa, prof. MUDr. Vladimír Palička, CSc., Dr.h.c.
Všechny kurzyPřihlášení#ADS_BOTTOM_SCRIPTS#Zapomenuté hesloZadejte e-mailovou adresu, se kterou jste vytvářel(a) účet, budou Vám na ni zaslány informace k nastavení nového hesla.
- Vzdělávání



